一种神经保护装置的制作方法
本发明涉及一种神经保护装置(neuroprotectionapparatus)。
背景技术:
诱发型低温(inducedhypothermia)是用于治疗医学病况的确定治疗处理和外科手术期间的确定治疗过程。诱发型低温可以被分为用于可控降低病人核心身体温度低于37℃的诱发型全身低温或用于可控降低特定器官或身体部位温度低于37℃的诱发型局部低温。诱发型低温分类定义了34-36.9℃的诱发型轻度低温,32-33.9℃的诱发型中度低温,30–31.9℃的诱发型中度/深度低温,和<30℃的深度诱发型低温。用于实现诱发型全身低温的常规技术包括,尤其是,整个身体浸入冰水中以降低核心身体温度,用以开心手术期间冷却病人的血液的心肺机等等。心肺机通常能够冷却病人的血液供给,从正常的37℃核心身体温度到变冷的33℃。用于诱发局部脑低温的常规技术包括,尤其是,用于中风病人头部的外部冷却的头盔、动脉内冷物灌注(intraarterialcoldinfusion)(iaci)方案等等。
人脑重量仅仅占人体重量的一小部分,通常在2-3%范围内,但是人大脑血流量通常是人心输出量的大约15%。因此,人脑温度改变比核心身体温度快的多,并且iaci方案已经显示出在数分钟内诱发高选择性脑温度降低并且达到目标局部温度比常规诱发型全身低温快10到30倍。iaci方案通常在10分钟内将人脑从核心身体温度变冷到32c°到34℃之间。
终止诱发型全身或局部脑低温会导致神经破坏,因为脑组织从它的诱发型低温状态升温过快。人脑从低温状态到正常核心身体温度的优选升温速度是大约每小时0.5℃。实施冷灌注(coldinfusion)诱发人脑进入低温状态和终止所述冷灌注之后,低温的人脑以大约每小时2℃的速度从它的低温状态自然升温到它的正常核心身体温度,由于输入的血流在正常37℃身体核心温度以及它的正在进行的大脑活动,这比优选的每小时0.5℃升温速度高得多。终止诱发型全身低温导致低温人脑以比每小时2℃低的速度自然升温,但是仍然比优选的每小时0.5℃升温速度高。
由于栓塞障碍或血栓形成,位于梗塞上游的充血边界区(这是由血管活性代谢物的积累和酸液过多导致的)和在血流的流动方向上位于该梗塞下游的附带灌流缺血性半影区(collaterallyperfusedischemicpenumbraregion),缺血性中风导致缺血性梗塞形成。这样的障碍可以是从大约70%闭塞和更大。通常当血液灌流(bloodperfusion)降低到低于大约20ml/100g/分钟,完全不同于大约50到60ml/100g/分钟的正常灌流时界定半影区。缺血性梗塞是不可逆的受伤脑组织同时半影区处于危险中,但是如果再灌流发生在相当短的几个小时之内是可抢救的。半影区的拯救可以通过诱导型全身或局部脑冷却帮助,这归因于氧需要减少:脑温度降低1℃使大脑氧消耗降低达大约5%,由此增加缺血性状况的耐受性。
iacis通常是在近端留置导管端灌注之前3℃到4℃的盐水溶液。iacis可能由合适的药物介导,该合适的药物包括,尤其是,tpa等等。典型的iaci方案包含几个小时的5到30cc/分钟的灌注,导致总盐水灌注为大约2公升到3公升。要求打算向中风病人实施iaci方案(为了缺血性脑损伤的神经保护)的临床实践者确定留置导管的最合适大脑目标位置。常规脑扫描技术包括,尤其是,mri、ct等等,其检测缺血性梗塞的三维边界和它的相关半影子,目的是为了将缺留置导管精确放置在血性梗塞的上游。脑扫描还包括关于动脉和/或静脉的闭塞程度信息、血管中的血流量和神经细胞的灌流(perfusioninneurons)。临床实践者使用的常规荧光检查单元能够相当精确地将留置导管放置在期望的位置。但是动脉障碍会导致灌注流从它的预期动脉到邻接动脉的相当大比例的改道,由此不冷却闭塞的下游半影。而且,留置导管还可以导致输入的盐水的流态的相当大的改变,这归因于与放置它的脑动脉相比它的相对较大尺寸。因此,很难预测半影正在被冷冻的灌注流冷却到什么程度。
美国圣地亚哥的塞茂普特克斯公司(thermopeutix,inc.,sandiego,usa)正在研发用于选择性冷却目标部位的系统和方法,包括具有供给内腔和递送内腔的导管,该供给内腔和递送内腔具有进口和出口。血液从供给内腔抽取并且在控制单元中冷却或加热。处理的血液经由递送内腔发送到目标区。塞茂普特克斯公司是,尤其是,美国专利号8,192,392(名称为选择性热处理的方法(methodsforselectivethermaltreatment),发明人是solar等人)的受让人。
神经保护装置和方法的公开包括:尤其是,由matthewaaronharoldneimark等人在神经介入手术杂志(journalofneurointerventionsurgery),2013;5:165-171上发表的“利用血管内颈动脉冷盐水灌注(icsi)选择性冷却期间的脑温度改变:使用利用积分数学模型拟合的人数据模拟(braintemperaturechangesduringselectivecoolingwithendovascularintracarotidcoldsalineinfusion(icsi):simulationusinghumandatafittedwithanintegratedmathematicalmodel)”公开了3d热模型,该3d热模型用于确定3d空间中球形截面的温度。该文章公开了使用明显优势的内部颈静脉血球温度(jugularvenousbulbbloodtemperature)(jvbt)作为同侧脑温度的替代。该文章公开了3d热模型按照两种模式被应用:(1)正演模型模式,其使用每个病人的特定最初状况运行3d热模型;(2)反演模型模式,其针对该模型拟合测量的jvbt数据。正演模式的输出提供预期的颈静脉温度,该预期的颈静脉温度可用做验证模型保真度的粗平均值(roughmeansofvalidatingmodelfidelity)。反演模式的输出提供颅内脑温度的评估(这可用作更好地评价icsi可行性的手段)以获得治疗脑温度。该文章讨论了颈静脉血液包含来自两个大脑半球的血液引流表面和深层脑组织的混合物(blooddrainingsuperficialanddeepbraintissue),幕下脑和颅外组织,这样有利于更精确测定颈动脉冷盐水灌注期间的实际的脑或同侧前循环区域(ipsilateralanteriorcirculationterritory)(iact)的温度。
美国专利号8,343,097(名称为:血管内冷却的系统和方法(systemsandmethodsforintravascularcooling),发明人为pile-spellman等人)公开了一种留置导管,该留置导管具有沿着它的多个传感器和反馈系统,该反馈系统被用于根据感应到的温度控制灌注液(infusate)的体积、温度和/或灌注液速度以在目标位置达到预定温度。美国专利号8,343,097图8显示了导引导管80,其用于引导用于递送灌注液的微导管86。纵向邻近微导管86的是电线92,电线92具有用以测量灌注液和血液混合物的参数的传感器96,用以测量参数(例如微导管86远端88处的注入液温度)的传感器98,用于测量回流的传感器100,和布置用于测量病人血液参数(例如病人核心身体温度)的传感器102。
需要一种神经保护装置,用于在诱发全身或局部脑低温的三个阶段期间帮助临床实践者监视脑温度,三个阶段如下:阶段1,用于将人脑从正常37℃身体核心温度冷却到稳态低温。阶段2,用于将人脑维持在稳态低温。阶段3,用于将人脑从稳态低温升温到正常37℃身体核心温度。还进一步需要改进的动脉冷物灌注(iaci)方案的实施,用于诱发局部脑低温。
技术实现要素:
本发明针对一种神经保护装置,该神经保护装置包括头皮温度测量获取机构(scalptemperaturemeasurementacquisitiondevice)和神经保护处理器(neuroprotectionprocessor),该头皮温度测量获取机构用于在诱发型低温期间获取病人头皮上的多个位置的头皮温度测量值(scalptemperaturemeasurements),该神经保护处理器用于在诱发型低温期间处理该头皮温度测量值,用于实时确定病人温度信息,用于显示在显示器上的人头部图像上。
在灌注冷冻的灌注液时大脑温度变化需要至少几分钟以相继地使脑、头颅和头皮变冷以在病人头皮上诱发可检测的温度变化,这样,本发明的神经保护装置提供近几乎实时的临床反馈。另外,大脑温度变化还是病人头部中一个或多个冷灌注源的位置的函数。因此,在病人的右侧大脑中动脉(mca)中布置单个冷灌注源的情况下,可检测温度变化出现在病人头部左侧将需要更长时间,与他的右侧不同。而且,到达低温稳态之后,病人头部右侧将比他的左侧更冷。
神经保护处理器可处理获取的头皮温度测量值用于确定所谓的病人头皮等温线图(patientscalpisothermmap)。该头皮温度测量值可以是诱发型全身或局部脑低温的结果。病人头皮等温线图通常包括至少两个头皮等温线,即最里面的头皮等温线(它是最冷的头皮等温线)和最外面的头皮等温线(它是最暖的头皮等温线,相当于正常头皮皮肤温度,取决于环境温度通常在34℃到35℃范围内)。人头部图像可优选是病人的头部图像。
神经保护处理器可处理人头部的上部大致半球形部分(anuppergenerallyhemisphericalsectionofahumanhead)(包括它的脑、头颅和头皮)的3d热模型的热力学信息,用于确定所谓的病人3d温度估计绘图(patient3dtemperatureestimationmapping)。病人3d温度估计绘图包括在如由3d热模型界定的人头部的上部大致半球形部分内的3d有限要素的温度估计。合适的3d热模型在迄今提到的“braintemperaturechangesduringselectivecoolingwithendovascularintracarotidcoldsalineinfusion:simulationusinghumandatafittedwithanintegratedmathematicalmodel”,neimarketal.,publishedinjneurointerventsurg2013:5:1651-71doi:10.1136/neurintsurg-2011-010150”中有描述。
该3d热模型可用于诱发型全身或局部低温。在诱发型全身低温中,3d热模型模拟四个递送变冷的血液到人脑的冷灌注源,即右边一对颈动脉的和椎动脉和左边一对颈动脉的和椎动脉。在诱发型局部脑低温中,当冷的灌注源将灌注液递送到人脑时该3d热模型通常模拟单个留置导管尖。通过该单个留置导管递送的灌注液可以是盐水、血液、混合的血液盐水灌注物等等。该3d热模型处理与冷灌注源有关的流参数(flowparameters),包括,尤其是,灌注温度、灌注流速等等。该流参数可从合适的留置导管得到,该留置导管在它的导管尖配备必需的传感器。而且,该神经保护处理器处理留置导管的导管尖的位置。该神经保护处理器可显示一个或多个标准的矢状面(sagittalplanes)、截向面(transverseplanes)和冠状面(coronalplanes),以及临床实践者选择的横截面上的3d有限要素的温度评估。该神经保护处理器优选显示有关病人头部的mri/ct扫描图像的3d有限要素的3d温度估计绘图。
根据本发明,一个优选具体实施方式的头皮温度测量获取机构(scalptemperaturemeasurementacquisitiondevice)包括一个或多个用于获取头皮温度测量值的热成像相机。根据本发明,另一个优选具体实施方式的头皮温度测量获取机构包括在与病人头皮接触的皮肤中的温度测量传感器阵列,该温度测量传感器阵列用于获取头皮温度测量值。所述头皮温度测量获取机构可包括用于病人的头皮外部冷却的头皮冷却装置(scalpcoolingarrangement),用于帮助中风脑的诱发型局部低温。该头皮温度测量获取机构可被设计为一次性医疗级别物品,用来供单个病人使用。或者,该头皮温度测量获取机构可被用来供多个病人使用。具有在与病人头皮接触的皮肤中的温度测量传感器阵列的单个病人使用头皮温度测量获取机构可以像弹力修身游泳帽(stretchfitswimcaps)。
该神经保护装置可包括计算机数据库,该计算机数据库具有基准中风脑临床图像(benchmarkstrokebrainclinicalimages)的基准中风脑临床图像集合(abenchmarkstrokebrainclinicalimagecollection)。每个该基准中风脑临床图像都包括闭塞、缺血性梗塞和下游半影区。该基准中风脑临床图像在缺血性梗塞的位置、闭塞百分比和相关半影区的大小方面存在不同。该基准中风脑临床图像还优选包括临床说明,该临床说明包括留置导管的放置、灌注液流速、灌注液温度和用于投予灌注液的灌注液持续时间的至少一个。临床实践者可参考该基准中风脑临床图像集合以帮助他为特定中风病人决定最合适的iaci方案。
该计算机数据库还可包括基准温度信息,该基准温度信息用于帮助临床实践者监控诱发型全身或局部脑低温。该基准温度信息可帮助临床实践者决定在实施iaci方案期间他是否需要调整留置导管的位置,灌注液温度和灌注液流速的一个或多个,由此提高它们的神经保护功效。该基准温度信息可在诱发型全身或局部脑低温的三个阶段期间帮助临床实践者。该基准温度信息可包括基准头皮等温线图的基准头皮等温线图集合和/或基准3d温度估计绘图的基准3d温度估计绘图集合。该基准头皮等温线图的基准头皮等温线图集合与基准中风脑临床图像的基准中风脑临床图像集合相互参照。类似地,该基准3d温度估计绘图的基准3d温度估计绘图集合与该基准中风脑临床图像的基准中风脑临床图像集合相互参照。
该神经保护作用处理器可被编程以在进行的诱发型全身或局部脑低温(anongoinginducedsystemicorlocalbrainhypothermia)期间比较获取的病人头皮温度测量值与相应的基准温度信息以确定基准误差指数。基准指数误差可用于指示一系列需要校正动作的临床事件。实例性的临床事件包括,尤其是,错误的人脑区域正在被冷却,人脑正在变冷到太低的低温温度,人脑正在以比优选的0.5℃升温速度高的速度升温,等等。该神经保护作用处理器可以比较该基准错误指数与基准误差阀值以自动发出报警,用于提醒临床实践者。
附图的简要说明
为了理解本发明并且看清楚它在实践中是如何实施的,现在仅仅通过非限制性例子参考相应的附图描述优选的具体实施方式,附图中同样的部分被同样地编号,并且其中:
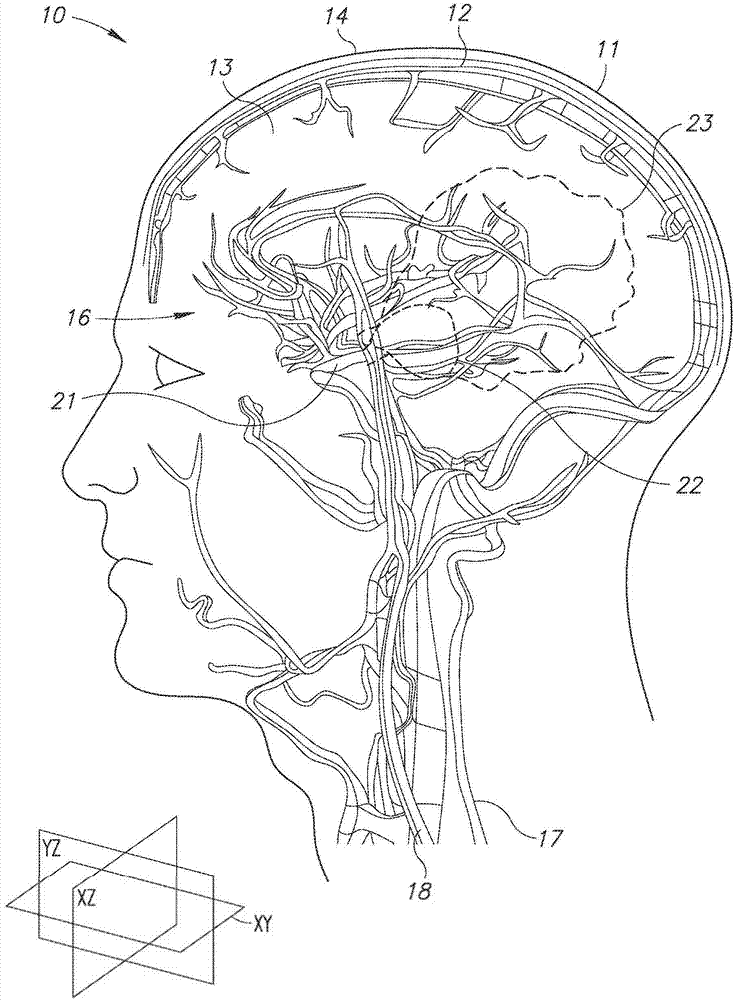
图1是中风病人的人头部示意图,该中风病人患有缺血性梗塞和下游半影区;
图2是神经保护装置的示意图,该神经保护装置用于在实施iaci方案期间的在人头部图像上显示病人头皮等温线图;
图3a到3d是显示实施iaci方案期间的中风病人头皮从它的起初态(inception)到稳定低温(steadystatehypothermia)的渐进冷却的示意图;
图4是神经保护装置的示意图,该神经保护装置用于在实施iaci方案期间的在人头部图像上显示病人头皮等温线图和病人3d温度估计绘图;
图5a到5d是显示图4的病人3d温度估计绘图和三个不同横截面的示意图;
图6是神经保护装置的示意图,该神经保护装置用于在人头部图像上显示病人头部等温线图和病人3d温度估计绘图,该病人处于诱发型全身低温之后的稳态低温;
图7是第一个具体实施方式的神经保护装置的头皮温度测量获取机构的示意图;
图8是第二个具体实施方式的神经保护装置的头皮温度测量获取机构的示意图;
图9是第三个具体实施方式的神经保护装置的头皮温度测量获取机构的示意图,类似弹力修身游泳帽;
图10是病人穿着图9的头皮温度测量获取机构的后视图;
图11是用于诊断中风病人的临床组件的示意图;
图12是用于将留置导管放置在中风脑的大脑目标位置的临床组件的示意图;
图13a是沿非中风脑的冠状截面的示意临床图像,显示了留置导管放置在大脑目标位置;
图13b是显示人头部图像和低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图13a留置导管的放置和12℃盐水灌注的15cc/分钟流速造成的;
图13c是显示人头部图像和低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图13a留置导管的放置和12℃盐水灌注的10cc/分钟流速造成的;
图13d是显示人头部图像和低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图13a放置留置导管和18℃盐水灌注的10cc/分钟流速造成的;
图14a是沿中风脑的冠状截面的示意临床图像,该中风脑具有70%闭塞和放置的留置导管,该留置导管用于在它的相关半影区诱发局部低温;
图14b是显示人头部图像上的低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图14a留置导管的放置造成的;
图15a是沿中风脑的冠状截面的示意临床图像,该中风脑具有70%闭塞和放置的留置导管,该留置导管用于在它的相关半影区诱发局部低温;
图15b是显示人头部图像上的低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图15a留置导管的放置造成的;
图16a是沿中风脑的冠状截面的示意临床图像,该中风脑具有90%闭塞和放置的留置导管,该留置导管用于在它的相关半影区诱发局部低温;
图16b是显示人头部图像上的低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图16a留置导管的放置造成的;
图17a是沿具有90%闭塞的中风脑的冠状截面并且显示了使用微型导管穿过该90%闭塞用于递送冷的盐水顺流到它的相关半影区的示意临床图像;
图17b是显示人头部图像上的低温稳态的病人头皮等温线图的示意图,该病人头皮等温线图是由图17a留置导管的放置造成的;
图18是向中风脑实施iaci方案的方法流程图。
本发明优选具体实施方式的详细描述
图1显示了病人头部10,该头部10包括头皮11、头颅12和脑13。头皮11通常被描述为具有五个层,包括最外面的头皮皮肤表面14。在25℃的标准环境温度下,正常的最外面的头皮皮肤表面温度ts是大约34℃和大约35℃之间,该温度低于37℃核心身体温度。脑13包括大脑循环结构16,该循环结构16包括一对右侧颈动脉17和椎动脉18(arightpairofacarotidartery17andavertebralartery18)。大脑循环结构16同样包括一对左侧颈动脉和椎动脉(aleftpairofacarotidarteryandavertebralartery)(未显示)。该对右侧和该对左侧颈动脉和椎动脉(eachpairoftherightpairandleftpairofacarotidarteryandavertebralartery)的每一对都递送大约350cc/分钟的组合血流速度。
病人是中风受害者,具有中风脑,该中风脑具有位于,例如,沿大脑中动脉(mca)的闭塞21。闭塞21通常会占据大脑动脉截面直径的从大约70%到大约90%。闭塞21导致缺血性梗塞22和下游半影区23。图1还显示了包括xy横向面、xz矢状面和yz冠状面的cartesian坐标系。
神经保护装置
图2显示了神经保护装置100,该神经保护装置100包括头皮温度测量获取机构101和神经保护处理器102a。头皮温度测量获取机构101用于在诱发型局部脑低温期间获取病人头皮上的多个位置的头皮温度测量值,神经保护处理器102a用于在诱发型局部脑低温期间处理获取的头皮温度测量值,用于实时确定病人头皮等温线图103,用于显示在显示器104上的人头部图像上。神经保护处理器102a运行等温线判定算法,用于处理获取的头皮温度测量值,用于实时确定病人头皮等温线图103。病人头皮等温线图103优选是彩色的,用多种颜色编码,利用蓝色/绿色调表示较冷的等温线,以及红色/橙色/黄色调表示较暖的等温线。
图2显示了神经保护装置100,神经保护装置100用于确定在通过留置导管204向中风病人实施iaci方案期间的病人头皮等温线图103。图2同样能显示使用神经保护装置100用于确定诱发型全身低温期间的病人头皮等温线。显示器104可以是电脑显示屏、可穿戴显示器等等。头皮温度测量获取机构101可以可选择地配备头皮冷却装置(scalpcoolingarrangement)106,头皮冷却装置106用于病人头皮的外部冷却,用于帮助诱发型全身或局部低温。
神经保护装置100包括用于录入病人信息和诱发型低温过程详情的操作界面107。病人详情包括,尤其是,名字、年龄、体重等等。诱发型低温过程详情包括,尤其是,日期、时间、临床实践者等等。操作界面107还能够使临床实践者在自由文本框中写入注释。
图3a到3d显示了在实施iaci方案期间中风病人头皮的渐进冷却,从在正常头皮皮肤温度ts的起初态到低温稳态,正如中风病人头皮上的冷点的形成所证明的。图3a显示了在开始实施iaci方案之前的病人头皮等温线图117,该病人头皮等温线图117包括正常头皮皮肤温度ts。图3b显示了在例如实施iaci方案10分钟之后的病人头皮等温线图118,该病人头皮等温线图118包括最里面的33℃头皮等温线和最外面的34℃头皮等温线。图3c显示了在例如实施iaci方案20分钟之后的病人头皮等温线图119,该病人头皮等温线图119包括最里面的32℃头皮等温线,中间的33℃头皮等温线和最外面的34℃头皮等温线。图3d显示了在低温稳态的病人头皮等温线图121,该病人头皮等温线图121包括最里面的31℃头皮等温线、两个中间的32℃和33℃头皮等温线和最外面的34℃头皮等温线。
图3a到3d,颠倒次序,即从图3d到图3a显示了中风病人头皮的渐进升温,从低温稳态到正常头皮温度ts,正如来自中风病人头皮的冷点的消失所证明的。中风脑的升温通常比中风脑的冷却慢的多,并且以0.5℃每小时的优选速率进行。因此从图3d到图3a的渐进升温比从图3a到3d的渐进冷却花费更长时间。
图2显示了神经保护装置100优选包括用于帮助诱发型全身或局部脑低温的临床管理的计算机数据库111。计算机数据库111包括基准中风脑临床图像113的基准中风脑临床图像集合112。基准中风脑临床图像113是为了达到防止半影区的进一步梗塞的最佳效果分析多个中风病人的治疗的基础上制成的。基准中风脑临床图像113的每一个都包括闭塞、缺血性梗塞和下游半影区。基准中风脑临床图像113在闭塞的位置和百分比、缺血性梗塞、梗塞的大小和位置,以及它的相关半影区的大小和位置方面存在不同。
基准中风脑临床图像113优选包括优选的用于放置留置导管的大脑目标位置。基准中风脑临床图像113优选包括有关优选的灌注液温度、优选的灌注液流速和优选的用于投予灌注液的灌注液投予时间的说明。基准中风脑临床图像113还优选包括有关使用微型导管的说明,该微型导管用于穿过几乎100%闭塞,用于直接将冷灌注液递送到下游半影区。
计算机数据库111还优选包括呈基准头皮等温线图116的基准头皮等温线图集合114形式的基准温度信息。临床实践者可在诱发型全身或局部脑低温期间使用基准头皮等温线图集合114以帮助他判断病人的脑是否正在根据预定的临床协议冷却。类似地,临床实践者可在病人的脑从诱发型低温状态到正常核心身体温度的恢复期间使用基准头皮等温线图集合114以帮助它判断病人的脑是否正在根据预定的临床协议升温,以避免过快升温,过快升温会无意中导致神经损害。
基准头皮等温线图集合114可包括诱发型全身或局部脑低温的三个阶段(即,从正常核心身体温度到稳态低温,维持稳态低温,和从稳态低温到正常核心身体温度的升温)期间的不同时间间隔的基准头皮等温线图116。诱发型局部脑低温的稳态经常在10到20分钟内到达。诱发型全身低温的稳态经常花费长得多的时间。连续基准头皮等温线图116之间的合适时间间隔为,例如3到5分钟之间。基准头皮等温线图集合114可包括在不同灌注液温度和/或不同灌注液流速的灌注期间获取的基准头皮等温线图116。基准头皮等温线图集合114可包括在不同血液温度和/或不同血液速度和/或不同体重的诱发型全身低温期间获取的基准头皮等温线图116。
基准头皮等温线图116的实例性使用如下:临床实践者注意到冷点正在在中风头皮上的一个位置形成,该位置与为最好治疗中风病人它应当形成的位置不匹配。临床实践者决定重新定位留置导管的导管尖以相应地更改形成冷点的位置。
临床实践者注意到冷点正在在中风头皮上的一个位置形成,该位置与它应当形成的位置匹配,但是形成得太慢。临床实践者决定不重新定位留置导管的导管尖,而是在相同的灌注液流速下降低正在投予的灌注液温度。或者,临床实践者可以决定在相同灌注液温度下增加灌注液流速。或者,此外,临床实践者可以决定同时更改灌注液流速和灌注液温度。
临床实践者考虑到在从稳态低温恢复到正常身体核心温度时病人的脑升温太快。临床实践者决定他将灌注液流速降低得太多并且决定增加灌注液流速以使升温慢下来。或者,临床实践者决定他将灌注液温度增加得太多并且决定降低灌注液温度以使升温慢下来。
神经保护处理器102a可以被编程以将病人头皮等温线图叠加在基准头皮等温线图上以帮助临床实践者区别它们之间的不同。神经保护处理器102a可以被编程以比较在进行的诱发型全身或局部脑低温期间获取的头皮温度测量值与相应的基准头皮温度测量值以确定基准误差指数。该基准误差指数可以使用众所周知的用于比较两组实际值和基准值的统计技术确定。该基准误差指数可能可以包括用于不同等温线的权重因子,例如,最冷的等温线可以比最暖的等温线权重高。神经保护处理器102a可将基准误差指数与基准误差阀值比较以自动发出警报,用以提醒临床实践者。合适的警报包括,尤其是,可视警报、可听警报、sms等等。
图4是在利用留置导管204实施iaci方案期间的神经保护装置100的示意图。神经保护装置100包括神经保护处理器102b,神经保护处理器102b用以实时确定病人头皮等温线图122和/或病人3d温度估计绘图123,用于显示在显示器上的人头部图像上。病人头皮等温线图122可以以类似于神经保护处理器102a的方式被确定或来源于病人3d温度估计绘图123。
神经保护处理器102b运行人头部的上部大致半球形部分(包括它的脑、头颅和头皮)的3d热模型,用以确定病人3d温度估计绘图123。合适的3d热模型可以基于数学模型,该数学模型被描述在迄今描述的“braintemperaturechangesduringselectivecoolingwithendovascularintracarotidcoldsalineinfusion:simulationusinghumandatafittedwithanintegratedmathematicalmodel”,neimarketal.,publishedinjneurointerventsurg2013:5:1651-71doi:10.1136/neurintsurg-2011-010150中。病人3d温度估计绘图123包括3d热模型的3d有限要素的温度估计。3d热模型的3d有限要素可以是彩色的(以与头皮等温线图103类似的方式编码)。
人脑具有类似但是不完全相同的结构,这样,3d热模型仅仅能模拟实例性人脑但不是特定病人脑,留置导管的导管尖的放置位置可以仅仅被估计到几毫米之内,但是这样的几毫米可导致大脑血流的相当大的变化。而且,留置导管的存在和动脉中的梗塞可相当大地更改中风脑中的大脑血流和/或冷灌注液流。因此,神经保护处理器102b以两种模式运行3d热模型,如下:3d热模型配置模式(3dthermalmodelconfigurationmode)和配置的3d热模型进行的程序模型(onfigured3dthermalmodelongoingproceduremode)。3d热模型配置模式意在用于向手边的特定诱发型全身或局部脑低温配置某些3d热模型参数,包括在3d热模型内确定留置导管的导管尖位置。配置的3d热模型进行的程序模式运行配置的3d热模型,用于病人诱发型低温程序的剩余部分。
3d热模型配置模式:神经保护处理器102b处理与灌注源有关的流参数(flowparameters)和获取的头皮温度测量值,该与灌注源有关的流参数包括,尤其是,灌注温度、灌注流速、灌注持续时间等等。该流参数可以从合适的留置导管得到,该留置导管在它的导管尖安装有必要的传感器。神经保护处理器102b还处理人脑中的留置导管的导管尖的位置。流参数可以在操作界面107手动输入。或者,该流参数可以被自动输入到神经保护处理器102b。例如,导管尖的位置可由磁性传感器确定。
神经保护处理器102b可以仅仅在迭代闭环模式内以正演模型模式运行3d热模型,如下:神经保护处理器102b处理诱发型低温的流参数(包括留置导管的放置、灌注液流速和灌注液温度),用于确定病人头部的上部大致半球形部分的病人3d温度估计绘图。神经保护处理器102b比较病人头皮上的特定位置的3d温度估计值与在此处获取的头皮温度测量值以确定它们之间的差异。神经保护处理器102b可以计算特定头皮位置的3d温度估计值与在此处获取的头皮温度测量值之间的偏差,从至少数十个头皮位置直到成千上万个头皮位置,这取决于头皮温度测量获取机构101。更大数目的头皮位置被考虑提高神经保护处理器102b的精确度,但是缺点是每个3d热模型的运行花费更长的时间。
神经保护处理器102b根据计算的偏差确定偏差指数。该偏差指数可以使用众所周知的用于比较两组实际值和估计值的统计技术确定。该偏差指数可能可以包括用于不同等温线的权重因子,例如,最冷的等温线可以比最暖的等温线权重高。神经保护处理器102b比较计算的偏差指数与偏差阀值用于确定是否重新定位3d热模型中的留置导管的放置。例如,偏差指数可以是全部头皮位置(在该位置已经获取实际头皮温度测量值)的平均温度差,并且偏差阀值可以是±0.5℃温度差。偏差阀值可以由临床实践者借助操作界面107随意设定。
在偏差指数小于偏差阀值的情况中,神经保护处理器102b配置3d热模型。但是如果偏差指数大于偏差阀值,神经保护处理器102b更改3d热模型中的留置导管的放置位置,并且重新运行3d热模型。留置导管的放置位置可根据三个流参数选择用于重新模拟目的,因为灌注液流速和灌注液温度可被测量到比留置导管的放置位置(该留置导管的放置位置可根据荧光镜检查图像(fluoroscopyimage)估计)高得多的精确度。
更改留置导管在动脉内的放置位置的方向取决于头皮温度估计值是否是比实际头皮测量温度的温度高或比实际头皮测量温度的温度低。在特定头皮位置的情况中,如果此处的头皮温度估计值比在此处获取的头皮温度测量值冷,那么3d热模型假定的留置导管的放置位于比运行3d热模型时它实际的位置沿动脉更下游。因此3d热模型需要重新运行,留置导管放置在更上游。但是如果头皮温度估计值比在此处获取的头皮温度测量值暖,那么3d热模型假定的留置导管的放置位于比运行3d热模型时它实际的位置沿动脉更上游。因此3d热模型需要重新运行,留置导管被放置在更下游。
或者,神经保护处理器102b可以以同样的两个模型模式(正如迄今neimark文章所描述的)运行3d热模型,即,以正演模型模式和反演模型模式。在正演模型模式中,神经保护处理器102b处理与灌注源有关的流参数,包括,尤其是,灌注温度、灌注流速和它的位置。在反演模型模式中,神经保护处理器102b处理获取的头皮温度测量值。
配置的3d热模型进行的程序模式:配置之后,神经保护处理器102b在进行的低温期间继续定期运行配置的3d热模型以将病人头皮等温线122和/或病人3d温度估计绘图123显示在显示器上的人头部图像上。考虑到在诱发型全身或局部脑低温期间可能发生的事件,神经保护处理器100在进行的程序模式期间继续从病人头皮获取头皮温度测量值作为备份安全措施。实例性事件可包括,尤其是,留置导管的移动、大脑血流的变化、沿留置导管形成堵塞等等。因此,在病人3d温度估计值与获取的头皮温度测量值之间的漂移比可接受的漂移大的情况中,那么临床实践者必须调查漂移的来源。
存储基准温度信息的计算机数据库111可进一步包括基准3d温度估计绘图126的基准3d温度估计绘图集合124。基准3d温度估计绘图126可以在诱发型全身或局部脑低温的三个阶段(即,从正常核心身体温度到稳态低温的冷却,维持稳态低温,和从稳态低温到正常核心身体温度的升温)的不同时间确定。临床实践者可以在进行的诱发型低温期间和将病人的脑恢复到正常核心身体温度期间使用基准3d温度估计绘图作为临床参考。
图5a显示了病人3d温度估计绘图123,并且图5b到5d显示了三个间隔的横截面127、128和129,如下:图5b显示了位于病人的中脑部分的最低的横截面127。图5c显示了位于病人的胼胝体体部水平(patient’slevelofbodyofcorpuscallosum)的中间的横截面128。图5d显示了位于病人的上矢状窦(sss)的最高的横截面129。该留置导管递送冷盐水,位于最低的横截面127的下游和中间的横截面128的上游,使得后者128显示出比前者127大的制冷效应,正如中间的横截面128所证明的,横截面128具有最低的横截面127缺失的32℃等温线。
图6显示了包括神经保护处理器102b的神经保护装置100,神经保护处理器102b用于在诱发型全身低温期间使用,用于在诱发型全身低温期间实时确定呈病人头皮等温线图131和/或病人3d温度估计绘图132形式的病人温度信息,用于显示在显示器上的人头部图像上。神经保护装置100从诱发型全身低温的起初态到稳态低温、维持稳态低温,和对于从稳态低温到正常核心身体温度的低温脑的升温来说,被同样地利用。神经保护处理器102b处理变冷的血液(例如,来自心肺机133)和获取的头皮温度测量值。该变冷的血液从它的一对右侧颈动脉和椎动脉和它的一对左侧颈动脉和椎动脉被递送到病人的头部。图6显示了诱发型全身低温使病人的头部两侧同样地变冷,这与诱发型局部脑低温不同,诱发型局部脑低温通常变冷病人头部的一侧超过他的另一侧。
头皮温度测量获取机构
图7显示了头皮温度测量获取机构101a被用作一个或多个热成像相机141,用于获取病人头皮的头皮温度测量值。热成像相机141优选被布置为使得在病人头皮的特定位置获取的头皮温度测量值可以被计算为来自不同热成像相机141的两个或多个头皮温度测量值的平均值。热成像相机141在25℃到40℃的温度范围内优选具有50milikelvin的温度分辨率和大于50,000像素,并且在7.5到14μm的红外光谱波长工作。该热成像相机优选具有大约每秒10次刷新的动态温度图刷新率。合适的热成像相机141包括,尤其是,从opgal(www.opgal.com)可购买得到的thermapp相机。每个热成像相机141都包括具有大约20-30cm的短焦长度的光学透镜,用于给病人的头皮成像。
图8显示了头皮温度测量获取机构101b,其被实现为顶部开口的刚性头部覆盖物142,头部覆盖物142具有底面143和具有边(rim)146的细长外周表面144,用于放置病人的头部,使得头部覆盖物142界定适应病人头皮的腔147。优选地,覆盖物142由热绝缘材料制成,例如,具有5-10毫米层厚的泡沫聚苯乙烯的聚碳酸酯。覆盖物142包括一个或多个类似于头皮温度测量获取机构101a的热成像相机141。头部覆盖物142可选择地包括头皮冷却装置106,用于从腔147抽取热量q,用于冷却病人头皮。头皮冷却装置106可以可选择地通过热电空对空模块(thermoelectricair-to-airmodule)实现。
图9和10显示了头皮温度测量获取机构101c,类似由热绝缘材料制成的弹性修身游泳帽,例如,橡胶和泡沫聚苯乙烯的组合。头皮温度测量获取机构101c包括在与病人头皮接触的皮肤中的温度测量传感器阵列161,用于获取头皮温度测量值。合适的温度测量传感器包括,尤其是,热敏电阻、热电偶等等。头皮温度测量获取机构101c优选是一次性单个病人使用物品。头皮温度测量获取机构101c可以可选择地配备有用于病人头皮的外部冷却的头皮冷却装置106。
温度测量传感器阵列161包括四个对齐的温度测量传感器串162。四个对齐的温度测量传感器阵串162与矢状面xz同方向,位于病人头部的两侧。相邻温度测量传感器阵串162之间的优选分离角大约是α=15-20°。每个温度测量传感器阵串162都包括在病人前额骨上面的最前面的传感器163a和位于稍微高于病人顶骨的最后面的传感器163b。沿温度测量传感器串162的邻近传感器163之间的距离是大约5mm和15mm之间,这样,每个温度测量传感器串包括大约25个传感器。因此,头皮温度测量获取机构101c包括大约25x8=200个传感器163。传感器163优选从头皮温度测量获取机构101c的内表面突出大约0.5mm到1.5mm之间,用于便于与最外面的头皮皮肤表面13紧密接触。合适的传感器163包括,例如,从murataltd,japan购买可得的ncp系列热敏电阻。生物相容性导热凝胶或胶粘材料优选用于便于最外面的头皮皮肤表面14的热测量。
用于确定和实施iaci方案的临床组件(clinicalset-upfordeterminingandadministeringiaciregimes)
图11和12显示了临床组件200,用于向中风脑确定和实施iaci方案,以使半影区的其它梗塞最小化。
临床组件200包括用于扫描中风病人头部10的扫描单元201,用于在显示屏203上显示脑扫描202。脑扫描202可以沿xy横向面、xz矢状面、yz冠状面,和临床实践者选择的其它面。合适的扫描单元201包括mri扫描单元和ct扫描单元。mri使用缺乏用于确定缺血性梗塞的三维边界的扩散和用于确定它的相关上游半影区的三维边界的灌注。ct使用灌流和血管造影(perfusionandangiography)用于确定缺血性梗塞和它的相关上游半影区的三维边界。扫描单元201能够提供用于清晰可视大脑血液循环结构的脑扫描。
脑扫描202提供最初临床中风信息,包括,尤其是,闭塞的位置和它的闭塞百分比,它的最终缺血性梗塞的边界、它的相关上游半影区的边界等等。临床实践者根据脑扫描202确定留置导管204的优选大脑目标位置以最好地诱发半影区23的治疗低温,以防止进一步梗塞。
合适的留置导管204包括,尤其是,具有3到5french尺寸的大脑血管造影诊断导管。留置导管204通常经由鞘导引器(sheathintroducer)(未显示)引入。合适的血管造影诊断导管包括,尤其是,从meritmedicalsystems,inc.,utah,usa(www.meritoem.com)购买可得的performa系列simmons2导管。这样的留置导管204包括用于保留在病人外部的近端204a和用于放置在大脑目标位置的远端204b。远端204b包括用于x射线成像目的不透明标志(opaquemarking)204c。这样的留置导管204包括用于能够使它航行到优选大脑目标位置的操舵工具。这样的留置导管204优选包括绝缘物,以避免加热从中风病人外部的它的近端到在优选大脑目标位置的它的远端的冷盐水。留置导管204可以可选择地是开口冲洗冷冻导管,正如pct国际申请号pct/il2013/050363(发明名称为具有冷却液冷却的热电组件的冷冻导管(cryocatheterwithcoolantfluidcooledthermoelectricmodule),以wipo国际公开号wo2013/164820公开)中所描述的。
临床组件200包括荧光检查单元207,用于帮助临床实践者将留置导管204放置在优选的大脑目标位置。荧光检查单元207在显示屏209上显示中风脑12的脑图像208和具有不透明标志204c的远端204b。临床组件200包括冷盐水的盐水源211和用于控制向中风病人实施iaci方案的控制装置212。控制装置212包括用于向中风病人投予冷盐水的蠕动泵(peristalticpump)213。
基准中风脑临床图像和基准头皮等温线图
图13a、14a、15a、16a和17a显示了颈内动脉(ica)26在交叉点27处分为大脑前动脉(aca)28和大脑中动脉(mca)29。图13a、14a、15a、16a和17a显示了留置导管204的放置,沿ica26推进mca29的最近部分。图13b、13c、13d、14b、15b、16c和17d显示了低温稳态的头皮等温线图。
图13a显示了在非中风脑中的留置导管204的放置250,用于提供变冷盐水的输入流。
图13b显示了对15cc/分钟流速的12℃盐水灌注来说,根据在病人头皮上获取的头皮温度测量值确定的最终病人头皮等温线图251。病人头皮等温线图251具有最里面的31℃头皮等温线,显示了皮肤头皮温度范围从变冷的31℃到正常头皮温度ts。
图13c显示了对于10cc/分钟流速的12℃盐水灌注来说,根据在病人头皮上获取的头皮温度测量值确定的最终病人头皮等温线图252。病人头皮等温线图252具有最里面的32℃头皮等温线,显示了皮肤头皮温度范围从变冷的32℃到正常头皮温度ts。病人头皮等温线图252与病人头皮等温线图251的比较显示了较低流速导致可预期的较小制冷。
图13d显示了对于10cc/分钟流速的18℃盐水灌注来说,根据在病人头皮上获取的头皮温度测量值确定的最终病人头皮等温线图253。病人头皮等温线图253具有最里面的33℃头皮等温线,显示了皮肤头皮温度范围从变冷的33℃到正常头皮温度ts。病人头皮等温线图253与头皮等温线图252的对照显示了较高的盐水灌注温度导致可预期的较小制冷。
图14a显示了沿mca29的70%闭塞254,位于相同的留置导管204的放置250的下游,例如约1cm。闭塞254导致梗塞256和下游半影区257。图14a显示了对来自预期下游半影区257大脑的其它部分来说,70%闭塞254将小部分的冷盐水的输入流从mca29转移到aca28。图14b显示了根据在病人头皮上的获取的头皮温度测量值确定的最终病人头皮等温线图258。病人头皮等温线图258具有最里面的32℃头皮等温线,显示了皮肤头皮温度范围从变冷的32℃到正常头皮温度ts。
图14b病人头皮等温线图258与图13b病人头皮等温线图251的比较显示了病人头皮等温线图258没有31°等温线,证实了冷灌注的更多制冷效应被分散到中风脑的其他区域,没有帮助必需冷却的半影区257。
图15a显示了留置导管204的放置259,位于70%闭塞254的上游,例如2cm。图15a显示了更朝向交叉点27靠近的留置导管204的放置,导致比图14a的放置250大得多的冷盐水的输入流从半影区257的转移。图15b显示了根据在病人头皮上获取的头皮温度测量值确定的最终病人头皮等温线图261。病人头皮等温线图261具有最里面的33℃头皮等温线,显示了皮肤头皮温度范围从变冷的33℃到正常头皮温度ts。iaci方案在最外面的头皮皮肤表面14的制冷效应减少是由于变冷的盐水主要从预期半影区257转移。
图15b和图14b的比较显示了图14a的留置导管204的放置250比图15a的留置导管204的放置259更有效地预防半影区257中的其它梗塞。因此,计算机数据库111优选包含基准中风脑临床图像112和基于图14a和14b而不是图15a和15b的基准头皮等温线图113。
图16a显示了90%闭塞262,其导致梗塞263和相关的下游半影区264。90%闭塞262通常导致比70%闭塞254的半影区257大的半影区264。图16a显示了留置导管204的放置266,用于提供变冷的盐水的输入流,用于使半影区264变冷。图16a显示了与图14a和15a相比,闭塞262将大部分输入的变冷盐水从用以使半影区264变冷的流向下游转移。
图16b显示了根据在病人头皮上获取的头皮温度测量值确定的最终病人头皮等温线图267。病人头皮等温线图267具有最里面的33℃头皮等温线,显示了皮肤头皮温度范围从变冷的33℃到正常头皮温度ts。病人头皮等温线图267和病人头皮等温线图258的比较显示病人头皮等温线图267具有比病人头皮等温线图258小的33°头皮等温线图,证明了冷灌注的更多制冷效应被分散到中风脑的其它区域中,没有帮助必需冷却的半影区264。
图17a显示了与图16a相同的留置导管204的放置266,以及使用微型导管268穿过90%闭塞262,用于递送冷盐水至此上游,例如1cm(fordeliveringcoldsalineupstreamtherefrombysay,1cm)。图17b显示了从病人的头皮上获取的最终病人头皮等温线图269。图17b显示了与病人头皮等温线图267相比,用于预防半影区264中的其它梗塞的微型导管268的有益效果。
向中风脑实施iaci方案的方法
图18是流程图,显示了使用神经保护装置100帮助向中风病人实施iaci方案。该使用包括,尤其是,下面的步骤:
步骤1:临床实施者获取中风脑的脑部扫描。
步骤2:临床实施者比较获取的脑扫描与基准中风脑临床图像集合,以选择与获取的脑扫描最紧密匹配的基准中风脑临床图像。
步骤3:临床实践者将留置导管插入在优选的大脑目标,用于根据选择的基准中风脑临床图像向中风脑实施iaci方案。
步骤4:临床实践者设置临床组件,以在灌注液预定的温度和预期的流速递送灌注液。
步骤5:临床实践者设置神经保护装置以获取病人头皮温度测量值。
步骤6:临床实践者利用神经保护装置监控iaci方案的三个阶段并且如果需要进行校正。
第1阶段:将病人头皮从正常头皮温度ts冷却到稳态低温。
第2阶段:将病人头皮维持在稳态低温。
第3阶段:将病人头皮从稳态低温升温到正常头皮温度ts。
在神经保护处理器102a和基准头皮等温线图集合114的情况中,临床实践者比较获取的病人头皮等温线图与相当于基准中风脑临床图像的基准头皮等温线图,以确定获取的病人头皮等温线图是否在可接受容限内。肯定地说,不要求临床实践者进行任何校正动作。否定地说,临床实践者应该进行校正动作,目的是减少获取的病人头皮等温线图与基准头皮等温线图之间的差异。这样的修正可以包括一次或多次移动留置导管,改变灌注液温度和改变灌注液流速。
例如,如果获取的脑扫描类似于图14a的基准中风脑临床图像,并且临床实践者疏忽地根据图15a的放置259,而不是根据图14a的放置250放置了留置导管,那么最终病人头皮等温线图类似于图15b的最终病人头皮等温线图261。因此,临床实践者会进行校正动作以将留置导管移动到图14a的放置250,使得最终病人头皮等温线图可在很大程度上匹配图14b的病人头皮等温线图258。
临床实践者可以以类似的方式利用神经保护处理器102b和基准3d温度估计绘图126的基准3d温度估计绘图集合124。
虽然对本发明的描述仅涉及有限个具体实施方式,但是应理解可在附件的权利要求书的范围内做出对本发明做出许多变化,修改和其它应用。
- 还没有人留言评论。精彩留言会获得点赞!