一种用于炮制白术的枳实汁及其提取方法与流程
本发明涉及一种用于炮制白术的枳实汁及其提取方法,属于医药领域。
背景技术:
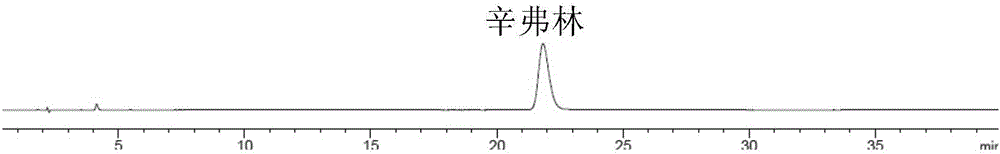
:枳实为芸香科植物酸橙(CitrusaurantiumL.)及其栽培变种或甜橙(C.sinensisOsbeck)的干燥幼果,主治积滞内停、痞满胀痛、大便秘结、泻痢后重。现代研究表明,枳实所含化学成分复杂,主要包含挥发油、黄酮类成分以及辛弗林、乙酰去甲辛弗林、N─甲基酪胺、γ─氨基丁酸、维生素A、B、C等等。枳实既是一种药,又可作为辅料用于炮制白术(AtractylodesmacroephalaKoidz.)。清代《握灵本草》记载了“枳实煎水渍炒”炮制白术的方法。经枳实汁炮制后,可达到缓和白术燥性,增强健脾和中理气的作用。然而,迄今为止对于枳实制白术的研究极少,此炮制方法仅见于古代文献中的粗略记载,未通过现代手段进行研究与剖析。作为炮制白术的辅料,枳实汁制备工艺的规范化及其质量的标准化对于白术炮制品药效的发挥具有重要意义。因此,亟需提供一种稳定可行的提取方法,以提取得到可用于炮制白术、使炮制品能够充分发挥祛燥健脾作用的枳实汁。技术实现要素:本发明的目的在于提供一种用于炮制白术的枳实汁及其提取方法。本发明提供了一种用于炮制白术的枳实汁的提取方法,包括如下步骤:称取枳实,加6~16倍体积量水,浸泡0~2.0h,煮沸0.5~3h,滤过,药渣重复提取1~2次,滤过,合并滤液,浓缩,即得。进一步地,所述枳实粒径为0.8~8mm。进一步地,所述枳实粒径为2~8mm。进一步地,浸泡时间为0~1.0h。进一步地,每次煮沸时间为1~1.5h。进一步地,每次提取加8~14倍体积量水。进一步地,浓缩至1mL枳实汁对应0.2g枳实。进一步地,所述的制备方法包括如下步骤:称取枳实,加12倍体积量水,浸泡0.5h,煮沸1.5h,滤过,药渣重复提取1次,滤过,合并滤液,浓缩,即得。本发明提供了根据所述制备方法提取得到的枳实汁。本发明提供了所述的枳实汁在制备白术炮制品中的用途。枳实含有复杂的化学成分,发明人经过前期研究,发现枳实提取物中辛弗林含量与枳实制白术炮制品药效的发挥具有较强的相关性。因此,本发明以辛弗林作为指标,通过考察提取过程中的各种条件参数,提供了一种稳定可行的枳实的提取工艺。采用本发明枳实汁炮制白术后,显著增强了白术的健脾作用,并能缓和其燥性。显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。附图说明图1为实验例2中阴性对照的专属性试验HPLC图;图2为实验例2中辛弗林对照品的专属性试验HPLC图;图3为实验例2中供试品的专属性试验HPLC图。具体实施方式本发明具体实施方式中使用的原料、设备均为已知产品,通过购买市售产品获得。实施例1本发明枳实汁的提取工艺称取枳实100g,加1430mL水浸泡30min,煮沸1.5h,滤过,药渣再加1200mL水煮沸1.5h,滤过,合并滤液,浓缩至500mL,即得本发明枳实汁。其中,1mL枳实汁相当于0.2g枳实提取原料。以下通过实验例证明本发明的有益效果。实验例1本发明枳实汁的功效实验1.实验材料1.1实验动物SPF级SD大鼠,体质量170-210g,雌雄各半,由四川省人民医院提供,动物合格证号:川实动管质SCXK(川)2013-15。SPF级KM小鼠,体质量18-22g,雄性,由四川省人民医院提供,动物合格证号:川实动管质SCXK(川)2013-15。1.2实验药物及试剂阳性药物蒙脱石散(规格3g,厂家:四川维奥制药有限公司,批号:151010);生白术饮片(1603025);枳实饮片(1603012);大黄饮片(批号:1603058);白术药液自制(浓度0.5g/ml);枳实制白术药液自制(1%枳实制白术药液,浓度0.5g/ml;5%枳实制白术药液,浓度0.5g/ml;10%枳实制白术药液,浓度0.5g/ml);大黄药液(自制);药液制备方法见以下实验方法部分;大鼠血清免疫球蛋白(IgG,批号:20160712)、大鼠血清免疫球蛋白(IgM,批号:20160712),均购于南京建成生物工程研究所;大鼠胃泌素ELISA试剂盒(GAS,批号:294r0714)、大鼠胃动素ELISA试剂盒(MTL,批号:434r0714)均购于天津安诺康生物技术有限公司;其余试剂均为分析纯。1.3实验仪器手术钳、手术剪、十万分之一分析天平(型号:BS323S、精度:0.001,北京赛多利斯仪器系统有限公司);优普纯水制造系统,数控超声波清洗器(型号:DL720D,上海之信仪器有限公司);ThermoScientific酶标仪(型号:CD3001,上海精科仪器厂);ThermoScientific离心机(型号:BC321,上海精科仪器厂);ACCU-CHEK血糖测定仪(Performa,Roche,USA);ACCU-CHEK血糖试纸(Performa,批号:474642,Roche,USA)。2.实验方法2.1药液制备2.1.1大黄药液将生大黄粉碎,用五倍体积量水浸泡30分钟后,煎煮15分钟,过滤,静置,取上清液,在50℃下浓缩至1g/mL,即得。2.1.2白术液称取生白术饮片,适当粉碎,加八倍体积量水,浸泡半小时,回流提取两次,每次1.5h,过滤,收集滤液,在60℃下浓缩至0.5g/mL,即得。2.1.31%枳实制白术液炮制:取生白术药材,加入枳实汁50mL(枳实汁的制备工艺同实施例1),对应的枳实提取原料为白术药材重量的1%,浸泡24h,不时翻动,直至汁尽药透,于药材温度为110℃炒制6min,取出,于40℃烘箱烘制24h,即得枳实制白术炮制品。称取枳实制白术(1:100)饮片,适当粉碎,加八倍体积量水,浸泡半小时,回流提取两次,每次1.5h,过滤,收集滤液,在60℃下浓缩至0.5g/mL,即得炮制品提取液。2.1.45%枳实制白术液炮制:取生白术药材,加入枳实汁50mL(枳实汁的制备工艺同实施例1),对应的枳实药材用量为白术的5%,浸泡24h,不时翻动,直至汁尽药透,于药材温度为110℃炒制6min,取出。于40℃烘箱烘制24h。即得。称取枳实制白术(5:100)饮片,适当粉碎,加八倍体积量水,浸泡半小时,回流提取两次,每次1.5h,过滤,收集滤液,在60℃下浓缩至0.5g/mL,即得。2.1.510%枳实制白术液炮制:取生白术药材,加入枳实汁50mL(枳实汁的制备工艺同实施例1),对应的枳实药材用量为白术的10%,浸泡24h,不时翻动,直至汁尽药透,于药材温度为110℃炒制6min,取出。于40℃烘箱烘制24h。即得。称取枳实制白术(10:100)饮片,适当粉碎,加八倍体积量水,浸泡半小时,回流提取两次,每次1.5h,过滤,收集滤液,在60℃下浓缩至0.5g/mL,即得。2.2动物分组小鼠:实验动物适应性饲养3天后,按体质量分层随机分为正常组、白术组、1%枳实制白术组、5%枳实制白术组、10%枳实制白术组,每组12只;大鼠:实验动物适应性饲养3天后,按体质量分层随机分为正常组、模型组、阳性药组、白术组、1%枳实制白术组、5%枳实制白术组、10%枳实制白术组,每组10只。2.3动物给药方法小鼠:在各组水瓶中精密加入200ml水,每日清晨,正常组灌胃等量生理盐水,其余各组灌胃相应药液0.3ml/只,正常进食24小时后测量水瓶中的剩余水量,计算出每只小白鼠的平均饮水量,连续7天;大鼠:分组后,正常组灌胃生理盐水4mL,其余各组灌胃大黄药液4ml,上下午各1次,共9d。第10d称重后,正常组、模型组上午灌胃等量生理盐水,阳性组、白术组、1%枳实制白术组、5%枳实制白术组、10%枳实制白术组上午灌胃相应的药液4ml,下午正常组灌胃等量生理盐水,其余各组均灌胃等量的100%生大黄液,连续10天。大鼠生化指标测定:最后一次给药后进食12h,测定大鼠血糖水平;腹股动脉取血后,脱颈处死,剖腹取脾脏、胃组织,用滤纸吸干脾脏组织液,称重,计算脾脏指数,取全血3500r/min离心10min后取上清液,用ThermoScientific酶标仪测定血清中血清蛋白IgG、IgM水平,取部分胃组织匀浆,3500r/min离心10min后取上清液,用ThermoScientific酶标仪测定胃组织中胃泌素、胃动素水平。数据统计分析:数据采用“均数±标准差”(x±s)表示,采用SPSS19.0统计软件包进行分析,组间比较采用twowayANOVA,posthocTtest在每个组样本量相同的情况下采用tukey'sttest,样本量不等采用LSD-Ttest;方差不齐的情况下,组间比较采用Brown-Forsythe的修正值。3.结果3.1小鼠体重结果表1小鼠体重(g)变化表注:与正常组比较:*P<0.05;与白术组比较:△P<0.05实验结果:与正常组相比,白术组体重有上升趋势,但两组间无显著性差异(P>0.05);与正常组相比,枳实制白术三个实验组均有显著上升(P<0.05);与白术组相比,枳实制白术三个实验组均有显著上升。以上结果表明,生白术的健脾作用不强,给药后小鼠体重未见明显提升;经本发明枳实汁炮制后,白术提升体重的效果显著增强,表明根据本发明提取工艺制备的枳实汁确能增强白术健脾强胃的功效。3.2小鼠饮水量结果表2小鼠平均每只每天饮水量(mL)注:与正常组比较:*P<0.05;与白术组比较:△P<0.05实验结果:与正常组相比,白术组小鼠饮水量第3天后显著上升(P<0.05);与正常组相比,枳实制白术三个实验组饮水量均无明显变化;与白术组相比,枳实制白术三个实验组饮水量均显著下降(P<0.05)。以上结果表明,生白术燥性较强;经本发明枳实汁炮制后,小鼠饮水量显著降低,表明根据本发明提取工艺制备的枳实汁确有抑制白术燥性的功效。3.3大鼠体重结果表3大鼠体重(g)变化表注:与正常组比较:*P<0.05;与白术组比较:△P<0.05实验结果:第5天,与正常组相比,其余组体重显著下降(P<0.05),与白术组相比,枳实制白术组体重显著上升(P<0.05);第9天,与正常组相比,其余组体重显著下降(P<0.05),与白术组相比,枳实制白术组体重显著上升(P<0.05);第15天,与白术相比,枳实制白术组体重显著上升(P>0.05);第19天,与白术组相比,枳实制白术组体重显著上升(P<0.05)。3.4大鼠血糖和脾脏指数结果大鼠血糖和脾脏指数测定结果如下表4,脾脏指数=脾脏重量/体重*100%。表4大鼠血糖及脾脏指数测定结果表注:与模型组比较:*P<0.05;与白术组比较:△P<0.05实验结果:大鼠血糖,与模型组相比,其余组显著下降(P<0.05);脾脏指数,与模型组相比,其余组显著上升(P<0.05),与白术相比,枳实制白术组显著上升(P<0.05)。3.5大鼠血清免疫球蛋白IgG、IgM测定结果表5大鼠免疫球蛋白IgG和IgM测定结果表注:与模型组比较:*P<0.05;与白术组比较:△P<0.05实验结果:大鼠血清免疫球蛋白IgG,与模型组相比,其余组显著上升(P<0.05),与白术相比,枳实制白术组显著上升(P<0.05);大鼠血清免疫球蛋白IgM,与模型组相比,其余组显著上升(P<0.05),与白术相比,枳实制白术组显著上升(P<0.05)。3.6大鼠胃组织胃动素、胃泌素测定结果胃动素(MTL)是由氨基酸组成的多肽,其分泌细胞集中分布于十二指肠和近端空肠粘膜窝内,在胃窦及下部小肠粘膜有少量存在,也存在于神经组织中。MTL主要功能是影响胃及肠道的动力,具有肠道“清道夫”的功效。胃动素水平升高,肠道蠕动加速,使肠内容物通过加快,临床表现为腹痛、腹泻等症状。胃泌素主要是由人体内细胞分泌的一种消化道激素,细胞以胃窦部最多,十二指肠次之,主要刺激壁细胞分泌盐酸,还能刺激胰液和胆汁的分泌,也有轻微地刺激主细胞分泌胃蛋白酶原等作用。表6大鼠胃动素、胃泌素测定结果表注:与模型组比较:*P<0.05;与白术组比较:△P<0.05实验结果:大鼠胃组织胃动素,与模型组相比,其余组显著下降(P<0.05);大鼠胃组织胃泌素,与模型组相比,其余组显著上升(P<0.05),与白术相比,枳实制白术组显著上升(P<0.05)。综合以上实验结果,与正常组相比,模型组大鼠体重、饮食量、自主活动量显著下降,大便不成形,泄泻症状明显,血糖水平升高,血清免疫球蛋白IgG、IgM水平显著下降,胃动素水平显著上升,胃泌素水平显著下降,综合以上辩证认为大鼠符合“脾虚泄泻”的中医模型。给予经本发明枳实汁炮制的白术后,大鼠的上述指标均有显著变化,且脾虚泄泻症状较生白术给药组有显著改善,表明经炮制后明显增强了白术的健脾功效。实验例2提取工艺中各条件参数对辛弗林转移率的影响1仪器与材料Agilent1260型高效液相色谱仪,Agilent公司;BT25S型1/10万电子分析天平,北京赛多利科学仪器有限公司;JA2003型1/1000电子分析天平,上海良平仪器仪表有限公司;BT25S电子天平,赛多利斯科学仪器(北京)有限公司。乙腈、甲醇均为色谱级,FisherScientific公司;水为超纯水,其他试剂均为分析纯(成都市科龙化工试剂)。枳实药材,批号1603012,购自四川科伦药业股份有限公司,经成都中医药大学中药鉴定教研室卢先明教授鉴定为芸香科植物酸橙(CitrusaurantiumL.)及其栽培变种或甜橙(C.sinensisOsbeck)的干燥幼果。辛弗林对照品购于中国药品生物制品检定所(供含量测定用,批号110727-201107)。2方法与结果2.1辛弗林的定量测定2.1.1色谱条件Agilentextend-C18色谱柱(250mm×4.6mm,5μm);流动相为甲醇-磷酸二氢钾溶液(取磷酸二氢钾0.6g,十二烷基磺酸钠l.0g,冰醋酸1ml,加水溶解并稀释至1000ml)(45:55)为流动相;体积流量1mL/min;柱温室温;检测波长275nm,进样量10μL。2.1.2对照品溶液的制备精密称取辛弗林对照品12.74mg,置于25mL容量瓶中,加适量水溶解,摇匀,超声30min,冷却,加水至刻度,摇匀,即得辛弗林对照品储备液。精密吸取4.6mL置10mL容量瓶中,加水至刻度,摇匀,即得辛弗林对照品溶液。2.1.3供试品溶液的制备精密量取枳实提取液5mL,置于10mL容量瓶中,加水至刻度,摇匀,过0.45μm微孔滤膜,备用。2.1.4专属性考察分别配制空白溶剂、对照品溶液、供试品溶液,按照“2.1”项下色谱条件进行试验,结果见图1~3。在该分析条件,辛弗林色谱峰理论塔板数大于5000,与其他组分的色谱峰分离良好,且无阴性干扰。结果表明,本方法具有较好的专属性。2.1.5线性关系考察分别准确移取“2.1.2”项对照品储备液适量,用甲醇稀释,制得辛弗林浓度分别为509.6、305.76、234.416、178.36、101.92、30.576ug/mL的混合对照品溶液,进样10μL测定。以对照品浓度(ug/mL)为横坐标(X),以峰面积积分值为纵坐标(Y),绘制标准曲线,经线性回归,回归方程为Y=4.53X-0.9649,r=0.99999,对照品辛弗林浓度在30.576~509.6μg/mL范围内线性关系良好。2.2辛弗林的转移率测定依据“2.1”项测得枳实汁中辛弗林的含量,按照转移率=(辛弗林含量×枳实汁体积/取样量中辛弗林质量)*100%的公式计算辛弗林转化率。以下实验中对药材的提取,均采用煎煮法进行。3实验结果3.1、枳实粒度对辛弗林转移率的影响分别称取枳实饮片、枳实粗颗粒(2-8mm)、枳实细粉(0.8-2mm)3份,每份100g,加8倍体积量水,提取两次,每次1.5h,合并滤液。提取液经HPLC检测,计算辛弗林转移率,结果见下表:表7枳实粒度对枳实提取液中辛弗林转移率的影响实验结果表明,枳实的粒度对辛弗林转移率产生明显影响,当枳实粒度为2-8mm时辛弗林转移率达到最高值。3.2、浸泡时间对辛弗林转移率的影响分别取枳实粗颗粒(2-8mm)5份,每份100g,加8倍体积量水,分别浸泡0、0.5、1.0、1.5、2.0h后,提取两次,每次1.5h,合并滤液。提取液经HPLC检测,计算辛弗林转移率,结果见下表:表8浸泡时间对枳实提取液中辛弗林转移率的影响实验结果表明,随着浸泡时间的增加,辛弗林的转移率先增加后减小,浸泡时间为0~1.0h时,辛弗林的转移率均能达到77%以上;其中,浸泡时间为0.5h时辛弗林的转移率达到最高。3.3、提取次数对辛弗林转移率的影响分别取枳实粗颗粒5份,每份100g,加8倍体积量水,浸泡0.5h后,分别提取1、2、3次,每次1.5h,合并滤液。提取液经HPLC检测,计算辛弗林转移率,结果见下表:表9提取次数对枳实提取液中辛弗林转移率的影响实验结果表明,提取次数对枳实汁提取过程影响显著,结合实际生产,提取2次为最佳。3.4、提取时间对辛弗林转移率的影响分别取枳实粗颗粒5份,每份100g,加8倍体积量水,浸泡0.5h后,提取2次,分别每次提取0.5h、1h、1.5h、2h、2.5h、3h,合并滤液。提取液经HPLC检测,计算辛弗林转移率,结果见下表:表10提取时间对枳实提取液中辛弗林转移率的影响实验结果表明,随着提取时间的增长,辛弗林的转移率先增加再减少,提取时间为1~1.5h时,辛弗林的转移率均能达到80%以上;其中,提取时间为1.5h时辛弗林的提取率最高。3.5、溶媒量对辛弗林转移率的影响分别称取枳实粗颗粒5份,每份100g,分别加6倍、8倍、10倍、12倍、14倍、16倍体积量水,浸泡0.5h后,提取2次,每次提取1.5h,合并滤液。提取液经HPLC检测,计算辛弗林转移率,结果见下表:表11溶媒量对枳实提取液中辛弗林转移率的影响实验结果表明,溶媒量对辛弗林转移率的影响显著,当溶媒量为8~14倍时,辛弗林的转移率均能达到80%以上;其中,溶媒量为8倍时辛弗林的转移率达到最高值。3.6、各提取参数对辛弗林转移率产生的综合影响分别称取枳实粗颗粒9份,每份100g,浸泡0.5h后分别按下表所示条件参数进行提取,合并滤液。提取液经HPLC检测,计算辛弗林转移率,结果见下表:表12各提取参数对枳实提取液中辛弗林转移率的影响编号提取次数提取时间溶媒量辛弗林转移率(%)111855.282211.51063.7523121270.5094211085.721521.51287.515622880.3017311287.854831.5882.5649321083.7491021.51290.390实验结果表明,最佳提取条件为:取枳实粗颗粒,加入12倍量水,浸泡30min,提取次数为两次,每次提取时间1.5h。实验例3本发明提取工艺的验证实验选取3批枳实饮片,均根据实验例2所述最优提取工艺进行验证,分别按照“2.1”“2.2”测定辛弗林的转移率,辛弗林转移率分别为89.08%、90.39%、89.75%,RSD为0.65%。验证结果说明本发明工艺条件稳定可行。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1