LGR4和R-spondin结合抑制剂及其在肿瘤治疗中的用途的制作方法
本发明涉及肿瘤免疫治疗领域,更具体地涉及lgr4和r-spondin结合抑制剂及其在肿瘤治疗中的用途。
背景技术:
肺癌是全球发病率和致死率最高的恶性肿瘤之一,由于饮食、环境、吸烟等多种因素的作用,肺癌在全球的发病率一直居高不下,每年均有数百万人被确诊为肺癌,其中绝大多数存活率不超过五年,肺癌已成为严重威胁人类健康和生命的一大痼疾。严重的骨转移和频繁的复发率是导致肺癌病人死亡的主要原因,由于肺部特殊的结构构造和细胞构成,同时肺癌细胞往往具有较低的免疫原性,造成多种靶向疗法和免疫疗法的治疗作用极其有限。肺癌发生时往往在肺部形成特殊的肿瘤微环境,其明显的特征之一是存在众多免疫细胞尤其是巨噬细胞的浸润,这与肺癌病人较差的预后和较低的存活率密切相关。
肿瘤相关巨噬细胞(tumorassociatedmacrophages,tam)是一类被发现大量浸润于多种肿瘤发生部位的巨噬细胞,临床数据和动物实验都证明,肿瘤组织中的巨噬细胞与癌症患者或者荷瘤实验动物的存活率及预后情况密切相关。目前基于肿瘤相关巨噬细胞的肿瘤治疗方法已成为肿瘤免疫疗法领域极具吸引力的新方向,靶向肿瘤相关巨噬细胞的免疫疗法极具临床应用价值。
技术实现要素:
本发明的目的在于提供一种lgr4和r-spondin结合抑制剂及其在肿瘤治疗中的用途。
具体地,本发明的目的在于提供一种利用lgr4胞外段蛋白封闭或阻断肿瘤组织中r-spondin蛋白与内源性lgr4受体的结合,进而调控肿瘤相关巨噬细胞功能极化转换,进而抑制肿瘤的发生发展的应用。更具体地,本发明主要涉及lgr4胞外段蛋白在肿瘤治疗领域的应用。
在本发明的第一方面,提供了一种抑制lgr4和r-spondin结合的抑制剂的用途,用于制备一制剂或组合物,所述的制剂或组合物用于调控巨噬细胞的功能表型转换。
在另一优选例中,所述的调控巨噬细胞的功能表型转换是指抑制巨噬细胞向m2表型极化,和/或促进巨噬细胞向m1表型极化。
在另一优选例中,所述的调控巨噬细胞的功能表型转换是指促进巨噬细胞由m2表型转换为m1表型。
在另一优选例中,所述的巨噬细胞为肿瘤相关巨噬细胞。
在另一优选例中,所述的制剂或组合物还用于选自下组的一个或多个用途:
(i)提高m1表型巨噬细胞的比例;
(ii)提高cd8+t细胞的比例;
(iii)治疗肿瘤;
(iv)调节肿瘤组织免疫微环境。
在另一优选例中,所述的肿瘤为富含巨噬细胞浸润和/或高表达r-spondin蛋白的肿瘤。
在另一优选例中,所述的抑制剂选自下组:
(a)特异性抑制lgr4表达和/或活性的拮抗剂;
(b)特异性抑制r-spondin表达和/或活性的拮抗剂;
(c)lgr4的结构类似物;
(d)r-spondin的结构类似物;
(e)上述各项的任意组合。
在另一优选例中,所述的拮抗剂包括microrna、sirna、shrna、或其组合。
在另一优选例中,所述的拮抗剂包括抗体,较佳地为单克隆抗体。
在另一优选例中,所述的抑制剂为lgr4胞外段蛋白。
在另一优选例中,所述的lgr4胞外段蛋白包括胞外段蛋白全长蛋白、胞外段蛋白片段。
在另一优选例中,所述的抑制剂为包含lgr4胞外段蛋白的融合蛋白。
在另一优选例中,所述的抑制剂为整合lgr4胞外段蛋白编码基因的car-t细胞。
在另一优选例中,所述的lgr4和r-spondin来源于人或非人哺乳动物。
在另一优选例中,所述的lgr4胞外段蛋白的氨基酸序列如seqidno.:1所示。
在另一优选例中,编码所述的lgr4胞外段蛋白的核苷酸序列如seqidno.:2所示。
在另一优选例中,所述组合物为药物组合物。
在另一优选例中,所述药物组合物包含(a)抑制lgr4和r-spondin结合的抑制剂;和(b)药学上可接受的载体。
在另一优选例中,所述药物组合物的剂型为注射剂型、或外用药物剂型。
在另一优选例中,所述药物组合物可以通过皮下注射、静脉注射、肌内注射的方式给药。
在本发明的第二方面,提供了一种筛选促进巨噬细胞由m2表型转换为m1表型的候选药物的方法,所述方法包括步骤:
(a)提供一待测化合物,并在检测所述待测化合物对lgr4和r-spondin结合的抑制情况,从而选出对lgr4和r-spondin结合有抑制作用的待测化合物,作为经初筛的化合物;以及
(b)测试所述经初筛的化合物对巨噬细胞表型转换的效果,从而选出具有促进巨噬细胞由m2表型转换为m1表型的化合物,作为候选药物。
在本发明的第三方面,提供了一种非治疗性地促进巨噬细胞由m2表型转换为m1表型的方法,包括步骤:
(a)在抑制lgr4和r-spondin结合的抑制剂存在下,培养巨噬细胞,从而促进巨噬细胞由m2表型转换为m1表型。
在另一优选例中,所述的巨噬细胞为肿瘤相关巨噬细胞。
在另一优选例中,所述的抑制剂为lgr4胞外段蛋白。
在本发明的第四方面,提供了一种调控巨噬细胞的功能表型转换的方法,包括步骤:
(i)给需要的对象施用抑制lgr4和r-spondin结合的抑制剂或包含所述抑制剂的组合物。
在另一优选例中,所述的对象包括人和非人哺乳动物。
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
图1显示了lgr4的缺失引起m2型巨噬细胞极化的减弱。
图1a显示了llc荷瘤小鼠脾脏巨噬细胞及肿瘤相关巨噬细胞中lgr4的表达差异。
图1b显示了lgr4配体rspo蛋白促进野生型巨噬细胞f4/80+cd206+m2型巨噬细胞的极化,而对于lgr4敲除型巨噬细胞该种促进作用减弱。
图1c、图1d和图1e分别显示了lgr4敲除巨噬细胞中m2标志蛋白agr1、ym-1、cd206mrna表达水平降低。
图1f显示lgr4敲除巨噬细胞中m2标志蛋白agr1、cd206蛋白表达水平降低。
图2显示了lgr4在不同肿瘤组织中的表达差异。
图3显示了lgr4胞外段原核表达载体的构建。
图3a显示了lgr4胞外段结构域。
图3b显示了p-et8a原核表达载体以及lgr4胞外段蛋白表达盒插入位置。
图4显示lgr4胞外段蛋白显著改善肿瘤微环境,抑制llc肿瘤的发生发展。
图4a显示了lgr4胞外段蛋白剂量依赖性抑制llc肿瘤发生发展。
图4b显示了rspo/lgr4通路阻断显著抑制llc肿瘤的生长。
图4c显示了rspo/lgr4通路阻断降低llc肿瘤微环境中m2型巨噬细胞(f4/80+cd206+)比例,同时提高cd8t细胞(cd3+cd8+)及m1型巨噬细胞(f4/80+cd16/32+)的比例。
图5显示了经过含m-csf集落刺激因子的条件培养基诱导培养7天后,f4/80+的成熟巨噬细胞纯度能够到到98%在以上,满足后续实验要求。
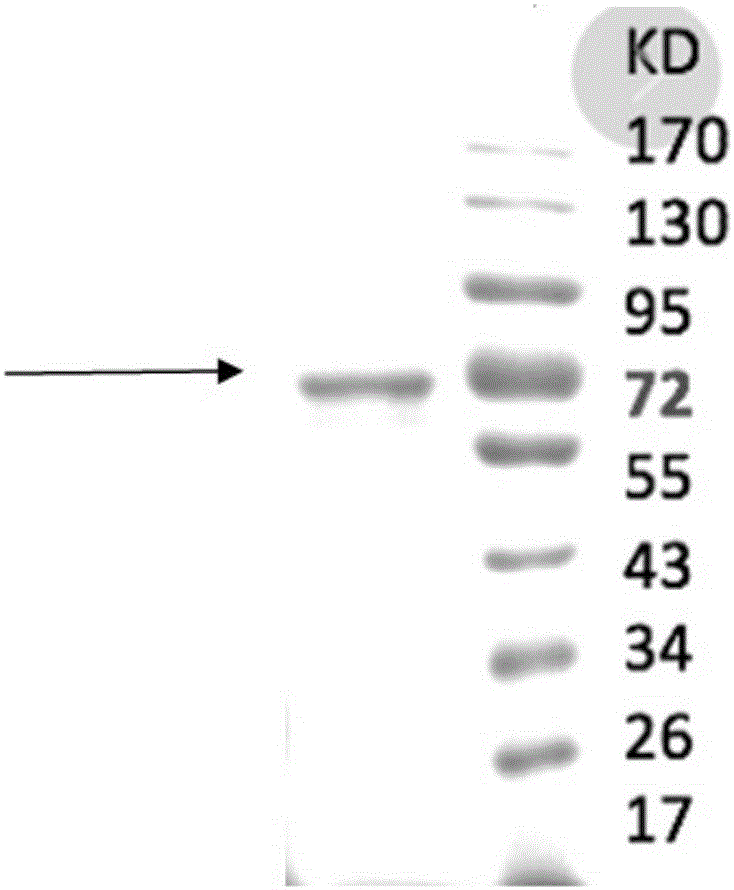
图6显示了表达的lgr4-ecd蛋白分子量的电泳结果。
图7显示了一种典型的shrna的结构。
具体实施方式
本发明人经过广泛而深入地研究,首次意外地发现lgr4基因能够调控肿瘤组织中肿瘤相关巨噬细胞的功能表型转换。具体地,lgr4基因与其配体r-spondin蛋白结合后能够促进肿瘤相关巨噬细胞朝向m2表型极化。原核表达的lgr4胞外段蛋白,其氨基酸序列如seqidno:1所示,通过皮下注射给药方式,该蛋白能够与内源性lgr4受体竞争性结合r-spondin蛋白,从而抑制了肿瘤相关巨噬细胞的m2型极化,同时提高了肿瘤组织中具备抗肿瘤功能的m1型巨噬细胞和cd8+t淋巴细胞的比例,可用于治疗富含巨噬细胞浸润同时高表达r-spondin蛋白的肿瘤类型。本发明涉及lgr4可作为调节肿瘤组织免疫微环境进而抑制肿瘤发生发展的药物作用靶点以及lgr4胞外段蛋白在肿瘤临床治疗上的应用,包括将lgr4胞外段基因整合进cart以促进cart在治疗实体瘤上的效果。在此基础上完成本发明。
肿瘤相关巨噬细胞
肿瘤相关巨噬细胞(tumorassociatedmacrophages,tam)是一类被发现大量浸润于多种肿瘤发生部位的巨噬细胞,临床数据和动物实验都证明,肿瘤组织中的巨噬细胞与癌症患者或者荷瘤实验动物的存活率及预后情况密切相关。巨噬细胞根据其表型和功能可大致分为两个大类,即促炎抗肿瘤的m1型和抑炎促肿瘤的m2表型,且根据所接收刺激信号的不同,两型巨噬细胞之间可以相互转化,体现为巨噬细胞高度的异质性和可塑性。tam拥有大量与抗炎促肿瘤的m2型巨噬细胞相似的特征,能够抑制抗肿瘤的免疫应答,促进肿瘤细胞逃脱机体免疫监视;同时,通过分泌大量的il-10、tgf-β、vegf等细胞因子和生长因子,促进肿瘤组织内部的血管新生、纤维化、上皮间质转换等;tam还能够与周围的肿瘤细胞、基质细胞甚至其它的免疫细胞相互作用和通信,为肿瘤细胞的增殖、存活、侵袭、转移提供了良好的局部微环境。目前基于肿瘤相关巨噬细胞的肿瘤治疗方法已成为肿瘤免疫疗法领域极具吸引力的新方向,靶向肿瘤相关巨噬细胞的免疫疗法极具临床应用价值。
lgr4
lgr4全称为富含亮氨酸基序的g蛋白偶联受体4(leucine-richrepeat-containinggprotein-coupledreceptor4),也叫g蛋白偶联受体48(gproteincouplereceptor48),属于lgr类g蛋白偶联受体家族ⅱ,geneid:107515。
lgr4受体可以与r-spondin蛋白家族(r-spondin1-4)高特异性和高亲和力结合,其ic50仅为2-230nm,因而该分泌蛋白家族被视为lgr4的内源性配体。lgr4与r-spondin蛋白结合后可极大地增强经典的wnt/β-catenin信号通路,在成体干细胞和毛囊干细胞发育、骨骼细胞平衡、生殖道发育、眼睑发育甚至在巨噬细胞的模式识别过程中均发挥着重要的调节作用。然而,lgr4与r-spondin蛋白的结合并不能激活经典的g蛋白信号通路。已经证实,lgr4及其配体r-spondin蛋白在多种人类恶性肿瘤中异常表达,绝大多数情况下其表达均高于正常组织,包括肺癌,胃癌、结直肠癌、乳腺癌、前列腺癌等,lgr4/r-spondin通过wnt或者wnt相关信号通路促进肿瘤细胞的增殖生长。
申请人发现,相比于正常组织的巨噬细胞,lgr4在小鼠肺癌组织肿瘤相关巨噬细胞中也呈现上调表达,并且已经通过体内体外实验证实lgr4正调控巨噬细胞m2表型的功能极化,结合r-spondin在肺癌组织中以及lgr4在肺癌肿瘤相关巨噬细胞中的高度表达,预示着可以通过阻断肺癌组织中lgr4/r-spondin的相互作用,在直接作用于肿瘤细胞本身的同时通过调控肿瘤相关巨噬细胞的功能表型从而调控肿瘤细胞赖以生存的微环境,进而抑制肿瘤的发生发展,对于肿瘤的免疫治疗具有重大的应用价值和意义。
lgr4和r-spondin结合抑制剂
如本文所用,“lgr4和r-spondin结合抑制剂”、“抑制lgr4和r-spondin结合的抑制剂”可互换使用,是指能够特异性抑制lgr4和r-spondin结合的制剂或组合物。
在另一优选例中,所述的lgr4和r-spondin结合抑制剂为lgr4抑制剂、r-spondin抑制剂、lgr4结构类似物、和/或r-spondin结构类似物。
在另一优选例中,所述的lgr4和r-spondin结合抑制剂为seqidno.:1所示的lgr4胞外段蛋白。
在另一优选例中,所述的lgr4和r-spondin结合抑制剂为抗lgr4单克隆抗体和/或抗lgr4单克隆抗体。
rna干扰(rnai)
在本发明中,一类有效的lgr4和r-spondin结合抑制剂是干扰rna。
如本文所用,术语“rna干扰(rnainterference,rnai)”是指:一些小的双链rna可以高效、特异地阻断体内特定基因的表达,促使mrna降解,诱使细胞表现出特定基因缺失的表型,其也称为rna干预或者rna干涉。rna干扰是高度特异的在mrna水平上的基因沉默机制。
如本文所用,术语“小干扰rna(smallinterferingrna,sirna)”是指一种短片段双链rna分子,能够以同源互补序列的mrna为靶目标降解特定的mrna,这个过程就是rna干扰途径(rnainterferencepathway)。
在本发明中,干扰rna包括sirna、shrna以及相应的构建物。在本发明中,所述的干扰rna可以特异性地针对lgr4的干扰rna、和/或特异性针对r-spondin的干扰rna。优选地,所述的干扰rna可以特异性地针对lgr4与r-spondin的结合区域。
在本发明中,一种典型的shrna如图7中的式ii所示,
式中,
seq’正向为seq正向序列对应的rna序列或序列片段;
seq’反向为与seq’正向基本上互补的序列;
x’为无;或为位于seq’正向和seq’反向之间的间隔序列,并且所述间隔序列与seq’正向和seq’反向不互补,
||表示在seq正向和seq反向之间形成的氢键。
巨噬细胞的功能表型转换的调控
本发明提供了一种抑制lgr4和r-spondin结合的抑制剂的用途,用于制备一制剂或组合物,所述的制剂或组合物用于调控巨噬细胞的功能表型转换。
本发明还提供一种调控巨噬细胞的功能表型转换的方法,包括步骤:(i)给需要的对象施用抑制lgr4和r-spondin结合的抑制剂或包含所述抑制剂的组合物。
本发明涉及含有lgr4和r-spondin结合抑制剂和药学上可接受的载体的药物组合物。
药学上可接受的载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、粉剂、及其组合。药物制剂应与给药方式相匹配。本发明的药物组合物可以被制成针剂形式,例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。诸如片剂和胶囊之类的药物组合物,可通过常规方法进行制备。药物组合物如针剂、溶液、片剂和胶囊宜在无菌条件下制造。本发明的药物组合也可以被制成粉剂用于雾化吸入。一种优选的剂型是口服制剂。此外,本发明药物组合物还可与其他治疗剂一起使用。
当本发明药物组合物被用于上述用途时,可与一种或多种药学上可接受的载体或赋形剂混合,如溶剂、稀释剂等,而且可以用如下形式口服给药:片剂、丸剂、胶囊、可分散的粉末、颗粒或悬浮液(含有如约0.05-5%悬浮剂)、糖浆(含有如约10-50%糖)、和酏剂(含有约20-50%乙醇),或者以无菌可注射溶液或悬浮液形式(在等渗介质中含有约0.05-5%悬浮剂)进行非肠胃给药。例如,这些药物制剂可含有与载体混合的约0.01-99%,更佳地约为0.1%-90%(重量)的活性成分。
本发明的药物组合物可以通过常规途径进行给药,其中包括(但并不限于):肌内、腹膜内、静脉内、皮下、皮内、口服、瘤内或局部给药。优选的给药途径包括口服给药、肌内给药或静脉内给药,涂抹给药。
此外,本发明的药物组合物还可与其他治疗肿瘤的药物联用。
本发明的主要优点包括:
1.本发明筛选出lgr4基因并揭示lgr4/r-spondin参与巨噬细胞m2表型功能的极化过程;基于此事实,将lgr4胞外段蛋白作为肿瘤组织中r-spondin1的竞争性结合蛋白,抑制肿瘤组织中肿瘤相关巨噬细胞朝向促肿瘤的m2型极化,同时提高m1型巨噬细胞和cd8+t细胞的比例,从而抑制肿瘤的发生发展。
2.本发明将lgr4/r-spondin1作为分子靶点或药物作用靶点,用以治疗两者高表达的肿瘤类型。
3.本发明提供了一种分离纯化的lgr4胞外段蛋白,所述lgr4胞外段蛋白具备如seqidno:1的氨基酸序列,该序列位于lgr4蛋白氨基酸序列的第28-528位。
4.本发明所述的lgr4胞外段蛋白能与r-spondin1特异性结合,所述蛋白可通过原核表达或者哺乳动物细胞表达获得,可以以单体或者融合蛋白形式表达并结合r-spondin1蛋白。
5.本发明构建了lgr4胞外段蛋白的原核表达载体,该载体为pet28a表达载体,构建完成的表达载体可称为pet28a-lgr4ecd表达载体,经宿主大肠杆菌bl21菌株表达,其中ecd意为胞外结合结构域。目前lgr4胞外结构域已经实现晶体解析,其结合r-spondin蛋白区域已明晰。但考虑到结合强度或者亲和力以及表达后蛋白折叠三维结构,本发明仍然采取表达lgr4胞外段全长序列策略,所述胞外段全长的氨基酸序列如seqidno:1所示。
6.本发明所述lgr4胞外段蛋白采用皮下给药方式,注射后实验小鼠并无明显不良反应。上述蛋白也可以采取静脉注射,肌内注射或者注射给药方式。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
实施例1
小鼠llc肺癌细胞皮下移植瘤模型的构建以及肿瘤相关巨噬细胞中lgr4表达水平的检测
小鼠路易斯肺癌细胞系llc细胞购自美国典型培养物保藏中心(atcc),按其说明要求培养于dulbecco’smodifiedeaglemedium(dmem)完全培养基中(10%胎牛血清,100μg/ml链霉素,100u/ml青霉素,非必需氨基酸购自gibco公司并按使用说明书稀释)。将llc细胞培养于6cm培养皿中,待其长至80%-90%皿底面积的时候,弃掉上层培养基,37℃预热pbs缓冲液洗涤两次,于皿中加入500μl0.25%胰蛋白酶+0.02%edta于37℃消化30s,随后加入等体积dmem完全培养基终止消化,离心,并用pbs缓冲液重悬细胞,调整细胞浓度至1×107/ml。
取上述细胞悬液经皮下注射8周龄左右大小的c57bl/6小鼠(华东师范大学实验动物中心,spf级),每只小鼠注射200μl。
两周后,颈椎脱臼处死荷瘤小鼠,手术取下肿瘤组织以及脾脏并将其于5ml0.25%胰蛋白酶消化液中捣碎消化5分钟,加入等体积dmem完全培养基终止消化,离心,随后用pbs重悬细胞,并调整细胞密度至1×108/ml.
各将2ml上述细胞悬液至于流式分析管中,每管加入3μlapc荧光基团标记的大鼠抗小鼠f4/80单克隆抗体(biolegend公司),充分混合均匀后置于4℃避光条件孵育40分钟,随后以2ml含2%胎牛血清的pbs缓冲液洗涤三次,最后一次将1mlpbs缓冲液重悬上述细胞。
流式细胞仪(bd公司)分选收集f4/80+的肿瘤相关细胞及脾脏巨噬细胞,待收集细胞数均达到2×105时停止收集。
将收集到的细胞以1000rpm/min离心3分钟,弃上清,各管加入1mltrizol裂解液(takara公司),裂解2分钟,随后4℃条件12000rpm/min离心10分钟,取上层水相,加入200μl氯仿(上海生工),静置2分钟,4℃条件12000rpm/min离心5分钟,取上层水相,加入等体积异丙醇(上海生工)静置5分钟后,4℃条件12000rpm/min离心5分钟,沉淀用800μl以depc水配制的75%乙醇重悬洗涤,4℃条件8000rpm/min离心5分钟后弃上清,待rna沉淀晾干后以50μlrnaasefree水或者depc水溶解,测试总rna抽提浓度及纯度。
将上述抽提的总rna进行逆转录获取cdna,所用试剂盒为takara公司生产的试剂盒,操作步骤及程序遵循生产说明书,反转录的rna总量为1000ng,反应程序为:37℃30分钟,85℃5秒钟,12℃保存。
将上述反转录获取的cdna作为模板,以β-actin作为内参基因,实时定量pcr检测lgr4表达水平,所用试剂盒为takara公司生产的sybr试剂盒,反应体系,操作步骤及程序遵循生产说明书。
结果如图1a所示,lgr4在肺癌肿瘤相关巨噬细胞中的表达水平明显高于正常脾脏组织巨噬细胞。
实施例2
小鼠骨髓来源巨噬细胞(bonemarrowderivedmacrophages,bmm)体外诱导培养
bmm体外诱导培养的方法如下:
1、取6-8周c57bl/6小鼠,颈椎脱臼处死,75%酒精体表消毒。
2、剪开腹部及外周皮肤,露出腹股沟,沿腹股沟处剪下小鼠两条后肢,注意不要剪断股骨。
3、用经过75%酒精处理过的剪刀和镊子剥离后肢肌肉,分离出胫骨和股骨(大腿骨和小腿骨)。
4、在无菌环境下(如超净工作台中),依次剪开胫骨和股骨两端,露出骨髓腔,用注射器吸取5ml左右bmm条件培养进行反复吹打,直到骨髓腔发白为止,由于胫骨较股骨细,建议采用1ml规格注射器进行吹洗。
5、用移液器反复吹打骨髓吹洗液,直到肉眼看不见较大团块(吹打不可用力过猛,避免对细胞造成严重剪切力损伤)。此时制备为骨髓细胞悬液。
6、将上述细胞悬液经过45μm孔径网筛过滤,计数,接板。一般于6cm培养皿接种1×107个总细胞为宜。
7、将细胞置于37℃、5%co2及适宜湿度的培养箱中培养5-7天,每2天更换培养液。
8、在第五或第七天,将细胞以胰蛋白酶(0.25%胰蛋白酶+0.02%edta)消化10分钟,终止,重悬,调整细胞密度为1×107/ml,接板于六孔培养板,每孔细胞数为1×106,培养基更换为普通dmem完全培养基,随后分别以10ng/mlil-4,500ng/ml重组鼠r-spondin1(r&d),500ng/ml重组鼠r-spondin3处理细胞,依据后续不同检测水平,分别施以不同时间或时间点处理。
其中,诱导bmm的条件培养基成分为:dmem基础培养基,10%fbs,100u/ml青霉素,100μg/ml链霉素,15%l929细胞培养上清。
结果如图5所示,经过该条件培养基诱导培养7天后,f4/80+的成熟巨噬细胞纯度能够达到98%在以上,表明该诱导培养方式具备可行性。
实施例3
bmm的流式细胞染色
将实施例2制备得到的lgr4+/+及lgr4-/-bmm培养于六孔培养板,更换为普通dmem完全培养基后分别以500ng/mlr-spondin1,500ng/mlr-spondin3处理细胞24小时,消化细胞,重悬,调整细胞密度为1×106/ml,取200μl细胞悬液置于流式分析管中进行染色。避光条件下,依次用apc标记的大鼠抗小鼠f4/80单克隆抗体(apc-anti-f4/80)以及fitc标记的大鼠抗小鼠cd206单克隆抗体(fitc-anti-cd206)4℃避光孵育40分钟,抗体用量为0.1μg/105细胞。染色结束后,各管用1ml含0.2%胎牛血清的pbs缓冲液洗涤细胞三次(800rpm/min,3分钟),最后以200μlpbs缓冲液重悬细胞,进行流式细胞仪分析。染色时设置同型对照组,单染组和实验组,其中同型对照组加入荧光标记同型对照igg抗体,单染组分别单独加入apc-anti-f4/80抗体或者fitc-anti-cd206抗体,实验组则两种抗体同时加入。
结果如图1b所示,其中f4/80+cd206+细胞为m2型巨噬细胞,可见r-spondin1和r-spondin3均可促进lgr4+/+而非lgr4-/-巨噬细胞朝向m2方向极化。
实施例4
实时定量pcr检测ym1,arg1和cd206的表达
将实施例2制备得到的lgr4+/+及lgr4-/-bmm培养于六孔培养板,更换为普通dmem完全培养基后以10ng/ml重组鼠il-4处理4小时,弃培养液,pbs缓冲液洗涤两次,trizol(takara)法抽提总rna,反转录获得cdna,实时定量pcr法检测各组ym1,arg1以及cd206的表达水平。所用试剂盒为takara公司生产的sybr试剂盒,反应体系,操作步骤及程序遵循生产说明书。
结果如图1c,图1d,图1e所示,lgr4的缺失抑制了巨噬细胞m2方向的功能极化。
实施例5
蛋白免疫印迹westernblot检测arg1,cd206的表达
将实施例2制备得到的lgr4+/+及lgr4-/-bmm培养于六孔培养板,更换为普通dmem完全培养基后以10ng/ml重组鼠,处理24小时,弃培养液,pbs缓冲液洗涤两次,每孔以200μl含有蛋白酶磷酸酶抑制剂cocktail(美国selleckchem公司,100×储液)的强ripa裂解液(500mmtrisph7.0,150mmnacl,0.1%triton-x-100,1%脱氧胆酸钠,0.1%sds)冰上裂解30分钟,将细胞裂解物收集至干净ep管中,12000rpm/min离心2分钟,将上清转移至另一干净的ep管,每管加入40μl5×loadingbuffer(配方见下文),混匀后置100℃水浴锅煮10分钟,随后将此充分变性后的样品进行sds-page凝胶电泳,其中5%聚丙烯酰胺浓缩胶,10%聚丙烯酰胺分离胶。每孔上样量15μl,60v低电压电泳20分钟后,更换100v高电压电泳120分钟;终止电泳,将带有蛋白的凝胶转移至0.2μm硝酸纤维素膜(nc膜,美国millipore公司)进行半干法转膜操作,转膜电压100v,时间90分钟;转膜结束后,将已成功转移有蛋白的nc膜置于含5%牛血清白蛋白(bsa)的pbs缓冲液中,摇床上轻摇封闭120分钟;pbs洗涤nc膜两次后,根据marker大小指示裁剪nc膜,将带有目的蛋白条带的nc膜分别以兔抗鼠arg1抗体,兔抗鼠cd206抗体以及鼠抗鼠β-actin抗体于4℃条件孵育过夜,pbst洗涤(10分钟,3次),避光条件下分别以绿色荧光基团偶联的山羊抗鼠以及绿色荧光基团偶联的山羊抗兔二抗进行孵育,孵育时间120分钟,pbst洗涤(10分钟,3次),随后以odyssey荧光扫膜仪进行曝光,其中β-actin为上样内参。
实验所用相关试剂配方如下:
pbs缓冲液:氯化钠(nacl),8g;氯化钾(kcl),0.2g;磷酸氢二钠(na2hpo4),1.44g;磷酸二氢钾(kh2po4),0.24g;调ph7.2,定容至1l。
1×电泳缓冲液:25mmtris,250mm甘氨酸,0.1%sds。
1×转膜缓冲液:48mmtris,39mm甘氨酸,0.037%sds,20%甲醇。
5×loadingbuffer:0.25mtris-hcl,ph6.8,25%β-巯基乙醇,10%sds,0.5%溴酚蓝,50%甘油。用时加入细胞裂解液,使之稀释成1×工作液。
pbst:含0.1%tween20的pbs缓冲液。
所使用电泳槽、转膜槽极其配套器材均购自biorad公司。
实验结果如图1f所示,lgr4的缺失使巨噬细胞中m2相关标志基因arg1,cd206表达水平下调。
实施例6
肿瘤数据库的检索
tcga(https://tcga-data.nci.nih.gov/tcga/tcgahome2.jsp)以及oncomine(https://www.oncomine.org/resource/login.html)肿瘤数据库的检索根据网站说明操作。其中tcga数据库采用cbioportal(http://www.cbioportal.org/index.do)检索工具进行检索,检索肺腺癌病人数据库选择“lungadenocarcinoma(tcga,provisional)”数据组;oncomine检索采用“rsop1”、“cancervsnormalanalysis”以及“tcgalung2”数据组。
分析结果如图2所示,lgr4及其配体rspo1在肺腺癌病人肿瘤标本中呈高表达。
实施例7
lgr4原核表达载体的构建以及lgr4胞外段蛋白表达纯化
lgr4原核表达载体为申请人前期构建,所用表达载体骨架为pet28a(+),通过基因工程操作技术将lgr4基因的多核苷酸序列连入其多克隆位点,表达后,目的蛋白lgr4胞外段蛋白n端融合表达6×his标签蛋白。重组质粒转化bl21大肠杆菌,涂带卡那霉素抗性的lb琼脂糖培养板,过夜培养后,挑取单克隆阳性菌落,置于含卡那霉素抗性的lb液体培养基摇床培养过夜,将过夜菌液全部转入1l含卡那霉素抗性的新鲜lb液体培养基中,37℃,220rpm/min摇床摇菌。随时用分光光度计监测菌液od值,待菌液od值达到0.6-0.8时,加入1ml0.8m的iptg进行诱导表达。诱导前取1ml菌液2000rpm/min离心两分钟,弃上清,往菌体中加入100μl1×sdsloadingbuffer,100℃水浴锅煮样10分钟,作为未诱导对照组,iptg诱导表达时间为4小时。
菌体收集及裂解:诱导结束后,将菌液分批次以11000rpm/min离心15分钟,弃上清,挑取少量菌体加入100μl1×sdsloadingbuffer,100℃水浴锅煮样10分钟,作为诱导对照组。剩余菌体加入20ml的裂解缓冲液(相关配方见下文,以下所用试剂同),漩涡振荡器充分摇匀,与-80℃冰箱反复冻融3次后,将菌液置于冰上进行超声破碎,破碎条件为:400w,每次超声时间5秒钟,间歇5秒钟,次数为300次,超声破碎前,往菌液中加入1ml蛋白酶抑制剂cocktail(美国selleckchem公司,100×储液)。
蛋白收集及纯化:将经超声破碎后的菌液11000rpm/min离心10分钟,小心吸出上清,分别取少量沉淀及上清,加入100μl1×sdsloadingbuffer,100℃水浴锅煮样10分钟,留作电泳上样,分泌表达蛋白主要存在于上清,包涵体表达时蛋白则主要存在于沉淀中。
由于目的蛋白融合表达6×his标签蛋白,故可用镍柱亲和层析法纯化目的蛋白,所用镍柱为qiagen公司生产的ni-ntaagarose纯化beads。蛋白纯化前:
清洗镍柱:所用ni-ntaagarose以20%乙醇溶液浸泡于4℃条件保存。使用前往塑料柱中灌注4mlni-ntaagarosebeads,稍作沉降,再往柱子中加满双脱水过柱清洗2次,弃流出液,以上操作于4℃条件下进行。
平衡镍柱:往清洗后的镍柱中加满平衡缓冲液,弃流出液,以上操作于4℃条件下进行。
蛋白样过柱纯化:将样品液小心灌满柱子,分多次灌注,静置过柱,弃流出液,以上操作于4℃条件下进行。
洗涤镍柱:样品过柱结束后,往镍柱中加满洗涤缓冲液,静置过柱,重复两次,弃流出液,以上操作于4℃条件下进行。
洗脱蛋白:往洗涤后的镍柱中加2ml洗脱缓冲液,收集流出液,于4℃条件下进行。
蛋白浓缩及保存:选择7okd规格的浓缩超滤管(购自美国millipore公司),使用前以双脱水清洗两次,清洗过程:4℃离心,6000rpm/min,5分钟。
加入蛋白样品,6000rpm/min离心20分钟后,倒掉收集管底部废液,往超滤管中补加无菌的pbs缓冲液,加满为止,继续离心,如此重复2次,最终使pbs缓冲液替换掉洗脱液中的咪唑。
浓缩结束后,超滤管上层中剩余液即为浓缩的目的蛋白,bca法测定总蛋白浓度后,分装保存于-80摄氏度超低分冰箱,使用时避免反复冻融。
本实例中所使用相关试剂及其配方如下:
裂解缓冲液:50mmtris,300mmnacl,ph8.0
洗涤缓冲液:50mmnah2po4,300mmnacl,ph8.0
洗脱缓冲液:50mmnah2po4,300mmnacl,250mm咪唑,ph8.0
平衡缓冲液:50mmnah2po4,300mmnacl,20mm咪唑,ph8.0
结果如图6所示,表达出的lgr4-ecd蛋白分子量大小为72kd左右,纯度高,无杂带。
实施例8
lgr4胞外段蛋白治疗浓度依赖实验
选取8周龄左右雄性c57bl/6小鼠分为三组,每组8只小鼠。戊巴比妥钠麻醉,用刮毛器除去背部毛发,随后每只小鼠经皮下在左侧背部注射5×105llc细胞。从注射肿瘤细胞后第二天开始,分别给三组小鼠右侧背部皮下给药,为:pbs空白对照组,10μg剂量组,20μg剂量组。连续给药5天,于注射肿瘤细胞后第十天开始用游标卡尺测量小鼠肿瘤体积,采用肿瘤体积=长×宽2,2的计算公式。
结果如图4a所示,显示了肿瘤体积随时间的变动图,可见随着lgr4胞外段蛋白给药浓度的上升,肿瘤体积明显被抑制。
实施例9
lgr4胞外段蛋白治疗实验
选取8周龄左右雄性c57bl/6小鼠分为六组,每组8只小鼠。戊巴比妥钠麻醉,用刮毛器除去背部毛发,随后每只小鼠经皮下在左侧背部注射5×105llc细胞。从注射肿瘤细胞后第二天开始,分别给六组小鼠右侧背部皮下给药,为:pbs空白对照组,20μglgr4胞外段蛋白剂量组,无关抗体igg对照组,抗小鼠r-spondin1单克隆抗体(根据说明书的中和计量计算,每只小鼠给药14μg),dmso空白对照组,blz945(csf-1r小分子抑制剂,可以减少肿瘤微环境中的m2型巨噬细胞)200mg/kg体重组(该组可作为阳性对照组)。连续给药5天,于注射肿瘤细胞后第十天开始用游标卡尺测量小鼠肿瘤体积,采用肿瘤体积=长×宽2,2的计算公式,
结果如图4b所示,显示了肿瘤体积随时间的变动图,可见随着lgr4胞外段蛋白剂量的增加,抗小鼠r-spondin1单克隆抗体以及blz945对小鼠肿瘤体积均具有明显抑制效果。
实施例10
成瘤小鼠给药后肿瘤组织巨噬细胞及t细胞分析
手术剪取如上述六组小鼠的肿瘤组织,于5ml0.25%胰蛋白酶消化液中捣碎消化5分钟,加入等体积dmem完全培养基终止消化,离心,随后用pbs重悬细胞,并调整细胞密度至1×108/ml.
各将200μl上述细胞悬液至于流式分析管中,分好同型对照管,单染管和双染管,每管加入0.5μl荧光基团标记的大鼠抗小鼠单克隆抗体,充分混合均匀后置于4℃避光条件孵育40分钟,随后以1ml含2%胎牛血清的pbs缓冲液洗涤三次,最后一次将200μlpbs缓冲液重悬上述细胞。流式细胞仪(bd公司)分析各组织中f4/80+cd206+的m2型巨噬细胞,f4/80+cd16/32+的m1型巨噬细胞以及cd3+cd8+的t细胞的比例。
结果如图4c所示,lgr4胞外段蛋白和抗小鼠r-spondin1单克隆抗体均能明显减少m2型肿瘤相关巨噬细胞同时增强cd8+t细胞的浸润。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
序列表
<110>华东师范大学
上海邦耀生物科技有限公司
<120>lgr4和r-spondin结合抑制剂及其在肿瘤治疗中的用途
<130>p2017-1528
<160>2
<170>patentinversion3.5
<210>1
<211>501
<212>prt
<213>智人(homosapiens)
<400>1
leucysalaalaprocyssercysaspglyaspargargvalaspcys
151015
serglylysglyleuthralavalprogluglyleuseralaphethr
202530
glnalaleuaspilesermetasnasnilethrglnleuprogluasp
354045
alaphelysasnphepropheleuglugluleuglnleualaglyasn
505560
aspleuserpheilehisprolysalaleuserglyleulysgluleu
65707580
lysvalleuthrleuglnasnasnglnleulysthrvalproserglu
859095
alaileargglyleuseralaleuglnserleuargleuaspalaasn
100105110
hisilethrservalprogluaspserphegluglyleuvalglnleu
115120125
arghisleutrpleuaspaspasnileleuthrgluvalprovalarg
130135140
proleuserasnleuprothrleuglnalaleuthrleualaleuasn
145150155160
asnileserserileproaspphealaphethrasnleuserserleu
165170175
valvalleuhisleuhisasnasnlysilelysserleuserglnhis
180185190
cyspheaspglyleuaspasnleugluthrleuaspleuasntyrasn
195200205
asnleuaspglupheproglnalailelysalaleuproserleulys
210215220
gluleuglyphehisserasnserileservalileproaspglyala
225230235240
phealaglyasnproleuleuargthrilehisleutyraspasnpro
245250255
leuserphevalglyasnseralaphehisasnleuseraspleuhis
260265270
serleuvalileargglyalaserleuvalglntrppheproasnleu
275280285
alaglythrvalhisleugluserleuthrleuthrglythrlysile
290295300
serserileproaspaspleucysglnasnglnlysmetleuargthr
305310315320
leuaspleusertyrasnaspileargaspleuproserpheasngly
325330335
cysargalaleuglugluileserleuglnargasnglnileserleu
340345350
ilelysgluthrthrpheglnglyleuthrserleuargileleuasp
355360365
leuserargasnleuilearggluilehisserglyalaphealalys
370375380
leuglythrilethrasnleuaspvalserpheasngluleuthrser
385390395400
pheprothrgluglyleuasnglyleuasnglnleulysleuvalgly
405410415
asnpheglnleulysaspalaleualaalaargaspphealaasnleu
420425430
argserleuservalprotyralatyrglncyscysalaphetrpgly
435440445
cysaspsertyralaasnleuasnthrgluaspasnserproglnasp
450455460
hisservalthrlysglulysglyalathraspalaalaasnalathr
465470475480
serthralagluserglugluhisserglnileileilehiscysthr
485490495
proserthrglyala
500
<210>2
<211>1503
<212>dna
<213>智人(homosapiens)
<400>2
ctctgcgctgcgccctgcagctgcgacggcgaccgtcgggtggactgctccgggaagggg60
ttgacggcggtaccggaggggctcagcgccttcacccaagcactggatatcagtatgaac120
aatatcactcagttaccagaagatgcatttaagaattttccttttctagaggagctacaa180
ctggctggtaacgacctttcttttatccacccaaaagccttgtctgggttgaaagaactc240
aaagtcctaaccctccagaacaatcagttgaaaacagtacccagtgaagccattcgtgga300
ctgagtgctttgcagtctctacgcttagatgccaaccatattacctcagtcccggaggac360
agttttgaagggctcgttcagttgcggcatctgtggctggatgacaacatcttgacggaa420
gtgcctgtgcgtccgctcagcaacctgccaaccctgcaggcgctgaccttggctctcaac480
aacatctcaagcatccccgacttcgcattcaccaacctttcaagcttggtagtgctgcat540
cttcataacaataaaattaaaagcctcagtcaacactgttttgatggactagataacctg600
gaaaccctggacttgaattataataacttggatgaatttcctcaggctattaaagccctt660
cccagccttaaagagctgggatttcacagtaattctatttctgttatcccggatggagca720
tttgctggtaatccactgctaagaactatccatttgtatgataatcctctgtcttttgtg780
gggaactcagcatttcacaacctgtctgatctgcattccttagtcattcgtggtgcaagc840
ctggtgcagtggttccccaatctggccggaactgtccatctggagagtctaaccttgaca900
gggacaaaaataagcagcatacctgatgatctgtgccaaaaccaaaagatgctgcggact960
ctggacttatcttataacgatataagagaccttccaagttttaatggttgtcgtgcattg1020
gaagaaatttcattgcagcgtaatcaaatctccctgataaaggaaactacttttcaaggc1080
ctaacatccctaaggattctagatctgagtagaaacctgattcgtgaaattcacagtgga1140
gcttttgcgaagcttgggacaattactaacctggatgtgagtttcaatgaattaacctca1200
tttcctacggaaggcctgaatgggctcaatcaacttaaacttgtgggtaacttccagctg1260
aaagatgccttggcagccagagactttgccaatctcaggtctctatcagtaccatatgct1320
tatcagtgttgtgcattttgggggtgtgactcttatgcaaatttaaacacagaagataac1380
agcccccaagaccacagtgtgacaaaagagaaaggtgctacagatgcagcaaatgccacc1440
agcactgctgaaagtgaagaacatagccaaataatcatccattgtacaccttcaacaggt1500
gct1503
- 还没有人留言评论。精彩留言会获得点赞!