痰热清在制备脑胶质瘤治疗药物中的新用途的制作方法
本发明涉及痰热清的一种新用途,具体为痰热清在制备脑胶质瘤治疗药物中的新用途。
背景技术:
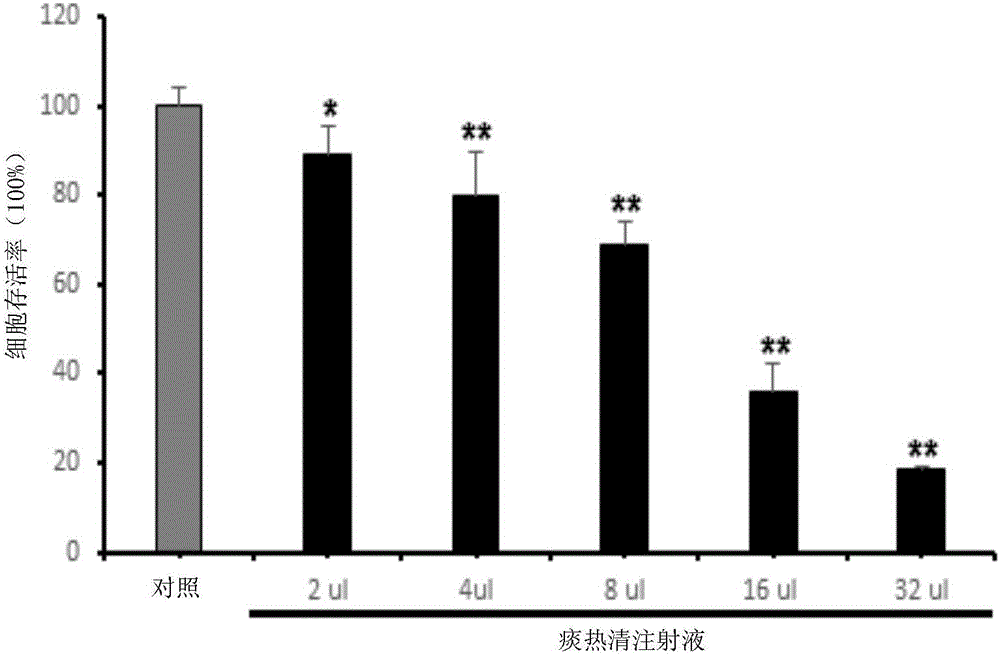
:脑胶质瘤是由于大脑和脊髓胶质细胞癌变所产生的、最常见的原发性颅脑肿瘤。年发病率约为3-8人/10万人口。如同其他肿瘤(疾病)一样,胶质瘤也是由于先天的遗传高危因素和环境的致癌因素相互作用所导致的。一些已知的遗传疾病,例如神经纤维瘤病(i型)以及结核性硬化疾病等,为脑胶质瘤的遗传易感因素。有这些疾病的患者,其脑胶质瘤的发生机会,要比普通人群高很多。此外,一些环境的致癌因素也可能与胶质瘤的发生相关。有研究表明,电磁辐射,例如手机的使用,可能与胶质瘤的产生相关。痰热清注射液是中医临床常用注射剂之一,由黄芩、熊胆粉、山羊角、金银花、连翘等科学组方,有清热解毒、化痰、解痉、抑菌、抗病毒、解热、免疫调节等作用。临床主要可用于呼吸系统疾病、肝胆疾病、消化系统疾病等。技术实现要素:本发明的目的是提供痰热清的一种新用途,具体为痰热清在制备脑胶质瘤治疗药物中的新用途。本发明提供了痰热清在制备脑胶质瘤治疗药物中的应用。所述脑胶质瘤具体可为胶质瘤细胞引起的脑胶质瘤。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护一种脑胶质瘤治疗药物,其活性成分为痰热清。所述脑胶质瘤具体可为胶质瘤细胞引起的脑胶质瘤。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护痰热清在制备抑制胶质瘤细胞增殖的药物中的应用。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护一种抑制胶质瘤细胞增殖的药物,其活性成分为痰热清。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护痰热清在制备杀伤胶质瘤细胞的药物中的应用。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护一种杀伤胶质瘤细胞的药物,其活性成分为痰热清。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护痰热清的入脑成分在制备脑胶质瘤治疗药物中的应用。所述脑胶质瘤具体可为胶质瘤细胞引起的脑胶质瘤。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护一种脑胶质瘤治疗药物,其活性成分为痰热清的入脑成分。所述脑胶质瘤具体可为胶质瘤细胞引起的脑胶质瘤。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护痰热清的入脑成分在制备药物中的应用;所述药物为具有抑制胶质瘤细胞增殖和/或杀伤胶质瘤细胞的功能的药物。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。本发明还保护一种药物,其活性成分为痰热清的入脑成分;所述药物为具有抑制胶质瘤细胞增殖和/或杀伤胶质瘤细胞的功能的药物。所述胶质瘤细胞可为脑胶质瘤细胞。所述胶质瘤细胞可为人源胶质瘤细胞。所述胶质瘤细胞具体可为u87细胞。以上任一所述痰热清具体可为痰热清注射液,例如上海凯宝药业股份有限公司生产的痰热清注射液。以上任一所述痰热清的入脑成分包括如下10种:绿原酸、隐绿原酸、新绿原酸、断氧化马钱子苷、熊去氧胆酸、鹅去氧胆酸、黄芩苷、白杨素苷、汉黄芩苷和千层纸苷。以上任一所述痰热清的入脑成分为如下10种:绿原酸、隐绿原酸、新绿原酸、断氧化马钱子苷、熊去氧胆酸、鹅去氧胆酸、黄芩苷、白杨素苷、汉黄芩苷和千层纸苷。本发明的发明人通过试验发现,痰热清注射液对胶质瘤细胞具有显著的抑制作用,并且痰热清中的大量成分可以透过血脑屏障,因此痰热清可用于治疗脑胶质瘤。附图说明图1为实施例1中第一次试验的结果。图2为实施例1中第二次试验的结果。图3为实施例1中第三次试验的结果。图4为实施例2中检测绿原酸、隐绿原酸、新绿原酸的图谱。图5为实施例2中检测断氧化马钱子苷的图谱。图6为实施例2中检测熊去氧胆酸、鹅去氧胆酸的图谱。图7为实施例2中检测黄芩苷的图谱。图8为实施例2中检测白杨素苷的图谱。图9为实施例2中检测汉黄芩苷、千层纸苷的图谱。具体实施方式以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。痰热清注射液(批号:1606122),上海凯宝药业股份有限公司。实施例1、痰热清对胶质瘤细胞增殖的影响u87细胞(人源胶质瘤细胞株):中国医学科学院细胞资源中心。实施例中的细胞浓度,均是采用细胞计数板计数活细胞得到的。实施例中的细胞培养液均为含10%(体积比)胎牛血清的mem/ebss培养液。实施例中的细胞培养均是置于37℃、含5%(体积比)co2的培养箱中进行的。1、取u87细胞,先进行胰酶消化,然后悬浮于细胞培养液中,得到细胞浓度为5×104个/ml的细胞悬液。2、取96孔板,每孔加入100μl步骤1制备的细胞悬液,培养24小时,然后吸弃上清。3、完成步骤2后,取所述96孔板,每孔加入100μl细胞处理液,培养24小时,然后吸弃上清。细胞处理液由细胞培养液和痰热清注射液组成,痰热清注射液浓度分别设置为:每毫升细胞处理液中含有32μl、16μl、8μl、4μl或2μl痰热清注射液。每个浓度设置四个重复孔。设置不加入痰热清注射液(即每毫升细胞处理液中含有0μl痰热清注射液)的对照。4、完成步骤3后,取所述96孔板,每孔加入100μl新鲜的细胞培养液和10μlcck-8试剂,培养45min。5、完成步骤4后,取所述96孔板,在酶标仪450nm的波长下测定各孔吸光度,计算细胞存活率。细胞存活率=试验孔的吸光度÷对照孔的吸光度×100%。进行三次重复试验。第一次试验的结果见表1和图1(注:与对照相比,*p<0.05,**p<0.01)。表1每毫升细胞处理液中痰热清注射液的含量0μl2μl4μl8μl16μl32μl细胞存活率平均值(%)10089.0979.5868.6835.6818.52标准差4.246.429.95.216.7660.4第二次试验的结果见表2和图2(注:与对照相比,*p<0.05,**p<0.01)。表2每毫升细胞处理液中痰热清注射液的含量0μl2μl4μl8μl16μl32μl细胞存活率平均值(%)10086.8779.2569.2232.5815.42标准差3.321.659.266.585.505.045第三次试验的结果见表3和图3(注:与对照相比,*p<0.05,**p<0.01)。表3每毫升细胞处理液中痰热清注射液的含量0μl2μl4μl8μl16μl32μl细胞存活率平均值(%)10088.0684.3264.3031.2816.49标准差12.0812.5618.173.546.943.66结果表明,痰热清注射液可以显著抑制u87细胞增殖,杀伤u87细胞,且呈剂量效应。实施例2、痰热清透过血脑屏障的试验实施例中所用的大鼠为雄性sd大鼠,spf级,6-7周龄,购自北京维通利华实验动物技术有限公司,许可证号:scxk(京)2016-0011。大鼠饲养于ivc笼具(独立通气笼,长×宽×高=461×274×229mm,意大利tecniplast),每笼3只,保持实验室环境温度为22℃,湿度为50%左右。进行试验前适应性饲养20天。10%水合氯醛(水合氯醛):国药集团化学试剂有限公司,批号为20130201。实施例中所用的采血管为cbas-c30肝素化采血管(cbas-c30heparin-coatedpolyurethanecatheters):solomonscientific,美国。一、最大耐受剂量试验1、股静脉插管手术大鼠试验前禁食12-16h,自由饮水。大鼠称重后,腹腔注射10%水合氯醛麻醉大鼠,然后仰卧位固定,右侧腹股沟部剪毛,碘酒消毒,75%酒精脱碘,然后切开长约1.5cm小口,钝性分离结缔组织、肌肉和神经,使股静脉暴露于视野下,然后剪一小口,小心插入静脉留置导管,结扎。将静脉留置导管从大鼠背部引出,并穿大鼠马甲,ivc笼具单笼饲养,过夜。2、最大耐受剂量试验大鼠分为3组,每组5只,股静脉插管手术的术后第二天,进行最大耐受剂量试验。最大耐受剂量试验中,通过股静脉插入的静脉留置导管进行给药。第一组大鼠,持续多次给药,每次给药在1min内完成,每两次给药的间隔时间为5min。第一次给予痰热清注射液的剂量为5ml/kg体重,之后每次给予痰热清注射液的剂量为2.5ml/kg,直至痰热清注射液的累积总剂量达到20ml/kg体重。持续观察,最后一次给药后,各个大鼠均安静不动,4h内均未死亡。第二组大鼠,持续多次给药,每次给药在1min内完成,每两次给药的间隔时间为5min。第一次给予痰热清注射液的剂量为10ml/kg体重,之后每次给予痰热清注射液的剂量为2.5ml/kg。当痰热清注射液的累积总剂量达到15ml/kg体重时,大鼠出现脚背反弓、抽搐、瘫倒、尾根部颤抖、挠脸等症状,但4h内均未死亡。第三组大鼠,一次性给予痰热清注射液,剂量为15ml/kg体重,在1min内完成。给药完成后,大鼠出现脚背反弓、抽搐、瘫倒、尾根部颤抖等症状,但2-3min后恢复正常,4h内均未死亡。根据最大耐受剂量试验中大鼠反应和未死亡等情况,确定15ml/kg体重为痰热清注射液的给药剂量。二、痰热清透过血脑屏障的试验1、股静脉插管手术同步骤一的1。2、分组并给药大鼠分为4组,每组4-6只,股静脉插管手术的术后第二天进行试验。第二组至第四组的给药剂量均为15ml/kg体重,均为单次给药,通过股静脉插入的静脉留置导管进行给药。第一组大鼠为空白对照组,不给药,麻醉,腹主动脉取血致死(20℃、2500r/min离心15min,取血浆)。剥离头枕部肌肉,暴露枕骨大孔,抽取干净的脑脊液。第二组大鼠,给药15min后麻醉,腹主动脉取血致死(20℃、2500r/min离心15min,取血浆)。剥离头枕部肌肉,暴露枕骨大孔,抽取干净的脑脊液。第三组大鼠,给药30min后麻醉,腹主动脉取血致死(20℃、2500r/min离心15min,取血浆)。剥离头枕部肌肉,暴露枕骨大孔,抽取干净的脑脊液。第四组大鼠,给药60min后麻醉,腹主动脉取血致死(20℃、2500r/min离心15min,取血浆)。剥离头枕部肌肉,暴露枕骨大孔,抽取干净的脑脊液。3、脑脊液样品的检测(痰热清注射液入脑成分研究)绿原酸标准品、熊去氧胆酸标准品、鹅去氧胆酸标准品、汉黄芩苷标准品购自中国食品药品检定研究院。断氧化马钱子苷标准品、白杨素苷标准品、千层纸苷标准品购自成都德锐可生物科技有限公司。隐绿原酸标准品、新绿原酸标准品、黄芩苷标准品购自上海源叶生物科技有限公司。取步骤2得到的脑脊液,进行lc-ms检测。采用美国agilentrrlc液相色谱仪及agilent6320trapms质谱。脑脊液上样样品的制备方法:取100μl脑脊液,用3倍体积色谱纯甲醇醇沉,涡旋,离心,吸取上清液,氮气流吹干,以50μl50%甲醇溶解,涡旋,离心。痰热清注射液用50%甲醇稀释至100倍体积,作为trq注射液样本。液相条件:色谱柱agilentzorbaxsbc18(4.6mm×150mm,5μm)。流动相为a液或b液或a液和b液的混合液。a液为含0.1%(体积比)甲酸的水溶液。b液为9体积份乙腈和1体积份甲醇混合得到的。梯度洗脱过程:0-5min,b液占流动相的体积分数为5%;5-45min,b液占流动相的体积分数由5%线性上升至90%;45-55min,b液占流动相的体积分数为90%。流动相流速为1.0ml·min-1,柱后4:1分流,进质谱的流速为0.2ml·min-1。进样量为10μl。柱温30℃。质谱条件:esi离子源,正离子检测。离子源条件为干燥气温度(gastemp)350℃,干燥气流量10l·min-1,雾化器压力40psi,毛细管电压(capillary)4000v。扫描范围:m/z50~1000。检测绿原酸、隐绿原酸、新绿原酸的图谱见图4。检测断氧化马钱子苷的图谱见图5。检测熊去氧胆酸、鹅去氧胆酸的图谱见图6。检测黄芩苷的图谱见图7。检测白杨素苷的图谱见图8。检测汉黄芩苷、千层纸苷的图谱见图9。检测绿原酸、隐绿原酸、新绿原酸、断氧化马钱子苷、熊去氧胆酸、鹅去氧胆酸、黄芩苷、白杨素苷、汉黄芩苷、千层纸苷的结果见表4。结果表明,痰热清注射液中的10个成分可以透过血脑屏障,进入脑脊液,该10个成分分别为绿原酸、隐绿原酸、新绿原酸、断氧化马钱子苷、熊去氧胆酸、鹅去氧胆酸、黄芩苷、白杨素苷、汉黄芩苷和千层纸苷。表4色谱峰保留时间(min)准分子离子成分鉴定14.6353[m-h]-绿原酸26.0353[m-h]-隐绿原酸39.5353[m-h]-新绿原酸412.2403[m-h]-断氧化马钱子苷516.8445[m-h]-黄芩苷617.8429[m-h]-白杨素苷718.1459[m-h]+汉黄芩苷818.5459[m-h]-千层纸苷928.6391[m-h]-熊去氧胆酸1033.7391[m-h]-鹅去氧胆酸当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1