包含维生素的组合物及其用途的制作方法
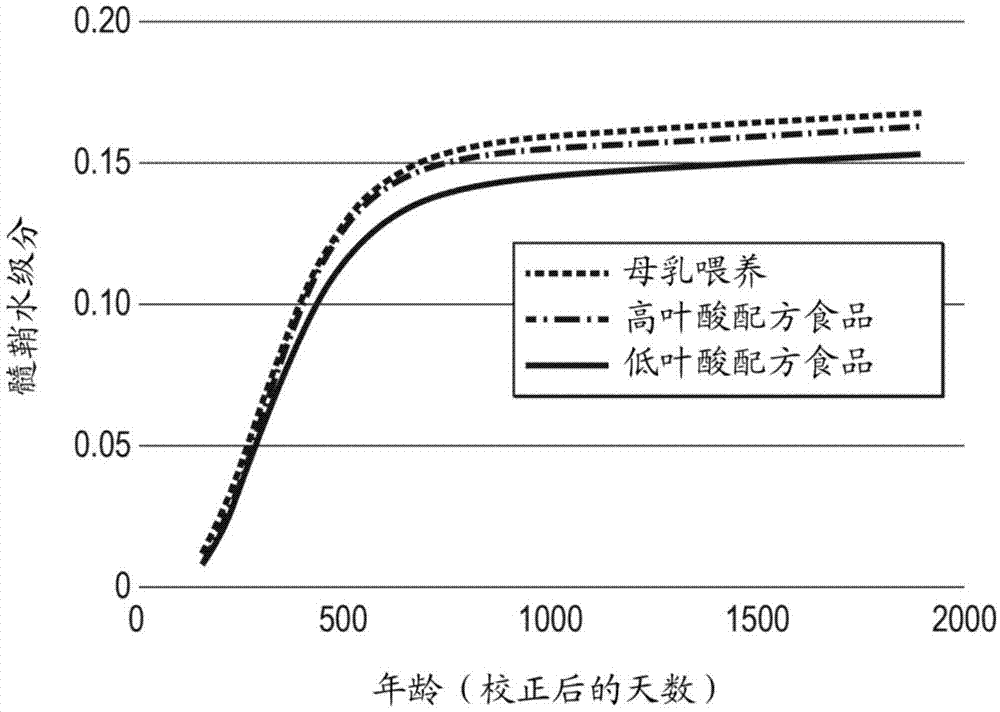
本发明涉及用于促进、支持或优化雌性个体的后代的从头髓鞘形成、和/或脑结构、和/或脑连接、和/或认知潜能、学习潜能和智力潜能中的一种或多种、和/或认知功能的组合物。
背景技术:
在子宫内以及在出生后的头几周或头几个月内,有大量外部因素可能影响婴儿的生长和发育。特别地,持续的研究更加明显地表明母亲的饮食可能影响婴儿的神经发育,特别是脑发育,并且所述影响可能有不可逆的短期和长期后果。子宫内以及出生后的前2年或3年,神经发育特别是脑发育较快,并且对向婴儿提供关键营养物质提出了特别高的要求。在该关键周期内,如果不能满足这些营养物质要求,可导致次优的神经发育,特别是次优的脑发育。一种过程在神经发育、特别是脑发育中起关键作用并且可能对营养因素特别敏感,该过程是从头髓鞘形成,通过该过程裸露轴突被纳入髓鞘。该过程、特别是其后的轨迹,在确定脑结构、特别是整个脑的有髓鞘物质的量和/或空间分布上起着关键作用。脑结构的相关性、特别是整个脑的有髓鞘物质的量和/或空间分布,对于认知功能和智力有很好的记载。本质上,脑中的髓鞘沿着神经元提供绝缘片,从而允许神经脉冲更快地传导。然而,它是影响脑连接的脑结构,特别是整个脑的髓鞘的量和/或空间分布,例如,通过何种途径以及如何快速且有效地以神经脉冲的形式在脑内,特别是在不同的脑区域之间传送消息。这种间脑通信可以在认知功能和学习中发挥作用,并且可能影响并且甚至用于生理限制智力、认知和/或学习潜能。因此,需要识别所需的营养物质,以促进、支持或优化从头髓鞘形成、特别是从头髓鞘形成轨迹,由此脑结构、特别是整个脑的有髓鞘物质的量和/或空间分布。另外需要提供可在孕前、怀孕期间和泌乳期间服用的组合物,以确保母亲被充分供给任何所述营养物质以满足其后代的需求,并由此促进、支持或优化所述后代的从头髓鞘形成、特别是从头髓鞘形成轨迹,并因此脑结构、更特别是整个脑的有髓鞘物质的量和/或空间分布。另外,需要找到优化所述后代的智力潜能和/或认知潜能和/或学习潜能和/或认知功能的方式。此外,重要的是确保母亲被充分供给所述营养物质,以确保其健康,并避免可能由于其后代对于所述营养物质的需求引起的其体内所述营养物质的任何消耗,以及任何相关的健康影响。令人惊讶的是,本发明人现在已经发现某些维生素可促进、支持或优化婴儿的从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是整个脑的有髓鞘物质的量和/或空间分布。技术实现要素:本发明基于包含至少一种维生素的母体补充剂,该母体补充剂用于在妊娠之前或期间以及/或者在后代正在从雌性个体接收母乳时施用于雌性个体。本发明的母体补充剂被视为对后代的从头髓鞘形成具有有益效果。通过母体补充剂促进、支持和/或优化从头髓鞘形成使母亲能够为自己的后代提供健康有益效果,包括在婴儿不再进行母乳喂养时对于婴儿之后生活的长期有益效果。本发明的第一方面因此涉及包含至少一种维生素的组合物,用于促进、支持或优化雌性个体的后代的以下各项中的一个或多个:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能;以及(vii)认知功能,其中所述组合物用于施用于雌性个体。令人惊讶的是,本发明人已经发现包含至少一种维生素的组合物可促进、支持或优化个体的从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是整个脑的有髓鞘物质的量和/或时空分布。当前发现源于纵向认知和脑成像研究的结果的营养分析的结果,其中检查和比较了从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,包括整个脑的有髓鞘物质的量和空间分布。该研究的另外细节和结果在随附示例中给出。本发明的第二方面涉及至少一种维生素,用于促进、支持或优化雌性个体的后代的以下各项中的一个或多个:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能;以及(vii)认知功能,其中所述至少一种维生素用于施用于雌性个体。本发明的第三方面涉及促进、支持或优化雌性个体的后代的以下各项中的一个或多个的方法:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能;以及(vii)认知功能,所述方法包括将治疗有效量的至少一种维生素施用于雌性个体。本发明的第四方面涉及至少一种维生素用于制备促进、支持或优化雌性个体的后代的以下各项中的一个或多个的组合物的用途:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能;以及(vii)认知功能,其中所述组合物用于施用于雌性个体。本发明的第五方面涉及包含至少一种维生素的组合物,其中所述组合物用作用于促进、支持或优化后代的以下各项中的一个或多个的孕前补充剂:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能;以及(vii)认知功能。附图说明图1-示出了母乳喂养的婴儿和幼儿的平均全脑(全白质)髓鞘形成轨迹与用包含不同水平的叶酸的两种商业配方食品喂养的婴儿和幼儿的平均全脑(全白质)髓鞘形成轨迹。图1a-示出了母乳喂养的婴儿和幼儿的平均区域髓鞘形成轨迹与用包含不同水平的叶酸的两种商业配方食品喂养的婴儿和幼儿的平均区域髓鞘形成轨迹。图1b-是示出与叶酸相关的有髓鞘脑区域的脑图像。图2-是示出与维生素b12相关的有髓鞘脑区域的脑图像。图2a-是示出与铁相关的有髓鞘脑区域的脑图像。图2b-是示出与锌相关的有髓鞘脑区域的脑图像。图2c-是示出与钙相关的有髓鞘脑区域的脑图像。图2d-是示出与磷相关的有髓鞘脑区域的脑图像。图2e-是示出与镁相关的有髓鞘脑区域的脑图像。图2f-是示出与鞘磷脂相关的有髓鞘脑区域的脑图像。图2g-是示出与磷脂酰肌醇相关的有髓鞘脑区域的脑图像。图2h-是示出与磷脂酰胆碱相关的有髓鞘脑区域的脑图像。图2i-是示出与胆碱相关的有髓鞘脑区域的脑图像。图2j-是示出与二十二碳六烯酸相关的有髓鞘脑区域的脑图像。图2k-是示出与花生四烯酸相关联的有髓鞘脑区域的脑图像。图3:示出了神经酸对神经元细胞密度和星形胶质细胞密度的影响。图4:示出了硬脂酸对神经元细胞密度和星形胶质细胞密度的影响。图5:示出了辛酸对神经元细胞密度和星形胶质细胞密度的影响。图6:示出了鞘磷脂对神经球数量和神经元增殖的影响。图7:示出了成分、婴儿配方食品、牛乳和人乳中主要sm物质的相对丰度。(误差条表示n=3时的标准偏差)。图8:示出了来自成分、婴儿配方食品、牛乳和人乳的sm级分的相对脂肪酸丰度。(误差条表示n=3时的标准偏差)。图9:在3号配方食品(绿色)或6号配方食品(蓝色)喂养的儿童的不同脑区域中,5岁以上的髓鞘形成轨迹。图10:在6号配方食品(蓝色)喂养或母乳喂养(母乳喂养最少90天)(紫色)的儿童的不同脑区域中,5岁以上的髓鞘形成轨迹。图11:在3号配方食品(绿色)喂养或母乳喂养(母乳喂养最少90天)(紫色)的儿童的不同脑区域中,5岁以上的髓鞘形成轨迹。图12:示出了dha在第18天和/或第30天对mbp、nf和/或mbp/nf的影响。图13:示出了硬脂酸在第14天、第18天和/或第30天对a2b5、mbp、mag、nf、mbp/nf和/或mag/nf的影响。图14:示出了维生素b12在第12天、第18天和/或第30天对a2b5、nf、mbp/nf和/或mag的影响。图15:示出了叶酸在第12天、第18天和/或第30天对a2b5、nf、mag、mag/nf和/或mbp/nf的影响。图16:示出了胆碱在第12天、第18天或第30天对a2b5、mag和/或mbp的影响。图17:示出了铁在第12天、第18天和/或第30天对a2b5、mbp、mag、nf和/或mag/nf的影响。图18:示出了锌在第12天、第18天和/或第30天对mbp、nf和/或mbp/nf的影响。图19:示出了磷在第12天、第18天和/或第30天对mag、nf和/或mag/nf的影响。图20:示出了镁在第22天、第18天和/或第30天对a2b5、mbp、nf、mag、mbp/nf和/或mag/nf的影响。图21:示出了铜在第12天和/或第18天对a2bf、mag和/或mag/nf的影响。图22:示出了磷脂酰胆碱在第12天对a2b5的影响以及在第18天对mag的影响。图23:示出了磷脂酰肌醇在第12天、第18天和/或第30天对a2b5、mbp、mag、nf、mag/nf的影响。图24:示出了磷脂酰丝氨酸在第12天和/或第18天对a2b5、nf和/或mag/nf的影响。图25:示出了鞘磷脂在第12天、第18天和/或第30天对a2b5、mag和/或mbp的影响。图26:示出了神经酰胺在第12天对a2b5的影响和在第18天对mag的影响。图27:示出了半乳糖神经酰胺在第12天和/或第30天对a2b5、mbp、nf和/或mbp/nf的影响。图28:示出了葡糖神经酰胺在第12天对a2b5和在第12天和第18天对nf的影响。图29:示出了d-赤型神经酰胺在第12天对a2b5和在第18天对mag的影响。图30:示出了神经酰胺-1-磷酸在第12天对a2b5以及在第18天对nf和mag的影响。图31:示出了单唾液酸神经节苷脂-3(gm3)在第12天、第18天和/或第30天对a2b5、mbp、mag和/或mbp/nf的影响。图32:示出了双唾液酸神经节苷脂3(gd3)在第12天、第18天和/或第30天对a2b5、mbp、nf和/或mag的影响。图33:示出了实施例7中使用的磷脂酰肌醇(pi)、磷脂酰胆碱、磷脂酰(pc)、磷脂酰丝氨酸(ps)和鞘磷脂的脂肪酸分布型。图34:示出了维生素b12对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图35:示出了ara对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图36:示出了硬脂酸对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图37:示出了锌对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图38:示出了磷脂酰肌醇对mag和mbpmrna表达的影响。图39:示出了gd3对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图40:示出了dha对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图41:示出了神经酸对mag和mbpmrna表达的影响的对mbp和betaiii共表达的影响。图42:示出了铁对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图43:示出了磷脂酰胆碱对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图44:示出了磷脂酰丝氨酸对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图45:示出了叶酸对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图46:示出了胆碱对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图47:示出了神经酰胺对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图48:示出了半乳糖神经酰胺对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图49:示出了葡糖神经酰胺对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图50:示出了神经酰胺-1-磷酸对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图51:示出了d-赤型神经酰胺对mag和mbpmrna表达的影响和对mbp和betaiii共表达的影响。图52:示出了鞘磷脂对mbp和betaiii共表达的影响。图53:示出了gm3对mbp和betaiii共表达的影响。图54a-是示出与母体dha摄入量相关联的有髓鞘脑区域的脑图像。图54b-是示出与母体胆碱摄入量相关联的有髓鞘脑区域的脑图像。图54c-是示出与母体铁摄入量相关联的有髓鞘脑区域的脑图像。图54d-是示出与母体叶酸摄入量相关联的有髓鞘脑区域的脑图像。图54e-是示出与母体维生素b12摄入量相关联的有髓鞘脑区域的脑图像。具体实施方式现在将更详细讲述本发明。应当注意,本申请描述的多个方面、特征、实施例和实施方案可以相容和/或可以组合在一起。为了清楚起见,下文报告的所有实施方案和方面将适用于为本发明以必要的变更描述的不同的实施方案和方面。在本发明的一方面,提供了包含至少一种维生素的合成组合物,该合成组合物用于促进、支持或优化雌性个体的后代的从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是整个脑的有髓鞘物质的量和空间分布(特别是如通过从头髓鞘形成和从头髓鞘形成轨迹所确定的),和/或脑连接,和/或智力潜能和/或认知潜能和/或学习潜能,和/或认知功能,其中所述组合物用于施用于雌性个体。通过促进、支持和/或优化从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是整个脑的有髓鞘物质的量和空间分布(特别是如通过从头髓鞘形成和从头髓鞘形成轨迹所确定的),和/或智力潜能和/或认知潜能和/或学习潜能,和/或认知功能,本发明的组合物可预防、降低风险和/或减轻所述个体的次优的从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是整个脑的有髓鞘物质的量和空间分布(特别是如通过从头髓鞘形成和从头髓鞘形成轨迹所确定的),和/或智力潜能和/或认知潜能和/或学习潜能。这可以是非治疗性或治疗性的。在本发明的上下文中,术语“包含”或“包括”不排除其它可能的要素。本发明的组合物(包括本文所述的多个实施方案)可包含下列要素、由或基本上由下列要素组成:本文所述的本发明的基本要素和必要限制,以及本文所述的或视需求而定的任何其它或可选成分、组分或限制。如本文所用,术语“促进”(“promote”或“promoting”)是指导致某个过程发生的因素或多个因素。如本文所用,术语“支持”(“support”或“supporting”)是指一旦某个过程开始发生便维持该过程的因素或多个因素。如本文所用,术语“优化”(“optimize”或“optimizing”)是指改善或增强。除非另外指明,所有指示营养物质的量表示为根据干燥营养组合物的重量的量。除非另外指明,否则本文表达的所有百分比都按重量计。术语“cfu”应理解为菌落形成单位。如本文所用,术语“治疗有效量”是指例如就后代的以下效果中一种或多种而言产生治疗作用的“活性物质”(在此为维生素或其混合物)的量:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能和(vii)认知功能。如本文所用,“代谢物”是指在代谢期间生成的物质。如本文所用,“代谢前体”是指一种物质,通过代谢反应从该物质形成另一种物质。其中营养物质可以不同形式包含在组合物中(以原样或以包含在营养物质中的盐、络合物或更加复杂的结构的形式),在下文中报告的量旨在原样引用营养物质的量。在一个优选的实施方案中,该组合物促进、支持或优化整个脑的有髓鞘物质的量和/或空间分布、特别是整个脑的有髓鞘物质的量和/或时空分布。在一个优选的实施方案中,该组合物促进、支持或优化从头髓鞘形成轨迹。由于人类母乳在婴儿营养方面是黄金标准,所以在母乳喂养、更特别是营养良好或营养丰富的母亲的完全母乳喂养的个体中测量或观察到的从头髓鞘形成轨迹可能被认为是最佳的。因此,如果本发明的组合物使得个体的从头髓鞘形成轨迹符合或更接近于在母乳喂养的,更特别是营养良好或营养丰富的母亲的完全母乳喂养的个体中测量或观察到的从头髓鞘形成轨迹,则可以认为该组合物优化个体的髓鞘形成轨迹。如果后代的从头髓鞘形成轨迹与所述母乳喂养的个体的轨迹上的任何等同/相同测量点之间的距离为至多50%、特别是至多25%、更特别是至多20%,则后代的从头髓鞘形成轨迹可以被认为符合或更接近于在母乳喂养的、更特别是完全母乳喂养的个体(特别是营养良好或营养丰富的母亲的母乳)中测量或观察到的从头髓鞘形成轨迹。在至多50%的范围内的非限制性示例包括50%、40%、30%、25%、20%、10%、5%、1%、0.5%和0.01%。特别是轨迹将被视为生物等效的。可在时间点的任意组合处测量髓鞘形成轨迹。特别地,时间点在人类个体的生命的前5年内、更特别是人类的生命的前2年或3年、甚至更特别是在人类的生命的第一年中。从头髓鞘形成轨迹可通过以下方式确定:在不同的时间点处、特别是在经过人类个体的生命的前5年、更特别是人类的生命的前2年或3年、甚至更特别是人类的生命的第1年的不同时间点处测量个体的髓鞘相关联的水级分和/或髓鞘相关联的水池。可使用多组分弛豫(mcr)磁共振成像(mri)技术,并且特别是使用mcdespot技术(deoni等人,2008年)来测量个体的髓鞘相关联的水级分和/或髓鞘相关联的水池。特别地,可通过使用mcdespot技术测量髓鞘相关联的水池来确定从头髓鞘形成轨迹(magn.reson.med.200860:1372-1387),其主题据此以引用方式并入)。如果本发明的组合物使一个或多个后代在标准神经发育测试中,例如在mullen早期学习量表上的分数符合或更接近于在母乳喂养的、更特别是完全母乳喂养的个体(特别是营养良好或营养丰富的母亲的母乳)中测量或观察到的分数,则该组合物可被认为是优化后代的认知功能。如果所述后代的标准化的神经发育测试分数中的一个或多个(例如mullen的t分数)与所述母乳喂养个体的标准化的神经发育测试分数中的一个或多个之间的差异小于一个标准偏差,更特别是小于标准化的测试分数的标准偏差的一半,例如小于10分,更特别是小于mullen的t分数的5分,特别是小于2分,则后代的认知和神经发育功能可被认为符合或更接近于在所述母乳喂养个体中测量的认知和神经发育功能。所述标准化神经发育测试分数(例如mullen的t分数),在所述个体和所述母乳喂养的个体中在相同时间点处测量。所述mullen分数可在任何适当的时间点处,并且特别是在人类个体出生后头3年内,更特别是人类出生后头2年,甚至更特别是在人类出生后头一年中测量。如本文所用,术语“雌性个体”是指雌性,尤其是在怀孕之前或期间,或者小孩出生后不久。优选地,雌性个体是哺乳动物个体、更优选地,是猫、狗或人类。甚至更优选地,雌性个体为人类。在所有情况下,雌性个体可能缺乏或临界缺陷(亚临床缺乏)一种或多种维生素,或者雌性个体通过其饮食不能获得一种或多种维生素的足够的每日供应。如本文所用,除非另外指明,术语“后代”涵盖雌性个体的任何发育阶段的后代,包括胎儿、新生儿、婴儿、儿童和成人或其它哺乳动物的胎儿、幼崽、或成年动物(例如猫和狗)。优选地,在本发明的任何实施方案中,术语后代与人类相关,是指新生儿、婴儿和儿童阶段,更优选为新生儿和婴儿阶段。优选地,在本发明的任何实施方案中,术语后代与其它哺乳动物相关(例如猫和狗),是指新生儿或婴儿阶段。如本文所用,术语“新生儿”是指新生儿个体。在人类中,术语新生儿通常是指不到4周的婴儿。如本文所用,术语“婴儿”是指至多12月龄的人类婴儿,并且包括早产婴儿和极早产婴儿,低出生体重的婴儿(即,无论是因为早产还是胎儿生长受限,体重低于2500g(5.5磅)的新生儿),以及小于胎龄(sga)的婴儿(即,出生体重低于相同胎龄的婴儿的第10百分位的婴儿)。如本文所用,术语“儿童”是指1至18岁的人,更优选是1至10岁的人,甚至更优选是1至5岁的人,并且甚至更优选是1至2岁的人。表述“幼儿”是指年龄介于一岁和五岁之间的儿童(包括学步儿)。“早产婴儿”或“早产儿”是指不足月生产的婴儿或幼儿。通常是指妊娠期满37周之前出生的婴儿。表述“足月儿”是指妊娠期37周后出生的婴儿。表述“产后期”或“产褥期”是儿童从出生后即刻算起并且延续约六周的时期。在一个优选的实施方案中,后代是配方食品喂养的婴儿或儿童。如本文所用,术语“配方食品喂养的婴儿或儿童”是指喂予婴儿配方食品和/或成长乳的婴儿或儿童。完全母乳喂养的婴儿或幼儿/仅用母乳喂养的婴儿或幼儿是指绝大部分营养物质和/或能量源于人类母乳的婴儿(“绝大部分”优选为至少90%或至少95%,或至少99%)。主要用婴儿配方食品喂养的婴儿/幼儿通常是指其营养物质和/或能量的营养源主要源于合成的婴儿配方食品、较大婴儿乳或成长乳的婴儿/幼儿。“主要”是指至少50%的那些营养物质和/或能量,或至少75%。如本文所用,术语“从头髓鞘形成”是指在生长和发育期间个体的脑中的裸露轴突进行髓鞘形成的过程。该过程在子宫内开始并且在人类个体的生命的前5年最丰富、特别是人类的生命的前2年或3年。更优选地,该术语是指从头髓鞘形成轨迹。如本文所用,术语“从头髓鞘形成轨迹”是指作为时间的函数的髓鞘形成的程度(如例如通过髓鞘水级分所测量的),并且特别是处于经过婴儿期和儿童期、特别是幼儿期,并且更特别是在人类个体的生命的前5年、更特别是人类的生命的前2年或3年、或生命的第一年。如本文所用,术语“脑结构”是指脑和特定脑区域内的灰质和白质的结构,并且特别地是指如通过从头髓鞘形成并且特别地从头髓鞘形成轨迹(即,通过髓鞘的从头结构沉积)所确定的脑和特定脑区域内的有髓鞘白质。更特别地,该术语是指整个脑的和/或特定脑区域中的有髓鞘物质的量和/或空间分布,并且甚至更特别地是整个脑的和/或特定脑区域中的有髓鞘物质的量和/或时空分布。如本文所用,术语“智力潜能”是指如由生理因素所决定的个体可获得的可能的智能和智力。特别地,智力潜能可以指流体智力。如本文所用,术语“流体智力”是指如由生理因素所决定的个体的神经潜能和/或个体的新型或抽象问题解决能力。这与至少部分地由学习或适应文化的知识决定的晶态智力不同。如本文所用,术语“认知潜能”是指如由生理因素所决定的个体获得的可能的认知和/或心智能力或心智容量。特别地,该术语可以是指以下中的一个或多个:信息处理潜能、感知潜能、注意力潜能、思维潜能、推理潜能、理解和记忆潜能、精神运动潜能(包括粗大运动和精细运动潜能)、视觉潜能(包括视觉接收潜能)、语言潜能(包括表达和接收语言潜能)、记忆和回忆潜能、集中潜能、执行功能潜能(包括解决问题、决策和抑制潜能)。如本文所用,术语“学习潜能”是指如由生理因素所决定的个体必须学习(例如通过经验、研究或被教导,个体能够如何轻松和/或快速获得知识或技能)的可能能力或容量。以及如由生理因素所决定的个体必须适应响应于环境因素的可能能力。维生素(特别是b9和/或b12)可特别有效地支持、促进或优化在以下脑区域中的从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是整个脑的有髓鞘物质的量和/或空间分布:小脑、脑干、颞叶、额叶、视觉皮质、运动和体感皮质。因此,维生素可特别有效地促进、支持或优化视力潜能、运动功能(包括运动潜能的协调和执行)和精神运动潜能。在本发明的优选的实施方案中,认知潜能选自视力潜能、运动功能(包括运动的协调和执行)和精神运动潜能。通过优化这些潜能,本发明的组合物可优化运动功能(包括运动的协调和执行)和/或精神运动功能和/或视力。维生素本发明的组合物包含一种或多种维生素。维生素是生物体以有限量需要的有机化合物和重要营养物质。维生素通常不能被人体足量合成,必须通过饮食来获得。补充对于治疗某些健康问题很重要。维生素按其生物和化学活性而不是其化学结构进行分类。因此,每种维生素是指多种同效维生素化合物,这些化合物共享与特定维生素相关的共同生物活性。此类化学物质被归类为通用类别,诸如“维生素a”,其包括化合物视黄醛、视黄醇和四种已知的类胡萝卜素。根据定义,同效维生素可以转化为体内维生素的活性形式,并且有时也可相互转化。目前普遍认可13种维生素,即a、b1、b2、b3、b5、b6、b7、b9、b12、c、d、e和k。维生素具有不同的生化功能。一些维生素(诸如维生素d)具有激素样功能,作为矿物质代谢的调节剂或细胞和组织生长和分化的调节剂(例如,某些形式的维生素a)。其它用作抗氧化剂(例如,维生素e,有时为维生素c)。维生素的数量最多,复合维生素b用作酶辅因子(辅酶)。在该作用中,维生素可紧密结合到酶,作为辅基的一部分;例如,生物素为参与脂肪酸生成的酶的一部分。它们也可能不像辅酶那样与酶催化剂紧密结合。例如,叶酸可在细胞中携带甲基、甲酰基和亚甲基基团。传统上单独通过食物摄入获得维生素,并且饮食的变化可能会极大地改变摄入维生素的类型和量。然而,自20世纪中期以来,维生素已经作为通用化学品生产,并且可作为廉价的半合成和合成来源的多种维生素膳食和食品补充剂和添加剂广泛获得。在一个优选的实施方案中,组合物包含维生素b9(也称为叶酸或叶酸盐)。叶酸或叶酸盐也称为维生素m、维生素bc(或叶酸类似物)、蝶酰基-l-谷氨酸和蝶酰基-l-谷氨酸盐。叶酸是合成生产的,并且在其被转化为叶酸盐的基础上用于强化食品和补充剂。叶酸是通过二氢叶酸还原酶(dhfr)转化成四氢叶酸盐(四氢叶酸)的合成氧化形式。维生素b9对许多身体功能是必不可少的。人类无法从头合成叶酸盐;因此,叶酸必须通过饮食来提供以满足他们的日常需求。人体需要叶酸来合成dna、修复dna和甲基化dna,以及充当某些生物反应中的辅因子。这对于帮助快速细胞分裂和生长尤其重要。儿童和成人都需要叶酸盐来产生健康的红血球并且预防贫血。叶酸可以原样或以其生理上可接受的盐(叶酸盐)或其混合物的形式掺入本发明的营养组合物中。在本发明的上下文中,术语“叶酸”包括存在于本发明的组合物中的所有叶酸,其为原样或以其生理上可接受的盐或其混合物的形式。优选地,叶酸以占组合物的约0.001%至约99.999%的量包含在组合物中。在一个优选的实施方案中,根据本发明的组合物包含一定水平的叶酸,使得来源于本发明的组合物的每日总摄入量为约50μg至约1000μg,更优选约60μg至约1000μg,甚至更优选约70μg至约700μg,甚至更优选约100μg至约500μg,更优选约200μg至约400μg。在一个优选的实施方案中,组合物包含一定量的叶酸,使得来源于本发明的组合物的每日总摄入量将不超过约1000μg。在一个优选的实施方案中,本发明的组合物包含维生素b12。维生素b12(也称为钴胺素)是水溶性复合维生素,其在脑/神经系统的正常机能和红血球形成中起着关键作用。维生素b12参与细胞代谢,特别是dna合成/调节,并且也在脂肪酸代谢和氨基酸代谢中起作用。动物不能产生维生素b12,而只能通过细菌发酵合成来进行工业生产。维生素b12涵盖一类化学相关的化合物(同效维生素),它们全部都显示类似的生物活性。它包含位于称为咕啉环的平面四吡咯环的中心的钴。维生素的基本结构的生物合成作为羟钴胺素,但是不同形式的维生素之间的转化可以在食用后发生在体内。通用合成形式的维生素是氰钴胺素,通过化学改性细菌羟钴胺素来产生。鉴于其优越的稳定性和低成本,这种形式被用于许多药物和补充剂中以及用于食品的强化。在体内,它被转化成人类生理形式甲基钴胺素和5'-脱氧腺苷钴胺素。维生素b12可以占组合物的约0.001%至约99.999%的量包含在组合物中。在一个优选的实施方案中,组合物包含一定量的维生素b12,使得来源于本发明的组合物的每日总摄入量为约0.2μg至约250μg,更优选约0.26μg至约50μg,更优选约0.5μg至约30μg,甚至更优选约1μg至约10μg,更优选约2μg至约6μg。在一个高度优选的实施方案中,组合物包含一定量的维生素b12,使得来源于本发明的组合物的每日总摄入量为约250μg。在一个优选的实施方案中,组合物包含一定量的维生素b12,使得来源于本发明的组合物的每日总摄入量不超过约50μg。维生素b12可以原样或以一种其生理上可接受的盐或其混合物的形式掺入本发明的组合物中。如果本发明的组合物包含b12和/或叶酸,则特别有利地是它另外包含b6。特定矿物质和其它维生素的存在及其量将根据许多因素而变化,例如,待施用组合物的人或动物的年龄、体重和状况。在一个优选的实施方案中,本发明的组合物包含维生素b1。维生素b1也称为硫胺素或硫胺。其结构由氨基嘧啶和通过亚甲基桥连接的噻唑环组成。噻唑被甲基和羟乙基侧链取代。硫胺素在世界卫生组织的基本药物清单上,该清单是基本卫生系统所需的最重要药物清单。维生素b1的磷酸盐衍生物参与许多细胞过程。最佳表征的形式是焦磷酸硫胺素(tpp),它是糖和氨基酸的分解代谢中的辅酶。在酵母中,tpp也是酒精发酵的第一步所需的。单硝酸硫胺是稳定的非吸湿性盐,常用于食品强化。所有活生物体都使用硫胺素,但它仅在细菌、真菌和植物中合成。动物必须从饮食中获得它,因此,对于人类来说,它是必需的营养物质。在哺乳动物中,缺乏会导致科尔萨科夫综合征、视神经病和影响周围神经系统(多神经炎)和/或心血管系统的称为脚气病的疾病。在不太严重的情况下,非特异性体征包括不适、体重减轻、烦躁和混乱。如果硫胺素缺乏未得到治疗,则可能致命。维生素b1可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素b1可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素b2。维生素b2也称为核黄素。具体地讲,核黄素的活性形式,即黄素单核苷酸(fmn)和黄素腺嘌呤二核苷酸(fad),用作多种黄素蛋白酶反应的辅因子,包括其它维生素的激活。它以前被称为维生素g。维生素b2可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素b2可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素b3。维生素b3(也称为尼克酸或烟酸)是在3-位具有羧基基团(cooh)的吡啶的衍生物。其它形式的维生素b3包括对应的酰胺和烟酰胺(“尼克酰胺”),其中羧基基团被羧酰胺基团(conh2)取代,以及更复杂的酰胺和酯。药物/补充尼克酸主要用于治疗高胆固醇血症和糙皮病(烟酸缺乏症)。饮食中烟酸不足会导致恶心、皮肤和口腔损伤、贫血、头痛和疲倦。缺乏烟酸也可在由于缺乏五种关键维生素(尼克酸、维生素c、硫胺素、维生素d和维生素a)导致的大流行性缺乏症中观察到,并且常见于普遍贫困和营养不良的地区。烟酸和烟酰胺是体内辅酶烟酰胺腺嘌呤二核苷酸(nad)和烟酰胺腺嘌呤二核苷酸磷酸(nadp)的前体。在酶nad+激酶的存在下,nad通过磷酸化转化成nadp。nadp和nad是许多脱氢酶的辅酶,参与氢转移过程。nad在脂肪、碳水化合物、蛋白质和乙醇的分解代谢中以及细胞信号传导和dna修复中很重要。nadp在合成代谢反应诸如脂肪酸和胆固醇合成中很重要。维生素b3可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素b3可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素b5。维生素b5(也称为泛酸或泛酸盐)是水溶性维生素,它是由泛解酸和β-丙氨酸形成的酰胺。只有泛酸的右旋(d)异构体具有生物活性,并且研究表明左旋(l)形式可以拮抗右旋异构体的效应。泛酸对于所有生命形式都是必不可少的,并且参与各种各样的生物过程。泛酸的缺乏可能有许多广泛的影响。动物需要泛酸来合成辅酶a(coa),以及合成和代谢蛋白质、碳水化合物和脂肪。几乎每种食物都含有少量泛酸,鳄梨、全麦谷物、豆类、蛋类、肉类、蜂王浆和酸奶中含有大量泛酸。它通常被发现为其醇类似物维生素原泛醇(泛酸)和泛酸钙。泛硫乙胺是膳食补充剂,其化学结构具有由两个硫原子连接的两个泛酸分子。泛硫乙胺的有效剂量比泛酸的维生素需要量高100倍以上。维生素b5可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素b5可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素b6。维生素b6是指可以在生物系统中相互转化的一组化学类似化合物。维生素b6(吡哆醛5'-磷酸,plp)的活性形式在氨基酸、葡萄糖和脂质代谢的许多酶反应中用作辅酶。更具体地讲,plp参与了常量营养物质代谢、神经递质合成、组胺合成、血红蛋白合成和功能以及基因表达的许多方面。维生素b6的若干种形式(同效维生素)是已知的:吡哆素(pn;最常见的形式为维生素b6补充剂)、吡哆素5'-磷酸盐(pnp)、吡哆醛(pl)、吡哆醛5'-磷酸盐(plp;代谢活性形式)、吡哆胺(pm)、吡哆胺5'-磷酸盐(pmp)、4-吡哆酸(pa)和吡哆醇(吡哆醇的半合成衍生物,其中两个吡哆素部分通过二硫桥结合)。除吡哆酸和吡硫醇以外的所有形式可以相互转化。通过吡哆醛激酶将吸收的吡哆胺转化为pmp,通过吡哆胺-磷酸转氨酶或吡哆醇5'-磷酸氧化酶将该吡哆醛激酶进一步转化为plp,该吡哆胺-磷酸转氨酶或吡哆醇5'-磷酸氧化酶还催化pnp向plp的转化。吡哆醇5’-磷酸氧化酶依赖于作为由核黄素(维生素b2)产生的辅因子的黄素单核苷酸(fmn)。维生素b6可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素b6可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素b7。维生素b7也称为生物素、维生素h或辅酶r。在结构上,它包含与四氢噻吩环稠合的脲基(四氢咪唑并酮)环,其中戊酸取代基连接到四氢噻吩环的碳原子之一。生物素是细胞生长、脂肪酸生产以及脂肪和氨基酸代谢所必需的。更具体地讲,生物素是羧化酶的辅酶,参与脂肪酸、异亮氨酸和缬氨酸的合成,以及糖异生。生物素缺乏是罕见的,因为一般来讲,肠道细菌产生的生物素超出了人体的日常需求。然而,存在许多代谢疾病,其中生物素的个体代谢是异常的,诸如将生物素共价连接到羧化酶上的全羧化酶合成酶的缺乏,其中生物素充当辅因子。生物素缺乏可能是由于膳食摄入不足或影响生物素代谢的一种或多种先天性遗传疾病的遗传造成的。亚临床缺乏可导致轻度症状,而先天性遗传疾病可能具有严重(甚至致命)的后果。生物素-硫胺素敏感性基底神经节疾病是需要生物素(和硫胺素)进行治疗的另一种潜在的危及生命的病症。维生素b7可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素b7可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素a。维生素a涵盖一类不饱和有机化合物,其包括视黄醇、视黄醛、视黄酸和若干种维生素原a类胡萝卜素以及β-胡萝卜素。所有形式的维生素a都具有连接到类异戊二烯链的β-紫罗兰酮环,称为视黄基基团。两种结构特征对维生素活性均是必需的。β-胡萝卜素具有两个连接的视黄基基团,其在体内用于贡献维生素a水平。α-胡萝卜素和γ-胡萝卜素具有单个视黄基基团,其赋予一定的维生素活性。类胡萝卜素β-隐黄质具有紫罗兰酮基团并且在人类中具有维生素活性。维生素a对于生长和发育很重要,用于维持免疫系统和良好的视力。更具体地讲,眼睛的视网膜需要视黄醛形式的维生素a,该视黄醛与蛋白质视蛋白结合以形成视紫质,该视紫质是暗视觉和色觉必需的光吸收分子。维生素a还与视黄酸(视黄醇的不可逆氧化形式)的作用非常不同,该视黄酸是上皮细胞和其它细胞的重要激素样生长因子。在动物源的食品中,维生素a的主要形式是酯,主要是棕榈酸视黄酯,其在小肠中转化为视黄醇。视黄醇用作维生素的储存形式,并且可被转化成其视觉活性醛形式(视黄醛)并且从其视觉活性醛形式转化。视黄醇是商业生产的并且作为酯(诸如视黄醇乙酸酯或棕榈酸酯)施用。维生素a也可以是胡萝卜素α-胡萝卜素、β-胡萝卜素、γ-胡萝卜素和叶黄素β-隐黄质(均含有β-紫罗兰酮环)的形式。维生素a可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素a可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素c。维生素c或l-抗坏血酸或仅有抗坏血酸盐(抗坏血酸的阴离子)是人类和某些其它动物物种的必需营养物质。维生素c涵盖在动物中具有类似活性的若干种同效维生素,包括抗坏血酸及其盐,以及分子的一些氧化形式,例如脱氢抗坏血酸。当这些中的任一者被引入细胞中时,抗坏血酸盐和抗坏血酸均天然存在于体内,因为形式根据ph相互转化。维生素c是至少八种酶促反应的辅因子,包括若干种胶原蛋白合成反应,当功能失调时,引起坏血病的最严重症状。抗坏血酸盐还可以充当抗氧化应激的抗氧化剂。所有动物和植物都需要抗坏血酸盐才能进行一系列必需的代谢反应。它由几乎所有生物体在内部制成。抗坏血酸盐的生物学作用是充当还原剂,为各种酶促反应和少数非酶促反应提供电子。通过谷胱甘肽和nadph依赖性酶促机制,维生素c、半脱氢抗坏血酸和脱氢抗坏血酸的单电子和双电子氧化形式可在体内分别还原。谷胱甘肽在细胞和细胞外液中的存在有助于将抗坏血酸盐维持在还原状态。维生素c可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素c可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素d。维生素d是指负责增强钙、铁、镁、磷酸盐和锌的肠吸收的一组脂溶性甾体化合物。维生素d在钙稳态和代谢中起重要作用。在人类中,该组中最重要的化合物是维生素d3(胆钙化醇)和维生素d2(麦角钙化醇)。胆钙化醇和麦角钙化醇可从饮食和补充剂中摄入。很少食品含有维生素d,并且维生素的主要天然来源是在皮肤中由胆固醇合成的,这取决于日照(特别是uvb辐射)。来自饮食或通过阳光皮肤合成的维生素d是生物失活的;活化需要在肝脏和肾脏中进行酶转化(羟化)。在肝脏中,胆钙化醇(维生素d3)被转化为骨化醇(其也称为骨化二醇(inn)),25-羟基胆钙化醇(又称为25-羟基维生素d3,缩写为25(oh)d3)。麦角钙化醇(维生素d2)在肝脏中被转化为25-羟基麦角钙化醇(又称为25-羟基维生素d2,缩写为25(oh)d2)。骨化醇的一部分被肾脏转化为骨化三醇,该骨化三醇是维生素d的生物活性形式。骨化三醇作为血液中的激素循环,从而调节血流中钙和磷酸盐的浓度并促进骨骼的健康生长和重塑。骨化三醇还影响神经肌肉和免疫功能。维生素d可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素d可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素e。维生素e是指包括生育酚和生育三烯酚的一组化合物。γ-生育酚是西方饮食中最常见的形式,通常可见于玉米油、大豆油、人造黄油和调料中。α-生育酚是维生素e的最具生物活性的形式,是饮食中维生素e的第二常见形式。维生素e的营养含量由α-生育酚活性定义。这种变体可见于小麦胚芽油、葵花油和红花油中。作为脂溶性抗氧化剂,它会停止脂肪经受氧化时形成的活性氧物质的产生。有助于α-生育酚活性的分子是由前缀α-、β-、γ-和δ-标识的四种生育酚和四种生育三烯酚。天然生育酚只以rrr构型出现。合成形式含有八种不同的立体异构体,被称为“全-外消旋”-α-生育酚。水溶性形式(诸如琥珀酸d-α-生育酚)用作食品添加剂。维生素e具有许多生物学功能,抗氧化功能是最为人所知的。α-生育酚是脂溶性抗氧化剂,其用作谷胱甘肽过氧化物酶途径中的抗氧化剂,从而通过与脂质过氧化链反应中产生的脂质自由基反应而保护细胞膜免受氧化。这样将移除自由基中间体并防止氧化反应继续。在该过程中产生的氧化的α-生育酚自由基可通过其它抗氧化剂(诸如抗坏血酸盐、视黄醇或泛醇)的还原而循环回到活性还原形式。其它形式的维生素e具有它们自己的独特特性;例如,γ-生育酚为可与亲电诱变剂反应的亲核物质。生育三烯酚没有被很好地理解,但据信在通过抑制hmg-coa还原酶的活性而保护神经元免受损害和胆固醇降低方面具有特殊作用。δ-生育三烯酚阻止固醇调节元素结合蛋白(srebp)的加工。维生素e可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素e可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含维生素k。维生素k涵盖人体需要的一组结构类似的脂溶性维生素,以完全合成某些蛋白质,这些蛋白质是凝血的先决条件。蛋白质的维生素k相关改性允许它们结合钙离子,否则它们不能这样做。在没有维生素k的情况下,凝血严重受损,并且出现不受控制的出血。低水平的维生素k还会削弱骨骼并促进动脉和其它软组织的钙化。在化学上,维生素k族包含2-甲基-1,4-萘醌(3-)衍生物。维生素k包括两种天然的同效维生素:维生素k1和维生素k2。维生素k2继而由许多相关的化学亚型组成,其中不同长度的碳侧链由原子的类异戊二烯基团构成。此外,三种合成类型的维生素k是已知的:维生素k3、k4和k5。维生素k1(也称为叶绿醌、植物甲萘醌或植物甲萘醌)由植物(特别是绿叶蔬菜)合成。它在动物中起着维生素的作用,并且执行维生素k的传统功能,包括其在凝血蛋白质生产中的活性。动物也可将其转化为维生素k2。两种形式的维生素均含有功能性萘醌环和脂族侧链。叶绿醌具有植基侧链。结肠中的细菌可将k1转化为维生素k2。此外,细菌通常加长维生素k2的类异戊二烯侧链以产生一系列维生素k2形式,最显著的是维生素k2的mk-7至mk-11同系物。除mk-4之外的所有形式的k2只能由细菌产生,所述细菌在无氧呼吸中利用这些形式。维生素k可以占组合物的约0.001%至约99.999%的量包含在组合物中。维生素k可以原样或以其一种生理上可接受的盐或其混合物的形式掺入本发明的组合物中。在一个高度优选的实施方案中,组合物包含以下各项中的一个或多个:1000至3000[mu]gβ胡萝卜素、10至80mg维生素c、1至2mg维生素bl、0.5至1.5mg维生素b6、0.5至2mg维生素b2、5至18mg尼克酸、0.5至2.0[mu]g维生素b12、100至800[mu]g叶酸、30至70[mu]g生物素、1至5[mu]g维生素d、3至10iu维生素e。附加组分在一个高度优选的实施方案中,本发明的组合物还包含以下成分中的一种或多种:矿物质、脂肪酸衍生物、胆碱和磷脂或其代谢物或代谢前体。根据组合物是否旨在每日施用/服用一次或更多次来选择这些附加成分中的每种的量。当本发明的组合物包含维生素和这些附加成分中的一种或多种时,其在促进、支持和/或优化从头髓鞘形成,特别是从头髓鞘形成轨迹、和/或脑结构、特别是整个脑的有髓鞘物质的量和空间分布、和/或脑连接、和/或认知潜能和/或智力潜能和/或学习潜能和/或认知功能方面可具有改善的效应。例如,这可能是因为所述成分在相同和/或单独的互补脑区域中实现从头髓鞘形成。改善的效应可以是协同的。在一个优选的实施方案中,组合物包含磷脂、其代谢物或代谢前体。如本文所用,术语“磷脂”是指任何磷脂。如本文所用,术语“磷脂”是指一种分子,该分子由连接至甘油“头部”的两种脂肪酸构成。甘油分子也连接至磷酸根基团。优选地,磷脂为式(i)的化合物其中:r1为o;x为nh或o;r2为c2-c44饱和或不饱和的、直链或支链的酰基基团;r3为式(ii)或式(iii)的取代基:r4选自c5或c6取代的或未取代的环状烷基或环状烯基基团、以及—(ch2)n—r7;r5为c2-c44饱和或不饱和的直链或支链的酰基基团;r6为c2-c44饱和烷基或烯基基团;r7为—n(ch3)3+、nh3+或式(iv)的取代基:并且n为1至4的整数,优选是1或2。如本文所用,术语“烷基”包括饱和直链和支链烷基基团,该烷基基团可被取代(单-或聚-)或不被取代。将相应地理解术语环状烷基。优选地,环状烷基基团为c3-8,更优选是c3-6环状烷基基团。如本文所用,术语“烯基”是指包含一个或多个双键的碳链,该碳链可为支链或非支链的,并且可被取代(单-或聚-)或不被取代。如本文所用,术语“酰基”是指基团r’(c=o)-,其中r’是饱和(烷基)或不饱和(烯基)的碳链。如本文所用,术语“无环”是指非环状的基团。在一个优选的实施方案中,r4是被一个或多个羟基基团取代的c6环状烷基或环状烯基基团。在一个优选的实施方案中,r4来源于肌糖(c6h12o6),甚至更优选来源于肌醇,即r4为:磷脂的非限制性示例包括磷脂酰肌醇、磷脂酰丝氨酸、磷脂酰乙醇胺、鞘磷脂和磷脂酰胆碱。在一个优选的实施方案中,磷脂选自磷脂酰胆碱、磷脂酰肌醇、磷脂酰丝氨酸、磷脂酰乙醇胺、鞘磷脂以及它们的混合物、以及前述物质中任一种的代谢前体和代谢物、以及它们的混合物。磷脂酰肌醇为式(v)的化合物:其中r8和r9各自独立地为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r8和r9各自独立地为c13至c43支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c44饱和或不饱和的脂肪酸残基,并且甚至更优选是c14至c24饱和或不饱和的脂肪酸残基。更特别地,r8和r9为c13至c23支链或非支链的无环烷基或无环烯基基团,其与它们的相邻羰基基团合在一起为c14至c24饱和或不饱和脂肪酸残基,其中衍生所述脂肪酸残基的脂肪酸选自:c14:0、c15:0、c16:0、c18:0、c20:0、c20:3、c20:4、c21:0、c22:0、c23:0、c24:0、c18:1n-9、c18:2n-6和c24:1n-9。甚至更特别是c18:0、c18:1n-9、c18:2、c20:3和c20:4。正如技术人员将会理解的那样。如本文所用,术语磷脂酰丝氨酸是指磷脂酰-l-丝氨酸。磷脂酰丝氨酸为式(vi)的化合物:其中r10和r11各自独立地为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r10和r11各自独立地为c13至c43支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c44饱和或不饱和脂肪酸残基,并且甚至更优选地为c14至c24饱和或不饱和脂肪酸残基。更特别地,r10和r11为c13至c23支链或非支链的无环烷基或无环烯基基团,其与其相邻羰基基团一起为c14至c24饱和或不饱和的脂肪酸残基,其中衍生脂肪酸残基的脂肪酸选自:c14:0、c15:0、c16:0、c18:0、c20:0、c20:3、c20:4、c21:0、c22:0、c23:0、c24:0、c18:1n-9、c18:2n-6和c24:1n-9。甚至更特别是c18:0、c18:1n-9、c20:4和c22:6。磷脂酰乙醇胺为式(vii)的化合物:其中r12和r13各自独立地为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r12和r13各自独立地为c13至c43支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c44饱和或不饱和脂肪酸残基,并且甚至更优选地为c14至c24饱和或不饱和脂肪酸残基。如本文所用,术语“鞘磷脂”是指脂质分子,或脂质分子的混合物,其中鞘氨醇主链用脂肪酸残基在氨基基团(-nh2)处酰化,并且其中鞘氨醇主链的位置1处的羟基基团与磷酸胆碱或磷酸乙醇胺基团连接。优选地,鞘磷脂为式(viii)的化合物或式(viii)的化合物的混合物:其中r14和r15各自独立地为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r14为c13至c43支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c44饱和或不饱和的脂肪酸残基。可衍生脂肪酸残基的c14至c44饱和或不饱和的脂肪酸的非限制性示例包括:c14:0、c15:0、c16:0、c18:0、c20:0、c21:0、c22:0、c23:0、c24:1、c25:0、c28:1、c30:2、c30:1、c30:0、c32:3、c32:2、c32:1、c32:0、c33:1、c34:3、c34:2、c34:1、c34:0、c35:2、c35:0、c36:4、c36:3、c36:2、c36:1、c36:0、c37:1、c37:0、c38:4、c38:3、c38:1、c38:0、c39:1、c39:0、c40:2、c40:1、c40:0、c41:2、c41:1、c41:0、c42:47、c42:3、c42:2、c42:1、c42:0、c44:3、c44:1。甚至更优选地,r14为c13至c23支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c24饱和或不饱和的脂肪酸残基,其中衍生脂肪酸残基的脂肪酸选自:c14:0、c15:0、c16:0、c18:0、c20:0、c21:0、c22:0、c23:0、c24:0、c18:1n-9、c18:2n-6和c24:1n-9。甚至更优选地,鞘磷脂为式(viii)的化合物的混合物,其中混合物使得包含在混合物中的脂肪酸残基(r14与相邻羰基基团一起)的总数主要是饱和脂肪酸,并且最不占优势的是不饱和脂肪酸。更优选地,混合物将使得混合物中80%至96%的所述脂肪酸残基是饱和脂肪酸,特别是c14、c15、c16、c18、c20、c22、c23、c24饱和脂肪酸,更特别是c16、c18、c20、c22和c24。磷脂酰胆碱为式(ix)的化合物:其中r16和r17各自独立地为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r16和r17各自独立地为c13至c43支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c44饱和或不饱和的脂肪酸残基,并且甚至更优选是c14至c24饱和或不饱和的脂肪酸残基。更特别地,r16和r17为c13至c23支链或非支链的无环烷基、或无环烯基基团,其与其相邻羰基基团一起为c14至c24饱和或不饱和的脂肪酸残基,其中衍生脂肪酸残基的脂肪酸选自:c14:0、c15:0、c16:0、c16:1、c18:0、c20:0、c20:1、c20:3、c20:4、c21:0、c22:0、c22:6、c23:0、c24:0、c18:1n-9、c18:2n-6和c24:1n-9。甚至更特别是c14:0、c16:0、c18:0、c18:1n-9、c18:2n-6、c20:1、c20:3、c20:4和c22:6。特别优选的磷脂包括磷脂酰胆碱、磷脂酰肌醇、磷脂酰丝氨酸和鞘磷脂,更特别是磷脂酰胆碱和/或鞘磷脂。在本发明的一个优选的实施方案中,磷脂是磷脂酰胆碱、磷脂酰肌醇、磷脂酰丝氨酸或鞘磷脂、或前述物质中任一者的代谢前体或代谢物。更优选地,磷脂为磷脂酰胆碱或鞘磷脂,或前述物质中任一者的代谢前体或代谢物。优选地,磷脂、其代谢前体和/或代谢物以组合物的至多99.999%的量包含在组合物中。优选地,鞘磷脂、其代谢前体和/或代谢物以组合物的至多99.999%的量包含在组合物中。更优选地,组合物以200mg至1000mg、400mg至700mg、650mg的量包含鞘磷脂。优选地,磷脂酰胆碱、其代谢前体和/或代谢物以组合物的至多99.999%的量包含在组合物中。更优选地,组合物以300mg至5000mg、1000mg至5000mg、3000mg至5000mg、4000mg至4500mg的量包含磷脂酰胆碱。优选地,磷脂酰肌醇、其代谢前体和/或代谢物以组合物的至多99.999%的量包含在组合物中。更优选地,组合物以50mg至400mg、100mg至250mg、200mg至210mg的量包含磷脂酰肌醇。优选地,磷脂酰丝氨酸、其代谢前体和/或代谢物以组合物的至多99.999%的量包含在组合物中。更优选地,组合物以50mg至500mg、200mg至500mg、400mg的量包含磷脂酰丝氨酸。优选地,磷脂酰乙醇胺、其代谢前体和/或代谢物以组合物的至多99.999%的量包含在组合物中。更优选地,组合物以50mg至500mg、200mg至500mg、400mg的量包含磷脂酰乙醇胺。如果代替磷脂或与磷脂组合将一种或多种磷脂的代谢前体和/或代谢物用于组合物中,则所述化合物的用量使得由所述组合物生理递送的磷脂的水平符合上文列出的那些。确定适当量完全在本领域技术人员的能力范围内。如本文所用,术语一种或多种磷脂的代谢前体和/或代谢物不包括胆碱。磷脂(特别是鞘磷脂、磷脂酰胆碱、磷脂酰肌醇、磷脂酰丝氨酸和/或磷脂酰乙醇胺)的代谢前体和/或代谢物的非限制性示例为:半乳糖神经酰胺、葡糖神经酰胺、鞘氨醇、鞘氨醇-1-磷酸、神经酰胺、d-赤型-二氢神经酰胺和神经酰胺-1-磷酸以及神经节苷脂。特别有效的磷脂包括磷脂酰胆碱、磷脂酰丝氨酸、磷脂酰肌醇和/或鞘磷脂,特别是鞘磷脂。在本发明的一个优选的实施方案中,磷脂为磷脂酰胆碱、磷脂酰丝氨酸、磷脂酰肌醇、鞘磷脂和/或上述中任一者的和/或上述中任一者的组合的代谢前体和/或代谢物。优选地,磷脂为鞘磷脂、其代谢前体和/或代谢物。磷脂、特别是鞘磷脂的特别有效的代谢前体和/或代谢物包括神经酰胺和神经节苷脂和神经节苷脂以及神经酰胺-1-磷酸和d-赤型-二氢神经酰胺。术语“神经酰胺”指示脂质分子,其中鞘氨醇主链用脂肪酸残基酰化。当术语神经酰胺用于本说明书时,其可标识单一神经酰胺物质以及单一神经酰胺物质的混合物。优选地,神经酰胺为式(ixa)的化合物或式(ixa)的化合物的混合物:其中r16a和r17a各自独立地为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r16a为c13至c43支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c44饱和或不饱和的脂肪酸残基。可衍生脂肪酸残基的c14至c44饱和或不饱和的脂肪酸的非限制性示例包括:c14:0、c15:0、c16:0、c18:0、c20:0、c21:0、c22:0、c23:0、c24:1、c25:0、c28:1、c30:2、c30:1、c30:0、c32:3、c32:2、c32:1、c32:0、c33:1、c34:3、c34:2、c34:1、c34:0、c35:2、c35:0、c36:4、c36:3、c36:2、c36:1、c36:0、c37:1、c37:0、c38:4、c38:3、c38:1、c38:0、c39:1、c39:0、c40:2、c40:1、c40:0、c41:2、c41:1、c41:0、c42:47、c42:3、c42:2、c42:1、c42:0、c44:3、c44:1。甚至更优选地,r16a为c13至c23支链或非支链的无环烷基或无环烯基基团,其与相邻羰基基团一起对应于c14至c24饱和或不饱和的脂肪酸残基,其中衍生脂肪酸残基的脂肪酸选自:c14:0、c15:0、c16:0、c18:0、c20:0、c21:0、c22:0、c23:0、c24:0、c18:1n-9、c18:2n-6和c24:1n-9,并且更特别地选自c16:0、c18:0、c20:0、c22:0和c24:0。甚至更优选地,神经酰胺为式(ixa)的化合物的混合物,其中混合物使得包含在混合物中的脂肪酸残基(r16a与相邻羰基基团一起)的总数主要是饱和脂肪酸,并且最不占优势的是不饱和脂肪酸。更优选地,混合物将使得混合物中80%至96%的所述脂肪酸残基是饱和脂肪酸,特别是c14、c15、c16、c18、c20、c22、c23、c24饱和脂肪酸,更特别是c16、c18、c20、c22和c24。如本文所用,术语“神经节苷脂”指示包含如本文所定义的式ixa的神经酰胺的残基的寡糖基神经酰胺脂质分子。当术语神经节苷脂用于本说明书时,其可标识单一神经节苷脂物质以及包含如本文所定义的式ixa的神经酰胺的残基的单一神经节苷脂物质的混合物。特别有效的神经节苷脂可以是单唾液酸神经节苷脂-3(gm3)神经节苷脂和/或双唾液酸神经节苷脂3(gd3)神经节苷脂。神经酰胺-1-磷酸和d-赤型-二氢神经酰胺包含如本文所定义的式ixa的神经酰胺的残基。鞘磷脂可通过神经酰胺和磷脂酰胆碱合成。因此,如果神经酰胺和/或一种或多种神经节苷脂与磷脂酰胆碱、其代谢前体或代谢物组合使用,则可能是特别有益的。包含于本发明组合物中的磷脂、其代谢前体和/或代谢物可为天然的,合成的或它们的混合物。所述代谢前体和/或代谢物可以其纯形式、或基本上纯的形式用于本发明的组合物中。另选地,它们可以包含它们的源的形式加入。适于组合物旨在被其食用的个体摄取的磷脂、其代谢前体和/或代谢物的任何源可用于本发明中。特别地,磷脂、其代谢前体或代谢物将来自天然源,其非限制性示例包括蛋、大豆、牛脑和/或哺乳动物乳或它们的提取物。大豆源的非限制性示例包括大豆卵磷脂食品添加剂,哺乳动物乳的非限制性示例包括牛乳、骆驼乳、绵羊乳、山羊乳,包括脱脂乳。乳的非限制性提取物包括蛋白质提取物(例如,乳清蛋白和酪蛋白)、乳脂肪球膜(mfgm)和包含它们的提取物。可用于本发明的磷脂、其代谢前体或代谢物(特别是鞘磷脂)的特别有用的源是富含α-乳白蛋白和/或非纯α-乳白蛋白的牛乳乳清蛋白浓缩物,其已从乳质乳清蛋白(特别是牛乳乳清蛋白)中提取。α-乳白蛋白是高品质的,易于消化的乳清蛋白,并且是在hm中发现的主要蛋白质。由于α-乳白蛋白和/或富含α-乳白蛋白的乳级分具有高含量的必需氨基酸(特别是色氨酸),所以其理想地用于低蛋白婴儿配方食品中。虽然α-乳白蛋白本身为蛋白质,但非纯源可包含鞘磷脂。在一个优选的实施方案中,磷脂、其代谢前体或代谢物(特别是鞘磷脂)以富含α-乳白蛋白的乳清蛋白浓缩物的形式或作为α-乳白蛋白使用。在一个更优选的实施方案中,使用富含α-乳白蛋白的牛乳清蛋白浓缩物或α-乳白蛋白,其具有一定的磷脂含量,特别是鞘磷脂含量,该含量高于500mg/100g干重的组合物。磷脂、其代谢前体或代谢物的另一个特别有用的源可以是mfgm或包含它们的提取物,特别是mfgm或来自牛乳的包含它们的提取物。如果mfgm或包含它们的提取物包含至少1%、2%、5%、10%、20%、30%、40%磷脂和/或至少0.1%、0.2%、0.5%至5%、0.8%至3%、1%至2%、1.6%、1.9%、1.8%的磷脂酰胆碱、磷脂酰肌醇、磷脂酰丝氨酸、磷脂酰乙醇胺和/或鞘磷脂,则可能是特别有益的。mfgm还可进一步包含镁、磷和/或钙,优选地浓度范围为0.05%至2%、0.1%至0.4%。包含磷脂和/或其代谢前体和/或代谢物(特别是鞘磷脂、磷脂酰胆碱和/或磷脂酰肌醇)的本发明组合物可特别有效地支持、促进或优化在以下脑区域中的一个或多个中的从头髓鞘形成、特别是从头髓鞘形成轨迹、和/或脑结构:小脑、视觉皮质、胼胝体、内囊、额叶、顶叶、颞叶、运动皮质、额叶皮质。这些脑区域与以下中的一个或多个相关联:视力、运动功能(包括运动的协调和执行)、半球形交互、语言功能、听觉功能(包括倾听和注意)、工作记忆、执行功能(包括解决问题、社交处理、和行为交互、空间推理、和语言)。在一个优选的实施方案中,组合物还包含矿物质营养物质。如本文所用,术语矿物质可指任何矿物质。矿物质的非限制性示例包括:铁、锌、钙、磷、铜、镁、碘、锰、氯化物、钾、钠、硒、铬以及它们的组合。矿物质通常以盐的形式添加。特别有效的矿物质包括铁和/或铜和/或锌和/或钙和/或磷和/或镁、特别是铁。在一个优选的实施方案中,本发明的组合物包含铁。铁优选地以占组合物的至多99.999%的量包含在本发明的组合物中。铁可以一种生理上可接受的盐的形式掺入本发明的组合物中,诸如例如:柠檬酸铁、磷酸铁、焦磷酸铁、抗坏血酸亚铁、碳酸亚铁、柠檬酸亚铁、富马酸亚铁、葡萄糖酸亚铁、乳酸亚铁、硫酸亚铁、或它们的混合物。铁也可以生理上可接受的铁络合物(诸如例如edta铁钠盐)或其混合物的形式掺入本发明的组合物中。如果将铁以亚铁盐或络合物(例如,上文列出的亚铁盐)的形式加入到组合物中,则fe2+更具生物可用性,并且因此可能更有益。在一个优选的实施方案中,根据本发明的组合物包含一定水平的铁,使得来源于本发明的组合物的每日总摄入量为约2mg至约50mg,更优选约2.5mg至约45mg,甚至更优选约2.7mg至约45mg,更优选约3mg至约30mg,或约5mg至约20mg。在一个优选的实施方案中,根据本发明的组合物包含一定水平的铁,使得来源于本发明的营养组合物的每日总摄入量将不超过约45mg。在另一个优选的实施方案中,根据本发明的组合物包含一定水平的铁,使得来源于本发明的营养组合物的每日总摄入量将不超过40mg。在本发明的上下文中,术语“铁”包括存在于本发明的组合物中的所有铁,其为游离形式,或者为生理上可接受的盐或其络合物的形式。在一个实施方案中,根据本发明的组合物包含锌。优选地,锌以占组合物的至多99.999%的量包含在本发明的组合物中。优选地,锌以一定量包含在组合物中,使得来源于本发明的组合物的每日总摄入量为约1mg至约50mg,更优选约1mg至约40mg,更优选约1.1mg至约40mg,甚至更优选约2mg至约20mg,甚至更优选地约5mg至约15mg,甚至更优选约8mg至约12mg。在一个高度优选的实施方案中,锌以一定量包含在组合物中,使得来源于组合物的每日总摄入量为约10mg。在一个优选的实施方案中,根据本发明的组合物包含一定水平的锌,使得来源于本发明的营养组合物的每日总摄入量将不超过约40mg。锌可以生理上可接受的盐的形式,和/或通过包含锌(更具体地讲为zn2+,诸如例如:硝酸锌、硫酸锌、葡萄糖酸锌、乙酸锌或它们的混合物)的任何来源,或以生理上可接受的锌络合物(诸如吡啶甲酸锌)或其混合物的形式掺入本发明的组合物中。在一个优选的实施方案中,本发明的组合物包含铜。优选地,铜以组合物的至多99.999%的量包含在本发明的组合物中。优选地,铜以一定量包含在组合物中,使得来源于本发明的组合物的每日总摄入量为约0.1mg至约10mg,更优选约1mg至约8mg,更优选约2mg至约6mg,甚至更优选约2mg至约5mg。在一个优选的实施方案中,根据本发明的组合物包含一定水平的铜,使得来源于本发明的营养组合物的每日总摄入量将不超过约10mg。铜(更具体地讲为cu2+)可以原样或以生理上可接受的盐的形式,和/或通过包含铜的任何来源掺入本发明的组合物中。例如,可将铜掺入到组合物中作为:硫酸铜和/或葡萄糖酸铜和/或碳酸铜、和/或柠檬酸铜、和/或铜-赖氨酸络合物。在一个优选的实施方案中,本发明的组合物包含镁。优选地,镁以组合物的至多99.999%的量包含在本发明的组合物中。优选地,镁以一定量包含在组合物中,使得来源于本发明的组合物的每日总摄入量为约35mg至约350mg,更优选约50mg至约250mg,更优选约100mg至约200mg。在一个优选的实施方案中,根据本发明的组合物包含一定水平的镁,使得来源于本发明的营养组合物的每日总摄入量将不超过350mg。镁(更具体地讲为mg2)可以原样或以生理上可接受的盐的形式,和/或通过包含镁的任何来源掺入本发明的组合物中。例如,碳酸镁、氯化镁、氧化镁、硫酸镁、葡萄糖酸镁、氢氧化镁、柠檬酸镁盐、正磷酸镁盐。在一个优选的实施方案中,本发明的组合物包含钙。优选地,钙以组合物的至多99.999%的量包含在本发明的组合物中。优选地,钙以一定量包含在组合物中,使得来源于本发明的组合物的每日总摄入量为约100mg至约2500mg,更优选约200mg至约2000mg,更优选约250mg至约1500mg,甚至更优选约500mg至约1000mg。在一个优选的实施方案中,根据本发明的组合物包含一定水平的钙,使得来源于本发明的营养组合物的每日总摄入量将不超过2500mg。钙(更具体地讲为ca2+)可以原样或以生理上可接受的盐的形式,和/或通过包含钙的任何来源掺入本发明的组合物中。例如,碳酸钙、氯化钙、柠檬酸钙盐、葡萄糖酸钙、甘油磷酸钙、乳酸钙、氢氧化钙、正磷酸钙盐。在一个优选的实施方案中,本发明的组合物包含磷。优选地,磷以组合物的至多99.999%的量包含在本发明的组合物中。优选地,磷以一定量包含在组合物中,使得来源于本发明的组合物的每日总摄入量为约70mg至约3500mg,更优选约100mg至约2500mg,更优选约200mg至约2000mg,甚至更优选约300mg至约1500mg,甚至更优选约500mg至约1000mg。在一个优选的实施方案中,根据本发明的组合物包含一定水平的磷,使得来源于本发明的营养组合物的每日总摄入量将不超过3500mg。磷可以原样或以生理上可接受的盐的形式和/或通过包含磷的任何源掺入本发明的组合物中,例如磷酸氢二钾、磷酸氢二钠、磷酸二氢钾、磷酸二氢钠、磷酸三钠、磷酸钙、磷酸氢钙以及它们的混合物。包含矿物质,特别是铁、锌、铜、钙、镁和磷中的一种或多种的组合物可特别有效地支持、促进或优化在以下脑区域中的一个或多个中的从头髓鞘形成、特别是从头髓鞘形成轨迹、和/或脑结构:小脑、脑干、视觉皮质、运动和体感皮质、胼胝体、额叶皮质、颞叶白质、内囊、前额皮质、运动皮质。这些脑区域与运动功能(包括运动的协调和执行)、视觉功能、半球形交互、执行功能、工作记忆、问题解决、社交情绪功能、语言、听觉功能、问题解决和/或工作记忆相关联。在一个优选的实施方案中,根据本发明的组合物包含胆碱。胆碱优选地以组合物的至多99.999%的量包含在本发明的组合物中。术语“胆碱”标识含有n,n,n-三甲基乙醇铵阳离子并且具有以下所示结构的季铵盐:在一个优选的实施方案中,抗衡离子x-选自氯离子、氢氧根、柠檬酸根、酒石酸氢根以及它们的混合物。除非另外指明,否则在本发明的上下文中,术语“胆碱”应旨在标识以游离形式(或作为其盐)存在于本发明营养组合物中的所有胆碱,诸如例如胆碱氢氧化物。优选地,胆碱以一定量包含在组合物中,使得来源于本发明的组合物的每日总摄入量为约100mg至约1000mg,更优选约200mg至约600mg,更优选约250mg至约550mg,甚至更优选约300mg至约500mg。优选地,胆碱以一定量包含在组合物中,使得来源于本发明的组合物的胆碱的每日总摄入量为约450mg。胆碱可以原样或以一种生理上可接受的盐(诸如例如:氯化胆碱、柠檬酸胆碱、酒石酸氢胆碱或其混合物)的形式掺入本发明的组合物中。胆碱可作为单种物质,作为构成不同胆碱物质的混合物的成分,或者通过添加包含一种或多种胆碱物质的天然或合成成分的方式掺入本发明的组合物中。如果代替胆碱或与胆碱组合使用胆碱的代谢前体和/或代谢物,则所述化合物的用量使得由所述组合物生理递送的胆碱的水平符合上文列出的那些。确定适当量完全在本领域技术人员的能力范围内。包含胆碱的本发明的组合物可特别有效地支持、促进或优化在以下脑区域中的从头髓鞘形成、特别是从头髓鞘形成轨迹、和/或脑结构:小脑、内囊、运动皮质、视觉皮质、丘脑、顶叶皮质和额叶。这些脑区域与运动功能(包括运动的协调和执行)、视力、工作记忆和/或执行功能和/或社交情绪推理和/或空间推理相关联。在一个优选的实施方案中,本发明的组合物包含脂肪酸衍生物。优选地,脂肪酸衍生物可以占组合物的至多99.999%的量包含在本发明的组合物中。如本文所用,术语“脂肪酸衍生物”包括脂肪酸(特别是游离脂肪酸)、和/或单酰基甘油(下文称为mag)、和/或二酰基甘油(下文称为dag)、和/或三酰基甘油(下文称为tag)和/或胆固醇酯。在一个优选的实施方案中,脂肪酸衍生物为游离的脂肪酸。在另一个优选的实施方案中,脂肪酸衍生物为mag、dag、tag和/或胆固醇酯。甚至更优选地,脂肪酸衍生物为tag。如本文所用,术语“mag”是指其中oh基团中的一个经改性与脂肪酸形成酯键的甘油分子。优选地,mag为式(x)的化合物其中r18、r19和r20中的两个是h,并且r18、r19和r20中的一个是c4至c44饱和或不饱和的酰基基团。更优选地,r18、r19和r20中的两个是h,并且r18、r19和r20中的一个是c10至c24(更优选地为c14至c24)饱和或不饱和酰基基团。如本文所用,术语“dag”是指其中oh基团中的两个经改性与脂肪酸形成酯键的甘油分子。优选地,dag为式(x)的化合物,其中r18、r19和r20中的一个是h,并且r18、r19和r20中的两个各自独立地为c4至c44饱和或不饱和的酰基基团。更优选地,r18、r19和r20中的两个各自独立地为c10至c24(更优选地为c14至c24)饱和或不饱和酰基基团。r18、r19和r20的两个c4至c44饱和或不饱和的酰基基团可以相同或不同。如本文所用,术语“tag”是指与三种脂肪酸形成酯键的甘油分子。优选地,如本文所用,tag是式(x)的化合物,其中r18、r19和r20各自独立地为c4至c44饱和或不饱和酰基基团,更优选地为c10至c24饱和或不饱和酰基基团,更优选地为c14至c24。r18、r19和r20中的三个c4至c44饱和或不饱和的酰基基团可全部相同,全部不同,或者两个可相同并且一个不同。如本文所用,术语“胆固醇酯”是指式(xi)的化合物:其中r21为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r21为c9至c43支链或非支链的无环烷基,或无环烯基基团,其与相邻羰基基团一起对应于c10至c44饱和或不饱和脂肪酸残基,更优选地为c14至c24饱和或不饱和脂肪酸残基。如本文所用,术语“脂肪酸”是指式(xii)的化合物其中r22为c2至c43支链或非支链的无环烷基或无环烯基基团。更优选地,r22为c9至c43支链或非支链的无环烷基或无环烯基基团。可被包含在脂肪酸衍生物(即,该脂肪酸衍生物可为游离脂肪酸或mag、dag、tag和/或胆固醇酯,所述mag、dag、tag和/或胆固醇酯的脂肪酸残基衍生自脂肪酸)中的c10至c44饱和或不饱和的脂肪酸的非限制性示例包括:c10:0、c12:0、c14:0、c15:0、c16:0、c16:1n-7、c18:0、c18:1n-7、c18:1n-9、c18:2n-6、18:3n-3、c20:0、c20:1n-9、c20:2n-6、c20:3n-6、c20:4n-6、20:5n-3、c21:0、c22:0、c22:1n-9、c22:6n-3c23:0、c24:1,特别是24:1n-9、c25:0、c28:1、c30:2、c30:1、c30:0、c32:3、c32:2、c32:1、c32:0、c33:1、c34:3、c34:2、c34:1、c34:0、c35:2、c35:0、c36:4、c36:3、c36:2、c36:1、c36:0、c37:1、c37:0、c38:4、c38:3、c38:1、c38:0、c39:1、c39:0、c40:2、c40:1、c40:0、c41:2、c41:1、c41:0、c42:47、c42:3、c42:2、c42:1、c42:0、c44:3、c44:1。特别地,所述脂肪酸将选自:c10:0、c12:0、c14:0、c16:0、c16:1n-7、c18:0、c18:1n-7、c18:1n-9、c18:2n-6、18:3n-3、c20:0、c20:1n-9、c20:2n-6、c20:3n-6、c20:4n-6、20:5n-3、c22:0、c22:1n-9、c22:6n-3、c24:1、24:1n-9。适于组合物旨在被其食用的个体摄取的任何脂肪酸衍生物可用于本发明中。特别地,脂肪酸衍生物将来自天然源,其非限制性示例包括蛋、藻类、鱼油、霉菌、酵母、种子、植物例如大豆以及动物源例如牛脑、和/或哺乳动物乳或其提取物。大豆源的非限制性示例包括大豆卵磷脂食品添加剂,哺乳动物乳的非限制性示例包括牛乳、骆驼乳、绵羊乳、山羊乳,包括脱脂乳。乳的非限制性提取物包括蛋白质提取物、乳脂肪球膜(mfgm)和包含它们的提取物。脂肪酸衍生物也可来自棕榈油、牛油、猪油、棉籽油、花生油。如果脂肪酸衍生物包含选自c20:4n-6、c22:6n-3、c24:1n-9、c16:0、c18:1n-9和c18.0(特别是c20:4n-6和/或c22:6n-3和/或c18:0)的饱和或不饱和脂肪酸,则可能是特别有利的。更特别是22:6n-3和/或c18:0。包含磷脂(特别是鞘磷脂、磷脂酰胆碱、磷脂酰丝氨酸、磷脂酰肌醇,更特别的是鞘磷脂)的组合物在与这些脂肪酸中的一种或多种组合使用时可能特别有效。c20:4n-6为花生四烯酸(下文称为ara)。c22:6n-3是二十二碳六烯酸(下文称为dha)。24:1n-9是神经酸。c18.0是硬脂酸。c16:0是棕榈酸。c18:1n-9是油酸。优选地,脂肪酸衍生物为daa和/或ara和/或硬脂酸。最特别是含有dha和/或硬脂酸的脂肪酸衍生物。在一个优选的实施方案中,根据本发明的组合物含有包含dha和/或ara和/或神经酸和/或硬脂酸的脂肪酸衍生物,特别是含有dha和/或ara的脂肪酸衍生物。优选地,包含dha和/或ara和/或神经酸和/或硬脂酸的脂肪酸衍生物可以占组合物的至多99.999%的量包含在本发明的组合物中。在一个优选的实施方案中,组合物以一定量包含dha,使得来源于本发明的组合物的每日总摄入量为约100mg至约1500mg,更优选约250mg至约1200mg,甚至更优选约800mg至约1200mg。在一个优选的实施方案中,组合物以一定量包含ara,使得来源于本发明的组合物的每日总摄入量为约100mg至约500mg,更优选约150mg至约450mg,甚至更优选约200mg至约400mg,更优选约250mg至约350mg,或约300mg。在一个优选的实施方案中,组合物以一定量包含神经酸,使得来源于本发明的组合物的每日总摄入量为约5mg至约80mg,更优选约5mg至约50mg,甚至更优选约8mg至约32mg。在一个优选的实施方案中,组合物以一定量包含硬脂酸,使得来源于本发明的组合物的每日总摄入量为约5mg至约80mg,更优选约5mg至约50mg,甚至更优选约4mg至约20mg。包含硬脂酸的脂肪酸衍生物存在于天然来源中,例如棕榈油、牛油、猪油、棉籽油、花生油。包含神经酸的脂肪酸衍生物存在于天然来源中,例如碎叶锦麦(cardaminegracea)、长叶茉莉(heliphilalongifola)、遏蓝菜(thlaspiperfoliatum)、旱金莲(tropaeolumspeciosum)、钱币草(lunariabiennis)、银扇草(lunariaannua)和蒜头果(malaniaoleifera)的种子油;霉菌瘤胃厌氧真菌(neocallismastixfrontalis)、禾白粉菌(erysiphegraminis)和白粉病(sphaerothecahumuli);大西洋假单胞菌(bacteriumpseudomonasatlantica);酵母酿酒酵母(saccharomycescerevisiae)和海洋硅藻圆柱菱形藻(marinediatomnitzschiacylindrus)。包含dha和/或ara的脂肪酸衍生物存在于天然来源,诸如蛋、藻类、真菌或鱼油、和植物。包含脂肪酸衍生物的油可具有各种来源,该脂肪酸衍生物包含dha和/或ara,并且通常包含其它多不饱和脂肪酸(pufa),特别是epa(二十碳五烯酸)。优选地,包含dha的脂肪酸衍生物以含有包含dha和/或ara的脂肪酸衍生物的鱼油的形式提供。鱼油通常包含5重量%或更多,优选地10重量%或更多的包含dha和/或ara的脂肪酸衍生物。通常也可获得含有大量从藻类或微生物获得的包含dha和/或ara的脂肪酸衍生物的油。例如,可使用从包含10重量%或更多,例如20重量%或更多的脂肪酸衍生物的藻类收获的油。如果根据本发明的营养组合物含有包含ara和dha的脂肪酸衍生物,则所述成分可例如以一定量包含在本发明的组合物中,使得dha:ara的重量比在4:1至1:4,例如3:1至1:3,例如2:1至1:2,例如1.5:1至1:1.5,特别是1.1:1至1:1.1的范围内。如果本发明的组合物包含脂肪酸衍生物的混合物,其中该混合物使得本发明的组合物中不饱和脂肪酸和/或脂肪酸残基与饱和脂肪酸和/或脂肪酸残基的重量比在1:1至1:2,1:1.2至1:1.9,1:1.25至1:1.5,1:3至1:4的范围内,则也可能是有益的。此外,当包含dha和/或ara的大量脂肪酸酯衍生物包含在本发明的组合物中时,如果包含饱和长链脂肪酸(特别是c20/24)的脂肪酸衍生物的总量增加,则可能是特别有益的。这些饱和长链脂肪酸可以是髓鞘的重要组分,使得其能够环绕并包覆轴突。优选地,在本发明的组合物中dha和/或aa与这些不饱和长链脂肪酸的重量比例如在1:1至1:10,1:2至1:9,1:3至1:4.5,1:3.5至1:4.5的范围内。本发明的包含脂肪酸衍生物(例如包含dha和/或aa的脂肪酸衍生物)的组合物可在以下脑区域中的一个或多个中特别有效地支持、促进或优化从头髓鞘形成、特别是从头髓鞘形成轨迹、和/或脑结构:小脑、内囊、颞叶、额叶、顶叶、运动和感觉皮质(包括运动的协调和执行)、视觉皮质、额叶皮质。该脑区域和视觉功能、运动功能和精神运动功能(包括运动功能的协调和执行)、和/或执行功能以及社交情绪功能相关联。本领域的技术人员可根据组合物的性质和用途识别适当量的上述营养物质、其代谢前体或代谢物。在一个优选的实施方案中,根据本发明的组合物包含磷脂(优选地为磷脂酰胆碱和/或鞘磷脂)、至少一种维生素(优选地为b9和/或b12)、铁、胆碱和dha。在一个优选的实施方案中,根据本发明的组合物包含磷脂(优选地为磷脂酰胆碱和/或鞘磷脂)、至少一种维生素(优选地为b9和/或b12)、铁、胆碱、dha、aa和锌。在一个优选的实施方案中,根据本发明的组合物包含至少一种维生素(优选地为b9和/或b12)、铁和胆碱。在另一个优选的实施方案中,根据本发明的组合物包含至少一种维生素(优选地为b9和/或b12)、铁和dha。在另一个优选的实施方案中,根据本发明的组合物包含至少一种维生素(优选地为b9和/或b12)、铁和叶酸。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、dha和胆碱。在另一个优选的实施方案中,根据本发明的组合物包含至少一种维生素(优选地为b9和/或b12)、dha和铁。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、dha和至少一种维生素(优选地为b9和/或b12)。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、胆碱和叶酸。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、至少一种维生素(优选地为b9和/或b12)、铁和dha。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、至少一种维生素(优选地为b9和/或b12)、胆碱和铁。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、至少一种维生素(优选地为b9和/或b12)、dha和胆碱。在另一个优选的实施方案中,根据本发明的组合物包含至少一种维生素(优选地为b9和/或b12)、铁、dha和胆碱。在另一个优选的实施方案中,根据本发明的组合物包含鞘磷脂、至少一种维生素(优选地为b9和/或b12)、铁、胆碱和dha。在一个实施方案中,根据本发明的组合物含有包含dha和/或ara的脂肪酸衍生物、维生素b12和/或叶酸、鞘磷脂和铁。本领域的技术人员可根据组合物的性质、目的、目标个体和剂量(例如每天组合物将被个体摄取多少次)来识别适当量的上述营养物质、其代谢前体或代谢物。通常,有效剂量将取决于个体的年龄、体型和健康状态,取决于个体的生活方式,组合物中营养物质的量,并且可能取决于个体的性别。本领域的技术人员将能够识别组合物中适当量的上述营养物质、代谢前体或代谢物,以便在施用后实现它们所允许的最高水平。优选的组合物类型本发明的组合物可为适用于直接施用于雌性个体的任何类型的组合物。根据本发明的组合物优选为固体形式。组合物可为例如咀嚼片、分散片、胶囊、锭剂、糖锭、口香糖、粉末(例如小袋形式)、条形小袋或装有粉末的带盖瓶的形式。优选地组合物为片剂、胶囊或粉末的形式。片剂或胶囊可以单位剂型提供,例如每日一次或两次施用,优选地每日一次施用。粉末组合物可以包含在小袋中。根据本发明的粉末组合物可用于撒在食物或饮料上。特别优选的实施方案以包含粉末的小袋形式提供根据本发明的组合物,其中粉末可分散到饮料中(例如水、果汁、奶等),以提供可口的营养物质液体供口服。在一个优选的实施方案中,该组合物为营养组合物。营养组合物可为例如营养全面的配方食品、营养补充剂、食物产品(诸如乳制品、冷藏或架藏稳定的饮料或汤)、饮食补充剂、代餐或营养棒。在一个优选的实施方案中,该组合物是旨在供成人(特别是怀孕女性)食用的食料。如本文所用,术语“营养组合物”是指滋养个体的组合物。该组合物可为营养全面的配方食品,例如包含蛋白质、碳水化合物和脂肪的源。该营养组合物可以经胃肠内、非肠道或静脉内施用。在一个优选的实施方案中,在肠内并且更优选地在口内摄入组合物。在本发明的一个优选的实施方案中,该组合物包含蛋白质源、脂质源和碳水化合物源中的一种或多种。例如,此类组合物可包含在约2g/100kcal至6g/100kcal的范围内的蛋白质,在约1.5g/100kcal至3g/100kcal范围内的脂质和/或在约1.7g/100kcal至12g/100kcal范围内的碳水化合物。如果组合物是液体,则其能量密度可介于60kcal/100ml和75kcal/100ml之间。如果组合物是固体,则其能量密度可介于60kcal/100g和75kcal/100g之间。在一个优选的实施方案中,该组合物为合成营养组合物。表述“合成组合物”是指通过化学和/或生物方法获得的混合物。优选地,该组合物为低变应原营养组合物。如本文所用,术语“低变应原营养组合物”是指不大可能引起变态反应的营养组合物。在本发明的一个优选的实施方案中,该组合物选自药物组合物、食物产品、食品提取物、饮料、食品添加剂、宠物护理产品、营养品和营养补充剂。在一个高度优选的实施方案中,该组合物为母体补充剂。该补充剂优选地在整个怀孕期间服用以积累各种组成组分的母亲储备,但据信在中期妊娠并更特别是晚期妊娠中的补充是特别有利的。同样补充可在产后继续,如果婴儿将以母乳喂养,则通过母亲消耗该组合物继续,或者以向婴儿直接施用相似的组合物继续,例如通过用于喂养婴儿的婴儿配方食品。在一个高度优选的实施方案中,组合物用于结合婴儿配方食品和/或1段婴儿配方食品和/或成长乳使用,其施用于出生后的婴儿。组合物也可结合婴孩食物和/或强化剂使用。优选地,婴儿配方食品和/或1段婴儿配方食品和/或成长乳和/或婴孩食物和/或强化剂也包含磷脂或其代谢物或代谢前体,其进一步促进、支持或优化婴儿的以下各项中的一个或多个:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;以及(vi)学习潜能;(vii)认知功能。表述“婴儿配方食品”是指旨在专用于供给出生后头4个月至6个月婴儿营养,而且本身可满足这类婴儿的多种营养需求的食料(符合欧盟委员会1991年5月14日颁发的针对婴儿配方食品和2段婴儿配方食品的第91/321/eec号指令中第1.2条的规定)。表述“1段婴儿配方食品”是指旨在专用于供给出生后不满4个月婴儿营养的食料。术语“2段婴儿配方食品”是指专用于供给4个月以上大的婴儿营养、并且是这类婴儿逐渐多元化的饮食中的主要液体成分的食料。在本发明的上下文中,术语“成长乳(gum)”是指营养配方食品,可在停止婴儿配方食品后将其提供给儿童。“成长乳”(或gum)从一岁开始使用。其通常为适合幼儿的特殊营养需求的含乳饮料。术语“婴孩食物”是指旨在专用于供给出生后不满1岁婴儿营养的食品。表述“强化剂”是指适宜与母乳或婴儿配方食品混合的液态或固态营养组合物。术语“离乳期”是指在婴儿饮食中逐步用其它食物替代母亲的乳汁的这一时期。“母亲的乳汁”是指母亲的母乳或初乳(=人类母乳=hbm)。本发明的组合物还可包含已知用于所涉及的组合物类型的任何其它另外成分或赋形剂。此类附加成分的非限制性示例包括:蛋白质、氨基酸、碳水化合物、低聚糖、脂质、益生元或益生菌、必需脂肪酸、核苷酸、核苷、其它维生素、矿物质和其它微量营养素。蛋白质的类型被认为对本发明无关紧要。因此,可使用例如基于乳清、酪蛋白及其混合物的蛋白质源。就乳清蛋白而言,可使用酸乳清或甜乳清或其混合物,以及以任何所需比例混合的α-乳白蛋白和β-乳球蛋白。乳清蛋白可为经改性的甜乳清。甜乳清是较易获得的奶酪制作过程的副产品,常用于制备基于牛乳的婴儿配方食品。然而,甜乳清中含有一种名为酪蛋白糖巨肽(cgmp)的组分,该组分不期望地富含苏氨酸,而色氨酸含量很少。将cgmp从甜乳清中去除可使得蛋白质中苏氨酸的含量更接近于人乳中苏氨酸的含量。然后可在这种经改性的甜乳清中补充那些有关的含量低的氨基酸(主要是组氨酸和色氨酸)。ep880902中描述了将cgmp从甜乳清中除去的方法,wo01/11990中描述了基于此类经改性的甜乳清的婴儿配方食品。该蛋白质可为完整的或水解的,或为完整蛋白质和水解蛋白质的混合物。例如对于被认为处于发生牛奶变态反应风险的个体而言,提供部分水解的蛋白质(水解程度介于2%和20%之间)可能是可取的。如果需要水解的蛋白质,则可根据需要并且如本领域已知的那样进行水解过程。例如,可通过如在ep322589中所述的两个步骤对乳清级分进行酶法水解,以制备乳清蛋白水解物。对于充分水解的蛋白质,可在55℃下先使用alcalase2.4l(ec940459),再使用neutrase0.5l(可得自诺和诺德发酵物公司(novonordiskfermentag)),然后使用胰酶,来对乳清蛋白进行三重水解。如果用作原料的乳清级分基本上不含乳糖,则发现该蛋白质在水解过程中经受少得多的赖氨酸封闭(lysineblockage)。这使得能够将赖氨酸封闭的程度从约15重量%的总赖氨酸降至低于约10重量%的赖氨酸;例如约7重量%的赖氨酸,这大大地提高了蛋白质源的营养质量。可使用任何合适的膳食蛋白质,例如动物蛋白质(诸如乳蛋白、肉蛋白和卵蛋白);植物蛋白(诸如大豆蛋白、小麦蛋白、大米蛋白和豌豆蛋白);游离氨基酸的混合物;或它们的组合。蛋白质的非限制性示例包括酪蛋白、α-乳白蛋白、乳清、大豆蛋白、大米蛋白、玉米蛋白、燕麦蛋白、大麦蛋白、小麦蛋白、黑麦蛋白、豌豆蛋白、卵蛋白、葵花籽蛋白、马铃薯蛋白、鱼蛋白、肉蛋白、乳铁蛋白、血清白蛋白、免疫球蛋白以及它们的组合。乳蛋白(诸如酪蛋白和乳清)和大豆蛋白是特别优选的。本发明的组合物可包含一种或多种氨基酸。氨基酸的非限制性示例包括亮氨酸、苏氨酸、酪氨酸、异亮氨酸、精氨酸、丙氨酸、组氨酸、异亮氨酸、脯氨酸、缬氨酸、半胱氨酸、谷氨酰胺、谷氨酸、甘氨酸、丝氨酸、精氨酸、赖氨酸、蛋氨酸、苯丙氨酸、色氨酸、天冬酰胺、天冬氨酸以及它们的组合。本发明的组合物可包含碳水化合物源。可使用任何碳水化合物源,诸如乳糖、蔗糖(saccharose)、麦芽糖糊精、果糖、葡萄糖、蜂蜜、蔗糖(sucrose)、玉米糖浆固形物、淀粉以及它们的组合。本发明的组合物可包含脂质源。脂质源可以是任何脂质。脂质源优选地提供组合物的5%至40%的能量,例如20%至30%的能量。可使用低芥酸菜籽油、玉米油以及高油酸葵花油的共混物来获得合适的脂肪分布型。优选的脂肪源包括乳脂肪和植物油。也可加入必需脂肪酸,即亚油酸和α-亚麻酸。在一个实施方案中,可添加含有丰富初加工的花生四烯酸(aa)和二十二碳六烯酸(dha)的少量油,诸如鱼油或微生物油。脂质源的n-6和n-3脂肪酸的比率优选地为约5:1至约15:1;例如约8:1至约10:1。脂质的非限制性示例包括:棕榈油、棕榈油精、高油酸葵花油、高油酸红花油、低芥酸菜籽油、鱼油、椰子油、牛乳脂、以及它们的组合。本发明的组合物可包含一种或多种必需脂肪酸。必需脂肪酸的非限制性示例包括亚油酸(la)、α-亚麻酸(ala)和多不饱和脂肪酸(pufa)。本发明的组合物还可包含神经节苷脂(单唾液酸神经节苷脂3(gm3)和双唾液酸神经节苷脂3(gd3))、其它磷脂(诸如,磷脂酰胆碱、磷脂酰乙醇胺、磷脂酰肌醇、磷酯酰丝氨酸)以及它们的组合。该组合物还可包含至少一种益生元,其量优选为约0.3%至约10%。益生元是不可消化的食品成分,其通过选择性地刺激结肠中一种或有限数量的细菌的生长和/或活性对宿主产生有益的影响,从而改善宿主健康状况。这些成分不可消化是指它们在胃或小肠中不能被分解和吸收,因而它们可以完整地通过胃和小肠到达结肠,在结肠处通过有益细菌选择性地发酵。益生元的示例包括特定低聚糖。益生元的非限制性示例包括:任选地含有果糖、半乳糖、甘露糖的低聚糖;膳食纤维,特别是可溶性纤维、大豆纤维;菊粉;以及它们的组合。优选的益生元为低聚果糖(fos)、低聚半乳糖(gos)、异麦芽低聚糖(imo)、低聚木糖(xos)、低聚阿拉伯木糖(axos)、低聚甘露糖(mos)、大豆低聚糖、糖基蔗糖(gs)、乳蔗糖(ls)、乳酮糖(la)、低聚帕拉金糖(pao)、低聚麦芽糖、树胶和/或其水解产物、果胶和/或其水解产物以及前述物质的组合。低聚糖的另外示例描述于wrodnigg,t.m.;stutz,a.e.(1999)angew.chem.int.ed.38:827-828和wo2012/069416(以引用方式并入本文)中。组合物还可包含至少一种益生菌菌株。益生菌是对宿主的健康或良好状态具有有益效果的微生物细胞制剂或微生物细胞组分。益生菌的非限制性示例包括:双歧杆菌属(bifidobacterium)、乳杆菌属(lactobacillus)、乳球菌属(lactococcus)、肠球菌属(enterococcus)、链球菌属(streptococcus)、克鲁维酵母菌属(kluyveromyces)、酵母属(saccharoymces)、假丝酵母属(candida),特别是选自长双歧杆菌(bifidobacteriumlongum)、乳酸双歧杆菌(bifidobacteriumlactis)、动物双歧杆菌(bifidobacteriumanimalis)、短双歧杆菌(bifidobacteriumbreve)、婴儿双歧杆菌(bifidobacteriuminfantis)、青春双歧杆菌(bifidobacteriumadolescentis)、嗜酸乳杆菌(lactobacillusacidophilus)、干酪乳杆菌(lactobacilluscasei)、副干酪乳杆菌(lactobacillusparacasei)、唾液乳杆菌(lactobacillussalivarius)、乳酸乳杆菌(lactobacilluslactis)、鼠李糖乳杆菌(lactobacillusrhamnosus)、约氏乳杆菌(lactobacillusjohnsonii)、植物乳杆菌(lactobacillusplantarum)、唾液乳杆菌(lactobacillussalivarius)、乳酸乳球菌(lactococcuslactis)、屎肠球菌(enterococcusfaecium)、酿酒酵母(saccharomycescerevisiae)、布拉酵母(saccharomycesboulardii)或它们的混合物,优选地选自长双歧杆菌ncc3001(atccbaa-999)、长双歧杆菌ncc2705(cncmi-2618)、长双歧杆菌ncc490(cncmi-2170)、乳酸双歧杆菌ncc2818(cncmi-3446)、短双歧杆菌菌株a、副干酪乳杆菌ncc2461(cncmi-2116)、约氏乳杆菌ncc533(cncmi-1225)、鼠李糖乳杆菌gg(atcc53103)、鼠李糖乳杆菌ncc4007(cgmcc1.3724)、屎肠球菌sf68(ncc2768;ncimb10415),以及它们的组合。如果存在益生菌的话,它的量优选地根据人或动物的年龄而变化。例如益生菌可按每剂型细菌数计以下面的量存在:约5百万至约2500百万、约10百万至约2500百万、约30百万至约2500百万、约50百万至约2500百万、约50百万至约1000百万、约75百万至约2500百万、约75百万至约1000百万、约100百万至约2500百万、约100百万至约1000百万、约250百万至约2500百万、约250百万至约1000百万、约500百万至约2500百万、约500百万至约1000百万、约750百万至约2500百万或约750百万至约1000百万、约10亿至约25亿、约15亿至约25亿。本发明的组合物还可包含膳食纤维。膳食纤维通过小肠而不被酶消化,并且起到天然膨松剂和轻泻剂的功能。膳食纤维可为可溶的或不溶的,并且一般来说两种类型的共混物是优选的。膳食纤维的合适源包括大豆、豌豆、燕麦、果胶、瓜尔胶、阿拉伯树胶、低聚果糖、低聚半乳糖、唾液乳糖以及来源于动物乳的低聚糖。优选的纤维混合物是菊粉与较短链低聚果糖的混合物。优选地,如果存在纤维,则纤维含量介于消耗的配方食品的10g/1和40g/1之间。根据政府机构推荐(诸如usrda),组合物也可包含矿物质和微量营养素,诸如微量元素和维生素。例如,本发明的组合物还可包含据悉日常饮食中必不可少并且营养显著量的一种或多种矿物质。已确定某些矿物质的最低需求量。矿物质的非限制性示例包括:钙、磷、碘、镁、铜、锰、氯化物、钾、钠、硒、铬、钼,以及它们的组合。矿物质通常以盐的形式添加。该组合物还可包含其它组分,诸如肌醇、牛磺酸和/或l-肉碱。例如,组合物可包含以下给定范围内的日剂量的以下微量营养素中的一种或多种:300mg至500mg的钙、50mg至100mg的镁、150mg至250mg的磷、5mg至20mg的铁、1mg至7mg的锌、0.1mg至0.3mg的铜、50[mu]g至200[mu]g的碘、5[mu]g至15[mu]g的硒、1000[mu]g至3000[mu]g的β胡萝卜素、10mg至80mg的维生素c、1mg至2mg的维生素b1、0.5mg至1.5mg的维生素b6、0.5mg至2mg的维生素b2、5mg至18mg的烟酸、0.5[mu]g至2.0[mu]g的维生素b12、100[mu]g至800[mu]g的叶酸、30[mu]g至70[mu]g的生物素、1[mu]g至5[mu]g的维生素d、3iu至10iu的维生素e。如果需要,可将一种或多种食品级乳化剂掺入到配方食品中;例如二乙酰基酒石酸单甘油酯和双甘油酯、卵磷脂以及单甘油酯和双甘油酯。相似地,可包含合适的盐和稳定剂。配方食品优选地经胃肠内施用;例如以用于通过奶或水重构的粉末或液态浓缩物、固体产品或即饮型饮料的形式。该组合物可任选地包含可具有有益效果的其它物质,诸如核苷酸、核苷等。核苷酸的非限制性示例包括胞苷一磷酸(cmp)、尿苷一磷酸(ump)、腺苷一磷酸(amp)、鸟苷一磷酸(gmp)、以及它们的组合。可用于本发明的组合物中的组合物的其它合适和所需成分在食品法典委员会(codexalimentarius)颁发的有关所涉及的营养组合物类型的指南中有所描述。在本发明中使用的组合物可通过任何合适的方式制备。例如,可通过将蛋白质源、碳水化合物源和脂肪源以合适的比例共混在一起来制备该组合物。如果使用乳化剂,则可将其包含在共混物中。此时可加入维生素和矿物质,但为了避免热降解,通常在稍晚一点的时候加入。在共混之前,可先将任何亲脂性维生素、乳化剂等物质溶解于脂肪源中。然后可混入水(优选经受反渗透的水),以形成液体混合物。随后可对液体混合物进行热处理,以降低细菌载量。例如,可将液体混合物迅速加热到约80℃至约110℃范围内的温度,保持约5秒至约5分钟。这可通过蒸汽喷射或热交换器(例如板式热交换器)来进行。然后,可例如通过急速冷却将液体混合物冷却到约60℃至约85℃。接着可将液体混合物均质化;例如分两个阶段进行:第一阶段在约7mpa至约40mpa下进行,第二阶段在约2mpa至约14mpa下进行。然后可进一步冷却均质化混合物,以加入任何热敏感组分;诸如维生素和矿物质。此刻便利地将均质的混合物的ph和固形物含量标准化。将经均质的混合物转移至合适的干燥装置(诸如喷雾干燥器或冷冻干燥器),并将其转化成粉末。该粉末的含水量应小于约5重量%。如果需要增加一种或多种益生菌,可根据任何合适的方法培养所述益生菌,然后例如通过冷冻干燥或喷雾干燥方式制备,以供添加到配方食品中。另选地,可从专业供应商诸如丹麦汉森公司(christianhansen)和日本森永乳业株式会社(morinaga)购买已被制成合适形式的细菌制剂,以供添加到食物产品中。此类细菌制剂可通过干混方式添加到配方食品中。磷脂(诸如鞘磷脂)可在该过程期间的任何阶段加入,但优选地在加热步骤之后添加。在一个优选的实施方案中,组合物包含具有高sn-2棕榈酸酯的甘油三酯,优选地在sn-2位具有超过33%的棕榈酸的甘油三酯。在一些优选的实施方案中,按重量计,棕榈酸占配方食品的总脂肪酸含量的约15%至约25%,诸如约15%至约20%,并且总棕榈酸含量的至少约30%,例如,约35%至约43%位于sn-2位。由脂类营养公司(lipidnutrition)出售的可商购获得的组合物是betapoltmb-55,其为来源于植物油的甘油三酯混合物,其中至少54%的棕榈酸处于甘油分子的sn-2位。在一个优选的实施方案中,本发明组合物的脂肪含量为约40重量%至50重量%(例如约43重量%至约45重量%)的betapoltmb-55。本领域的技术人员将了解,在不脱离本发明的实质和范围的情况下,配方食品中所使用的高sn-2脂肪的百分比以及sn-2棕榈酸酯的总量可以有所变化,并且可使用不同的高sn-2棕榈酸酯油。在另一个实施方案中,常规食物产品(诸如酸奶或早餐谷物)可富含至少一种维生素。在又一个实施方案中,可制备以足以在个体中实现期望效应的量包含至少一种维生素的组合物。该组合物可以是例如片剂、胶囊、锭剂或液体的形式。该补充剂还可包含保护性水性胶体(诸如树胶、蛋白质、改性淀粉)、粘结剂、成膜剂、包封剂/材料、壁/壳材料、基质化合物、包衣、乳化剂、表面活性试剂、增溶剂(油、脂肪、蜡、卵磷脂等)、甜味剂、质构剂、吸附剂、载体、螯合剂、填充剂、共化合物、分散剂、润湿剂、加工助剂(溶剂)、流动剂、掩味剂、增重剂、胶凝剂、凝胶形成剂、抗氧化剂和抗微生物剂。组合物还可包含常规的药物添加剂和佐剂、赋形剂和稀释剂,包括但不限于:水、任何来源的明胶、植物胶、木素磺酸盐、滑石、糖类、淀粉、阿拉伯树胶、植物油、聚亚烷基二醇、风味剂、增稠剂、防腐剂、稳定剂、乳化剂、缓冲剂、润滑剂、着色剂、润湿剂、填充剂等。健康有益效果本发明的组合物对其母亲在孕前或怀孕期间,或在产后泌乳期间被施予此类组合物的婴儿或幼儿的脑的从头髓鞘形成,特别是从头髓鞘形成轨迹具有积极效应。此类积极效应可包括促进和/或支持婴儿或幼儿的最佳从头髓鞘形成,特别是从头髓鞘形成轨迹,这可确定适当的认知、智力和学习潜能,认知技能和能力以及学习的发育。最优的从头髓鞘形成轨迹也可防止形成认知损害或认知延缓。在使用包含至少一种维生素的组合物几天,几周或数月或数年后可以观察到健康效应。本发明的效应可为预防性的(例如避免次优的从头髓鞘形成、特别是脑中的从头髓鞘形成轨迹、脑结构、脑连接、认知、智力和/或学习潜能或认知功能)或有疗效的(例如,恢复最优从头髓鞘形成、特别是脑中从头髓鞘形成轨迹、脑结构、脑连接、认知、智力和/或学习潜能或认知功能)。与婴儿相关的健康效应可通过如下面实施例中所示的各种方法来测量。如上述公开中显而易见的,本发明的组合物可用于促进、支持或优化个体(其母亲在孕前或怀孕期间或者在产后泌乳期间服用了此组合物)的从头髓鞘形成、特别是从头髓鞘形成轨迹、和/或脑结构、特别是脑中有髓鞘物质的量和/或空间分布、和/或脑连接和/或智力潜能、和/或认知潜能和/或学习潜能和/或认知功能。在本发明的另一个方面,提供了促进、支持或优化个体(特别是配方食品喂养的个体)的从头髓鞘形成,特别是从头髓鞘形成轨迹,和/或脑结构,特别是脑中的有髓鞘物质的量和/或空间分布,和/或脑连接,和/或智力潜能和/或认知潜能和/或学习潜能,和/或认知功能的方法,该方法包括在妊娠之前、期间或之后,或在泌乳期间将根据本发明的包含至少一种维生素的组合物喂予所述个体的母亲。本文所述的本发明的组合物的效应可具有长期健康益处。痴呆(例如阿尔茨海默病)导致个体的思维和记忆能力下降,以及情绪和语言问题。个体患有痴呆、特别是阿尔茨海默病的风险通常与人的智力能力或智力相关联。因此,通过优化个体的智力、认知和/或学习潜能,个体患痴呆、特别是阿尔茨海默病的风险可能降低。各种其它精神障碍和/或神经障碍(例如,自闭症和精神分裂症)也与脑结构有关,并且特别是与整个脑的白质的量和/或空间分布有关。通过促进、支持或优化个体的从头髓鞘形成、特别是从头髓鞘形成轨迹、和/或脑结构,可能防止精神障碍和/或神经障碍(例如自闭症),或者降低患这些障碍的风险,或者降低所述病症的严重程度。如对于本领域技术人员显而易见的,母亲直接服用维生素而不是以组合物的形式服用可获得与本文所公开的相同的益处。因此,维生素可以本文所述的任何方法或用途直接用于代替本发明的组合物。如对于本领域技术人员进一步显而易见的,如果将所述维生素,特别是b12和/或b9与一些成分中的一种或多种分别、相继和/或同时施用,则可能是特别有益的:矿物质、脂肪酸衍生物、胆碱和磷脂或其代谢物或代谢前体。如本文所用,“同时”意指与至少一种维生素同时施用附加成分。优选地,附加成分作为根据本发明的组合物的一部分同时施用。如本文所用,“相继”意指在至少一种维生素之前或之后的一定时间段内施用附加成分。时间延迟将根据附加成分和/或磷脂、或其代谢物或代谢前体的性质而变化。如本文所用,“分别”意指例如在施用附加制剂和至少一种维生素之间存在相当大的间隔,使得在施用附加成分时其维生素可能不再以治疗有效量存在于雌性个体的血流中。在一个优选的实施方案中,附加成分在至少一种维生素之前至少2小时、或至少4小时、或至少8小时、或至少12小时、或至少24小时、或至少48小时施用。在另一个优选的实施方案中,附加成分在至少一种维生素之后至少2小时、或至少4小时、或至少8小时、或至少12小时、或至少24小时、或至少48小时施用。本发明的所有细节同样适用于包含至少一种维生素(特别是b12和/或b9)的组合物,并且适用于直接使用至少一种维生素,特别是b12和/或b9和/或任何其它成分。在一个实施方案中,本发明提供了促进、支持或优化在脑中显示次优的从头髓鞘形成轨迹的婴儿或幼儿的从头髓鞘形成的手段,该次优的从头髓鞘形成轨迹可导致认知缺陷、认知能力受损和/或次优的认知发育。此类婴儿可为早产或低出生重量婴儿或小于胎龄的婴儿。本发明还适用于促进、支持或优化足月出生的婴儿或幼儿的髓鞘形成。所有婴儿可得益于本发明,因为所有婴儿都易于或可能易于在脑中形成次优髓鞘形成轨迹。在此类婴儿或幼儿中,在脑中获得接近营养良好的或营养充足的母亲的母乳喂养的婴儿(优选地是出生后的头几个月完全母乳喂养的婴儿)的髓鞘形成轨迹是特别有利的。其在认知能力方面的确为他们提供了健康的状态,这些认知能力与在营养良好的或营养充足的母亲的母乳喂养的婴儿身上观察到的一致。在一个实施方案中,婴儿和幼儿为0至3个月大、0至6个月大、或0至12个月大、或0至36个月大或0至60个月大。施用可将本发明的组合物施用于孕前、怀孕期间或泌乳期间或它们的组合的雌性个体。在一个实施方案中,在产前将本发明的组合物施用于雌性个体并因此间接传输至发育胚或胎儿,例如经由胎盘或羊水。换句话讲,当在怀孕期间将组合物施用于母亲时,后代是在子宫内接触本发明的组合物。产前施用组合物可防止后代的次优髓鞘形成以及与其相关联的效应的发作或减小其风险。在另外的另选的实施方案中,在产后将本发明的组合物施用于泌乳雌性,并因此经由摄入母乳间接传输至新生儿或婴儿,即后代接触化合物仅通过母乳实现。在一个高度优选的实施方案中,该组合物用于在孕前施用于雌性个体,例如希望怀孕的雌性个体。孕前施用根据本发明的组合物可影响子宫内环境。优选地,在本发明的任何方面或任何实施方案中,孕前补充或施用是指在怀孕前的约1-24个月、1-18个月、1-12个月、1-6个月或1-3个月施用。在一个优选的实施方案中,在怀孕前至少1周,或至少2周、或至少3周、或至少1个月、或至少2个月、或至少3个月、或至少4个月、或至少5个月、或至少6个月、或至少12个月、或至少18个月或24个月施用组合物,例如施用于旨在或尝试怀孕的女性。在另一个优选的实施方案中,组合物用于施用于孕期(例如产前)的雌性个体。如本文所用,“产前”是指出生之前、怀孕期间或与怀孕相关的时期。如本文所用,除非另外指出,对于怀孕期间施用(即产前施用)根据本发明的组合物的引用特别是指在妊娠期的任何部分期间或整个妊娠期施用。在本发明的一个优选实施方案中,组合物的施用在怀孕之后尽快开始,至少直到胚胎形成的时期结束。例如,在人类中,胚胎形成时期涵盖发育的前8周(妊娠期的10周)。在一个优选的实施方案中,在整个妊娠期施用组合物。在另一个优选的实施方案中,在妊娠期的大部分期间施用本发明的组合物。在本发明的任何实施方案中,施用时间可在以下范围内:怀孕的第一周、前两周、第一个月、妊娠前三月、妊娠中三月或妊娠末三月。优选地,施用可继续至少直到后代的出生。在一个优选的实施方案中,自怀孕后直至出生(即整个妊娠期时期)尽快施用组合物。在人类中,施用优选地持续以下周期:约1周至出生、约2周至出生、约4周至出生、约8周至出生、约12周至出生、约18周至出生、约24周至出生。在本发明的任何实施方案中,本发明的组合物可另外地在孕前施用于雌性个体以及怀孕期间和/或泌乳期间施用于雌性个体。在一个高度优选的实施方案中,该组合物用于在出生后(例如在产后泌乳期间)施用于雌性个体。在此期间,婴儿可经由来自母亲的母乳接收组合物的有益效果。出生后,可在泌乳期间的部分或整个泌乳期间施用组合物。因此,在一个实施方案中,本发明涉及用于泌乳产后雌性个体的组合物,该组合物包含至少一种维生素,用于促进、支持或优化由所述雌性个体母乳喂养的婴儿的以下各项中的一项或多项:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;(vi)学习潜能;以及(vii)认知功能。对于泌乳雌性个体的引用是指完全或部分母乳喂养其后代的雌性个体。如本文所用,除非另外指明,对于泌乳期间施用根据本发明的组合物的引用包括在产后的任何时间施用化合物,在该时间内后代完全或部分地摄入母乳(个体的母乳)。例如泌乳期间的施用时期可为自泌乳发生开始,直至离乳过程结束,即直至后代停止摄入母乳。在此期间,后代可完全或部分地摄入母乳。优选地,在泌乳期间施用组合物包括在泌乳发生之后施用1-24个月、2-20个月、3-18个月、6-12个月、4-12个月或4-8个月的时间段,在此期间后代完全或部分地摄入母乳。可以预见,本发明的组合物在刚出生后(0-4周、0-8周、0-12周、0-24周)施用于婴儿特别有利,因为在该时间髓鞘形成过程已经开始并且有了明显发展。在一个特别优选的实施方案中,如果后代完全或部分地摄入母乳,在泌乳发生后在泌乳期间施用本发明的组合物两周。在一个优选的实施方案中,向雌性个体施用组合物在产后开始,即并非在怀孕期间,而是从泌乳发生开始。组合物可有利地用于促进、支持或优化婴儿的上述方面的一个或多个,其中组合物在产后泌乳期间被施用于婴儿的母亲,并且可在之后的生活中观察到婴儿身上有益效果,例如在童年期间和/或青春期期间。在另一个实施方案中,本发明的组合物在产前(即从怀孕到出生的任何时间段)以及产后泌乳期间(即从出生直至离乳过程结束(即后代已停止摄入母乳)的任何时间段)都予以施用。另外,在本发明的任何实施方案中,可如上文就产前施用所定义在产前的任何时间段施用组合物,以及如上文就泌乳期间所定义在产后的任何时间段施用组合物,以及在如上所述的这些时间的任何组合中施用。在另一个实施方案中,本发明的组合物作为雌性个体的孕前、孕中或泌乳期间的饮食补充剂,用于促进从头髓鞘形成。另外,当单独用作孕前补充剂时,或以组合形式用作怀孕和/或泌乳期间的补充剂时,本发明的组合物可对未来的后代提供健康有益效果。在一个优选的实施方案中,本发明的组合物被施用于雌性个体持续2周至52周的时间段。在一个优选的实施方案中,其被施用于雌性个体持续2周至24周的时间段,或2周至12周的时间段。在一个更优选的实施方案中,本发明的组合物被施用于雌性个体持续2周至52周,并且在婴儿或幼儿出生或母乳喂养中断后不久后开始。在一个实施方案中,本发明的组合物被喂予母亲持续2周至24周,或2周至12周,并且在婴儿或幼儿出生或母乳喂养中断后不久后开始。在一个实施方案中,母体补充剂用于结合婴儿配方食品和/或1段婴儿配方食品和/或成长乳使用,其施用于出生后的婴儿。组合物也可结合婴孩食物和/或强化剂使用。优选地,婴儿配方食品和/或1段婴儿配方食品和/或成长乳和/或婴孩食物和/或强化剂也包含至少一种维生素,这促进、支持或优化婴儿的以下各项中的一个或多个:(i)从头髓鞘形成;(ii)脑结构;(iii)脑连接;(iv)智力潜能;(v)认知潜能;以及(vi)学习潜能;(vii)认知功能。应当理解,可自由组合本文所公开的本发明的所有特征,而且在不脱离权利要求书所限定的本发明范围的前提下,可对这些特征作出变型和修改。此外,如果特定的特征存在已知的等同物,则应将这些等同物并入本说明书中,如同在本说明书中明确提到这些等同物。下面是用于举例说明本发明的一系列非限制性示例。实验部分:方法、定义和材料mri(磁共振成像):使用白质成像技术获得介于0和5岁之间婴儿和儿童的mri脑扫描。该技术提供定量测量,髓鞘水级分(mwf),其为脑中髓鞘含量的替代标记。当在幼儿早期映射为时间的函数时,可以产生髓鞘形成轨迹。婴儿配方食品组合物:向参与研究的婴儿喂予六种婴儿配方食品,分析它们的髓鞘相关的营养物质的组成/水平。在不同品牌/供应商的标准市售婴儿配方食品中测试营养组合物,并显示其中所含的营养物质的不同水平。认知能力:粗大运动、视觉接收和语言(表达性和接收性)的年龄标准化的(t)分数来源于mullen早期学习量表,这是用于婴儿和6岁或年纪更小的儿童的早期认知发育的标准化的和经过验证的测量工具。母体营养摄入量:怀孕期间的母体营养摄入量在妊娠34周时使用自动自行管理24小时(asa24)膳食评估工具进行评估,这种基于web的工具能够实现多次自动编码的自行管理24小时回忆。营养物质分析6种婴儿配方食品组合物中的每种中的营养物质示于表1中。表1临床研究1婴儿参与者该研究中包括的婴儿是从正常脑和行为发育的较大纵向研究中提取的:布朗大学对成熟过程中髓鞘形成和行为的评估(bambam)。为了专注于神经型发育,已知在学习、神经或精神障碍方面具有潜在风险因素的儿童在招募和登记期间被特别排除。因此,有子宫内酒精或违禁物质暴露的儿童,早产儿(<妊娠37周)或多胎生产,胎儿超声异常,合并妊娠(例如,先兆子痫),apgar评分<8,入住nicu,神经障碍(例如,头部损伤、癫痫),婴儿、父母或兄弟姐妹中的精神障碍或发育障碍(包括需要药物治疗的母亲抑郁症)被排除在外。正在进行的筛查(诸如自闭症mcat,或行为问题cbcl)进一步用于移除具有临床上有关行为或明显医学病症(诸如自闭症谱系障碍)的入选儿童。回顾性数据和前瞻性数据的组合经由以下各项从父母获得:详细的病历和父母面谈,了解所使用的婴儿配方食品的类型、母乳喂养与配方食品喂养的百分比、以及完全母乳喂养的时间长度。该信息在每次研究访问时更新,大约每6个月对2岁以下的儿童进行一次该研究访问,并且年龄较大的儿童则每年进行一次该研究访问。使用该信息,将儿童分类为2组:1号,完全配方食品喂养;和2号,完全母乳喂养至少90天(3个月)。在3个月内喂予母乳和配方食品的组合的儿童被排除在我们的分析之外。完全配方食品喂养组中的婴儿根据在前3个月使用的主要婴儿配方食品的父母报告来进一步细分。主要配方食品被定义为给定90%的时间或更多(例如,在父母在假期期间使用替代品牌的情况下)。使用这些标准,将94名完全配方食品喂养的婴儿和幼儿选入1号组。这些儿童包括13名接受2号配方食品的儿童;28名接受5号配方食品的儿童;8名接受3号配方食品的儿童;39名接受4号配方食品的儿童;5名接受1号配方食品的儿童和1名接受6号配方食品的儿童。关于平均年龄、妊娠持续时间、出生体重、男女比例、种族比例、母亲教育程度、家庭规模以及家中使用的语言(除英语外)的数量,也选择了52名完全母乳喂养的婴儿的样本并与配方食品喂养组进行匹配。表1a中提供了每种配方食品的分组。表1a用于纵向和营养分析的数据明细配方食品1配方食品2配方食品5配方食品3配方食品4配方食品6母乳喂养n儿童51328839152n测量11275614643106成像方法和分析使用mcdespot(t1和t2的多组分驱动平衡单脉冲观察)白质成像技术来扫描每个婴儿,deoni等人(magn.reson.med.2008,60:1372-1387),其在整个脑中的每个点处提供了髓鞘水级分(mwf)的定量测量—髓鞘含量的测量。所有婴儿在自然(即,非镇静)睡眠期间使用声学消声mcdespot成像方案进行扫描。总成像时间在从对于年龄最小的学步儿19分钟到对于年龄较大的4岁儿童24分钟的范围内。所有数据都是在配备有12通道头rf阵列的siemens3ttimtrio扫描仪上获取的。为了最小化扫描内部运动,将儿童用小儿medvac真空固定袋(美国cfi医疗解决方案(cfimedicalsolutions,usa))和泡沫垫包裹。通过减小峰值梯度幅度和转换速率,并且使用噪声隔离扫描仪孔插入件(安静屏障hd复合材料,美国ultrabarrier公司(ultrabarrier,usa))来降低扫描仪噪声。还使用了minimuff儿科耳罩和电动耳机(德国mrconfon公司(mrconfon,germany))。用儿科脉搏血氧测量系统和红外相机连续地监测儿童。所有儿童在mri扫描的持续时间内都保持睡眠,并且分析数据中不存在运动伪影。在图像对准,非脑信号移除,以及对主磁场和传输磁场(b0和b1)不均匀性的校正之后,将三池信号模型(包括髓鞘相关联的水;轴突内外水;和无交换的自由水池)拟合至mcdespot数据以得出基于体素的mwf标测图。然后将每个儿童的标测图与研究特定模板非线性对准。对应于5个双侧区域(额侧、颞侧、枕侧、顶侧和小脑wm)以及胼胝体的主体、膝部和压部的白质遮罩由普通数据库创建,注册到共同模板,并且叠加到每个儿童的mwf标测图上。然后为每个儿童确定每个区域的平均值,并用于随后的发育分析和轨迹建模。发育差异:为了检查母乳喂养的婴儿和配方食品喂养的婴儿之间的发育差异,以及不同配方食品喂养的婴儿之间的发育差异,使用了非线性混合效应建模方法。修改的gompertz生长模型独立地拟合至1号组和2号组,以及每个配方食品子组。四个gompertz模型参数中的每一个然后使用非配对t测试在母乳喂养组和配方食品喂养组之间,并且使用方差分析在4个配方食品子组之间进行比较,然后进行事后tukey测试以确定配方食品组中的哪些不同。认知评估和分析除mr成像外,使用mullen早期学习量表msel(mullenem,1995年)在扫描后7天内评估每个儿童的一般认知能力和技能。msel提供对精细运动和粗大运动控制、接收性和表达性语言以及视觉接收领域的行为发育的广泛评估。来自这些领域的年龄标准化的t分数可以合并为三个综合分数:早期学习综合分数(elc,包括精细运动、视觉接收、表达性和接收性语言);非言语发育商数(nvdq,包括精细运动和视觉接收分数);以及语言发育商数(vdq,包括表达性和接收性语言分数)。与mwfmri数据一样,检查在母乳喂养的婴儿和配方食品喂养的婴儿之间,以及在不同配方食品子组之间elc、vdq和nvdq的潜在组平均差异。除了平均值比较之外,使用假设线性趋势的混合效应建模来研究这三个综合值的纵向变化。实施例1来自横截面分析的营养驱动因素识别从上述组群中,在婴儿期喂予不同婴儿配方食品的5岁以下儿童被包括在大型相关分析中,以检查配方食品营养组成与脑髓鞘形成之间的关系。针对其营养组合物分析了该组群中6种最常用的配方食品。构建模拟所有定量的营养物质和儿童年龄的单一通用线性模型(glm)。然后在每个图像体素或脑内的点处计算营养物质含量和髓鞘含量值(针对儿童年龄调整)之间的spearman等级相关性。使用基于群集的校正方法,将显著性定义为针对第1类误差校正的p<0.05。将关联或趋势定义为p<0.15。在初始分析中,表1中示出的全部22种营养物质导致动力不足的模型。为了减少模型中的营养组分的数量,我们检查了营养间相关性。使用0.9的保守阈值,我们排除了在各种配方食品中彼此高度相关的营养组分。这产生了最终模型,其包括铁、鞘磷脂、叶酸、胆碱、dha、锌和磷脂酰胆碱。p<0.05:铁、鞘磷脂、叶酸、胆碱、dha。p<0.15:锌和磷脂酰胆碱。发现彼此高度相关的营养组分是:叶酸和维生素b12。dha和aa。锌、钙、镁、铜和磷。磷脂酰胆碱、磷脂酰丝氨酸和磷脂酰肌醇。对于叶酸,在脑中,特别是在小脑、运动皮质、视觉皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果报告于图1b中。对于维生素b12,在脑中,特别是在小脑、视觉皮质、运动和体感皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2中报告。对于铁,在脑中,特别是在小脑、视觉皮质、内囊、运动和体感皮质、胼胝体、额叶皮质、颞叶白质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果报告于图2a中。对于锌,在脑中,特别是在小脑、视觉皮质、内囊、运动和体感皮质、胼胝体、额叶皮质、颞叶白质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2b中报告。对于钙,在脑中,特别是在小脑、视觉皮质、运动和体感皮质、胼胝体、额叶皮质、颞叶白质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2c中报告。对于磷,在脑中,特别是在小脑、视觉皮质、运动和体感皮质、前额皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果报告于图2d中。对于镁,在脑中,特别是在小脑、视觉皮质、内囊、胼胝体、额叶皮质、运动皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2e中报告。对于鞘磷脂,在脑中,特别是在小脑、视觉皮质、内囊、额叶、顶叶、颞叶中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2f中报告。对于磷脂酰肌醇,在脑中,特别是在小脑、视觉皮质、运动皮质、额叶皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果报告于图2g中。对于磷脂酰胆碱,在脑中,特别是在小脑、视觉皮质、内囊、额叶、顶叶、颞叶中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2h中报告。对于胆碱,在脑中,特别是在小脑、视觉皮质、丘脑、顶叶皮质和额叶中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2i中报告。对于dha,在脑中,特别是在小脑、初级和次级运动皮质、内囊、视觉皮质、额叶皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2j中报告。对于aa,在脑中,特别是在小脑、内囊、顶叶、运动和感觉皮质、视觉皮质、额叶皮质中随时间推移观察到与髓鞘形成(髓鞘水级分)的关联。结果在图2k中报告。实施例2a)来自纵向研究的整个脑髓鞘形成轨迹从可用数据中,使用来自其婴儿配方食品(此类配方食品的组合物在下表3中报告)含有不同量的叶酸和维生素b12的儿童的重复mwf数据来计算纵向髓鞘发育(从头髓鞘形成)的轨迹。使用纵向非线性混合效应方法计算轨迹。将修改的gompertz生长模型拟合至每个配方食品组的儿童的数据。结果报告于图1中。表3:(低叶酸/b12含量)(高叶酸/b12含量)叶酸107mcg/100g306mcg/100g维生素b124.93mcg/100g8.34mcg/100gb)来自纵向研究的平均区域脑髓鞘形成轨迹从可用数据中,使用来自其婴儿配方食品(此类配方食品的组合物在下表2a中报告)含有不同量的叶酸和维生素b12的儿童的重复mwf数据来计算纵向髓鞘发育(从头髓鞘形成)的平均区域轨迹。使用纵向非线性混合效应方法计算轨迹,并且将修改的gompertz生长模型拟合至每个配方食品组的儿童的数据。结果在图1a中报告。表3a(低叶酸/b12含量)(高叶酸/b12含量)叶酸98.8mcg/100g306mcg/100g维生素b124.66mcg/100g8.34mcg/100g临床研究2参与者:母亲-婴儿对在美国科罗拉多儿童医院,以混合横截面/纵向群组采集21个母子对的可用数据集。从当地社区抽取孕妇,入选标准如下:至少18岁,讲英语(第一语言),单胎妊娠,在孕期无吸烟、酒精或违禁药物使用情况,胎儿超声无异常,在怀孕前或怀孕期间无高血压或糖尿病史,无重大精神病学或学习障碍(包括重度抑郁症)或使用精神科药物的个人史,没有关于其他儿童的重大精神病学或学习障碍的报告,怀疑体内有金属或其他mri禁忌。这些标准旨在提供不具有神经发育异常或改变的主要风险因素的一般健康群组。婴儿的入选标准为:父母说英语(第一语言),单胎妊娠,足月(37周妊娠之后)出生,在孕期未暴露于烟、酒精或违禁药物,胎儿超声无异常,没有进新生儿重症监护病房,apgar评分>=8,母亲在孕前或怀孕期间无高血压或糖尿病史,父母或兄弟姐妹无重大精神病学或学习障碍历史,婴儿无神经系统创伤历史,无其他神经系统病症(例如,癫痫),怀疑体内有金属或其他mri禁忌。取得所有父母的知情同意书,包括对美国、mri和其他实验室设施的描述、总体研究方案以及关于将获得的每项测量的具体细节。成像方法和分析使用mcdespot(t1和t2的多组分驱动平衡单脉冲观察)白质成像技术来扫描每个婴儿,deoni等人(magn.reson.med.2008,60:1372-1387),其在整个脑中的每个点处提供了髓鞘水级分(mwf)的定量测量-髓鞘含量的测量。所有婴儿在自然(即,非镇静)睡眠期间使用声学消声mcdespot成像方案进行扫描。使用优化方案获取全脑(1.7×1.7×1.7)mm3数据,该方案包括用于主磁场和发射磁场不均匀性校正的附加步骤(deoni等人,2008;deoni,2011;deoni等人,2013)。在采集和处理(包括运动校正、头骨剥离、b0和b1地图校准以及基于体素的参数估计)之后,使用多步注册方法(deoni等人,2012;dean等人,2014c;2014d),将计算出的t1、t2和mwf“地图”与mni空间非线性对齐。分析中包括的儿童在90至180天龄之间进行了一次mri扫描,平均为117天+/-71天龄。相关性分析:为了研究妊娠期34周的母体营养摄入量数据与约3至6个月的婴儿脑中髓鞘含量之间的关联,执行相关性分析(pearson)。实施例3从上述群组可以看出,母体营养摄入量数据与婴儿脑髓鞘含量相关联。以下营养物质在p<0.001的水平上表现出显著性:dha、胆碱、铁、b12和叶酸。使用掩膜显著性的所识别区域,然后观察那些掩膜中的髓鞘水级分与母体营养值之间的相关性(实际上为部分相关性,因为我们纳入了年龄的效应),我们有如下发现:b12:r2=0.39胆碱:r2=0.33dha:r2=0.44叶酸:r2=0.173铁:r2=0.18对于dha、胆碱、铁、b12和叶酸,在以下脑区域观察到与母体摄入量和髓鞘形成(髓鞘水级分)的关联:b12:小脑、颞叶、额叶叶酸:小脑、脑干铁:小脑、脑干胆碱:小脑、内囊、运动皮质dha:小脑、内囊、颞叶、额叶皮质、运动皮质结果报告于图54a至54e中。实施例4供应商和原液溶液化合物公司cat号cas号原液辛酸sigmao390712407-250mm神经酸fluka8711750637-610mm硬脂酸fluka8567957-11410mm鞘磷脂sigmas07568518710-610mm载体和剂量培养基组合物和培养方法1)神经基础完全培养基神经基础培养基(lifetechnologiescorp,21103-049号)50xb27补充剂(lifetechnologiescorp,12587-010号)2mml-谷氨酰胺(lifetechnologiescorp,25030-149号)1x青霉素-链霉素(lifetechnologiescorp,15140-122号)2)具有生长因子(gf)的神经基础完全培养基具有gf混合物的上述配方1mtris(mw121.14,fisherscibp152)肝素(sigmah3149)bsa(sigmaa7030)dna酶、rna酶、蛋白酶游离水(fishersciac327390010)egf(gibcophg0311)bfgf小瓶(gibcophg0021)3)无胆碱的神经基础培养基(lifetechnologies,定制配制,无l-谷氨酰胺,无酚红)注意:完全培养基和具有gf的完全培养基与上述相同。神经祖细胞(npc)库的生成:e14小鼠新皮质的解离所需试剂:dpbs(1x)+10%青霉素/链霉素神经基础培养基/10%青霉素/链霉素/10xhepes工序:收获e14幼犬脑并置于冰冷的dpbs(1x)+10%青霉素/链霉素中,然后使用解剖显微镜将其解剖。从每只幼犬中,将一个脑半球置于2ml神经基础培养基/10%p/s/10xhepes中,并将另一个脑半球置于另一个管中。将来自每个管的组织无菌且手动解离成单细胞,加入神经基础的完整培养基并在130g下离心5分钟。然后将组织重新悬浮于具有gf的神经基础的完整培养基中,并且置于100mm×20mm的康宁悬浮培养皿(430591号)中。细胞使用1:3比率传代两次,在此之后将它们离心(130g,5分钟),重悬于冷冻培养基(10%dmso和神经基础完全培养基,无gf)中并在液氮(ln2)中冷冻。融化细胞以用于复合筛选将小瓶从ln2中移除,迅速解冻,并将细胞逐滴转移到15ml锥形瓶中。加入10ml的完全神经基础培养基。将细胞转移至悬浮培养皿中,并且置于培养箱中2小时。在1.5小时处,检查细胞。根据健康状况和数目,估计所需的平板数量,并且将适当量的完全神经基础培养基加温。2小时后,将细胞置于15ml锥形管中并在130g下旋转5分钟。然后将细胞重悬于具有gf的神经基础培养基(每10ml培养基3ul的gf)中。然后使细胞生长过夜,随后在实验中使用。在仅用于神经球计数和直径的96孔板中平板接种细胞corningcostar3474,96孔板,超薄附件细胞的解离和平板接种将3-4ml细胞从倾斜板中取出并添加至15ml锥形物。将剩余培养基中的一些用于冲洗板。将所有剩余的培养基拉出并放入到15ml锥形管中,并且在130g下旋转5分钟。移除所有培养基。将细胞轻轻地重悬于5ml温热的pbs中,再次旋转。然后移除pbs,随后将细胞轻轻地重悬于500μlaccutase(corningtmaccutasetm细胞分离溶液,25058ci号)中。然后用1000μl尖端轻轻吸移细胞以使团块破碎,然后将它们置于摇动水浴中5-10分钟,此后经常用手涡旋它们。培养基如下文所指示来制备,所有培养基具有gf:化合物辛酸对照物/载体低胆碱/载体1%bsa低中等1:5辛酸:癸酸神经酸对照物/载体低胆碱/载体中等胆碱/载体低中等高硬脂酸对照物/载体低胆碱/载体中等胆碱/载体低中等高鞘磷脂对照物/载体低胆碱/载体中等胆碱/载体低中等高对照物和化合物培养基用2号培养基制备并且含有29um胆碱,低(5um)和中等(70um)胆碱培养基用3号培养基制备。化合物公司catcas号原液载体/溶解剂量1剂量2氯化胆碱sigma2697867-48-l7mmpbs5μm70μm使用1000μl尖端轻轻吸移培养基,然后使用200μl尖端以进一步分散细胞。团块不大于约3-5个细胞。将5-10ml的温热培养基(gf)添加到稀释酶。添加2ml的培养基。用1000ul移液管将此吸移,然后用一次性移液管加入3ml。细胞在平板接种前滤过细胞培养批准的40μm过滤器。取出1ml以对细胞进行计数。再次旋转细胞。将培养基从细胞团块中移除,加入1ml的制备培养基(无gf)。用1000ul移液管吸移细胞。在250μl的适当的培养基中制备细胞稀释液(24,000个细胞/孔)。每天涡旋细胞并生长2天。固定和染色1.将细胞固定在罩中。为了固定和随后的免疫组织化学分析,去除100μl培养基并加入100ul4%pfa的1×pbs以固定细胞,同时对神经球进行手动计数,然后用1×pbs洗涤细胞两次,持续5分钟,并且留在1×pbs中,包裹在箔中并在4℃下放置过夜,或进行dapi染色。移除100ulpbs并且在室温下加入100ul抗体(ab)染色溶液(1%山羊血清,1×pbs,和0.1%tritonx)块持续1小时。去除ab染色溶液。然后将细胞用ab染色溶液中的dapi1:5000染色,每孔100μl,然后将细胞在室温下在黑暗中温育15分钟。然后将细胞在ab染色溶液中洗涤2次持续五分钟。使用gecytell成像器或lsm710,zeiss共聚焦显微镜成像,并用imagej软件(美国国立卫生研究院)分析神经球的直径。在用于单层分化或edu掺入测定法的24孔板中平板接种细胞化合物辛酸对照物/载体低胆碱/载体中等胆碱/载体低中等高神经酸对照物/载体低胆碱/载体中等胆碱/载体低中等高硬脂酸对照物/载体低胆碱/载体中等胆碱/载体低中等高鞘磷脂对照物/载体低胆碱/载体中等胆碱/载体低中等高在用于以下测定之前,将24孔玻璃底板(mattekp24g-1.0-13-fcase,玻璃底24孔板)用聚-l-鸟氨酸(sigmap4957)和纤连蛋白(sigmaf1141)涂覆。参见上面的细胞的解离和平板接种。将细胞平板接种(每孔10,000个细胞)在具有gf的完整培养基中持续24小时(每孔500ul)。一旦细胞被连接,它们便被转换为缺乏胆碱的培养基,其它化合物培养基或适当的培养基。分化测定:神经元、神经胶质和npc标记表达的定量在24小时后,确保将细胞连接到板,然后小心地去除培养基。加入500μl的含有2%nu血清(血清替代物)(corningtmnu-血清生长培养基补充剂,cb55004号)、对照物、低胆碱或中等胆碱培养基的化合物培养基。注意:培养基不包含gf。对照物和化合物培养基用2号培养基制备并且含有29um胆碱,低(5um)和中等(70um)胆碱培养基用3号培养基制备。将细胞在加上2%nu血清的培养基中培养9天,每隔2天更换一次培养基。为了固定和随后的免疫组织化学分析,移除培养基,将细胞用1×pbs漂洗一次保持5分钟,并用4%pfa的1×pbs在4℃下固定15分钟。然后用1×pbs洗涤细胞两次持续5分钟,留在1×pbs中,包裹在箔中并在4c下放置过夜,或立即对它们进行初级抗体染色。用于分化的染色去除pbs并加入足够的ab染色溶液(1%山羊血清,1×pbs和0.1%tritonx)以覆盖底部,将块保持在室温下1小时。在合适量的ab染色溶液中制备初级抗体稀释液,每孔250ul(抗体仅在冰上短时间保存,鼠抗map2或tuj11:500(神经元标记),兔抗gfap(神经胶质标记)1:1000,鸡抗巢蛋白cfp(egfp抗体(祖细胞标记))1:1000。去除ab染色溶液,并且将初级抗体的溶液加入到每个室中。将细胞包裹在箔中并保持在4℃下过夜。然后用400ul的ab染色溶液洗涤细胞一次持续5分钟以移除初级抗体。制备次级抗体溶液(对于每个室250ul足够)(山羊抗小鼠alexa4881:2000,抗兔cy3(1:500),抗鸡alexa6471:500,以及1:5000dapi)。将细胞在黑暗中在室温下温育1小时,并在ab染色溶液中洗涤2次持续五分钟。然后将它们保持在4℃下或使用gecytell成像器或lsm710,zeiss共聚焦显微镜成像,并用imagej软件(美国国立卫生研究院)进行分析。微管相关蛋白2(map2),神经元β-微管蛋白iii(tuj1),神经胶质纤维酸性蛋白(gfap)和巢蛋白cfp(egfp抗体)。每个标记表达在收集的图像上进行测量(imagej中的积分密度测量)并且被归一化为dapi荧光,标记所有原子核(积分密度测量)。辛酸用神经元β-微管蛋白iii(tuj1)标记,随后的化合物用微管相关蛋白2(map2)标记。单层培养npc增殖测定(掺入edu-s相标记)在24小时后,确保已将细胞连接到板,然后小心地去除培养基。加入加上gf的500μl的化合物培养基。将细胞在适当培养基中培养3天。对照物和化合物培养基用2号培养基制备并且含有29um胆碱,低(5um)和中等(70um)胆碱培养基用3号培养基制备。使用edualexa555成像试剂盒(lifetechnologies,c10338号)测量edu掺入。在第3天结束时,在固定之前,将edu以10μm添加至每个孔持续30分钟。为了固定和随后的免疫组织化学分析,去除培养基,用1×pbs漂洗细胞一次持续5分钟,并且用1×pbs中的4%pfa在4℃下固定15分钟,然后用1×pbs洗涤细胞两次持续5分钟,留在1×pbs中,包裹在箔中并在4℃下放置过夜,或进行染色。去除pbs并加入足够的ab染色溶液(1%山羊血清,1×pbs和0.1%tritonx)以覆盖底部,将块保持在室温下1小时。针对edu对细胞进行染色。将细胞在黑暗中在室温下温育30分钟。将细胞用1×pbs洗涤并用dapi1:5000ul染色15分钟。用1×pbs洗涤细胞一次,然后在4℃下放在pbs中,或立即使用gecytell成像器(细胞活力应用)或lsm710,zeiss共聚焦显微镜进行成像(使用imagej软件(美国国立卫生研究院)分析)。结果示于表4至表8和图3至图6中。表4-神经酸对神经元细胞密度和星形胶质细胞密度的效应神经元星形胶质细胞对照物0.4361890.642448低na0.4675880.621784中等na0.565630.721512高na0.5394480.70279表5硬脂酸对神经元细胞密度和星形胶质细胞密度的效应神经元星形胶质细胞对照物0.440.64低sa0.540.68中等sa0.660.81高sa0.640.85表6辛酸对神经元细胞密度和星形胶质细胞密度的效应神经元星形胶质细胞对照物1.14.1低oa1.23.7中等oa1.86.1高oa1.77.9表7鞘磷脂对神经球数量的效应鞘磷脂对照物低中等高平均(平均值)10394121219表8鞘磷脂对神经元增殖的效应dapi对照物262低sm280中等sm314高sm305实施例5实验部分样品成分c2:富含α乳白蛋白的乳清蛋白浓缩物(样品管理器id:k2q-00030);包含富含α乳白蛋白的乳清蛋白浓缩物的第一婴儿乳(样品管理器id:k2q-00032);牛乳(全脂乳);人类母乳(在分娩后的第4周后收集的6个单独样品的质量控制池;美国密歇根州圣路易斯的lee生物解决方案公司(leebiosolutions,stlouis,mi,usa))。从乳制品中提取磷脂奶粉:将1g量的均质粉末称量到50ml玻璃烧瓶中,并稀释到20ml的纯蒸馏水中。将溶液在40℃下在水浴中加热30分钟。将体积为500μl的该溶液置于10ml玻璃管中。牛乳和人乳:将500μl量的匀化液体等分至10ml玻璃管。使用9.5ml的氯仿/甲醇(2+1)的混合物,通过uplc-ms/ms(rdls-mp-80138-rev01)一式三份定量人母乳中的mp后提取分析物。简而言之,将管摇动并置于40℃的超声浴中15分钟,然后以2500rpm离心10分钟。将体积为2ml的氯化钾溶液(0.88%,m/m)加入到液相中,然后摇动并以2500rpm离心10分钟。将下层有机相转移至玻璃小瓶中,在温和的n2流下蒸发至干,并且在注入lc-ms之前在500μl的氯仿/甲醇(9+1)中重构。通过联接到质谱的液相色谱法(lc-ms)分析磷脂分析在配备thermoscientificdionexultimate3000快速分离lc系统的qexactive加轨道阱(德国不来梅港市赛默飞世尔科技公司(thermofisherscientific,bremen,germany))上进行。用(a)乙酸铵10mm和(b)乙腈的流动相组合物在hilic柱(100×2.1(i.d.)mm;1.7μm)上进行分离。注射体积设定为10μl,并且梯度在15分钟内从95%b开始到70%b结束,在70%b处保持1分钟,在3分钟内返回到初始条件并平衡6分钟。qexactive加轨道阱配备有以正离子模式运行的大气压化学电离(apci)探针。apci和ms参数如下:电晕放电电流4.0μa,鞘气体和辅助气体分别为24和5个任意单位;毛细管和汽化器温度分别为320℃和390℃,扫气流量为0个任意单位,并且s-透镜rf水平为80。自动增益控制(agc)目标值被设置为1×106个电荷,并且最大注射时间为100ms,分辨率为35’000,并且每个全ms1次微扫描。agc设置为1×106个电荷,并且最大注射时间为250ms,分辨率为17'500,在数据独立分段模式下进行1次微扫描。使用所选母离子的包含列表,其归一化碰撞能量为30%。在曲线模式下在133-2000da的质量范围内采集数据。施加外部质量校准。系统由xcalibur3.0(thermofisherscientific)控制。使用精确质量从总离子色谱图中提取sm物质。母离子对应于磷脂酰胆碱在神经酰胺中的源内损失。基于lipidview数据库和文献,使用包含列表对在母离子上构建的57个sm区域异构体进行特异性断裂,所述母离子对应于神经酰胺与水损失[cer-h2o+h+]的m/z(trenerryv.c.,akbaridoustg.,plozzat.,rochforts.,walesw.j.,auldistm.,ajilounis.ultra-high-performanceliquidchromatography-iontrapmassspectrometrycharacterisationofmilkpolarlipidsfromdairycowsfeddifferentdiets.foodchemistry2013,141,1451-1460(trenerryv.c.、akbaridoustg.、plozzat.、rochforts.、walesw.j.、auldistm.、ajilounis.,来自饲喂不同饲料的奶牛的乳极性脂质的超高效液相色谱-离子阱质谱表征,《食品化学》,2013年,第141卷,第1451-1460页);godzienj.,ciborowskim.,martinez-alcazarm.p.,samczukp.,kretowskia.,barbasc.rapidandreliableidentificationofphospholipidsforuntargetedmetabolomicswithlc-esi-qtof-ms/ms.journalofproteomeresearch2015,14,3204-3216(godzienj.、ciborowskim.、martinez-alcazarm.p.、samczukp.、kretowskia.、barbasc.,用lc-esi-qtof-ms/ms快速而有效的识别无目标代谢组学的磷脂,《蛋白质组学研究杂志》,2015年,第14期,第3204-3216页))。用火焰离子化检测器(gc-fid)通过气相色谱法对脂肪酸甲酯(fame)的分析将sm级分在8.5分钟和10分钟之间收集到玻璃管中,每个样品5次。在n2流下溶剂蒸发后,在mp之后通过气相色谱法对人乳中的脂肪酸的定量进行一式三份的fame分析(rdls-mp-8980-00030-rev01-fame_人乳脂肪,2012年,1.0版本)。结果和讨论亲水性相互作用液相色谱(hilic)用于分离pl类(即,磷脂酰肌醇(pi)、磷脂酰丝氨酸(ps)、磷脂酰乙醇胺(pe)、磷脂酰胆碱(pc)和sm)。基于在轨道阱质谱仪中检测到的假分子离子的准确质量来指定单独sm物质内的碳数量和不饱和度。为了在成分、婴儿配方食品、牛乳和人乳之间进行比较,确定sm物质的相对丰度。不同乳制品中的sm物质在分析样品中检测到45种sm物质(表9)。表9:在成分、婴儿配方食品、牛乳和人乳样品中检测到的sm物质(由x表示)。仅在人乳中检测到的sm物质以粗体表示。sm成分婴儿配方食品牛乳人乳sm成分婴儿配方食品牛乳人乳sm24:1xsm37:1xxxxsm25:0xxxxsm37:0xxxxsm28:1xxxxsm38:4xsm28:0xxxxsm38:3xsm30:2xxxxsm38:2xxxxsm30:1xxxxsm38:1xxxxsm30:0xxxxsm38:0xxxxsm32:3xxxxsm39:1xxxxsm32:2xxxxsm39:0xxxxsm32:1xxxxsm40:2xxxxsm32:0xxxxsm40:1xxxxsm33:1xxxxsm40:0xxxxsm34:3xxxxsm41:2xxsm34:2xxxxsm41:1xxxxsm34:1xxxxsm41:0xxxxsm34:0xxxxsm42:4xsm35:2xxxxsm42:3xxsm35:0xxxxsm42:2xxxxsm36:4xxxxsm42:1xxxxsm36:3xxxxsm42:0xxxxsm36:2xxxxsm44:3xxsm36:1xxxxsm44:1xxxxsm36:0xxxx物质sm24:1、sm38:4、sm38:3和sm42:4在人乳中仅以微量水平发现。sm物质的相对丰度根据峰面积除以每个样品的色谱中对应于sm物质的所有峰面积的总和来估计不同乳制品内sm的相对丰度(%)。图7示出了成分、婴儿配方食品、牛乳和人乳中主要sm物质的相对丰度。成分和婴儿配方食品中存在的sm物质的相对丰度与牛乳相当,并与一些物种(例如,sm32:1、sm32:0、sm33:1、sm34:1、sm38:0、sm39:1、sm39:0和sm41:1)的人乳部分略有不同,在人乳中比在成分、婴儿配方食品和牛乳中更低。而sm36:2、sm36:1、sm36:0、sm37:1、sm38:2、sm38:1、sm40:1、sm42:2和sm42:1与其它乳制品相比在人乳中具有更高的相对丰度。人乳样品包括在出生后4周内或之后收集的6个单独样品的质量控制池。知道人乳中的sm丰度随饮食和哺乳时间的变化而变化,这可部分地解释观察到的差异。然而,尽管一些sm物质的相对丰度存在差异,但在婴儿配方食品和牛乳中也发现了>85%的在人乳中检测到的sm物质。值得注意的是,对于从ms迹线提取的给定m/z,可建议不同的lcbfa组合(例如,sm34:1可对应于smd18:1/16:0、d18:0/16:1、d16:1/18:0等)。因此,我们评估了gcfa曲线,以收集关于不同乳制品之间sm分子结构的更多信息。来自不同乳制品的sm级分中的脂肪酸分布型通过首先将sm分馏,然后通过gc-fid分析级分中存在的fa来研究sm的区域异构体结构。如上所述进行sm的分馏以用于lc-ms分析,但是在这种情况下,将流出物导入5ml玻璃管而不是ms。然后在随后的gc分析之前使每个级分经受甲基化工序。在sm级分内的fa的相对丰度在图8中示出。如图8所示,sm级分主要含有饱和fa(即,肉豆蔻酸14:0、十五酸15:0、棕榈酸16:0、硬脂酸18:0、花生酸20:0、二十二酸22:0、二十三酸23:0和二十四酸24:0)。在来自所有乳制品的sm级分中观察到更高比例的sfa(表10)。这与文献一致,揭示了在sm级分中碳链高于18的sfa的高分布。这种高量的sfa反映了sm的结构作用,即降低了乳脂肪球膜的流动性并保持了刚性。表10:在来自不同乳制品的sm级分中检测到的sfa、mufa和pufa的百分比。单不饱和fa(mufa)在sm级分中占fa的约4%-11%。油酸18:1n-9和神经酸24:1n-9是检测到的2个mufa。有趣的是,与其它乳制品相比,在人乳中发现24:1n-9具有相对较高比例,并且这与文献一致。与其它产品相比,在测试的婴儿配方食品和人乳中发现仅有的pufa亚油酸18:2n-6相对较高。最后,在sm级分中未检测到ω-3pufa。这也符合见于文献中的数据,示出花生四烯酸(aa,20:4n-6)、二十碳五烯酸(epa,20:5n-3)和二十二碳六烯酸(dha,22:6n-3)主要存在于pe、pi和ps中。实施例5在群研究中报告的用于婴儿喂养的两种主配方食品为婴儿配方食品#3和婴儿配方食品#6。和#6相比,婴儿配方食品#3和婴儿生命中前5年期间增加的整体髓鞘发育相关联。比较2种配方食品(图9、图10、图11)。经由我们的纵向混合效应方法计算出的轨线示出,gompertz生长曲线参数在所调查的每个脑区域中不同。在表12中提供了婴儿配方食品#5和#6的髓鞘相关的营养物质的特定营养物质分析。实施例6在群研究中报告的用于婴儿喂养的两种主配方食品为婴儿配方食品#3和婴儿配方食品#6。和#6相比,婴儿配方食品#3和婴儿生命中前5年期间增加的整体髓鞘发育相关联。比较2种配方食品(图9、图10、图11)。经由我们的纵向混合效应方法计算出的轨线示出,gompertz生长曲线参数在所调查的每个脑区域中不同。在表12中提供了婴儿配方食品#5和#6的髓鞘相关的营养物质的特定营养物质分析。表12-6种婴儿配方食品中髓鞘相关的营养物质的营养物质分析。实施例7神经元与ol的共培养如先前由charles等人(2000年)所述来培养神经元/少突细胞。将妊娠17天的怀孕雌性大鼠通过颈脱位法(wistar大鼠)处死并从子宫中取出胎儿。将前脑取出,并且置于含有2%的青霉素-链霉素(ps)和1%的牛血清白蛋白(bsa)的leibovitz冰冷培养基(l15)中。通过在37℃下胰蛋白酶酶化20分钟(胰蛋白酶edta1x)解离前脑。通过加入含有ii级dna酶i(0.1mg/ml)和10%胎牛血清(fcs)的dulbecco改性eagle培养基(dmem)来终止反应。然后通过10ml吸管吸入挤出3次将细胞机械解离。然后将细胞在4℃下以180×g在l15培养基中的一层bsa(3.5%)上离心10分钟。弃去上清液,并且将沉淀细胞重悬于含有10%的fcs的dmem中。然后将细胞在4℃下以515×g离心10分钟。弃去上清液,并将团块的细胞重悬于包含补充有2%b27、2mml-谷氨酰胺(lglu)、2%ps溶液、1%fcs和10ng/ml血小板衍生生长因子(pdgf-aa)的神经基础组成的培养基中。使用台盼蓝排除测试在neubauer血细胞计数器中对活细胞进行计数。将细胞以20000个细胞/孔的密度接种在用聚-l-赖氨酸和层粘连蛋白预涂覆的96孔板中。接种后一天(培养第1天),将细胞与测试化合物(选自表13中列出的那些)或雌二醇一起温育。对照细胞不与测试化合物或雌二醇一起温育。使用雌二醇作为阳性对照物。已知雌二醇诱导opc增殖。雌二醇对ol分化的积极效应也已被证实,因为其对早期髓鞘形成过程有影响。还公布了雌二醇对神经突生长的积极效应(参见alevaro等人,2010年来查看)。在加湿的培养箱中,将板在37℃下保持在空气(95%)-co2(5%)的气氛中。每隔一天用新鲜培养基和测试化合物或对照化合物替换一半培养基。测试化合物或对照化合物在实验持续时间内保持在限定浓度。在1个培养物上测试化合物(每个条件6个孔)。然后在培养的第12、18或30天使用细胞来测量opc增殖,opc到ol的分化和早期髓鞘形成过程(髓鞘包裹),或ol的成熟(髓鞘成熟)和成熟髓鞘形成过程(髓鞘包裹)之一。opc的增殖-a2b5阳性细胞和总轴突长度(nf)的测量在培养的第12天,将细胞用无水乙醇(95%)和纯乙酸(5%)的冷混合物固定5分钟。然后使细胞透化,并用含有0.1%的皂苷和1%fcs的磷酸盐缓冲盐水(pbs)的溶液在室温下封闭非特异性位点15分钟。然后将细胞与在小鼠中产生的单克隆抗-a2b5缀合alexa488在含有1%fcs、0.1%皂苷的pbs中的1/200稀释液处在室温下温育2小时,并且与在兔中产生的抗nf(磷酸化和非磷酸化的神经丝200)在含有1%fcs、0.1%皂苷的pbs中的1/500稀释液处在室温下温育2小时。用alexafluor568山羊抗兔在具有1%fcs、0.1%皂苷的pbs中的1/400稀释液处在室温下显示该抗体1小时。量化opc的总数(a2b5阳性细胞的数量)(以评估增殖),测量轴突网络(总轴突长度(nf))以评估化合物对神经元网络的效应(髓鞘形成的质量与轴突网络的质量直接相关)。opc到ol的分化和髓鞘形成过程(髓鞘包裹)-mag阳性细胞的数量和面积、重叠mag/nf包裹、以及总轴突长度(nf)的测量在培养的第18天,将细胞用无水乙醇(95%)和纯乙酸(5%)的冷混合物固定5分钟。然后使细胞透化,并用含有0.1%的皂苷和1%fcs的磷酸盐缓冲盐水(pbs)的溶液在室温下封闭非特异性位点15分钟。然后将细胞与在小鼠中产生的单克隆抗-mag在含有1%fcs、0.1%皂苷的pbs中的1/400稀释液处,并且与在兔中产生的抗nf(磷酸化和非磷酸化的神经丝200)在含有1%fcs、0.1%皂苷的pbs中的1/500稀释液处在室温下温育2小时。用cf488a山羊抗-小鼠在具有1%fcs、0.1%皂苷的pbs中的1/800稀释液处,并且用alexafluor568山羊抗-兔在具有1%fcs、0.1%皂苷的pbs中的1/800稀释液处在室温下显示这些抗体1小时。量化ol的总数(mag阳性细胞的数量和面积)(以评估分化过程),以及围绕轴突对opc的包裹(重叠mag/nf包裹)(髓鞘形成过程)。测量轴突网络(总轴突长度(nf))以评估化合物对神经元网络的效应。ol的成熟(髓鞘成熟)-mbp阳性细胞的数量和面积、重叠mbp/nf包裹、以及总轴突长度(nf)的测量在培养的第30天,将细胞用无水乙醇(95%)和纯乙酸(5%)的冷混合物固定5分钟。然后使细胞透化,并用含有0.1%的皂苷和1%fcs的磷酸盐缓冲盐水(pbs)的溶液在室温下封闭非特异性位点15分钟。然后将细胞与在小鼠中产生的单克隆抗-mbp在含有1%fcs、0.1%皂苷的pbs中的1/1000稀释液处,并且与在兔中产生的抗nf(磷酸化和非磷酸化的神经丝200)在含有1%fcs、0.1%皂苷的pbs中的1/500稀释液处在室温下温育2小时。用cf488a山羊抗小鼠在具有1%fcs、0.1%皂苷的pbs中的1/800稀释液处,并且用alexafluor568山羊抗兔在具有1%fcs、0.1%皂苷的pbs中的1/400稀释液处在室温下显示这些抗体1小时。评估ol的总数(mbp阳性细胞的数量和面积)(以评估ol成熟)以及围绕轴突对髓鞘的包裹(重叠mbp/nf(包裹))。测量轴突网络(总轴突长度(nf))以评估化合物对神经元网络的效应。对于所有测量,完成一次培养(每个条件6个孔)。对于每个测试条件,每个孔采集30张图片(每张图片代表一个场),并且使用配备有led灯(激发360/480/565和发射460/535/620)的imagexpress(分子装置)以20倍放大率进行分析。30张图片为自动拍摄,并且占培养孔的总表面的80%。结果按照神经突网络的累计平均长度(以μm计)表示,或每个场针对给定标记(mag或mbp)来标记髓鞘。测量nf与mag或mbp之间的重叠面积以评估包裹。为了评估opc群体、mag阳性细胞群体、mbp阳性细胞群体,完成每个图片(=场)的阳性细胞的数量的自动计数。结果以每个场的阳性细胞的平均数表示。所有图像都在相同条件下拍摄。表13结果示于图12至图32中实施例8材料和方法1.喂料层制备:新生儿皮质的解离以及混合神经胶质培养物的保持将新鲜解剖的脑加入37℃水浴中保持3分钟,然后通过p1000移液管尖端切割皮质以产生较小的片段。每个脑中加入75μl的opc木瓜蛋白酶溶液,然后将组织在37℃水浴中温育20分钟。然后向组织悬浮液中加入混合的神经胶质培养物以使opc木瓜蛋白酶溶液失活。随后使用无菌火焰抛光玻璃巴斯德移液管磨碎组织,然后每个脑加入4ml的混合的神经胶质培养基。将细胞以1200rpm(约300g)离心5分钟,然后将细胞重悬于温热混合的神经胶质培养基中并平板接种到pll涂覆的烧瓶中。接种后4小时,进行完全培养基更换以便去除由磨碎产生的大部分碎片,并促进培养活力。培养3天后,进行2/3培养基更换,并且不进行随后的培养基更换。然后将细胞保持在培养物中直至融合。2.海马神经元制备从spraguedawley大鼠的胚胎(e18)幼仔中分离海马神经元。简而言之,在动物处死后,分离脑,从脑半球的内侧移除脑膜,然后解剖出海马体并保持在4℃下直至过程完成。然后将组织与2.5%胰蛋白酶在37℃水浴中温育15分钟,然后轻轻洗涤并保存在培养基中。通过用功能化的无菌巴斯德移液管反复吸移海马体来进行海马体解离。机械解离后,将细胞以期望的密度接种在神经元平板接种培养基中,使其恢复4小时,然后置于竞争性神经元培养基中。3.从混合的神经胶质培养物纯化opc以建立ol/海马神经元共培养物在混合的神经胶质培养的第9天,将烧瓶在5%co2组织培养物培养箱中的轨道摇动器上以50rpm摇动45分钟。这种摇动的目的是从单层去除任何松散粘附的污染细胞。然后更换培养基,并用补充有5μg/ml胰岛素的4ml的新鲜混合的神经胶质培养基代替。然后将烧瓶重新置于摇动器上,平衡约3小时,然后以220rpm摇动约16小时(过夜)。第二天早晨,收集含有小神经胶质细胞和opc细胞的混合神经胶质培养基,并将其预平板接种在p100培养皿中(未经培养处理)30分钟以便纯化opc细胞;小神经胶质细胞立即开始粘附于培养皿,而opc细胞仍留在上清液培养基中。在预平板接种30分钟后,收集培养基,并且对ol进行计数并接种于1mlol培养基的最终体积中的海马神经元上。进行完全ol培养基(负cntf)更换,然后将细胞保持在培养物中直到适当的实验时间。对于成熟实验,实验工序如下:a.opc在10div的星形胶质细胞的喂料层上的生长b.opc的分离(第0天)c.化合物的施用(第3天)d.在第4天、第7天和第10天对成熟的定量评价。对于髓鞘形成实验,实验工序如下:a.海马神经元的生长,直到完全神经元网络成熟(14div)b.opc在10div的星形胶质细胞的喂料层上的伴随生长c.opc的分离以及与神经元的共培养(第14天)d.化合物的施用(第15天)e.在共培养的第15天、第18天、第21/23天和第28/29天(共培养平板接种后1天,在化合物处理前)对髓鞘形成的定量评价4.图像的获取将不同实验时间点处的所有培养物在室温(rt)下固定在4%多聚甲醛和4%蔗糖中10分钟。将初级抗体和次级抗体在室温下施加在gdb缓冲液(30mm磷酸盐缓冲液,ph7.4,含有0.2%明胶、0.5%tritonx-100和0.8mnacl)持续2小时。用适当的标记对细胞进行染色(使用的初级抗体:抗-a2b5抗体(abcamcat.ab53521)、大鼠抗mbp(bio-radcat.aa82-87)、少突细胞标记o4抗体(r&dsystemscat.mab1326)、抗βiii微管蛋白mab(promegacat.g7121);使用的二抗:alexa抗大鼠555(lifetecha-21434)、alexa抗小鼠488(lifetecha-11009))。免疫细胞化学染色后,所有图像用arrayscanxti(thermoscientific)获得;在2×2的仓中目标被放大20倍。对于每个条件和复制副本(一式三份),最少拍摄15个图像。为了分析所有获取的图像,使用hcsstudio细胞分析软件,特别是“扫描”应用程序。opc木瓜蛋白酶溶液(在mem中制成)木瓜蛋白酶溶液1.54mg/mll-半胱氨酸360μg/mldna酶i60μg/ml混合的神经胶质培养基(在dmem中制成)fbs10%青霉素/链霉素(0.33%,来自原液)33单位/ml青霉素和33μg/ml链霉素glutamax1%ol培养基dmem100xol-补充剂牛胰岛素(来自1mg/ml原液)glutamax人全转铁蛋白(来自33mg/ml原液)b27补充剂fbscntf(来自50ng/μl原液)结果示于图34至图53中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1