产生具有增强的Fc受体结合的经有序多聚化的免疫球蛋白Fc组合物的人蛋白片段的融合蛋白的制作方法
本申请要求2016年7月22日提交的美国临时申请第62/365,921号和2016年7月22日提交的美国临时申请第62/365,919号的优先权,其内容通过引用整体并入本文。
以电子形式提交的文本文件的描述
与本文一起以电子形式提交的文本文件的内容通过引用整体并入本文:序列表的计算机可读格式副本(文件名:glik_019_01wo_seqlist_st25.txt,记录日期:2017年7月24日,文件大小:68千字节)。
本发明一般涉及免疫学、自身免疫、炎症和肿瘤免疫学领域。更具体地,本发明涉及包括天然连接的免疫球蛋白fc结构域的生物活性仿生分子(其表现出改变的fc受体结合和增强的与补体系统的元素的结合)、包括这种仿生物质的组合物以及制备和使用这种仿生物质的方法。本发明进一步涉及治疗或预防病理病状,例如补体介导的疾病、自身免疫性疾病、炎性疾病、血液病症和癌症。
背景技术:
自20世纪50年代早期以来,人血浆中的免疫球蛋白产品已经被用于治疗免疫缺陷病症,并且最近被用于自身免疫性和炎性疾病。人ivig(hivig)是由混合人血浆制备的无菌、纯化的免疫球蛋白g(igg)产品的制剂,其通常含有超过90%的未修饰的igg,仅有少量和可变量的多聚免疫球蛋白,iga或igm(rutter等人,《美国皮肤病学会杂志(jamacaddermatol)》,2001年,6月;44(6):1010-1024)。ivig最初用作igg替代疗法以预防低igg水平患者的机会性感染(baerenwaldt,《临床免疫学专家评论(expertrevclinimmunol)》,6(3),p425-434,2010)。然而,今天hivig最常见的用途是治疗慢性炎性脱髓鞘性多发性神经病,并且它还被许可用于治疗特发性血小板减少性紫癜(itp)、格林-巴利综合症和川崎病。
混合人ivig源自数万名献血者,含有非常小且可变部分(0.1-5%)的igg1聚集体,其模拟了天然igg1可溶性聚集体的天然作用,尽管hivig是一种有效的临床治疗,但仍存在一些缺点,包含无菌性不足的可能性、杂质或传染原(包含病毒和朊病毒)的存在、本混合人血液产品的缺乏、批次差异、费用高、可能影响肾功能的大蛋白质负荷(1-2g/kg)和长施用时间长(4-8小时,有时会分散在多天)。此外,多批hivig之间的iga含量可能存在差异,并且可能在iga缺乏接受者中引起过敏和过敏性反应。另外,由于每位患者需使用大量hivig以及对人类献血者的依赖,hivig的制造昂贵且供应有限。
天然免疫球蛋白igg1fc结合十多种配体,天然的配体包含c1q、经典fc受体、新生儿受体fcrn、铁、蛋白质a、fcrl1-6、trim21和dc-sign。免疫球蛋白(ig)与这些配体的相互作用通过ig的fc结构域介导。已经主要在单个单克隆抗体背景下描述了igg1的fc结构域中的各种点突变,其导致改变的与经典iggfc受体(fcγr;fcγri、fcγriia、fcγriib和fcγriii)的结合、改变的与补体蛋白的结合和改变的效应子功能(例如,抗体依赖性、细胞介导的细胞毒性(adcc)、吞噬作用(adcp)或补体依赖性细胞毒性(cdc))。
在临床上,有数据表明hivig的少数多聚级分在治疗由病理免疫复合物介导的某些疾病方面不成比例地有效,并且已经观察到痕量(<1-5%)igg以聚集形式存在于ivig中,而igg二聚体可以占hivig的5-15%。据认为,由于亲合力增加,此小比例的多聚igg在与iggfc受体(fcγr)结合的方面超过了病理性免疫复合物。因此,考虑到在亲和力与亲和性相互作用之间呈现的复杂性,目前尚不清楚文献中描述的点突变(其中许多改变给定单克隆抗体的亲和力)将如何影响由多聚fc构成的分子与fcγr或补体蛋白结合的能力。多聚或聚集fc向靶配体(包含但不限于fcγr和补体c1q)呈递多价fc,导致通过未聚集免疫球蛋白或单克隆抗体未见的亲和结合。
技术实现要素:
本发明涉及包括斯托拉多体(stradomer)单元的生物活性仿生分子,其中斯托拉多体单元的fc结构域包括一个或多个点突变和多聚化结构域。如本文所述,先前描述的用于修饰抗体功能(例如,减少或消除单克隆抗体中的经典fcγr结合)的突变在多聚化斯托拉多体背景下不具有相同的作用。在多聚化斯托拉多体背景下的此些突变的作用是完全不可预测的。在一个方面,本文所述的仿生分子具有保持或增强的与补体c1q的结合和/或保持或增强的与经典fcγr的结合。提供了包括生物活性融合蛋白仿生物的组合物及其使用方法。
在一些实施例中,本发明提供了一种斯托拉多体单元,其包括:至少一个同源二聚igg1fc结构域,其包括对应于所述fc结构域的第236、267、268、324和/或299位中的至少一个的一个或多个点突变;和至少一个多聚化结构域。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的第236位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变g236r。在一些实施例中,所述斯托拉多体单元进一步包括所述fc结构域的第233位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、g236e、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、g236d、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、s267q、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、s267g、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、s267k、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、s267d、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、g236d、s267q、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、g236q、s267d、h268f和s324t。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、g236d、s267d、h268f和s324t。
在一些实施例中,本发明提供了一种斯托拉多体单元,其包括所述fc结构域的第267、268、324和299位处的点突变,其中第299位处的所述点突变是除t299s或t299c之外的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变s267q、h268f、s324t和t299a。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变s267d、h268f、s324t和t299a。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变s267h、h268f、s324t和t299a。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变s267e、h268f、s324t和t299a。
在一些实施例中,所述斯托拉多体单元进一步包括所述fc结构域的第328位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变s267e、h268f、s324t和l328f。
在一些实施例中,所述斯托拉多体单元进一步包括所述fc结构域的第234和235位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变l234a、l235a、s267e、h268f和s324t。
在一些实施例中,所述斯托拉多体单元进一步包括所述fc结构域的第233、234、235位处的点突变和第236位处的缺失。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变e233p、l234v、l235a、s267e、h268f、s324t和第236位处的缺失。
在一些实施例中,所述斯托拉多体单元包括所述fc结构域的第299位处的点突变,其中第299位处的所述点突变是除t229s或t299c之外的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变t299a。
在一些实施例中,所述斯托拉多体单元进一步包括所述fc结构域的第430位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述点突变t299a和e430g。
在一些实施例中,本发明提供了斯托拉多体单元,其包括:至少一个同源二聚igg1fc结构域,其包括所述igg1fc结构域的第299位处的点突变,和第430、440和/或345位的一个或多个另外的点突变;和位于所述至少一个同源二聚igg1fc结构域的c末端的igg2铰链多聚化结构域,其中所述斯托拉多体单元多聚化成经多聚化的斯托拉多体,其包括与其它普通斯托拉多体或亲本斯托拉多体(“六聚斯托拉多体)相比更高百分比的包括6个同源二聚单元的斯托拉多体。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的第299、345、430和440位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变t299a、e345r、e430g和s440y。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的第299、430和440位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述点突变t299a、e430g和s440y。
在一些实施例中,本文所述的斯托拉多体单元包括所述fc结构域的第299和345位处的点突变。在一些实施例中,所述斯托拉多体单元包括所述fc结构域的所述所述点突变t299a和e345r。在一些实施例中,所述斯托拉多体单元包括fc结构域的所述点突变t299a。
在一些实施例中,本文所述的斯托拉多体单元包括所述fc结构域的第297、298或299位处的突变,并且结合c1q,抑制cdc,并保持与fcγri、fcγriia、fcγriib和/或fcγriii的结合。在一些实施例中,本文所述的斯托拉多体单元包括所述igg1fc结构域的第299位处的点突变和第430、440和/或345位处的一个或多个另外的点突变,并且相对于不包括第299、345、430和/或440位中的一个或多个处的点突变的相同结构的同源二聚斯托拉多体单元表现出增强的与补体蛋白的结合。在一些实施例中,所述补体蛋白是c1q。在。在一些实施例中,本文所述的斯托拉多体单元抑制补体依赖性细胞毒性(cdc)。在一些实施例中,本文所述的斯托拉多体单元包括第299、345、430和/或440位中的一个或多个处的点突变,并且相对于不包括第299、345、430和/或440位中的一个或多个处的点突变的相同结构的同源二聚斯托拉多体单元表现出保持或增强的与fcγri、fcγrii和/或fcγriii的结合。在一些实施例中,本文所述的斯托拉多体单元包括第236、267、268、324和/或299位中的一个或多个处的点突变,并且相对于不包括第236、267、268、324和/或299位中的一个或多个处的点突变的相同结构的斯托拉多体表现出增强或保持的与fcγri、fcγrii和/或fcγriii的结合。
在一些实施例中,本文所述的斯托拉多体单元包括igg1的eem或del多形性。在一些实施例中,本文所述的斯托拉多体单元包括多聚化结构域,其选自由以下组成的组:igg2铰链、异亮氨酸拉链和gpp结构域。在一些实施例中,多聚化结构域产生所述斯托拉多体单元的多聚体。在一些实施例中,所述斯托拉多体单元的所述多聚体是高阶多聚体。在一些实施例中,所述斯托拉多体单元的所述多聚体包括十二个同源二聚斯托拉多体单元。在一些实施例中,所述斯托拉多体单元的所述多聚体包括十八个同源二聚斯托拉多体单元。在一些实施例中,本文所述的斯托拉多体单元表现出增强的与低亲和力fcγ受体的结合。
在一些实施例中,本文所述的斯托拉多体单元从氨基末端到羧基末端包括前导序列;包括igg1铰链、igg1ch2和igg1ch3的fc结构域;和igg2铰链。在此些实施例中,所述斯托拉多体单元可以包括氨基酸序列,其选自由以下组成的组:seqidno:7-26和seqidno:28-29。在一些实施例中,所述斯托拉多体单元包括氨基酸序列,其选自由以下组成的组:seqidno:30-32。在一些实施例中,本文所述的斯托拉多体单元从氨基末端到羧基末端包括前导序列、igg2铰链、igg1铰链和包括igg1ch2和igg1ch3的fc结构域。在此些实施例中,所述斯托拉多体单元可以包括根据seqidno:27的氨基酸序列。
在一些实施例中,本发明提供了一种包括两个或更多个本文所述的斯托拉多体单元的簇状斯托拉多体。在一些实施例中,本发明提供了包括本文所述的簇状斯托拉多体的组合物。在一些实施例中,所述组合物是富集的异质组合物,其包括高分子量物种多聚体,其包括本文所述的经多聚化的同源二聚体。在一些实施例中,高分子量多聚体包括六聚体条带及以上的多聚体。在一些实施例中,所述高分子量多聚体包括12聚体条带及以上的多聚体。在一些实施例中,所述高分子量多聚体包括18聚体条带及以上的多聚体。在一些实施例中,相对于先前描述的包含gl-2045的多聚化斯托拉多体,所述高分子量多聚体包括增加百分比的六聚体。在一些实施例中,相对于先前描述的多聚化斯托拉多体,所述高分子量多聚体包括增加百分比的六聚体、十二聚体和十八聚体。
在一些实施例中,本发明提供了一种治疗或预防补体介导的疾病、抗体介导的疾病、自身免疫性疾病、炎性疾病、过敏或血液病症的方法,所述方法包括向有需要的受试者施用本文所述的斯托拉多体或其组合物。在一些实施例中,所述抗体介导的疾病选自由以下组成的组:肺出血-肾炎综合症;实体器官移植排斥;抗体介导的同种异体移植物排斥;黄斑变性;冷凝集素病;溶血性贫血;视神经脊髓炎;神经性肌强直;边缘性脑炎;莫旺综合症;重症肌无力;兰伯特伊顿肌无力综合症;自主神经病;阿尔茨海默氏病;动脉粥样硬化;帕金森病;僵人综合症或过度惊骇;反复自然流产;休斯综合症;系统性红斑狼疮;自身免疫性小脑性共济失调;结缔组织病,包含硬皮病、干燥综合症;多肌炎;类风湿性关节炎;结节性多动脉炎;crest综合症;心内膜炎;桥本氏甲状腺炎;混合性结缔组织病;通道病;与链球菌感染相关的小儿自身免疫性神经精神疾病(pandas);与抗n-甲基-d-天门冬氨酸受体抗体相关的临床病状,特别是nr1、接触素相关蛋白2、ampar、glur1/glur2、谷氨酸脱羧酶、glyrα1a、乙酰胆碱受体、vgccp/q型、vgkc、musk、gaba(b)r;水通道蛋白-4;和天疱疮。在一些实施例中,所述自身免疫性疾病是类风湿性关节炎。在一些实施例中,所述自身免疫性疾病是自身免疫相关的视力损失或听力损失。在一些实施例中,所述补体介导的疾病选自由以下组成的组:重症肌无力、溶血性尿毒症综合症(hus)、非典型溶血性尿毒症综合症(ahus)、阵发性睡眠性血红蛋白尿症(pnh)、膜性肾病、视神经脊髓炎、抗体介导的同种异体移植物排斥、狼疮性肾炎和膜增生性肾小球肾炎(mpgn)。在一些实施例中,所述血液病症是镰状细胞病。
在一些实施例中,所述斯托拉多体静脉内、皮下、口服、腹膜内、舌下、口腔、经真皮、通过真皮下植入或肌肉内施用。
在一些实施例中,本发明提供了一种治疗或预防与补体介导的疾病、抗体介导的疾病、自身免疫性疾病、炎性疾病、过敏或血液病症相关的疼痛或由其引起的疼痛的方法,所述方法包括向有需要的受试者施用本文所述的六聚斯托拉多体或其组合物。在一些实施例中,所述抗体介导的疾病选自由以下组成的组:肺出血-肾炎综合症;实体器官移植排斥;视神经脊髓炎;神经性肌强直;边缘性脑炎;莫旺综合症;重症肌无力;兰伯特伊顿肌无力综合症;自主神经病;阿尔茨海默氏病;动脉粥样硬化;帕金森病;僵人综合症或过度惊骇;反复自然流产;休斯综合症;系统性红斑狼疮;自身免疫性小脑性共济失调;结缔组织病,包含硬皮病、干燥综合症;多肌炎;类风湿性关节炎;结节性多动脉炎;crest综合症;心内膜炎;桥本氏甲状腺炎;混合性结缔组织病;通道病;与链球菌感染相关的小儿自身免疫性神经精神疾病(pandas);与抗n-甲基-d-天门冬氨酸受体抗体相关的临床病状,特别是nr1、接触素相关蛋白2、ampar、glur1/glur2、谷氨酸脱羧酶、glyrα1a、乙酰胆碱受体、vgccp/q型、vgkc、musk、gaba(b)r;水通道蛋白-4;和天疱疮。在一些实施例中,所述自身免疫性疾病是类风湿性关节炎或自身免疫相关的视力损失或听力损失。在一些实施例中,所述补体介导的疾病选自由以下组成的组:重症肌无力、溶血性尿毒症综合症(hus)、非典型溶血性尿毒症综合症(ahus)、阵发性睡眠性血红蛋白尿症(pnh)、膜性肾病、视神经脊髓炎、抗体介导的同种异体移植物排斥、狼疮性肾炎和膜增生性肾小球肾炎(mpgn)。在一些实施例中,所述血液病症是镰状细胞病。
在一些实施例中,所述斯托拉多体静脉内、皮下、口服、腹膜内、舌下、口腔、经真皮、通过真皮下植入或肌肉内施用。
附图说明
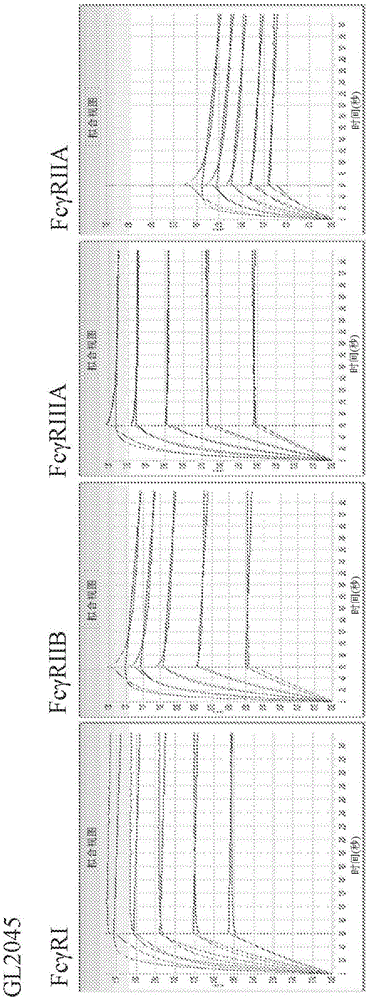
图1示出了通过生物层干涉测量法(fortebiooctet)测量的斯托拉多体gl-2045与fcγri、fcγriib、fcγriiia、fcγriia或fcrn的结合。
图2a提供了gl-2045和g990的每种fc受体的rumax、c1qelisa和cdc抑制数据的雷达图。图2b提供了gl-2045和g990的每种fc受体在300秒时的ru(ru300s)的雷达图。
图3a提供了gl-2045和普通斯托拉多体g1032的每种fc受体的rumax、c1qelisa和cdc抑制数据的雷达图。图3b提供了gl-2045和普通斯托拉多体g1032的每种fc受体在300秒时的ru(ru300s)的雷达图。
图4a提供了gl-2045和普通斯托拉多体g1023的每种fc受体的rumax、c1qelisa和cdc抑制数据的雷达图。图4b提供了gl-2045和普通斯托拉多体g1023的每种fc受体在300秒时的ru(ru300s)的雷达图。
图5a提供了gl-2045和普通斯托拉多体g1049的每种fc受体的rumax、c1qelisa和cdc抑制数据的雷达图。图5b提供了gl-2045和普通斯托拉多体g1049的每种fc受体在300秒时的ru(ru300s)的雷达图。
图6示出了通过生物层干涉测量法测量的斯托拉多体g1049与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图7示出了通过生物层干涉测量法测量的斯托拉多体g990与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图8示出了通过生物层干涉测量法测量的斯托拉多体g1103与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图9示出了通过生物层干涉测量法测量的斯托拉多体g1104与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图10示出了通过生物层干涉测量法测量的斯托拉多体g1102与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图11示出了通过生物层干涉测量法测量的斯托拉多体g1101与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图12示出了通过生物层干涉测量法测量的斯托拉多体g1109与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图13示出了通过生物层干涉测量法测量的斯托拉多体g1111与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图14示出了通过生物层干涉测量法测量的斯托拉多体g1114与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图15示出了通过生物层干涉测量法测量的斯托拉多体g1117与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图16示出了通过生物层干涉测量法测量的斯托拉多体g1125与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图17示出了通过生物层干涉测量法测量的斯托拉多体g1094与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图18示出了通过生物层干涉测量法测量的斯托拉多体g1092与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图19示出了通过生物层干涉测量法测量的斯托拉多体g1107与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图20示出了通过生物层干涉测量法测量的斯托拉多体g1068与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图21示出了通过生物层干涉测量法测量的斯托拉多体g1099与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图22示出了通过生物层干涉测量法测量的斯托拉多体g1097与fcγri、fcγriib、fcγriiia或fcγriia的结合。
图23示出了通过生物层干涉测量法(fortebiooctet)测量的斯托拉多体g1098与fcγri、fcγriib、fcγriia或fcγriia的结合。
图24示出了通过生物层干涉测量法(fortebiooctet)测量的斯托拉多体g1126与fcγri、fcγriib、fcγriia或fcγriia的结合。
图25示出了通过生物层干涉测量法(fortebiooctet)测量的斯托拉多体g1127与fcγri、fcγriib、fcγriia或fcγriia的结合。
图26a到图26f是凝胶,示出了相同的gl-2045和测试的衍生斯托拉多体化合物所基于的亲本化合物(g994或g998)、衍生斯托拉多体化合物形成多聚体。化合物gl-2045、g994、1103和1104示出在图26a中。化合物gl-2045、g994、g1102、g1101、g1125和g1109示出在图26b中。化合物gl-2045、g998、g1111、g1114和g1117示出在图26c中。化合物gl-2045、g998、g1068、g1094和g1092示出在图26d中。化合物gl-2045、g998和g1107示出在图26e中。化合物gl-2045、g1099和g1097示出在图26f中。
图27提供了gl-2045、g1099、g1097、g1098、g1126和g1127的非还原凝胶运行的图像。
图28示出了通过elisa测量的普通斯托拉多体的c1q结合。
图29示出了通过elisa测量的普通斯托拉多体g1102、g1114和g1069的c1q结合。
图30示出了普通斯托拉多体化合物g1097和g1099的cdc抑制测定。cdc+6%表示补体和cd20抗体的加入。阳性对照是细胞+cdc+6%(细胞,血清补体和抗体),阴性对照是细胞+6%(细胞,血清补体,无抗体)。
图31示出了普通斯托拉多体化合物(g1097和g1099)和六聚普通斯托拉多体化合物(g1098、g1126和g1127)的cdc抑制测定。cdc+6%表示补体和cd20抗体的加入。阳性对照是细胞+cdc+6%(细胞,血清补体和抗体),阴性对照是细胞+6%(细胞,血清补体,无抗体)。
图32a和图32b示出了使用可在www.cbs.dtu.dk/services/netnglyc/在线获取的netnglyc服务器基于计算机预测模型的亲本斯托拉多体、g2045(图32a)和亲本斯托拉多体的无糖基化变体(t299a点突变,图32b)的预测糖基化位点。netnglyc服务器使用检查asn-xaa-ser/thr序列背景下的序列的人工神经网络预测人类蛋白质中的n-糖基化位点。
具体实施方式
本文所述的免疫调节化合物的合理分子设计方法包含免疫活性仿生物质的重组和/或生物化学产生,其表现出保持或增强的与补体蛋白和/或fcγr(包含fcγri、fcγriia、fcγriib和/或fcγriii)的结合。本文提供的组合物可用于治疗例如补体介导的疾病、抗体介导的疾病、自身免疫性疾病、炎性疾病、过敏或血液病症。
如本文使用,当在权利要求书和/或说明书中与术语“包括”结合使用时,词语“一个(a/an)”的使用可以表示“一个(one)”,但是它也符合“一个或多个”、“至少一个”和“一个或多于一个”的含义。
如本文使用,术语“补体”是指补体级联的任何小蛋白质,在文献中有时被称为补体系统或补体级联。如本文使用,术语“补体结合”或“与补体结合”是指补体级联的任何组分的结合。补体级联的组分是本领域已知的,并且描述于例如《詹韦氏免疫生物学(janeway’simmunobiology)》,第8版,murphy编辑,garlandscience出版社,2012。目前已知有三种主要的补体途径:经典途径、可替代途径和凝集素结合途径。一旦蛋白质c1q与完整免疫球蛋白igm的一个或多个分子或完整免疫球蛋白igg1、igg2或igg3的至少两个分子结合,经典补体途径就被激活,之后形成c1qc1rc1并切割c4。不同的补体激活途径通过经典c3转化酶(c4bc2a)或可替代c3转化酶(c3bbb)的作用收敛于c3b的生成。c3b本身是可替代c3转化酶以及经典和可替代c5转化酶的关键组分,其中每一种都介导下游补体激活。补体激活导致补体依赖性细胞毒性(cdc),并且过度补体激活可能是有害的并且与几种疾病相关,包含重症肌无力、溶血性尿毒症综合症(hus)和阵发性睡眠性血红蛋白尿症(pnh)。已示出单克隆抗体fc区的改变增强或减少补体结合(moore等人,《单克隆抗体(mabs.)》,2(2):181-9(2010)。
在一些实施例中,本文提供的斯托拉多体是六聚斯托拉多体。本文中的术语“六聚斯托拉多体”是指多聚化以形成相较于非六聚斯托拉多体更高百分比的包括六个斯托拉多体单元的经多聚化的斯托拉多体和/或包括六个斯托拉多体单元的斯托拉多体的多聚体(例如,十二聚体或十八聚体)的斯托拉多体。六聚斯托拉多体能够结合补体级联的一个或多个组分,并且还可以结合一种或多种经典fc受体和/或与新生儿受体fcrn结合。在一个实施例中,六聚斯托拉多体与六聚补体c1q紧密结合。
“直接连接”是指两个序列彼此连接,没有插入或外来序列,例如由限制酶识别位点插入dna或克隆片段中衍生的氨基酸序列。本领域普通技术人员将理解,“直接连接”囊括氨基酸的加入或去除,只要多聚化能力基本上不受影响。
“同源的”是指在给定核酸的整个序列或氨基酸序列上的同一性。例如,“80%同源”是指给定序列与要求保护的序列具有约80%的同一性,并且可以包含插入、缺失、取代和框移。本领域普通技术人员将理解,可以进行序列比对以考虑插入和缺失,以确定序列的整个长度上的同一性。
如本文使用的术语“分离”多肽或肽是指不具有天然存在的对应物或已经从天然伴随其的组分中分离或纯化的多肽或肽,其例如在组织中,例如胰腺、肝脏、脾脏、卵巢、睾丸、肌肉、关节组织、神经组织、胃肠组织、或乳腺组织或肿瘤组织(例如,乳腺癌组织)、或体液(例如,血液、血清或尿液)。通常,当多肽或肽至少70%(干重)不含与其天然缔合的蛋白质和其它天然存在的有机分子时,其被认为是“分离的”。优选地,本发明的多肽(或肽)的制剂分别为至少80%,更优选至少90%,最优选至少99%(干重)的本发明的多肽(肽)。由于化学合成的多肽或肽因其性质而与天然伴随其的组分分离,因此合成的多肽或肽是“分离的”。
本发明的分离多肽(或肽)可以例如通过从天然来源(例如,从组织或体液)中提取;通过表达编码多肽或肽的重组核酸;或通过化学合成而获得。在与其天然来源不同的细胞系统中产生的多肽或肽是“分离的”,因为它必然不含天然伴随其的组分。在一些实施例中,本发明的分离多肽仅包括对应于igg1fc单体和igg2铰链多聚化结构域的序列(seqidno:4),并且不包括可以有助于克隆或纯化蛋白质的其它序列(即,引入的限制酶识别位点或纯化标签)。在此些实施例中,多肽序列可以包括前导序列。分离度或纯度可以通过任何合适的方法测量,例如柱色谱、聚丙烯酰胺凝胶电泳或hplc分析。
如本文使用的术语“fcγr”和“fcγ受体”包含免疫细胞表面上表达的fcγ受体蛋白家族的每个成员,如nimmerjahn等人,《免疫(immunity)》,2006年1月;24(1):19-28中所述,或者可能在以后定义。其目的是,本文所述的术语“fcγr”囊括fcγri、rii和riii家族的所有成员。fcγ受体包含低和高亲和力fcγ受体,包含但不限于人类的fcγri(cd64);fcγrii(cd32)及其同种型和同种异型fcγriialr、fcγriiahr、fcγriib和fcγriic;fcγriii(cd16)及其同种型fcγriiia和fcγriiib。技术人员将认识到,本发明包含与fcγr和fcγr同源物结合的化合物,例如davis等人(《国际免疫学(int.immunol)》,16(9):1343-1353)描述的那些,将适用于未来的fcγr和可能尚未发现的相关同种型和同种异型。
已经描述了hivig与新生儿fc受体(fcrn)结合并使其完全饱和,并且fcrn的这种竞争性抑制可能在hivig的生物活性中起重要作用(例如,jin等人,《人体免疫学(humanimmunology)》,2005,66(4)403-410)。由于与fcγr强烈结合的免疫球蛋白也至少在某种程度上与fcrn结合,因此技术人员将认识到,能够与一种以上fcγ受体结合的斯托拉多体也将与fcrn结合并可以使其完全饱和。
如本文使用的术语“功能性变体”是指通过与参考序列同源性相关的序列,其能够介导与参考序列(当为多肽时)相同的生物学作用,或其编码能够介导与由参考序列(当为多核苷酸时)编码的多肽相同的生物学作用的多肽。例如,本文所述的任何仿生物质的功能性变体将与参考序列具有特定的序列同源性或同一性,并且将能够进行类似于由参考序列编码的蛋白质的免疫调节。功能性序列变体包含多核苷酸和多肽。序列同一性通常可以使用blast2.0(基本局部比对搜索工具)进行评估,使用默认参数进行操作:滤波器-开启,评分矩阵-blosum62,字大小-3,e值-10,空位罚分-11,1和比对-50。在一些实施例中,功能性变体包括与本文提供的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少99%序列同一性的氨基酸序列。
在整个说明书中,除非另有说明,否则igg重链中残基的编号是eu索引的编号,如kabat等人,《免疫相关蛋白序列(sequencesofproteinsofimmunologicalinterest)》,第5版,公共卫生署,国立卫生研究院,贝塞斯达,马里兰州(1991)中,其通过引用明确地并入本文。“如kabat中的eu索引”是指人igg1eu抗体的编号。
igg1存在两种人多形物,称为del和eem多形物。根据kabat编号,del多形物具有第356位处的d和第358位处的l;eem多形物具有第356位处的e和第358位处的m。本文提供的斯托拉多体可以包括del或eemigg1多形物。因此,即使在del多形性背景下明确表达了特定突变体的句子,但本领域技术人员将理解,可以对eem多形物进行相同的突变以产生相同的结果。
ivig仿生物质的结构组分
如本文使用,术语“仿生物质”、“仿生分子”、“仿生化合物”和相关术语是指模拟了另一种化合物的功能的人造化合物,例如混合人静脉内免疫球蛋白(“hivig”)、单克隆抗体或抗体的fc片段。“生物活性”仿生物质是具有与其天然存在的对应物相同或相似的生物活性的化合物。“天然存在的”是指通常在生物体中发现的分子或其部分。天然存在还指基本上天然存在。“免疫活性”仿生物质是表现出与天然存在的免疫活性分子相同或相似的免疫活性的仿生物质,例如抗体、细胞因子、白细胞介素和本领域已知的其它免疫分子。在优选实施例中,本发明的仿生物质是如本文所定义的斯托拉多体。如本文使用的“亲本仿生物质”是指用作本文所述化合物(例如,gl-2045和gl-2019)的基础的非突变仿生物质。
国际pct公开号wo2008/151088和美国专利第8,680,237号通过引用整体并入本文,并且公开了使用连接的免疫球蛋白fc结构域以产生用于治疗病理病状(包含自身免疫性疾病和其它炎症病状)的hivig的经有序多聚化的免疫球蛋白fc仿生物质(生物活性有序多聚体被称为斯托拉多体)。wo2008/151088和us8,680,237中描述的某些斯托拉多体包含短序列,包含斯托拉多体的各个组分之间的限制位点和亲和标签。国际pct公开号wo2012/016073和美国专利申请公开第2013/0156765号公开了斯托拉多体,其中各个组分直接连接,而不是通过限制位点或亲和标签分开。wo2012/016073还具体公开了一种多聚化斯托拉多体,gl-2045,其包括igg1fc结构域,其中igg2铰链多聚化结构域与其c-末端直接连接,并且其相对于n-末端连接的构建体(gl-2019,描述于wo2008/151088)表现出增强的多聚化和补体结合。在某些实施例中,本文所述的斯托拉多体单元包括gl-2045或gl-2019的fc区中的一个或多个点突变,其相对于先前描述的分子导致增强的补体结合和/或fcγr结合和/或fcrn结合。
gl-2045的结构是:igg1铰链-igg1ch2-igg1ch3-igg2铰链,并且gl-2045的氨基酸序列在seqidno:7和8中提供。如本文使用,术语“gl-2045背景上的斯托拉多体”等是指具有igg1铰链-igg1ch2-igg1ch3-igg2铰链结构并且包括相对于gl-2045的一个或多个氨基酸突变、插入或缺失的斯托拉多体。gl-2019的结构是:igg2铰链-igg1铰链-igg1ch2-igg1ch3(seqidno:9)。如本文使用,术语“gl0-2019背景上的斯托拉多体”等是指具有igg2铰链-igg1铰链-igg1ch2-igg1ch3结构并且包括相对于gl-2019的一个或多个氨基酸突变、插入或缺失。
以下段落在结构和功能上定义了本发明的仿生物质的构建单元,然后定义了仿生物质本身。然而,首先要注意的是,如上所述,本发明的每种仿生物质具有至少一个fc结构域和一个多聚化结构域。至少,每个fc结构域是二聚多肽(或是较大多肽的二聚区域),其包括两个肽链或臂(单体),其缔合以形成功能性fcr结合或补体结合位点和能够将所得的同源二聚体多聚化成更高阶的多聚体的多聚化结构域。因此,本文讨论的各个片段和结构域的功能性形式通常以二聚形式存在,最通常为同源二聚或基本上同源二聚形式。本文讨论的各个片段和结构域的单体是必须与第二链或臂缔合以形成功能性二聚结构的单链或臂。
fc片段
“fc片段”是用于描述在免疫球蛋白的羧基末端常规发现的蛋白质区域或蛋白质折叠结构的技术术语。fc片段可以通过使用酶消化(例如,木瓜蛋白酶消化)从单克隆抗体的fab片段中分离,这是一个不完全且不完美的过程(参见mihaesco和seligmann,《实验医学学报(journalofexperimentalmedicine)》,第127卷,431-453(1968))。结合fab片段(含有抗原结合结构域),fc片段构成全抗体,表示这里即为完整的抗体。fc片段由抗体重链的羧基末端部分组成。fc片段中的每条链的长度在约220到265个氨基酸之间,并且链通常经由二硫键连接。fc片段通常含有一个或多个独立的结构折叠或功能性亚结构域。特别地,fc片段囊括fc结构域,其在本文中定义为结合fcγ受体的最小结构。分离的fc片段由二聚化的两个fc片段单体(例如,抗体重链的两个羧基末端部分;本文进一步定义)构成。当两个fc片段单体缔合时,所得的fc片段具有补体和/或fcr结合活性。
fc部分片段
“fc部分片段”是包括少于抗体的整个fc片段的结构域,其保持了足够的结构以具有与fc片段相同的活性,包含fc受体结合活性和/或补体结合活性。因此,fc部分片段可以缺少部分或全部铰链区、部分或全部ch2结构域、部分或全部ch3结构域、和/或部分或全部ch4结构域,这取决于fc部分结构域所衍生自的抗体的同种型。fc部分片段的另一个实例包含包括igg1的ch2和ch3结构域的分子。在本实例中,fc部分片段缺少igg1中存在的铰链结构域。fc部分片段由两个fc部分片段单体构成。如本文进一步定义,当两个这种fc部分片段单体缔合时,所得的fc部分片段具有fc受体结合活性和/或补体结合活性。
fc结构域
如本文使用,“fc结构域”描述了可以与fc受体(fcr)结合或由其结合的最小区域(在较大多肽背景下)或最小蛋白质折叠结构(在分离蛋白背景下)。在fc片段和fc部分片段中,fc结构域是允许分子与fc受体结合的最小结合区。虽然fc结构域可以限于由fc受体结合的离散同源二聚多肽,但是也很清楚的是,fc结构域可以是部分或全部fc片段,以及部分或全部fc部分片段。当术语“fc结构域”用于本发明时,技术人员将其认为是指多于一个fc结构域。fc结构域由两个fc结构域单体构成。如本文进一步定义,当两个这种fc结构域单体缔合时,所得的fc结构域具有fc受体结合活性和/或补体结合活性。因此,fc结构域是可以结合补体和/或fc受体的二聚结构。本文所述的斯托拉多体包括fc结构域,其包括改变斯托拉多体结合补体和/或fc受体的能力的一个或多个突变。
fc部分结构域
如本文使用,“fc部分结构域”描述了fc结构域的一部分。fc部分结构域包含各个重链恒定区结构域(例如,ch1、ch2、ch3和ch4结构域)和不同免疫球蛋白类和亚类的铰链区。因此,本发明的人fc部分结构域包含igg1的ch1结构域、igg1的ch2结构域、igg1的ch3结构域和igg1的铰链区以及igg2。其它物种中对应的fc部分结构域将取决于该物种中存在的免疫球蛋白及其命名。优选地,本发明的fc部分结构域包含igg1的ch1、ch2和铰链结构域以及igg2的铰链结构域。本发明的fc部分结构域可以进一步包括这些结构域和铰链中的多于一个的组合。然而,本发明的各个fc部分结构域及其组合缺少结合fcr的能力。因此,fc部分结构域及其组合包括少于fc结构域。fc部分结构域可以连接在一起以形成具有补体和/或fc受体结合活性的肽,从而形成fc结构域。在本发明中,fc部分结构域与fc结构域一起用作构建单元以产生如本文所定义的本发明的仿生物质。每个fc部分结构域由两个fc部分结构域单体构成。当两个这种fc部分结构域单体缔合时,形成fc部分结构域。
如上所述,fc片段、fc部分片段、fc结构域和fc部分结构域中的每一个是二聚蛋白质或结构域。因此,这些分子中的每一个由两个单体构成,其缔合以形成二聚蛋白质或结构域。虽然上文讨论了同源二聚形式的特性和活性,但是如下讨论单聚肽。
fc片段单体
如本文使用,“fc片段单体”是单链蛋白,当与另一fc片段单体缔合时,其包括fc片段。因此,fc片段单体是构成全抗体fc片段的抗体重链之一的羧基末端部分(例如,包含igg的铰链区、ch2结构域和ch3结构域的重链的连续部分。在一个实施例中,fc片段单体至少包括铰链区的一条链(铰链单体)、ch2结构域的一条链(ch2结构域单体)和ch3结构域的一条链(ch3结构域单体),其连续连接以形成肽。在一个实施例中,ch2、ch3和铰链结构域来自不同的同种型。在一个特定实施例中,fc片段单体含有igg2铰链结构域和igg1ch2和ch3结构域。
fc结构域单体
如本文使用,“fc结构域单体”描述了单链蛋白,当与另一fc结构域单体缔合时,其包括可以与补体结合的fc结构域。两个fc结构域单体的缔合产生一个fc结构域。
在一个实施例中,本发明的fc结构域单体不含有外来序列,如在国际pct公开号wo2008/151088中描述的先前描述的fc结构域单体。相反,本发明的fc结构域单体在一个末端(例如,fc单体的n末端)上直接连接前导序列(例如,seqidno:1)并在另一个末端(例如,fc单体的c末端)上直接连接多聚化结构域(例如seqidno:4、5或6)。本领域技术人员将认识到,虽然构建体是用前导序列产生的,但随后该序列被切割。因此,在优选实施例中,成熟蛋白质将不含有前导序列。
技术人员将理解,本发明进一步囊括fc结构域单体的功能性变体在构建fc片段单体、fc部分片段单体、斯托拉多体单体和本发明的其它单体中的用途。fc结构域单体的功能性变体将与天然fc结构域单体序列具有至少约50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性。
类似地,本发明还囊括fc部分结构域单体的功能性变体在构建fc片段单体、fc部分片段单体、fc结构域单体、斯托拉多体单体和本发明的其它单体中的用途。fc部分结构域单体的功能性变体将与天然fc部分结构域单体序列具有至少约50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性。
在一个实施例中,fc结构域单体从氨基末端到羧基末端包括包括igg1铰链、igg1ch2和igg1ch3的fc结构域,和igg2铰链(gl-2045背景),其中单体包括fc结构域中的一个或多个点突变。在一个实施例中,fc结构域单体从氨基末端到羧基末端包括igg2铰链和包括igg1铰链、igg1ch2和igg1ch3的fc结构域(gl-2019背景),其中单体包括fc结构域中的一个或多个点突变。
斯托拉多体
在特定实施例中,本发明的仿生物质包含斯托拉多体。斯托拉多体是能够结合两种或更多种fc受体,从而向fc受体(例如,低亲和力和高亲和力经典fcr和新生儿受体(fcrn))、补体以及其它受体和fc相互作用分子呈递功能性多价fc的仿生化合物。斯托拉多体优选地表现出显著改善的相对于fc结构域的结合。先前已经在美国专利申请公开第2010/0239633号和第2013/01516767号以及国际pct公开号wo2017/019565中描述了多种不同的物理斯托拉多体构象。先前已经公开了结合大多数或全部与免疫球蛋白igg1fc结合的配体的斯托拉多体(例如gl-2045)(美国专利第8,690,237号以及美国专利申请公开第2010-0239633号和第2013-0156765号)。这些斯托拉多体结构包含向fc受体呈递多于一个fc的支链和直链设计;簇状斯托拉多体,包含向fc受体呈递多于一个fc的本发明的经多聚化的斯托拉多体;和核心斯托拉多体,包含经由fc连接到核心部分(例如,通过使用igmch4结构域和/或j链)而向fc受体呈递多于一个fc的那些。
显而易见的是,上文讨论的fc片段、fc部分片段、fc结构域和fc部分结构域用于构建各种斯托拉多体构象。此外,同样如上文讨论,单个fc结构域单体和fc部分结构域单体首先被产生以形成同源二聚多聚化斯托拉多体单元,并且通过包含多聚化结构域(例如,igg2铰链)而多聚化以形成本发明的簇状斯托拉多体(或经多聚化的斯托拉多体)。在国际pct公开号wo2008/151088、wo2012/016073和wo2017/019565中详细描述了具体的斯托拉多体构型,其内容通过引用整体并入本文。具体地,这些申请中描述的任何斯托拉多体结合补体和/或fcγ受体的能力可以通过斯托拉多体序列的fc结构域部分的第233位和/或第234位和/或第235位和/或第236位和/或第238位和/或第267位、和/或第268位、和/或第297位、和/或第324位和/或第299位、和/或第430位、和/或第345位、和/或第440位中的一个或多个处的突变进一步增强。
斯托拉多体单元单体
如本文使用,术语“斯托拉多体单元单体”是指单个连续的肽分子,当与至少第二斯托拉多体单元单体缔合时,其形成包括至少一个fc结构域的斯托拉多体单元。通常,斯托拉多体单元由两个缔合的斯托拉多体单元单体构成,斯托拉多体也可以含有三个或更多个斯托拉多体单元单体。因此,当提及斯托拉多体单元和同源二聚斯托拉多体单元时,本领域技术人员将理解,包括三个或更多个斯托拉多体单元单体的这种结构囊括在这些术语中,只要fcγr结合保持基本上完整。在优选实施例中,斯托拉多体单元由两个相同的斯托拉多体单元单体(例如,同源二聚体)构成。然而,在一些实施例中,斯托拉多体单元可以由两个彼此相差至少一个氨基酸残基的斯托拉多体单元单体构成,使得所得的斯托拉多体单元是异源二聚蛋白。
斯托拉多体单元单体可以具有当与另一个斯托拉多体单元单体缔合以形成“斯托拉多体单元”时将形成一个、两个、三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个、十五个、十六个、十七个、十八个或更多个fc结构域的氨基酸序列。斯托拉多体单元单体可以进一步具有当与另一个斯托拉多体单元单体缔合以形成斯托拉多体单元时将形成一个、两个、三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个、十五个、十六个、十七个、十八个或更多个fc部分结构域的氨基酸序列。
在斯托拉多体单元背景下将形成fc结构域和fc部分结构域的斯托拉多体单元单体区域可以简单地从斯托拉多体单元单体分子的连续区域的羧基末端排列到氨基末端。包括斯托拉多体单元单体的特定fc结构域单体和fc部分结构域单体的排列并非是关键性的。然而,排列必须允许在两个斯托拉多体单体缔合时形成两个功能性fc结构域。在一个实施例中,本发明的斯托拉多体含有igg1fc单体的n末端和前导肽(seqidno:1)的c末端之间的直接连接以及igg1fc的c末端和igg2铰链多聚化结构域(seqidno:4)的n末端之间的直接连接。在一个实施例中,本发明的斯托拉多体含有igg2铰链多聚化结构域(seqidno:4)的n-末端和前导肽(seqidno:1)的c末端之间的直接连接以及igg2铰链多聚化结构域的c末端和igg1fc单体的n末端之间的直接连接。
作为一个澄清实例,技术人员将理解,包括所示点突变的本发明的斯托拉多体分子可以通过制备编码具有所需点突变的fc结构域单体的多核苷酸分子并编码多聚化区域来构建。可以将此多核苷酸分子插入表达载体中,该表达载体可以用于转化细菌群或转染哺乳动物细胞群。然后可以通过在适当的培养条件下培养转化的细菌或转染的哺乳动物细胞来产生斯托拉多体单元单体。例如,通过用染料木素/g418选择细胞,可以实现延续稳定转染细胞库的克隆细胞系。可替代地,可以在cmv启动子的控制下,用编码本发明的斯托拉多体的dna(例如,编码根据seqidno:7-34中任一个的斯托拉多体的dna)瞬时转染细胞。然后,表达的斯托拉多体单元单体可以在使用斯托拉多体间单体键连接的斯托拉多体单元单体的自聚集或斯托拉多体单元单体的缔合时形成功能性斯托拉多体单元。然后,可以使用例如蛋白a或蛋白g柱通过亲和色谱从细胞培养基中纯化表达的斯托拉多体单元。本领域技术人员将理解,核酸构建体中包含的前导肽仅用于促进斯托拉多体单元单体肽的产生,并且在表达成熟蛋白质时被切割。因此,本发明的生物活性仿生物质不包括前导肽。
簇状斯托拉多体
如上所述,本发明的斯托拉多体是能够与两种或更多种fc受体(优选两种或更多种fcγr)结合的仿生化合物,并且可以具有三种物理构象:连续、簇状或核心。在一个优选实施例中,本发明的斯托拉多体是簇状斯托拉多体,在本文中也被称为“经多聚化的斯托拉多体”。在簇状斯托拉多体或经多聚化的斯托拉多体背景下,术语“斯托拉多体单元”或“多聚化斯托拉多体单元”是指由两个能够与一种或多种fcr(例如,fcγr)结合,能够与其它多聚化斯托拉多体单元多聚化并且当与另一个多聚化斯托拉多体单元缔合时能够与两种或更多种fcr结合的单体(例如,斯托拉多体单元单体)构成的二聚蛋白质。通过一些其它方式(即通过使用核心部分)形成斯托拉多体的斯托拉多体单元简称为斯托拉多体单元,因此多聚化斯托拉多体单元是一种包括多聚化结构域的斯托拉多体单元。“斯托拉多体单元单体”是指单个连续的肽分子,当与至少第二斯托拉多体单元单体缔合时,其形成包括至少一个fc结构域并在经多聚化的斯托拉多体背景下包括至少一个多聚化结构域的斯托拉多体单元。多聚化斯托拉多体单元的斯托拉多体单元单体在本文中被称为“多聚化斯托拉多体单元单体”。在一个斯托拉多体单元上含有多个fc结构域的连续斯托拉多体可以被分类为簇状斯托拉多体单元或多聚化斯托拉多体单元,只要该分子还含有至少一个多聚化结构域。因此,簇状斯托拉多体或经多聚化的斯托拉多体是能够结合两个或更多个fcγr和/或补体组分(例如,c1q)的仿生化合物。在一些实施例中,本发明的经多聚化的斯托拉多体包括六个多聚化斯托拉多体单元并且能够结合c1q分子的所有六个头部。
如上所述,在经多聚化的斯托拉多体背景下,斯托拉多体单元包括至少一个fc结构域和至少一个“多聚化结构域”,并且在本文中被称为“多聚化斯托拉多体单元”。多聚化结构域是已知在天然存在的蛋白质中引起蛋白质多聚化的氨基酸序列,其实例描述于美国专利申请公开第2013-0156765号和第2014-0072582号,其出于所有目的通过引用整体并入。如本文使用,“多聚化”是指多个(即,两个或更多个)单独的多聚化斯托拉多体单元连接或结合在一起,例如以形成多聚化斯托拉多体单元的二聚体、三聚体、四聚体、五聚体、六聚体等(例如以形成经多聚化的斯托拉多体)。通常,本文所述的多聚化结构域包括导致二聚蛋白质(例如,多聚化斯托拉多体单元)进一步多聚化的肽序列。肽多聚化结构域的实例包含igg2铰链、异亮氨酸拉链、胶原甘氨酸-脯氨酸-脯氨酸(gpp)重复和锌指。在一些实施例中,多聚化结构域可以是igg2铰链、异亮氨酸拉链或其组合。
在一个特定实施例中,多聚化结构域是igg2铰链。如本领域已知,人igg2的铰链区可以形成共价二聚体(yoo,e.m.等人,《免疫学杂志(j.immunol.)》,170,3134-3138(2003);salfeld等人,《自然生物技术(naturebiotech.)》,25,1369-1372(2007))。igg2的二聚体形成可能由igg2铰链结构中的c-c键介导(yoo等人,2003),表明单独的铰链结构可以介导二聚体形成,尽管igg2铰链相互作用是可变的和动态的。然而,在人血清中发现的igg2二聚体的量是有限的,并且估计总igg2的少于10%作为同源二聚体的二聚体存在(yoo等人,2003)。此外,没有定量证据表明igg2的多聚化超出了同源二聚体的二聚体(yoo等人,2003)。也就是说,尚未发现天然igg2在人血清中形成更高阶的多聚体。相反,含igg2铰链的多聚化斯托拉多体单元(即,gl-2045、g019和g051,如wo2012/016073中所述)形成高度稳定的、更高阶的经多聚化的斯托拉多体,如非还原性sds-page凝胶,分析超速离心,以及在37℃和100%湿度下3个月的稳定性研究所证明。特别地,含igg2铰链的经多聚化的斯托拉多体的制剂令人惊讶地包括比人血清中天然igg2观察到的10%更高百分比的二聚体。例如,经多聚化的斯托拉多体(包含同源二聚体的二聚体、三聚体、四聚体和更高阶的多聚体)的百分比通常超过20%并且可以超过30%、40%、50%、60%、70%、80%或甚至90%。
人igg2铰链单体的氨基酸序列如下:erkccvecppcp(seqidno:4)。seqidno:4中4个半胱氨酸中任何一个的突变可能与斯托拉多体单元的大大降低的多聚化有关。igg2铰链单体有两个c-x-x-c部分。因此,本发明的斯托拉多体单元单体可以包括igg2铰链单体的完整12氨基酸序列,或四个氨基酸核心中的任一个或两个,以及fc结构域单体。虽然核心结构的x-x可以是任何氨基酸,但是在一个优选实施例中,x-x序列是v-e或p-p。领域技术人员将理解,除了核心四氨基酸结构之外,igg2铰链单体还可以包括铰链序列的任何部分,包含全部igg2铰链序列和部分或全部igg2ch2和ch3结构域单体序列。不受理论束缚,igg2铰链多聚化结构域可以通过与斯托拉多体单元的任何部分相互作用而形成多聚体。也就是说,一个斯托拉多体单元的igg2铰链可以结合另一个斯托拉多体单元的igg2铰链,从而形成同源二聚体的二聚体,或同源二聚体的更高阶的多聚体,同时相对于天然igg1fc保持增加的与fc受体和/或补体组分的功能性结合。可替代地,一个多聚化斯托拉多体单元的igg2铰链结构域可以结合另一个多聚化斯托拉多体单元的igg1铰链,从而形成同源二聚体的二聚体,或同源二聚体的更高阶的多聚体,同时相对于天然igg1fc保持增加的与fc受体和/或补体组分的功能性结合。一个多聚化斯托拉多体单元的igg2铰链结构域还可能与igg1fc结构域的另一部分(即另一个多聚化斯托拉多体单元的ch2或ch3结构域)结合以形成同源二聚体的二聚体,或同源二聚体的更高阶的多聚体,同时相对于天然igg1fc保持增加的与fc受体和/或补体组分的功能性结合。
亮氨酸和异亮氨酸拉链还可以用作多聚化结构域。已知亮氨酸和异亮氨酸拉链(卷曲螺旋结构域)有助于蛋白质二聚体、三聚体和四聚体的形成(harbury等人,《科学(science)》,262:1401-1407(1993);o'shea等人,《科学(science)》,243:538(1989))。通过利用异亮氨酸拉链的自然趋势形成三聚体,可以产生簇状斯托拉多体。
虽然技术人员将理解可以使用不同类型的亮氨酸和异亮氨酸拉链,但是在一个优选实施例中,使用来自gcn4转录调节剂的经修饰的异亮氨酸拉链(morris等人,《分子免疫学(mol.immunol.)》,44:3112-3121(2007);harbury等人,《科学(science)》,262:1401-1407(1993))。经修饰的异亮氨酸拉链的氨基酸序列是gggsikqiedkieeilskiyhieneiarikkligerghggg(seqidno:5)。该异亮氨酸拉链序列仅是可以用作多聚化结构域的几种可能序列中的一种。虽然可以使用seqidno:5中所示的整个序列,但是序列的下划线部分代表可以用于本发明的簇状斯托拉多体中的异亮氨酸拉链的核心序列。因此,本发明的多聚化斯托拉多体单元单体可以包括异亮氨酸拉链的完整氨基酸序列,或28氨基酸核心,以及一个或多个fc结构域单体。技术人员还将理解,除了核心28氨基酸结构之外,异亮氨酸拉链可以包括拉链的任何部分,因此可以包括多于28个氨基酸但少于整个序列。
甘氨酸-脯氨酸-脯氨酸(gpp)重复是在人胶原中发现的导致胶原蛋白:蛋白质结合的氨基酸序列。虽然技术人员将理解不同类型的gpp重复可以用作多聚化结构域,但是在一个优选实施例中,使用了如fan等人(《faseb杂志(fasebjournal)》,3796,第22卷,2008)所述的gpp重复(seqidno:6)。该gpp重复序列仅是可以用于fc结构域单体的多聚化的几种可能序列之一。虽然可以使用seqidno:6中所示的整个序列,但是也可以使用不同长度的重复以促进本文所述的多聚化斯托拉多体单元的多聚化。同样,gpp重复中含有不同氨基酸的重复还可以被取代。
无论是由于氨基酸取代还是由于培养条件,糖基化改变也可以影响本发明的仿生物质的多聚化。糖基化对肽多聚化的影响在本领域中得到充分描述(例如,gralnick等人,《美国国家科学院院院刊(proceedingsofthenationalacademyofsciencesoftheunitedstatesofamerica)》,第80卷,第9期,[第1部分:生物科学](1983年5月1日),第2771-2774页;asanuma等人,《国际会议系列)(internationalcongressseries)》,第1223卷,2001年12月,第97-101页),并在下面进一步讨论。
术语“经多聚化的斯托拉多体”在本文中用于指由两个或更多个多聚化斯托拉多体单元构成的能够与至少两个fcr结合的多聚化合物。例如,当至少一个多聚化斯托拉多体单元(即,包括一个或多个fc结构域和一个或多个多聚化结构域的至少一个同源二聚多肽)经由多聚化结构域连接到至少一种其它多聚化斯托拉多体单元时,多聚化斯托拉多体单元多聚化以形成经多聚化的斯托拉多体。所得的经多聚化的斯托拉多体可以包括2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、12个、13个、14个、15个、16个、17个、18个或更多个多聚化斯托拉多体单元。在特定实施例中,本文所述的经多聚化的斯托拉多体表现出缓慢的与fcγ-受体(fcγr)和/或补体组分的解离(亲和性特性)。
应理解,本文公开的斯托拉多体和其它仿生分子可以衍生自包含人在内的多种物种中的任何物种。实际上,本发明的任何一种仿生分子中的fc结构域或fc部分结构域可以衍生自来自多于一种(例如,来自两种、三种、四种、五种或更多种)物种的免疫球蛋白。然而,它们将更通常衍生自单一物种。此外,应当理解,本文公开的任何方法(例如,治疗方法)可以应用于任何物种。通常,应用于目标物种的仿生物质的组分都将衍生自该物种。然而,也可以使用其中所有组分属于不同物种或来自多于一种物种(包含或不包含应用相关方法的物种)的仿生物质。
包括本发明的斯托拉多体和其它仿生物质的fc结构域和fc部分结构域的特异性ch1、ch2、ch3、ch4结构域和铰链区可以独立地选择,无论是在免疫球蛋白亚类方面,还是在它们所衍生自的生物体方面。因此,本文公开的斯托拉多体和其它仿生物质可以包括fc结构域和部分fc结构域,其独立地源自各种免疫球蛋白类型,例如人igg1、igg2、igg3、igg4、iga、iga1、igd、ige和igm,小鼠igg2a,或狗iga或igb。类似地,每个fc结构域和部分fc结构域可以衍生自多种物种,优选哺乳动物物种,包含非人灵长类动物(例如,猴子、狒狒和黑猩猩)、人类、鼠科动物、家鼠、牛科动物、马科动物、猫科动物、犬科动物、猪科动物、兔子、山羊、鹿、绵羊、雪貂、沙鼠、豚鼠、仓鼠、蝙蝠、鸟类(例如,鸡、火鸡和鸭)、鱼类和爬行动物,以产生物种特异性或嵌合性斯托拉多体分子。各个fc结构域和部分fc结构域也可以是人源化的。
本领域技术人员将认识到,不同的fc结构域和部分fc结构域将提供不同类型的功能。例如,fcrn与igg免疫球蛋白特异性地结合,而不与其它种类的免疫球蛋白结合。本领域普通技术人员还将理解,可以使各种有害后果与特定ig结构域的使用相关,例如过敏性反应与iga输注相关。本文公开的仿生物质通常应设计成避免这种作用,但是在特定情况下可能需要这种作用。
另外的ivig仿生物质
另外的ivig仿生物质描述于美国专利申请公开第2015-0218236号、第2017-0088603号、第2016-0229913号、第2017-0081406号、第2017-0029505号以及国际pct公开号wo2016/009232、wo2016/139365、wo2017/005767、wo2017/013203和wo2017/036905。尽管这些描述在用于描述单个组分的语言中略有不同,但是其中描述的每种化合物基本上描述了由二聚多肽构成的多聚fc化合物,所述二聚多肽包括缔合以形成至少两个功能性fc结构域(例如,斯托拉多体单元)的连续连接的fc结构域单体。连接fc结构域单体的连接子可以是共价键(例如,肽键)、肽连接子或非肽连接子。此外,fc结构域单体之间缔合以形成功能性fc结构域的性质并非是关键性的,只要它允许形成能够结合经典fc受体和/或补体组分的功能性fc结构域(例如,半胱氨酸键或静电相互作用)。
fc受体的选择性免疫调节剂(sif)
us2016/0229913描述了作为fc受体的选择性免疫调节剂(sif)的斯托拉多体,其包含包括第一fc结构域单体、连接子和第二fc结构域单体的第一多肽;包括第三fc结构域单体的第二多肽;和包括第四fc结构域单体的第三多肽。所述第一和第三fc结构域单体组合以形成第一fc结构域,并且所述第二和第四fc结构域单体组合以形成第二fc结构域单体。因此,这些化合物通过三个独立多肽(sif3tm)的缔合形成两个功能性fc结构域。us2016/0229913中公开的另外的实施例描述了包括多至5个fc结构域单体的化合物的形成。这些化合物基本上包括通过序列突变组装的连续连接的fc结构域(参见us2005/0249723和us2010/0239633)和单独的fc结构域单体(其变体公开于us2006/0074225)。
尾部fc多聚体
国际pct公开号wo2015/132364、wo2017/005767和wo2017/013203,美国专利申请公开第2015/0218236号公开了一种治疗自身免疫性疾病或炎性疾病的方法,其包括向有需要的患者施用作为多fc治疗剂的斯托拉多体。其中描述的多fc治疗剂包括5个、6个或7个多肽单体单元,其中每个单体单元包括fc受体结合部分,其包括两个igg重链恒定区。每个igg重链恒定区包括经由二硫键与相邻多肽单体的igg重链恒定区的半胱氨酸残基连接的半胱氨酸残基。由于us2015/0218236中描述的肽“单体”由两条igg重链构成,它们实际上是二聚蛋白质(例如,fc结构域)。在us2015/0218236的一些实施例中,单体单元进一步包括尾部区域,其有助于将单体单元组装成聚合物(例如,多聚体)。因此,其中使用的“尾部”具有与本文和us2010/0239633和us2013/0156765中描述的多聚化结构域几乎相同的目的。
包括第309位处的突变的fc多聚体
美国专利申请公开第2017-0081406号和第2017-0088603号描述了一种经多聚化的斯托拉多体,其是由多肽单体单元构成的多fc治疗剂,其中每个多肽单体包括fc结构域。每个所述fc结构域由两个重链fc区构成,每个重链fc区包括第309位处的半胱氨酸(us2017-0081406)或第309位处的半胱氨酸以外的氨基酸(us2017-0088603)。因此,us2017-0081406和us2017-0088603中描述的多肽“单体”实际上是二聚蛋白质(例如,如本文使用的fc结构域单体)。us2017-0081406和us2017-0088603中的每个重链fc区在其c-末端与尾部融合,使得单体组装成多聚体。因此,其中使用的“尾部”具有与本说明书中描述的多聚化结构域几乎相同的目的。
由连续连接的fc结构域单体构成的fc多聚体
美国专利申请公开第2010/0143353号描述了一种连续多克隆抗体,其是包括igg的至少第一和第二fc片段的多fc治疗剂,igg的第一igg片段中的至少一个包括至少一个ch2结构域和铰链区,并且其中igg的第一和第二fc片段通过铰链结合形成链。在us2010/0143353的一些实施例中,基本上相似的链缔合以形成二聚体。在us2010/0143353的其它实施例中,多条基本相似的链缔合以形成多聚体。如本文所述,fc片段囊括fc结构域。因此,us2010/0143353中公开的治疗剂包括能够结合至少两种fc受体并组装成多聚体的多聚化fc治疗剂。
普通斯托拉多体
本发明的免疫活性化合物是同源二聚体的多聚体,其中每个同源二聚体具有与补体和/或fcγr和/或新生儿受体(fcrn)结合的能力。因此,当经多聚化时,免疫活性仿生物质含有至少两个同源二聚体,每个同源二聚体具有与补体、和/或fcγr(包含fcγri、fcγrii和/或fcγriii)、和/或fcrn结合的能力。本文提供的斯托拉多体是“普通斯托拉多体”。本文的术语“普通斯托拉多体”是指能够结合补体级联的一个或多个组分和经典fcr(包含fcrn)的斯托拉多体。在一些实施例中,本文描述的普通斯托拉多体不一定表现出相对于一种fcr而优先与另一种fcr结合或不一定表现出优先结合fcr或补体蛋白。在一些实施例中,本文所述的普通斯托拉多体表现出优先与一种或多种fcr结合或优先与补体蛋白结合。因此,本文描述的普通斯托拉多体不同于例如在国际pct公开号wo2017/019565中描述的斯托拉多体实施例,其描述了包括斯托拉多体的补体优先的多fc治疗剂。补体优先的斯托拉多体包括多聚化结构域,并且进一步包括fc结构域的ch1和/或ch2区域中的点突变,使得补体优先的斯托拉多体能够优先结合一个或多个补体组分,例如c1q。这种优先结合直接通过增加的与补体组分的结合来实现,或间接地通过减少的斯托拉多体与经典fc受体的结合来实现。
通常,本发明的免疫活性仿生物质被设计成与天然igg1或对应的亲本仿生物质相比保持或增加补体和/或fcγr结合。在一个实施例中,本发明的仿生物质结合补体系统的组分,包含但不限于c1q、c1r、c1s、c4、c4a、c4adesarg、c3、c3a、c3adesarg、c4b2a3b、c3b、ic3b(包含ic3b1、ic3b2、c3dg、c3d和/或c3g)、c5、c5a、c5b、c6、c7、c8和c9,并且因此可以充当“补体汇”。在一个实施例中,本发明的仿生物质表现出保持或增强的与c1q的结合。在一个实施例中,本发明的仿生物质结合c5b-9膜攻击复合物上游的补体系统的组分。在一个实施例中,本发明的仿生物质结合c5a上游的补体系统的组分。在一个实施例中,与亲本斯托拉多体相比,本发明的仿生物质表现出减少的c5a和膜攻击复合物形成。
在一个实施例中,与天然igg1或亲本仿生物质相比,本发明的仿生物质表现出保持或增强的与fcγr(包含fcγri和/或fcγriia和/或fcγriib和/或fcγriii)的结合。在一个实施例中,本发明的仿生物质表现出保持或增强的fcγri和/或fcγriia和/或fcγriib和/或fcγriii结合和保持或增强的补体c1q结合。事实上,相对于先天免疫球蛋白igg1,增强的与补体途径的组分和/或fcγr的结合的程度可能是非常显著的,接近或超过补体途径和/或fcγr的组分与在某些情况下可能存在于人类的聚集igg1的结合。“聚集天然igg的免疫活性”是指经多聚化的igg的在免疫系统暴露于igg聚集体时影响免疫系统的功能的性质。天然经多聚化的igg的具体性质包含改变的与fcγr的特异性结合、免疫细胞表面上fcγr的交联、或经多聚化的igg的效应子功能,例如adcc、adcp或补体固定(参见例如nimmerjahn等人,《实验医学学报(jexpmed.)》,2007;204:11-15;augener等人,《血液(blut.)》,1985;50:249-252;arase等人,《实验医学学报(jexpmed.)》,1997;186:1957-1963;teeling等人,《血液(blood.)》,2001;98:1095-1099;anderson和mosser,《免疫学杂志(jimmunol.)》,2002;168:3697-3701;jefferis和lund,《免疫学快报(immunologyletters.)》,2002;82:57;banki等人,《免疫学杂志(jimmunol.)》,2003;170:3963-3970;siragam等人,《临床研究杂志(jclininvest.)》,2005;l15:155-160)。通常通过与同源二聚igg的性质比较来评价这些性质。
在一些实施例中,本发明的仿生物质和组合物结合补体组分c1q和/或c4和/或c4a和/或c3和/或c3a和/或c5和/或c5a。在一些实施例中,本发明的仿生物质和组合物结合c3b。在一些实施例中,本发明的仿生物质和组合物结合补体分子,例如c1q、c3或c3b,防止或减少补体系统的下游激活(例如,减少c5的切割,减少c5a和/或c5b的产生,和/或减少膜攻击复合物的形成,和/或减少末端补体复合物的形成)并防止或减少下游补体介导的功能,例如补体依赖性细胞毒性、炎症或血栓形成。在一些实施例中,本发明的仿生物质和组合物与升高的c4a、c3a和/或c5a水平相关,并且这些升高的水平与抗炎或抗血栓形成临床特征相关。
在一些实施例中,本发明的仿生物质和组合物具有另外的优点:相对于完整免疫球蛋白或亲本仿生物质增强的多聚化。在一些实施例中,本发明的仿生物质和组合物多聚化以形成高阶多聚体。在一些实施例中,本发明的仿生物质和组合物具有优点:与完整免疫球蛋白相同或增强的补体结合和增强的多聚化。在一些实施例中,本发明的仿生物质和组合物表现出保持或增强的与fcγri、fcγriia、fcγriib或fcγriii的结合和增强的多聚化。在一些实施例中,本发明的仿生物质和组合物表现出保持或增强的补体结合,保持与fcγri、fcγriia、fcγriib和fcγriii的结合,并且具有增强的多聚化。
在一个实施例中,本发明的仿生物质和组合物可具有经修饰的效应子功能,例如相对于先天免疫球蛋白igg1或亲本仿生物质或组合物的经修饰的补体依赖性细胞毒性(cdc)、adcp和/或adcc。在一些实施例中,相对于先天免疫球蛋白igg1或亲本仿生物质或组合物,本发明的仿生物质和组合物可以更大程度地抑制效应子功能,例如补体依赖性细胞毒性(cdc)、adcp和/或adcc。
突变和功能性变体
本发明囊括包括fc结构域和fc部分结构域的斯托拉多体,所述fc结构域和fc部分结构域具有与fc结构域或fc部分结构域的天然存在的氨基酸序列不同的氨基酸。包含在本发明的仿生化合物中的优选fc结构域对补体和/或fcγr具有可测量的特异性结合亲和力。特异性结合通常通过标记配体的量来评估,所述配体随后在结合测定中可被过量的未标记配体置换。然而,这并不排除本领域公认的评估特异性结合的其它方法(例如,mendel和mendel,《生物化学学报(biochemj.)》,1985年5月15日;228(l):269-72)。特异性结合可以以本领域公知的各种方式测量,例如表面等离子体共振(spr)技术(可通过
本领域可获得许多fc结构域和fc结构域单体的一级氨基酸序列和x射线晶体学结构。参见例如woof等人,《自然评论-免疫学(natrevimmunol.)》,2004年2月;4(2):89-99。具有fcγ受体结合能力的代表性fc结构域包含来自人igg1的fc结构域(seqidno:2和3)。这些天然序列已经过广泛的结构-功能分析,包含功能性序列的定点诱变作图。基于这些现有的结构-功能研究和可获得的晶体学数据,本领域技术人员可设计功能性fc结构域序列变体,同时保留补体和/或fcγr结合能力。例如,可以加入半胱氨酸残基以增强单体之间的二硫键或缺失半胱氨酸残基以改变斯托拉多体同源二聚体之间的相互作用。此外,本领域技术人员可以设计功能性fc结构域序列变体,同时保留增强的补体和/或fcγr结合能力,或者可以设计功能性fc结构域序列变体,其具有甚至进一步增强的补体和/或fcγr结合能力。
氨基酸改变可以在fc结构域的整个序列中发现,或者可以分离成包括fc结构域的特定fc部分结构域。用于本发明的斯托拉多体和其它仿生物质的fc结构域的功能性变体将与天然fc结构域具有至少约50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性。类似地,用于本发明的斯托拉多体和其它仿生物质的fc部分结构域的功能性变体将与天然fc部分结构域具有至少约50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性。
氨基酸改变可以减少、增加斯托拉多体与fcrn、经典fcγr和/或补体组分的结合亲和力或使其保持不变。这些改变包含缺失、加入和其它取代。在优选实施例中,这种氨基酸改变将是保守氨基酸取代。保守氨基酸取代通常包括以下组内的改变:甘氨酸和丙氨酸;缬氨酸、异亮氨酸和亮氨酸;天冬氨酸和谷氨酸;天冬酰胺、谷氨酰胺、丝氨酸和苏氨酸;赖氨酸、组氨酸和精氨酸;和苯丙氨酸和酪氨酸。另外,氨基酸改变可以增强多聚化,例如通过加入半胱氨酸残基。
免疫球蛋白(ig)与fcγr和补体系统的组分的相互作用通过ig的fc结构域介导,并且完整抗体分子的fc区中的突变在抗体特性和功能方面具有可预测的结果。参见例如moore等人,《单克隆抗体(mabs)》,2:2;18(2010)和shields等人,《生物化学杂志(journalofbiologicalchemistry)》,276;6591(2001)。然而,本发明人惊奇地发现,先前描述的用于修饰抗体功能(例如以减少或消除单克隆抗体中的经典fcγr结合)的突变在多聚化斯托拉多体背景下不具有相同的作用。事实上,在多聚化斯托拉多体背景下的特定突变的作用是完全不可预测的。
例如,示出了第236位和第328位处的双突变(tai等人,《血液(blood)》,119;2074(2012))或第233位处的单突变(shields等人,《生物化学杂志(j.biol.chem.)》,276(9):6591(2001)以减少抗体或免疫球蛋白fc与经典fcγr的结合。特别地,示出了第236位和第328位处的双突变以消除抗体或免疫球蛋白与fcγri的结合(tai等人,2012)。然而,发明人惊奇地发现,在多聚化斯托拉多体背景下的这些突变进一步包括第267位、第268位和/或第324位处的补体增强突变,fcγri结合令人惊讶地保持在某些多聚化斯托拉多体中。此外,描述了第234位和第235位处的突变以减少免疫球蛋白与经典fcγr的结合(arduin,《分子免疫学(molecularimmunology)》,65(2):456-463(2015)),并以减少c1q结合(wo2015/132364;arduin等人,《分子免疫学(molecularimmunology)》,65(2):456-463(2015);boyle等人,《免疫(immunity)》,42(3):580-590(2015))。然而,在多聚化斯托拉多体背景下,这些点突变不抑制fc与经典fcγr或c1q的结合。此外,预计第233位和第236位处的双突变(e233p和g236r)会减少fc与所有经典fcr的结合;然而,本发明人意外地发现,包括在这两个位置处的突变的几种突变组合令人惊讶地导致了相对于未突变的亲本斯托拉多体的保持或增加与一种或多种fcr的结合。
另外,先前描述了第328位处的突变(l328f)以增加fc仅与fcγriib的结合(chu等人,《分子免疫学(molecularimmunology)》,45;3926(2008));然而,本发明人惊奇地发现,在至少第267位、第268位和第324位处的另外的突变背景下,包括第328位的突变的斯托拉多体导致以不可预测的方式增加的与除fcγriib之外的一种或多种经典fcγr的结合。此外,先前描述了第238位处的突变以增加fc与fcγriib的结合并以减少fc与fcγri和fcγriia的结合,同时描述了第265位处的突变以减少所有经典fcγr结合(mimoto等人,《蛋白质工程、设计和选择(proteinengineering,design,andselection)》,第1-10页(2013))。然而,本发明人先前已发现在多聚化斯托拉多体背景下的第238位和第265位处的突变进一步包括第267位、第268位和/或第324位处的至少一个补体增强突变,并导致强烈的与fcγriia的结合。
因此,本领域已知的氨基酸突变对抗体具有特定作用的作用,例如预测增加或减少fc与特定fcγr的结合或改变在抗体背景下的c1q结合的突变,在多聚化斯托拉多体背景下无法预测。
此外,即使在斯托拉多体背景下,突变的作用同样是不可预测的,因为在没有任何引入的突变的情况下,亲本构建体本身(即gl-2045和gl019)的功能是不可预测的。例如,尽管gl-2045和g019具有完全相同的组分,并且其事实上除了igg2铰链区相对于igg1fc结构域的位置之外是完全相同的分子,但是这些分子表现出截然不同的关于补体结合的活性。尽管两种分子都多聚化并结合fc受体,但是gl-2045表现出强烈的与所有fc受体以及补体c1q的结合和cdc的抑制。相反,g019不能很好地结合补体c1q或抑制cdc,尽管g019仅在定向上不同于gl-2045(参见wo2012/016073)。因此,同一fc位置中存在的相同突变对两个相同但igg2铰链相对于igg1fc结构域的位置不同的斯托拉多体的作用也无法预测,因为即使当没有突变存在时,这两个斯托拉多体具有不同的功能特性。
举例来说,wo2017/019565中描述的化合物g996和g999都具有moore等人公开的三重突变,其预期增加c1q结合(s267e/h268f/s324t)以及另外的突变g236r。这两种化合物之间的唯一区别是g996在gl-2045背景上并且包括c末端igg2铰链,而g999在g019背景上并且包括n末端igg2铰链。gl-2045背景(g996)上的斯托拉多体中的这一组突变相对于经典fcγr优先保持与c1q的fc结合,而g019背景(g999)上的斯托拉多体中的同一组突变导致撤消与c1q的fc结合。在另外一组充分表征的突变中的这种功能二分突出了在多聚化斯托拉多体背景下产生的突变的不可预测性。此外,当两个斯托拉多体除一个或多个特定位置处的一个或多个突变以外彼此相同时,即使突变是结构上相似的氨基酸,这两个斯托拉多体也可以具有截然不同的功能特性。因此,基于关于单克隆抗体的文献,无法预测斯托拉多体的任何区域内的任何突变或一组突变对多聚化斯托拉多体的活性的作用。
fc与fcγr和补体蛋白的接触不仅通过蛋白质-蛋白质相互作用介导,而且通过与fc上存在的有助于结合亲和力的聚糖的相互作用介导。因此,除了天然fc结构域的氨基酸序列组成外,fc结构域的碳水化合物含量在fc结构域结构和功能上起重要作用。参见例如shields等人,《生物化学杂志(j.biol.chem.)》,2002年7月;277:26733-26740;wright和morrison,《免疫学杂志(j.immunol)》,1998年4月;160:3393–3402。n-聚糖存在于在igg1fc结构域的第297-299位发现的在asn-xaa-ser/thr/cys序列子(其中xaa是任何氨基酸)的许多分泌和膜结合糖蛋白上。
已经通过单克隆抗体的igg1fc结构域中的糖基化模式的各种改变,包含已知糖基化位点的点突变n297(shields等人,《生物化学杂志(j.biol.chem.)》,2001年2月;276:6591-6604;lund等人,《分子免疫学(mol.immunol.)》,1992;29;53-59)和酶促fc去糖基化(mimura等人,《生物化学杂志(journalofbiologicalchemistry)》,276,第45539-45547页(2001)),证明了糖基化在fc结构域与fcγr结合中的重要性。这些数据证明,经由第297位的突变的igg1fc结构域的无糖基化导致了fc与所有经典fcγr的结合的抑制和与c1q的结合的抑制(sazinsky等人,《美国国家科学院院院刊(procnatlacadsciusa.)》,2008年12月23日;105(51))。本发明人发现,在gl-2045背景上的多聚化斯托拉多体背景下,fc结构域的第297位处的点突变导致关于与经典fcγr受体结合的不可预测的作用。例如,包括第297位处的突变与突变h268f和s324t以及另外的s267e突变的组合的多聚化斯托拉多体表现出与fcγri、fcγriib和c1q的亲和结合(g998,描述于wo2017/019565)。然而,第297位处的突变与突变h268f和s324t以及另外的s267r突变的组合仅表现出与fcγri的结合;完全撤消了与fcγriib和c1q的结合(g1132,描述于wo2017/019565)。
在单克隆抗体背景下,在糖基化共有序列的第299位处引入的单点突变t299a导致保持与fcγriia结合的无糖基化fc,并且在位置s298和t299处的特异性双突变(s298g/t299a)产生保持与fcγriia和fcγriib结合但不结合fcγriiia、fcγri或c1q的无糖基化fc(sazinsky等人,《美国国家科学院院院刊(procnatlacadsciusa.)》,2008年12月23日;105(51))。第299位处存在的侧链的性质也示出为对fcγr结合是重要的,因为糖基化t299s突变减少了跨所有经典fcγr的结合(参见pct/us2008/085757)。然而,在多聚化斯托拉多体背景下的第299位处的点突变的引入证明了对与经典fcγr和c1q的结合的不可预测的作用。例如,在多聚化斯托拉多体(g1099)背景下的t299a突变的引入导致保持或增强的不仅与fcγriia,而且与fcγri、fcγriib、fcγriiia和c1q的fc结合。在另外的突变(例如,267、268和324)背景下的t299a突变的作用不可预测地影响与fcγr和c1q的fc结合。例如,在多聚化斯托拉多体背景下的h268f、s324t和t299a突变与s267e、s267q、s267d、s267h或s267n突变的组合的引入导致保持与所有经典fcγr结合的斯托拉多体,并且表现出与c1q的高度结合(参见本文所述的g1068、1094、1092、1107和1095)。相反,在多聚化斯托拉多体背景下的h268f、s324t和t299a突变与s267r或s267k突变的组合的引入导致不保持与fcγriia、fcγriib或c1q结合但保持与fcγri(g1096,描述于wo2017/019565)或fcγri和fcγriiia(g1093,描述于wo2017/019565)高度结合的斯托拉多体。
此外,引入多fc治疗剂中的类似的无糖基化突变证明了在一些情况下与多聚化斯托拉多体背景下相同突变的作用完全相反的功能性作用。例如,通过在另外的六聚多fc治疗剂中引入n297a突变来去除297-299序列子处的n-聚糖,完全消除了与所有经典fcγr的结合(blundell等人,《生物化学杂志(j.biol.chem.)》,jbc.m117.795047,2017)。然而,如上所述,第297位处的突变表现出对本文所述的多聚化斯托拉多体结合经典fcγr的能力的可变作用,并导致保持或增强的与fcγri和fcγriib的结合。此外,包括t299a突变的本文所述的多聚化斯托拉多体的无糖基化六聚实施例表现出保持的与所有经典fcγr以及c1q(本文所述的g1098、1126和1127)的结合。技术人员将认识到,第297位、第298位、第299位处的突变或其组合将可能导致fc的糖基化水平降低,因为所有三个位置都包括在糖基化共有序列内。然而,基于单克隆抗体背景下描述的作用或甚至在其它看似相似的多fc治疗剂背景下描述的作用,无法预测多聚化斯托拉多体背景下的这些无糖基化突变的作用。
除了点突变的引入之外,可以使用例如包含特定细胞系或体外酶促修饰的特定蛋白质表达系统来控制碳水化合物或聚糖含量。因此,本发明包含包括fc结构域的斯托拉多体单元(具有获得结构域的天然抗体的天然碳水化合物含量)以及与天然抗体相比具有改变的碳水化合物含量的那些仿生化合物。在另一个实施例中,与对应的亲本斯托拉多体的同源二聚体组分相比,多聚化斯托拉多体的特征在于不同的糖基化模式。例如,本文所述的多聚化斯托拉多体可以包括一个或多个氨基酸突变,其导致fc结构域的无糖基化。在这种实施例中,多聚化斯托拉多体是亲本斯托拉多体的无糖基化变体。
减少单克隆抗体中fc与fcr的结合亲和力的突变可以减少、增加与普通斯托拉多体中的fcr的结合或使其保持不变,其中亲合力的作用可能会或不会超过配体结合减少的作用。通过知晓抗体突变无法预测结果。鉴于单克隆抗体对其fcγr和补体靶标(其可以通过引入突变而上调或下调)具有亲和力,斯托拉多体向fcγr并向补体呈递多价fc,因此更依赖于亲合力来结合其靶标。相反,单克隆抗体通常不具有通过其fc结构域的亲和结合。这些特征突出了这样的事实:斯托拉多体和单克隆抗体从根本上不同,不仅在结构方面,而且在功能和实用性方面。
普通斯托拉多体的优选实施例
本文所述的斯托拉多体提供相对于亲本斯托拉多体增强的补体和/或fcγr结合。因此,本文描述的斯托拉多体是“普通斯托拉多体”,其结合补体级联的一个或多个组分并且还与一种或多种fcγr结合。在特定实施例中,本文所述的普通斯托拉多体令人惊讶地相对于其它普通斯托拉多体(例如,g019或gl-2045)优先形成六聚体、12聚体(例如,六聚体的二聚体)和/或18聚体(例如,六聚体的三聚体),并且与亲本斯托拉多体或亲本斯托拉多体的无糖基化的非六聚变体相比提供增强或保持的补体结合和/或fcγ受体结合。在一些实施例中,本文所述的斯托拉多体包括fc结构域,其中fc结构域包括第299位或第297位处的点突变,并且在本文中被称为“无糖基化突变体”或“无糖基化变体”,因为这些位置的突变改变了iggfc的正常糖基化模式。
具有点突变g236r的gl-2045背景上的斯托拉多体(seqidno:10)在本文中被称为g990。在一些实施例中,g990表现出与fcγri的最小结合,不与fcγriia、fcγriib和fcγriiia的结合(图2a、图2b和图7),以及低c1q结合和不能抑制cdc(图2a)。
包括突变e233p、g236e、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:11)在本文中被称为1103。在一些实施例中,g1103表现出强烈的与fcγri的结合,略微减少的与fcγriia和fcγriiia的结合和与fcγriib的最小结合(图8)。在一些实施例中,g1103表现出与c1q的高度结合和抑制cdc的能力,其中ic50约为5μg/ml。
包括突变e233p、g236d、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:12)在本文中被称为1104。在一些实施例中,g1104表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图9)。在一些实施例中,g1104表现出与c1q的高度结合(图28)和抑制cdc的能力,其中ic50约为5μg/ml。
包括突变e233p、g236n、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:15)在本文中被称为1105。在一些实施例中,g1105表现出强烈的与fcγri的结合和略微减少的与fcγriia、fcγriib和fcγriiia的结合。在一些实施例中,g1105还表现出高c1q结合和抑制cdc的能力。
包括突变e233p、s267q、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:13)在本文中被称为1102。在一些实施例中,g1102表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图10)。在一些实施例中,g1102表现出与c1q的高度结合(图28和图29)和抑制cdc的能力,其中ic50约为7.5μg/ml。
包括突变e233p、s267d、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:14)在本文中被称为1101。在一些实施例中,g1101表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图11)。在一些实施例中,g1101表现出与c1q的高度结合(图28)和抑制cdc的能力,其中ic50约为5μg/ml。
包括突变e233p、s267e、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:16)在本文中被称为1109。在一些实施例中,g1109表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图12)。在一些实施例中,g1109表现出与c1q的高度结合。
包括突变e233p、s267h、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:17)在本文中被称为1125。在一些实施例中,g1125表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图16)。在一些实施例中,g1125表现出与c1q的高度结合和抑制cdc的能力,其中ic50约为5μg/ml。
包括突变e233p、g236d、s267q、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:18)在本文中被称为1111。在一些实施例中,g1111表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图13)。在一些实施例中,g1111表现出与c1q的高度结合和抑制cdc的能力,其中ic50约为5μg/ml。
包括突变e233p、g236q、s267d、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:19)在本文中被称为1114。在一些实施例中,g1114表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图14)。在一些实施例中,g1114表现出与c1q的高度结合和抑制cdc的能力,其中ic50约为5μg/ml。
包括突变e233p、g236d、s267d、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:20)在本文中被称为1117。在一些实施例中,g1117表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合(图15)。在一些实施例中,g1117表现出与c1q的高度结合(图29)和抑制cdc的能力,其中ic50约为5μg/ml。
鉴于shields等人(shields等人,《生物化学杂志(j.biol.chem.)》,276(9):6591(2001)),g1103、1104、1105、1102、1101、1109、1125、1111、1114和1117的上述结果特别令人惊讶,其揭示了第233位或第236位处的突变导致撤消与fcγri、fcγriia、fcγriib和fcγriiia的结合。这些结果进一步突出了在斯托拉多体背景下给定点突变的不可预测性。
包括突变s267q、h268f、s324t和t299a的gl-2045背景上的斯托拉多体(seqidno:21)在本文中被称为1094。令人惊讶的是,在一些实施例中,g1094表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合,尽管包括t299a无糖基化突变(图17)。在一些实施例中,g1094表现出与c1q的高度结合(图28)和抑制cdc的能力,其中ic50约为12.5μg/ml。
包括突变s267d、h268f、s324t和t299a的gl-2045背景上的斯托拉多体(seqidno:22)在本文中被称为1092。令人惊讶的是,在一些实施例中,g1092表现出强烈的与fcγri、fcγriia、fcγriiia和fcγriib的结合,尽管包括t299a无糖基化突变(图18)。在一些实施例中,g1092表现出与c1q的高度结合(图28)和抑制cdc的能力,其中ic50约为10μg/ml。
包括突变s267h、h268f、s324t和t299a的gl-2045背景上的斯托拉多体(seqidno:23)在本文中被称为1107。令人惊讶的是,在一些实施例中,g1107表现出强烈的与fcγri、fcγriia和fcγriib的结合和略微减少的与fcγriiia的结合,尽管包括t299a无糖基化突变(图19)。在一些实施例中,g1107表现出与c1q的高度结合和抑制cdc的能力,其中ic50约为12.5μg/ml。
包括突变s267e、h268f、s324t和t299a的gl-2045背景上的斯托拉多体(seqidno:24)在本文中被称为1068。令人惊讶的是,在一些实施例中,g1068表现出强烈的与fcγri、fcγriia和fcγriib的结合,尽管包括t299a无糖基化突变。g1068还表现出减少的与fcγriiia的结合(图20)。在一些实施例中,g1068表现出与c1q的高度结合(图28)和抑制cdc的能力,其中ic50约为10μg/ml。
包括突变t299a和e430g的gl-2045背景上的斯托拉多体(seqidno:25)在本文中被称为1097。在一些实施例中,g1097可以被称为亲本斯托拉多体的无糖基化非六聚变体。令人惊讶的是,在一些实施例中,g1097表现出强烈的与fcγri、fcγriia、fcγriib和fcγriiia的结合,尽管包括t299a无糖基化突变(图22)。在一些实施例中,g1097表现出比gl-2045亲本斯托拉多体更强的cdc抑制,其中ic50约为20μg/ml。在一些实施例中,g1097令人惊讶地表现出比亲本斯托拉多体(gl-2045)或亲本斯托拉多体的另一种无糖基化变体(g1099)更强的cdc抑制(图31)。
包括突变t299a的gl-2045背景上的斯托拉多体(seqidno:26)在本文中被称为g1099。在一些实施例中,g1099还可以被称为亲本斯托拉多体的无糖基化非六聚变体。令人惊讶的是,在一些实施例中,g1099表现出强烈的与fcγri、fcγriia、fcγriib和fcγriiia的结合,尽管包括t299a无糖基化突变(图21)。在一些实施例中,g1099表现出中等程度的cdc抑制(图31),其中ic50约为30μg/ml。
包括突变e233p、l234v、l235a、s267e、h268f、s324t和第236位处的缺失的gl-2045背景上的斯托拉多体(seqidno:29)在本文中被称为1023。令人惊讶的是,在一些实施例中,g1023表现出强烈的与fcγri、fcγriia、fcγriib和fcγriiia的结合。鉴于shields等人(shields等人,《生物化学杂志(j.biol.chem.)》,276(9):6591(2001)),这些结果特别令人惊讶,其揭示了第233位或第236位处的突变导致撤消与fcγri、fcγriia、fcγriib和fcγriiia的结合。这些结果进一步突出了在斯托拉多体背景下给定点突变的不可预测性。在一些实施例中,g1023与c1q强烈结合并抑制cdc。
包括突变l234a、l235a、s267e、h268f和s324t的gl-2045背景上的斯托拉多体(seqidno:28)在本文中被称为1032。令人惊讶的是,在一些实施例中,g1032表现出强烈的与fcγri、fcγriia、fcγriib和fcγriiia的结合,以及强c1q结合(图28)和cdc抑制。考虑到l234a/l235a突变的存在,这些结果特别令人惊讶,其先前已被描述为撤消c1q结合(参见wo2015/132364;arduin等人,《分子免疫学(molecularimmunology)》,65(2):456-463(2015);boyle等人,《免疫(immunity)》,42(3):580-590(2015))。
包括突变s267e、h268f、s324t和l328f的g019背景上的斯托拉多体(seqidno:27)在本文中被称为1049。在一些实施例中,g1049表现出强烈的与fcγri、fcγriia和fcγriib的结合和略微减少的fcγriiia结合(图6),以及强c1q结合和cdc抑制(图5a)。考虑到l234a/l235a突变的存在,这些结果是令人惊讶的,其先前已被描述为撤消c1q结合(参见wo2015/132364)。此外,先前已经描述了l234f突变抑制与fcγriiia的结合。尽管g1049与fcγriiia的结合略微减少,但是在多聚化斯托拉多体背景下未观察到该作用。
表1中提供了本公开所囊括的示例性普通斯托拉多体的氨基酸序列。
表1.示例性普通斯托拉多体
*对于斯托拉多体g1023,第236位处的g的缺失被示出为删除线/粗体文本。
六聚普通斯托拉多体
在一些实施例中,本文所述的普通斯托拉多体相对于其它普通斯托拉多体(例如,g019或gl-2045)优选地形成六聚经多聚化的斯托拉多体。这些六聚经多聚化的斯托拉多体提供六个结合位点结合,与多聚c1q复合物的六个头部互补。分离的c1q头部相当弱地与抗体的fc部分,其中亲和力为100μm(hughes-jones和gardner,《分子免疫学(molec.immun.)》,16,697-701(1979))。然而,抗体与抗原表面上的多个表位结合使抗体聚集并促进几个c1q头部的结合,导致约为10nm的增强的亲和力(burton等人,《分子免疫学(molec.immun.)》,22,161-206(1985))。以这种方式,本发明的六聚仿生物质和组合物可以表现出保持或增强的与c1q的结合亲合力或亲和性,表现为补体汇,即使这些斯托拉多体没有fab(因此没有fc的fd部分)并且无法与聚集的抗体一样在抗原表面上结合多个表位。本发明的六聚仿生物质,类似于ivig中聚集体的fc部分或类似于聚集抗体,可以类似地以高亲和性结合补体组分c1q、c4、c4a、c3、ic3b、c3a、c3b、c5或c5a,而完整的分离免疫球蛋白的fc部分对于这些补体组分具有低结合亲合力并无亲和性。因此,一种经多聚化的六聚斯托拉多体可以具有比当量单位的当前可用疗法更有效的对补体激活调节的作用。
先前已经认为,增加的补体c1q结合和激活依赖于与病原体的直接结合或依赖于在先的抗体fab与靶抗原的结合和随后的c1q结合(c.a.janeway等人,《免疫生物学:健康与疾病的免疫系统(immunobiology:theimmunesysteminhealthanddisease.)》,第5版)。然而,据报道,抗cd38单克隆抗体中第345位处的单点突变(e435r)使调理细胞的c1q亲合性增加5倍,并且在没有与病原体的直接结合和先前的与cd38的结合的情况下使cdc增加10倍。该突变与430和440处的点突变(e430g、s440y)组合,也直接激活人血清中的补体(diebolder等人,《科学(science)》,343,1260-1263(2014))。这些数据表明抗体fab与靶细胞上表达的靶抗原的结合不是经典补体激活所需的第一步,并突出了调节补体激活的潜在治疗机会,而不依赖于抗体与靶细胞的结合。diebolder等人进一步表明,e435r/e430g/s440y三重突变体增加的补体激活部分是由于突变体抗体在溶液中形成六聚体的能力,因此形成六聚c1q蛋白的互补对应物。还已报道人gp-120抗体(igg1-b12)和人2g12抗体的六聚排列(saphire等人,《晶体学报d(actacrystallogrd.)》,57,168-171(2001);saphire等人,《科学(science)》,293,1155-1159(2001);wu等人,《细胞报告(cellrep.)》,5,1443-1455(2013))。
另外,已经描述了通过突变天然igg1fc序列的第309位或第310位而制备的fc六聚体(美国专利公开第2015/0218236号)。通过这些特异性点突变的作用,fc和作为尾部的igmch4结构域被示出聚集在一起以形成六聚结构,其被认为增加了对fcγr的亲合性。然而,这些化合物具有降低的c1q结合或没有fcγr的优先c1q结合,并且通常无法抑制cdc。wo2015/132364还描述了通过第309位和/或第310位的突变形成并且包含igmch4尾部的六聚化合物。wo2015/132364进一步描述了预测具有不同功能的一系列突变,其主要基于描述单克隆抗体背景下的特异性点突变的文献。然而,如本文所述,尽管在单克隆抗体背景下很好地表征了这些突变中的某些突变,但是它们在经多聚化的斯托拉多体背景下产生了截然不同的作用。
在一些实施例中,本文所述的仿生化合物令人惊讶地主要形成六聚体、12聚体(例如,六聚经多聚化的斯托拉多体的二聚体)和/或18聚体(例如,六聚经多聚化的斯托拉多体的六聚体的三聚体)。在这种实施例中,可以基本上纯化这些经多聚化的斯托拉多体组合物以去除低阶多聚体(例如,同源二聚体、和/或二聚体、和/或三聚体、和/或四聚体、和/或五聚体,如图27中所示),其可以以低浓度存在,以及以去除大于八聚体的多聚体。在一些实施例中,纯化经多聚化的斯托拉多体组合物的六聚级分以产生六聚经多聚化的斯托拉多体的富集的或基本上均质的组合物,其具有保持和/或增强的与fcγr和/或补体蛋白(例如,c1q)的结合。在一些实施例中,纯化经多聚化的斯托拉多体组合物的12聚体级分以产生12聚体经多聚化的斯托拉多体的富集的或基本上纯的同源组合物,其具有保持或增强的与fcγr和/或补体蛋白(例如,c1q)的结合。在一些实施例中,纯化经多聚化的斯托拉多体组合物的18聚体级分以产生18聚体经多聚化的斯托拉多体的富集的或基本上纯的同源组合物,其具有保持或增强的与fcγr和/或补体蛋白(例如,c1q)的结合。
本发明人发现,在多聚化斯托拉多体单元背景下的点突变t299a/e345r、t299a/e430g/s440y和t299a/e345r/e430g/s440y导致六聚经多聚化的斯托拉多体的形成,和相对于天然igg、亲本斯托拉多体或亲本斯托拉多体的无糖基化非六聚变体的增加的补体结合。因此,在一个方面,本公开提供了包括点突变t299a和点突变e430g、e345r和/或s440y中的一个或多个的多聚化斯托拉多体单元及其经多聚化的斯托拉多体。在一些实施例中,本公开进一步提供了包括位置t299a、e430g、e345r和s440y处的点突变的多聚化斯托拉多体单元及其经多聚化的斯托拉多体。在一些实施例中,本公开提供了包括位置t299a和e345r处的点突变的多聚化斯托拉多体单元及其经多聚化的斯托拉多体。在一些实施例中,本公开提供了包括位置t229a、e430g和s440y处的点突变的多聚化斯托拉多体单元及其经多聚化的斯托拉多体。
在gl-2045背景上具有第299位、第430位和第440位处的点突变的六聚体斯托拉多体(seqidno:30)在本文中被称为g1098。在一些实施例中,g1098表现出比亲本斯托拉多体(gl-2045)或亲本斯托拉多体的非六聚无糖基化变体(例如,g1099和g1097)更强的cdc抑制(图31),并且保持与fcγri、fcγriib、fcγriia和fcγriiia的结合(图23)。
在gl-2045背景上具有第299位和第345位处的点突变的六聚斯托拉多体(seqidno:31)在本文中被称为g1127。在一些实施例中,g1127表现出比亲本斯托拉多体(gl-2045)或亲本斯托拉多体的非六聚无糖基化变体(例如,g1099和g1097)更强的cdc抑制(图31),并且保持与fcγri、fcγriib、fcγriia和fcγriiia的结合(图25)。
在gl-2045背景上具有第299位、第345位、第430位和第440位处的点突变的六聚斯托拉多体(seqidno:32)在本文中被称为g1126。在一些实施例中,g1126表现出比亲本斯托拉多体(gl-2045)或亲本斯托拉多体的非六聚无糖基化变体(例如,g1099和g1097)更强的cdc抑制(图31),并且保持与fcγri、fcγriib、fcγriia和fcγriiia的结合(图24)。表2中示出了示例性普通斯托拉多体的氨基酸序列。已经突变的氨基酸位置以粗体和下划线标出。
表2.示例性六聚斯托拉多体
本领域技术人员将理解,当级分包含特定分子量的斯托拉多体时,所有具有较高分子量的斯托拉多体也可以被纯化(例如,同源二聚体及以上,同源二聚体及以上的二聚体,三聚体及以上,六聚体及以上,或12聚体及以上,或18聚体及以上)。技术人员还将理解,最大分子量的级分也可以用标准下游制造工艺纯化,留下例如18聚体及以下或12聚体及以下。蛋白质纯化的标准下游制造工艺是本领域已知的,并且可以包含但不限于尺寸排阻色谱、离子交换色谱、自由流动电泳、亲和色谱和/或高效液相色谱(hplc)。这些方法可以用于选择性纯化多聚体(包含六聚体、12聚体和/或18聚体)的任何组合,并去除较低阶的多聚体(例如,同源二聚体、二聚体、三聚体、四聚体和/或五聚体)的任何组合。例如,在一些实施例中,可以纯化令人惊讶地形成六聚体、12聚体或18聚体的化合物的组合物以仅去除同源二聚体,产生经多聚化的斯托拉多体的异质组合物。在一些实施例中,可以纯化令人惊讶地形成六聚体、12聚体或18聚体的化合物的组合物以去除同源二聚体、二聚体、三聚体、四聚体和五聚体,产生六聚、12聚体和18聚体经多聚化的斯托拉多体的异质组合物。
在一些实施例中,纯化经多聚化的斯托拉多体组合物(即由6-12个多聚化斯托拉多体单元构成的经多聚化的斯托拉多体)的六聚至12聚体级分,以产生6聚体至12聚体经多聚化的斯托拉多体的异质组合物,其具有保持和/或增强的与fcγr和/或补体蛋白(例如,c1q)的结合。在一些实施例中,纯化经多聚化的斯托拉多体组合物的六聚和12聚体级分,以产生六聚和12聚体经多聚化的斯托拉多体的富集的或基本上纯的异质组合物,其具有保持和/或增强的与fcγr和/或或补体蛋白(例如,c1q)的结合。在一些实施例中,纯化经多聚化的斯托拉多体组合物(即,由6-18个多聚化斯托拉多体单元构成的经多聚化的斯托拉多体)的六聚至18聚体级分,以产生6聚体至18聚体经多聚化的的异质组合物,其具有保持和/或增强的与fcγr和/或补体蛋白(例如,c1q)结合。在一些实施例中,纯化经多聚化的斯托拉多体组合物的六聚、12聚体和18聚体级分,以产生六聚、12聚体和18聚体经多聚化的斯托拉多体的富集的或基本上纯的异质组合物,其具有保持和/或增强的与fcγr和/或补体蛋白(例如,c1q)的结合。在一些实施例中,纯化经多聚化的斯托拉多体组合物的12聚体级分和18聚体级分,以产生12聚体和18聚体经多聚化的斯托拉多体的富集的或基本上纯的异质组合物,其具有保持或增强的与fcγr和/或补体蛋白(例如,c1q)的结合。
在一些实施例中,经多聚化的斯托拉多体包括6聚体、12聚体、18聚体或其任何组合,其功能类似于gl-2045。在一些实施例中,相对于亲本仿生物质(gl-2045),本文所述的六聚(和/或12聚体和/或18聚体)经多聚化的斯托拉多体化合物表现出保持或增强的与fcγr和/或补体(例如,c1q)的结合,并且具有另外的以下优点:与gl-2045相比具有显著更高的平均分子量并且具有更少的不同分子量的多聚体。具体地,本文所述的经多聚化的斯托拉多体化合物(例如,1098、1126和1127)以比gl-2045高得多的水平(占总蛋白的百分比)形成六聚体水平及以上的多聚体(图27)。因此,本发明的化合物不与较低阶的多聚体一起施用,所述较低阶的多聚体在结合c1q和抑制cdc方面活性较低。因此,相对于gl-2045,本发明的化合物可能需要较低的剂量和/或较少的纯化。
“免疫调节活性”、“调节免疫应答”、“调节免疫系统”和“免疫调节”是指通过改变一种或多种免疫细胞(包含其细胞类型中的一种细胞类型的成熟或细胞类型成熟为其它细胞类型)的活性、能力和相对数量来改变免疫系统。例如,免疫调节可以是免疫应答的抑制或激活。例如,在一个方面,免疫调节可以是指诱导t细胞或b细胞中的无应答性或耐受性。如本文使用,术语“耐受性”是指t细胞或b细胞中或整个免疫应答中的状态,其中t细胞或b细胞或其它免疫细胞不响应其同源抗原或不响应其通常会响应的抗原、表位或其它信号。作为另一个实例,记忆b细胞的免疫调节可以导致某些记忆b细胞的选择性凋亡,同时伴随特定抗体产生的减少。作为另一个实例,免疫调节活性可以导致促炎细胞因子或通常在自身免疫性疾病中升高的细胞因子(例如,il-6和il-8)的减少。作为另一个实例,免疫调节活性可以导致nkt细胞的激活,随后分泌和切割tgf-β。阻断免疫细胞受体以阻止受体激活也囊括在“免疫调节”中,并且可以被单独称为“抑制性免疫调节”。在另一方面,免疫调节可以是免疫应答的增强或激活。例如,免疫调节可以是指t细胞或b细胞的激活。作为另一个实例,未成熟单核细胞的免疫调节可以产生更多成熟单核细胞、树突细胞、巨噬细胞或破骨细胞的群体,所有这些都衍生自未成熟的单核细胞。作为另一个实例,nk细胞的免疫调节可以导致增强的adcc。作为另一个实例子,免疫调节活性可以导致具有表型的细胞群的增加,该表型以其它方式可能不会以高水平表达,例如cd8β+/cd11c+细胞。例如,免疫细胞受体可以通过免疫活性仿生物质结合并激活细胞内信号传导以诱导各种免疫细胞改变,其分别被称为“激活免疫调节”。
树突细胞的调节可以促进或抑制抗原呈递给t细胞,例如通过诱导cd86和/或cd1a在树突细胞表面上的表达。cd1a是mhc类i相关糖蛋白,其在抗原呈递细胞,特别是树突细胞的表面上表达。cd1a参与脂质抗原向t细胞的呈递。cd86也在抗原呈递细胞的表面上表达,并为t细胞提供共刺激作用。cd86是t细胞表面上cd28和ctla-4的配体,分别发送激活和抑制信号。因此,cd86及其同源受体的表达水平决定了是否会诱导耐受性或特异性免疫应答。在一个优选实施例中,本发明的斯托拉多体能够调节免疫应答,部分是通过诱导cd86和cd1a在抗原呈递细胞,特别是树突细胞的表面上的表达。
单核细胞成熟的调节是指单核细胞分化成成熟的树突细胞(dc)、巨噬细胞或破骨细胞。可以调节分化以加速成熟的速率或方向和/或增加经历分化的单核细胞的数量。可替代地,可以在分化速率和/或经历分化的细胞数量方面减少分化。
药物组合物
本文所述的斯托拉多体组合物的施用将经由任何常用途径,即口服、胃肠外或局部施用。示例性途径包含但不限于口服、鼻腔、口腔、直肠、阴道、眼科、皮下、肌肉内、腹膜内、静脉内、动脉内、瘤内、脊柱、鞘内、关节内、动脉内、蛛网膜下、舌下、口腔粘膜、支气管、淋巴、子宫内、皮下、肿瘤内、整合在可植入装置(例如,缝合线)上或可植入装置(例如,可植入聚合物)、硬膜内、皮质内或真皮。这种组合物通常作为如本文所述的药学上可接受的组合物施用。在一个优选实施例中,分离斯托拉多体静脉内或皮下施用。
如本文使用的术语“药学上可接受的载剂”包含任何和所有溶剂、分散介质、包衣、抗细菌和抗真菌剂、等渗和吸收延迟剂等。这种用于药物活性物质的介质和试剂的用途是本领域熟知的。除非任何常规的介质或试剂与本发明的载体或细胞不相容,否则考虑其在治疗组合物中的用途。补充的活性成分也可以掺入组合物中。
本发明的斯托拉多体组合物可以配制成中性或盐形式。药学上可接受的盐包含酸加成盐(与蛋白质的游离氨基基团形成)并且是与无机酸(诸如例如盐酸或磷酸)或有机酸(例如,乙酸、草酸、酒石酸、扁桃酸等)形成的。与游离羧基基团形成的盐也可以衍生自无机碱(诸如例如氢氧化钠、氢氧化钾、氢氧化铵、氢氧化钙或氢氧化铁)和有机碱(例如,异丙胺、三甲胺、组氨酸、普鲁卡因等)。
通过将所需量的斯托拉多体掺入适当的溶剂(按需含有上面列举的各种其它成分)并随后过滤灭菌来制备无菌可注射溶液。在一些实施例中,配制无菌可注射溶液用于肌肉内、皮下或静脉内施用。通常,通过将各种灭菌活性成分掺入无菌媒剂中来制备分散体,所述无菌媒剂含有基础分散介质和来自上面列举的那些的所需其它成分。在用于制备无菌可注射溶液的无菌粉末的情况下,优选的制备方法是真空干燥和冷冻干燥技术,其从其先前无菌过滤的溶液中产生活性成分和任何另外的所需成分的粉末。
此外,一个实施例是一种适于口服施用的斯托拉多体组合物,并且在含有或不含惰性稀释剂的药学上可接受的载剂中提供。载剂应是可同化的或可食用的,并且包含液体、半固体(即糊状物)或固体载剂。除非任何常规的介质、试剂、稀释剂或载剂对接受者或对其中含有的斯托拉多体制剂的治疗效果有害,否则其在用于实施本发明方法的口服施用的斯托拉多体组合物中的用途是适当的。载剂或稀释剂的实例包含脂肪、油、水、盐溶液、脂质、脂质体、树脂、粘合剂、填充剂等,或其组合。如本文使用的术语“口服施用”包含口服、口腔、肠内或胃内施用。
在一个实施例中,所述斯托拉多体组合物以任何方便和实用的方式(即通过溶解、混悬、乳化、混合、包封、微囊化、吸收等)与载剂组合。这些程序对于本领域技术人员来说是常规的。
在一个具体实施例中,粉末形式的斯托拉多体组合物与半固体或固体载剂充分组合或混合。混合可以以任何方便的方式进行,例如研磨。还可以在混合过程中加入稳定剂,以便保护组合物免受治疗活性的损失(即胃中的变性)。用于口服施用组合物的稳定剂的实例包含缓冲剂、胃酸分泌的拮抗剂、氨基酸(例如,甘氨酸和赖氨酸)、碳水化合物(例如,葡萄糖、甘露糖、半乳糖、果糖、乳糖、蔗糖、麦芽糖、山梨糖醇、甘露醇等)、蛋白水解酶抑制剂等。更优选地,对于口服施用组合物,稳定剂还可以包含胃酸分泌的拮抗剂。
此外,与半固体或固体载剂组合的口服给施用斯托拉多体组合物可以进一步配制成硬壳或软壳明胶胶囊、片剂或丸剂。更优选地,明胶胶囊、片剂或丸剂是肠溶包衣的。肠溶包衣防止组合物在ph为酸性的胃或肠上部中的变性。参见即美国专利第5,629,001号。在到达小肠时,其中的碱性ph溶解包衣并允许组合物释放以与肠细胞相互作用,例如派尔集合淋巴结m细胞。
在另一个实施例中,将粉末形式的斯托拉多体组合物与产生包封免疫活性仿生物质的纳米颗粒或与免疫活性仿生物质连接的材料充分组合或混合。每个纳米颗粒的尺寸小于或等于100微米。纳米颗粒可以具有粘膜粘附性质,其允许不具有口服生物可利用性的免疫活性仿生物质的胃肠吸收。
在另一个实施例中,在有或没有稳定剂的情况下,将粉末状组合物与液体载剂(例如即水或盐溶液)组合。
可以使用的特定的斯托拉多体制剂是免疫活性仿生蛋白质在基于低渗磷酸盐的不含钾的缓冲液中的溶液,其中缓冲液的组成如下:6mm磷酸二氢钠一水合物、9mm磷酸氢二钠七水合物、50mm氯化钠,ph7.0+/-0.1。低渗缓冲液中免疫活性仿生蛋白质的浓度可以为10μg/ml到100mg/ml。该制剂可以经由任何施用途径施用,例如但不限于静脉内施用。
此外,可以将与半固体载剂组合的用于局部施用的斯托拉多体组合物进一步配制成乳膏或凝胶软膏。用于形成凝胶软膏的优选载剂是凝胶聚合物。用于制备本发明凝胶组合物的优选聚合物包含但不限于卡波姆、羧甲基纤维素和普朗尼克聚合物。具体地,将粉末状fc多聚体组合物与含有聚合剂(例如,卡波姆980)的含水凝胶以0.5%至5%wt/体积的强度组合,涂抹于皮肤以治疗皮肤上或皮肤下的疾病。如本文使用的术语“局部施用”包含涂抹于真皮、表皮、皮下或粘膜表面。
此外,可以将斯托拉多体组合物配制成用于皮下或真皮下植入的聚合物。用于可植入药物输注聚合物的优选制剂是通常被认为是安全的试剂,并且可以包含例如交联葡聚糖(samanthahart,理学硕士论文,“从新型交联葡聚糖凝胶中洗脱抗生素:定量(elutionofantibioticsfromanovelcross-linkeddextrangel:quantification)”,弗吉尼亚工学院和州立大学,2009年6月8日)、葡聚糖-酪胺(jin等人(2010),《组织工程部分a(tissueeng.parta.)》,16(8):2429-40)、葡聚糖-聚乙二醇(jukes等人(2010),《组织工程部分a(tissueeng.parta.)》,16(2):565-73)、或葡聚糖-戊二醛(brondsted等人(1998),《受控释放杂志(j.controlledrelease)》,53:7-13)。本领域技术人员将知道,可以形成许多类似的聚合物和水凝胶,其中掺入固定在聚合物或水凝胶中的斯托拉多体,并且将孔径控制为所需的直径。
在配制时,溶液以与剂量配方相容的方式并且以治疗有效量施用,以导致症状的改善或补救。该制剂易于以多种剂型施用,例如可吸收溶液、药物释放胶囊等。剂量的一些变化可以根据所治疗的受试者的病状而发生。在任何情况下,负责施用的人可以确定个体受试者的适当剂量。此外,对于人类施用,制剂符合fda标准和其它类似监管机构要求的无菌性、一般安全性和纯度标准。
施用途径将自然地随所治疗疾病的位置和性质而不同,并且可以包含例如真皮内、经真皮、真皮下、肠胃外、鼻腔、静脉内、肌肉内、鼻内、皮下、经皮、气管内、腹膜内、肿瘤内、灌注、灌洗、直接注射和口服施用。
在一个实施例中,斯托拉多体静脉内、皮下、口服、腹膜内、舌下、口腔、经真皮、直肠、通过真皮下植入或肌肉内施用。在特定实施例中,斯托拉多体静脉内、皮下或肌肉内施用。在一个实施例中,斯托拉多体以约0.01mg/kg到约1000mg/kg的剂量施用。在另一个实施例中,斯托拉多体以约0.1mg/kg到约100mg/kg施用。在又一个实施例中,斯托拉多体以约0.5mg/kg到约50mg/kg施用。在再一个实施例中,斯托拉多体以约1mg/kg到约25mg/kg施用。在再一个实施例中,斯托拉多体以约5mg/kg到约15mg/kg施用。该斯托拉多体可以至少每天、每周、每两周或每月施用一次。可以使用两阶段剂量方案,其中第一剂量阶段包括第二剂量阶段的约0.1%到约300%。
在另一个实施例中,在施用一种或多种另外的药物和/或治疗剂之前、期间或之后施用斯托拉多体。在另一个实施例中,另外的药物活性剂包括类固醇;生物抗自身免疫药物,例如单克隆抗体、融合蛋白或抗细胞因子;非生物抗自身免疫药物;免疫抑制剂;抗生素;和抗病毒剂;细胞因子;或其它能够充当免疫调节剂的试剂。在又一个实施例中,类固醇是强的松、强的松龙、可的松、地塞米松、莫米松、睾酮、雌激素、氧雄龙、氟替卡松、布地奈德、倍氯米松、沙丁胺醇或左旋沙丁胺醇。在又一个实施例中,单克隆抗体是依库丽单抗、英夫利昔单抗、阿达木单抗、利妥昔单抗、托珠单抗、戈利木单抗、奥法木单抗、ly2127399、贝利单抗、维妥珠单抗、美泊利单抗、耐昔妥珠单抗、纳武单抗、地努妥昔单抗(dinutuximab)、苏金单抗、依伏库单抗、博纳吐单抗、帕博利珠单抗、雷莫芦单抗、维多珠单抗、司妥昔单抗、奥滨尤妥珠单抗、阿多曲妥珠单抗、瑞西巴库单抗、帕妥珠单抗、本妥昔单抗、依匹单抗、地诺单抗、卡那单抗、尤特克单抗、卡妥索单抗、兰尼单抗、帕尼单抗、那他珠单抗、贝伐单抗、西妥昔单抗、依法利珠单抗、奥马珠单抗、托依妥单抗-i131(toitumomab-i131)、阿仑单抗、吉妥珠单抗、曲妥珠单抗、帕利珠单抗、巴司利单抗(basilixumab)、达克珠单抗、阿昔单抗、木罗诺单抗(murononomab)或赛妥珠单抗。在又一个实施例中,融合蛋白是依那西普或阿巴西普。在又一个实施例中,抗细胞因子生物物质是阿那白滞素。在又一个实施例中,抗风湿非生物药物是环磷酰胺、甲氨蝶呤、硫唑嘌呤、羟氯喹、来氟米特、米诺环素、有机金化合物、弗司马替尼(fostamatinib)、托法替尼、依托考昔或柳氮磺吡啶。在又一个实施例中,免疫抑制剂是环孢菌素a、他克莫司、西罗莫司、吗替麦考酚酯、依维莫司、okt3、抗胸腺细胞球蛋白、巴利昔单抗、达克珠单抗(daclizumumab)或阿仑单抗。在又一个实施例中,在施用化学治疗剂之前、期间或之后施用斯托拉多体。在又一个实施例中,当一起施用时,斯托拉多体和另外的治疗剂表现出治疗协同作用。在一个实施例中,在施用另外的治疗剂之前施用斯托拉多体。在另一个实施例中,在施用另外的治疗剂的同时施用斯托拉多体。在又一个实施例中,在施用另外的治疗剂之后施用斯托拉多体。
在一个实施例中,将斯托拉多体共价固定地施用于可植入装置。在一个实施例中,将斯托拉多体固定到缝合线上。在另一个实施例中,将斯托拉多体固定到移植物或支架上。在另一个实施例中,将斯托拉多体固定到心脏瓣膜、整形外科关节置换物或植入的电子导线上。在另一个实施例中,将斯托拉多体固定并埋入可植入基质内。在一个优选实施例中,将斯托拉多体固定并埋入可植入水凝胶中。在一个实施例中,水凝胶由葡聚糖、聚乙烯醇、聚丙烯酸钠或丙烯酸酯聚合物构成。在另一个实施例中,将斯托拉多体固定在水凝胶中,所述水凝胶的孔径足够大以允许免疫细胞进入与固定的斯托拉多体相互作用并然后返回循环。在另一个实施例中,水凝胶的孔径为5到50微米。在一个优选实施例中,水凝胶的孔径为25-30微米。
在另一个实施例中,施用斯托拉多体以治疗具有物种特异性或嵌合性斯托拉多体分子的人类、非人灵长类动物(例如,猴子、狒狒和黑猩猩)、小鼠、大鼠、牛科动物、马、猫、狗、猪、兔、山羊、鹿、绵羊、雪貂、沙鼠、豚鼠、仓鼠、蝙蝠、鸟类(例如,鸡、火鸡和鸭)、鱼类和爬行动物。在另一个实施例中,人类是成人或儿童。在又一个实施例中,施用斯托拉多体以预防补体介导的疾病。在另一个实施例中,施用斯托拉多体以防止伴侣动物和家畜中的疫苗相关自身免疫性病状。
如本文使用的术语“肠胃外施用”包含任何施用形式,其中化合物被吸收到受试者体内而不涉及经由肠吸收。用于本发明的示例性肠胃外施用包含但不限于肌肉内、静脉内、腹膜内、肿瘤内、眼内、鼻腔或关节内施用。
此外,本发明的斯托拉多体可以任选地在另一种药物试剂之前、期间或之后施用。
以下是特定示例性疾病的各种药物制剂类别和优选施用途径的具体实例:
口腔或舌下可溶性片剂:心绞痛、结节性多动脉炎。
静脉内、肌肉内或皮下:重症肌无力、溶血性尿毒症综合症(hus)、非典型溶血性尿毒症综合症(ahus)、阵发性睡眠性血红蛋白尿症(pnh)、膜性肾病、视神经脊髓炎、抗体介导的同种异体移植物排斥、狼疮性肾炎、膜增生性肾小球肾炎(mpgn)、特发性血小板减少性紫癜、包涵体肌炎、副蛋白血症性igm脱髓鞘性多发性神经病、坏死性筋膜炎、天疱疮、坏疽、皮肌炎、肉芽肿、淋巴瘤、败血症、再生障碍性贫血、多系统器官衰竭、意义不明的多发性骨髓瘤和单克隆丙种球蛋白病、慢性炎性脱髓鞘性多发性神经根神经病、炎性肌病、血栓性血小板减少性紫癜、肌炎、贫血、瘤形成、溶血性贫血、脑炎、脊髓炎、脊髓病(尤其与人类t细胞嗜淋巴细胞病毒-1相关)、白血病、多发性硬化症和视神经炎、哮喘、表皮坏死松解症、兰伯特-伊顿肌无力综合症、重症肌无力、神经病、葡萄膜炎、格林-巴利综合症、移植物抗宿主病、僵人综合症、伴抗yo抗体的副肿瘤性小脑变性、伴抗hu抗体的副肿瘤性脑脊髓炎和感觉神经病、系统性血管炎、系统性红斑狼疮、自身免疫性糖尿病神经病、急性特发性自主神经功能失调神经病、伏格特-小柳-原田三氏综合症、多灶性运动神经病、与抗/gml相关的下运动神经元综合症、脱髓鞘、膜增生性肾小球肾炎、心肌病、川崎病、类风湿性关节炎和伊文氏综合症im-itp、cidp、ms、皮肌炎、重症肌无力、肌肉萎缩症。如本文使用的术语“静脉内施用”包含经由静脉内注射或输注将本发明的化合物或组合物递送至全身循环的所有技术。
真皮凝胶、洗液、乳膏或贴片:白癜风、带状疱疹、痤疮、唇炎。
直肠栓剂、凝胶或输注液:溃疡性结肠炎、痔疮炎症。
口服丸剂、锭剂、胶囊剂或肠溶包衣剂:克罗恩病、口炎性腹泻、肠易激综合症、炎性肝病、巴雷特食管。
皮质内:癫痫、阿尔茨海默氏病、多发性硬化症、帕金森病、亨廷顿氏舞蹈病。
腹腔内输注或植入:子宫内膜异位。
阴道内凝胶或栓剂:细菌性、滴虫性或真菌性阴道炎。
医疗装置:涂覆在冠状动脉支架、假体关节上。
普通斯托拉多体的治疗应用
在一个实施例中,提供了一种用于治疗或预防疾病或病状(例如,自身免疫性疾病、炎性疾病或补体介导的疾病或病状)的方法,其包含向有需要的受试者施用包括igg1fc结构域和多聚化结构域的斯托拉多体。在一些实施例中,实施例,斯托拉多体优先形成六聚体。在一些实施例中,与天然免疫球蛋白fc、亲本斯托拉多体或亲本斯托拉多体的无糖基化变体相比,斯托拉多体表现出增强的fcγr和/或补体结合。
基于合理的设计和体外和体内验证,本发明的斯托拉多体将作为重要的生物药物用于治疗炎性疾病和病症,以及用于改变多种其它背景下的免疫功能,例如用于过敏、癌症、自身免疫性疾病、传染性疾病和炎性疾病的生物免疫疗法。适用于用本文公开的免疫活性仿生物质治疗的医学病状包含由补体激活或补体介导的效应子功能(包含增加的或不适当的补体活性)引起或与其相关的任何疾病。这些医学病状包含目前或之前已经用补体结合药物(例如,依库丽单抗)治疗的那些。依库丽单抗与补体蛋白c5(经典补体途径中c1和c1q下游的补体蛋白)结合,抑制其切割和随后的补体介导的细胞裂解。本发明的仿生物质为本领域已知的其它补体结合药物提供了安全有效的替代方案。例如,在一些实施例中,本发明的仿生物质结合c1q,即经典补体途径的c1复合物中的第一亚单元。适用于用免疫活性仿生物质治疗的医学病状包含但不限于重症肌无力、溶血性尿毒症综合症(hus)、非典型溶血性尿毒症综合症(ahus)、阵发性睡眠性血红蛋白尿症(pnh)、膜性肾病、视神经脊髓炎、抗体介导的同种异体移植物排斥、狼疮性肾炎、黄斑变性、镰状细胞病和膜增生性肾小球肾炎(mpgn)。适用于用本文所述的免疫活性仿生物质治疗的另外的医学病状包含目前常规用广泛免疫抑制疗法(包含hivig)治疗的那些或其中已经发现hivig在临床上有用的那些,例如自身免疫性血细胞减少、慢性炎性脱髓鞘性多发性神经病、格林-巴利综合症、重症肌无力、抗因子viii自身免疫性疾病、皮肌炎、血管炎和葡萄膜炎(参见vandermeche等人,《新英格兰医学杂志(n.engl.j.med.)》,326,1123(1992);p.gajdos等人,《柳叶刀i(lanceti)》,406(1984);sultan等人,《柳叶刀ii(lancetii)》,765(1984);dalakas等人,《新英格兰医学杂志(n.engl.j.med.)》,329,1993(1993);jayne等人,《柳叶刀(lancet)》,337,1137(1991);lehoang等人,《眼部免疫学和炎症(ocul.immunol.inflamm.)》,8,49(2000)),和其中可以使用或已经在临床使用中使用的单克隆抗体的那些癌症或炎性疾病病状。
可以通过作为本发明的主题的化合物有效治疗的那些中包含的病状包含细胞因子网络失衡的炎性疾病、由致病性自身抗体或自身攻击性t细胞介导的自身免疫性病症、或慢性复发性自身免疫性、炎性或传染性疾病或过程的急性或慢性期。在某些实施例中,本发明的斯托拉多体可以用于控制、管理、预防或治疗受试者中的疼痛。“疼痛”是指受试者体内的不舒服感和/或不愉快感。疼痛严重程度可以从轻微到严重,疼痛频率可以是偶尔、很少、频繁或持续。此外,疼痛症状可被分类为急性疼痛或慢性疼痛。在一些实施例中,疼痛可以是伤害性疼痛(即,由组织损伤引起的疼痛)、神经性疼痛或心因性疼痛。在一些实施例中,伤害性疼痛可以由疾病发病机理引起的创伤、感染或损伤引起。在一些实施例中,疼痛由疾病(例如,本文所述的炎性疾病、自身免疫性疾病、补体介导的疾病或癌症)引起或与其相关。在特定实施例中,本发明的斯托拉多体可以用于治疗与本文所述的疾病或病症相关或由其引起的疼痛。
此外,具有涉及补体的炎性组分的其它医学病状将受益于用斯托拉多体治疗,例如肌萎缩侧索硬化、亨廷顿氏舞蹈病、阿尔茨海默氏病、帕金森病、心肌梗塞、中风、乙型肝炎、丙型肝炎、人类免疫缺陷病毒相关炎症、肾上腺脑白质营养不良和癫痫症(尤其是被认为与病毒后脑炎相关的那些,包含拉斯姆森综合症、韦斯特综合症和伦诺克斯-加斯托二氏综合症)。
使用本文所述的分离斯托拉多体进行治疗的一般方法是向患有疾病或病状的受试者施用治疗有效量的分离的免疫活性仿生物质以实现治疗。在一些实施例中,疾病或病状可以大致分类为细胞因子网络失衡的炎性疾病、由致病性自身抗体或自身攻击性t细胞介导的自身免疫性病症、或慢性复发性疾病或过程的急性或慢性期。
如本文使用的术语“治疗(treating/treatment)”是指向受试者施用治疗有效量的本发明的斯托拉多体,使得受试者的疾病或病状或者疾病或病状的症状得到改善。改善是疾病或病状或者疾病或病状的症状的任何改善或补救。改善是可观察或可测量的改善,或者可以是对受试者的总体幸福感的改善。因此,本领域技术人员认识到,治疗可以改善疾病病状,但是可能不是疾病的完全治愈方法。具体地,受试者中的改善可以包含以下一种或多种:炎症减少;炎症实验室标志物(如c-反应蛋白)减少;自身免疫性减少,如以下一项或多项所证明:自身免疫性标志物(例如,自身抗体)或血小板计数、白细胞计数或红细胞计数的改善,皮疹或紫癜减少,虚弱、麻木或刺痛减少,高血糖患者的血糖水平升高,关节疼痛、炎症、肿胀或退化减轻,痉挛和腹泻频率和量减少,心绞痛减少,组织炎症减少或发作频率降低;癌症肿瘤负荷减少,肿瘤进展时间延长,癌症疼痛减轻,生存率提高或生活质量提高;或骨质疏松进展延缓或改善。
如本文使用的术语“治疗有效量”是指导致疾病或病状的症状改善或补救的量。
如本文使用,“预防”可以指完全预防疾病症状,延迟疾病症状的发作或减轻随后发展的疾病症状的严重程度。
本文使用的术语“受试者”是指根据本文所述的方法施用本发明的斯托拉多体的任何哺乳动物受试者。在一个具体实施例中,本公开的方法用于治疗人类受试者。本公开的方法还可以用于治疗非人灵长类动物(例如,猴子、狒狒和黑猩猩)、小鼠、大鼠、牛科动物、马、猫、狗、猪、兔、山羊、鹿、绵羊、雪貂、沙鼠、豚鼠、仓鼠、蝙蝠、鸟类(例如,鸡、火鸡和鸭)、鱼类和爬行动物,以产生物种特异性或嵌合性斯托拉多体分子。
在一些实施例中,本发明的斯托拉多体用于治疗补体介导的疾病。如本文使用,术语“补体介导的疾病”和“补体相关的疾病”是指补体系统发挥作用的疾病和病状。例如,补体介导的疾病包含涉及补体系统激活异常的疾病。在一些实施例中,可以通过抑制补体级联来治疗、预防或减少补体介导的疾病。补体相关疾病是本领域已知的,并且包含但不限于冷凝集素疾病、溶血性贫血;重症肌无力、溶血性尿毒症综合症(hus)、非典型溶血性尿毒症综合症(ahus)、志贺毒素大肠杆菌相关溶血性尿毒症综合症(stec-hus)、系统性血栓性微血管病(tma)、阵发性睡眠性血红蛋白尿症(pnh)、视神经脊髓炎、复发性视神经脊髓炎(nmo)、抗体介导的移植同种异体移植物排斥,巴勒奎尔-西蒙斯综合症、哮喘、红斑狼疮、自身免疫性心脏病、多发性硬化症、炎性肠病、缺血-再灌注损伤、阿尔茨海默氏病、帕金森病、肌萎缩侧索硬化、脊髓损伤、黄斑变性(包含因子h(y402h)相关性黄斑变性、年龄相关性黄斑变性(amd))、遗传性血管性水肿和膜增生性肾小球肾炎(mpgn)、类风湿性关节炎(ra)、急性呼吸窘迫综合症(ards)、在心肺旁路手术期间的补体激活、皮肌炎、天疱疮、狼疮性肾炎、膜性肾病、肾小球肾炎和血管炎、iga肾病、急性肾衰竭、冷球蛋白血症、抗磷脂抗体综合症、葡萄膜炎、糖尿病性视网膜病、血液透析、慢性闭塞性肺窘迫综合症(copd)和吸入性肺炎。补体相关疾病还可以包含各种其它自身免疫性、炎性、免疫性、神经性、风湿性或传染原相关性疾病。
在一个实施例中,相对于其它补体结合分子,本发明的斯托拉多体提供了更优异的安全性和有效性。在另一个实施例中,相对于抗c5抗体依库丽单抗,本发明的斯托拉多体表现出更优异的安全性和有效性。
已证实补体抑制减少抗体介导的疾病(参见例如stegall等人,《美国移植杂志(americanjournaloftransplantation)》,2011年11月;11(1):2405-2413)。本发明的斯托拉多体也可以用于治疗抗体介导的疾病或病状。自身抗体介导许多已知的自身免疫性疾病,并且可能在许多其它自身免疫性疾病中发挥作用。可以使用本发明的斯托拉多体的公认的抗体介导的疾病包含但不限于抗肾小球基底膜抗体介导的肾炎(包含肺出血-肾炎综合症);实体器官移植中的抗供体抗体(供体特异性同种抗体);视神经脊髓炎中的抗水通道蛋白-4抗体;神经性肌强直、边缘性脑炎和莫旺综合症中的抗vgkc抗体;重症肌无力中的抗烟碱型乙酰胆碱受体和抗musk抗体;兰伯特伊顿肌无力综合症中的抗vgcc抗体;通常与肿瘤有关的边缘性脑炎中的抗ampar和抗gaba(b)r抗体;僵人综合症或过度惊骇中的抗glyr抗体;反复自然流产、休斯综合症和系统性红斑狼疮中的抗磷脂、抗心磷脂和抗β2糖蛋白i抗体;僵人综合症、自身免疫性小脑性共济失调或边缘性脑炎中的抗谷氨酸脱羧酶抗体;新描述的综合症中的抗nmda受体抗体(包含边缘和皮层下特征,其中通常在年轻成人和儿童中出现显著的运动障碍,其通常与卵巢畸胎瘤相关但可以是非副肿瘤性的);系统性红斑狼疮中的抗双链dna、抗单链dna、抗rna、抗sm和抗c1q抗体;结缔组织疾病(包含硬皮病、干燥综合症和多肌炎)中的抗核和抗核仁抗体,包含抗ro、抗la、抗scl70、抗jo-1;类风湿性关节炎中的抗类风湿因子抗体;结节性多动脉炎中的抗乙型肝炎表面抗原抗体;crest综合症中的抗着丝点抗体;心内膜炎中或作为其风险的抗链球菌抗体;桥本氏甲状腺炎中的抗甲状腺球蛋白、抗甲状腺过氧化物酶和抗tsh受体抗体;混合性结缔组织病和系统性红斑狼疮中的抗u1rnp抗体;和天疱疮中的抗桥粒芯糖蛋白和抗角质形成细胞抗体。
本发明的斯托拉多体可以用于治疗病状,包含但不限于充血性心力衰竭(chf)、血管炎、红斑痤疮、痤疮、湿疹、心肌炎和其它心肌病状、系统性红斑狼疮、糖尿病、脊椎病、滑膜成纤维细胞、和骨髓基质;骨质流失;佩吉特氏病,破骨细胞瘤;多发性骨髓瘤;乳腺癌;废用骨量减少;营养不良、牙周病、戈谢病、郎格罕氏细胞组织细胞增生症、脊髓损伤、急性化脓性关节炎、骨软化症、库欣综合症、单骨性纤维性结构不良,多骨性纤维性结构不良、牙周重建和骨折;结节病;溶骨性骨癌、肺癌、肾癌和直肠癌;骨转移、骨疼痛管理、和体液性恶性高钙血症、强直性脊柱炎和其它脊柱关节病;移植排斥、病毒感染、血液肿瘤和肿瘤样病状,例如霍奇金淋巴瘤;非霍奇金淋巴瘤(伯基特淋巴瘤、小淋巴细胞淋巴瘤/慢性淋巴细胞白血病、蕈样真菌病、套细胞淋巴瘤、滤泡性淋巴瘤、弥漫性大b细胞淋巴瘤、边缘区淋巴瘤、毛细胞白血病和淋巴浆细胞白血病)、淋巴细胞前体细胞肿瘤(包含b细胞急性淋巴细胞白血病/淋巴瘤、t细胞急性淋巴细胞白血病/淋巴瘤)、胸腺瘤、成熟t细胞和nk细胞肿瘤(包含外周t细胞白血病、成人t细胞白血病/t细胞淋巴瘤和大颗粒淋巴细胞白血病)、郎格罕氏细胞组织细胞增生症、髓样瘤(例如,急性髓性白血病(包含成熟的aml、无分化的aml)、急性早幼粒细胞白血病、急性髓单核细胞白血病和急性单核细胞白血病)、骨髓增生异常综合症、和慢性骨髓增生性病症(包含慢性髓性白血病)、中枢神经系统肿瘤(例如,脑肿瘤(胶质瘤、成神经细胞瘤、星形细胞瘤、成神经管细胞瘤、室管膜瘤和成视网膜细胞瘤))、实体瘤(鼻咽癌、基底细胞癌、胰腺癌、胆管癌、卡波西肉瘤、睾丸癌、子宫癌、阴道癌或宫颈癌、卵巢癌、原发性肝癌或子宫内膜癌)、血管系统肿瘤(血管肉瘤和血管外皮细胞瘤)或其它癌症。
本文的“癌症”是指或描述哺乳动物中通常以不受调节的细胞生长为特征的生理病状。癌症的实例包含但不限于癌、淋巴瘤、胚细胞瘤、肉瘤(包含脂肪肉瘤、成骨肉瘤、血管肉瘤、内皮肉瘤、平滑肌肉瘤、脊索瘤、淋巴管肉瘤、淋巴管内皮肉瘤、横纹肌肉瘤、纤维肉瘤、粘液肉瘤和软骨肉瘤)、神经内分泌瘤、间皮瘤、滑膜瘤、神经鞘瘤、脑膜瘤、腺癌、黑素瘤和白血病或淋巴恶性肿瘤。此类癌症的更特定实例包含鳞状细胞癌(例如,上皮鳞状细胞癌)、肺癌(包含小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状细胞癌)、小细胞肺癌、腹膜癌、肝细胞癌、胃癌(包含胃肠癌)、胰腺癌、成胶质细胞瘤、宫颈癌、卵巢癌、肝癌、膀胱癌、肝癌、乳腺癌、结肠癌、直肠癌、结直肠癌、子宫内膜癌或子宫癌、唾液腺癌、肾癌、前列腺癌、外阴癌、甲状腺癌、肝癌、肛门癌、阴茎癌、睾丸癌、食道癌、胆道瘤、尤文氏瘤、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、囊腺癌、髓样癌、支气管癌、肾细胞癌、胆管癌、绒毛膜癌、精原细胞瘤、胚胎癌、维尔姆斯瘤、睾丸瘤、肺癌、膀胱癌、上皮癌、胶质瘤、星形细胞瘤、成神经管细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、成血管细胞瘤、听神经瘤、少突神经胶质瘤、脑膜瘤、黑素瘤、成神经细胞瘤、成视网膜细胞瘤、白血病、淋巴瘤、多发性骨髓瘤、瓦尔登斯特伦巨球蛋白血症、骨髓增生异常疾病、重链疾病、神经内分泌瘤、神经鞘瘤和其它癌、以及头颈癌。
本发明的斯托拉多体可以用于治疗自身免疫性疾病。如本文使用的术语“自身免疫性疾病”是指多于80种疾病和病状的可变组。在所有这些疾病和病状中,潜在的问题是身体的免疫系统攻击身体本身。自身免疫性疾病影响所有主要的身体系统,包含结缔组织、神经、肌肉、内分泌系统、皮肤、血液、呼吸系统和胃肠系统。自身免疫性疾病包含例如系统性红斑狼疮、类风湿性关节炎、多发性硬化症、重症肌无力和1型糖尿病。
可使用本发明的组合物和方法治疗的疾病或病状可以是血液免疫过程,包含但不限于镰状细胞病、特发性血小板减少性紫癜、同种免疫/自身免疫性血小板减少症、获得性免疫性血小板减少症、自身免疫性中性粒细胞减少症、自身免疫性溶血性贫血、细小病毒b19相关红细胞再生障碍、获得性抗因子viii自身免疫、获得性血管性血友病、意义不明的多发性骨髓瘤和单克隆丙种球蛋白病、败血症、再生障碍性贫血、纯红细胞再生障碍、戴-布二氏贫血、新生儿溶血病、免疫介导的中性粒细胞减少症、血小板输注无效、新生儿输注后紫癜、溶血性尿毒症综合症、系统性血管炎、血栓性血小板减少性紫癜或伊文氏综合症。
疾病或病状也可以是神经免疫过程,包含但不限于格林-巴利综合症、慢性炎性脱髓鞘性多神经根神经病、副蛋白血症性igm脱髓鞘性多发性神经根神经病、兰伯特-伊顿肌无力综合症、重症肌无力、多灶性运动神经病、与抗/gml相关的下运动神经元综合症、脱髓鞘、多发性硬化症和视神经炎、僵人综合症、伴抗yo抗体的副肿瘤性小脑变性、副肿瘤性脑脊髓炎、伴抗hu抗体的感觉神经病、癫痫、脑炎、脊髓炎、脊髓病(尤其与人类t细胞嗜淋巴细胞病毒-1相关)、自身免疫性糖尿病神经病、阿尔茨海默氏病、帕金森病、亨廷顿氏舞蹈病或急性特发性自主神经功能失调神经病。
疾病或病状也可以是与听力损失或视力损失相关的炎症或自身免疫。例如,疾病或病状可以是与自身免疫相关的听力损失,例如噪声引起的听力损失或与年龄相关的听力损失,或者可能与诸如听力装置(例如,耳蜗植入物)之类的装置的植入有关。在一些实施例中,本文提供的组合物可以在植入装置之前、同时或之后施用于受试者。
疾病或病状也可以是风湿性疾病过程,包含但不限于川崎病、类风湿性关节炎、费耳蒂氏综合症、anca阳性血管炎、自发性多肌炎、皮肌炎、抗磷脂综合症、反复自然流产、系统性红斑狼疮、幼年特发性关节炎、雷诺综合症、crest综合症或葡萄膜炎。
疾病或病状也可以是皮肤免疫疾病过程,包含但不限于中毒性表皮坏死松解症、坏疽、肉芽肿、自身免疫性皮肤水疱性疾病(包含寻常型天疱疮、大疱性类天疱疮、落叶型天疱疮、白癜风)、链球菌中毒性休克综合症、硬皮病、系统性硬化症(包含弥漫性和局限性皮肤系统性硬化症、或特应性皮炎(尤其是类固醇依赖性))。
疾病或病状也可以是肌肉骨骼免疫疾病过程,包含但不限于包涵体肌炎、坏死性筋膜炎、炎性肌病、肌炎、抗核心蛋白聚糖(bj抗原)肌病、副肿瘤性坏死性肌病、x连锁空泡性肌病、青霉胺诱发的多肌炎、动脉粥样硬化、冠状动脉疾病或心肌病。
疾病或病状也可以是胃肠免疫疾病过程,包含但不限于恶性贫血、自身免疫性慢性活动性肝炎、原发性胆汁性肝硬化、乳糜泻、疱疹样皮炎、隐源性肝硬化、反应性关节炎、克罗恩病、惠普尔病、溃疡性结肠炎、或硬化性胆管炎。
疾病或病状也可以是移植物抗宿主病、抗体介导的移植物排斥、骨髓移植后排斥、传染病后炎症、淋巴瘤、白血病、瘤形成、哮喘、伴抗β细胞抗体的1型糖尿病、干燥综合症、混合性结缔组织病、爱迪生氏病、伏格特-小柳-原田三氏综合症、膜增生性肾小球肾炎、肺出血-肾炎综合症、格雷夫斯病、桥本氏甲状腺炎、韦格纳氏肉芽肿病、微小多动脉炎、许尔-斯特劳斯综合症、结节性多动脉炎或多系统器官衰竭。
如本文使用,“过敏”包含由ige介导的所有免疫反应以及模拟了ige介导的反应的那些反应。过敏由过敏原诱导,包含蛋白质、肽、碳水化合物及其组合,其引发ige或ige样免疫应答。示例性过敏包含坚果过敏、花粉过敏和昆虫叮咬过敏。示例性过敏原包含毒藤和橡树中的漆酚;室内粉尘抗原;桦树花粉组分betv1和betv2;芹菜中的15kd抗原;苹果抗原mald1;桃子中的prup3;猫尾草花粉过敏原phlp1;黑麦草中的lolp3、lolpi或lolpv;百慕大草中的cynd1;尘螨过敏原尘螨derp1、derp2或derf1;麸质中的α-麦醇溶蛋白和γ-麦醇溶蛋白表位;蜂毒磷脂酶a2;花生中的arah1、arah2和arah3表位。
本发明进一步包括有效治疗由传染原引起的疾病的方法和组合物。传染原包含但不限于细菌、真菌、寄生虫和病毒试剂。这些传染原的实例包含以下:葡萄球菌、耐甲氧西林金黄色葡萄球菌、大肠杆菌、链球菌、奈瑟氏球菌、球菌、肠杆菌、肠球菌、耐万古霉素肠球菌、隐球菌、组织胞浆菌病、曲霉菌、假单胞菌、弧菌、弯曲杆菌、巴斯德氏菌、博德特氏菌、弗朗西斯氏菌、布鲁氏菌、军团菌、拟杆菌、革兰氏阴性杆菌、梭菌、棒状杆菌、丙酸杆菌、革兰氏阳性杆菌、炭疽、放线菌、诺卡氏菌、分枝杆菌、密螺旋体、疏螺旋体、钩端螺旋体、支原体、解脲支原体、立克次氏体、衣原体、念珠菌、系统性真菌病、机会性真菌病、原生动物、线虫、吸虫、绦虫、腺病毒、疱疹病毒(包含例如单纯疱疹病毒和爱泼斯坦巴尔病毒和带状疱疹病毒)、痘病毒、乳多空病毒、肝炎病毒(包含例如乙型肝炎病毒和丙型肝炎病毒)、乳头状瘤病毒、正黏液病毒(包含例如甲型流感、乙型流感和丙型流感)、副黏液病毒、冠状病毒、小核糖核酸病毒、呼肠孤病毒、外衣病毒、黄病毒、布尼亚病毒、棒状病毒、轮状病毒、呼吸道合胞病毒、人类免疫缺陷病毒和逆转录病毒。示例性传染性疾病包含但不限于念珠菌病、念珠菌血症、曲霉菌病、链球菌性肺炎、链球菌性皮肤和口咽病状、革兰氏阴性败血症、结核病、单核细胞增多症、流感、由呼吸道合胞病毒引起的呼吸道疾病、疟疾、血吸虫病和锥虫病。
在另一个实施例中,本文所述的斯托拉多体可以用于起动输注系统,其中从患者抽取血液,并且在将血液引回患者体内之前使其与斯托拉多体短暂接触一段时间,约半小时到约三小时。在这种形式的细胞疗法中,患者自身的效应子细胞暴露于离体固定在基质上的斯托拉多体,以便通过效应子细胞暴露于斯托拉多体来调节效应子细胞。然后,将包含调节后的效应子细胞的血液输注回患者体内。这种起动输注系统可以具有许多临床和治疗应用。
本文公开的斯托拉多体也可以在各种背景下容易地用于改变免疫系统应答以影响免疫应答谱的特异性改变。改变或调节受试者中的免疫应答是指增加、减少或改变免疫应答的比例或组分。例如,细胞因子产生或分泌水平可以根据需要通过靶向补体以及fcr与设计用于结合补体并与那些受体相互作用的斯托拉多体的适当组合来升高或降低。抗体产生也可能增加或减少;可以改变两种或多种细胞因子或免疫细胞受体的比例;或者可以产生其它类型的细胞因子或抗体。
在一个优选实施例中,患有自身免疫性或炎性疾病的受试者的免疫应答发生改变,包括向受试者施用治疗有效量的本文所述的斯托拉多体的步骤,其中治疗有效量的斯托拉多体改变了受试者中的免疫应答。理想地,该干预治疗了受试者中的疾病或病状。改变的免疫应答可以是增加的或减少的应答,并且可以涉及改变的细胞因子水平,包含il-6、il-10、il-8、il-23、il-7、il-4、il-12、il-13、il-17、tnf-α和ifn-α中的任一个的水平。在一个优选实施例中,il-6或il-8响应于疗法而减少。在一个特别优选实施例中,il-6和il-8响应于疗法而减少。然而,本发明不受所述仿生物质的任何特定作用机制的限制。改变的免疫应答可以是受试者中改变的自身抗体水平。改变的免疫应答可以是受试者中改变的自身攻击性t细胞水平。
例如,减少自身免疫性疾病中tnf-α产生的量可以具有治疗作用。其实际应用是抗tnf-α抗体疗法(例如,
本文所述的斯托拉多体可以用于调节来自免疫细胞(包含树突细胞、巨噬细胞、破骨细胞、单核细胞或nk细胞)的共刺激分子的表达或抑制这些相同的免疫细胞的分化、成熟或细胞因子分泌(包含白细胞介素-12(il-12),或增加的细胞因子分泌,包含白细胞介素-10(il-10)、或白细胞介素-6(il-6)或il-1rα)。技术人员还可以通过将免疫细胞暴露于免疫活性仿生物质并测量免疫细胞功能的调节来验证免疫活性仿生物质的功效,其中免疫细胞是树突细胞、巨噬细胞、破骨细胞或单核细胞。在一个实施例中,免疫细胞在体外暴露于免疫活性仿生物质,并且进一步包括确定细胞表面受体的量或细胞因子产生量的步骤,其中细胞表面受体的量或细胞因子产生量的变化表示免疫细胞功能的调节。在另一个实施例中,免疫细胞暴露于用于自身免疫性疾病的模型动物体内免疫活性仿生物,进一步包括评估自身免疫性疾病的改善程度的步骤。
本文所述的斯托拉多体也可以用作装置的部件。例如,在一些实施例中,本文提供的斯托拉多体可以涂覆在装置上,例如医学植入物。例如,斯托拉多体可以涂覆在冠状动脉支架上或者作为纳米颗粒疗法的一部分来涂敷,以增强渗透和延长药物释放,例如用于葡萄膜炎或黄斑变性的眼内使用。本文所述的斯托拉多体也可以用作诊断剂的组分。在一些实施例中,技术人员可以通过确定斯托拉多体的使用对哪些患者可能特别有益而使疗法个性化。例如,技术人员可以将患者的免疫细胞暴露于免疫活性仿生物质,并通过流式细胞术或细胞因子谱测量免疫细胞的激活或成熟的调节,以标识高应答者。
过量的补体激活和/或沉积可能是有害的并且与许多疾病相关,包含重症肌无力、溶血性尿毒症综合症(hus)和阵发性睡眠性血红蛋白尿症(pnh)。衰老的大脑与显著增加的补体组分c1q的水平相关(stephan等人,《神经科学杂志(j.neuroscience)》,2013年8月14日,33(33):13460-13474)。补体系统深入涉及乙酰胆碱受体抗体相关的重症肌无力的发病机理(
本文引用的所有参考文献都通过引用整体并入。
实例
实例1:普通斯托拉多体
采用各种方法生成具有增强的经典结合和增强的补体结合的斯托拉多体。生成了三聚体,其中至少一个点突变被引入fc结构域。具体地,在wo2012/016073中描述的gl-2045斯托拉多体的fc结构域的第233位、第234位、第235位、第236位、第267位、第268位、第299位、第324位、第345位、第430位和第440位进行突变。示例性斯托拉多体的氨基酸序列如上表1所示。
对于生成的每种斯托拉多体,确定经典fcγr结合、补体c1q结合和cdc抑制的水平,并与亲本斯托拉多体,gl-2045(igg1铰链-igg1ch2igg1ch3-igg2铰链)进行比较。
评估了普通斯托拉多体或亲本斯托拉多体gl-2045与fcγri、fcγriib、fcγriiia,fcγriia的结合。使用fortebiooctet仪器通过生物层干涉测量法测量解离的ru值。his标记的受体蛋白在购自fortebio的1x动力学分析缓冲液中与传感器尖端结合,之后通过将传感器尖端转移至含有纯化的所选斯托拉多体的1x动力学缓冲液来测量受体/蛋白质的开启速率。通过将传感器尖端转移至1x动力学缓冲液来测量关闭速率,并且使用fortebio软件从测量的最大结合计算ru值。生物层干涉测量法检测固定在生物传感器尖端表面上的配体与溶液中的分析物之间的结合。当发生结合时,它在生物传感器尖端处产生光学厚度的增加,这导致波长偏移(检测为“ru”的应答单位)。最大结合水平(rumax)是平衡时样品结合的最大可能量,其使传感器表面上的配体量饱和。ru300是解离300秒后的残留样品结合,可用于表征测试物品与测试配体的解离速率。
为了表征化合物,通过生物层干涉测量法(rumax)测量的对4种fc受体的最大结合、与c1q的elisa结合和补体依赖性细胞毒性的抑制在本文提供的数据中给出。
对于c1q结合,将96孔板在1xpbs中用c1q(sigmacat#:c17401μg/ml)涂覆过夜。在涂覆之后,将板用标准洗涤缓冲液(pbs+0.05%吐温20)洗涤3次,并用封闭缓冲液(1%bsa+1xpbs+0.05%吐温20)在室温下封闭2小时。在封闭之后,将板与100μl/孔的封闭缓冲液中稀释的化合物一起温育,并用标准洗涤缓冲液洗涤3次。通过与1:5000生物素化的小鼠抗人igg1(cat#555869,bdbiosciences)和链霉亲和素-hrp(cat#:7100-05southernbiotech)(100μg/孔)一起在室温下温育1小时,然后用洗涤缓冲液洗涤3次,之后根据制造商方案使用标准tmb方法显色15分钟来检测c1q结合的化合物。在450nm处读取吸光度。结果总结如表3所示。
图1中提供了gl-2045的示例性fc受体结合数据。普通斯托拉多体的fcγr结合的总结提供于下表3中。
表3:普通斯托拉多体活性的总结
nd=无数据,对于cdc抑制*=抑制,并且n.i.=无抑制
评估每种斯托拉多体的多聚体形成。简而言之,将每种斯托拉多体的3μg样品与20mm碘乙酰胺混合并温育10分钟,然后将样品装载到3-8%tris-甘氨酸非还原蛋白凝胶上。样品在150伏下运行约1.2小时。结果在图26a到图26f中提供,其显示,所有本文所述的多聚化斯托拉多体形成经多聚化的斯托拉多体(例如,同源二聚体及以上的二聚体)。
实例2-普通斯托拉多体的增强的补体结合
进行研究以评估普通斯托拉多体与c1q的结合,其结果总结在表3中。
对于c1q结合,将96孔板在pbs中用c1q(sigmacat#:c17401μg/ml)涂覆过夜。在涂覆之后,将板用标准洗涤缓冲液(pbs+0.05%吐温20)洗涤3次,并用封闭缓冲液(1%bsa-0.05%pbs吐温)在室温下封闭2小时。在封闭之后,将板与100μl/孔的封闭缓冲液中稀释的化合物一起温育,并用标准洗涤缓冲液洗涤3次。通过与1:5000生物素化的小鼠抗人igg1(cat#555869,bdbiosciences)和链霉亲和素-hrp(cat#:7100-05southernbiotech)(100μl/孔)一起在室温下温育1小时,然后用洗涤缓冲液洗涤3次,之后根据制造商方案使用标准tmb方法显色15分钟来检测c1q结合的化合物。在450nm处读取吸光度。
还进行研究以评估普通斯托拉多体与c3、c3b、c4和c5的结合。对于c3结合,将96孔板用c3补体组分(quidel,#a401;pbs中1μg/ml)在4℃下涂覆过夜,然后用300μlpbs1x0.1%吐温20洗涤3次。将板用pbs1x+2%bsa+0.05%吐温20在室温下封闭2小时。将待测试的化合物(gl-2045、g1097、g1098、g1099、g1126或g1127)在封闭缓冲液中在室温下与结合的c3一起温育2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。通过生物素小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)1/5000(ea.)在pbs-bsa-(100μl/孔)中在室温下1小时,然后洗涤4次(300μlpbs1x0.1%吐温20)来检测与c3相互作用的化合物。用每孔100μl的tmb底物试剂显色20分钟,并用50μlh2so41m终止反应,并且在450/650nm处读取吸光度。
对于c3b结合,将96孔板用c3b补体组分(genwaybiotech#gwb-8ba994,1xpbs中1μg/ml)涂覆。每孔加入100μlc3b补体组分,并在4℃下温育过夜,然后洗涤3次(300μlpbs1x0.1%吐温20)。将板在封闭缓冲液(pbs1x+2%bsa+0.05%吐温20)中在室温下封闭2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。将本文所述的普通斯托拉多体在封闭缓冲液中在室温下与c3b反应4小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。用生物素化的小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)1/5000(ea.)在100μl封闭缓冲液中在室温下1小时来检测结合的化合物。用tmb底物试剂在室温下显色20分钟,并用50μl1mh2so4终止反应。在450/650nm处读取吸光度。
对于c4结合,将96孔板用c4补体组分(quidel#a402,pbs中1μg/ml)涂覆。每孔加入100μlc4补体组分,并在4℃下温育过夜,然后洗涤3次(300μlpbs1x0.1%吐温20)。将板在封闭缓冲液(pbs1x+2%bsa+0.05%吐温20)中在室温下封闭2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。将待测试的化合物(gl-2045、g1097、g1098、g1099、g1126或g1127)在封闭缓冲液中在室温下与c4反应2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。用生物素化的小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)1/5000(ea.)在100μl封闭缓冲液中在室温下1小时来检测结合的化合物。用tmb底物试剂在室温下显色20分钟,并用50μl1mh2so4终止反应。在450/650nm处读取吸光度。
对于c5结合,将96孔板用c5补体组分(quidel#a403,pbs中1μg/ml)涂覆。每孔加入100μlc5补体组分,并在4℃下温育过夜,然后洗涤3次(300μlpbs1x0.1%吐温20)。将板在封闭缓冲液(pbs1x+2%bsa+0.05%吐温20)在室温下重新封闭2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。将待测试的化合物(gl-2045、g1097、g1098、g1099、g1126或g1127)在封闭缓冲液中在室温下与c5反应2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。用生物素化的小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)1/5000(ea.)在100μl封闭缓冲液中在室温下1小时来检测结合的化合物。用tmb底物试剂在室温下显色20分钟,并用50μl1mh2so4终止反应。在450/650nm处读取吸光度。
这些研究的结果将显示,本文所述的普通斯托拉多体比亲本斯托拉多体(例如,gl-2045或g019)更有效地或和其一样有效地结合补体组分。
实例3-六聚斯托拉多体
产生了三聚体,其中至少一个点突变被引入fc结构域。具体地,在wo2012/016073中描述的gl-2045斯托拉多体的fc结构域的第299位和第345位、第430位、第440位中的一个或多个进行以下突变:t299a、e345r、e430g和s440y。示例性斯托拉多体的氨基酸序列如上表1和表2所示。
对于生成的每种斯托拉多体,确定经典fcγr结合、六聚体形成和cdc抑制的水平。
评估了斯托拉多体与fcγri、fcγriia、fcγriib和fcγriiia的结合。his标记的受体蛋白(5μg/ml)在购自fortebio的1x动力学分析缓冲液(cat.#18-1092)中与抗his传感器尖端(抗penta-hishis1k,cat.#18-5121)结合300秒。将加载的传感器转移至没有标记的受体或配体的1x动力学分析中,以便获得60秒的基线测量。在获得基线之后,通过将传感器尖端转移至含有纯化的所选斯托拉多体的1x动力学缓冲液来以50μg/ml、25μg/ml和12.5μg/ml的浓度下测量受体/蛋白质的开启速率300秒。通过将传感器尖端转移至1x动力学缓冲液来测量关闭速率600秒,并且使用fortebio软件从测量的最大结合计算ru值。生物层干涉测量法检测固定在生物传感器尖端表面上的配体与溶液中的分析物之间的结合。当发生结合时,它在生物传感器尖端处产生光学厚度的增加,这导致波长偏移(检测为“ru”的应答单位)。最大结合水平(rumax)是平衡时样品结合的最大可能量,其使传感器表面上的配体量饱和。ru300是解离300秒后的残留样品结合,可用于表征测试物品与测试配体的解离速率。
为了评估本文所述的六聚斯托拉多体的能力,将表达cd20的will-2细胞与抗cd20单克隆抗体一起温育20分钟,之后将细胞离心并重悬于新鲜培养基中。然后将细胞在96孔板中在含有本文所述的每种斯托拉多体的培养基(以下六种斯托拉多体浓度之一:100μg/ml、50μg/ml、25μg/ml、12.5μg/ml、6.25μg/ml或3.125μg/ml)中温育。将血清加入细胞混悬液中,以便引发补体依赖性细胞裂解,并将板在37℃下温育3小时。用promegacytotoxglo测定定量细胞死亡。将细胞毒素测定试剂加入板的每个孔中,并将板在室温下在黑暗中温育15分钟。在promegaglomax发光计上读取15分钟后的发光,并从该读数计算细胞死亡。
评估每种斯托拉多体的六聚体形成。简而言之,将每种斯托拉多体的3μg样品与20mm碘乙酰胺混合并温育10分钟,然后将样品装载到3-8%tris-甘氨酸非还原蛋白凝胶上。样品在150伏下运行约1.2小时。结果在图27中提供,并显示g1098、1126和1127优先形成六聚复合物。此外,图27清楚地显示g1098、1126和1127形成相较于gl-2045高得多的高分子量(六聚体及以上的条带)物种的水平,作为总蛋白质的百分比。
预期t299a点突变导致本文所述的斯托拉多体的无糖基化。如图32a所示,预测亲本斯托拉多体(gl-2045,seqidno:7或8)的序列在第297位具有n-糖基化位点,其中糖基化共有序列是297n-x-299t。第297位处的天冬酰胺残基是聚糖共价连接的实际位点,第299位处的苏氨酸残基是识别位点的一部分。如图32b所示,预测第299位的突变(t299a)去除了该糖基化位点,从而导致无糖基化斯托拉多体。
通过凝胶分析证实了本文所述的每种斯托拉多体化合物的无糖基化。如图27所示,与g2045(糖基化)亲本斯托拉多体相比,具有t299a突变的每种斯托拉多体具有更高的迁移度。
g1099是具有插入gl-2045骨架中的一个突变(t299a)的斯托拉多体并且被生成以减少与fcγr的经典结合。令人惊讶的是,如图23所示,g1099没有表现出基于t299a点突变所预期的减少的经典结合。g1099结合补体蛋白的能力得以保持,并且可能增强,因为g1009能够以剂量依赖性方式抑制cdc活性,其中ic50为30μg/ml(图31)。
g1097是具有插入gl-2045骨架中的两个突变(t299a和e340g)的斯托拉多体并且被生成以减少与fcγr的经典结合并增强补体结合。令人惊讶的是,如图24所示,g1097没有表现出基于t299a点突变所预期的减少的经典结合。然而,与亲本斯托拉多体的无糖基化变体(g1099)相比,g1097结合补体蛋白的能力增强,因为g1097能够以剂量依赖性方式抑制cdc活性,其中ic50为20μg/ml(图31)。该ic50远低于g1099的ic50(30μg/ml)。
g1098是具有插入gl-2045骨架中的三个突变(t299a、e340g和s440y)的斯托拉多体并且被生成以减少与fcγr的经典结合并增强补体结合。令人惊讶的是,如图23所示,g1098没有表现出基于t299a点突变所预期的减少的经典结合。然而,与亲本斯托拉多体的无糖基化变体(g1099)相比,g1098结合补体蛋白的能力增强,因为g1098能够以剂量依赖性方式抑制cdc活性,其中ic50为10μg/ml(图31)。该ic50远低于g1099的ic50(30μg/ml)。g1098的凝胶分析进一步证明g1098优先多聚化以形成六聚斯托拉多体,这是仅具有t299a突变(g1099)或与e430g组合(g1097)未见的特征(图27)。
g1126是具有插入gl-2045骨架中的四个突变(t299a、e345r、e430g和s440y)的斯托拉多体并且被生成以减少与fcγr的经典结合并增强补体结合。令人惊讶的是,如图27所示,g1126没有表现出基于t299a点突变所预期的减少的经典结合。然而,与亲本斯托拉多体的无糖基化变体(g1099)相比,g1126结合补体蛋白的能力增强,因为g1098能够以剂量依赖性方式抑制cdc活性,其中ic50为5μg/ml(图31)。该ic50远低于g1099的ic50(30μg/ml)。g1126的凝胶分析进一步证明g1126优先多聚化以形成六聚斯托拉多体,这是仅具有t299a突变(g1099)或与e430g组合(g1097)未见的特征(图27)。
g1127是具有插入gl-2045骨架中的两个突变(t299a和e345r)的斯托拉多体并且被生成以减少与fcγr的经典结合并增强补体结合。令人惊讶的是,如图25所示,g1127没有表现出基于t299a点突变所预期的减少的经典结合。然而,与亲本斯托拉多体的无糖基化变体(g1099)相比,g1127结合补体蛋白的能力增强,因为g1127能够以剂量依赖性方式抑制cdc活性,其中ic50为5μg/ml(图31)。该ic50远低于g1099的ic50(30μg/ml)。g1127的凝胶分析进一步证明g1127优先多聚化以形成六聚斯托拉多体,这是仅具有t299a突变(g1099)或与e430g组合(g1097)未见的特征(图27)。
本文所述的斯托拉多体(例如,g1098、g1126和g1127)与gl-2045类似,因为它们出乎意料地保持了经典结合(尽管含有t299a无糖基化突变),并且进一步表现出通过cdc抑制测量的保持的与补体蛋白的结合。在一些实施例中,与gl-2045相比,本文所述的斯托拉多体化合物表现出更优异的与经典fcγ受体和补体蛋白的结合。尽管不希望受理论束缚,但是这种增加的结合可能是由于六聚g1098、g1126和g1127化合物中存在的亲合力的增加,这在亲本化合物的无糖基化非六聚形式中是不存在的。
研究结果的全面总结在表4中提供。
表4.六聚斯托拉多体活性的总结
(*)表示不优选六聚体形成
实例4-六聚斯托拉多体的增强的补体结合
进行研究以评估六聚斯托拉多体与c1q、c3、c4和c5的结合。
对于c1q结合,将96孔板在pbs中用c1q(sigmacat#:c17401μg/ml)涂覆过夜。在涂覆之后,将板用标准洗涤缓冲液(pbs+0.05%吐温20)洗涤3次,并用封闭缓冲液(1%bsa-0.05%pbs吐温)在室温下封闭2小时。在封闭之后,将板与100μl/孔的封闭缓冲液中稀释的化合物一起温育,并用标准洗涤缓冲液洗涤3次。通过与1:5000生物素化的小鼠抗人igg1(cat#:555869,bdbiosciences)和链霉亲和素-hrp(cat#:7100-05southernbiotech)(100μl/孔)一起在室温下温育1小时,然后用洗涤缓冲液洗涤3次,之后根据制造商方案使用标准tmb方法显色15分钟来检测c1q结合的化合物。在450nm处读取吸光度。
对于c3结合,将96孔板用c3补体组分(quidel#a401;pbs中1μg/ml)在4℃下涂覆过夜,然后用300μlpbs1x0.1%吐温20洗涤3次。将板用pbs1x+2%bsa+0.05%吐温20在室温下封闭2小时。将待测试的化合物(gl-2045、g1097、g1098、g1099、g1126或g1127)在封闭缓冲液中在室温下与结合的c3一起温育2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。通过生物素化的小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)1/5000(ea.)在1xpbs-2%bsa-0.5%吐温20(100μl/孔)中在室温下1小时,然后洗涤4次(300μlpbs1x0.1%吐温20)来检测与c3相互作用的化合物。用100μl/孔的tmb底物试剂显色20分钟,并用50μlh2so41m终止反应,并且在450/650nm处读取吸光度。
对于c4结合,将96孔板用c4补体组分(quidel#a402,pbs中1μg/ml)涂覆。每孔加入100μlc4补体组分,并在4℃下温育过夜,然后洗涤3次(300μlpbs1x0.1%吐温20)。将板在封闭缓冲液(pbs1x+2%bsa+0.05%吐温20)中在室温下封闭2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。将待测试的化合物(gl-2045、g1097、g1098、g1099、g1126或g1127)在封闭缓冲液中在室温下与c4反应2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。用生物素化的小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)1/5000(ea.)在100μl封闭缓冲液中在室温下1小时来检测结合的化合物。用tmb底物试剂在室温下显色20分钟,并用50μl1mh2so4终止反应。在450/650nm处读取吸光度。
对于c5结合,将96孔板用c5补体组分(quidel#a403,pbs中1μg/ml)涂覆。每孔加入100μlc5补体组分,并在4℃下温育过夜,然后洗涤3次(300μlpbs1x0.1%吐温20)。将板在封闭缓冲液(pbs1x+2%bsa+0.05%吐温20)中在室温下封闭2小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。将待测试的化合物(gl-2045、g1097、g1098、g1099、g1126或g1127)在封闭缓冲液中在室温下与c5反应4小时,然后洗涤3次(300μlpbs1x0.1%吐温20)。用生物素化的小鼠抗人igg1(bd#555869)+链霉亲和素-hrp(cat#:7100-05southernbiotech)(各自1/5000稀释)在100μl封闭缓冲液中在室温下1小时来检测结合的化合物。用tmb底物试剂在室温下显色20分钟,并用50μl1mh2so4终止反应。在450/650nm处读取吸光度。
这些研究的结果将显示,六聚斯托拉多体和亲本斯托拉多体(gl-2045)或亲本斯托拉多体的无糖基化非六聚变体(g1097和g1099)一样有效地或比其更有效地结合补体组分。
实例7-用于治疗关节炎的普通斯托拉多体
评估了本文提供的普通斯托拉多体(包含六聚斯托拉多体)在治疗类风湿性关节炎小鼠模型中的功效。使用胶原诱导的关节炎模型,其中在第0天和第21天用不完全弗氏佐剂乳化的ii型牛胶原(4mg/ml)免疫dba小鼠。每周称重小鼠并每天对关节炎的迹象进行评分。对每个爪进行评分,并将全部四个评分的总和记录为关节炎指数(ai)。最大可能ai为16,如下:0=无可见作用;1=一个脚趾的水肿和/或红斑;2=2个关节的水肿和/或红斑;3=多于2个关节的水肿和/或红斑;4=整个爪子和脚趾的严重关节炎,包含肢体变形和关节强直。从第22天开始,基于平均ai将胶原免疫的小鼠分成治疗组。测量ai约14个治疗日,然后使小鼠安乐死。在治疗日期间,用表1中描述的普通斯托拉多体、对照斯托拉多体(gl-2045)、pbs或用强的松龙作为阳性对照治疗小鼠。
研究的结果将显示,与对照相比,用本文所述的普通斯托拉多体治疗的小鼠表现出更轻的关节炎疾病。
实例5-用于治疗和预防itp的普通斯托拉多体
进行研究以评估普通斯托拉多体(包含六聚斯托拉多体)在特发性血小板减少性紫癜(itp)中的作用。在暴露于小鼠整联蛋白抗-iib抗体后诱导低血小板计数,所述小鼠整联蛋白抗-iib抗体包覆血小板上的整联蛋白受体。简而言之,在抽血和血小板计数后第1天,向8周龄的c57bl/6小鼠注射gl-2045或表1中所述的任何普通斯托拉多体。在抽血和血小板计数后第2天,通过腹膜内注射施用200μlpbs中2μg抗体剂量的鼠抗iib抗体治疗小鼠,以诱导血小板损失。在第3天、第4天和第5天继续血小板计数抽血和抗iib抗体注射。在第2天到第5天每天给予ivig阳性对照。用drewscientifichemavet950血细胞计数器进行血小板计数。在第2天给予普通斯托拉多体和对照斯托拉多体一次。通过尾静脉切口收集血液并与柠檬酸盐缓冲液混合以防止凝结。
该研究的结果将显示,用本文所述的普通斯托拉多体治疗的小鼠表现出比对照治疗的小鼠更轻的itp。
实例6-治疗实验性自身免疫性神经炎的普通斯托拉多体
进行研究以评估普通斯托拉多体(包含六聚斯托拉多体)在实验性自身免疫性神经炎(ean)的动物模型中的作用。鼠ean模型是在人类急性炎性脱髓鞘性多发性神经根神经病上广泛使用的动物模型。简而言之,用全牛外周神经髓鞘免疫lewis大鼠,并随机分入对照组(gl-2045和ivig)和实验治疗组(表中所述的任何普通斯托拉多体)。在临床缺陷发作(通常为第9天或第10天开始的体重减轻)时,连续两天用上述治疗方案iv治疗大鼠。
在临床、电生理学和组织学上评估ean大鼠。通过每日临床分级和体重变化评价临床疾病严重程度。电生理学研究包含检查复合肌肉动作电位(camp)和运动传导速度(mcv)的幅度。在疾病高峰期,处死每组的一部分大鼠,收集坐骨神经并分析组织病理学变化。
该研究的结果将显示,用本文所述的普通斯托拉多体治疗的大鼠表现出比对照治疗的小鼠更轻的ean。
序列表
<110>gliknikinc.
block,davids.
olsen,henrik
<120>产生具有增强的fc受体结合的经有序多聚化的免疫球蛋白
fc组合物的人蛋白片段的融合蛋白
<130>glik-019/01wo310975-2167
<150>us62/365,921
<151>2016-07-22
<150>us62/365,919
<151>2016-07-22
<160>32
<170>patentin版本3.5
<210>1
<211>20
<212>prt
<213>人工序列
<220>
<223>前导序列
<400>1
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrgly
20
<210>2
<211>232
<212>prt
<213>智人
<400>2
gluprolyssercysasplysthrhisthrcysproprocysproala
151015
progluleuleuglyglyproservalpheleupheproprolyspro
202530
lysaspthrleumetileserargthrprogluvalthrcysvalval
354045
valaspvalserhisgluaspprogluvallyspheasntrptyrval
505560
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
65707580
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
859095
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
100105110
leuproalaproileglulysthrileserlysalalysglyglnpro
115120125
arggluproglnvaltyrthrleuproproserarggluglumetthr
130135140
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
145150155160
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
165170175
lysthrthrproprovalleuaspseraspglyserphepheleutyr
180185190
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
195200205
sercysservalmethisglualaleuhisasnhistyrthrglnlys
210215220
serleuserleuserproglylys
225230
<210>3
<211>232
<212>prt
<213>智人
<400>3
gluprolyssercysasplysthrhisthrcysproprocysproala
151015
progluleuleuglyglyproservalpheleupheproprolyspro
202530
lysaspthrleumetileserargthrprogluvalthrcysvalval
354045
valaspvalserhisgluaspprogluvallyspheasntrptyrval
505560
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
65707580
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
859095
asptrpleuasnglylysglutyrlyscyslysvalserasnlysala
100105110
leuproalaproileglulysthrileserlysalalysglyglnpro
115120125
arggluproglnvaltyrthrleuproproserargaspgluleuthr
130135140
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
145150155160
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
165170175
lysthrthrproprovalleuaspseraspglyserphepheleutyr
180185190
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
195200205
sercysservalmethisglualaleuhisasnhistyrthrglnlys
210215220
serleuserleuserproglylys
225230
<210>4
<211>12
<212>prt
<213>智人
<400>4
gluarglyscyscysvalglucysproprocyspro
1510
<210>5
<211>41
<212>prt
<213>智人
<400>5
glyglyglyserilelysglnilegluasplysileglugluileleu
151015
serlysiletyrhisilegluasngluilealaargilelyslysleu
202530
ileglygluargglyhisglyglygly
3540
<210>6
<211>16
<212>prt
<213>人工序列
<220>
<223>gpp多聚化结构域
<400>6
glyproproglyproproglyproproglyproproglyproprogly
151015
<210>7
<211>264
<212>prt
<213>智人
<400>7
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>8
<211>264
<212>prt
<213>智人
<400>8
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>9
<211>263
<212>prt
<213>智人
<400>9
metgluthraspthrleuleuleutrpvalleuleuleuvalprogly
151015
serthrglygluarglyscyscysvalglucysproprocysproglu
202530
prolyssercysasplysthrhisthrcysproprocysproalapro
354045
gluleuleuglyglyproservalpheleupheproprolysprolys
505560
aspthrleumetileserargthrprogluvalthrcysvalvalval
65707580
aspvalserhisgluaspprogluvallyspheasntrptyrvalasp
859095
glyvalgluvalhisasnalalysthrlysproargglugluglntyr
100105110
asnserthrtyrargvalvalservalleuthrvalleuhisglnasp
115120125
trpleuasnglylysglutyrlyscyslysvalserasnlysalaleu
130135140
proalaproileglulysthrileserlysalalysglyglnproarg
145150155160
gluproglnvaltyrthrleuproproserarggluglumetthrlys
165170175
asnglnvalserleuthrcysleuvallysglyphetyrproserasp
180185190
ilealavalglutrpgluserasnglyglnprogluasnasntyrlys
195200205
thrthrproprovalleuaspseraspglyserphepheleutyrser
210215220
lysleuthrvalasplysserargtrpglnglnglyasnvalpheser
225230235240
cysservalmethisglualaleuhisasnhistyrthrglnlysser
245250255
leuserleuserproglylys
260
<210>10
<211>264
<212>prt
<213>智人
<400>10
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuargglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>11
<211>264
<212>prt
<213>智人
<400>11
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleugluglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>12
<211>264
<212>prt
<213>智人
<400>12
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuaspglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>13
<211>264
<212>prt
<213>智人
<400>13
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalglnphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>14
<211>264
<212>prt
<213>智人
<400>14
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalaspphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>15
<211>264
<212>prt
<213>智人
<400>15
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuasnglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>16
<211>264
<212>prt
<213>智人
<400>16
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalgluphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>17
<211>264
<212>prt
<213>智人
<400>17
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalhisphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>18
<211>264
<212>prt
<213>智人
<400>18
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuaspglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalglnphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>19
<211>264
<212>prt
<213>智人
<400>19
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuglnglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalaspphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>20
<211>264
<212>prt
<213>智人
<400>20
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproproleuleuaspglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalaspphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>21
<211>264
<212>prt
<213>智人
<400>21
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalglnphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>22
<211>264
<212>prt
<213>智人
<400>22
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalaspphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>23
<211>264
<212>prt
<213>智人
<400>23
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalhisphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>24
<211>264
<212>prt
<213>智人
<400>24
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalgluphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>25
<211>264
<212>prt
<213>智人
<400>25
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglyalaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>26
<211>264
<212>prt
<213>智人
<400>26
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>27
<211>264
<212>prt
<213>智人
<400>27
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluarglyscyscysvalglucysproprocyspro
202530
gluprolyssercysasplysthrhisthrcysproprocysproala
354045
progluleuleuglyglyproservalpheleupheproprolyspro
505560
lysaspthrleumetileserargthrprogluvalthrcysvalval
65707580
valaspvalgluphegluaspprogluvallyspheasntrptyrval
859095
aspglyvalgluvalhisasnalalysthrlysproarggluglugln
100105110
tyrasnserthrtyrargvalvalservalleuthrvalleuhisgln
115120125
asptrpleuasnglylysglutyrlyscyslysvalthrasnlysala
130135140
pheproalaproileglulysthrileserlysalalysglyglnpro
145150155160
arggluproglnvaltyrthrleuproproserargaspgluleuthr
165170175
lysasnglnvalserleuthrcysleuvallysglyphetyrproser
180185190
aspilealavalglutrpgluserasnglyglnprogluasnasntyr
195200205
lysthrthrproprovalleuaspseraspglyserphepheleutyr
210215220
serlysleuthrvalasplysserargtrpglnglnglyasnvalphe
225230235240
sercysservalmethisglualaleuhisasnhistyrthrglnlys
245250255
serleuserleuserproglylys
260
<210>28
<211>264
<212>prt
<213>智人
<400>28
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproglualaalaglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalgluphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>29
<211>264
<212>prt
<213>智人
<400>29
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaproprovalalaglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalgluphegluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnserthrtyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
thrasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
aspgluleuthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>30
<211>264
<212>prt
<213>智人
<400>30
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproarggluproglnvaltyrthrleuproproserarg
145150155160
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglyalaleuhisasnhis
225230235240
tyrthrglnlystyrleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>31
<211>264
<212>prt
<213>智人
<400>31
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproargargproglnvaltyrthrleuproproserarg
145150155160
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglyalaleuhisasnhis
225230235240
tyrthrglnlystyrleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
<210>32
<211>264
<212>prt
<213>智人
<400>32
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrglygluprolyssercysasplysthrhisthrcyspro
202530
procysproalaprogluleuleuglyglyproservalpheleuphe
354045
proprolysprolysaspthrleumetileserargthrprogluval
505560
thrcysvalvalvalaspvalserhisgluaspprogluvallysphe
65707580
asntrptyrvalaspglyvalgluvalhisasnalalysthrlyspro
859095
argglugluglntyrasnseralatyrargvalvalservalleuthr
100105110
valleuhisglnasptrpleuasnglylysglutyrlyscyslysval
115120125
serasnlysalaleuproalaproileglulysthrileserlysala
130135140
lysglyglnproargargproglnvaltyrthrleuproproserarg
145150155160
gluglumetthrlysasnglnvalserleuthrcysleuvallysgly
165170175
phetyrproseraspilealavalglutrpgluserasnglyglnpro
180185190
gluasnasntyrlysthrthrproprovalleuaspseraspglyser
195200205
phepheleutyrserlysleuthrvalasplysserargtrpglngln
210215220
glyasnvalphesercysservalmethisglualaleuhisasnhis
225230235240
tyrthrglnlysserleuserleuserproglylysgluarglyscys
245250255
cysvalglucysproprocyspro
260
- 还没有人留言评论。精彩留言会获得点赞!