可逆保护的硫醇化亲电脂肪酸作为前药的制作方法
本申请要求于2016年10月5日提交的美国临时申请号62/404,368的权益,其全部内容通过引用并入本文。
技术实现要素:
本发明的各种实施方式涉及硫醇加合的硝基脂肪酸(“硫醇化脂肪酸”)的合成和用途。本发明的各种实施方式涉及包含有效量的硫醇化脂肪酸的药物组合物。本发明的各种实施方式涉及用于治疗炎症、肥胖症、代谢综合征、急性肾病、慢性肾病以及降低胃肠道副作用的方法,该方法包括向有此需要的受试者给药有效量的硫醇化脂肪酸。
政府利益
本发明是在由国立卫生研究院授予的资助号hl-058115、hl-64937和at006822下的政府支持下完成的。美国政府对本发明具有一定的权利。
附图说明
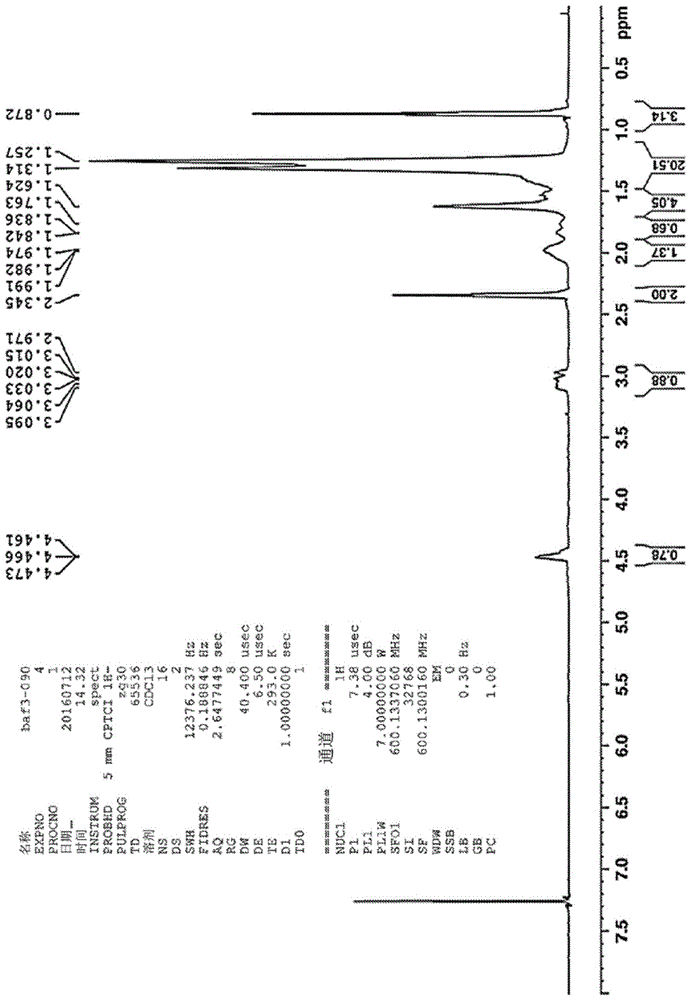
图1:oa-no2-sx的nmr谱。
图2:oa-no2-sx诱导的ho-1转录。
图3:oa-no2-sx诱导的nqo-1转录。
图4:oa-no2-sx诱导的gclm转录。
图5:oa-no2-sx在时间过程中诱导的ho-1转录。
图6:oa-no2-sx在时间过程中诱导的nqo-1转录。
图7:oa-no2-sx在时间过程中诱导的gclm转录。
具体实施方式
本发明不限于所描述的特定过程、组合物或方法,这是因为它们可以变化。说明书中使用的术语仅用于描述特定形式或实施方式的目的,并不旨在限制本发明的范围。除非另外定义,否则本文中使用的所有技术和科学术语具有的含义与本领域普通技术人员通常理解的含义相同。本文提及的所有出版物均通过引用整体并入本文。本文中的任何内容均不应被解释为承认本发明无权凭借在先发明而先于此类公开内容。
术语“衍生物”是指衍生自类似化合物的化合物,或者如果一个或多个原子被其他原子或原子团取代,则可以设想成由其他化合物产生的化合物。
术语“生物样品”是指组织、细胞、流体、细胞提取物、匀浆组织提取物,或者在合适的生理学上可接受的载体中的一种或多种酶的混合物,诸如包括但不限于脂质体、白蛋白和脂蛋白的混合物。
本发明的化合物可以以各种异构体形式存在,包括构型异构体、几何异构体和构象异构体,以及以各种互变异构形式存在,特别是那些在氢原子的连接点和一些结构异构体上不同的形式,在其中有不同数量的重复单元。术语“异构体”旨在包括本发明化合物的所有异构体形式,包括化合物的互变异构形式。
本文所述的某些化合物可以具有不对称中心并且因此以不同的对映体形式和非对映体形式存在。本发明的化合物可以是光学异构体或非对映异构体的形式。因此,本发明包括其光学异构体、非对映异构体及它们的混合物形式的化合物,包括外消旋混合物。本发明化合物的光学异构体可通过已知技术获得,诸如不对称合成、手性色谱、模拟移动床技术或者通过使用光学活性拆分剂经由立体异构体的化学分离。除非另有说明,“立体异构体”指化合物的一种立体异构体,其基本上不含该化合物的其他立体异构体。因此,具有一个手性中心的立体异构纯化合物基本上不含该化合物的相反对映体。具有两个手性中心的立体异构纯化合物基本上不含该化合物的其他非对映异构体。
术语“前药”指化合物的衍生物,其可以在体外或体内在生物条件下水解、氧化或以其他方式反应以提供活性化合物,特别是本发明的化合物。前药的实例包括但不限于,本发明化合物的衍生物和代谢物,其包括可生物水解的基团,诸如硝酸基、亚硝酸基、亚硝基化合物、可生物水解的酰胺、可生物水解的酯、可生物水解的氨基甲酸酯、可生物水解的硫醇基、可生物水解的硫酯、可生物水解的硒化物和可生物水解的磷酸酯类似物(例如,单磷酸酯、二磷酸酯或三磷酸酯)。例如,具有羧基官能团的化合物的前药是羧酸的低级烷基酯。羧酸酯是通过酯化分子上存在的任何羧酸部分而方便地形成的。前药通常可以使用熟知的方法制备,诸如burger’smedicinalchemistryanddrugdiscovery6thed.(wiley,2001)和designandapplicationofprodrugs(harwoodacademicpublishersgmbh,1985)所描述的方法。
如本文和所附权利要求书中所用,除非上下文另有明确说明,单数形式“一(a)”、“一(an)”和“该”包括复数指代。因此,例如,提及“细胞”是指一种或多种细胞及本领域技术人员已知的其等同物等。
如本文所用,术语“约”指所使用数的数值加或减10%。因此,约100mg意味着在90mg-110mg的范围内。
当与治疗手段联合使用时,“给药”指向患者施用治疗剂,由此该治疗剂正面地影响其靶向的组织。因此,如本文所用,当与本文所述的化合物联合使用时术语“给药”可以包括但不限于,通过例如静脉注射向受试者全身地提供本文所述的化合物,由此使治疗剂到达靶标组织。“给药”组合物可以通过例如注射、口服给药、局部给药或通过这些方法与其他已知技术结合来实现。给药可以是自我给药,其中需要这种治疗的受试者给药治疗剂或者可以由医学或其他健康护理专业人员或需要这种治疗的受试者的看护人来进行给药。
如本文所用的术语“动物”、“患者”或“受试者”包括但不限于,人和非人脊椎动物,诸如野生动物、家畜和农场动物。
术语“改善”用于表示本发明改变了其被提供、施加或给药的组织的特性和/或物理属性。术语“改善”还可以与疾病状态联合使用,使得当疾病状态“改善”时,与疾病状态相关的症状或生理特征减小、减少或消除。
术语“抑制”包括给药本发明化合物以预防症状的发作,缓解症状,或消除疾病、病症、疾患或其一种症状或多种症状。
“药学上可接受的”是指载体、稀释剂或赋形剂必须与制剂的其他成分相容并且对其接受者无害。
如本文所用,术语“治疗剂”是指用于阻止、对抗、改进、改善、预防、抑制、阻断或逆转患者的不希望的病症、疾病或症状的药剂,如特定实施方式所示。部分地,本发明的实施方式涉及炎性病症、肥胖症、代谢综合征、急性肾病、慢性肾病、动脉粥样硬化形成、脂肪生成、内膜增生、局部缺血/再灌注(i/r)和异型生物质损伤后的肾损伤、局灶性心肌i/r损伤、angii诱导的系统性高血压、肺动脉高压、心脏和肺纤维化、炎性肠疾病、伤害感受、中风、运动神经元变性、糖尿病、哮喘、copd、代谢综合征、高甘油三酯血症、脂肪肝疾病和自身免疫性疾病。
组合物的“治疗有效量”或“有效量”是为达到所希望效果即为了阻止、对抗、改进、改善、预防、抑制、阻断或逆转患者的不希望的病症、疾病或者症状而计算的预定量,如可以由特定实施方式所示。例如,“治疗方法”实施方式中所述的“治疗有效量”是为了达到所希望的治疗效果,即阻止、对抗、改进或改善不希望的病症、疾病或症状而计算的预定量。例如,“预防方法”实施方式中所述的“治疗有效量”是为了达到所希望的治疗效果,即在其发生之前预防或抑制或阻断不希望的病症、疾病或症状而计算的预定量。部分地,本发明的实施方式涉及炎性病症、肥胖症、代谢综合征、急性肾病、慢性肾病、动脉粥样硬化形成、脂肪生成、内膜增生、局部缺血/再灌注(i/r)和异型生物质损伤后的肾损伤、局灶性心肌i/r损伤、angii诱导的系统性高血压、肺动脉高压、心脏和肺纤维化、炎性肠疾病、伤害感受、中风、运动神经元变性、糖尿病、哮喘和copd。本发明方法考虑的活性包括医学治疗和/或预防治疗,视情况而定。当然,根据本发明给药以获得治疗和/或预防效果的化合物的具体剂量将由围绕病例的特定情况确定,包括例如给药的化合物、给药途径和正在治疗的病症。然而,将要理解的是,给药的有效量将由医师根据相关情况确定,包括待治疗的病症、待给药的化合物的选择和所选择的给药途径,并且因此,本文包括的剂量范围不旨在以任何方式限制本发明的范围。本发明化合物的治疗有效量通常是使得当其以生理学上可耐受的赋形剂组合物给药时足以在组织中实现有效的全身浓度或局部浓度的量。
如本文所用的术语“治疗(treat)”、“治疗(treated)”、“治疗(treating)”、“减轻”、“改善”或“促进”指治疗性治疗和预防性或预防的措施,其中目的是预防或减缓(减轻)不希望的生理病症、疾患或疾病,或者为了获得有益的或期望的临床结果。出于本发明的目的,有益的或期望的临床结果包括但不限于,缓解病症、疾患或疾病的症状;减小病症、疾患或疾病的程度;稳定(即,不恶化)病症、疾患或疾病的状态;保持病症、疾患或疾病;延迟病症、疾患或疾病发病或减缓病症、疾患或疾病的进展;以及缓和(无论是部分的还是全部的),无论是可检测的还是不可检测的,或者是病症、疾患或疾病的增强或改善。减轻或促进包括引起临床上显著的响应而没有过多的副作用。
一般而言,术语“组织”指在呈现特定功能中结合起来的类似特化细胞的任何聚集。
硝基脂肪酸是通常在对氧化和硝化应激响应下或在饮食中升高的化合物。这些化合物已被认为是各种病症(诸如炎性病症、肥胖、代谢综合征、急性肾病、慢性肾病、动脉粥样硬化形成、脂肪生成、内膜增生、肾脏i/r和异型生物质损伤、局灶性心肌i/r损伤、angii诱导的系统性高血压、肺动脉高压、心脏和肺纤维化、炎性肠病、伤害感受、中风、运动神经元变性、糖尿病、哮喘和copd)的潜在抗氧化和抗炎治疗剂。特别地,硝基油酸(no2-oa)是许多研究的主题。硝基油酸影响许多调节通路,包括nrf2、nf-κb、热休克因子(hsf)、ppar-γ,其引起了抗氧化和抗炎作用。此外,硝基油酸引起了黄嘌呤氧化酶、可溶性环氧化物水解酶和5-脂氧合酶的直接酶抑制。由硝基脂肪酸修饰的其他通路包括:细胞外信号调节激酶、jun氨基末端激酶、p38丝裂原活化蛋白激酶、信号转导子和转录活化因子1、tnf受体相关因子6和toll样受体4。
然而,使用硝基油酸作为候选药物的一个潜在障碍是由于β-氧化反应和前列腺素还原酶1还原硝基烯烃和肝脏首过以及与谷胱甘肽的可逆内收和排泄中的快速代谢。为了增加功效,药物必须经受首过代谢。活性药物将在肠道微生物群和肝脏内代谢,并且因此必须加以保护,以便适当地将有效量的活性药物递送到循环中。
通过可逆硫醇化硝基烯烃来修饰no2-oa防止了其代谢失活,从而保持了no2-oa的潜在亲电特性。
本文提出的本发明的实施方式通常涉及硫醇化的亲电不饱和活化脂肪酸,特别是硫醇化不饱和硝化脂肪酸。如本文所用,“活化脂肪酸”是指具有至少一个与脂肪酸的饱和或不饱和脂肪链的不饱和碳共价结合的吸电子基团的脂肪酸。这种活化脂肪酸可以包括在烃链上任意数量的位置处被任意数量的吸电子基团取代的脂肪链,并且这种吸电子基团与碳-碳双键可以缔合或不缔合。类似地,本文所述的硫醇化活化脂肪酸可以包括具有任何数量双键的脂肪链,其与吸电子基团可以缔合或不缔合;以及含硫基团,即硫醇基团。在某些实施方式中,含硫基团可以位于不饱和脂肪链的贝塔(β)碳、伽马(χ)碳或德尔塔(δ)碳上,其中吸电子基团连接至阿尔法(α)碳。
硝基烯烃的亲电双键由h(s)xr可逆保护,形成了硫醇化活化脂肪酸。该硫醇化活化脂肪酸现在是前药并且避免了首过期间的代谢过程。在失去保护基团后,亲电双键再生,如下所示:
例如,一些实施方式的硫醇化活化脂肪酸可以具有通式i:
其中,r是氢(-h)、甲基或c2至c6烷基、烯基或炔基,或(s)xr可以是含硫官能团,诸如,硫基(-sooh)、磺基(-soooh)或硫氰酸根(-scn),x为1至5的整数,且q和m各自独立地为1至10的整数。式i的化合物包括在β碳上的含硫基团。
其他硫醇化活化脂肪酸包括通式ii的化合物:
其中,r是氢(-h)、甲基或c2至c6烷基、烯基或炔基,或(s)xr可以是含硫官能团,诸如,硫基(-sooh)、磺基(-soooh)或硫氰酸根(-scn),x为1至5的整数,且q和m各自独立地为1至10的整数。式ii的化合物包括δ碳上的含硫基团。
在一些实施方式中,对于式i或ii,r可以是双官能烷基、烯基或炔基,其与活化脂肪酸的羧基连接形成桥联或环状结构。在此类实施方式中,含硫部分可位于β、χ或δ碳上。例如,通式iiia和iiib的化合物,其包括在β碳上环化的双官能含硫部分:
其中每个y独立地为氧(o)或氮(n),每个x独立地为1至5的整数,并且q、m、p和t各自独立地为1至10的整数。
在一些实施方式中,含硫基团可以连接两个活化脂肪酸。例如,本发明的各种实施方式涉及通式iv的化合物:
其中r1和r2独立地选自-h和任何吸电子基团,包括但不限于-coh、-cor、-cooh、-coor、-cl、-f、-br、-i、-cf3、-cn、-so3-、-so2r、-so3h、-nh3+、-nh2r+、-nhr2+、-nr3+以及-no2;其中r1和r2中的至少一个是吸电子基团;其中y1和y2独立地选自-h、-coh、-cor、-cooh和-coor;其中r1和r2中的至少一个是吸电子基团;以及其中x是1至5的整数,q、m、p和t独立地是1至10的整数,并且含有相同组分的组合物。
本发明的各种实施方式涉及通式va、vb和vc的化合物:
其中x是1至5的整数,q、m、p和t独立地是1至10的整数,并且含有相同组分的组合物。
其他实施方式包括式vi的化合物:
其中x是1至5的整数,并且含有相同组分的组合物。
在一些实施方式中,该化合物是如式vii所示的硫醇化硝基-油酸(no2-oa-sx)物质:
吸电子基团可以以顺式或反式构型定位在原始双键中,或在sp3手性/立体异构中心以r或s绝对立体化学定位。例如,在一种实施方式中,硫醇化活化脂肪酸可以具有一个吸电子基团,而在另一种实施方式中,硫醇化活化脂肪酸可以在沿烃链的多个位置被多个吸电子基团取代。虽然本发明的硫醇化活化脂肪酸可以具有位于沿羧基末端碳与末端甲基(ω-位置)之间的脂肪族烃链的任何碳上的吸电子基团,但在一些实施方式中,可将吸电子基团定位于羧基末端碳和/或甲基末端碳的约3个碳内,并且在其他实施方式中,吸电子基团可以定位于羧基末端碳和/或甲基末端碳的5个碳内。在其他实施方式中,吸电子基团可以定位于羧基末端碳和/或甲基末端碳的7个碳内,并且在另外的实施方式中,吸电子基团可以位于羧基末端碳和/或甲基末端碳的9个碳内。
在某些实施方式中,吸电子基团可以定位于源自活化脂肪酸的双键的碳上,形成“吸电子乙烯基”基团。这种乙烯基的吸电子基团可以在双键的任一侧。本发明实施方式包括的脂肪酸可以具有位于脂肪族烃链上的任何碳上的一个或多个吸电子乙烯基,并且有几种方式使得不饱和脂肪酸可以具有一个吸电子基团。在一种实施方式中,硫醇化活化油酸(十八碳-9-烯酸),其源自18碳,ω-9脂肪酸,在9h(c-9)和10th(c-10)之间具有一个双键(表示为“18:1”),可以在c-9或c-10处具有吸电子基团,并且在间隔位置处具有硫醇基(-sr)。在另一种示例性实施方式中,硫醇化活化亚油酸(十八碳-9,12,-二烯酸),其源自18碳,ω-6脂肪酸,在ω-6(c-13)和-7(c-12)碳以及ω-9(c-10)和10(c-9)碳之间具有两个双键(表示为“18:2”),可以在c-9或c-10或c-12或c-13处具有吸电子基团并且在相应的间隔邻位处具有的硫醇基(-sr)。类似地,最初具有3、4、5、6或更多个双键的其他多不饱和脂肪酸可以在任何原始双键碳上的任一位置具有一个吸电子,并且在相应的间隔邻位处具有硫醇基(-sr),包括所有可能的位置排列和吸电子基团。
在其他实施方式中,单或多不饱和脂肪酸可以具有两个吸电子基团,并且有几种方式使得不饱和脂肪酸可以具有两个吸电子基团。例如,在一种实施方式中,硫醇化活化亚油酸(十八碳-9,12,-二烯酸),其源自18碳,ω-6脂肪酸,在ω-6(c-13)和-7(c-12)碳以及ω-9(c-10)和10(c-9)碳之间具有两个双键(表示为“18:2”),可以在c-9、c-10、c-12或c-13的任何两个位置处具有吸电子基团,具有以下可能的排列:c-9和c-12,c-9和c-13,c-10和c-12,或c-10和c-13,以及在相应的间隔邻位处具有一个或多个硫醇基(-sr)。
类似于具有一个吸电子基团或两个吸电子基团的前述化合物,其还可以具有三个、四个、五个或更多个吸电子基团。按照上述相同的逻辑,在具有一个吸电子基团或两个吸电子基团的前述化合物中,共轭或非共轭的具有3、4、5、6或更多个双键的多不饱和脂肪酸可以在任何双键碳上的任何位置处具有多个吸电子(三个、四个、五个或更多个作为用于取代许可的可用位置),包括位置、亲核取代基和吸电子基团的所有可能的排列。另外,在如上所述的任何实施方式中,任何数量的非吸电子基团可以与活化脂肪酸的脂肪链的碳共价结合。例如,在一些实施方式中,本发明的硫醇化活化脂肪酸可以包括一个或多个甲基、c2-c6烷基、烯基或炔基或氨基共价连接至硫醇化活化脂肪酸的脂族链的一个或多个碳。
术语“吸电子基团”在本领域中是公认的并且是指取代基从相邻原子吸引价电子的趋势,即,取代基相对于相邻原子是电负性的。术语“亲核基团”或“给电子基团”在本领域中是公认的并且是指取代基向相邻原子提供过量的价电子的趋势,即,取代基相对于相邻原子是正电性的。哈米特西格玛(hammettsigma)(σ)常数给出了吸电子能力水平的量化(参见,例如,j.march,advancedorganicchemistry,mcgrawhillbookcompany,newyork,(1977edition)pp.251-259)。哈米特常数值对于给电子基团通常是负的并且对于吸电子基团是正的。例如,对位取代的nh2(σ[p])的hammet常数约为-0.7,以及硝基的σ[p]约为+0.8。
本发明的实施方式包括任何已知的吸电子基团。例如,吸电子基团可包括但不限于,醛基(-coh)、酰基(-cor)、羧基(-cooh)、酯基(-coor)、卤素(-cl、f、-br等)、氟甲基(-cf3)、氟代烷基(-cfnh2-nr)、氰基(-cn)、亚砜基(-sor)、磺酰基(-so2r)、磺酸基(so3r)、1°,2°和3°铵基(-nr3+)和硝基(-no2),其中每个r可以独立地是氢基、甲基或c2至c6烷基、链烯基或炔基。在一些实施方式中,吸电子基团可以是具有至少约0.2σ的强吸电子基团,并且在某些实施方式中,吸电子基团可以形成偶极。例如,在特定实施方式中,吸电子基团可以是硝基、铵基或磺酰基。在其他实施方式中,本发明的硫醇化活化脂肪酸可以另外被非吸电子基团或给电子基团取代,包括例如硫醇基(-sr)、醇(-oh)、逆酯(-oocr)、烷基、烯基、炔基、1°和2°氨基(-nr2)、含n杂环(-n=、-nr-)、硝酸酯基(-ono2)、亚硝酸酯基(-ono)等。
实施方式的脂肪酸可以是本领域已知的任何不饱和和多不饱和脂肪酸。术语“脂肪酸”描述脂肪族一元羧酸。各种实施方式包括具有脂肪族烃链的活化脂肪酸,具有脂肪族烃链的活化脂肪酸与已鉴定的天然存在的脂肪酸相同或相似。例如,已知天然存在的脂肪酸的脂肪族烃链通常是非支链的并且含有从约4个至约24个偶数个碳,并且其他包括在脂肪族烃链中具有12个至18个碳的脂肪酸。在其他实施方式中,脂肪酸可以在脂肪族烃链中具有大于24个碳。本发明的实施方式包括这样的天然存在的脂肪酸以及非天然存在的脂肪酸,其可以含有奇数个碳和/或包含杂原子的非天然存在的接头。因此,本发明的一些实施方式包括具有奇数个碳原子的脂肪酸,例如从5个至23个碳,并且在其他实施方式中,从11个至17个碳。在其他实施方式中,实施方式的脂肪酸可具有大于23个碳。本发明的天然和非天然存在的脂肪酸还可以沿烃链的一个或多个位置处支化,并且在各种实施方式中,每个支链可以包括从1个至24个碳、2个至20个碳或4个至18个碳的脂肪族烃链,其中每个支链可具有偶数个或奇数个碳。
各种实施方式的脂肪酸的脂肪族烃链可以是不饱和的或多不饱和的。术语“不饱和的”是指具有包括至少一个双键和/或取代基的脂肪族烃链的脂肪酸。相反,“饱和的”烃链不包括任何双键或取代基。因此,烃链的每个碳是“饱和的”并且具有最大数量的氢。“多不饱和”通常是指具有带有多于一个双键的烃链的脂肪酸。各种实施方式的不饱和或多不饱和脂肪酸的双键可以在沿脂肪族烃链的任何位置处,并且可以是顺式或反式构型。术语“顺式”是指在双键中与双键相邻的碳在同一侧,并且术语“反式”是指在双键中与双键相邻的碳在相对侧。通常“顺式”与z相同,“反式”与e相同,但有时用于命名化合物的iupac规则将给出与非碳取代基相反的情况,这是硝基烯烃的典型情况。例如,硝基烯烃可以具有两个碳基团“顺式”,但优先考虑化合物命名的两个基团(烯烃的一个碳上的硝基和烯烃的另一个碳上的碳基团)是相对的,因此是e。因此,“顺式”双键的硝基烯烃类似物称为e硝基烯烃。类似地,“反式”双键的硝基烯烃类似物称为z硝基烯烃。不希望受理论束缚,沿碳链的顺式构型的双键(顺式碳链,但是e硝基烯烃)可以在烃链中引起弯曲。沿着碳链的“反式”构型的双键(反式碳链但是z硝基烯烃)可能不会引起烃链弯曲。本发明的实施方式可以包括具有顺式或反式构型的双键的硫醇化活化脂肪酸,并且包括可以包括以下的组合物:包含硫醇化活化脂肪酸和硫醇化活化脂肪酸的区域异构体的顺式和反式的组合。
许多不饱和和多不饱和脂肪酸是已经鉴定了的并且已知它们是天然存在的。这种不饱和或多不饱和天然存在的脂肪酸通常在其脂肪族烃链中包含偶数个碳。例如,天然存在的不饱和或多不饱和脂肪酸可以具有4、6、8、10、12、14、16、18、20、22等个碳并且可包括欧米伽(ω)-3、ω-5、ω-6、ω-7、ω-9碳-碳双键。任何此类脂肪酸可用于本发明的实施方式中。符号“ω”用于表示脂肪族烃链的末端甲基碳。ω-x脂肪酸的双键的位置是从ω碳x数量个碳的碳-碳键。例如,ω-6脂肪酸在从ω-碳倒数的第6个和第7个碳之间具有双键,并且ω-3脂肪酸在从ω-碳倒数的第3个和第4个碳之间具有双键。本发明的各种实施方式包括硝化的ω-3脂肪酸,包括但不限于亚麻酸、α-亚麻酸、二十碳五烯酸、二十二碳五烯酸、二十二碳六烯酸和十八碳四烯酸;硝化的ω-5脂肪酸,包括但不限于肉豆蔻酸;硝化的ω-6脂肪酸,包括但不限于亚油酸、γ-亚油酸、二高-γ-亚油酸和花生四烯酸;硝化的ω-7脂肪酸,包括但不限于共轭亚油酸和棕榈油酸;以及硝化的ω-9脂肪酸,包括但不限于油酸和芥酸。当然,本发明的脂肪酸也可以使用iupac命名法来指代,其中双键的位置通过从羧酸的碳计数来确定,并且‘c-x’指使用iupac命名法的脂肪族烃中的碳,其中x是从羧酸(包括羰基碳本身)计数的碳的数量。本发明的实施方式还包括天然存在的脂肪酸及其衍生物的合成等同物。
本发明的其他实施方式包括不饱和或多不饱和的非天然存在的脂肪酸,其可以具有奇数个碳,诸如,例如5、7、9、11、13、15、17、19、20、21等。如在天然存在的脂肪酸中,与非天然存在的脂肪酸相关的一个或多个双键可以位于沿脂肪族烃链的任何位置,并且双键可以以顺式或反式构型。在其他实施方式中,非天然存在的脂肪酸可包括中断脂肪族烃链的一个或多个接头基团。例如,在一些实施方式中,活化脂肪酸在脂肪族烃链内的任何位置可以具有一个或多个非碳-碳键,诸如例如酯、醚、乙烯基醚、硫醚、氨基、亚胺等。
本发明的各种实施方式包括不饱和或多不饱和脂肪酸,其可以在脂肪酸的脂肪族链的任何两个碳之间具有碳-碳双键,并且在这种多不饱和脂肪酸中可以存在任何数量的碳-碳双键。例如在一些实施方式中,多不饱和脂肪酸可具有2、3、4、5、6或更多个碳-碳双键。在这种实施方式中,多于一个碳-碳双键中的每个碳-碳双键可以单独地以顺式或反式构型。在一些实施方式中,硫醇化活化脂肪酸衍生自与具有相关吸电子基团的多不饱和脂肪酸的至少一个碳-碳双键反应,并且在其他实施方式中,这种多不饱和脂肪酸的多于一个碳-碳双键可以具有相关的吸电子基团与。另外,在这样的实施方式中,吸电子基团可以与原始碳-碳双键的碳或与碳-碳双键的碳直接相邻的碳缔合,并且硫醇可以与原始碳-碳双键的其他碳或与碳-碳双键的碳直接相邻的碳缔合。例如,在一些实施方式中,吸电子基团可以连接到前碳-碳双键的阿尔法(α)碳,并且在其他实施方式中,吸电子基团可以与前碳-碳双键的贝塔(β)碳缔合。在那些实施方式中,硫醇将分别连接到前碳-碳双键的贝塔(β)碳,并且在其他实施方式中,吸电子基团可以与前碳-碳双键的阿尔法(α)碳缔合。
在特定实施方式中,具有至少一个吸电子基团的不饱和脂肪酸可以是共轭脂肪酸。在这样的实施方式中,脂肪族链中的两个碳-碳双键彼此相邻,使得它们之间不存在亚甲基。这种共轭化合物通常称为1,3-二烯或共轭脂肪酸。这种1,3-二烯可以包括位于1,3-二烯的1、2、3和/或4位以及与二烯相邻的两个碳的6个位置中的任何位置的一个或多个吸电子基团(位于0位和5位,相对于鉴定1,3-二烯中的碳的1、2、3、4方法)。例如,一个相关的吸电子基团可以连接到上面鉴定的6个位置中的任何一个,即连接到二烯上的1、2、3或4位或连接到与1,3-相邻的任一个碳上(位于0位或5位,如上所述)。在另外的实施方式中,两个相关的吸电子基团可以连接到六个可能位置中的任何两个,三个相关的吸电子基团可以连接到六个可能位置中的任何两个,四个相关的吸电子基团可以连接到六个可能位置中的任何两个,五个相关的吸电子基团可以连接到六个可能的位置中的任何两个,以及六个相关的吸电子基团可以连接到六个可能位置中的任何两个。总之,本发明的实施方式包括连接至1,3-二烯中上述六个位置中的任何一个位置的吸电子基团的任何构型。
在某些实施方式中,本发明的硫醇化活化脂肪酸可以在制备后进行异构化使得双键的顺式/反式构型、碳链中双键的位置或者两者都可以改变。例如,在一些实施方式中,硫醇化活化脂肪酸可以由具有与碳-碳双键的伽马碳连接的吸电子基团的碳-碳双键制备。在制备之后,碳-碳双键可以进行异构化使得吸电子基团现在在异构化后与碳-碳双键共轭。这种异构化可以在制备后的任何时间自发发生,并且可以得到组合物,该组合物可以最初制备成包括硫醇化活化脂肪酸的单一种类,其随后包括最初产生的首先制备的活化脂肪酸的异构体的组合。
在其他实施方式中,可以修饰硫醇化活化脂肪酸的羧基末端。例如,在一些实施方式中,硫醇化活化脂肪酸可以包括与脂肪酸的羧基末端缔合的甘油以产生甘油脂,并且这种甘油脂可为甘油单酯、甘油二酯或甘油三酯,其中甘油二酯或甘油三酯的至少一种脂肪酸可以是硫醇化活化脂肪酸,并且任何剩余的脂肪酸可以是饱和或不饱和的脂肪酸。类似地,在其他实施方式中,碳水化合物可以与硫醇化活化脂肪酸的羧基末端缔合以形成糖脂。在这种实施方式中,本领域已知的任何碳水化合物可以是糖脂的碳水化合物部分,包括但不限于半乳糖和葡萄糖。在其他实施方式中,碳水化合物可以与甘油酯缔合,该甘油酯与硫醇化活化脂肪酸的羧基末端缔合,以形成甘油-糖脂,其可以具有与甘油-糖脂的甘油部分缔合的一种或两种活化脂肪酸,并且,在仅有一种活化脂肪酸与甘油-糖脂缔合的实施方式中,甘油上的剩余位置可以包括饱和或不饱和脂肪酸或氢、烷基或官能团,诸如例如,醇、胺、磷酸、膦酸、硫醇、磺酸等。在某些实施方式中,本发明的活化脂肪酸的羧基末端可以与磷酸缔合以形成磷脂。在这样的实施方式中,磷酸可以通过羧基末端与脂肪酸直接缔合,或者磷酸可以与甘油二酯缔合,其中一个或两个活化脂肪酸与甘油部分连接,并且在仅有一个硫醇化活化脂肪酸与甘油连接的实施方式中,甘油上的剩余位置可以包括饱和或不饱和脂肪酸或氢、烷基或官能团,诸如例如,醇、胺、磷酸、膦酸、硫醇、磺酸等。在另外的实施方式中,活化脂肪酸的羧基末端可以与胆固醇或其他甾醇部分缔合。在其他实施方式中,羧基末端可以通过共价连接第二活性剂来修饰。在特定实施方式中,包括甘油的羧基末端修饰可以不包括硝基。不希望受理论束缚,硫醇化活化脂肪酸的羧基末端的修饰可以增强给药后活化脂肪酸的分配(区分,partitioning),并且还可以通过抑制给药后线粒体中的贝塔氧化来改善活化脂肪酸的复原力(恢复性,resilience)。
本发明化合物提高了作为硫醇化分子内二聚体存在的活化脂肪酸的生物利用度。亲电子烯烃的硫醇化通过肠道和肝脏的首过代谢来保护分子。这种保护通过防止烯烃被前列腺素还原酶1的还原和通过延迟谷胱甘肽的加合而发生。此外,多硫化物链越长,分子的稳定性越大,提供了活化脂肪酸在循环中的延长释放。当硫醇化硝基脂肪酸释放硝基脂肪酸和硫化氢时,提供了额外的保护措施。
本文所示的一些实施方式中,硫醇化脂肪酸释放多硫化氢,并且在至少一种实施方式中释放硫化氢。硫化氢(h2s)以及一氧化氮和一氧化碳是生物活性气体,通常称为气体递质(gasotransmitter)或气体介质(gasomediator)。h2s由细胞内的半胱氨酸通过胱硫醚γ裂解酶、胱硫醚β合成酶或3-巯基丙酮酸硫转移酶作为反式硫化途径的延伸来合成,并且主要以其阴离子形式hs-发现。hs-的反应性主要受其还原性和亲核性以及硫与过渡金属形成复合物的能力的影响。h2s修饰蛋白质、调节离子通道功能、抑制细胞凋亡并限制内皮细胞、平滑肌细胞、炎症细胞、线粒体、内质网和核转录因子中的氧化应激。特别地,h2s激活katp和瞬时受体电位(trp)通道并抑制大电导ca2+敏感k+(bkca)通道、t型钙通道和m型钙通道以及改变nf-κb核转位和许多激酶,包括p38、erk和akt。这些改变的细胞和代谢途径与改善的心血管稳态和健康有关。h2s积极参与血管保护、血压调节并防止心肌损伤和炎症。
在一些实施方式中,可以给药硫醇化脂肪酸以达到h2s的生理学和/或药理学水平以保护血管、调节血压并限制心肌损伤和炎症。硫醇化脂肪酸将在循环中释放h2s以保护远端器官免于炎症、缺血和再灌注、灌注不足、缺氧和组织缺氧并维持血管稳态。
在本文所述的实施方式中,硫醇化活化脂肪酸的治疗有效量为从约5毫克至约5000毫克。在上述各种实施方式中,硫醇化活化脂肪酸的治疗有效量可以是每日剂量或在下限量和上限量的范围内的单剂量。在一些实施方式中,下限量是约5mg、约10mg、约25mg、约50mg、约75mg、约100mg、约125mg、约150mg、约175mg、约200mg、约225mg、约250mg、约275mg、约300mg、约325mg、约350mg、约375mg、约400mg、约425mg、约450mg、约475mg、约500mg、约525mg、约550mg、约575mg、约600mg、约625mg、约650mg、约675mg、约700mg、约725mg、约750mg、约775mg、约800mg、约825mg、约850mg、约875mg、约900mg、约925mg、约950mg、约975mg、约1000mg、约1500mg、约2000mg、约2500mg、约3000mg、约3500mg、约4000mg、约4500mg。在一些实施方式中,上限量为约5000mg、约4500mg、约4000mg、约3500mg、约3000mg、约2500mg、约2000mg、约1500mg、1000mg、约975mg、约950mg、约925mg、约900mg、约875mg、约850mg、约825mg、约800mg、约775mg、约750mg、约725mg、约700mg、约675mg、约650mg、约625mg、约600mg、约575mg、约550mg、约525mg、约500mg、约475mg、约450mg、约425mg、约400mg、约375mg、约350mg、约325mg、约300mg、约275mg、约250mg、约225mg、约200mg、约175mg、约150mg、约125mg、约100mg、约75mg或约50mg。在一些实施方式中,日剂量可以是先前公开的范围的上限和下限之间的任何范围。在一些实施方式中,日剂量可以为从约25mg至小于约450mg、约25mg至约425mg、约25mg至约400mg、约25mg至约375mg、约25mg至约350mg、约25mg至约325mg、约25mg至约300mg、约25mg至约275mg、约25mg至约250mg、约25mg至约225mg、约25mg至约200mg、约25mg至约175mg或约25mg至约150mg。在一些实施方式中日剂量可以为从约50mg至约450mg、约75mg至约450mg、约100mg至约450mg、约150mg至约450mg、约175mg至约450mg、约200mg至约450mg、约225mg至约450mg、约250mg至约450mg或约275mg至约450mg。
在本文所述的实施方式中,如上所述的日剂量可每天给药一次。在本文所述的实施方式中,如上所述的日剂量可以每天两次等量给药。在本文所述的实施方式中,如上所述的日剂量可以每天三次等量给药。在本文所述的实施方式中,如上所述的日剂量可以每天四次等量给药。
在本文所述的实施方式中,硫醇化活化脂肪酸的治疗有效量可随治疗进展而变化。例如,当治疗通过给药周期进行时,日剂量(或剂量方案)可以增加或减少,或者日剂量可以在整个给药期间增加或减少。
上述硫醇化活化脂肪酸可以制备成药学上可接受的制剂。术语“药学上可接受的”在本文中用于表示该化合物适用于药物产品中。例如,药学上可接受的阳离子包括金属离子和有机离子。更优选的金属离子包括但不限于,适当的碱金属盐、碱土金属盐和其他生理学上可接受的金属离子。示例性离子包括其通常化合价的铝、钙、锂、镁、钾、钠和锌。优选的有机离子包括质子化的叔胺和季铵阳离子,包括部分三甲胺、二乙胺、n,n'-二苄基乙二胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、葡甲胺(n-甲基葡糖胺)和普鲁卡因。示例性的药学上可接受的酸包括但不限于,盐酸、氢碘酸、氢溴酸、磷酸、硫酸、甲磺酸、乙酸、甲酸、酒石酸、马来酸、苹果酸、柠檬酸、异柠檬酸、琥珀酸、乳酸、葡糖酸、葡糖醛酸、丙酮酸、草酰乙酸、富马酸、丙酸、天冬氨酸、谷氨酸、苯甲酸等。
本发明的硫醇化活化脂肪酸的异构体和互变异构形式以及这些化合物的药学上可接受的盐也包括在本发明中。示例性的药学上可接受的盐由甲酸、乙酸、丙酸、琥珀酸、乙醇酸、葡糖酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、葡糖醛酸、马来酸、富马酸、丙酮酸、天冬氨酸、谷氨酸、苯甲酸、邻氨基苯甲酸、甲磺酸、硬脂酸、水杨酸、对羟基苯甲酸、苯乙酸、扁桃酸、扑酸(embonic)(帕莫酸(pamoic))、甲磺酸、乙磺酸、苯磺酸、泛酸、甲苯磺酸、2-羟基乙磺酸、磺胺酸、环己基氨基磺酸、褐藻酸(algenic)、βl羟基丁酸、半乳糖二酸和半乳糖醛酸制备。
与本发明的硫醇化活化脂肪酸结合使用的合适的药学上可接受的碱加成盐包括金属离子盐和有机离子盐。示例性金属离子盐包括但不限于,适合的碱金属(第ia族)盐、碱土金属(第iia族)盐和其他生理学上可接受的金属离子。这些盐可以由铝、钙、锂、镁、钾、钠和锌的离子制成。优选的有机盐可以由叔胺和季铵盐制成,包括部分三甲胺、二乙胺、n,n'-二苄基乙二胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、葡甲胺(n-甲基葡糖胺)和普鲁卡因。所有上述盐可以由本领域技术人员通过常规方法由本发明相应的化合物制备。
在本文所述的实施方式中,给药治疗有效量的硫醇化活化脂肪酸或其药学上可接受的盐还包括给药第二剂。在本文所述的实施方式中,第二剂可选自由以下组成的组:ace抑制剂、血管紧张素ii受体阻断剂或其组合。在一些实施方式中,第二剂可以是依那普利(elanapril)。在本文所述的实施方式中,ace抑制剂可以选自由以下组成的组:培哚普利、卡托普利、依那普利、赖诺普利、雷米普利、佐芬普利、喹那普利、贝那普利、咪达普利、群多普利、西拉普利和福辛普利。在本文所述的实施方式中,血管紧张素ii受体阻断剂可以选自由以下组成的组:阿齐沙坦、坎地沙坦、依普沙坦、厄贝沙坦、氯沙坦、奥美沙坦、替米沙坦、缬沙坦、非马沙坦和螺内酯。
在本文所述的实施方式中,第二剂的治疗有效量为从约2.5毫克至小于约250毫克。在本文所述的实施方式中,第二剂的日剂量可以为从约5mg至约200mg、约10mg至约150mg、约15mg至约100mg、约20mg至约75mg、约25mg至约50mg或约30mg至约40mg。
本发明的硫醇化活化脂肪酸可以任何常规方式通过它们具有活性的任何途径给药。给药可以是全身的或局部的。例如,给药可以是但不限于,肠胃外、皮下、静脉内、肌肉内、腹膜内、透皮、口服、口腔或眼部途径,或鼻内、阴道内、通过吸入、通过积存注射或通过植入。在本文所述的实施方式中,给药可以是肠胃外给药或静脉内给药,所有给药均存在或不存在有利于延长的全身摄取、组织半衰期和细胞内递送的稳定添加剂。因此,本发明化合物(单独或与其他药物组合)的给药方式可以是可注射的(包括皮下或肌内注射的短效、积存、植入和颗粒形式)。在本文所述的实施方式中,可以将包含硫醇化活化脂肪酸的可注射制剂沉积至损伤或炎症部位,诸如,例如,由于关节镜检查、血管成形术、支架置入、旁路手术等的手术切口部位或炎症部位。
本发明的各种实施方式还涉及用于给药硫醇化活化脂肪酸的方法。具体的给药方式可以变化并且可以取决于适应症。临床医生可以根据临床医生已知的方法调整或定量(titrate)特定给药途径和剂量方案的选择,以获得最佳临床响应。化合物的给药量是治疗有效量。待给药的剂量取决于所治疗的受试者的特征,例如,所治疗的特定动物、年龄、体重、健康、同时治疗的类型(如果有的话)和治疗频率,并且可以由本领域技术人员(例如,由临床医生)容易地确定。本领域技术人员将理解,剂量可以在指导下确定,例如,根据goodman&gilman'sthepharmacologicalbasisoftherapeutics,ninthedition(1996),appendixii,pp.1707-1711或根据goodman&gilman'sthepharmacologicalbasisoftherapeutics,tenthedition(2001),appendixii,pp.475-493,这两者都通过引用整体并入本文。此外,在根据动物研究确定人体等效剂量中,可以使用美国卫生与公众服务部食品药品管理中心(u.s.departmentofhealthandhumanservicesfoodanddrugadministrationcenter)的药物评估和研究的出版物(drugevaluationandresearch'spublication)。
http://www.fda.gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm8932.pdf.
含有上述发明的化合物和合适载体的药物制剂可以是各种形式,包括但不限于,包括有效量的本发明的硫醇化活化脂肪酸的固体、溶液、粉末、流体乳液、流体悬浮液、半固体和干粉。本领域还已知活性成分可以与药学上可接受的稀释剂、填充剂、崩解剂、粘合剂、润滑剂、表面活性剂、疏水载体、水溶性载体、乳化剂、缓冲剂、湿润剂、保湿剂、增溶剂、抗氧化剂、防腐剂等一起包含在这些制剂中。给药的手段和方法是本领域已知的,并且技术人员可以参考各种药理学的指导参考文献。例如,modernpharmaceutics,banker&rhodes,marceldekker,inc.(1979);和goodman&oilman's,thepharmaceuticalbasisoftherapeutics,6thedition,macmillanpublishingco.,newyork(1980),这两者都通过引用整体并入本文。
本发明的化合物可以配制用于通过注射,例如通过推注或连续输注进行肠胃外或静脉内给药。用于注射的制剂可以以单位剂型存在,例如在带有添加的防腐剂的安瓿或多剂量容器中。该组合物可以采取如油性或水性载体中的悬浮液、溶液或乳液的这些形式,并且可以含有配制剂诸如悬浮剂、稳定剂和/或分散剂。
可以使用合适的分散剂或润湿剂和悬浮剂根据已知技术配制可注射制剂,例如无菌可注射水性或油性悬浮液。无菌可注射制剂还可以是在无毒的肠胃外可接受的稀释剂或溶剂中的无菌可注射溶液或悬浮液,例如,作为1,3-丁二醇中的溶液。可以使用的可接受的载体和溶剂包括水、林格氏溶液和等渗氯化钠溶液。此外,无菌的固定油通常用作溶剂或悬浮介质。为此目的,可以使用任何温和的固定油,包括合成的甘油单酯或甘油二酯。此外,脂肪酸稀释剂诸如油酸可用于制备注射剂。可用于本发明实施方式的其他脂肪酸稀释剂包括,例如,硬脂酸、金属硬脂酸盐、硬脂酰富马酸钠、脂肪酸、脂肪醇、脂肪酸酯、山嵛酸甘油酯、矿物油、植物油、石蜡、亮氨酸、二氧化硅、硅酸、滑石、丙二醇脂肪酸酯、聚乙氧基化蓖麻油、聚乙二醇、聚丙二醇、聚亚烷基二醇、聚氧乙烯-甘油脂肪酸酯、聚氧乙烯脂肪醇醚、聚乙氧基化甾醇、聚乙氧基化蓖麻油、聚乙氧基化植物油等中的一种或多种。在一些实施方式中,脂肪酸稀释剂可以是脂肪酸的混合物。在一些实施方式中,脂肪酸可以是脂肪酸酯、脂肪酸的糖酯、脂肪酸的甘油酯或乙氧基化的脂肪酸酯,并且在其他实施方式中,脂肪酸稀释剂可以是脂肪醇,诸如,例如,脂肪醇、月桂醇、棕榈醇、棕榈醇酸、十六烷醇、辛醇(caprylalcohol)、辛酰醇(caprylylalcohol)、油醇、亚麻醇、花生四烯醇、山嵛醇、异山嵛醇、鲨油醇(selachylalcohol)、鲛肝醇和亚油醇等及它们的混合物。
本发明的其他实施方式包括如上所述制备的硫醇化活化脂肪酸,其配制成用于口服给药的固体剂型,包括胶囊、片剂、丸剂、粉剂和颗粒剂。在这种实施方式中,活性化合物可以与一种或多种惰性稀释剂诸如蔗糖、乳糖或淀粉混合。如在通常的实践中,这些剂型还可以包含除惰性稀释剂之外的其他物质,例如润滑剂,诸如硬脂酸镁。在胶囊、片剂和丸剂的情况下,剂型还可以包含缓冲剂,并且可以另外用肠溶包衣制备。
在本文所述的实施方式中,治疗有效量的硫醇化活化脂肪酸以药物组合物的形式。固体剂型的硫醇化活化脂肪酸的制备可以变化。例如,在一种实施方式中,硫醇化活化脂肪酸的液体或明胶制剂可以通过将硫醇化活化脂肪酸与一种或多种脂肪酸稀释剂(诸如上述那些)组合并向液体混合物中加入增稠剂以形成明胶来制备。然后可以将明胶以单位剂型封装以形成胶囊。在另一示例性实施方式中,可以将如上所述制备的硫醇化活化脂肪酸的油性制剂冻干以形成固体,该固体可以与一种或多种药学上可接受的赋形剂、载体或稀释剂混合以形成片剂,并且在另一种实施方式中,油性制剂的硫醇化活化脂肪酸可以结晶以形成固体,该固体可以与药学上可接受的赋形剂、载体或稀释剂混合以形成片剂。
可以用于口服给药硫醇化活化脂肪酸的其他实施方式包括液体剂型。在这种实施方式中,液体剂型可以包括药学上可接受的乳液、溶液、悬浮液、糖浆和酏剂,其含有本领域常用的惰性稀释剂,诸如水。这种组合物还可包含佐剂,诸如润湿剂、乳化剂和悬浮剂,以及甜味剂、调味剂和芳香剂。
在另外的实施方式中,本发明的硫醇化活化脂肪酸可以配制成积存制剂。这种长效制剂可以通过植入(例如,皮下或肌肉内)或通过肌内注射给药。积存注射可以以约1个月至约6个月或更长的间隔给药。因此,例如,化合物可以用合适的聚合材料或疏水材料(例如,作为可接受油中的乳液)或离子交换树脂配制,或配制成微溶衍生物,例如配制成微溶盐。
用于可注射制剂的其他合适的稀释剂包括但不限于下面描述的那些:
植物油:如本文所用,术语“植物油”是指由植物油的乙氧基化形成的化合物或化合物的混合物,其中至少一条聚乙二醇链与植物油共价结合。在一些实施方式中,乙氧基化的量可以为从约2个至约200个、约5个至100个、约10个至约80个、约20个至约60个或约12个至约18个乙二醇重复单元内变化。植物油可以是氢化的或未氢化的。合适的植物油包括但不限于,蓖麻油、氢化蓖麻油、芝麻油、玉米油、花生油、橄榄油、向日葵油、红花油、大豆油、苯甲酸苄酯、芝麻油、棉籽油和棕榈油。其他合适的植物油包括可商购的合成油,诸如但不限于,miglyoltm810和812(可购自瑞典的dynamitnobelchemicals)、neobeetmm5(可购自drewchemicalcorp.)、alofinetm(可购自jarchemindustries)、lubritabtm系列(可购自jrspharma)、sterotextm(可购自abiteccorp.)、softisantm154(可购自sasol)、crodurettm(可购自croda)、fancoltm(可购自fanningcorp.)、cutinatmhr(可购自cognis)、simulsoltm(可购自cjpetrow)、emcontmco(可购自amisolco.)、lipvoltmco、ses和hs-k(可购自lipo)以及sterotextmhm(可购自abiteccorp.)。包括芝麻油、蓖麻油、玉米油和棉籽油的其他合适的植物油,包括r.c.rowe和p.j.shesky,handbookofpharmaceuticalexcipients,(2006),5thed.中列出的那些,其通过引用整体并入本文。合适的聚乙氧基化植物油包括但不限于,cremaphortmel或rh系列(可购自basf)、emulphortmel-719(可购自stepan产品)以及emulphortmel-620p(可购自gaf)。
矿物油:如本文所用,术语“矿物油”是指未精制和精制(轻质)矿物油。合适的矿物油包括但不限于,avatechtm等级(可购自avatarcorp.)、drakeoltm等级(可购自penreco)、siriustm等级(可购自shell)以及citationtm等级(可购自avatercorp.)。
蓖麻油:如本文所用,术语“蓖麻油”是指由蓖麻油的乙氧基化形成的化合物,其中至少一条聚乙二醇链与蓖麻油共价结合。蓖麻油可以是氢化的或未氢化的。聚乙氧基化蓖麻油的同义词包括但不限于聚氧乙烯蓖麻油、氢化聚氧乙烯蓖麻油、聚乙二醇甘油蓖麻酸酯(mcrogolglyceroliricinoleas)、聚乙二醇甘油羟基硬脂酸酯(macrogolglycerolihydroxystearas)、聚氧乙烯35蓖麻油和聚氧乙烯40氢化蓖麻油。合适的聚乙氧基化蓖麻油包括但不限于,nikkoltmhco系列(可购自nikkochemicalsco.ltd.),诸如nikkolhco-30、hc-40、hc-50和hc-60(聚乙二醇-30氢化蓖麻油、聚乙二醇-40氢化蓖麻油、聚乙二醇-50氢化蓖麻油和聚乙二醇-60氢化蓖麻油),emulphortmel-719(蓖麻油40摩尔-乙氧基化物,可购自stepanproducts),cremophoretm系列(可购自basf),其包括cremophorerh40、rh60和el35(分别为聚乙二醇-40氢化蓖麻油、聚乙二醇-60氢化蓖麻油和聚乙二醇-35氢化蓖麻油)和
甾醇:如本文所用,术语“甾醇”是指衍生自甾醇分子的乙氧基化的化合物或化合物的混合物。合适的聚乙酰化甾醇包括但不限于,peg-24胆固醇醚、solulantmc-24(可购自amerchol);peg-30胆甾烷醇,nikkoltmdhc(可购自nikko);植物甾醇,generoltm系列(可购自henkel);peg-25植物甾醇,nikkoltmbpsh-25(可购自nikko);peg-5大豆甾醇,nikkoltmbps-5(可购自nikko);peg-10大豆甾醇,nikkoltmbps-10(可购自nikko);peg-20大豆甾醇,nikkoltmbps-20(可购自从nikko);以及peg-30大豆甾醇,nikkoltmbps-30(可购自nikko)。如本文所用,术语“peg”是指聚乙二醇。
聚乙二醇:如本文所用,术语“聚乙二醇”或“peg”是指含有式-o-ch2-ch2-的乙二醇单体单元的聚合物。合适的聚乙二醇可以在聚合物分子的每个末端具有游离羟基,或者可以具有与低烷基例如甲基醚化的一个或多个羟基。同样合适的是具有可酯化羧基的聚乙二醇的衍生物。可以用于本发明的聚乙二醇可以是任何链长或分子量的聚合物,并且可以包括支化。在一些实施方式中,聚乙二醇的平均分子量为约200至约9000。在一些实施方式中,聚乙二醇的平均分子量为约200至约5000。在一些实施方式中,聚乙二醇的平均分子量为约200至约900。在一些实施方式中,聚乙二醇的平均分子量为约400。合适的聚乙二醇包括但不限于聚乙二醇-200、聚乙二醇-300、聚乙二醇-400、聚乙二醇-600和聚乙二醇-900。名称中的破折号后面的数字是指聚合物的平均分子量。在一些实施方式中,聚乙二醇是聚乙二醇-400。合适的聚乙二醇包括但不限于carbowaxtm和carbowaxtmsentry系列(可购自dow)、lipoxoltm系列(可购自brenntag)、lutroltm系列(可购自basf)和plurioltm系列(可购自basf)。
丙二醇脂肪酸酯:如本文所用,术语“丙二醇脂肪酸酯”是指在丙二醇或聚丙二醇与脂肪酸之间形成的单醚或二酯,或它们的混合物。用于衍生丙二醇脂肪醇醚的脂肪酸包括但不限于本文限定的那些。在一些实施方式中,单酯或二酯衍生自丙二醇。在一些实施方式中,单酯或二酯具有约1个至约200个氧丙烯单元。在一些实施方式中,分子的聚丙二醇部分具有约2个至约100个氧丙烯单元。在一些实施方式中,单酯或二酯具有约4个至约50个氧丙烯单元。在一些实施方式中,单酯或二酯具有约4个至约30个氧丙烯单元。合适的丙二醇脂肪酸酯包括但不限于,丙二醇月桂酸酯:lauroglycoltmfcc和90(可购自gattefosse);丙二醇辛酸酯:capryoltmpgmc和90(可购自gatefosse);以及丙二醇二辛酸酯/二癸酸酯(propyleneglycoldicaprylocaprate):labrafactmpg(可购自gatefosse)。
硬脂酰聚乙二醇甘油酯:硬脂酰聚乙二醇甘油酯是指主要由硬脂酸合成或主要由硬脂酸衍生的化合物合成的聚乙二醇化甘油酯,尽管其他脂肪酸或衍生自其他脂肪酸的化合物也可用于合成。合适的硬脂酰聚乙二醇甘油酯包括但不限于,
在一些实施方式中,稀释剂组分包括甘露醇、乳糖、蔗糖、麦芽糖糊精、山梨糖醇、木糖醇、粉末化纤维素、微晶纤维素、羧甲基纤维素、羧乙基纤维素、甲基纤维素、乙基纤维素、羟乙基纤维素、甲基羟乙基纤维素、淀粉、羧甲基淀粉钠(sodiumstarchglycolate)、预胶化淀粉、磷酸钙、金属碳酸盐、金属氧化物或金属铝硅酸盐中的一种或多种。
用于固体和/或液体剂型的示例性赋形剂或载体包括但不限于:
山梨糖醇:合适的山梨糖醇包括但不限于,pharmsorbidexe420(可购自cargill)、liponic70-nc和76-nc(可购自从lipochemical)、neosorb(可购自roquette)、partechsi(可购自merck)和sorbogem(可购自spipolyols)。
淀粉、羧甲基淀粉钠和预胶化淀粉包括但不限于,r.c.rowe和p.j.shesky,handbookofpharmaceuticalexcipients,(2006),5thed.中描述的那些,其通过引用整体并入本文。
崩解剂:崩解剂可包括交联羧甲基纤维素钠、羧甲基纤维素钙、交聚维酮、海藻酸、海藻酸钠、海藻酸钾、海藻酸钙、离子交换树脂、基于食用酸和碱性碳酸盐组分的泡腾体系、粘土、滑石、淀粉、预胶化淀粉、羧甲基淀粉钠、纤维素絮状物、羧甲基纤维素、羟丙基纤维素、硅酸钙、金属碳酸盐、碳酸氢钠、柠檬酸钙或磷酸钙中的一种或多种。
在某些实施方式中,待治疗的病症可以是但不限于,炎性病症、肥胖症、代谢综合征、急性肾病、慢性肾病、动脉粥样硬化形成、脂肪生成、内膜增生、肾脏i/r和异型生物质损伤、局灶性心肌i/r损伤、angii诱导的系统性高血压、肺动脉高压、心脏和肺纤维化、炎性肠病、伤害感受、中风、运动神经元变性、糖尿病、哮喘和copd。
在某些实施方式中,炎性病症可以是器官维护用于移植、骨关节炎、慢性阻塞性肺病(copd)、动脉粥样硬化、高血压、同种异体移植物排斥、盆腔炎性疾病、溃疡性结肠炎、克罗恩病、肺部过敏性炎症、恶病质、中风、充血性心力衰竭、肺纤维化、肝炎、胶质母细胞瘤、格林-巴利综合征、系统性红斑狼疮病毒性心肌炎、移植后器官保护、急性胰腺炎、肠易激综合征、自身免疫性疾病、自身炎症性疾病、动脉狭窄、器官移植排斥和烧伤、慢性肺损伤和呼吸窘迫、胰岛素依赖型糖尿病、非胰岛素依赖型糖尿病、高血压、肥胖症、关节炎、神经退行性疾病、狼疮、莱姆病、痛风、败血症、体温过高、溃疡、小肠结肠炎、骨质疏松症、病毒或细菌感染、巨细胞病毒、牙周病、肾小球肾炎、结节病、肺部疾病、肺部炎症、肺纤维化、哮喘、后天性呼吸窘迫综合征、烟草致肺病、肉芽肿形成、肝纤维化、移植物抗宿主病、术后炎症、血管成形术、支架置入或旁路移植、冠状动脉旁路移植术(cabg)后冠状动脉和外周血管再狭窄、急性和慢性白血病、b淋巴细胞白血病、肿瘤性疾病、动脉硬化、动脉粥样硬化、心肌炎症、牛皮癣、免疫缺陷、弥散性血管内凝血、系统性硬化症、肌萎缩侧索硬化症、多发性硬化症、帕金森病、阿尔茨海默病、脑脊髓炎、水肿、炎症性肠病、高ige综合征、癌症转移或生长、过继性免疫治疗、再灌注综合征、放射性烧伤、秃头症、缺血、心肌梗塞、动脉狭窄、类风湿性关节炎、冠状动脉再狭窄、神经认知下降和胰岛素抵抗。
在本文所述的实施方式中,治疗炎症、肥胖症、代谢综合征、急性肾病和慢性肾病的方法包括向有此需要的受试者给药有效量的硫醇化活化脂肪酸和药学上可接受的赋形剂。
在本文所述的实施方式中,治疗炎症、肥胖症、代谢综合征、急性肾病和慢性肾病的方法包括向有此需要的受试者给药有效量的硫醇化活化脂肪酸和药学上可接受的赋形剂,其中硫醇化活化脂肪酸提供了活化脂肪酸的延长释放。
在本文所述的实施方式中,治疗炎症、肥胖症、代谢综合征、急性肾病和慢性肾病的方法包括向有此需要的受试者给药有效量的硫醇化活化脂肪酸和药学上可接受的赋形剂,其中防止了活化脂肪酸烯烃被前列腺素还原酶1还原。
在本文所述的实施方式中,治疗炎症、肥胖症、代谢综合征、急性肾病和慢性肾病的方法包括向有此需要的受试者给药有效量的硫醇化活化脂肪酸和药学上可接受的赋形剂,其中活化脂肪酸与谷胱甘肽的加合被延迟。
在本文所述的实施方式中,治疗炎症的方法包括向有此需要的受试者给药有效量的硫醇化活化脂肪酸和药学上可接受的赋形剂,其中减少了受试者胃肠道的负面副作用。胃肠道的副作用可包括腹泻、痉挛性刺激、炎症性肠病、结肠炎和溃疡。
通过参考以下实施例将更容易理解如此概括描述的本发明,这些实施例是以举例说明的方式提供的,并不旨在限制本发明。
实施例
实施例1:
通过硝基-油酸与3-5倍过量的硫化钠或硫氢化钠在甲醇和ph9磷酸盐缓冲液的溶液中直接反应合成了示例性的硫醇化亲电子脂肪酸。出于溶解性将硝基-油酸(no2-oa)酸溶解在甲醇中并缓慢加入到硫化物在缓冲液中的溶液中,然后在室温下在氮气氛下搅拌两个小时。淬灭反应并用稀酸和饱和氯化铵水溶液短暂搅拌,然后分配并用乙醚萃取。通过标准方法处理该溶液并通过快速色谱法纯化。通过nmr和lcms分析将产物鉴定为二聚体,具有可变数量的桥联硫原子的非对映异构体的组合。
然后测试了纯化的硫醇化no2-oa是否在小鼠巨噬细胞(raw264.7)中表达所需的基因表达调控和抗氧化表型。这通过与对照相比血红素加氧酶1、nad(p)h脱氢酶醌1和谷氨酸-半胱氨酸连接酶修饰物亚基的nrf2依赖性转录的激活增加来反映。硫醇化no2-oa在raw264.7细胞中诱导了剂量依赖性抗氧化响应,类似于no2-oa在4和8小时。然而,在稍后的时间点,被硫醇化no2-oa活化的基因的诱导远大于no2-oa处理(16小时和24小时)。此外,高效液相色谱串联质谱分析表明,硫醇化no2-oa释放出游离的no2-oa,然后显示出类似的贝塔-氧化和脂肪酸饱和度曲线。这些结果支持了硫醇化no2-oa可成为可行的前药候选物,其避免了首过胃肠道和肝脏的药物失活,并且在硫醇化产物的逆转时显示出与游离no2-oa类似的代谢和生物学特征。
总结:成功合成并纯化了oa-no2-sx前药,在图1中示出了nmr谱图,nrf2依赖性基因(ho-1、nqo-1、gclm)由oa-no2-sx诱导并且oa-no2-sx的代谢曲线表明来自前药的oa-no2的释放和代谢。
用纯化的硫醇化no2-oa处理小鼠巨噬细胞(raw264.7)4小时。rna使用trizol方法提取,使用nanodrop技术定量,逆转录成cdna,并且然后使用taqman测定进行了定量pcr。与对照(介质改变或低或高浓度甲醇,其用作溶剂化oa-no2或oa-no2-sx的载体)相比,硫醇化no2-oa处理4小时后血红素加氧酶1(ho-1,图2)、nad(p)h脱氢酶醌1(nqo-1,图3)和谷氨酸-半胱氨酸连接酶修饰亚基(gclm,图4)的nrf2依赖性转录呈剂量依赖性增加。在4小时时间点50μmoa-no2-sx的浓度诱导的ho-1、nqo-1和gclm(分别为18.0倍、6.8倍和6.3倍)的nrf2活化曲线与5μmoa-no2(对于ho-1、nqo1和gclm分别为23.5倍、7.7倍、6.8倍)相似。
实验细节:在每个实验中,raw264.7细胞用7.5、15、50和100μmoa-no2-sx,5μmoa-no2两种浓度的甲醇(meoh)处理,以匹配最低和最高量的载体(5和100μm)和单独介质对照。在每个实验中,每个处理组有两个或三个生物学重复。处理后,rna使用trizol方法提取,使用nanodrop技术定量,逆转录成cdna,并且然后使用taqman测定进行了定量pcr(qpcr)。在每个qpcr实验中,每个rna样品有两个技术重复。然后对每个生物重复平均两个技术重复。图中的条表示生物学重复的平均值±平均值的标准误差(sem)。
结果:在raw264.7细胞中的oa-no2-sx和oa-no2处理4小时后nrf2依赖性转录血红素加氧酶1(ho-1)、nad(p)h醌脱氢酶1(nqo-1)和伽马-谷氨酸半胱氨酸连接酶(gclm)增加。
小鼠巨噬细胞(raw264.7)使用50μmoa-no2-sx、5μmoa-no2、meoh(向raw细胞中添加最高量的载体以匹配最高浓度,对于oa-no2-sx其为50μm)和单独介质处理4、8、16和24小时。rna使用trizol方法在每个时间点提取,使用nanodrop技术定量,逆转录成cdna,并且然后使用taqman测定进行了定量pcr。在图5中,与介质和载体对照相比,ho-1稳态mrna水平对于oa-no2-sx(116.5倍)和oa-no2(30.7倍)两者约8小时均达到最大值,并且通过24小时后恢复至基础水平。在16小时,用oa-no2-sx处理(7.5倍)的ho-1mrna水平仍然显著升高,而oa-no2处理恢复到基线(类似于介质和载体对照)。在图6中,对于oa-no2(分别为115.0倍和98.9倍)的nqo-1mrna水平在8至16小时之间达到峰值。然而,在16小时与oa-no2相比,使用oa-no2-sx的nqo-1mrna水平显著更高(oa-no2-sx为701.1倍相对于oa-no2为98.9倍)。在16小时,相比于1.7倍5μmoa-no2处理,oa-no2-sx(30.0倍)的升高仍然存在gclmmrna水平(图7)的类似趋势。图5-7中的数据表明,在后来的时间点,硫醇化no2-oa活化的基因的诱导远大于no2-oa处理(主要在8和16小时,并在24小时达到较小程度),这表明硫醇化no2-oa是可行的前药。
实验细节:小鼠巨噬细胞(raw264.7)用50μmoa-no2-sx、5μmoa-no2、meoh(向raw细胞中加入最高量的载体以匹配最高浓度,其对于oa-no2-sx为50μm)和单独介质处理4、8、16和24小时。rna使用trizol方法在每个时间点提取,使用nanodrop技术定量,逆转录成cdna,并且然后使用taqman测定法对ho-1、nqo-1和gclm(与肌动蛋白复合)进行定量pcr。在每个独立实验中,每个处理在每个时间点具有至少两个生物学重复。数据代表两个独立的实验,即平均值±sem。
结果:50μmoa-no2-sx或5μmoa-no2处理4、8、16和24小时后,血红素加氧酶1(ho-1)、nad(p)h醌脱氢酶1(nqo-1)和伽马-谷氨酸-半胱氨酸连接酶(gclm)的时间过程。
- 还没有人留言评论。精彩留言会获得点赞!