用于选择放射疗法治疗方案的系统和方法与流程
本发明总体上涉及一种用于治疗癌症等的调制的放射疗法,并且具体地涉及一种用于为患者选择放射疗法治疗方案的方法。
技术实现要素:
用于放射疗法的医疗设备利用高能辐射治疗肿瘤组织。为患者生成治疗方案以准确地控制辐射的量以及其位置,以确保肿瘤组织接收足够的辐射以被破坏,并且确保对周围和邻近的非肿瘤组织的损伤最小化。此外,辐射传递的方式(例如,角度、强度、持续时间)可能会影响治疗方案的质量和效率。
放射疗法过程通常涉及治疗规划和治疗输送。放射疗法过程通常从获取三维患者图像开始,所述图像诸如计算机断层扫描(ct)图像或磁共振图像(mri)。接着,绘出或成型相关的解剖结构。这些结构能够被分类为要被辐射的目标区域,或者分类为对其辐射应当被最小化的敏感结构。然后准备治疗方案,其被优化以在最小化对敏感结构的辐射的同时最大化对靶区的治疗。
治疗规划试图在向肿瘤输送辐射的同时避免对健康器官(例如,脊髓、心脏、直肠等)的辐射。更具体地,治疗规划目标在于使辐射的目标区域与风险器官(其是位于肿瘤附近的健康器官)之间的剂量梯度最大化。通常而言,将从若干个不同的角度治疗大体积的肿瘤,并适当调整辐射束的强度和形状。使用会聚在肿瘤的部位的多个射束的目的在于减少对周围非肿瘤组织区域的剂量。选择辐射肿瘤的角度以避免会导致辐射到肿瘤部位附近特别敏感的结构的角度。用于特定肿瘤的射束的角度和强度形成用于该肿瘤的治疗方案。
在放射疗法应用中,治疗规划还试图在肿瘤内提供均匀的剂量分布。放射疗法治疗以小增量(称为小部分)输送辐射以破坏癌细胞,同时使健康细胞有机会恢复。肿瘤中的均匀剂量分布将对肿瘤中健康细胞的损害限制在可恢复的水平,同时仍然输送足够的辐射来破坏癌细胞并防止它们生长。
一旦治疗方案准备就绪,就由治疗输送系统来执行治疗方案,并且通过治疗输送系统来输送规定的辐射。治疗输送系统通常包括对患者进行支撑的治疗床和具有辐射源的台架,所述辐射源围绕治疗床旋转以从不同角度向肿瘤输送辐射。当台架旋转时,治疗床相对于台架在线性方向上平移。因此,从台架上的辐射源输送的辐射是沿着螺旋路径输送的。螺旋输送路径部分特征在于其节距,所述节距是对治疗床在一次台架旋转期间移动的距离的测量。研究已经显示由旋转的台架创建的螺旋路径节距和平移治疗床大大影响目标剂量分布的均匀性,并且因此影响治疗方案的质量和效率。然而,选择适合于治疗的节距存在一些困难。因此,在治疗规划阶段期间优选节距能够改善整体治疗输送。
如本文所使用,积分通量是穿过垂直于辐射射束的区域单位的光子或x射线的数量。积分通量率是每单位时间的积分通量。强度是每单位时间穿过单位区域的能量。积分通量和强度与患者身体中发生了什么无关,且更具体地不是剂量。剂量是由于辐射影响组织而被组织吸收的能量的量。辐射剂量用戈瑞(gy)为单位进行测量,其中每个gy与在单位质量的组织中吸收的固定量的能量(例如,1焦耳/kg)相对应。剂量与积分通量不同,而是随着积分通量增加而增加/随着积分通量减小而减小。
本发明涉及一种为患者选择放射疗法治疗方案的方法。所述治疗方案通过辐射输送系统来实现,所述辐射输送系统包括能够围绕治疗床旋转的台架,其中治疗床可相对于台架在线性方向上移动。治疗床和台架的移动创建具有节距的螺旋输送路径。辐射输送系统还包括辐射模块,所述辐射模块联接到所述台架并且能够分布辐射射束,其中所述射束具有与辐射积分通量相对应的射束权重。所述方法包括:由控制器接收包括来自包括期望的剂量、期望的剂量分布和剂量约束条件的列表中的至少一个的目标,优化节距以获得优化的节距,优化射束权重以获得优化的射束权重,基于所优化的节距和所优化的射束权重来确定来自包括治疗方案和剂量的以下列表中的至少一个,以及输出治疗方案和剂量中的至少一个。
在另一实施例中,本发明涉及一种放射疗法治疗系统,所述放射疗法治疗系统包括具有孔的台架和被配置为支撑患者的治疗床,其中所述治疗床可在所述孔内在线性方向上移动。辐射模块联接到所述台架,并且可围绕所述治疗床旋转,所述辐射模块被配置成将辐射射束朝向患者输送。所述辐射射束具有与辐射积分通量相对应的射束权重。治疗床的线性移动和辐射模块的旋转创建辐射输送的螺旋路径,并且所述螺旋路径具有节距。计算机与台架、辐射模块和治疗床通信。计算机包括控制器,所述控制器被配置成:优化辐射输送模块的节距,优化辐射射束的射束权重,基于优化的节距和优化的射束权重来确定治疗计划和剂量中的至少一个,以及输出治疗方案和剂量中的至少一个。
在另一实施例中,本发明涉及为患者选择放射疗法治疗方案的方法。治疗方案通过辐射输送系统来实现,所述辐射输送系统包括能够围绕治疗床旋转的台架和辐射模块,其中治疗床可相对于台架在线性方向上移动,辐射模块联接到所述台架并且能够分布辐射射束,其中所述射束具有与辐射积分通量相对应的射束权重。所述方法包括:由控制器接收包括来自包括期望的剂量、期望的剂量分布和剂量约束条件的列表中的至少一个的目标,以及接收第一节距和第一射束权重。所述方法进一步包括:由控制器使用第一几何结构来调整第一节距,以确定调整的节距;由控制器使用第二几何结构来调整第一射束权重,以确定调整的射束权重;由控制器将调整的射束权重从第二几何结构转换为第一几何结构;以及由控制器基于调整的节距和调整的射束权重来计算调整的剂量,其中所述调整的剂量用第一几何结构表示。
通过考虑详细描述和附图,本发明的其它方面将变得显而易见。
附图说明
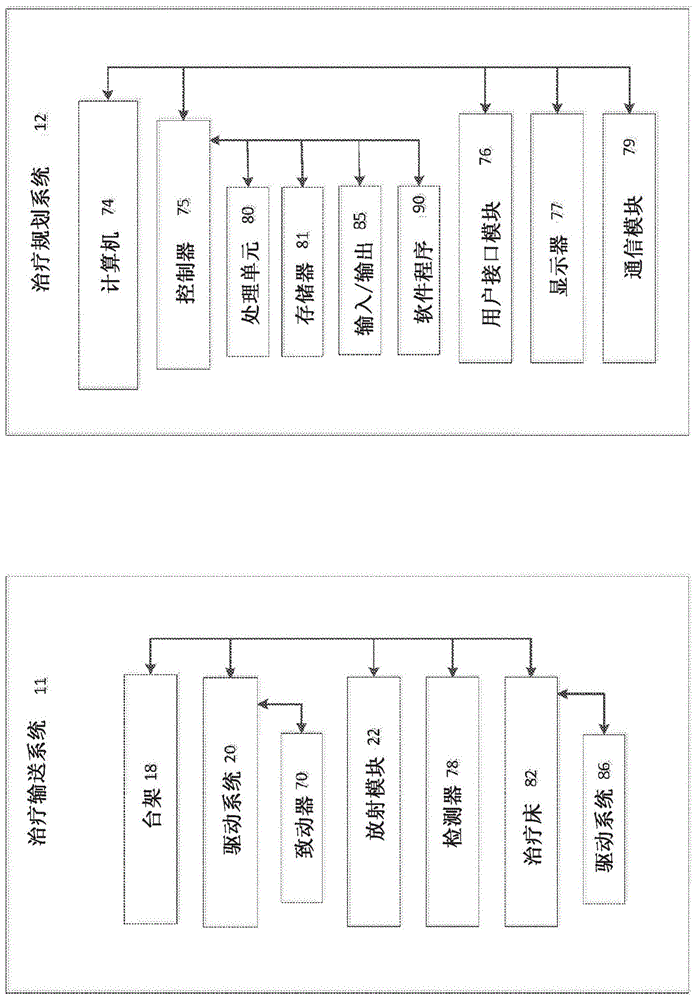
图1是放射疗法治疗系统的示意图。
图2是放射疗法治疗系统的透视图。
图3是能够在图2中图示的放射疗法治疗系统中使用的多叶准直器的透视图。
图4是放射疗法治疗系统中使用的软件程序的示意图。
图5是根据本发明的实施例的用于为患者选择放射疗法治疗方案的方法的流程图。
图6是根据本发明的实施例的优化治疗疗法系统的方法的流程图。
图7是根据本发明的实施例的优化治疗疗法系统的方法的流程图。
图8是图示根据本发明的实施例的优化治疗疗法系统的各种循环的流程图。
具体实施方式
在详细地解释本发明的任何实施例之前,将要理解的是,本发明的应用不限于以下描述中阐述的或以下附图中示出的部件的构造和布置的细节。本发明还具有其它实施例,并且能够以各种方式来实践或实施本发明。而且,将要理解的是,本文所使用的措辞和术语用于描述的目的,且不应当被视为是限制性的。本文中使用的“包括”、“包含”或“具有”以及其变化形式意指涵盖其后面列出的项目和其等效形式以及附加的项目。除非另有说明或限制,否则术语“安装”、“连接”、“支撑”和“联接”以及其变化形式被广泛地使用,并且涵盖直接和间接安装件、连接件、支撑件和联接件。本文使用术语“使优化”、“优化”和“最佳”意指指代改进或增强,且不限于理想或最佳结果。
虽然诸如上部、下部、向下、向上、向后、底部、前方、后部等方向引用可以在本文中用来描述附图,但是为了方便起见,这些引用是相对于附图(如正常观察的)做出的。这些方向不意图是字面意思或以任何形式限制本发明。另外,诸如“第一”、“第二”和“第三”等术语在本文中用于描述的目的,而不是意图指示或暗示相对重要性或意义。
另外,应当理解,本发明的实施例可以包括硬件、软件和电子部件或模块,出于讨论的目的,可以就如大多数部件是仅在硬件中实现的那样来说明和描述所述硬件、软件和电子部件或模块。然而,本领域普通技术人员基于阅读该详细描述将会认识到,在至少一个实施例中,本发明的基于电子的方面可以以(例如,在非暂时性计算机可读介质上存储的)软件实现。为此,应当注意的是,多个基于硬件和基于软件的装置以及多个不同的结构部件可以被利用来实现本发明。另外,并且如后续段落中所描述,附图中示出的特定机械配置意图例示本发明的实施例,并且其它替代机械配置是可能的。
图1和图2图示根据本发明的一个实施例的为患者14提供放射疗法的放射疗法治疗系统10。放射疗法治疗系统10包括治疗输送系统11和治疗规划系统12。放射疗法治疗能够包括基于光子的放射疗法、近距离放射疗法(brachytherapy)、电子束疗法、质子、中子、粒子疗法或其它类型的治疗疗法。
治疗输送系统
治疗输送系统11包括台架18。台架18支撑辐射模块22,所述辐射模块22包括辐射源24和生成辐射的射束30的线性加速器(或linac)26。虽然图2中示出的台架18是环形台架(即,其通过完整的360°圆弧延伸以创建完整的环或圆圈),但是也可以采用其它类型的安装布置。例如,可以使用c型部分环形台架或机器人臂台架布置。也可以采用能够将辐射模块22定位在相对于患者14的各种旋转和/或轴向位置处的任何其它架构。另外,辐射源24可以在不遵循台架18的形状的路径中行进。例如,虽然所图示的台架18总体上是圆形的,但是辐射源24也可以在非圆形路径中行进。台架18包括驱动系统20,所述驱动系统20可操作以操纵台架18的位置和/或台架18内辐射模块22的位置。如本文所使用,短语“台架旋转”、“台架的旋转”和“台架的移动”意图指代台架18的移动或台架18内辐射模块22的移动。驱动系统20能够由计算机74和/或控制器75(下文中为控制器)来控制。所图示的实施例的台架18限定了在治疗期间患者14移动到其中的台架孔32。
辐射模块22还包括调制装置34,所述调制装置34可操作以修改或调制辐射射束30。由辐射源24生成的射束30被调制装置34成型为扇形射束30。扇形射束30能够被概念化为许多不同的小射束30a,所述许多不同的小射束30a一起形成射束30。在其它实施例中,射束30具有不同的形状。调制装置34对辐射射束30进行调制,并且将该辐射射束30引向患者14。具体地,辐射射束30被引导朝向患者14的含有靶位38的部分。患者14还可能具有一个以上的需要接收放射疗法的部分。所述部分可以包括患者的整个身体,但是总体上小于患者的整个身体,并且能够由二维区域和/或三维体积进行限定。一个部分可以包括一个或多个感兴趣区域。例如,期望接收辐射的部分(可以被称为靶位38或靶区域)是感兴趣区域的示例。另一类型的感兴趣区域是风险区域。如果一个部分包括风险区域,则辐射射束30被优选地从风险区域转移。例如,被引导朝向风险区域的概念化的小射束30a能够被调制装置34阻挡或限制,而被引导朝向靶位38的概念化的小射束30a能够穿过调制装置34。
这种调制有时被称作强度调制放射疗法(“imrt”)。imrt是用于本质上改变被引导到患者的射束强度的若干放射疗法技术的通用术语。调制装置34能够在空间上、时间上或以两种方式改变射束30。调制装置34能够包括如图2中图示的准直装置42。准直装置42包括限定和调整辐射射束30可以穿过其的孔50的大小的一组狭口(jaw)46。狭口46包括上部狭口54和下部狭口58。上部狭口54和下部狭口58是可移动的,以调整孔50的大小。
在一个实施例中,并且如图3中图示的,调制装置34能够包括多叶准直器62(或mlc),以提供辐射射束30的强度调制,所述多叶准直器62包括可操作以从第一位置移动到第二位置的多个交错的叶片66。还应当注意的是,叶片66能够移动到最小打开位置与最大打开位置之间的任何位置。在辐射射束30到达患者14上的靶位38之前,所述多个交错的叶片66对辐射射束30的强度、大小和形状进行调制。通过按顺序地和单调地将叶片66移动到期望的位置以阻挡或暴露特定的小射束30a来发生射束30的调制,从而总体上实现射束30的期望形状。概念化的小射束30a被暴露的时间的量是控制小射束30a输送的辐射量的一种方法。由诸如马达或气阀等致动器70独立地控制叶片66中的每一个,使得叶片66能够快速地打开和关闭以容许或阻挡辐射的通道。致动器70能够由计算机74和/或控制器75进行控制。在所图示的实施例中,致动器70是控制台架18的驱动系统20的部件。
从概念上讲,叶片66能够被控制以各自选择性地允许或阻挡小射束30a穿过调制装置34并且到达靶位38上。通过独立地控制叶片66,调制装置34能够阻挡某些小射束30a并且允许其它小射束30a。在一些实施例中,叶片66以二态方式操作,借此叶片66从完全打开位置直接移动到完全关闭位置。当叶片66以二态方式操作时,调制装置34通常被配置成在时间上调制射束30的强度。在时间上调制射束30涉及控制每个叶片66维持打开或关闭的时间量,并且因此控制每个小射束30a暴露的大概时间。从小射束30a期望的辐射越多,叶片66保持打开的时间越长。叶片66保持打开的时间量被称为叶片打开时间。在其它实施例中,调制装置34能够在空间上调制射束30的强度。具体地,叶片66能够移动到完全打开位置与完全关闭位置之间的各种位置,以部分阻挡或减小小射束30a穿过的部分。在一些实施例中,调制装置34使用时间调制技术和空间调制技术的组合。
不论是否在时间上或空间上调制小射束30a,调制每个射束以具有小射束权重。小射束权重对应于辐射的积分通量和由靶位38接收的剂量。正弦图含有关于射束30的调制的信息。当在时间上调制小射束30a时,正弦图含有关于相对于总投射时间每个叶片66是打开的时间量的信息。然后,正弦图被用来引导辐射的输送。如下面将进一步详细地解释,通过治疗规划系统12来计算和优化小射束权重和相应的正弦图。
进一步参考图1,治疗输送系统11还能够包括检测器78,例如,接收辐射射束30的千伏电压检测器或兆伏电压检测器。线性加速器26和检测器78还能够作为计算机断层摄影(ct)系统进行操作,以生成患者14的ct图像。线性加速器26将辐射射束30朝向患者14中的靶位38发射。靶位38吸收一些辐射。检测器78检测或测量被靶位38吸收的辐射量。当线性加速器26围绕患者14旋转并朝向患者14发射辐射时,检测器78从不同角度收集吸收数据。所收集的吸收数据被传输给控制器75,用于处理吸收数据并且生成患者的身体组织和器官的图像。所述图像还能够示出骨骼、软组织和血管。
能够用具有扇形几何结构、多切面几何结构或锥形束几何结构的辐射射束30来获得ct图像。另外,能够用输送兆伏电压能量或千伏电压能量的线性加速器26来获得ct图像。还应当注意的是,所获得的ct图像能够与先前(从诸如其它ct扫描仪、mri系统和pet系统等的放射疗法治疗系统10或其它图像获取装置)获得的ct图像进行配准(registered)。例如,先前获得的患者14的ct图像能够包括通过轮廓成形(contouring)过程制成的识别靶位38。新获得的患者14的ct图像与先前获得的ct图像进行配准,以有助于在新ct图像中识别靶位38。配准过程能够使用刚性的配准工具或可变形的配准工具。图像数据能够作为三维图像或一系列二维图像被呈现在显示器上。另外,包括图像的图像数据能够是(用于三维图像的)体素或(用于二维图像的)像素。在本说明书中术语“图像元素”一般被用于指代二者。
治疗输送系统11还包括患者支撑装置,(图2中图示的)诸如支撑患者14的治疗床82。治疗床82或其至少部分沿着轴线84移进或移出辐射野。治疗床82还能够沿着如图2中图示的x轴和z轴移动。在本发明的其它实施例中,患者支撑装置能够是适于支撑患者的身体的任何部分的装置。患者支撑装置不限于必须支撑患者的整个身体。系统11还能够包括驱动系统86,所述驱动系统86可操作以操纵治疗床82的位置。驱动系统86能够由控制器75进行控制。治疗床82能够被控制为以恒定速度移动通过台架,或者能够被控制为以某个间隔开始和停止。治疗床82还能够被控制为以变化的速度移动通过台架。治疗方案能够包括被递送给控制器75从而以恒定速度或变化的速度将治疗床82移动通过台架或者以某个间隔开始和停止治疗床82的指令。还可以“在进行中(onthefly)”调整治疗方案,以在输送治疗时调整治疗床的规划的运动,从而适应治疗期间剖体或患者移动的意外变化。这些“在进行中的”变化可以被并入治疗方案中,或者治疗输送系统可以仅对特定治疗部分做出变化。
在治疗输送期间,控制器75控制驱动系统20和驱动系统86,以分别操纵台架18和治疗床82的位置,从而使辐射模块22能够从不同的角度和侧面朝向靶位38引导辐射。在图示的实施例中,控制器75控制驱动系统86,以沿着轴线84将治疗床82移进和移出台架18的孔32。因此,治疗床82相对于台架18平移。同时,控制器75控制驱动系统20,以围绕治疗床82旋转台架18和/或辐射模块22。台架18的旋转移动和治疗床82的线性平移一起创建了辐射输送的螺旋路径。
辐射的螺旋轨迹部分特征在于其节距。螺旋的节距被限定为平行于螺旋的轴线测量的、一个完整螺旋转角的高度。在图示的实施例中,通过台架和治疗床的组合移动来完成螺旋轨迹。因此,相对于本文所描述的治疗输送系统11,节距是治疗床82的直线移动相对于台架18的旋转移动的度量。换句话说,能够通过控制台架18和治疗床82相对于彼此的移动来实现螺旋的特定节距。
螺旋辐射输送的一个复杂性在于螺旋连接效应或者“螺纹效应”。当在螺旋路径中输送辐射时,辐射源24与38之间的距离(即,源到点的距离)随着台架18围绕轴线84旋转到不同角度而变化。对于不在轴线上的任何靶位38也是如此,从而意味着不沿着台架18的旋转的轴线84定位。在图示的实施例中,不沿y轴线84定位的任何靶位38将随着台架18围绕y轴线旋转而具有变化的源到点距离。因为源到点距离变化,所以辐射的积分通量也随着台架18的旋转而变化,从而导致在输送的剂量上的波动(即,不均匀性)。在剂量输送上的这个波动通常称为螺纹效应。已经确定的是,用于输送辐射的特定螺旋路径,特别是螺旋节距能够影响螺纹效应的程度。因此,治疗规划系统的一个方面目标在于优化用于输送放射疗法的螺旋路径的节距。
治疗规划系统
治疗规划系统12被用来使针对正在被治疗的个人14的放射疗法个性化。治疗规划系统12帮助识别靶位38的特征(例如,大小、位置等)和任何风险区域。治疗规划系统12然后帮助创建适合于这些特征的治疗方案。治疗方案可以包括规定的剂量和诸如剂量体积直方图(dvh)的剂量分布。治疗方案还可以识别用于管理所规定的剂量的参数。例如,在一些实施例中,治疗方案包括所需要的放射疗法疗程的数目(即,次数)的分解,以及用于每个疗程的特定治疗方案和剂量。另外,治疗方案可以指定治疗输送系统11的用于管理放射疗法的参数。例如,治疗方案可以包括用于机器的指令,所述指令指定治疗床82和台架18的速度、节距和叶片调制参数,诸如叶片打开时间和/或小射束权重。
节距是在治疗规划阶段期间能够选择以便减小螺纹效应并优化治疗方案的参数中的一个。如先前所提及的,用于输送辐射的特定螺旋路径,特别是节距可能会影响治疗方案的质量和效率。在图示的实施例中,节距是治疗床82的线性移动相对于台架18的旋转移动的度量。更具体地,节距能够被限定为治疗床82在台架18的一次旋转期间移动的射野宽度的一部分。在其它实施例中,节距的定义能够根据实现螺旋输送路径的方式而改变。例如,在其它实施例中,可以通过在将治疗床保持在固定位置处的同时旋转和平移台架来创建螺旋辐射输送。
选择最佳螺旋节距能够减小螺纹效应,从而得到更加均匀的辐射分布。研究已经确认影响螺纹效应的至少四个因素,包括射束发散、平方反比定律、衰减和圆锥效应。这些因素导致针对每个患者的不同的最佳节距值。在给定的治疗方案中,可能存在减小螺纹效应并且帮助产生更加均匀的辐射分布的一个以上最佳节距值。
由于当选择节距时考虑的因素的数量,选择最佳节距可能是困难的。此外,与最佳节距中的一个稍有不同的节距可能会导致剂量均匀性和/或输送效率的急剧恶化。当调制小射束30a和选择最佳小射束权重时,出现选择最佳节距时的另一困难。在许多当前系统中,节距和小射束权重无法被单方面优化。实际上,一旦选择了节距,就基于所选择的节距来调制小射束30a。如果在后面确定应当使用不同的节距,则通常从过程的开端重新开始射束30的调制。本文所描述的治疗规划系统12提供一种用于选择放射疗法治疗方案的系统和方法,所述系统和方法允许同时优化节距和射束30的调制。
治疗规划系统12包括计算机74,所述计算机74被实现为要由医疗人员访问的操作员站。计算机74包括控制器75、用户接口模块76、显示器77和通信模块79。控制器75和用户接口模块76包括软件和硬件的组合,所述软件和硬件的组合是可操作的尤其用于控制治疗输送系统11的操作和显示器77上呈现的信息。
控制器75包括例如处理单元80(例如,微处理器、微控制器、或其它合适的可编程装置)、存储器81和软件程序90。处理单元80可以表示一个或多个通用处理器、诸如数字信号处理器的专用处理器或诸如控制器或现场可编程门阵列的其它类型的装置。
应当理解,虽然控制器75、用户接口模块76、显示器77和通信模块79被图示为单个服务器或计算装置的一部分,但是治疗规划系统12的这些部件能够分布在多个服务器或计算装置上。类似地,治疗规划系统12能够包括多个控制器75、用户接口模块76、显示器77和通信模块79。
存储器81包括例如只读存储器(“rom”)、随机存取存储器(“ram”)、电可擦除可编程只读存储器(“eeprom”)、闪速存储器、硬盘、sd卡或另一合适的磁性、光学、物理或电子存储器装置。处理单元80连接到存储器81,并且执行软件程序90,所述软件程序90能够被存储在ram(例如,在执行期间)、rom(例如,通常是永久性的)或诸如另一存储器或光盘的另一非暂时性计算机可读介质中。附加地或可替选地,存储器81被包括在处理单元80中。控制器75还包括输入/输出(“i/o”)系统85,所述输入/输出(“i/o”)系统85包括用于在控制器75内的部件与治疗规划系统12的其它部件之间传递信息的例程。包括在治疗规划系统12的实施方式中的软件被存储在控制器75的存储器81中。软件包括例如固件、一个或多个应用、程序数据、一个或多个程序模块和其它可执行指令。控制器75被配置成从存储器进行检索,并且执行尤其是与下面描述的方法有关的指令。
用户接口模块76被配置用于治疗规划系统12的用户控制,并且被配置成将各种参数输入到治疗规划系统12中。例如,用户接口模块76可操作地耦合到控制器75,以控制显示器77上呈现的信息。在一个实施例中,用户使用接口模块76来录入用于优化和创建治疗方案的多个机器参数和临床数据。用户接口模块76能够将由用户输入的信息发送给控制器75和/或处理单元80。用户接口模块76能够包括实现对治疗规划系统12的期望水平的控制所需要的数字和模拟输入装置或数字和模拟输出装置的组合。例如,用户接口模块76能够包括输入装置,诸如触摸屏显示器、多个旋钮、多个刻度盘、多个开关、多个按钮等。
显示器77是例如液晶显示器(“lcd”)、发光二极管(“led”)显示器、有机led(“oled”)显示器、电致发光显示器(“eld”)、表面传导电子发射显示器(“sed”)、场发射显示器(“fed”)、薄膜晶体管(“tft”)lcd等。在其它构造中,显示器77是超有源矩阵oled(“amoled”)显示器。
在一些实施方式中,治疗规划系统12还被配置成经由通信模块79连接到网络94(例如,wan、lan等),以访问其它程序、软件、或治疗规划系统12、或治疗输送系统11。通信模块79能够包括网络接口,诸如以太网卡或无线网卡,所述网络接口允许治疗规划系统12通过诸如局域网或互联网的网络发送和接收信息。在一些实施例中,通信模块79包括驱动器,所述驱动器被配置成从诸如键盘、鼠标、打印机等各种输入和/输出装置接收数据以及向各种输入和/或输出装置发送数据。数据通信可以使用诸如wi-fi、蓝牙、zigbee等的各种各样的通信协议中的任何一个经由无线局域网(“lan”)发生。附加地或可替选地,数据通信可以通过广域网(“wan”)(例如,基于tcp/ip的网络等)发生。
通信模块79还与任何版本的医学数字成像和通信(dicom)协议或其它要求的协议相兼容。dicom是由nema开发的国际通信标准,其限定用于在不同医疗设备之间传递医学图像相关数据的格式。dicomrt指代特定于辐射疗法数据的标准。
图1和图3中的双向箭头一般表示双向通信和其指示的信息传递。然而,对于一些医疗和计算机设备,仅单向通信和信息传递可能是必要的。
处理单元80执行在计算机可读介质中存储的指令。所述指令可以包括各种部件或模块,所述部件或模块被配置成当由处理单元80执行时执行特定功能。例如,软件程序90包括多个模块或应用,所述多个模块或应用彼此交互或通信,以将指令提供给处理单元80,用于为患者生成治疗方案、修改或调整治疗方案、获取患者的图像、以及控制治疗输送系统11的部件。将要理解的是,除了下面详细描述的模块之外,软件程序90还能够包括多种模块。
软件程序90包括治疗规划模块89,所述治疗规划模块89与用户接口模块76和控制器75的其它部件交互,以创建患者的治疗方案并且在显示器77上显示与治疗方案相关的各种“屏幕”或“页面”。用户接口的屏幕可以包括但不限于图像、图表、图解、字段、列、行、对话框、制表符、按钮、单选按钮和下拉菜单。用户接口的屏幕并不限于任何特定布置。
在一个实施例中,治疗规划系统12能够表示将治疗规划模块89作为基于网络的工具或应用托管的服务器。因此,用户能够通过诸如互联网的网络来访问治疗规划模块89。因此,在一些实施例中,不要求用户将治疗规划模块89永久地安装在控制器75上。实际上,用户能够使用诸如internet
治疗计划模块89能够包括多个子模块。图4更加详细地图示软件程序90和治疗规划模块89。在一个实施例中,治疗规划模块89包括临床数据输入模块95、机器参数模块97、优先级排序模块99、优化模块100和治疗方案生成模块101。以下更加详细地说明这些子模块的功能。在其它实施例中,治疗规划模块89能够包括将不同的功能提供给治疗规划系统12的更多或更少的模块。
如图4中所示,软件程序90还包括图像模块102,所述图像模块102可操作以获取或接收患者14的至少一部分的图像。图像模块102能够为诸如ct成像装置的机载(on-board)或在线图像装置生成指令,以根据期望的协议获取患者14在治疗开始之前、在治疗期间以及在治疗之后的图像。例如,机载或在线图像装置能够包括辐射源和检测器,其中辐射源将kv或mv的辐射输送给患者,所述kv或mv的辐射由检测器收集并且被处理成三维(例如,ct)图像。对于ct图像,包括患者图像的数据由图像元素组成,所述图像元素表示在放射疗法治疗系统中存储为数据的图像元素。这些图像元素可以是用于表示图像数据的任何数据结构,包括二维像素或三维体素。图像能够被存储在存储器中或数据库中,并且由图像模块102检索以供后续使用。所述图像能够被治疗规划模块89使用以为患者14创建治疗方案。
在一个方面中,图像模块102在患者14基本上处于治疗位置的同时获取患者14的图像。其它离线成像装置或系统可以被用于获取患者14的预治疗图像(例如,三维),诸如非定量ct、mri、pet、spect、超声波、透射成像、透射检查(fluoroscopy)、基于rf的定位等。所获取的图像能够用于确定靶区域和敏感结构的相对位置。另外,所获取的图像能够用于患者14相对于台架或其它点的配准/对准,和/或用于确定或预测要被输送给患者14的辐射剂量。所获取的图像还能够用于确定患者14在先前治疗期间接收的辐射剂量。图像模块102还可操作以在患者正在接收治疗的同时获取患者14的至少一部分的图像,以确定患者14正在实时接收的辐射剂量。
临床数据输入模块95允许用户输入与患者14的治疗相关的不同临床目的和约束条件(一起称为“目标”)。所述目标能够包括固定的或期望的剂量。特定临床目标通常取决于要被治疗的患者的形态或病情。具体地,临床目标取决于患者14的将由系统10进行治疗的感兴趣区域(例如,肿瘤的类型和/或大小)。另外,临床目标取决于用于每个感兴趣区域的特定辐射剂量治疗值。在一个实施例中,临床目标能够包括:积极治疗(aggressivetreatment)、敏感结构保留(sensitivestructuresparing)等。如果治疗过程的焦点为肺肿瘤,则通过数据输入模块95输入的临床数据将取决于肿瘤位置和总体上与治疗肺肿瘤相关联的辐射剂量。在一个实施例中,临床数据(例如,经由用户接口模块76)被用户直接地输入到临床数据输入模块95。在其它实施例中,临床数据输入模块95自动地检索在存储器81中存储的临床数据。临床数据输入模块95允许用户同时输入或选择多个临床目标。
机器参数模块97允许用户输入或选择要在治疗规划模块89中使用的多个机器参数。这些机器参数是用户可见参数,所述参数被用于控制对患者的辐射输送的特定方面。例如,机器参数与台架、辐射输送装置和治疗床相关。在一个实施例中,机器参数能够包括:狭口宽度、节距、台架速度、治疗床速度、台架位置和治疗床位置。另外,机器参数能够包括辐射输送的类型:螺旋辐射治疗输送、静态辐射治疗输送、摇摆台架辐射治疗输送和运行开始/停止辐射治疗输送。在一个实施例中,机器参数被用户(例如,经由用户接口模块76)直接输入到机器参数模块97。在其它实施例中,机器参数模块97自动地检索在存储器81中存储的机器参数。在机器参数被输入到机器参数模块97中之后,用户能够选择要在创建治疗方案的过程中使用的一个或多个机器参数。
优先级排序模块99将由临床数据输入模块95选择的临床目标中的至少一个优先化。临床目标中的一些具有极限或固定值,并且其它临床目标是灵活的并且能够在优化和生成治疗方案的过程期间进行调整,这将在下面更加详细地解释。例如,因为非常高的辐射剂量将会损害脊髓,所以输送用于治疗脊髓的辐射剂量不能够超过特定值。在一些实施例中,优先级排序模块99与优化模块100同时地操作。例如,优化模块100在遵守由优先级排序模块设置的固定限制的同时优化灵活参数。
优化模块100用所选择的机器参数优化优先的临床目标。在一些实施例中,当用户选择多于一个机器参数时,优化模块100用所有的所选择的机器参数优化优先的临床目标。优化模块100将用户输入转换为详细的机器指令,所述详细的机器指令以治疗方案的形式被转发给放射治疗装置。该放射治疗装置接收这些机器指令,并且产生规划的放射治疗剂量。如上面所提及,优化模块100与优先级排序模块99同时地操作。优化过程是连续的过程。优化模块100用所选择的机器参数优化优先的临床目标,用户查看结果,并且然后用户能够用机器参数优化不同的临床目标。因此,优化模块100能够同时优化多组机器指令。另外,在一些实施例中,优化模块100能够在输送治疗期间执行优化过程。
治疗方案生成模块101包括用于基于从其它模块中的至少一个生成的数据而为患者14生成治疗方案的指令,所述其它模块包括数据输入模块95、机器参数模块97、优化模块100和优先级排序模块99。治疗方案生成模块101能够用从子模块95、97、99和100接收的数据生成若干治疗方案。另外,治疗方案生成模块101能够使用由医务人员输入到系统10的、从存储器或数据库检索的、从其它模块接收的、或由系统10以其它方式获取的数据。数据能够包括患者14的至少一部分的一个或多个图像(例如,规划图像和/或预治疗图像)。这些图像可以被图像模块102以先前段落中描述的方式进行获取和处理。生成的治疗方案提供用于将治疗辐射输送给患者14的指令。例如,治疗方案包括用于靶区域的辐射剂量分布。治疗方案生成模块101能够将治疗方案分解成多个治疗部分,并且能够基于由医务人员输入的辐射剂量处方而确定用于每个部分或每次治疗的辐射剂量。将治疗方案分解成各小部分的过程被称为分割(fractionation)。
在生成了治疗方案之后,用户能够选择所生成的方案中的一个用于患者14。治疗输送系统11根据所选择的治疗方案将辐射输送给患者14。例如,患者14接收针对治疗方案的每个部分规定的辐射剂量。在每个部分输送之前,使患者定位在治疗床82上,并且相对于治疗输送系统11配准和对准。将要理解的是,治疗方案不是静态的,并且在整个治疗过程中能够变化。例如,治疗方案能够适合于并入在输送这些部分中的一个时发现的变化(例如,解剖变化、机器参数变化等)。治疗方案然后在未来各部分中实现这些变化。
图5到图8图示用于选择放射疗法治疗方案的各种方法。本文所描述的各种方法能够在软件程序90以及治疗规划模块89和子模块95、97、99、100、101的帮助下由控制器75的处理单元80执行。本文中针对这些方法描述的各种步骤能够同时、并行、或以与图示的串行执行方式不同的顺序来执行。所述方法还能够使用比所图示的实施例中示出的更多或更少的步骤来执行。
图5是图示根据本发明的实施例的选择放射疗法治疗方案的方法150的流程图。所述方法150包括获取患者14的含有靶位38的部分的图像(步骤154)并且视需要对图像进行轮廓界定。如上所述,能够使用图像模块102结合治疗输送系统11来获取图像。图像被用于识别感兴趣的区域(roi)(步骤158)。例如,识别靶位38以及风险区域和敏感结构。
在步骤154和步骤158期间获得的信息能够被输入到临床数据输入模块95中。另外,能够将临床目标(即,目的和约束条件)添加到临床数据输入模块95和优先级排序模块99(步骤162)。用户还将一系列方案设置输入到机器参数模块97中(步骤162)。例如,所述设置能够尤其包括输送模式的类型、射野宽度、狭口模式和节距。在整个方法150中输入的数据能够通过用户接口模块76录入并且被存储在存储器81上。如果需要,用户能够利用优先级排序模块99来使目标优先化。
治疗规划系统12然后参与优化过程(步骤166),以计算针对临床目标协调机器参数的最佳治疗方案。具体地,控制器75与优化模块100通信并执行指令,以基于录入到临床数据模块95、机器参数模块97和优先级排序模块99中的数据来确定用于输送治疗的最佳机器参数。
一旦优化模块100完成优化过程并且计算治疗方案,控制器75就在治疗方案模块101的帮助下执行分割过程(步骤170)。在分割过程期间,治疗方案模块101使用在优化过程期间计算的治疗方案(步骤166)为治疗的每个部分确定辐射剂量。换句话说,总治疗方案被分成不同的剂量,这些剂量将在数个不同的治疗疗程期间施用,所述治疗疗程中的每一个输送总规定剂量的部分。
图6到图8图示根据一个实施例的执行方法150的优化过程(步骤166)的各种方法200和300。这些方法200和300寻求优化治疗输送系统11的参数,以实现所规定的剂量。不同方法200和300的许多方面是可互换的,并且能够被重新组合成其它方法。治疗输送系统11的节距和小射束权重是能够通过方法200和300优化的参数中的两个。更具体地,针对每个小射束30a确定了叶片打开时间和小射束权重的模式,以便实现目标或所规定的剂量。与小射束30a的调制相关的此信息能够由正弦图来表示,这能够被用于引导辐射的输送。
方法200和方法300能够优化节距,以减小螺纹效应并且提高治疗输送的质量和效率。在一些现有方法中,可以优化治疗输送系统的其它参数,然而,该过程期间不调整节距。实际上,为整个优化过程选择固定的节距。如果需要不同的节距,则将从开端重新开始优化过程。因此,现有方法中未优化节距。
本文示出的方法200和方法300能够优化节距以及优化小射束权重。换句话说,在整个优化过程中,能够在不必将这些值中的一个保持为固定值的情况下优化小射束权重和节距二者。实际上,能够在优化过程期间(步骤166)调整小射束权重正弦图和节距二者。针对优化过程(步骤166)的部分,通过保持其它参数恒定,能够独立地优化节距和小射束权重。然而,在完整优化过程(步骤166)期间没有必要将节距保持恒定。另外,在一些实施例中,优化节距和小射束权重二者,而在其它实施例中,仅优化了节距和小射束权重中的一个。
图6图示根据一个实施例的执行方法150的优化过程(步骤166)的方法200。根据方法200,优化治疗输送系统11的节距(步骤204)。在一些实施例中,在节距被优化时,通过保持小射束权重的值恒定来独立地优化节距。能够通过控制器72优化节距,所述控制器72能够执行指令以实施多种标准优化技术中的任何一种,所述多种标准优化技术包括线性模型、非线性模型、梯度优化方法和渐进优化方法。在一些实施例中,初始节距能够被用作起始点,并且控制器75能够执行用于优化模块100的指令,以确定最接近初始节距的最佳节距。优化迭代的数目可以改变。在一些实施例中,控制器75在确定最佳节距之前能够执行多个优化迭代。在其它实施例中,在移动到下一步骤之前使用单个优化迭代。另外,在一些实施例中,用户能够指示控制器75执行预确定数目的优化迭代。可替选地,用户可以查看在每个迭代之后计算的节距,并且能够手动地使控制器75停止执行另一个优化迭代。
方法200还包括优化小射束权重的调制(步骤208)。更具体地,控制器75执行用于优化模块100的指令,以执行调制小射束30a的过程,从而实现期望的剂量(或规定剂量)。如上所述,关于小射束权重的调制的信息能够由小射束权重正弦图表示。与节距的优化(步骤204)类似,控制器75能够执行小射束权重优化的多个迭代(步骤208)。如上所述,能够改变迭代的数目,并且能够以多种方式终止小射束权重的优化。在一些实施例中,在优化小射束权重时,通过将节距保持恒定来独立地优化小射束权重。
在一些实施例中,节距的优化(步骤204)和小射束权重的优化(步骤208)可以作为不同的和单独的循环顺序地发生。例如,可以在控制器75优化小射束权重正弦图(步骤208)之前优化节距(步骤204)。在这种情况下,在开始小射束权重的优化之前可以完全地优化节距,使得能够用最佳节距来开始小射束权重的优化。
在其它实施例中,作为组合的交替循环,同时执行节距的优化(步骤204)和小射束权重的优化(步骤208)。例如,在交替循环中,控制器75能够在执行用于优化节距(步骤204)的指令与执行用于优化小射束权重(步骤208)的指令之间交替,直到充分地优化了节距和小射束权重二者为止。换句话说,优化小射束权重(步骤208)的一个或多个迭代被优化节距(步骤204)的一个或多个迭代中断。在这种情况下,能够基于对小射束权重调制的调整而在小射束权重优化的每个迭代或每几个迭代之间更新节距。
例如,优化循环可以包括优化小射束权重(步骤208)的单个迭代,随后是优化节距(步骤204)的单个迭代。通过返回优化小射束权重(步骤208)的另一单个迭代来重复该循环,并且反复地执行所述循环。优化循环能够包括任何数目的优化迭代,并且所述迭代能够以任何顺序发生。例如,所述循环可以包括优化节距的一系列两个迭代,随后是优化小射束权重的一系列三个迭代。在一些实施例中,在一个系列的迭代之后完成优化过程(步骤166),而在其它实施例中,能够重复所述系列。在每个优化迭代之间,可以调整节距和小射束权重中的一个或二者。
在一些实施例中,当确定所期望的小射束权重时,能够通过忽略治疗输送系统11的螺旋路径来实现小射束权重的优化。实际上,通过将台架18的移动建模为圆形轨迹的序列来确定小射束权重,所述圆形轨迹被治疗床82位置的线性移动的小增量分离开。该几何结构被称为“轴向几何结构”。换句话说,使用轴向几何结构而不是使用螺旋几何结构来优化和调制小射束权重。这将小射束权重与使用螺旋几何结构的节距的优化有效地分离。图7和图8图示通过利用不同几何结构的组合来优化节距和小射束权重从而执行方法150的优化过程(步骤166)的方法300。
一旦优化了节距和小射束权重二者,控制器就执行指令74以计算剂量并确定治疗方案(步骤212)。在一些实施例中,控制器75执行指令以在优化节距(步骤204)的每个迭代之后或在优化小射束权重(步骤208)的每个迭代之后或二者之后计算剂量。控制器75能够将所计算的剂量与所期望的剂量或剂量体积直方图进行比较,以识别节距和/或小射束权重是否足以实现期望的剂量。另外,控制器75能够确定所计算的剂量是否满足优先级排序模块99的临床目标和要求。当所计算的剂量满足临床目标时,控制器75能够基于优化的节距和优化的小射束权重来确定治疗方案(步骤212)。一旦控制器75确定治疗方案,控制器75就能够输出治疗方案(步骤216)。
图7图示实现方法150的优化过程(步骤166)的另一方法300。方法300以输入的初始参数作为起始点开始(步骤304)。例如,能够由用户输入初始节距和初始小射束权重正弦图。所述初始参数也能够由控制器75基于已经输入到其它模块95、97和99中的信息,或者基于存储器81中保存的预先确定图表而输入。在图示的实施例中,初始正弦图表示具有相等权重的小射束30a。在其它实施例中,初始正弦图表示不同的小射束权重集合。除了初始节距和初始正弦图之外,能够添加先前未输入到模块95、97、99和100中的任一个中的任何临床目标(步骤304)。例如,可以输入期望的剂量和限制特定区域或结构可以接收的辐射量的一组临床约束条件。
然后,控制器75执行指令以计算根据输入参数得到的剂量(步骤308a)。在图示的实施例中,基于初始节距和初始小射束权重正弦图来计算剂量。控制器75能够将所计算的剂量与目标进行比较(步骤308a)。例如,控制器75能够确定所计算的剂量与所期望的剂量或所期望的剂量体积正弦图有多接近。控制器75还能够确定所计算的剂量是否在约束条件的范围内。在一些实施例中,从方法300中省略步骤304和步骤308a。
控制器75然后执行用于优化模块100的指令,以执行优化过程来调整小射束权重(步骤312)。更具体地,控制器75通过执行小射束权重调制的多个迭代来优化小射束权重,以实现期望的剂量。在每个优化迭代期间,从前一迭代调整小射束权重。在第一迭代期间,从初始正弦图调整小射束权重,所述初始正弦图表示具有相等小射束权重的小射束30a。在图示的实施例中,小射束权重30a的优化基于轴向几何结构,其中台架18被建模为移动通过一系列的圆形轨迹,所述一系列的圆形轨迹被治疗床82位置的小增量分离开。换句话说,基于台架18的被治疗床82的离散线性平移分离开的一组离散圆形旋转来计算小射束的优化。另一方面,使用螺旋几何结构来计算剂量,所述螺旋几何结构被建模为将台架18的连续旋转与治疗床82的连续平移相结合以形成螺旋。因此,在计算剂量之前,使小射束权重正弦图从轴向几何结构转换为螺旋几何结构(步骤316)。
控制器75然后执行指令,以基于在优化期间确定的调整的小射束权重来计算剂量(步骤308b)。在一些实施例中,在优化小射束权重的每个迭代之后计算剂量。在这种情况下,在优化小射束权重的每个迭代之间,使小射束权重正弦图转换为螺旋几何结构。在其它实施例中,仅每几个优化迭代来计算剂量。在这种情况下,仅当计算剂量时,可以使小射束权重正弦图转换为螺旋几何结构。例如,每当优化模块100执行全剂量迭代时能够执行节距优化,同时所有近似剂量迭代能够完全在轴向几何结构上操作。
方法300还包括优化治疗输送系统11的节距(步骤320)。控制器75执行用于优化模块100的指令以确定最接近初始节距输入的最佳节距。在终止优化过程之前,控制器75能够执行优化节距的多个迭代。在一些实施例中,在节距被调整之前调整小射束权重,然而,在其它实施例中,节距首先被调整。而且,如上面相对于方法200所讨论的,小射束权重优化和节距优化可以例如使用交替的循环同时发生。可替选地,小射束权重优化和节距优化可以作为顺序地发生的不同和单独的循环执行。另外,能够变化迭代的数目,并且能够以如上面相对于方法200所描述的多种方式终止小射束权重和节距的优化。
控制器75然后可以执行指令以基于在优化期间确定的调整的节距来计算剂量(步骤308c)。如上面相对于步骤308b所描述,可以在一些优化迭代而不是其它迭代之间计算剂量。另外,在一些实施例中,在计算剂量和确定治疗方案之前,使节距转换为新的几何结构(参见图8中的步骤324)。例如,节距可以被转换为不同的螺旋几何结构。
虽然在使用螺旋几何结构优化的节距并且使用轴向几何结构优化的小射束权重的情况下图示方法300,但是也能够使用多种其它几何结构。例如,在一些实施例中,使用第一螺旋几何结构优化节距,并且使用与第一几何结构不同的第二螺旋几何结构优化小射束权重。在该实施例中,当确定治疗方案时,使节距和小射束权重转换为相同的几何结构。这能够以多种方式完成。例如,可以使节距从第一几何结构转换为第二几何结构,可以使小射束权重从第二几何结构转换为第一几何结构,或者可以使节距和小射束权重二者转换为第三几何结构。在其他实施例中,使用第一螺旋几何结构优化节距,使用第一轴向几何结构优化小射束权重,并且然后使节距和小射束权重二者转换为第三几何结构。能够在每个优化循环之间或者仅在完成优化过程之后转换节距和小射束权重的几何结构。
在一些实施例中,优化的节距、优化的小射束权重、或治疗方案可以包括变化的几何结构。例如,优化的节距可以是变化的节距,使得节距在治疗方案的不同部分使用不同的几何结构。换句话说,节距在治疗方案的第一部分期间可以具有第一螺旋几何结构,并且在治疗方案的第二部分期间可以具有第二螺旋几何结构。
图8图示可用的不同优化循环中的一些。通过循环a来表示节距优化的单个迭代(步骤320)。循环a包括将节距转换为新的几何结构的可选步骤(步骤324)。当不同的几何结构被用来计算小射束权重或计算剂量以及确定治疗方案时,可能需要的是,将节距的几何结构转换为小射束权重的几何结构,或者转换为被用于计算剂量和确定治疗方案的几何结构。然而,该步骤不是始终需要的。通过循环b来表示小射束权重优化的单个迭代(步骤312)。类似于循环a,循环b包括将小射束权重转换为新几何结构的可选步骤(步骤316)。小射束权重可以被转换为优化节距的几何结构,或者转换为被用于计算剂量和确定治疗方案的另一几何结构。优化节距和小射束权重二者的迭代组合循环a和循环b。这能够被称为ab循环。
而且,如先前所提及,每次优化节距或小射束权重时可以不执行剂量计算(步骤308)。因此,在不需要在之后计算剂量的情况下(步骤308),循环c表示节距的优化(步骤320)。循环c一般也将不包括将节距转换为新的几何结构(步骤324)。然而,在一些实施例中,即使当剂量未被计算时,也可以将节距转换为新的几何结构。在不需要在之后计算剂量(步骤308)的情况下,循环d表示小射束权重的优化(步骤316)。与循环c一样,循环d一般将不包括将小射束权重转换为新几何结构的步骤(步骤316),但是一些实例中可以包括该步骤(步骤316)。当最后一次计算剂量并且剂量满足临床目标时,控制器75确定治疗方案。控制器75能够使用最近优化的节距和优化的小射束权重来确定治疗方案。
能够通过将一系列优化循环组合在一起来执行方法300,类似地相对于方法200所讨论的那些。循环a到循环d能够被组合成各种系列,以完成方法150的完整优化过程(步骤166)。例如,可以根据以下系列:badbca—重复两次使用方法300来执行优化过程(步骤166)。在该实施例中,根据交替的系列同时地优化节距和小射束权重。控制器还能够执行用于优化模块100的指令以遵循作为单独的循环优化节距和小射束权重的系列。例如,可以被遵循以下系列:ccacca—ddbddb。在该实施例中,在优化小射束权重正弦图之前,完全地优化了节距。图7还通过“可选的重复”记号指示可以重复优化循环的方式中的一些。
超出方法200和方法300中描述的那些步骤的附加步骤可以被包括在优化过程(步骤166)中。例如,控制器75可以执行指令以对小射束权重应用缩放因子。这允许将剂量按比例增大或按比例减小,以实现所期望的剂量或主要剂量体积直方图点。另外,控制器75可以执行指令,以对小射束权重相互变化的程度进行限制。小射束30a的权重之间的变化程度被称为调制系数。当小射束权重开始变化太多(例如,一个叶片66相对于另一个叶片66打开非常长的时间量)时,控制器75能够限制(或钳制)小射束权重不同的程度。在一个实施例中,通过取小射束权重的平均值,并且将其乘以用户选择的调制系数(例如,2.0)来确定所述极限。这将变成最大可能的小射束权重。当小射束权重超出最大值时,控制器能够执行指令以将该小射束权重减小到最大值。
一旦优化了小射束权重正弦图和节距(步骤166),控制器75执行以通过实现分割过程来完成方法150(步骤170)。如本文所描述,方法200、300主要在治疗规划阶段期间使用,以帮助确定最佳治疗方案。在其它实施例中,能够在治疗期间执行方法200、300,使得能够在治疗中途调整治疗输送系统11的节距和小射束权重。
以下权利要求中阐述了本发明的各种特征和优点。
- 还没有人留言评论。精彩留言会获得点赞!