包含芫花树花提取物或其分离物作为有效成分的神经退行性疾病预防或者治疗用药学组合物的制作方法
本发明涉及包含芫花树花提取物或其分离物作为有效成分的神经退行性疾病预防或者治疗用药学组合物以及保健功能食品。
背景技术:
神经退行性疾病(neurodegenerativediseases)与神经细胞退化、丧失功能和种种死亡情况的症状相关。具有神经退行性疾病的患者在认知(cognitive)或者运动(motor)能力方面可经历严重的退化,并且这些疾病主要是进行性的,因此作为结果可显然地减少他们的生活质量和对生活的期待。
这些疾病包括:帕金森病(parkinson'sdisease;pd)、阿尔茨海默氏病(alzheimer’sdisease;ad)、肌萎缩性侧索硬化症(amyotrophiclateralsclerosis;als)、亨廷顿病(huntington’sdisease;hd)、额颞叶痴呆(frontotemporaldementia)、皮质基底核退化症(corticobasaldegeneration)、进行性核上性麻痹(progressivesupranuclearpalsy;psp)以及其他疾病。
另一方面,已知许多神经退行性疾病涉及nurr1(核受体相关1(nuclearreceptorrelated1))蛋白质。nurr1意指也被已知的nr4a2(核受体亚科4,a组,第二成员(nuclearreceptorsubfamily4,groupa,member2))的核受体相关1蛋白质,其已知为由人的nr4a2基因加密。所述nurr1蛋白质为一种孤儿核受体(orphannuclearreceptor),虽然尚未查明对所述nurr1蛋白质的配体(ligand),但已经查明了nurr1蛋白质执行在大脑中维持多巴胺系统(dopaminergicsystem)的核心作用。若nurr1或nr4a2基因出现异常,则多巴胺系统的功能受损而诱发帕金森病,不仅如此,也成为类风湿性关节炎、精神分裂症和躁郁症等广范围的炎症以及神经性疾病的诱因,并且这是广为人知的。由所述nurr1的功能障碍诱发的代表性神经退行性疾病是帕金森病。
帕金森病的主要症状是颤抖、僵硬、运动缓慢以及步态异常症状等,是现代老龄化社会的主要疾病之一,并且是在脑的黑质(substantianigra)和纹状体(corpusstriatum)部位缺乏称为多巴胺(dopamin)的神经递质而引起的慢性疾病。
作为用于治疗如上所述的帕金森病的药物,已知的有左旋多巴(l-dopa)制剂、多巴胺受体作用剂、抗胆碱药剂、咪多吡(eldepryl)等,这些药物大部分并不是治疗病因,而是起到调节症状的作用,因此需要持续服用药物。尽管到目前为止作为治疗帕金森病治疗剂已经生产并商业化了许多的药,但尚未开发出用于完全治疗帕金森病的本质性的治疗剂。
最近,已经报道了活化nurr1蛋白质功能的化合物对帕金森病具有良好的药效,从而可以用作帕金森病治疗剂的疾病靶标,其中nurr1蛋白质在多巴胺神经细胞的分化、生长以及维持中起着重要作用。
在本申请人在之前申请的韩国专利注册第10-1631589中,已经证实过芫花树茎和/或根提取物干预nurr1蛋白质的活化,并且当注射于患有帕金森病的动物样本时,确认到帕金森病的症状缓解。
然而,对于本申请人在在先申请的芫花树茎和/或跟提取物,在用于开发天然产物新药的非临床稳定性试验中的回复突变试验和染色体异常试验中被确认为具有遗传毒性。
为了改善如上所述的问题,本发明人发现在中药配方上用作药材的芫花树花没有遗传毒性的同时在神经退行性疾病的预防或者治疗方面更有效,从而完成了本发明。
(现有技术文献)
(专利文献)
韩国注册专利第10-1631589号
技术实现要素:
要解决的问题
本发明的目的在于,提供包含芫花树花提取物或其分离物作为有效成分的神经退行性疾病的预防或者治疗用药学组合物。
另外,本发明的目的在于,提供包含芫花树花提取物或其分离物的神经退行性疾病的预防或者改善用保健功能食品。
解决问题的方案
以下,详细说明本发明。
作为用于达到上述目的的一实施方式,本发明提供包含芫花树花(daphnegenkwaflower)提取物及其分离物作为有效成分的神经退行性疾病的预防或者治疗用药学组合物。
在本发明中使用的术语“芫花树(daphnegenkwa)”是双子叶植物纲、桃金娘目、瑞香科属落叶灌木,也称为药鱼草树、老鼠花树。芫花树主要生长在海岸附件,在中医学中使用于治疗利尿、水肿、肾炎等症状。芫花树的干花蕾称为芫花或莞花,用作药材,并且具有轻微的毒性。众所周知,芫花树花提取物含有芫花素(genkwanin)、羟基芜花素(hydroxygenkwanin)、芹菜素(apigenin)以及谷甾醇(sitosterol)等,除此之外,含有苯甲酸(benzoicacid)和刺激性的精油物质。
在本发明中,使用的术语“芫花树花提取物”意指从芫花树花或者花蕾获取的提取物,优选为意指用水或者有机溶剂对芫花树花或者花蕾进行提取而获取的提取物,具体地说意指用水、c1至c4的低级烷基醇或者这些混合溶剂提取而获取的提取物。
本发明一实施例的芫花树花提取物优选用80%乙醇提取的提取物。
根据本发明的一实施例,对于芫花树花和/或花蕾,使用水、甲醇、乙醇、丁醇等的c1至c4低级烷基醇等的有机溶剂或者c1至c4低级烷基醇水溶液而获取芫花树花提取物。所述芫花树花提取物可包含芫花素n(genkwaninn)或者芫花酯甲(yuanhuacine)。
所述芫花素n为由以下化学式1表示的萜类化合物,具体地,为二萜酯化合物,可通过对本发明所属领域的技术人员公知的方法制造,优选地,可从芫花树花或者花蕾提取、分离。
化学式1
所述芫花酯甲为由以下化学式2表示的萜类化合物,具体地,为二萜酯化合物,可通过对本发明所属领域的技术人员公知的方法制造,优选地,可从芫花树花或花蕾提取并分离。
化学式2
在本发明中使用的术语“分离物”意指使用特定溶剂从所述芫花树花提取物分离具有本发明中作为目的的活性的物质而得到的活性分离物(fraction)。
根据本发明的其他一实施例,对于所述获取的芫花树花提取物利用己烷、乙酸乙酯、丁醇或蒸馏水等的有机溶剂的混合溶剂而分离并获取各个溶剂的分离层,然后利用色层分析等的所属技术领域公知的分离方法分离并提制高纯度的活性成分,进而可制造出分离物。通过多种提纯方法得到的分离物也包含在本发明的分离物内。所述芫花树花提取物的分离物可包含芫花素n(genkwaninn)或者芫花酯甲。
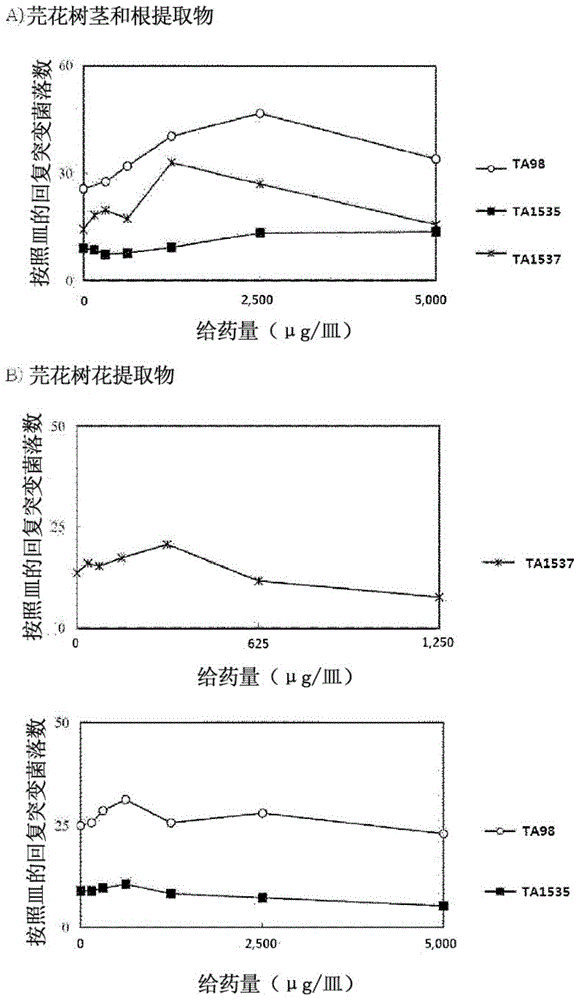
本发明的芫花树花提取物或者其分离物除了通过上述的提取溶剂提取的提取物之外,还不限制地包含通过通常的精制过程的提取物。本发明人已确认本申请人在在先申请的国内专利注册第10-1631589号的芫花树茎和根提取物在用于开发作为天然物新药的非临床安全性试验中的回复突变试验以及染色体异常试验中具有遗传毒性(图1a)。另一方面,芫花树花提取物的遗传毒性试验结果,确认到在回复突变试验以及染色体异常试验中都不具有遗传毒性(图1b)。
本发明人还比较并分析了芫花树花提取物以及芫花树茎和根提取物的有效成分的结果,在芫花树花提取物以及芫花树茎和根提取物中全部检测到作为有效成分的芫花素n及芫花酯甲。对各个有效成分进行定量结果,确认到芫花树花提取物中的芫花素n(genkwaninn)及芫花酯甲的量相比于芫花树茎和根提取物分别多约7.32倍及1.23倍(图2)。
另外,比较及实验芫花树花提取物以及芫花树茎和根提取物的nurr1蛋白质的活性度的结果,确认到本发明的芫花树花提取物相比于芫花树茎和根提取物表示出更高的活性(图4)。
再则,本发明人对6-ohda诱导性帕金森动物样本给食调配有芫花树花提取物的饲料,之后进行阿扑吗啡诱导的旋转试验(apomorphine-inducedrotatinotest),从试验结果可确认到相比于给食一般饲料的对照组显著减少旋转数(图5)。
如上所述,本发明人确认到芫花树花提取物增加nurr1蛋白质活性度,进而对预防或治疗由直接受nurr1蛋白质影响的多巴胺神经细胞的损伤诱发的多种疾病方面具有效果。所述多种疾病为,例如帕金森病以及帕金森病之外的由nurr1的功能障碍诱发的多种神经退行性疾病。
因此,可以知道本发明的包含芫花树花提取物或者其分离物作为有效成分的药学组合物在nurr1蛋白质的活化方面具有效果,因此对预防或治疗由直接受nurr1蛋白质的活性影响的多巴胺性神经细胞的损伤诱发的多种疾病方面具有效果。所述多种疾病为,例如帕金森病以及帕金森病之外的nurr1的功能障碍诱发的多种神经退行性疾病。
本发明中使用的术语“神经退行性疾病”意指神经细胞退化、丧失功能、且坏死的情况下出现的症状相关的疾病,包括:帕金森病(parkinson'sdisease;pd)、阿尔茨海默氏病(alzheimer’sdisease;ad)、肌萎缩性侧索硬化症(amyotrophiclateralsclerosis;als)、亨廷顿病(huntington’sdisease;hd)、额颞叶痴呆(frontotemporaldementia)、皮质基底核退化症(corticobasaldegeneration)、进行性核上性麻痹(progressivesupranuclearpalsy;psp)。优选地,本发明的神经退行性疾病是帕金森病。
本发明的药学组合物,除了上述记载的有效成分或其分离物之外,可包含药学上可接受的载体、赋形剂或稀释剂。所述载体、赋形剂或稀释剂可以举乳糖、葡萄糖、蔗糖、山梨糖醇、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯胶、海藻酸钠、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁和矿物油。
本发明的药学组合物分别根据通常的方法以散剂、颗粒剂、片剂、胶囊、悬浮液、乳剂、糖浆剂、气雾剂等的口服型制剂、外用制剂、栓剂或灭菌注射液的形态进行剂型化来使用。详细地,在进行剂型化时,可使用常规使用的填充剂、加重剂、粘合剂、润湿剂、崩解剂、表面活性剂等稀释剂或赋形剂来调配。用于口服的固形制剂包括片剂、丸剂、散剂、颗粒剂、胶囊等,但不限于此。这种固形制剂可混合至少一种赋形剂,例如淀粉、碳酸钙、蔗糖、乳糖、明胶等来调配。另外,除了单纯的赋形剂之外也可适用诸如硬脂酸镁、滑石粉的润滑剂等。用于口服的液状物除了液体石蜡之外,还可添加各种赋形剂,例如,保湿剂、甜味剂、芳香剂、保存剂等来进行调配。用于非口服的制剂包括灭菌水溶液、非水溶剂、悬浮液、乳液、冷冻干燥制剂以及栓剂。非水溶性溶剂及悬浮液可使用丙二醇、聚乙二醇、诸如橄榄油的植物油、诸如油酸乙酯的可注射酯等。栓剂的基剂可使用威泰索尓(witepsol)、聚乙二醇、吐温(tween)61、可可脂、(三)月硅酸甘油酯、甘油明胶(glycerogelatine)等。
本发明的药学组合物,根据目标的方法可口服或者非口服(例如,适用于静脉、皮下腹腔内或者局部)。
本发明的药学组合物可以以药学上有效的量,即可以以在医学性预防或者治疗上能够适用的合理的受益/风险比例,以预防或者治疗疾病而充分注射的量来给药。有效用量水准根据疾病的重症程度、药物的活性、患者的年龄、体重、健康、性别、患者对药物的敏感程度、使用的本发明的组合物的给药时间、给药途径以及排放比例、治疗时间、包含与所使用的本发明的组合物调配或同时使用的药物的要素以及其他医学领域公知的要素而不同,但是可由本发明所属领域的技术人员适当的选择。
本发明的包含芫花树花提取物或其分离物作为有效成分的药学组合物的给药量或者服用量根据患者年龄、身体条件、体重等而变为多样化,但优选通常在0.01~1,000mg/kg(体重)/1日范围内给药。然后,在1日有效给药量范围内可一日一次或者一日分多次给药。
作为用于达到上述目的的其他一实施方式,提供包含本发明的芫花树花提取物或其分离物的神经退行性疾病的预防或者改善用保健功能食品。
在本发明中使用的术语“保健功能食品”意指根据保健功能食品的相关法律第6727号使用具有有利于人体的功能性的原料或者成分制造及加工的食品;所谓“功能性”意指以要得到在针对人体的结构及功能调节营养素或者生理学作用等的保健用途方面有用的效果为目的而进行摄取的情形。
在使用本发明的芫花树花提取物或其分离物用作食品添加剂的情况下,可在食品或者饮料直接添加所述提取物或其分离物或者与其他食品添加剂一同组合使用。在制造食品或者饮料时添加本发明的芫花树花提取物或其分离物时,对于其添加量不作特别限制,但是对于最终食品的重量可以以1至5重量%,优选为1至3重量%的添加量来添加。但是,在以健康以及卫生为目的或者以调节健康为目的长时间摄取时,添加量可以在所述范围以下,但在安全方面没有问题时,也可使用所述范围以上的量。
同时,对于所述食品或者饮料的种类不做特别限制,但是全部包括常规意义上的食品或者饮料,优选地,包括:肉类、香肠、面包、巧克力、糖类、零食类、饼干类、披萨、泡面、其他面类、口香糖类、包括冰淇淋类的酪农制品、各种汤、饮料、茶、口服液、酒精饮料以及综合维生素等。
在将本发明的芫花树花提取物或其分离物添加于食品的情况下,可与各种营养素、维生素、电介质、香精、着色剂、果胶酸及其盐、海藻酸及其盐、有机酸、保护性胶体增稠剂、ph调节剂、稳定剂、防腐剂、甘油、酒精等的辅助成分一起添加。
在将本发明的芫花树花提取物或其分离物添加于饮料的情况下,如同常规饮料作为附加成分可包含各种甜味剂或天然碳水化合物等。此时,所述甜味剂不会被特别限制于此,而是可使用诸如索马甜、甜叶菊提取物的天然甜味剂或者诸如糖精、阿斯巴甜的合成甜味剂等;所述天然碳水化合物并不会被特别限制于此,可使用单糖(例如,葡萄糖、果糖等)、二糖类(例如,麦芽糖,蔗糖等)、多糖类(例如,糊精、环糊精等)、糖醇(例如,木糖醇、山梨糖醇、赤藓糖醇(erythitol)等)等。
对于本发明的芫花树花提取物或其分离物,确认到了安全性,并且包含本发明的芫花树花提取物或其分离物的保健功能食品可表现出预防或者改善神经退行性疾病的效果。
作为用于达到上述目的的又一实施方式,本发明提供神经退行性疾病的预防或者治疗方法,该方法包括:将包含芫花树花提取物或其分离物作为有效成分的药学组合物给药至需要所述药学组合物的对象体的步骤。
本发明中使用的术语‘芫花树(daphnegenkwa)’、‘芫花树花提取物’、‘分离物’、‘神经退行性疾病’及‘给药’等术语与上述说明相同。
本发明中的所述对象体指动物,典型的为,以利用本发明的提取物的治疗来能够表现出有益效果的哺乳动物。作为这些对象体的优选例包括与人类相同的灵长类。另外,与其相同的对象体包括具有神经退行性疾病症状或可能具有与神经退行性疾病症状相同症状的危险的对象体全部。
作为用于达到上述目的的又一实施方式,本发明提供用于神经退行性疾病的预防或者治疗的芫花树花提取物或其分离物的使用。
作为用于达到上述目的的又一实施方式,本发明提供用于生产具有神经退行性疾病的预防或者治疗效果的药剂的芫花树花提取物或其分离物的使用。
本发明中使用的术语‘芫花树(daphnegenkwa)’、‘芫花树花提取物’、‘分离物’及‘神经退行性疾病’等术语与上述说明相同。
发明效果
发明的包含本芫花树花提取物或其分离物作为有效成分的药学组合物在不表现出其他副作用的同时,还在恢复根据神经受损的nurr1蛋白质的活性抑制方面具有优秀的效果,从而在因nurr1蛋白质的活性抑制诱发的神经退行性疾病的预防或者治疗方面有优秀的效果。
附图说明
图1a示出诱发芫花树茎和/或根提取物的回复突变诱变;图1b示出芫花树花提取物未出现回复突变诱变。ta98意指鼠伤寒沙门氏菌(salmonellatyphimurium)ta98菌株;ta1535意指鼠伤寒沙门氏菌(salmonellatyphimurium)ta1535菌株;ta1537意指鼠伤寒沙门氏菌(salmonellatyphimurium)ta1537菌株。
图2是示出通过lc-ms/ms方法分析芫花树花提取物的有效成分的结果。a)是标准物质dgh-1(m/z105.2>591.2)以及dgh-2(m/z105.1>639.2),在b)中dgf-ex意指芫花树花提取物、dg-ex意指芫花树茎和/或根提取物。
图3是通过荧光素酶分析显示根据芫花树花提取物浓度的nurr1蛋白质活性度变化的示意图。con-3ul意指对照组(1%dmso)、(**:p<0.01)。
图4是示出通过荧光素酶分析显示根据芫花树茎和/或根提取物与芫花树花提取物的各个浓度的nurr1蛋白质活性度变化的比较实验结果的示意图。dg-ex意指芫花树茎和/或根提取物;dgf-ex意指芫花树花提取物。
图5是示出对于6-ohda(6-羟基多巴胺(6-hydroxydopamine))诱导性帕金森病动物样本给食芫花树提取物2周或者4周之后的旋转试验(rotationtest)结果的示意图。
图6是示出对于6-ohda(6-羟基多巴胺(6-hydroxydopamine))诱导性帕金森病动物样本给食芫花树提取物4周之后通过免疫组化分析观察中脑黑质部多巴胺神经细胞的变化的图面。
图7是示出对于6-ohda(6-羟基多巴胺(6-hydroxydopamine(6-羟基多巴胺))诱导性帕金森病动物样本给食芫花树提取物4周之后比较中脑黑质部多巴胺神经细胞的数的变化的图。pbs意指未注射6-ohda的组;6-ohda意指注射6-ohda的组;6od+1o意指注射6-ohda之后给食10mg/kg芫花树花提取物的组;6od+50意指注射6-ohda之后给食50mg/kg芫花树花提取物的组。
具体实施方式
以下,通过实施例更加详细说明本发明。但是,这些实施例是用于示例性说明本发明,本发明的范围并不限于这些实施例。
比较例1:芫花树茎和/或根提取物的遗传毒性试验
为了确认本申请人在在先申请的韩国专利注册第10-1631589号的芫花树茎和/或根提取物试验管中(invitro)遗传毒性,如下实施了回复突变实验和染色体异常实验。
1-1.制造芫花树茎和根提取物
切细芫花树的茎14kg与根6kg,之后在120l的80%乙醇浸泡48小时,之后进行过滤而分离固形分和初次液状成分。将所述分离的固形分重新在120l的80%乙醇浸泡24小时,之后进行过滤而得到二次液状成分。混合所述获取的初次液状成分与二次液状成分,将所述混合物在减压下进行浓缩,之后将残留物进行冷冻并干燥,从而制造出1140.9g的芫花树茎及根提取物(以下,可称为“dg-ex”)。
1-2.回复突变实验
为了确认芫花树茎及根提取物的遗传毒性,在作为glp(良好实验室规范(goodlaboratorypractice))机关的(株)biotoxtech公司根据食品药品安全局指南实施了回复突变实验。
为了确认作为试验物质的、从所述1-1获取的dg-ex是否有基因突变诱发性,利用作为组氨酸需求性菌株的鼠伤寒沙门氏菌(salmonellatyphimurium)ta98、ta100、ta1535、ta1537和作为色氨酸需求性菌株的大肠杆菌(escherichiacoli)wp2uvra(pkm101)针对代谢活化系统存在(s9+)以及代谢活化系统不存在(s9-)的情况实施了回复突变试验。
(1)计量设定试验
为了设定作为本试验的回复突变试验的最大计量,将从指南推荐的5,000μg/皿(plate)作为最大计量,以下以公比4用1,250、313、78.1以及19.5μg/皿实施计量设定试验。
其结果,在代谢活化系统不存在下的ta98菌株的5,000μg/皿、ta100、ta1535以及ta1537菌株的313μg/皿以上,代谢活化系统存在下的ta100、ta1535以及ta1537菌株的5,000μg/皿中观察到由dg-ex导致的生长抑制。在代谢活化系统不存在下的wp2uvra(pkm101)菌株,在代谢活化系统存在下的ta98以及wp2uvra(pkm101)菌株中没有观察到生长抑制。
因此,如下表1设定了作为本试验(即,回复突变试验)的计量。另外,设定了阴性对照组以及阳性对照组。
表1
在代谢活化系统不存在及存在下的所有计量中都未观察到作为试验物质的dg-ex的沉淀。
(2)回复突变实验
向各个菌株将试验物质dg-ex以所述浓度分别进行处理后进行培养,之后用肉眼计数回复突变菌落数。并且,将该结果显示于下表2。
表2
s.d:标准偏差
*:表示生长抑制
其结果,在代谢活化系统存在下的ta1537菌株的1,250μg/皿中回复突变菌落数相比于阴性对照组能够再现性地增加了2倍以上,在2,500μg/皿以上中观察到通过dg-ex的生长抑制,从而观察到回复突变菌落数减少的倾向。
在代谢活化系统不存在下的ta98、ta100、ta1535、ta1537及wp2uvra(pkm101)菌株和代谢活化系统存在下的ta98、ta100、ta1535及wp2uvra(pkm101)菌株中,不论在试验物质组中是否存在代谢活化系统,针对各个菌株的所有计量,回复突变菌落数并未超出阴性对照组的2倍,并且并未观察到计量依赖性的增加。
针对各个菌株的阳性对照组的回复突变菌落数相比于阴性对照组确实增加了2倍以上。并且,将结果显示图1。
如图1a所示,在本试验条件下,试验物质dg-ex在代谢活化系统存在下的ta1537菌株中回复突变菌落数增加到阴性对照组的2倍以上,因此判定为有基因突变诱发性。
1-3.染色体异常实验
为了确认芫花树茎和根提取物的遗传毒性,在作为glp(良好实验室规范(goodlaboratorypractice))机关的(株)biotoxtech公司根据食品药品安全局指南实施了染色体异常试验。
为了确认作为试验物质的、从所述1-1获取的dg-ex的染色体是否有结构异常诱发性,使用作为哺乳类的培养细胞株的chl(中国仓鼠肺(chinesehamsterlung))/iu细胞评价了是否有染色体的结构异常诱发性。
(1)细胞增殖抑制试验
为了设定作为本试验的染色体异常试验的最高计量,将dg-ex5,000μg/ml作为最高计量,以下用2,500、1,250、625、313、156、78.1、39.1以及19.5μg/ml实施了细胞增殖抑制试验。细胞增殖抑制试验是dg-ex处理之后计算相对细胞增加数量(relativepopulationdoubling,rpd)作为抑制细胞增殖的指标。
其结果,在代谢活化系统不存在及存在下、在连续处理法的代谢活化系统不存在下观察到细胞毒性。明确抑制50%以上的计量是短时间处理法的代谢活化系统不存在及存在下的1,250μg/ml以上、连续处理法的代谢活化系统不存在下的625μg/ml以上。
因此,如下表3设定了本试验的计量。另外,设定了阴性对照组及阳性对照组。
表3
在短时间处理法的代谢活化系统不存在及存在下、连续处理法的代谢活化系统不存在下的2,500μg/ml以上中观察到试验物质的沉淀。
(2)染色体异常试验
染色体异常试验结果,短时间处理法的代谢活化系统存在下的450及900μg/ml中具有数值异常的细胞出现频率为12.5和13.0%,与阴性对照组(0%)相比统计学上显然增加。具有结构异常的细胞的出现频率是6.0以及8.0%,与阴性对照组(0%)相比统计学上显然增加(未示出数据)。
短时间处理法的代谢活性系统不存在下及连续处理法的代谢活化系统不存在下具有染色体异常的细胞出现频率不足5%,未确认到染色体异常诱变作用,并且与阴性对照组相比时也未观察到统计性的显然性。
在针对各个处理系列的阳性对照组中,具有结构异常的细胞的出现频率在10%以上,与阴性对照组相比时统计学上显然增加。
据此,为了明确针对短时间处理法的代谢活化系统存在下的结构异常的疑阳性结果,以下表4的计量通过与本试验相同的方法实施了确认试验。
表4
确认试验结果,在短时间处理法的代谢活化系统存在下的900、1,000、1,100以及1,200μg/ml中确认到具有数值异常的细胞的出现频率为12.5、11.5、10.0以及8.5%;与阴性对照组比较统计学上显然增加。确认到具有结构异常的细胞的出现频率为7.5、7.0、8.5以及4.5%,与阴性对照组相比统计学上显然增加。将其结果显示在下表5中。
表5
简称:ctg:染色单体裂隙、csg:染色体裂隙、ctb:染色单体断裂、cte:染色单体互换、csb:染色体断裂、cse:染色体互换、frg:碎裂、end:核内复制、pol:多倍体、b[a]p:苯并[a]芘、rpd:相对群体倍增、trt-rectime:治疗-恢复时间、裂隙-(gap-):具有除了裂隙之外的结构异常的细胞的总数、裂隙+(gap+):具有包括裂隙的结构异常的细胞的总数。
a):从具有染色体异常的细胞数除外的
*:p<0.01、#:p<0.05、##:p<0.01
从以上结果来看,确认到在本试验条件下试验物质dg-ex在短时间处理法的代谢活化系统存在下具有数值异常的细胞的出现频率在10%以上,具有结构异常的细胞的出现频率在5%以上不足10%,因此判定为有染色体异常诱发性。
实施例1:制造芫花树花提取物
将芫花树的花部位3.5kg在70l的80%乙醇中浸泡48小时,之后进行过滤而分离固形分和初次液状成分。将分离的所述固形分重新在70l的80%乙醇中浸泡24小时,进行过滤而获取二次液状成分。混合获取的所述初次液状成分与二次液状成分,之后将所述混合物在减压下进行浓缩,之后将残留物进行冻结并干燥,从而制造出859g的芫花树花提取物(以下,可称为“dgf-ex”)。
实施例2:芫花树花提取物的有效成分分析
分析了从所述实施例1获取的作为芫花树花的提取物的dgf-ex的有效成分。为了比较,也一同分析了从所述比较例1-1获取的作为芫花树及根提取物的dg-ex的有效成分。
在芫花树茎和根提取物有两种有效成分,即dgh-1与dgh-2,其中dgh-1的uv吸光系数(uvextinctioncoefficient)非常低,因此很难通过hplcuv方法分析提取物所含的dgh-1。因此,为了能够有效地分析在提取物中的有效物质dgh-1与dgh-2,用lc-ms/ms的mrm(multiplereactionmonitoring,质谱多反应监测)方法进行了分析。mrm方法是通过检测具有特定产物离子(production)的母离子(parention)来分析复杂样品中的特定物质的方法。
其结果,标准物质dgh-1和dgh-2化合物分别是在3.81分、6.99分检测到的,且在注入0.1ug时分别表示出1.05x104、1.8x104强度(intensity),从而是以相似的敏感度通过mrm方法被检测到的(图2a)。
另外,将各个提取物以10μg/ml浓度溶解于meoh,之后将10μl进行hplc,之后利用mrm方式的lc-ms/ms进行了分析。在芫花树花提取物(dgf-ex)与茎根提取物(dg-ex)中全部检测到有效成分dgh-1和dgh-2(图2b)。
实施例3:芫花树花提取物的遗传毒性试验
为了确认从所述实施例1获取的芫花树花提取物的试管内(invitro)遗传毒性,如下执行了回复突变实验以及染色体异常实验。
3-1回复突变实验
为了确认芫花树花提取物的遗传毒性,在作为glp(良好实验室规范(goodlaboratorypractice)机关的(株)biotoxtech公司根据食品药品安全局指南实施了染色体异常试验。
为了确认作为试验物质的、从所述实施例1获取的dgf-ex是否有基因突变诱发性,利用作为组氨酸需求性菌株的鼠伤寒沙门氏菌(salmonellatyphimurium)ta98、ta100、ta1535、ta1537和作为色氨酸需求性菌株的大肠杆菌(escherichiacoli)wp2uvra(pkm101)菌株针对代谢活化系统存在(s9+)以及不存在(s9-)的情况实施了回复突变试验。
(1)计量设定试验
为了设定本试验的最高计量,将从指南推荐的5,000μg/皿作为最高计量,以下以公比4用1,250、313、78.1以及19.5μg/皿实施了计量设定试验。
其结果,在代谢活化系统不存在下的ta98及ta1535菌株的1,250μg/皿以上、ta100菌株的313μg/皿以上、ta1537菌株的78.1μg/皿以上,代谢活化系统存在下的ta98及ta1535菌株的5,000μg/皿以上、ta100以及ta1537菌株的1,250μg/皿以上观察到根据试验物质dgf-ex的生长抑制。在代谢活化系统不存在及存在下的wp2uvra(pkm101)菌株中没有观察到生长抑制。
因此,如下表6设定了作为本试验的回复突变试验的计量。另外,设定了阴性对照组以及阳性对照组。
表6
(2)回复突变试验
向各个菌株按照所述浓度处理试验物质dgf-ex并进行培养,之后用肉眼对回复突变菌落数进行计数。将其结果显示在下表7。
表7
s.d:标准偏差
*:表示生长抑制
其结果,在试验物质中与是否有代谢活化系统不相关地对各个菌株的所有计量,回复突变菌落数没有超出阴性对照组的2倍,并且也没有观察到计量依赖性的增加。在阳性对照组中各个菌株的回复突变菌落数与阴性对照组相比确实地增加了2倍以上。将其在图1中示出。
如图1b所示,试验物质dgf-ex在代谢活化系统存在下的ta98、ta1535、ta1537的菌株中对所有计量,回复突变菌落数没有超出阴性对照组的2倍,并且没有出现回复突变诱发性。
在代谢活化系统不存在下的ta98及ta1535菌株的625μg/皿以上、ta100菌株的156μg/皿以上、ta1537菌株的87.1μg/皿,在代谢活化系统存在下的ta98及ta1535菌株的2,500μg/皿以上、ta100菌株的1,250μg/皿、ta1537菌株的625μg/皿以上观察到由试验物质引起的生长抑制。在代谢活化系统不存在及存在下的wp2uvra(pkm101)菌株中没有观察到生长抑制。
从上述结果来看,判定本试验条件下试验物质dgf-ex没有遗传突变诱发性。
3-2.染色体异常试验
为了确认芫花树花提取物的遗传毒性,在作为glp(良好实验室规范(goodlaboratorypractice))机关的(株)biotoxtech公司根据食品药品安全局指南实施了染色体异常试验。
为了确认作为试验物质的、从所述实施例1获取的dg-ex是否有染色体结构性异常诱发性,使用作为哺乳类的培养细胞株的chl(中国仓鼠肺(chinesehamsterlung))/iu细胞评价了是否有染色体的结构性异常诱发性。
(1)细胞增殖抑制试验
为了设定作为本试验的染色体异常试验的最高计量,将dgf-ex5,000μg/ml作为最高计量,以下用2,500、1,250、625、313、156、78.1、39.1及19.5μg/ml实施了细胞增殖抑制试验。
其结果,在代谢活化系统不存在及存在下、连续处理法的代谢活化系统不存在下观察到了细胞毒性。明确抑制细胞增殖50%以上的计量是短时间处理法的代谢活化系统不存在下以及存在下的625μg/ml以上、连续处理法的代谢活化系统不存在下的156μg/ml以上。计算抑制大约55%的细胞增殖的计量的结果为,短时间处理法的代谢活化系统不存在的428.3μg/ml以及存在的725μg/ml,连续处理法的代谢活化系统不存在的133.1μg/ml。
因此,如下表8设定了本试验的计量。另外,设定了阴性对照组以及阳性对照组。
表8
(2)染色体异常试验
染色体异常试验结果,短时间处理法的代谢活化系统不存在下及存在下的,连续处理法的代谢活化系统不存在下的具有染色体异常的细胞的出现频率不足5%,没有确认到染色体异常诱发作用,与阴性对照组相比也没有观察到统计学上显然的差异。在针对各个处理组的阳性对照组中,具有结构异常的细胞的出现频率为10%以上,在与阴性对照组比较时,统计学上显然地增加。将其结果显示在下表9。
表9
简称:ctg:染色单体裂隙、csg:染色体裂隙、ctb:染色单体断裂、cte:染色单体互换、csb:染色体断裂、cse:染色体互换、frg:碎裂、end:核内复制、pol:多倍体、mmc:丝裂霉素cb[a]p:苯并[a]芘、rpd:相对群体倍增、trt-rectime:治疗-恢复时间、裂隙-(gap-):具有除了裂隙之外的结构异常的细胞的总数、裂隙+(gap+):具有包括裂隙的结构异常的细胞的总数。
a):从具有染色体异常的细胞数中除外的
*:p<0.01
从上述结果,在本试验条件下试验物质dgf-ex的染色体异常诱发性判定为阴性。
实施例4:针对nurr1蛋白质活性的芫花树花提取物的效果确认
为了确认从所述实施例1获取的dgf-ex的nurr1蛋白质活性,利用gal4鉴定系统(gla4assaysystem)执行了nurr1蛋白质活性实验。
将gal4-lbd质粒、gal4能够结合的荧光素酶(luciferase)质粒及β-半乳糖苷酶(β-galactosidase)转染于源自人的神经母细胞(neuroblast)的be(2)c细胞,之后将dgf-ex以1、25以及40ppm的浓度处理16小时,将如此处理的细胞在37℃,5%二氧化碳培养基中培养20小时,之后在dmso中溶解提取物,而在对照组处理1%dmso,之后执行了荧光素酶荧光分析。将其结果显示于图3。
如图3所示,确认到在be(2)c细胞中根据dgf-exnurr1蛋白质的活性增加。dgf-ex是在1ppm以及25ppm的浓度下有意义地活化了nurr1蛋白质。尤其是,在以25ppm的浓度处理dgf-ex时,体现出了最大活性,与对照组相比表现出约2倍以上的nurr1蛋白质活化的活性。
另外,利用如上的方法比较了dgf-ex与从所述比较例1获取的dg-ex的nurr1蛋白质活性,并将其结果显示于图4。
如图4所示,dgf-ex相比于dg-ex,在1、10以及50ppm下分别表现出21、23、120%的高活性。
实施例5:在帕金森病动物样本中的芫花树花提取物的效果确认
为了确认芫花树花提取物对帕金森病动物样本的影响执行了本试验。
为了特异地杀死中脑黑质中存在的多巴胺性神经元,作为实验组对18只6周龄的sd大鼠(koatech公司)利用立体定位工具(stereotaxictool)在脑部的ap(-4.3)、ml(-1.8)、dv(-8.2)部位和ap(-5.0)、ml(-1.8)、dv(-8.2)部位直接注入6-ohda(0.2μg/μl,最终容积5μl)制备了帕金森病动物样本。在给予所述6-ohda30分钟之前给予25mg/kg的地昔帕明(desipramine),进而抑制了多巴胺性神经细胞之外的细胞死亡。另外,作为对照组对6只6周龄的sd大鼠(koatech公司)注入了pbs,来代替6-ohda。
在注入6-ohda的18只中,对于6只给予一般饲料(对照组),对于6只给食以芫花树花提取物的一日计量成为50mg/kg的方式调配的饲料,对于剩余6只给食以芫花树花提取物的一日计量成为100mg/kg的方式调配的饲料。
在手术后2周及4周时执行了旋转试验(rotationtest)。若对帕金森病动物样本注射作为多巴胺受体作用物质的阿扑吗啡(apomorphine),则由多巴胺的神经切除后超敏感症(denervationsupersensitivity)而诱发向病变相反侧的旋转。这可利用旋转运动测量仪(rotometer)定量测量。并且,将该结果显示在图5。
如图5所示,芫花树花提取物相比于公知的芫花树根提取物的常规给药浓度,即便以低浓度给药,在喂食饲料2周及4周后的、包括由阿扑吗啡引起的旋转数的大鼠中,确认到显著降低。
实施例6析帕金森病动物样本中的芫花树花提取物的效果的免疫组化学分析
在所述实施例5中,在确认芫花树花提取物对帕金森动物样本的治疗效果之后,追加调查了中脑黑质(substantianigra)部位中,实际上是否因给药芫花树花提取物而抑制了神经细胞的死亡。
与以所述实施例5相同的方式制备帕金森病动物样本之后,在手术后第四周杀死大鼠后用4%的多聚甲醛(paraformaldehyde)进行灌流(perfusion)之后取出脑部。用振动切片机(vibratome)将所述脑部制备成40μm的薄片(section),之后用酪氨酸羟化酶(tyrosinehydroxylase)抗原实施了免疫染色(immunostaining)。用3%过氧化氢液处理所述薄片之后用pbs清洗三次,之后用5%马血清(horseserum)在常温下封闭1小时,之后将酪氨酸羟化酶抗原在4℃下进行整夜处理。用pbs清洗所述薄片(section),之后将抗兔(anti-rabbit)igg进行二次处理,之后将抗生物素蛋白-生物素化的过氧化物酶复合物(avidin-biotinylatedperoxidasecomplex)和3,3'-二氨基联苯胺进行处理。在显微镜下观察上色而被染色的多巴胺神经元,并将结果显示于图6,并且对神经细胞数进行计数,将该结果显示图7。
如图6所示,若将注入6-ohda的左侧黑质(6-ohda)和未注入6-ohda的右侧黑质部位(unlesioned)进行比较,则投入一般饲料(vehicle)的大鼠的情况在注射6-ohda的黑质部位中的多巴胺神经细胞,与正常黑质相比,显然减少。但是,将芫花树花提取物(dgf)以10mg/kg与50mg/kg给药的情况下,确认到在注射6-ohda的黑质中也保持与正常黑质部位类似水准的神经细胞。
另外,如图7所示,注入6-ohda的结果97.5%的多巴胺神经细胞死亡,但是在给药10mg/kg与50mg/kg的芫花树花提取物(dgf)时,确认到了显然抑制多巴胺神经细胞死亡(分别死亡39.6%以及70.1%)。
据此,可以知道芫花树花(dgf)提取物强力抑制由6-ohda引起的多巴胺神经细胞死亡。
- 还没有人留言评论。精彩留言会获得点赞!