用于治疗慢性阻塞性肺病的医药组合物及其方法与流程
本发明涉及一种用于治疗慢性阻塞性肺病的医药组合物,以及其方法。
背景技术:
干细胞为具有广泛性治疗应用潜力的多能性细胞。干细胞疗法已成为对哮喘、支气管肺发育不全症以及慢性阻塞性肺病等肺部疾病的有潜力的疗法。在临床前研究中,干细胞治疗对肺病显示出良好的结果,此外,临床研究指出对晚期的慢性阻塞性肺病病人施用干细胞是安全的且无明显不良反应。在以干细胞为基础的疗法中,在肺部疾病的临床前及临床应用通常使用静脉注射以施用干细胞。
us9415036b2公开了一种医药组合物,用于骨关节疾病的急性及/或慢性治疗或预防,其包含适当的药物载体或稀释剂、多糖及/或糖胺聚糖、抗发炎剂以及干细胞。
技术实现要素:
在一方面,本发明提供一种用于治疗慢性阻塞性肺病的医药组合物。该医药组合物包括有效量的人类间质干细胞,人类血清白蛋白,以及医药上可接受的载体或稀释剂。
另一方面,本发明提供一种在有需要的个体中治疗慢性阻塞性肺病的方法。该方法包含步骤:对该个体施用医药组合物,其包含有效量的人类间质干细胞,人类血清白蛋白,以及医药上可接受的载体或稀释剂。
根据本发明,该医药组合物可通过包含以下步骤的方法制备:将该人类间质干细胞与该医药上可接受的载体或稀释剂混合,该医药上可接受的载体或稀释剂补充有有效量的人类血清白蛋白。
应了解先前的一般描述及以下的详述均仅为示例性及解释性且并不限制本发明。
附图说明
本发明先前的概述以及以下详述在配合附图阅读时得以更好地被了解。为说明本发明,在附图中显示目前优选的实施例。
在附图中:
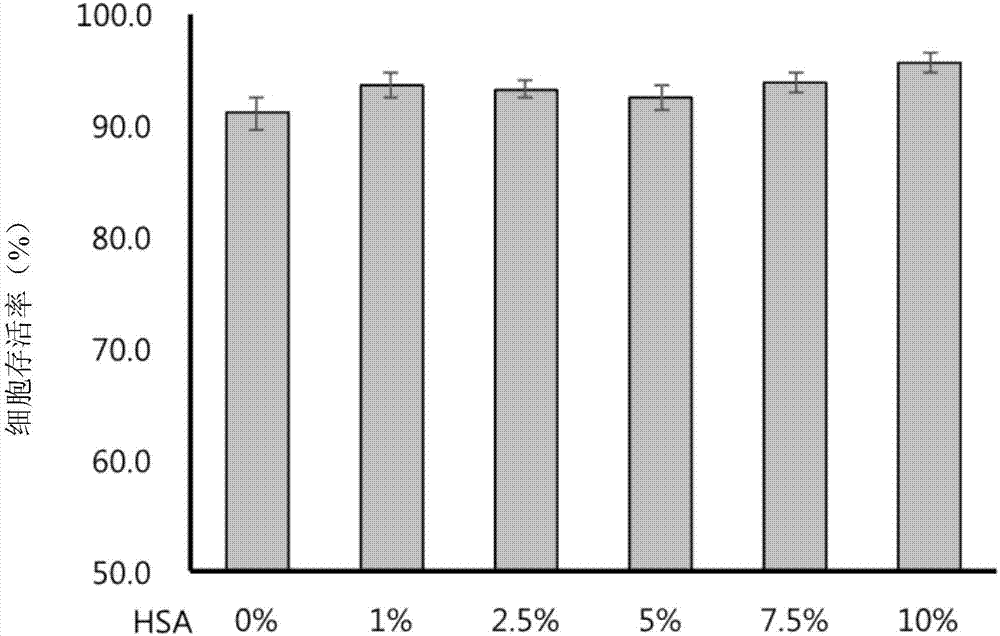
图1a显示hsa对间质干细胞的存活率无影响。图1b显示hsa对间质干细胞的细胞数目无影响。
图2显示hsa增强干细胞疗法对慢性阻塞性肺病的功效。与组别2比较:*:p<0.05;**:p<0.01;***:p<0.001。与组别4比较:#:p<0.05;##:p<0.01;###:p<0.001。
具体实施方式
在一方面,本发明提供一种用于治疗慢性阻塞性肺病(copd)的医药组合物。该医药组合物包括有效量的人类间质干细胞,人类血清白蛋白(hsa),以及医药上可接受的载体或稀释剂。
另一方面,本发明提供一种在有需要的个体中治疗慢性阻塞性肺病(copd)的方法。该方法包含步骤:对该个体施用医药组合物,其包含有效量的人类间质干细胞,人类血清白蛋白(hsa),以及医药上可接受的载体或稀释剂。
本文中所使用的术语“间质干细胞”包括自成人组织(例如,骨髓、脂肪细胞,以及牙周膜)分离的细胞,以及自胎儿组织、胎盘以及脐带血中分离的细胞。在本发明的一些实施例中,间质干细胞源自于选自于由羊膜、绒毛盘膜、绒毛膜及脐带所组成的群组的胎盘相关组织。
根据一个具体实施例,该医药上可接受的载体或稀释剂为生理盐水。
根据本发明,人类血清白蛋白的量可有效增强干细胞疗法对慢性阻塞性肺病的功效,且可由本领域技术人员通过常规实验而决定。
根据本发明的部分具体实施例,基于该医药上可接受的载体或稀释剂的体积,该人类血清白蛋白具有自0.5%(w/v)至25%(w/v)的范围的量,优选为自1%(w/v)至10%(w/v)的范围的量。
在本文中所使用的w/v意指g/ml。
根据本发明,该医药组合物可通过包含以下步骤的方法制备:将该人类间质干细胞与该医药上可接受的载体或稀释剂混合,该医药上可接受的载体或稀释剂补充有该人类血清白蛋白。
所述方法可进一步包含将人类间质干细胞悬浮培养于该医药上可接受的载体或稀释剂一段时间,以将人类间质干细胞的状态转化为在干细胞疗法中更有效地治疗慢性阻塞性肺病的状态。本领域技术人员,通过常规实验,可决定培养人类间质干细胞的适当时间,使得该医药组合物,相较于未在使用前通过所述方法“活化”的医药组合物,对于治疗慢性阻塞性肺病更为有效。换言之,本发明的用于治疗慢性阻塞性肺病的方法可进一步包含初步步骤:将该人类间质干细胞与该医药上可接受的载体或稀释剂混合,该医药上可接受的载体或稀释剂补充有该人类血清白蛋白,以及培养该医药组合物以将该人类间质干细胞的状态转化为在干细胞疗法中更有效地治疗慢性阻塞性肺病的状态。
然而,含有干细胞的医药组合物通常在一段相对长的时间内慢慢施用至有需要的个体,本发明的医药组合物也可在该人类间质干细胞与该医药上可接受的载体或稀释剂混合后不久使用,其中该医药上可接受的载体或稀释剂补充有该人类血清白蛋白。
本发明通过以下实施例进一步说明,其提供作为示例之用而不限制本发明。
实施例
实施例1:间质干细胞的制备
在获得捐赠者的书面知情同意书后收集全期胎盘。间质干细胞源自于羊膜(am)、绒毛膜盘(cd)、绒毛膜(cm)以及脐带(uc)。在37℃、饱和湿度以及5%co2下将源自于胎盘的间质干细胞培养、扩增及维持于含有fbs及碱性成纤维细胞生长因子(basicfgf)的α-mem中,且当细胞达到80%密度时进行继代培养。细胞在使用前储存于低温条件下。
实施例2:hsa对间质干细胞的存活率或细胞数目无影响
1x107个间质干细胞(如实施例1所述而制备)与补充有不同量(0、1%(w/v)、2.5%(w/v)、5%(w/v)、7.5%(w/v)、10%(w/v),基于生理盐水的体积)的人类血清白蛋白的生理盐水混合,培养4小时。细胞存活率及细胞数目通过细胞计数器(
实施例3:hsa增强干细胞疗法对慢性阻塞性肺病的功效
1x107个间质干细胞(如实施例1所述而制备)与补充有不同量(0、1%(w/v)、2.5%(w/v)、5%(w/v)、7.5%(w/v)、10%(w/v),基于生理盐水的体积)的hsa的生理盐水混合,培养4小时。正常人类肺纤维母细胞mrc-5经8%香烟烟雾萃取物(cse)处理24小时,接着与或不与间质干细胞共同培养48小时。间质干细胞通过使用具有0.4μm膜孔径的24孔插入盘与cse-损伤的mrc-5细胞共同培养。mrc-5细胞的细胞存活率通过cck-8检测法来分析,结果显示于图2。如可从图2中看到,hsa(1%(w/v))或间质干细胞单独对cse-损伤的mrc-5细胞在细胞存活率上展现中等的有益功效。然而,hsa及间质干细胞的组合对于恢复cse-损伤的mrc-5细胞显示了非预期性的协同作用。
本领域技术人员将理解可对上述具体实施例进行改变而不背离其广泛的发明概念。因此,应当理解的是,本发明不限于所公开的特定具体实施例,而是意在涵盖在权利要求书所界定的本发明的精神与范畴内的修改。
参考文献:
[1]spees,j.l.,r.h.lee,andc.a.gregory,mechanismsofmesenchymalstem/stromalcellfunction.stemcellresther,2016.7(1):p.125.
[2]jin,z.,etal.,biologicaleffectsandmechanismsofactionofmesenchymalstemcelltherapyinchronicobstructivepulmonarydisease.jintmedres,2015.43(3):p.303-10.
[3]mohammadian,m.,etal.,effectofbonemarrowderivedmesenchymalstemcellsonlungpathologyandinflammationinovalbumin-inducedasthmainmouse.iranianjournalofbasicmedicalsciences,2016.19(1):p.55-63.
[4]mobius,m.a.andb.thebaud,celltherapyforbronchopulmonarydysplasia:promisesandperils.paediatrrespirrev,2016.20:p.33-41.
[5]huh,j.w.,etal.,bonemarrowcellsrepaircigarettesmoke-inducedemphysemainrats.amjphysiollungcellmolphysiol,2011.301.
[6]hoffman,a.m.,etal.,lung-derivedmesenchymalstromalcellpost-transplantationsurvival,persistence,paracrineexpression,andrepairofelastase-injuredlung.stemcellsdev,2011.20.
[7]schweitzer,k.s.,etal.,adiposestemcelltreatmentinmiceattenuateslungandsystemicinjuryinducedbycigarettesmoking.amjrespircritcaremed,2011.183.
[8]weiss,d.j.,etal.,aplacebo-controlled,randomizedtrialofmesenchymalstemcellsincopd.chest,2013.143(6):p.1590-1598.
[9]ribeiro-paes,j.t.,etal.,unicentricstudyofcelltherapyinchronicobstructivepulmonarydisease/pulmonaryemphysema.internationaljournalofchronicobstructivepulmonarydisease,2011.6:p.63-71.
[10]ribeiro-paes,j.t.,etal.,aprotocolpropositionofcelltherapyforthetreatmentofchronicobstructivepulmonarydisease.revportpneumol,2014.20(2):p.84-91.
[11]stolk,j.,etal.,aphaseistudyforintravenousautologousmesenchymalstromalcelladministrationtopatientswithsevereemphysema.qjm,2016.109(5):p.331-6.
[12]cheng,s.-l.,c.-h.lin,andc.-l.yao,mesenchymalstemcelladministrationinpatientswithchronicobstructivepulmonarydisease:stateofthescience.stemcellsinternational,2017.2017:p.1-14.
[13]liu,x.,q.fang,andh.kim,preclinicalstudiesofmesenchymalstemcell(msc)administrationinchronicobstructivepulmonarydisease(copd):asystematicreviewandmeta-analysis.plosone,2016.11(6):p.e0157099.
[14]antunes,m.a.,etal.,mesenchymalstemcelltrialsforpulmonarydiseases.jcellbiochem,2014.115.
[15]antunes,m.a.,etal.,effectsofdifferentmesenchymalstromalcellsourcesanddeliveryroutesinexperimentalemphysema.respiratoryresearch,2014.15(1):p.118.
[16]francis,g.l.,albuminandmammaliancellculture:implicationsforbiotechnologyapplications.cytotechnology,2010.62(1):p.1-16.
[17]boldt,j.,useofalbumin:anupdate.brjanaesth,2010.104(3):p.276-84.
[18]raoufinia,r.,etal.,overviewofalbuminanditspurificationmethods.advpharmbull,2016.6(4):p.495-507.
- 还没有人留言评论。精彩留言会获得点赞!