一种提高生物材料抗钙化性能的处理方法及其生物材料与流程
本发明涉及一种提高生物材料抗钙化性能的处理方法及其生物材料,属于生物医学材料以及医疗器械
技术领域:
。
背景技术:
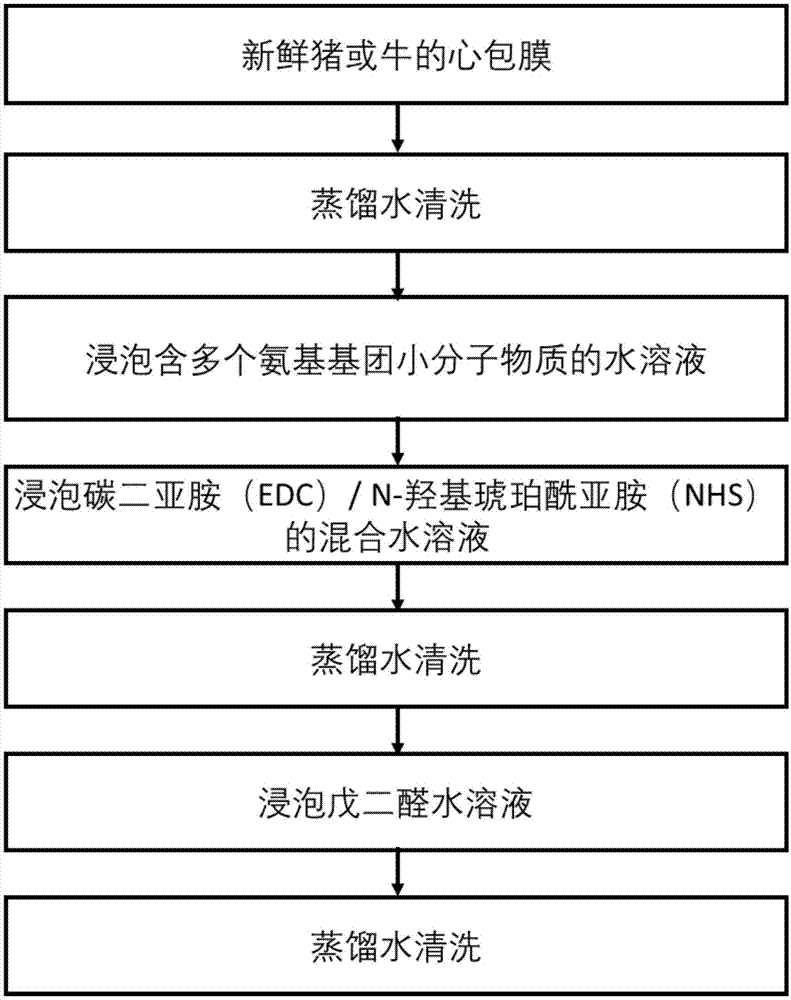
心脏瓣膜疾病是一种常见的瓣膜衰退疾病。在解剖学上表现为血液通路变窄或瓣膜关闭不全。心脏瓣膜疾病的治疗包括开胸瓣膜置换手术以及经皮心脏瓣膜置换手术。开胸手术对病人创伤大、风险高、恢复慢、需体外循环支持,很多患者无法接受。经皮心脏瓣膜置换手术因为对病人创伤小、风险低,成为未来瓣膜手术的主要趋势。生物心脏瓣膜是指一类用于替换人体病变心脏瓣膜的生物医学材料。生物心脏瓣膜一般由猪心包膜、牛心包膜等通过戊二醛交联制备而成。戊二醛交联处理具有操作简单,成本低以及胶原蛋白交联程度高的特点,是目前生物心脏瓣膜化学交联的行业首选。然而,戊二醛交联的生物心脏瓣膜存在容易降解以及钙化的问题,导致生物心脏瓣膜只有10年左右的有效使用年限。因此,通过优化生物心脏瓣膜的化学交联方法,提升生物心脏瓣膜的结构稳定性以及抗钙化性能,对于科学研究以及相关产业领域的发展具有重大意义。技术实现要素:本发明的目的是为了解决上述现有技术的不足而提供一种提高生物材料抗钙化性能的处理方法,能有效提升生物心脏瓣膜等生物材料的结构稳定性以及抗钙化性能,潜在地延长其使用寿命。为了实现上述目的,本发明所述的一种提高生物材料抗钙化性能的处理方法,具体包括以下步骤:s1、获取生物材料;s2、用蒸馏水浸泡清洗;s3、然后将步骤s2清洗后的生物材料浸泡于含多个氨基基团小分子物质且质量溶度为0.1-10%的水溶液当中;s4、然后然后将步骤s2处理后的生物材料在碳二亚胺/n-羟基琥珀酰亚胺的摩尔溶度为0.1-1m的混合溶液催化下通过心包膜上的羧基和多个氨基基团小分子物质发生化学交联反应;s5、然后再一次用蒸馏水浸泡清洗;s6、再用戊二醛为0.25-1%的水溶液浸泡;s7、最后用蒸馏水浸泡清洗。根据本发明提供的制备方法中,在步骤s1种:采集新鲜的生物材料,如猪或牛的心包组织,并于4摄氏度低温湿润状态下保存。根据本发明提供的制备方法中,在步骤s2中,采用柔和摩擦和流体压力在振荡条件之下用蒸馏水清洗心包组织,去除粘附的非心包和非胶原组织。所述清洗通过渗压休克实现对心包组织有效脱细胞,且优选地,清洗持续到没有可见的粘附的非心包或非胶原组织。优选地,是于4摄氏度100rpm转速振荡条件之下蒸馏水清洗2小时。根据本发明提供的制备方法中,在步骤s3中,将生物材料浸泡于含多个氨基基团小分子物质的质量溶度为0.1-10%的水溶液(精氨酸、赖氨酸、谷氨酸、天冬氨酰、聚乙烯亚胺当中的一种或多种的组合)当中2-24小时,于室温或者37摄氏度的振荡条件之下进行。这个步骤需要确保含多个氨基基团小分子物质达到接近饱和的物理渗透,从而尽可能多地引入外源性氨基基团。根据本发明提供的制备方法种,在步骤s4中,将生物材料浸泡于碳二亚胺(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide,edc)/n-羟基琥珀酰亚胺(n-hydroxysuccinimide,nhs)的摩尔溶度为0.1-1m的混合水溶液当中2-24小时,于室温或者37摄氏度的振荡条件之下进行204。这个步骤将实现前一步骤渗透室温氨基基团小分子物质与心包组织发生稳定的化学交联,从而实现除去胶原之外的其他细胞外基质,包括弹性蛋白的稳定交联。根据本发明提供的制备方法种,在步骤s5中,进行蒸馏水清洗。这个清洗步骤将清除没有反应的氨基基团小分子物质以及碳二亚胺/n-羟基琥珀酰亚胺混合水溶液。优选的是于4摄氏度100rpm转速振荡条件之下蒸馏水清洗2小时。根据本发明提供的制备方法中,在步骤s6中,将生物材料浸泡于戊二醛的质量溶度为0.25-1%的水溶液当中24-72小时,于室温或者37摄氏度的振荡条件之下进行。这个步骤将实现大部分胶原组织的稳定交联,提高整个心包组织的结构稳定性,降低以至于消除免疫原性。根据本发明提供的制备方法中,在步骤s7中,进行蒸馏水清洗。这个清洗步骤将清除没有反应的残留戊二醛。优选的是于4摄氏度100rpm转速振荡条件之下蒸馏水清洗2小时。根据本发明提供的方法,其中所述生物材料为动物组织或由天然高分子材料制成的人工生物材料。所述动物组织为心包膜、瓣膜、肠膜、脑膜、肺膜、血管、皮肤或韧带等。所述天然高分子材料为胶原、弹性蛋白、透明质酸和明胶等。本发明所述方法,不限于经皮介入生物心脏瓣膜,也适用于开胸瓣膜置换手术所用的生物材料。本发明还提供一种经上述方法处理的生物材料,以及含有该种生物材料的医疗器械,如介入生物瓣、人工血管、人工皮肤、人工心肌补片。本发明提供的一种提高生物材料抗钙化性能的处理方法及其生物材料,至少具有以下优势:本发明提供的方法能够提升生物材料结构的稳定性,特别是除去胶原蛋白之外其他细胞外基质包括弹性蛋白的结构稳定性。本发明提供的方法能够提升生物材料的力学强度,特别是单轴拉伸断裂应力。本发明提供的方法能够提升生物材料的抗钙化性能。附图说明为了进一步澄清一个或多个本发明的上述以及其他的优点和特性,通过参照附图中示出的特定实施方案,呈现一个或多个本发明更具体的描述。图1是制备的生物心脏瓣膜的具体流程图;图2是戊二醛交联原理以及含多个氨基基团小分子物质组合交联原理对比图;图3是采用本发明实施方案1所述方法制备的生物心脏瓣膜的抵抗胶原蛋白酶、弹性蛋白酶之后切片染色结果图;图4是采用本发明实施方案1所述方法制备的生物心脏瓣膜的单轴拉伸应力应变曲线;图5是采用本发明实施方案1所述方法制备的生物心脏瓣膜的体外挂钙量定性结果图。具体实施方式下面结合附图和实施例对本发明进一步说明。实施例1:本实施例提供的一种提高生物材料抗钙化性能的处理方法,在全部实施方案中,新鲜猪心包膜来自当地屠宰场。精氨酸、戊二醛、碳二亚胺、弹性蛋白酶、n-羟基琥珀酰亚胺、弹性蛋白酶、氯化钙、磷酸二氢钠来自于成都贝斯特试剂公司。胶原蛋白酶来自于sigma-aldrich公司。如图1所示,本实施例的提供的处理方法包括以下步骤:s1、获取生物材料;s2、用蒸馏水浸泡清洗;s3、然后将步骤s2清洗后的生物材料浸泡于含多个氨基基团小分子物质且质量溶度为0.1-10%的水溶液当中;s4、然后将步骤s3处理后的生物材料在碳二亚胺/n-羟基琥珀酰亚胺的摩尔溶度为0.1-1m的混合溶液催化下通过心包膜上的羧基和多个氨基基团小分子物质发生化学交联反应;s5、然后再一次用蒸馏水浸泡清洗;s6、再用戊二醛为0.25-1%的水溶液浸泡;s7、最后用蒸馏水浸泡清洗。根据本发明提供的制备方法中,在步骤s1种:采集新鲜的生物材料,如猪或牛的心包组织,并于4摄氏度低温湿润状态下保存。根据本发明提供的制备方法中,在步骤s2中,采用柔和摩擦和流体压力在振荡条件之下用蒸馏水清洗心包组织,去除粘附的非心包和非胶原组织。所述清洗通过渗压休克实现对心包组织有效脱细胞,且优选地,清洗持续到没有可见的粘附的非心包或非胶原组织。优选地,是于4摄氏度100rpm转速振荡条件之下蒸馏水清洗2小时。根据本实施例提供的制备方法中,在步骤s3中,将生物材料浸泡于含多个氨基基团小分子物质的质量溶度为0.1-10%的水溶液(精氨酸、赖氨酸、谷氨酸、天冬氨酰、聚乙烯亚胺当中的一种或多种的组合)当中2-24小时,于室温或者37摄氏度的振荡条件之下进行。这个步骤需要确保含多个氨基基团小分子物质达到接近饱和的物理渗透,从而尽可能多地引入外源性氨基基团。根据本实施例提供的制备方法种,在步骤s4中,将生物材料浸泡于碳二亚胺(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide,edc)/n-羟基琥珀酰亚胺(n-hydroxysuccinimide,nhs)的摩尔溶度为0.1-1m的混合水溶液当中2-24小时,于室温或者37摄氏度的振荡条件之下进行204。这个步骤将实现前一步骤渗透室温氨基基团小分子物质与心包组织发生稳定的化学交联,从而实现除去胶原之外的其他细胞外基质,包括弹性蛋白的稳定交联。根据本实施例提供的制备方法种,在步骤s5中,进行蒸馏水清洗。这个清洗步骤将清除没有反应的氨基基团小分子物质以及碳二亚胺/n-羟基琥珀酰亚胺混合水溶液。优选的是于4摄氏度100rpm转速振荡条件之下蒸馏水清洗2小时根据本实施例提供的制备方法中,在步骤s6中,将生物材料浸泡于戊二醛的质量溶度为0.25-1%的水溶液当中24-72小时,于室温或者37摄氏度的振荡条件之下进行。这个步骤将实现大部分胶原组织的稳定交联,提高整个心包组织的结构稳定性,降低以至于消除免疫原性。根据本实施例提供的制备方法中,在步骤s7中,进行蒸馏水清洗。这个清洗步骤将清除没有反应的残留戊二醛。优选的是于4摄氏度100rpm转速振荡条件之下蒸馏水清洗2小时。根据本实施例提供的方法,其中所述生物材料为动物组织或由天然高分子材料制成的人工生物材料。所述动物组织为心包膜、瓣膜、肠膜、脑膜、肺膜、血管、皮肤或韧带等。所述天然高分子材料为胶原、弹性蛋白、透明质酸和明胶等。本实施例所述方法,不限于经皮介入生物心脏瓣膜,也适用于开胸瓣膜置换手术所用的生物材料。本实施例还提供一种经上述方法处理的生物材料,以及含有该种生物材料的医疗器械,如介入生物瓣、人工血管、人工皮肤、人工心肌补片。为了更好的区分,在本实施中的现有方法的对照组采用0.25%戊二醛水溶液交联24h,然后进行蒸馏水清洗。而本实施例中的具体做实验时采用,具体采用以下比例:在步骤s3中用10%精氨酸水溶液浸泡2小时,在步骤s4中采用0.2m碳二亚胺(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide,edc)/0.1mn-羟基琥珀酰亚胺(n-hydroxysuccinimide,nhs)混合水溶液交联处理2小时,蒸馏水清洗,在步骤s6中,采用0.25%戊二醛水溶液交联24小时。蒸馏水清洗。之后将现有技术与本实施例1进行相关酶降解测试、单轴拉伸测试以及体外钙化测试。体外酶降解是指将心包膜浸泡于酶降解溶液(100u/ml的弹性蛋白酶;60u/ml的胶原蛋白酶)当中24小时,然后称量心包膜的重量损失。单轴拉伸测试是指将心包膜材料简称2*35mm的哑铃型试样,然后采用力学实验机进行测试。体外钙化测试指将心包膜浸泡于含有高钙磷元素的溶液(20mm氯化钙cacl2加20mm磷酸二氢钠nah2po4)当中72小时,然后检测心包膜材料的挂钙量。评估时,发现对照组样品抵抗胶原蛋白酶以及弹性蛋白酶的性能提升,如表1所示(n=3)。表1发现对照组样品单轴拉伸断裂应力提升。如表2所示(n=3)。表2样品组单轴拉伸断裂应力mpa对照组9.88±0.23精氨酸实验组17.46±0.18发现对照组样品抗钙化性能提升。如表3所示(n=3)。表3样品组挂钙量camg/l/mg组织干重对照组2.610±0.124精氨酸实验组1.624±0.193最终结论:如图2可以看出戊二醛只能交联胶原蛋白,但是无法交联弹性蛋白。因为弹性蛋白缺少活性氨基。通过含多个氨基基团小分子物质组合交联,可以提供额外交联连接点,通过碳二亚胺与弹性蛋白上的羧基交联。如图3可以看出采用本方法处理的材料比对照组在酶降解之后具有更好的结构稳定性。如图4可以看出采用本方法处理的材料比对照组具有更大的最大断裂拉伸应力。如图5可以看出采用本方法处理的材料比对照组具有更好的抗钙化性能。实施例2:本实施例提供的一种提高生物材料抗钙化性能的处理方法,在全部实施方案中,新鲜猪心包膜来自当地屠宰场。精氨酸、戊二醛、碳二亚胺、弹性蛋白酶、n-羟基琥珀酰亚胺、弹性蛋白酶、氯化钙、磷酸二氢钠来自于成都贝斯特试剂公司。胶原蛋白酶来自于sigma-aldrich公司。本实施例的提供的处理方法包括以下步骤:s1、获取生物材料;s2、用蒸馏水浸泡清洗;s3、然后将步骤s2清洗后的生物材料浸泡于含多个氨基基团小分子物质且质量溶度为3%的水溶液当中;s4、然后将步骤s3处理后的生物材料在碳二亚胺/n-羟基琥珀酰亚胺的摩尔溶度为0.5m的混合溶液催化下通过心包膜上的羧基和多个氨基基团小分子物质发生化学交联反应;s5、然后再一次用蒸馏水浸泡清洗;s6、再用戊二醛为0.5%的水溶液浸泡;s7、最后用蒸馏水浸泡清洗。实施例3:本实施例提供的一种提高生物材料抗钙化性能的处理方法,在全部实施方案中,新鲜猪心包膜来自当地屠宰场。精氨酸、戊二醛、碳二亚胺、弹性蛋白酶、n-羟基琥珀酰亚胺、弹性蛋白酶、氯化钙、磷酸二氢钠来自于成都贝斯特试剂公司。胶原蛋白酶来自于sigma-aldrich公司。本实施例的提供的处理方法包括以下步骤:s1、获取生物材料;s2、用蒸馏水浸泡清洗;s3、然后将步骤s2清洗后的生物材料浸泡于含多个氨基基团小分子物质且质量溶度为8%的水溶液当中;s4、然后将步骤s3处理后的生物材料在碳二亚胺/n-羟基琥珀酰亚胺的摩尔溶度为1m的混合溶液催化下通过心包膜上的羧基和多个氨基基团小分子物质发生化学交联反应;s5、然后再一次用蒸馏水浸泡清洗;s6、再用戊二醛为1%的水溶液浸泡;s7、最后用蒸馏水浸泡清洗。因此,本实施例提供的一种提高生物材料抗钙化性能的处理方法及其生物材料,至少具有以下优势:本实施例提供的方法能够提升生物材料结构的稳定性,特别是除去胶原蛋白之外其他细胞外基质包括弹性蛋白的结构稳定性。本实施例提供的方法能够提升生物材料的力学强度,特别是单轴拉伸断裂应力。本实施例提供的方法能够提升生物材料的抗钙化性能。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1