大黄酸在制备防治肝性脑病的药物中的用途的制作方法
本发明涉及医药技术领域,具体地说,是大黄酸在制备防治肝性脑病的药物中的用途。
背景技术:
肝性脑病(hepaticencephalopathy,he)是门脉高压和肝硬化最严重的并发症之一,发病率可达50%到70%,一年生存率低于50%,诊断后3年降至25%以下。据报道,慢性肝病患者的轻微肝性脑病(mhe)发生率高达50%,超过50%的轻微肝性脑病患者在30个月内就转换为显性肝性脑病。同时,肝性脑病也增加了患者住院时间,再入院率和死亡的风险,对家庭和社会都造成极大的经济负担。临床上治疗肝性脑病多以降氨和调节肠道菌群为主,目前暂无有效的防治措施,现代医学亦缺乏对肝性脑病的有效药效评价,临床急需探索防治肝性脑病有效的特色新药。
大黄酸,在植物界分布广泛,包括蓼科、豆科、芸香科及百合科等多种植物,是中药芦荟、大黄等的主要有效成分,安全性较好。大黄酸具有(1)抗肿瘤作用:通过改变细胞及细胞膜骨架的功能,阻断肿瘤细胞葡萄糖的摄入,葡萄糖的磷酸化作用受到抑制,并造成线粒体功能障碍,使肿瘤细胞的糖代谢和耗氧量受到影响。从而抑制肿瘤细胞增殖,加速其发展和死亡。(2)清除自由基:大黄酸对大鼠脑匀浆脂质过氧化反应引起的极弱化学发光现象均有淬灭作用,大黄能清除和抑制脂质过氧化。(3)抗病原微生物及抗炎作用:大黄酸具有显著的抗白色念球菌、毛癣菌及曲霉菌等抗菌活性,在抗病原微物生和抗炎方面均有极大的发展空间。(4)泻下:大黄酸可以有效抑制lovo细胞aqp2和aqp4的基因转录与翻译。还可通过抑制cec-aqp2和aqp4的表达,使结肠内水含量增加从而发挥泻下效应。
专利文献2011800664026公开了胃和结肠的配制剂,具体公开了包含非渗透性泻药的组合物,其中所述非渗透性泻药包括矿物油、芦荟、大黄酸和/或替加色罗等中的一种或多种;其中所述组合物、制剂或配制剂被制备、标记或配制用于改善或治疗肠道疾病,其中任选地,具有肠功能紊乱构成的肠道疾病或疾病状态包括炎症性肠病(ibd)、克罗恩病、肝性脑病等。然而在该专利中,大黄酸作为非渗透性泻药使用,该文没有公开大黄酸作为唯一活性成分防治肝性脑病。文献《大黄对肝性脑病多靶点的治疗作用》公开大黄治疗肝性脑病疗效显著,其中大黄中含有蒽酮和双蒽酮衍生物大黄酸、番泻叶等。然而在该文献中并没有公开大黄治疗肝性脑病的药效活性成分。文献《大黄提取物对急性肝衰大鼠肝性脑病的防治作用》公开大黄是治疗肝性脑病的有效药物,但与其疗效相关的药效物质尚未明确。现有技术中,应用大黄酸作为唯一药效成分防治肝性脑病还未见报道。
技术实现要素:
本发明所要解决的技术问题是针对缺乏药物用于肝性脑病治疗的现状,提供大黄酸在制备防治肝性脑病的药物中的用途。
本发明的第一个目的是针对现有技术中的不足,提供大黄酸或其药学上可接受的盐的制药新用途。
本发明的第二个目的是针对现有技术中的不足,提供一种防治肝性脑病的药物。
本发明的第三个目的是针对现有技术中的不足,提供一种防治肝性脑病的药物组合物。
为实现上述第一个目的,本发明采取的技术方案是:
大黄酸或其药学上可接受的盐在制备预防和/或治疗肝性脑病的药物中的应用。
作为一个优选例,所述的大黄酸或其药学上可接受的盐作为唯一活性成分,或者与其他预防或治疗肝性脑病的药物共同作为活性成分。
所述预防是本领域常规的预防,较佳地指当存在可能的导致肝性脑病诱发因素时,使用药后防止或降低肝性脑病产生的可能性。所述治疗是本领域常规的治疗,较佳地指阻止肝性脑病进一步发展,或者保护肝功能、减少肝坏死、改善肝损伤和脑损伤。
所述其他预防或治疗肝性脑病的药物可以是现有技术中已知的任何对防治肝性脑病有积极作用的药物,较佳地为盐酸精氨酸、l-鸟氨酸-l-门冬氨酸、纳洛酮、l-肉毒碱中的一种或多种。
为实现上述第二个目的,本发明采取的技术方案是:
一种防治肝性脑病的药物,防治肝性脑病的药效成分为大黄酸或其药学上可接受的盐。
较佳地,所述的大黄酸或其药学上可接受的盐作为唯一活性成分,或者与其他预防或治疗肝性脑病的药物共同作为活性成分。
为实现上述第三个目的,本发明采取的技术方案是:
一种防治肝性脑病的药物组合物,防治肝性脑病组分包括大黄酸或其药学上可接受的盐。
较佳地,所述的大黄酸或其药学上可接受的盐作为唯一活性成分,或者与其他预防或治疗肝性脑病的药物共同作为活性成分。
本发明还提供一种快速防治肝性脑病的药物,所述防治肝性脑病的药效成分为大黄酸或其药学上可接受的盐。
较佳地,在上述药物或药物组合物中,还包括与大黄酸同时施用后对防治肝性脑病有积极作用的药物成分和/或使大黄酸稳定性提高的药学上可接受的成分。
较佳地,在上述药物或药物组合物中,还包括一种或多种制药学上可接受的辅助成分。所述制药学上可接受的辅助成分为赋形剂、填充剂或稀释剂。
更佳地,所述药物或药物组合物包括0.01~99.99%大黄酸或其药学上可接受的盐,以及0.01~99.99%的辅助成分,所述百分比为占所述药物或药物组合物的质量百分比。
本发明的药物或药物组合物为本领域常规的各种剂型,较佳的为固体、半固体或液体的形式,可以为水溶液、非水溶液或混悬液,更佳的为粉剂、颗粒剂、片剂、胶囊剂、丸剂、溶液、悬浮液或注射液等。所述药物或药物组合物的给药途径较佳的为注射给药或口服给药。所述注射给药较佳的包括静脉注射、肌肉注射、腹腔注射、皮内注射或皮下注射等途径。
在本发明中,所述大黄酸或其药学上可接受的盐可通过商业购买所得。其中所述其药学上可接受的盐为本领域常规的盐,较佳地为胆碱盐,葡萄糖胺盐或氨基丁三醇盐。
基于发明人的偶然发现,本发明提供一种以大黄酸或大黄酸的盐作为药效成分的防治肝性脑病药物,这种药物具有防治肝性脑病效果显著、用药量少、起效快等优点。
本发明提出的大黄酸在制备防治肝性脑病药物中的应用属于首次公开。经硫代乙酰胺(taa)和四氯化碳(ccl4)诱导的肝性脑病模型实验重复验证,结果证实,大黄酸能降低血氨,可减轻肝脏和脑组织炎症,具有显著保护肝功能,减少肝坏死,改善肝损伤和脑损伤。因此,大黄酸或大黄酸的盐能用于制备防治肝性脑病药物,具有良好的开发用途前景。
附图说明
附图1.1为taa诱导的急性肝衰竭后肝性脑病大鼠血氨结果。
附图1.2为taa诱导的急性肝衰竭后肝性脑病大鼠肝病理结果。
附图1.3为taa诱导的急性肝衰竭后肝性脑病大鼠脑病理结果。
附图1.4为taa诱导的急性肝衰竭后肝性脑病大鼠肝功能结果。
附图1.5为taa诱导的急性肝衰竭后肝性脑病大鼠脑相关mrna的表达。
附图2.1为ccl4诱导的肝硬化后肝性脑病大鼠血氨结果。
附图2.2为ccl4诱导的肝硬化后肝性脑病大鼠肝组织he染色结果。
附图2.3为ccl4诱导的肝硬化后肝性脑病大鼠肝组织天狼星红染色结果。
附图2.4为ccl4诱导的肝硬化后肝性脑病大鼠肝功能结果。
具体实施方式
下面结合具体实施方式,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明记载的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1taa诱导的大鼠肝性脑病模型证实大黄酸可以显著防治肝性脑病的进展和形成。
1材料与方法
1.1实验动物
wistar雄性大鼠30只,spf级,体质量(200±20)g,上海中医药大学实验动物中心提供。动物许可证号:syxk(沪2014-008)。动物中心饲养、造模和观察,自由饮食饮水。
1.2药物与试剂
taa(中国医药集团上海化学试剂公司,产品批号:20160930)、大黄酸(由上海融禾医药科技发展有限公司制作,产品批号:140930),血氨试剂盒、血清tbil、alt、ast、总胆汁酸(tba)、总蛋白(tp)、alb检测试剂盒和he剂盒均购自南京建成生物工程研究所,tnf-α和il-1引物由上海冠泰生物科技有限公司(biotnt)设计合成。
1.3模型制备
参照terblanche等[terblanchej,hickmanr.animalmodelsoffulminanthepaticfailure[j].digestivediseases&sciences,1991,36(6):770-4.]提出的方法造模,模型组大鼠以350mg/kg的剂量腹腔注射3.5%taa溶液(以0.9%氯化钠溶液稀释),共3天。正常对照组大鼠腹腔注射等量的0.9%氯化钠溶液。
1.4分组及给药
按照体质量分层随机的方法将大鼠分为正常对照组(n组)、模型组(m组)、大黄酸组(h组),每组各10只。适应性饲养1周后,h组以10ml/kg体质量的剂量(30mg/kg)灌胃,1次/d,共7天;n组与m组以等体积生理盐水灌胃。灌胃第4天,m组和h组均以taa造模,24和48h后予以重复。第7天造模结束后,禁食12h,于第8天取材。
1.5统计学方法
应用spss22.0软件对数据进行统计分析。计量资料均用均数±标准差
2结果
2.1一般情况
与正常组相比,模型组血氨显著升高(p<0.01);大黄酸组血氨水平显著降低(p<0.01),(图1.1)。
2.2肝组织病理学观察
he染色显示正常对照组肝细胞结构清晰,肝板呈索条状,汇管区无扩大无坏死,未见明显病理组织学改变;与正常对照组比较,模型组大鼠肝组织出现明显的肝细胞排列紊乱,肝小叶结构不清,可见不同程度的坏死、肿胀、变形、点片状、小灶或大灶碎屑状坏死;与模型组比较,大黄酸组大鼠肝组织坏死、肿胀、变性、炎症细胞浸润均有不同程度减轻(图1.2)。
2.3脑组织病理学观察
正常对照组脑细胞结构清晰,未见异常;模型组可见坏死细胞,形态学表现为核形态不规则、染色质散播于胞质、细胞膜不完整以及胞质减少,染色质浓缩伴核固缩。大黄酸组脑组织病理学改善明显(图1.3)。
2.4肝功能检测
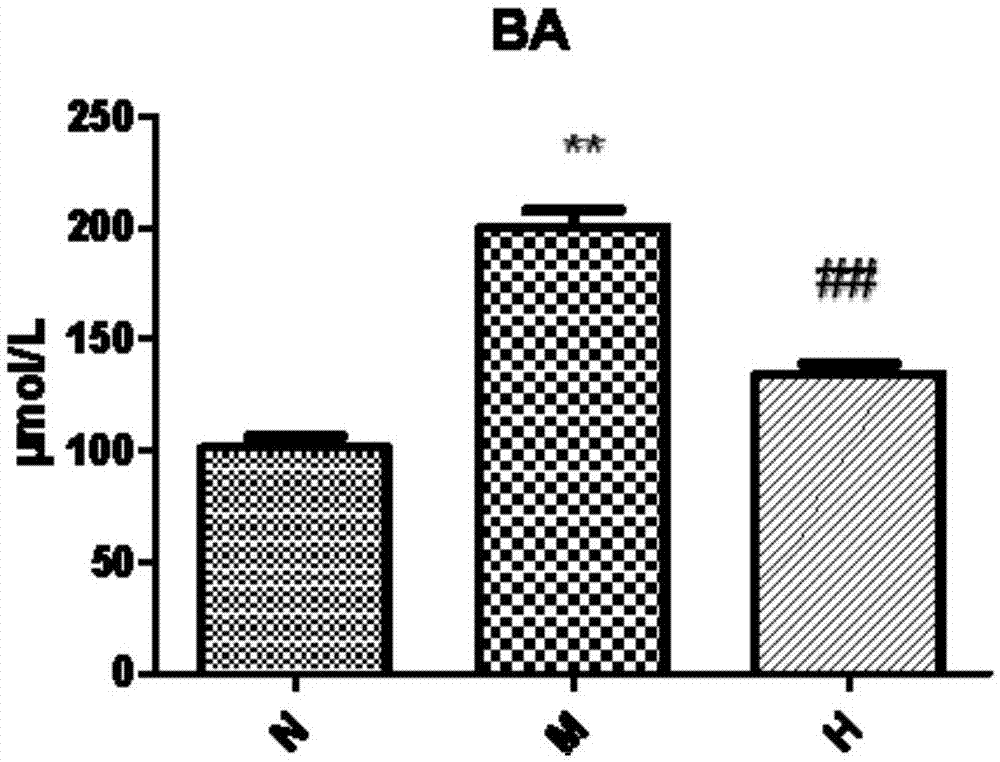
与正常对照组相比,模型组的tbil、alt、ast、tba水平均明显升高(p值均<0.01)、tp和alb水平均明显降低(p值均<0.01)。与m组相比,大黄酸组的tbil、alt、ast和tba水平均显著降低(p值均<0.01)、alb(p值<0.01)和tp水平明显升高(p值<0.05)(图1.4)。
2.5脑组织相关mrna表达
与正常对照组相比,模型组脑组织的tnf-a和il-1显著上升(p<0.01);与模型组相比,大黄酸组tnf-α和il-1显著降低,p<0.01)(图1.5)。
实施例2ccl4诱导的大鼠肝性脑病模型证实大黄酸可以显著防治肝性脑病的进展和形成。
1材料与方法
1.1动物
wistar雄性大鼠30只,spf级,体质量(200±20)g,上海中医药大学实验动物中心提供。动物许可证号:syxk(沪2014-008)。动物中心饲养、造模和观察,自由饮食饮水。
1.2药物与试剂
ccl4(中国医药集团上海化学试剂公司,产品批号:20170713)、大黄酸(由上海融禾医药科技发展有限公司制作,产品批号:140930),血氨试剂盒、血清tbil、alt、ast、总胆汁酸(tba)、总蛋白(tp)、alb检测试剂盒和he、天狼星红染色试剂盒均购自南京建成生物工程研究所。
1.3模型制备和分组给药
模型组大鼠以50%ccl4腹腔注射9w制造肝硬化模型,9w末,以taa(250mg/kg)腹腔注射诱导肝性脑病,24h后重复一次。自实验第6w起开始灌胃,h组以10ml/kg体质量的剂量(30mg/kg)灌胃,1次/d;n组与m组以等体积生理盐水灌胃。造模结束后,禁食12h,取材待检。
1.4统计学方法
应用spss22.0软件对数据进行统计分析。计量资料均用均数±标准差
2结果
2.1一般情况
与正常组相比,模型组血氨显著升高(p<0.01);大黄酸组血氨水平显著降低(p<0.01),(图2.1)。
2.2肝组织he染色观察
he染色显示正常对照组肝细胞结构清晰,肝板呈索条状,汇管区无扩大无坏死,未见明显病理组织学改变;与正常对照组比较,模型组大鼠肝组织出现明显的肝细胞排列紊乱,肝小叶结构不清,可见不同程度的坏死、肿胀、变形、点片状、小灶或大灶碎屑状坏死;与模型组比较,大黄酸组大鼠肝组织坏死、肿胀、变性、炎症细胞浸润均有不同程度减轻(图2.2)。
2.3肝组织天狼星红染色观察
天狼星红染色显示模型组大鼠胶原沉积明显,肝小叶间形成较厚汇管区和中央静脉间的纤维间隔,可见完整的假小叶;大黄酸组与模型组相比胶原纤维增生程度分期显著降低(图2.3)。
2.4肝功能检测
与正常对照组相比,模型组的tbil、alt、ast、tba水平均明显升高(p值均<0.01)、tp和alb水平均明显降低(p值均<0.01)。与m组相比,大黄酸组的tbil、alt、ast和tba水平均显著降低(p值均<0.05)、alb和tp水平明显升高(p值均<0.01)(图2.4)。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!