一种血管内激光斑块消融系统及方法与流程
本发明属于血管消融技术领域,具体涉及一种血管内激光斑块消融系统及方法。
背景技术:
cto(chronictotalocclusion,慢性完全闭塞病变)是指是指闭塞血管段前向血流timi0级,同时其闭塞时间大于或等于三个月的病变,它约占全部冠脉造影检出病变的1/5,尽管不断涌现新器械和新技术,cto手术成功率有了很大的提高,但cto病变被认为是目前pci(percutaneouscoronaryintervention,经皮冠状动脉介入治疗)治疗领域最大的难题。
目前,cto病变一般使用导丝、旋磨等方法对完全闭塞血管进行开通,但其存在手术成功率低,普遍存在并发症、再狭窄和再闭塞发生率较高的风险。
cto-pci最常见的手术失败原因是导丝无法穿过闭塞处,其次是球囊无法通过病变,对cto实施机械旋磨切割时,也存在介入治疗器械由于病变处纤维钙化程度较重而导致介入机械嵌顿在病变中的危险。而激光斑块消融因为避免了血管内栓塞,所以相对于旋磨,更不易引起无复流及围手术期心梗等并发症,但是因为激光消融需要使用大功率激光器,所以当光脉冲能量超过端面损伤的阈值时,极易发生光纤端面损坏的情况,导致导管的出光效率降低,从而降低消融效率。除此之外,即使在光脉冲能量低于端面损伤阈值时,光纤纵向仍然可能发生熔融现象,而导致这一现象的主要原因则是由于激光的高空间相干性,从而直接阻断导管中光的传输。
技术实现要素:
为了解决现有技术中存在的上述问题,本发明提供了一种血管内激光斑块消融系统及方法,本发明要解决的技术问题通过以下技术方案实现:
本发明实施例提供了一种血管内激光斑块消融系统,包括:
控制模块,用于发送第一激光能量;
耦合模块,用于接收所述第一激光能量并进行处理,得到第二激光能量;
消融模块,用于接收所述第二激光能量,并根据所述第二激光能量对病灶组织进行消融处理。
在本发明的一个实施例中,所述控制模块包括:
人机交互单元,用于获取消融能量参数;
反馈控制器,用于根据所述消融能量参数确定第一激光能量参数;
所述激光器,用于根据所述第一激光能量参数发送所述第一激光能量。
在本发明的一个实施例中,所述激光器的波长范围为300~1800nm。
在本发明的一个实施例中,所述激光器的光脉冲宽度为5~15ns。
在本发明的一个实施例中,所述耦合模块包括:
脉冲复制单元,用于对所述第一激光能量进行处理,得到第三激光能量;
空间相干性调节单元,用于对所述第三激光能量进行处理,得到所述第二激光能量。
在本发明的一个实施例中,所述脉冲复制单元包括:
啁啾镜,分别与所述激光器、所述空间相干性调节单元连接,用于对所述第一激光能量进行处理,得到所述第三激光能量。
在本发明的一个实施例中,所述空间相干性调节单元包括:
散射片,用于接收所述第三激光能量并转换成第四激光能量;
第一透镜,用于接收所述第四激光能量并转换成第五激光能量;
多模光纤,用于接收所述第五激光能量并转换成第六激光能量;
第二透镜,用于接收所述第六激光能量并转换成第七激光能量;
第三透镜,用于将所述第七激光能量转换成第二激光能量,并发送给所述消融模块。
在本发明的一个实施例中,所述消融模块包括:
导丝,用于引导导管到达所述病灶组织;
所述导管,用于接收所述第二激光能量,并对所述病灶组织进行消融处理。
在本发明的一个实施例中,所述光纤束中光纤的数量为30~90根。
本发明的另一个实施例提供了一种血管内激光斑块消融方法,包括以下步骤:
获取第一激光能量;
对所述第一激光能量进行处理,得到第二激光能量;
根据所述第二激光能量对病灶组织进行消融处理。
与现有技术相比,本发明的有益效果:
1.本发明提供的血管内激光斑块消融系统,通过脉冲复制单元,降低了激光器发射的激光能量的峰值能量,从而避免损坏光纤端面,提高了导管的出光效率,进一步提高了消融效率;
2.本发明提供的血管内激光斑块消融系统,通过空间相干性调节单元,降低了激光能量的空间相干性,降低了光束质量,从而避免了高空间相干性带来的光纤熔融,使激光的传输更加畅通,进一步提高了消融效率。
3.本发明的血管内激光斑块消融系统适用于多种血管类型,只需要根据不同的血管类型选择不同直径的导管,方便了使用。
附图说明
图1为本发明实施例提供的一种血管内激光斑块消融系统的结构示意图;
图2为本发明实施例提供的另一种血管内激光斑块消融系统的结构示意图;
图3为本发明实施例提供的一种血管内激光斑块消融系统的脉冲复制单元的结构示意图;
图4为本发明实施例提供的一种血管内激光斑块消融系统的脉冲复制模块的脉冲示意图;
图5为本发明实施例提供的另一种血管内激光斑块消融系统的脉冲复制模块的脉冲示意图;
图6为本发明实施例提供的一种血管内激光斑块消融系统的空间相干性调节单元的结构示意图;
图7为本发明实施例提供的一种血管内激光斑块消融系统的消融模块的结构示意图;
图8为图7的右视图;
图9为本发明实施例提供的一种血管内激光斑块消融方法的流程示意图。
具体实施方式
下面结合具体实施例对本发明做进一步详细的描述,但本发明的实施方式不限于此。
实施例一
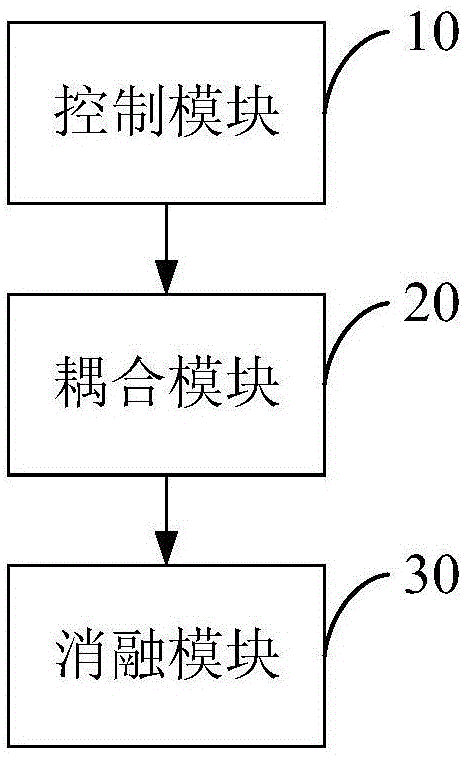
请同时参见图1和图2,图1为本发明实施例提供的一种血管内激光斑块消融系统的结构示意图;图2为本发明实施例提供的另一种血管内激光斑块消融系统的结构示意图;一种血管内激光斑块消融系统,包括:控制模块10、耦合模块20,消融模块30。
控制模块10,用于发送第一激光能量。
耦合模块20,用于接收第一激光能量并进行处理,得到第二激光能量;
消融模块30,用于接收第二激光能量,并根据第二激光能量对病灶组织进行消融处理。
进一步地,控制模块10包括:人机交互单元101、反馈控制器102以及激光器103。
进一步地,人机交互单元101用于获取消融能量参数。
消融能量也就是消除病灶组织所需要的第二激光能量,人机交互单元也就是操作面板,在操作面板上选择需要的消融能量参数。
需要说明的是,人机交互单元101可以为任意一种满足发明需要的操作面板,本发明实施例在此不作限定。
进一步地,反馈控制器102用于根据消融能量参数确定第一激光能量参数,也就是调整激光器103输出的第一激光能量,也就是说,反馈控制器102根据病灶部位需要的能量选择激光器103输出的第一激光能量。
进一步地,反馈控制器102的工作原理为:接收人机交互单元101发送的信号,然后判断该信号,再选择激光器103输出的第一激光能量,最后触发激光器103。
进一步,激光器103用于发送第一激光能量并传输至耦合模块20,激光器103主要用于根据反馈控制器102输出第一激光能量,并将第一激光能量传输给耦合模块20进行下一步处理。
进一步地,激光器103的波长范围为300~1800nm,在该范围内的激光器103可以满足病灶组织需要的第一激光能量。
需要说明的是,第一激光能量为激光器103发出的初始能量。
进一步地,耦合模块20包括:脉冲复制单元201、空间相干性调节单元202。
由于激光消融需要使用大功率的激光器,所以当光脉冲能量超过端面损伤的阈值时,极易发生光纤端面损坏的情况,导致导管的出光效率降低,从而降低消融效率,解决该问题的主要方法是将一个光脉冲分成两个甚至多个光脉冲、或者直接降低峰值功率从而提高消融效率。本发明针对这一问题,设计了脉冲复制单元201,脉冲复制单元201用于对第一激光能量进行处理,得到第三激光能量。
请参见图3,图3为本发明实施例提供的一种血管内激光斑块消融系统的脉冲复制单元的结构示意图。在一个具体实施例中,脉冲复制单元201包括:半波片2011、第一偏振分光镜2012、第二偏振分光镜2013、第一反射镜2014以及第二反射镜2015。
半波片2011用于将激光器发射的第一激光能量的光脉冲分成相位差为θ的两个光脉冲,将两个光脉冲分别定义为a光和b光,第一偏振分光镜2012用于将半波片2011产生的a光和b光分开,其中,a光沿直线射入第二偏振分光镜2013,b光经过第一反射镜2014和第二反射镜2015后,射入第二偏振分光镜2013,经过第二偏振分光镜2013的a光和b会重新合并,从而在脉冲复制单元201中输出两个光脉冲,其中b光所经历的折反光路的光程可以通过调节第一反射镜2014和第二反射镜2015的位置进行调节,从而实现了两个脉冲时间间隔δt的调节,δt的大小由激光器103的光脉冲宽度决定,δt太大的话达不到消融效果,太小会导致光纤端面烧焦,达不到脉冲复制目的,优选地,激光器103的光脉冲宽度为5~15ns,也就是说,δt为5~15ns。
请参见图4,图4为本发明实施例提供的一种血管内激光斑块消融系统的脉冲复制模块的脉冲示意图,从图中可以看出,该脉冲复制模块201将一个能量为e的光脉冲输出为两个能量为e/2的光脉冲,且两个光脉冲的输出时间间隔为δt。
请参见图5,图5为本发明实施例提供的另一种血管内激光斑块消融系统的脉冲复制模块的脉冲示意图。在一个具体实施例中,脉冲复制单元201包括啁啾镜,啁啾镜分别与控制模块10中的激光器103、空间相干性调节单元202连接,用于接收激光器103发出的第一激光能量并进行处理,得到第三激光能量。如图6所示,啁啾镜能把能量为e的光脉冲拉宽,从而直接起到降低峰值功率的作用。
需要说明的是,第三激光能量指的是第一激光能量经过脉冲复制单元201,光脉冲经过调整之后的激光能量。
此外,当光脉冲能量低于端面损伤的阈值时,光纤纵向仍然可能发生熔融现象,导致这一现象的主要原因是由于激光的高空间相干性,当横模之间的干涉出现干涉相长时,会导致多模光纤内局部能量骤增,并超过玻璃材料的损伤阈值,从而将光纤熔融,从而造成光纤损伤,损伤带来的最直接的效果就是阻断光的传输,即导管不出光,无法进行消融。本发明针对这一问题,设计了空间相干性调节单元202,空间相干性调节单元202用于对第三激光能量进行处理,得到第二激光能量。
进一步地,空间相干性调节单元202包括:散射片2021、第一透镜2022、多模光纤2023、第二透镜2024、第三透镜2025。
进一步地,散射片2021用于接收第三激光能量并转换成第四激光能量。
当经过脉冲复制单元201之后的第三激光能量的光束为高斯光束,形成的光斑在各个位置的能量不同,会导致病灶组织有的地方被消融掉,有的地方未被消融。散射片2021的作用是为了将高斯光束转变为平顶光束,从而光斑在各个位置的能量都相同。
需要说明的是,第四激光能量为转换成平顶光束以后的第三激光能量。
进一步地,第一透镜2022用于接收第四激光能量并转换成第五激光能量。
需要说明的是,第一透镜2022为凸透镜。
第一透镜2022的作用是为了把经过散射片2021转换后的平顶光束汇聚成直径为1.25~2.00mm的光束。
需要说明的是,第五激光能量为光束直径为1.25~2.00mm的第三激光能量。
进一步地,多模光纤2023用于接收第五激光能量并转换成第六激光能量。
进一步地,多模光纤2023为大芯径多模光纤,大芯径多模光纤与普通的光纤相比,直径更大(一般大于125μm),同样大小的能量照射到大芯径光纤上时,单位面积上承受的能量相对于普通光纤更小,所以光纤更不易被烧坏。
因此,通过多模光纤2023的第五激光能量,光束相干性进一步降低,即光束质量进一步降低。
需要说明的是,第六激光能量通过多模光纤2023后,光束质量进一步降低的第三激光能量。
进一步地,第二透镜2024用于接收第六激光能量并转换成第七激光能量。
需要说明的是,第二透镜2024为非球面透镜。
第二透镜2024的作用是把通过多模光纤2023后的光束变为平行光束。
需要说明的是,第七激光能量为经过多模光纤2023后转换为平行光束的第三激光能量。
进一步地,第三透镜2025用于将第七激光能量转换成第二激光能量,并发送给消融模块30。
需要说明的是,第三透镜2025为凸透镜。
第三透镜2025将经过第二透镜2024的平行光束进行聚焦,从而使经过第三透镜2025的出射光可以耦合进入消融模块30。
第二激光能量指的是经过耦合模块20处理之后得到的激光能量。
由于从激光器103直接输出的光束发散角较小,或者说平行性很好,因此光束质量很高,但在激光消融系统中,高质量的光束会带来高的空间相干性,从而导致光纤熔融,因此需要将高质量的光束变为低质量的光束,而空间相干性调节单元202中的散射片2021以及多模光纤2023,其本质上的作用就是降低光束的质量,从而降低空间相干性。
进一步地,请同时参见图7和图8,图7为本发明实施例提供的一种血管内激光斑块消融系统的消融模块的结构示意图;图8为图7的右视图。消融模块30包括:导丝301、导管302。
导丝301用于引导导管302达到病灶组织。
进一步地,导管302包括外管3021、显影环3022、光纤束3023、远端外管以及近端外管。
外管3021用来保护导管302的内部结构。
显影环3022位于远端外管的前端,用来在x光下确定导管302在血管中的位置,显影环3022主要用于确定导管302的位置,以防止导管插错血管。
光纤束3023由若干光纤3024组成,若干光纤3024穿过导管302,用于传递激光器103发射的激光能量,从而直接到达病灶组织。
在一个具体实施例中,光纤3024的数量为30~90根,具体的光纤根数随着导管302的直径具体确定,本发明实施例在此不作限定。
导管302远离耦合模块20的一端的端面为导管尖端3025,导管尖端3025的上设置有导丝腔3026,导丝301从导丝腔3026穿出,从而引导导管302到达病灶组织。
为了防止远端外管戳破血管,因此远端外管选用的材料较软;而近端外管用于推送导管302,因此选用的材料更硬。
进一步地,远端外管和近端外管的材料均可以为peek(聚醚醚酮)或者pebax(尼龙弹性体),由于peek或者pebax材料均有不同的型号,可以根据具体需要选择不同型号的peek或者pebax材料作为远端外管材料或者近端外管材料。
需要说明的是,远端外管或者近端外管的材料也可以为其他适用于本方案的材料,本发明实施例在此不作具体限定。
需要说明的是,远端外管指靠近导管尖端3025的一端,而近端外管指靠近耦合模块20的一端。
进一步地,远端外管的长度为20~50cm,近端外管的长度为150~200cm。
在进行消融处理时,通过推送近端外管,将导管302推送至病灶组织所在的血管,直到导管尖端3025将直接接触血管内病灶组织,并通过光纤束3023将激光器103发射的能量传递给病灶组织,从而达到对病灶位置进行消融的目的。
请参见图9,图9为本发明实施例提供的一种血管内激光斑块消融方法的流程示意图,本发明的另一个实施例提供了一种血管内激光斑块消融方法,该消融方法也为消融系统的使用方法,具体包括以下步骤:
步骤(a):获取第一激光能量。
在导丝和x光的引导下,将导管置入待消融的病灶组织,用户根据病灶的种类,通过人机交换单元101选择不同大小的消融能量,反馈控制器102将根据用户的选择调整激光器103的输出能量,也就是确定第一激光能量。
步骤(b):对第一激光能量进行处理,得到第二激光能量。
激光器103输出的第一激光能量将通过耦合模块20中的脉冲复制单元201和空间相干性调节单元202进行处理,降低了第一激光能量的峰值功率以及空间相干性,从而得到第二激光能量。
步骤(c):根据第二激光能量对病灶组织进行消融处理。
消融模块30通过光纤束3023接收耦合模块20传输的第二激光能量,并传输至导管尖端,从而对病灶组织进行消融处理。
在消融过程中,耦合模块30中的探测器将对系统进行不间断的能量监测,以判断是否正常工作,若系统工作状态出现异常,将通过耦合模块中的报警装置进行报警。
与现有的血管内激光斑块消融系统相比,本发明设计了脉冲复制单元,通过不同的光学器件的组合,降低了激光器发射的激光能量的峰值能量,避免了因光纤端面损坏带来的导管出光效率和消融效率降低问题;
此外,本发明还设计了空间相干性调节单元,通过不同的光学器件的组合,降低了激光能量的空间相干性,降低了光束质量,从而避免了高空间相干性带来的光纤熔融,进一步避免了术中因光纤熔融所带来的导管无法进行消融的现象;
此外,本发明的血管内激光斑块消融系统适用于多种血管类型,只需要根据不同的血管类型选择不同直径的导管,方便了使用。
以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!