治疗痴呆的装置、操作该装置的方法和程序与流程
本发明涉及一种用于治疗痴呆的装置、一种操作该装置的方法以及一种程序。
背景技术:
目前,据称日本的痴呆患者人数约为260万之多。随着老龄人口的迅速增长,痴呆患者的数量也将在未来增加,到2020年将超过300万。此外,据估计,全世界痴呆患者的数量为3500万,据推测,到2030年将达到6500万,到2050年将达到11500万。此外,作为痴呆的疾病类型,脑血管性痴呆和阿尔茨海默氏病占所有痴呆的大部分,并且还有许多患者同时表现出这两种痴呆的症状。
作为针对脑血管性痴呆的措施,已经进行了针对高血压、脂质代谢异常或糖尿病的药物治疗,并且例如减轻了运动不足、吸烟、暴饮暴食或压力。但是,尚未开发出用于治疗脑血管性痴呆的药物。另外,对于阿尔茨海默氏病的痴呆,作用机理是乙酰胆碱途径的活化和谷氨酸抑制的药剂等是可商购的,但是其治疗效果并不总是足够的。因此,需要开发治疗痴呆的有效手段。
本发明的发明人先前已经证实了通过低强度脉冲超声(lipus)在猪缺血性心脏中的血管生成和左心室功能的改善(非专利文献1)。近年来,lipus已经在例如整形外科、肠胃病学、神经病学和牙科领域引起了广泛的关注,并且已经在临床上进行了骨折治疗。但是,没有报告具体证实未聚焦的超声能量照射对痴呆的治疗效果。
现有技术文献
非专利文献
非专利文献1:hanawak.shimokawah,etal.plosone.2014;9:e104863
技术实现要素:
技术问题
本发明的目的是提供一种与现有技术的药物治疗等不同的新颖的痴呆治疗方法。
解决方案
在上述情况下,本发明的发明人发现了,痴呆可以由通过将从超声探头照射后传播的未聚焦的超声能量(而不是从超声探头照射后被聚焦的聚焦超声能量)传播到大脑的广泛范围而引起的血管生成等来治疗。本发明是基于这样的新颖的发现。
因此,本发明提供根据以下各项目的超声生成器、操作治疗痴呆的装置的方法和程序:
项目1、一种治疗痴呆的装置,包括:
多个超声探头;
超声换能器,其布置在每个所述超声探头中,并配置为将未聚焦的超声能量传播到大脑;和
超声生成器,其连接到每个所述超声探头。
项目2、根据项目1的装置,其中,未聚焦的超声能量以倒锥形形状扩散,该倒锥形形状的直径朝向照射方向逐渐增大。
项目3、根据项目2的装置,其特征在于,直径增大的所述倒锥形形状的未聚焦的超声能量的倾斜面的展开角度为50°~100°。
项目4、根据项目1至3中的任一项的装置,其中,所述超声生成器被配置为控制所述超声换能器,以在所述多个超声探头之间依次照射所述未聚焦的超声能量。
项目5、根据项目4的装置,其中,以0.15/fms或更大的间隔执行来自所述多个超声探头的未聚焦的超声能量照射,其中,f表示待发送的脉冲的频率(mhz)。
项目6、根据项目1至5中任一项该的装置,其中,所述多个超声探头中的每一个还包括超声接收元件,用于接收从互不相同的超声探头照射并透过大脑的超声。
项目7、根据项目6该的装置,还包括用于根据透过的超声的接收强度来评估超声的治疗效果的工具。
项目8、根据项目6或7该的装置,还包括输出调整工具,用于根据透过的超声的接收强度来调整待输出的超声的输出。
项目9、一种操作治疗痴呆的装置的方法,该装置包括:
多个超声探头;
超声换能器,其布置在每个所述超声探头中,并配置为将未聚焦的超声能量传播到大脑;和
超声生成器,其连接到每个所述超声探头,
所述方法包括以下步骤:通过所述超声生成器的控制,使布置在每个所述超声探头中的所述超声换能器生成未聚焦的超声能量。
项目10、一种存储在治疗痴呆的装置中的程序,该装置包括:
多个超声探头;
超声换能器,其布置在每个所述超声探头中,并配置为将未聚焦的超声能量传播到大脑;和
超声生成器,其连接到每个所述超声探头,
所述程序被配置为使所述装置执行以下功能:通过所述超声生成器的控制而使布置在每个所述超声探头中的所述超声换能器生成未聚焦的超声能量。
项目11、一种治疗痴呆的方法,包括以下步骤:通过多个超声探头、布置在每个所述超声探头中并配置为将未聚焦的超声能量传播到大脑的超声换能器、以及连接到每个所述超声探头的超声生成器的使用,将从布置在每个所述超声探头内的超声换能器产生的未聚焦的超声能量传播到患者的大脑。
本发明的有益效果
根据本发明,通过用未聚焦的超声能量照射,可以将超声能量传播到大脑的广泛区域,从而使得血管生成、神经元增加等,因此可以治疗认知功能障碍。因此,根据本发明,可以提供不同于现有技术的药物治疗等的新颖的痴呆治疗方法。
附图说明
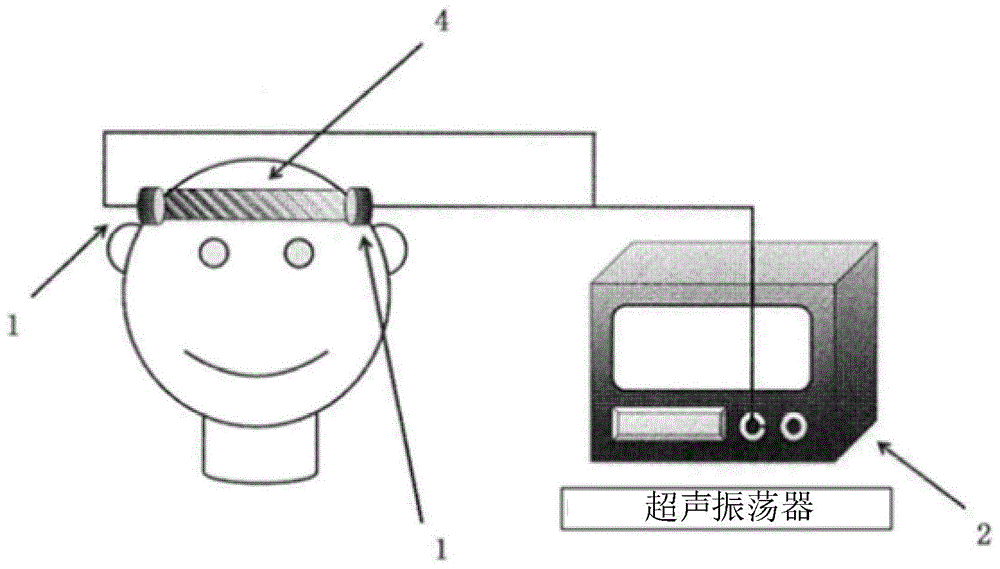
图1是根据本发明的典型实施例的装置的示意图。
图2是超声探头的截面示意图。
图3是本发明的一个实施例中的超声能量扩散的示意图。
图4是在一实施例中的超声探头1的侧视图,其中,扩散以倒锥形形状发生,其直径朝向照射方向逐渐增大。
图5是在颞区上布置两个超声探头的一实施例的示意图。
图6是表示一实施例中的超声的波形的图。
图7是isppa和ispta的说明图。
图8是根据本发明的一实施例的方法的示意图(受试者的姿势)。图8的顶部:受试者处于坐姿,实际上戴着用于固定探头的固定头带。图8的底部:受试者处于卧姿,实际上戴着用于固定探头的固定头带。
图9是实例1-1的测试方法的示意图。bcas手术后1周每隔一天进行3次辐照:20分钟×3次/天。使用激光散斑装置来比较各组的脑血流(cbf)的程度。在术后第28天进行认知行为测试。在第3、7和28天分别进行组织学/生化分析采样。
图10是实例1-1的概要和表示其结果的图。认知行为测试:用于通过lipus治疗来抑制认知功能障碍。y-迷宫测试的结果(通过利用具有正常认知功能时选择与a→b→c不同的路径的小鼠的行为来评估认知功能的方法)
图11是表示实例1-1的结果的图像和图。
图12是表示实例1-1的结果的图像和图。
图13是表示实例1-1的结果的图像和图。
图14是表示实例1-1的结果的图像和图。即使在手术后一个月,少突胶质前体细胞也比未治疗组的多。
图15是表示实例1-1的结果(opc和分裂细胞的评价)的图像。两者都倾向于通过lipus治疗而增加。
图16是实例1-2的测试方法的示意图。从3个月龄开始,每月一次:20分钟×3次/天。在6个月龄时认知行为测试后处死。照射条件与bcas模型相同。
图17是实例1-2的概要和表示其结果的图。认知功能评估:用于通过lipus治疗抑制认知功能障碍。y-迷宫测试的结果(通过利用具有正常认知功能时选择与a→b→c不同的路径的小鼠的行为而来评估认知功能的方法)。
图18是用于表示实例1-2的结果(组织中淀粉样蛋白β的积累)的图像和图。lipus治疗可减少淀粉样蛋白β的积累。
图19是在实例2中一种情况的示意解释图,其中从一个探头开始进行超声照射与从另一个探头开始进行超声照射之间以0.3ms的间隔进行照射(使用人类颅骨进行研究。在骨密度/骨厚度与超声透过率之间的关系)。0.5mhz和1.0mhz处的斜率巧合地重合。认为仅需要考虑厚度。因此,可以从厚度预测透过率。
图20是实例2中的骨密度或骨厚度与超声透过率之间的关系的测试结果的说明。
图21是关于在实例2中研究用于将超声传播到大脑的较宽范围的照射角度的说明图。
图22是表示实例2中的骨密度或骨厚度与超声透过率之间的关系的测试结果的图。
图23是关于在实例2中研究用于将超声传播到大脑的较宽范围的照射角度的说明图(计算提供了元素曲率半径的基础。从人类颅骨的头部高度、头部宽度和头部长度估计理想的照射范围。在这种情况下,考虑到透镜的凸度为15mm。假设要求的照射角度为60°至90°。
图24说明了实例3-1中的治疗方案。
图25是表示实例3-1-1的结果的图像和图。
图26是表示实例3-1-2的结果的图。
图27是实例3-2中的治疗方案的图示。
图28是表示实例3-2-1的结果的图像和图。
图29是表示实例3-2-2的结果的图。
图30是表示实例4-1的结果的图。
图31是表示实例4-2的结果的图。
图32是表示实例4-3的结果的图。
图33是表示实例4-3的结果的图。
具体实施方式
治疗痴呆的装置
下面参考附图描述本申请的发明。本发明提供一种治疗痴呆的装置,包括:多个超声探头;超声换能器,其布置在每个超声探头中,并配置为将未聚焦的超声能量传播至大脑;和超声生成器,其连接到每个超声探头。
这里,“治疗痴呆的装置”有时简称为痴呆治疗装置。在本发明中,“痴呆”包括脑血管性痴呆、阿尔茨海默氏病、同时显示两者的症状等。另外,在本发明中,术语“痴呆”也包括诸如轻度认知障碍的症状。
图1是根据本发明的典型实施例的装置的示意图。如图1所示,本发明的痴呆治疗装置包括多个超声探头1和连接到每个超声探头1的超声生成器2。图2是超声探头的示意图。在每个超声探头中设置有配置成将未聚焦的超声能量传播到大脑的超声换能器3。在本发明中,如图2所示,通常为一个超声探头1布置单个超声换能器3。电能通过布线等从超声生成器2传递到超声换能器3(未示出)而向其施加电压,从而使超声换能器3振动。超声换能器3的振动的频率、时间段、时序等由超声生成器2控制。此外,可以通过切换超声生成器2的控制信号而使得同一超声换能器3充当超声接收元件。
在本发明中,当使得一个超声换能器的超声照射表面具有凸形弯曲形状时,或者多个超声换能器以凸形弯曲形状布置时,超声的方向可以是未聚焦的方向,未聚焦的超声能量可以有效地传播到大脑,因此,痴呆可以通过海马体中血管生成而至的神经细胞激活以及胼胝体中少突胶质前体细胞的活性的增强以及随之而来的白质病变的减少而得以治疗。
在本发明中,未聚焦的超声能量是指在没有聚焦成一点或一条直线的情况下扩散的超声能量。在本发明中,未聚焦的超声能量优选以倒锥形形状扩散,倒锥形形状的直径朝向照射方向逐渐扩大。直径扩大的倒锥形形状的未聚焦的超声能量的倾斜表面的展开角度优选为50°至100°,更优选为60°至90°。如图3所示,超声能量通常以近似圆锥形形状(底表面部分可以是弯曲表面)扩散。在图4中示出了其中以直径朝向照射方向逐渐增大的倒锥形形状发生扩散的实施例中的超声探头1的侧视图。在本发明中,在图4中,倒锥形形状的未聚焦的超声能量的倾斜表面的展开角度在直径上表示为θ。在一典型实施例中,两个超声探头1优选布置在颞区中(图5)。这是优选的,因为这样一来,如上所述,通过未聚焦的超声能量以倒锥形形状的扩散,超声能量可以传播到大脑的大部分区域,例如,至少包括海马体和胼胝体的部分,通常是整个大脑(图5)。
在本发明中,从通过轻柔的超声刺激促进血管生成、神经元增加等的观点出发,照射的超声的振幅(声压)优选为例如3.0mpa以下、更优选为0.7mpa以下的低强度。同时,在本发明中,照射的超声的强度的下限没有特别限制,但是从治疗的有效性的观点出发,优选例如为0.1mpa以上,更优选为0.2mpa以上。在本发明中,对超声的强度、照射的超声的频率没有特别限制,例如可以在0.5mhz~1.5mhz,优选0.5mhz~1.0mhz的范围内适当设定。
在本发明中,对用于超声换能器的材料没有特别限制,只要该材料能够生成上述未聚焦的超声能量即可,但是其实例包括树脂(例如,noryl树脂、聚缩醛、离聚物树脂,和聚氨酯树脂)和金属(例如铜合金)。另外,对生成超声的各超声探头的部分的尺寸没有特别限制,例如,当生成超声的部分的形状为大致圆形时,其直径优选为1.0cm~5.0cm,更优选为2.0cm~4.0cm。另外,生成超声的每个探头的部分的形状没有特别限制,并且该形状可以适当地设计为例如近似圆形、近似椭圆形、或多边形(例如三角形、四边形(例如正方形、矩形、平行四边形或梯形)、五边形,六边形,七边形或八边形)。另外,其尺寸也可以适当地设置为例如与上面关于近似圆形描述的尺寸相对应的尺寸,使得超声可以传播到大脑的较宽区域。
另外,在本发明中,当多个超声探头用于从头部的不同部位照射未聚焦的超声能量时,超声可以传播到大脑的更宽范围。在本发明中,从安全性的角度出发,更具体地,从抑制由于从多个部位照射的超声能量向大脑的重叠传播而导致的过多的超声能量向大脑传播的角度,优选的是,超声生成器控制超声换能器以便在多个超声探头之间依次照射未聚焦的超声能量。在本发明中,要在多个超声探头之间依次地照射未聚焦的超声能量,意味着在多个超声探头中,在同一时间段内超声是仅由其中一个超声探头生成的,即超声不是从两个以上超声探头同时生成的,如下所示:首先,从多个超声探头中的一个超声探头生成超声,其间不从任何其他超声探头生成超声,然后从另一个超声探头生成超声,其间不从任何其他超声探头生成超声……。
在本发明中,从每个超声探头生成的超声传输通过颅骨传播到大脑,并被与布置超声探头位置相对的一侧上的颅骨反射,继而再在超声探头的方向上传播。然后,反射的超声再次被与布置超声探头位置相对的一侧上的颅骨反射,继而传播。在此期间,超声当在大脑中传播以及被颅骨反射时会衰减。因此,从每个超声探头生成的超声在大脑中往复多次,而每次超声被颅骨反射时都会被衰减。
因此,在本发明中,当在多个超声探头之间依次照射未聚焦的超声能量时,优选以一定间隔从多个超声探头生成超声,从而即使从一个超声探头生成的未聚焦的超声能量的照射波或反射波被衰减并且与从下一个超声探头生成的未聚焦的超声能量重叠,也能防止过多的超声刺激。从上述角度出发,在本发明中,优选以0.15/f(f表示待传输的脉冲的频率(mhz))ms以上、更优选0.30/fms以上的间隔来执行采用多个超声探头的未聚焦的超声能量照射。另外,从在短时间内获得更高的治疗效果的角度出发,优选以0.60/f(f(mhz)以如上所述)ms以下、更优选0.30/fms以下的间隔来执行采用多个超声探头的未聚焦的超声能量照射。在本发明中,频率是指传输的超声的频率。
这里,除非另有说明,否则,未聚焦的超声能量照射的间隔是指由于上述原因当通过从一个超声探头开始超声照射、结束从该超声探头的超声照射、从下一个超声探头开始超声照射、结束从下一个超声探头的超声照射……时从一个超声探头的超声照射的结束到从下一个超声探头的超声照射的开始的时间段。
在本发明中,照射的超声是非连续的波,并且其周期数量没有特别限制,但是可以在例如从1周到64周、优选从24周到40周的范围内适当地设置。这里,超声的周期数量是指从超声照射的开始到超声照射的结束的宽度内的周期数量(本文有时称为脉冲宽度)。例如,在具有图6所示的波形的超声的情况下,周期数量为32个周期。超声的治疗时间没有特别限定,但是例如,根据患者的症状、超声的强度等,可以在每次治疗1分钟~60分钟、优选15分钟~25分钟的范围内适当设定。另外,每天的治疗次数也没有特别限定,例如可以在1~4次、优选2~3次的范围内适当设定。对所进行的治疗的频率也没有特别限制,并且可以适当地设定在例如每周1次至7次、优选2次至3次的范围内。治疗间隔也没有特别限制,例如,当一组治疗涉及以上述频率进行5天至10天(更优选6天至8天)的治疗时,优选以1个月至4个月一次的间隔连续进行治疗(例如,每1个月至3.5个月一次),除非有不良事件等。
可以基于isppa、ispta等来调节超声的强度。这里,isppa是指脉冲宽度内的平均强度。ispta是指重复周期内的平均强度。在图7中,示出了超声的isppa和ispta。
另外,照射的超声的ispta没有特别限制,但是从在轻度超声刺激下促进血管生成、增加神经元等的角度出发,可以在例如720mw/cm2以下、优选100mw/cm2至150mw/cm2的范围内适当地设置。当使用多个超声探头时,ispta被表示为各超声探头照射的超声的ispta之和。另外,在本发明中,照射的超声的占空比(dutycycle)没有特别限制,但是可以适当地设定在例如0.1%至50%、优选0.1%至20%的范围内。
这里,占空比是指在一定时间内进行超声照射而在一定时间内暂停超声照射的一个周期的时间段内的超声的照射时间的比率。换句话说,占空比是指一个周期内超声的照射时间与【超声的照射时间+照射停顿时间】之比。当使用多个超声探头时,占空比被表示为各超声探头的照射超声的占空比之和。
另外,如稍后所述,当传输通过颅骨时,从超声探头生成的超声会大大衰减。另外,衰减的程度根据超声通过的颅骨的厚度而变化。因此,优选地,通过例如在痴呆诊断时基于拍摄的头部ct图像将颅骨的厚度输入到超声生成器中,该装置根据颅骨的厚度的数值计算出适当输出的推定值,并作为超声发射以进行治疗。在这样的实施例中,超声生成器包括用于输入颅骨的厚度的数值的工具,以及用于从输入值计算适当输出的推定值的计算工具。
另外,在本发明中,优选地,多个超声探头各自进一步包括用于接收从互不相同的超声探头照射并通过大脑传输的超声的超声接收元件。包括这种接收元件的实施例是优选的,因为可以监视从每个超声探头发出并通过大脑传输的超声强度是否在预先假定的范围内。可以接收和使用自身发送的超声。如上所述,通过切换来自超声生成器的控制信号,超声换能器也可以用作接收元件。因此,在本发明中,其中“多个超声探头各自进一步包括用于接收从互不相同的超声探头照射并通过大脑传输的超声的超声接收元件”的装置还包括其中超声探头各自包括超声换能器的装置,并且超声换能器也用作接收元件。在这样的实施例中,例如,合适的是使用布置在多个超声探头(例如,超声探头之一)的一部分中的超声换能器作为接收元件,并使用布置在任一其他超声探头中的超声换能器作为发射元件。另外,可以通过在经过一定时间段之后在发射元件和接收元件之间切换来使用多个超声换能器中的至少一部分。
另外,优选地,该装置还包括用于根据透过的超声的接收强度来评估超声的治疗效果的工具。例如,通过这种工具,可以计算接收到的超声的强度的积分值以执行:使用该积分值作为指标的治疗效果的评估;当积累值达到预定值时具有一定效果的治疗已经结束的评估;等等。
另外,优选地,该装置还包括输出调整工具,用于根据透过超声的接收强度来调整待输出的超声的输出。更具体地,输出调整工具的实例是用于在由接收元件接收的超声的声压等于或高于预定值时减小输出的反馈工具(处理器)。
当由接收元件接收的超声能量的强度等于或高于预定值时用于减小输出的标准值没有特别限制,但是考虑到安全标准等,可以适当地设定为例如0.1mpa以下、优选为0.05mpa以下的声压。在本发明的优选实施例中,可以预先进行以下设置:当接收元件接收到具有超过在上述范围内设置的上限值的强度的超声时,输出减小。另外,本发明的装置可以包括例如文件,在该文件中写入用于执行稍后所述的本发明的操作装置的方法或治疗方法的过程。
治疗痴呆的装置的操作方法和治疗痴呆的方法
本发明还提供一种治疗痴呆的装置的操作方法,该装置包括:多个超声探头;超声换能器,其布置在每个超声探头中,并配置为将未聚焦的超声能量传播至大脑;和超声生成器,其连接到每个超声探头;该方法包括通过超声生成器的控制使布置在每个超声探头中的超声换能器生成未聚焦的超声能量的步骤。
在典型实施例中,如图1所示,在使得超声探头1与头部接触的状态下执行本发明的方法。与超声探头1接触的部位没有特别限制,但是优选使超声探头1与颞区(太阳穴)接触,因为颅骨相对较薄以利于超声向大脑的传播。可以将凝胶适当地施加到超声探头1的超声生成部分和/或与超声探头相接触的头部部分上,从而可以将超声有效地传播到大脑。此外,如图1所示,超声探头1可以用头带4固定。此外,如图8所示,受试者的姿势可以是坐姿,也可以是卧姿。另外,待进行本发明的方法的受试者的实例包括哺乳动物,例如小鼠、大鼠、人、猴子、狗和猪。其中,优选是人。
本发明还提供了一种治疗痴呆的方法,该方法包括以下步骤:通过使用超声探头、布置在每个超声探头中并配置为将未聚焦的超声能量传播至大脑的超声换能器、以及连接到每个超声探头的超声生成器,将从布置在多个超声探头的每一个中的超声换能器生成的未聚焦的超声能量传播到患者的大脑。
对于用于本发明的那些方法的装置,超声的照射条件等,可以采用与上述“治疗痴呆的装置”部分中所述的那些类似的。
程序
本发明提供了一种存储在治疗痴呆的装置中的程序,该装置包括:多个超声探头;超声换能器,其布置在每个超声探头中,并配置为将未聚焦的超声能量传播至大脑;和超声生成器,其连接到每个超声探头;该程序被配置为使装置执行通过超声生成器的控制使布置在每个超声探头中的超声换能器生成未聚焦的超声能量的功能。
本发明的程序可以用于使上述治疗痴呆的装置(包括在装置中的计算机)生成未聚焦的超声能量。另外,在以下实施例中,即,在本发明的装置中,多个超声探头各自还包括用于接收从互不相同的超声探头照射并透过大脑的超声的超声接收元件的实施例中,本发明的程序可以使该装置执行根据透过超声的接收强度来评估超声的治疗效果的功能。例如,程序可以通过计算接收到的超声的强度的积分值,并将该积分值作为指标与预先设定的值进行比较,从而使装置评价治疗效果是高还是低。另外,程序可以使装置计算接收到的超声的强度的积分值,并在积分值达到预先设置的预定值时评估具有一定效果的治疗已经结束。另外,在这样的实施例中,装置可以包括用于这样的评估的显示部分。在这种情况下,本发明的程序可以使装置(计算机)执行在显示部分上显示如上所述获得的评估的功能。进一步地,在这样的实施例中,本发明的程序可以使装置(计算机)执行输出调整功能,该输出调整功能根据透过超声的接收强度来调整待输出的超声的输出。更具体地,当由接收元件接收的超声的声压等于或高于预定值时,该程序使例如用于减小输出的反馈工具(处理器)执行输出调整。
上面已经参考示出了特定实施例的附图描述了本发明。然而,很明显,本发明不限于那些实施例。例如,每个超声探头和超声生成器之间的连接可以如图1所示那样被有线连接,或者也可以是无线连接的。同样关于超声探头的数量,已经通过使用两个超声探头的实施例进行了描述,但是也可以使用三个或更多个超声探头。例如,可以通过使两个超声探头与两个颞区(太阳穴)接触,并且使另一个超声探头与枕骨和颈背之间的边界部分(枕骨大孔)接触,来进行超声照射。
实例
以下通过具体实例举例说明本发明,但是本发明不限于这些实例。
实例1:超声治疗的痴呆治疗效果的验证
实例1-1血管性痴呆模型(双侧颈总动脉狭窄(bcas)模型)
在占血管性痴呆大多数的皮质下血管性痴呆中,慢性脑缺血被认为是重要的病理机制。在bcas模型中,当脑缺血长时间持续时,就会形成类似于人类的白质病变,从而引起更高的功能障碍。因此,bcas模型是目前最标准的血管性痴呆模型。因此,在该实例中,对这种bcas模型的整个大脑进行超声照射以验证对痴呆的治疗效果。
具体地,通过文献中记载的方法(shibatam等,stroke.2004年11月;35(11):2598-603)对9~12周龄的c57bl/6雄鼠(n=10~15)进行治疗,从而生成bcas模型。作为假手术组,使用未经bcas治疗的9~12周龄的c57bl/6雄鼠。
bcas术后1周内(bcas术后1天、3天和5天)进行了3次超声照射。每天3次进行超声照射20分钟。
使用激光散斑装置(omegawave生产,omegazonemini2)测量bcas术前组、1天组、2天组、4天组、7天组和28天组中每个组的脑血流(cbf)程度。另外,还执行了:使用脑组织标本的各种免疫染色(免疫荧光染色)、使用蛋白质的免疫印迹(westernblotting)的表达分析、使用rna测序的基因表达分析等。
照射条件如下所述,并且使用矩形超声探头进行照射,其中每个矩形超声探头的面积为3.75cm2(1.5cm×2.5cm),从而使超声传播到模型的整个大脑。
照射条件:
强度(ispta):100mw/cm2
频率:1.875mhz
周期数量:32个周期
重复频率:6khz
该测试的概要如图9所示。认知行为测试的结果如图10所示。在图10中,侵入次数表示侵入分支的总数,而自发交替表示小鼠的自发交替。(【侵入不同分支的三次相继侵入的次数】/【侵入y-迷宫的所有分支的次数-2])。超声治疗显著抑制了认知行为测试中的认知功能障碍。
白质病变(胼胝体)的评价
如图11所示,超声治疗显著保持了髓鞘结构,并且还增加了形成髓鞘的成熟少突胶质细胞的数量。在图11的左侧,标题为“通过lipus治疗保持脑鞘结构”,显示了胼胝体的kb染色图像。在图11的右边的图中,白质病变表示胼胝体中白质的脱髓鞘病变的程度。在图11的左侧,标题为“在lipus治疗组中成熟少突胶质细胞增加”,显示了胼胝体的gst-p免疫染色的图像。在图11的右边的图中,纵轴上的gst-p阳性细胞的数量表示每单位面积的成熟少突胶质细胞的数量。如图11所示,超声治疗显著保持了髓鞘结构,并且还增加了形成髓鞘的成熟少突胶质细胞的数量。在图12的顶部的标题为“在lipus组中未成熟神经元增加”的标题下,显示了dcx免疫荧光染色的图像。在图12底部的左侧的标题为“通过lipus治疗使海马毛细血管增加”的标题下,显示了海马体的cd31免疫染色的图像。在图12的底部的右图中,纵轴上的cd31阳性细胞的数量表示每单位面积的毛细血管的数量。如图12所示,在海马体中,未成熟的神经元增加,毛细血管也增加。
ki67免疫染色的图像显示在图13的左上方,olig2免疫染色的图像显示在其左下方。在图13的右侧的图中,纵轴上的ki67阳性细胞的数量和olig2阳性细胞的数量分别表示经历细胞分裂的细胞数量和少突胶质前体细胞的数量。因此,在评估急性期组织时获得了图13,超声治疗倾向于增加胼胝体中生长的细胞,并增加olig2阳性细胞。有鉴于此,通过双重荧光免疫染色证实了分裂/生长细胞是否为少突胶质前体细胞,结果,它们肯定是融合了,从而表明分裂/生长细胞为少突胶质前体细胞(opc)。使用rna-sequencing的基因全分析还证实了与少突胶质细胞(例如olig2)的分化和生长相关的基因变化。
另外,胼胝体中的olig2免疫染色的图像显示在图14的左侧。在图14右侧的图中,纵轴上的olig2阳性细胞的数量表示术后28天少突胶质前体细胞的数量。因此,如图14所示,即使在手术后一个月,超声治疗组中的opc也显著增加,表明效果持续存在。另外,在图15中,示出了术后3天的海马体的olig2免疫染色的图像和ki67免疫染色的图像。如图15中所示,在海马体中,olig2阳性细胞和ki67阳性细胞也倾向于增加,并且结果与术后1个月进行评估的图11的结果并不矛盾。因此说明,胼胝体中opc的生长以及海马体中血管生成和未成熟神经元的增加影响了认知功能的提高。
实例1-2阿尔茨海默氏病模型(转基因)
使用转基因小鼠(5xfad)作为阿尔茨海默氏病小鼠模型,按照图16中所示的方案,以与bcas模型相同的方式进行超声治疗。对5xfad模型进行每月一次进行一组超声检查,并观察到6个月大。
结果如图17和图18所示。如图17所示,超声治疗抑制了认知功能障碍。在图18中,示出了4g8免疫染色(淀粉样蛋白β染色)的图像。如图18所示,说明通过超声治疗减少淀粉样蛋白β的积累的可能性。分子表达分析发现超声治疗可导致内皮一氧化氮合酶(enos)大量表达,提出enos可能有助于提高认知功能。
实例2:考虑安全性的人的超声照射方法的研究
以下是可用的超声照射的安全标准。
(1)globalmaximumacousticoutput(ao)建议的720w/cm2以下
(2)tyles’sstatedlimit建议的500mw/cm2以下
因此,在以下研究中,在ispta为250mw/cm2以下的范围内进行了超声照射。
使用人类颅骨验证了能够在临床上影响超声治疗强度的因子。收集了总共七个67至96岁的男性和女性捐赠尸体的颞骨,分别测量了其骨密度和骨厚度,然后分别测量了其超声透过率。
测试在0.5mhz和1.0mhz下进行。结果如下所述。在0.5mhz下,透过性与骨厚度之间的相关系数为-0.53,并且骨密度与透过性之间的相关系数为0.30。在1.0mhz下,透过性与骨厚度之间的相关系数为-0.88,透过性与骨密度之间的相关系数为-0.30。根据这些数据,例如对1.0mhz进行了多变量分析,结果发现透过性和骨厚度具有p<0.001的显著性,但是透过性和骨密度之间没有显著的趋势。结果表明,仅“骨厚度”需要被视为患者方的参数。在这种情况下,调整后的r平方(针对自由度调整的确定系数)为0.7472,这表明可以根据骨厚度预测透过性。回归分析发现,骨厚度与超声透过率之间存在相关性。在图19中,示出了通过进一步执行多变量分析获得的结果。骨密度与超声透过率之间无相关性,骨厚度与超声透过率之间无显著相关性,并且r平方在1.0mhz时对结果较高,这表明可以从厚度的值预测透过率。即,表明了在经颅超声照射中,只有患者的骨厚度是需要的参数。
此外,在人类颞骨的一般厚度为大约2mm至大约3mm的情况下,例如在0.5mhz的频率的情况下,一次骨-脑透射的超声透过率在功率方面为25%至50%(振幅方面从50%到70%)(图20)。因此,就到达大脑时的功率而言,从超声探头照射的超声已经衰减了25%至50%。
如果使用左右颞区的探针进行两点交替照射(图21),则假设超声在大脑中的传播速度为1540m/s,则500khz的波长为3.08mm,32个波在一个脉冲中传播3.08×32=98.56mm。在图21中,示出了在aist人体测量数据库(2001日本人头部的人体测量数据库)(https://www.dh.aist.go.jp/database/head/#stats)所描述的成年人的头部宽度、总头部高度和头部长度等的平均值。根据上述值,假设头部的最短直径为174mm(数据库,男性头部宽度的最大直径),则到达对侧颅骨所需的时间为0.174m/1540m/s=0.113ms。
同时,在较高的频率(约1db/cm/mhz)下,大脑对超声的吸收会增强。在20db衰减的情况下功率变为1/100,因此在0.5mhz在0.2db/cm的条件下(参见1999年出版的丸善出版有限公司(maruzenpublishingco.,ltd)出版的《超声手册》第731页的表格),100cm传播才能使功率变为1/100。即,认为以1m/1540m/s=0.00065s=0.65ms的间隔进行照射时,先前的照射波的影响可以忽略。
实际上,在100cm传播中,被骨骼反射100cm/17.4cm=6次,因此,通过反射(通过骨骼出射)的影响,可以进一步提高安全性。
根据使用上述人类颅骨的研究,超声在一次骨-脑透过中的衰减在振幅方面大约为一半到大约70%,在这种情况下,相当于在功率方面从25%到50%。这表明以0.3ms的间隔照射不会引起问题(通过骨骼将功率减半,并且通过大脑中的衰减功率变为1/50)。
因此,当从一个探头开始进行超声照射与从另一探头开始进行超声照射之间的间隔为0.3ms时进行照射(图22)时,0.5mhz时占空比为10cm/50cm=20%。考虑到上述情况,认为不可能由于0.5mhz的干扰波和小于20%的占空比而导致局部能量增加。
另外,认为可以通过从太阳穴照射超声而将超声传播到整个大脑,其中使用圆柱形探头,其照射超声的部分的直径设置为33mm,直径扩大的倒锥形形状的未聚焦的超声能量的倾斜表面的展开角度为77°,其中假定受试者的头宽和头高分别为70mm至80mm和100mm至130mm,则从(图23)。
可以认为,在上述条件下进行超声照射时,以与上述实例1相同的方式,通过超声的物理刺激在人体内也可获得痴呆的治疗效果。
实例3证明仪器的功效的测试
为了揭示该仪器对痴呆的两种主要病理状况,即对脑血管性痴呆(vad)和阿尔茨海默氏病(ad)的有效性,使用相应的小鼠模型进行了研究。在此仪器中显示主要功效的结果如下所述。在这些结果中,用图表显示了认知功能测试的结果,该结果也被认为是临床设置的终点,而图中显示了被认为是对其机制研究最重要的因子的脑血流。
3-1使用vad模型小鼠的研究
生成双侧颈总动脉狭窄(bcas)小鼠作为vad模型,并分为lipus组(治疗组)或对照组(非治疗组)。将lipus设置为从bcas手术后的第二天开始照射到整个大脑,按照图24中所示的时间表进行治疗干预。lipus治疗后,进行随访观察,直到术后28天,并且进行了脑血流的测量和认知行为测试。另外,基于rna-sequencing和bio-plex的全分析,使用全脑组织进行生物化学分析,并通过组织免疫染色进行评估。
3-1-1使用vad模型小鼠分析脑血流的经时变化
治疗干预之后,在2小时、4天和28天后测量了脑血流,结果发现,lipus组中的脑血流的降低得到了显著抑制(图25)(n=9-10,假手术;n=20-25,bcas)(*p<0.05;***p<0.0005;二元anova,多重t-检验)。所有结果均表示为平均值±标准误差。
3-1-2使用vad模型小鼠的认知功能测试
在治疗干预28天后进行了y-迷宫测试和被动回避测试,结果发现lipus组中的认知功能障碍得到了显著抑制(图26a和图26b)(假手术;n=12-16,bcas;n=13-17)(*p<0.05,**p<0.005;二元anova,多重t-检验)。所有结果均表示为平均值±标准误差。此外,这种效果一直维持到术后3个月(p<0.05)。
3-1-3使用vad模型小鼠的超声治疗影响的生化分析
发现超声治疗显著增强了与血管生成/少突胶质前体细胞相关的基因的表达(olig2;p<0.05,enos;p<0.05,cxcr4;p<0.05,fgf2;p<0.05)。此外,通过免疫印迹分析发现主要是血管生成分子的表达显著增强(enos;p<0.05,cxcr4;p<0.05,fgf2;p<0.005,vegf;p<0.05),并且还发现神经营养因子的表达显著增强(bdnf;p<0.05,ngf;p<0.05)。这里,olig2表示少突胶质细胞转录因子2,enos表示内皮一氧化氮合酶,cxcr4表示cxc趋化因子受体4,fgf2表示成纤维细胞生长因子2,vegf表示血管内皮生长因子,bdnf表示脑源性神经营养因子,ngf表示神经生长因子。
3-1-4使用vad模型小鼠的超声治疗影响的组织学分析
超声治疗减少了白质损伤(p<0.05),并促进了血管生成/少突胶质前体细胞的生长(每个p<0.05)。此外,未成熟神经细胞增多(p<0.05)。
3-2使用ad模型小鼠的研究
使用5xfad转基因小鼠作为ad模型,确认了对ad的有效性和安全性。根据vad模型执行了评估方法。将5xfad转基因小鼠分为lipus组(治疗组)或对照组(非治疗组)。将lipus设置为照射到整个大脑,按照图27所示的时间表进行治疗干预。lipus治疗之后,进行随访观察,直到术后28天,并且进行了脑血流的测量和认知行为测试。另外,基于rna-sequencing和bio-plex的全分析,并通过组织免疫染色进行评估,使用全脑组织进行生化分析。
3-2-1使用ad模型小鼠分析脑血流的经时变化
从初始治疗开始3个月时,lipus组中流过整个大脑的血流显著得以保持(图28)(每组n=14)(*p<0.05,t-检验)。所有结果均表示为平均值±标准误差。
3-2-2使用ad模型小鼠的认知功能测试
治疗干预之后,进行了y-迷宫测试,结果发现,在初次治疗后3个月,lipus组中的认知功能障碍得到了显著抑制(图29)(每组n=18)(***p<0.0005,t-检验)。所有结果均表示为平均值±标准误差。
3-2-3使用ad模型小鼠(神经营养因子)的超声治疗的影响的生化分析
lipus组中,enos和神经营养因子的表达显著增强(enos;p<0.05,bdnf;p<0.05,ngf;p<0.05),并且,淀粉样蛋白β(42)得以降低(p<0.05)。
3-2-4使用ad模型小鼠(淀粉样蛋白β)的超声治疗的影响的生化分析
超声处理显著减少了淀粉样蛋白β(42)在整个大脑中的积累(p<0.05)。此外,小胶质细胞增生显著减少(p<0.05),并且发现血管生成倾向于被促进(p=0.19)。
实例4展示仪器的使用方法的测试
4-1最佳频率条件的研究
在使用人颞骨(待在外部安装治疗仪器的部位)进行的超声透过性评估中,透过率在较低频率下具有较高的值(y=-0.098x+0.59,2cm颅骨的预计透过率:60.6%;0.5mhz,y=-0.098x+0.78,2cm颅骨的预计透过率:41.6%;1.0mhz)(图19)。另外,尽管该报告是关于聚焦的超声的,但是已经描述了频率与机械指数(mi)和热指数(ti)的关系。以下条件的频率约为0.5mhz:该条件与用发现有效果的小鼠的基础研究中的99mw/cm2的条件接近;并且该条件是指在大脑中未发生空化(mi值0.25;在较坏的情况下是在水中发生空化的情况mi值=1.0的四分之一),且在这种条件下没有发生温度过度升高(ti未升高2℃或更高)。此外,在使用人脐静脉内皮细胞的体外实验中,即使在0.5mhz的频率下也发现了vegf表达的增强(p<0.05)(图30)。考虑到上述情况,考虑到透过性和安全性,认为0.5mhz是最佳的。
4-2最佳占空比的研究
在使用人脐静脉内皮细胞的体外实验中,通过将占空比条件在1%、20%和40%之间变化,同时将频率固定在0.5mhz来评估vegf表达的变化。结果如下:在占空比为1%和40%时,未发现vegf表达增强,而在占空比为20%时发现vegf表达显著增强(p<0.05)(图31)。考虑到上述情况,在0.5mhz的频率下,占空比约20%被认为是最佳的,但是考虑到关于干扰波的安全性的初步计算,期望占空比为20%或更低,因此认为最佳占空比为20%(每个探头10%)。
4-3最佳治疗条件的研究
使用培养的血管内皮细胞研究了照射条件。在0.05mpa至2.2mpa的范围内,作为可在凸形换能器中设定的声压,对培养的血管内皮细胞进行超声照射,并评估vegf、fgf2和enos的mrna表达。认为该治疗的有效性与vegf、fgf2和enos的表达量相关。因此,在该研究中,当其mrna的表达量与对照组相比显著高时,可以认为照射条件是有效的。
结果如图32所示,表明将组织振幅设定为0.05mpa至0.5mpa是重要的。为了在脑组织中获得该声压,据估计,在元件正下方的声压理想地落在0.1mpa至1.5mpa的范围内。
接着,考虑到患者的接触部位的接触温度也上升,在以下两组条件下使用脑血管内皮细胞评价vegf的表达量:条件1:元件正下方的声压:1.3mpa(组织振幅:0.15mpa)和总占空比:5%;条件2:元件正下方的声压:0.9mpa(组织振幅:0.1mpa)和总占空比:10%。结果,在条件1下vegf的表达量具有显著高的值,因此判断条件1是理想的治疗条件。
4-4治疗时间/周期的最佳设置
在使用两只不同的ad模型小鼠的基础研究中,在20分钟×3次的治疗条件下发现了有效性。此外,就治疗周期而言,在脑血管性痴呆模型中进行的治疗直至3个月的随访观察发现,在超声治疗组中发现的认知功能障碍的抑制作用一直维持到术后3个月(p<0.05)。考虑到上述情况,以20分钟×3次的条件每3个月进行治疗可能是合适的。
工业适用性
如上所述,仅在日本,痴呆患者的数量就高达约260万,并且,该数量还在不断增加。因此,强烈需要开发一种新颖的治疗方法。因此,与现有技术的药物治疗等不同,可以提供治疗痴呆的新方法的本发明是非常有用的。
- 还没有人留言评论。精彩留言会获得点赞!