包含细菌菌株的组合物的制作方法
本发明涉及包含从哺乳动物消化道分离的细菌菌株的组合物以及此类组合物在治疗疾病中的用途的领域。
背景技术:
人类肠道被认为在子宫中是无菌的,但是在出生之后它立即暴露于各种各样的母体和环境微生物。然后,发生动态时间段的微生物定居和繁衍,这被诸如以下的因素影响:分娩方式、环境、饮食和宿主基因型,全部这些都影响肠道微生物群的组成,在早期生命期间尤其如此。随后,微生物群稳定化并且变得成熟[1]。人类肠道微生物群含有多于500-1000种不同的种系型,它们基本上属于两种主要的细菌分类:拟杆菌门和厚壁菌门[2]。由人类肠道的细菌定居产生的成功的共生关系已产生各种各样的代谢、结构、保护性和其他有益的功能。所定居的肠道的增强的代谢活动确保以其他方式难以消化的膳食组分随着副产物的释放而被降解,从而为宿主提供重要的营养物质来源。相似地,肠道微生物群的免疫学重要性被充分地认知并且在无菌动物中例示,所述无菌动物具有在引入共生细菌之后在功能上重构的受损免疫系统[3-5]。
微生物群组成的动态变化已在肠胃病症诸如炎性肠病(ibd)中有所记载。例如,梭菌(clostridium)集群xiva细菌的水平在ibd患者中降低,而大肠杆菌(e.coli)的数量增加,从而表明肠道内共生生物和病原生物平衡的变化[6-9]。
在认识到某些细菌菌株对于动物肠道可能具有的潜在积极作用之后,已提出各种菌株用于治疗各种疾病(参见,例如[10-13])。另外,已经提出某些菌株,主要包括乳杆菌(lactobacillus)和双歧杆菌(bifidobacterium)菌株,用于治疗与肠不直接相关的各种炎性和自身免疫性疾病(关于综述参见[14]和[15])。然而,不同疾病与不同细菌菌株之间的关系以及特定细菌菌株对于肠道和在全身水平下以及对于任何特定类型的疾病的准确作用并未被良好地表征,特别是对于神经退行性障碍而言。
最近,本领域对可能在人类脑部疾病中发挥病理生理作用的肠道微生物群的改变的兴趣日益增加[16]。临床前和临床证据强烈表明大脑发育与微生物群之间存在联系[17]。大量的临床前文献表明,大脑与肠道微生物群之间存在双向信号传导,涉及多个神经分泌和内分泌信号传导系统。确实,微生物群中梭菌物种水平的增加与脑部障碍有关[18],而拟杆菌门和厚壁菌门的失衡也与脑部发育障碍有关[19]。已表明,肠道共生菌(包括双歧杆菌属(bifidobacterium)、乳杆菌属(lactobacillus)、萨特氏菌属(sutterella)、普雷沃菌属(prevotella)和瘤胃球菌属(ruminococcus)的那些共生菌)以及产碱杆菌科(alcaligenaceaefamily)水平的改变参与了免疫介导的中枢神经系统(cns)障碍,但受到表明患者与健康受试者之间的微生物群没有改变的研究的质疑[10]。狄氏副拟杆菌(parabacteroidesdistasonis)已被提出用于治疗各种病症,包括哮喘、类风湿性关节炎和多发性硬化症[20]
与哮喘和类风湿性关节炎一样,多发性硬化症主要由免疫系统介导。免疫系统攻击中枢神经系统中的有髓鞘的轴突,从而破坏髓鞘,称为斑块或病灶。脱髓鞘尤其发生在视神经、软膜下脊髓、脑干、小脑和皮质旁和室周白质区中发生。
由此,多发性硬化症具有与其他神经退行性疾病(诸如帕金森氏病、阿尔茨海默氏病或痴呆)不同的病理。例如,多发性硬化症通常在20多岁和30多岁的患者中诊断出,而许多其他神经退行性疾病(诸如帕金森氏病、阿尔茨海默氏病和痴呆)主要在年龄超过65岁的患者中诊断出。
与许多神经退行性疾病一样,帕金森氏病主要由错误折叠蛋白的积累介导。帕金森氏病是涉及α-突触核蛋白的积累的突触核蛋白病,所述α-突触核蛋白在神经元体的细胞浆内的路易体中作为不可溶的纤丝聚集。α-突触核蛋白的积累具有毒性,并且损害线粒体、溶酶体和内质网的功能,并干扰微管运输。
已针对非甾体抗炎药物(nsaid)诸如布洛芬治疗各种神经疾病的功效进行测试,但是nsaid对于神经退行性疾病(如帕金森氏病)的临床影响仍然不清楚。虽然一些研究已显示慢性nsaid使用预防帕金森氏病,但是其他研究不能证实存在显著关系。最近的元分析(meta-analysis)表明,使用非阿司匹林nsaid(特别是布洛芬)使pd的风险降低15%,而使用阿司匹林未显示任何作用[21]。
目前,微生物群与人类脑部疾病之间联系的实际作用并未被良好地表征。因此,需要更直接的分析研究来鉴定改变微生物群对神经退行性障碍的治疗作用。
在本领域中需要治疗神经退行性障碍的新方法。还需要表征肠道细菌的潜在作用,以便可以开发出使用肠道细菌的新疗法。
技术实现要素:
发明人已经开发出用于治疗和预防神经退行性障碍的新疗法。本发明人已认识到来自副拟杆菌属的细菌菌株可以有效治疗神经退行性疾病。如在实施例中所述,施用包含狄氏副拟杆菌的组合物可以预防活性氧并预防炎症,因此充当神经保护剂。发明人还已确定,用狄氏副拟杆菌进行的治疗可以减少促炎分子诸如nfκb和il-6被lps和突变体α-突触核蛋白a53t活化。发明人已经确定,在体外用狄氏副拟杆菌进行的治疗可以降低组蛋白脱乙酰化活性和脂质过氧化,这可以帮助减少细胞死亡和细胞凋亡。发明人还已确定,狄氏副拟杆菌可以产生可以减轻炎症和氧化应激的吲哚。此外,发明人还证明了,用狄氏副拟杆菌进行的治疗可以增加犬尿氨酸水平。
发明人还发现用狄氏副拟杆菌进行的治疗增加了bdnf的活化。bdnf是一种神经营养生长因子,其已被证明能增强神经元的分化和存活。因此,本发明的组合物可以用于增强神经细胞存活以治疗或预防神经退行性疾病的方法中。
在第一实施方案中,本发明提供一种包含副拟杆菌属的细菌菌株的组合物,其用于治疗或预防神经退行性障碍的方法。
在特定实施方案中,本发明提供一种包含副拟杆菌属的细菌菌株的组合物,其用于治疗或预防选自由以下组成的组的疾病或病状的方法:帕金森氏病,包括进行性核上性麻痹、进行性核上性麻痹、steele-richardson-olszewski综合征、正常压力脑积水、血管或动脉硬化性帕金森病和药物诱发的帕金森病;阿尔茨海默氏病,包括本森氏综合症(benson'ssyndrome);多发性硬化症;亨廷顿氏病;肌萎缩性侧索硬化症;卢·格里格病(lougehrig'sdisease);运动神经元疾病;朊病毒病;脊髓小脑共济失调;脊髓性肌萎缩;痴呆,包括路易体、血管和额颞痴呆;原发性进行性失语;轻度认知损害;hiv相关的认知损害和皮质基底节变性。
在优选的实施方案中,本发明提供一种包含副拟杆菌属的细菌菌株的组合物,其用于治疗或预防帕金森氏病的方法,所述帕金森氏病诸如与一般炎症状态有关的环境、家族或帕金森氏病。发明人已确定,用副拟杆菌菌株进行的治疗可以减少环境和家族帕金森氏病的体外模型中促炎分子诸如nfκb和il-6被lps和突变体α-突触核蛋白a53t活化。在优选的实施方案中,本发明提供一种包含狄氏副拟杆菌菌种的细菌菌株的组合物,其用于治疗帕金森氏病。使用狄氏副拟杆菌的组合物对治疗帕金森氏病可以是特别有效的。
在一些实施方案中,本发明的组合物用于治疗或预防早发性神经退行性疾病的方法。在一些实施方案中,本发明的组合物用于预防或延迟神经退行性障碍的发作或进展的方法。
在本发明的优选的实施方案中,组合物中的细菌菌株是狄氏副拟杆菌。还可以使用紧密相关的菌株,诸如具有与狄氏副拟杆菌的细菌菌株的16srrna序列具有至少95%、96%、97%、98%、99%、99.5%或99.9%同一性的16srrna序列的细菌菌株。优选地,所述细菌菌株具有与seqidno:1、2、3、4、5、6、7、8或9具有至少95%、96%、97%、98%、99%、99.5%或99.9%同一性的16srrna序列。优选地,序列同一性是针对seqidno:9。优选地,用于本发明的细菌菌株具有由seqidno:9表示的16srrna序列。
在某些实施方案中,本发明的组合物用于口服施用。口服施用本发明的菌株可以对神经退行性障碍有效。另外,口服施用对于患者和从业人员来说是方便的并且允许递送到肠道和/或部分或完全定殖于肠道。
在某些实施方案中,本发明的组合物包含一种或多种药学上可接受的赋形剂或载体。
在某些实施方案中,本发明的组合物包含已冻干的细菌菌株。冻干是用于制备允许递送细菌的稳定组合物的有效且方便的技术。
在某些实施方案中,本发明提供一种包含如上所述的组合物的食物产品。
在某些实施方案中,本发明提供一种包含如上所述的组合物的疫苗组合物。
另外,本发明提供一种治疗或预防神经退行性障碍的方法,其包括施用包含副拟杆菌属的细菌菌株的组合物。
在本发明的某些实施方案中,所述组合物用于治疗脑损伤。本发明的组合物的神经保护活性及其降低组蛋白脱乙酰酶活性(hdac)水平的能力可以使它们可用于治疗脑损伤。在优选的实施方案中,本发明的组合物用于治疗中风,例如治疗中风引起的脑损伤。
附图说明
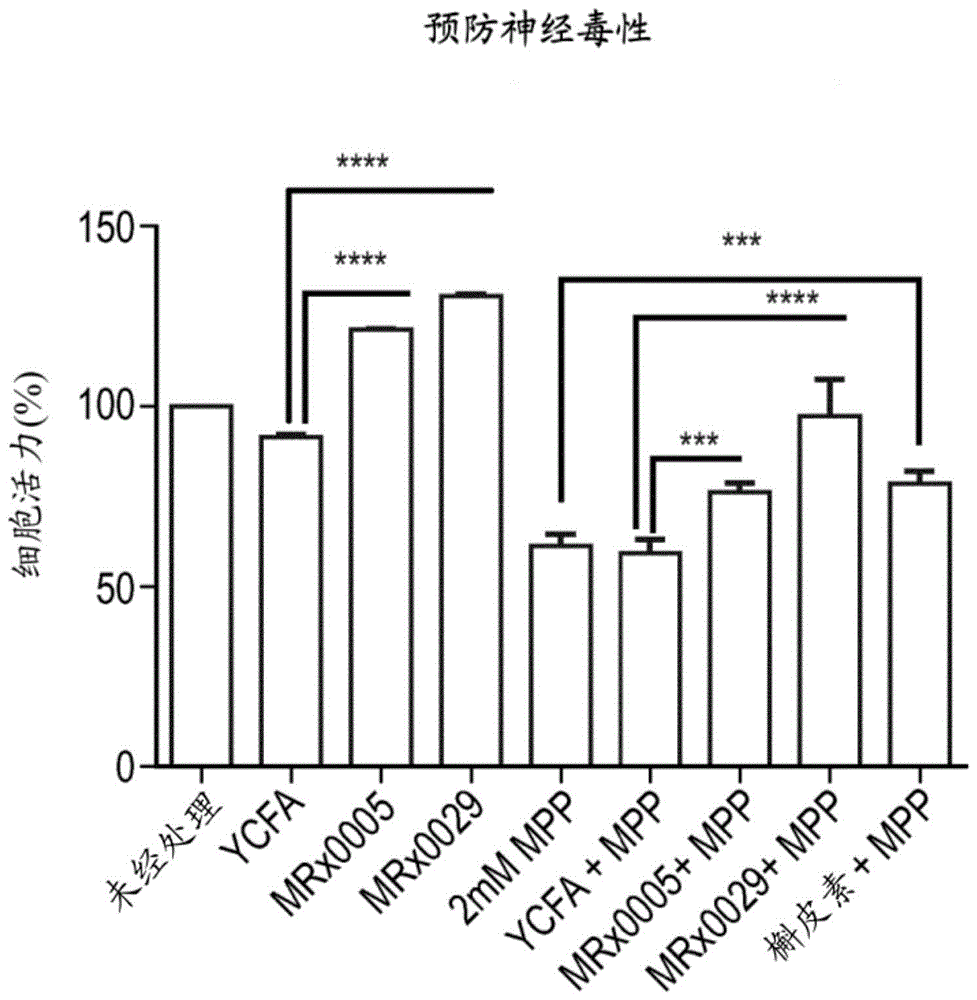
图1:神经母细胞瘤细胞的细胞活力
图2a:il-6分泌的下调图2b:il-8分泌的下调
图3:α-突触核蛋白il-6和il-8分泌的抑制
图4:α-突触核蛋白诱导的nfκb启动子活化的抑制
图5:lps诱导的nfκb启动子活化的抑制
图6:抗氧化能力的变化
图7:总抗氧化能力的变化(脂质氧化)
图8:组蛋白脱乙酰酶(hdac)活性的变化
图9:吲哚产生水平
图10:犬尿氨酸产生水平
图11:神经保护–细胞活力。图11示出了与图1相同的数据。
图12:代谢物的产生水平–大脑中的神经递质
图13:代谢物的产生水平–上清液中的有机酸
图14:对肠屏障功能的影响
图15:bdnf产生水平
图16:(a)u373细胞,(b)shsy-5y细胞中ros水平的变化
图17:大脑中神经递质的产生
图18:海马受体表达的变化–a)催产素受体,b)加压素受体,c)糖皮质激素受体和d)盐皮质激素受体
图19:a)促肾上腺皮质激素释放激素(crh),b)bdnf表达和c)tlr4的海马表达的变化
图20:a)海马促肾上腺皮质激素释放激素受体1(crfr1)表达的变化和b)促肾上腺皮质激素释放激素受体2(crfr2)表达
图21:a)肿瘤坏死因子,b)白介素1b和c)il-6的海马表达的变化
图22:a)海马整合素αm(cd11b)表达的变化和b)海马血清素1a受体(5-ht1a受体)表达的变化
图23:a)海马谷氨酸离子型受体nmda型亚基2a(grin2a)的变化和b)谷氨酸离子型受体nmda型亚基2b(grin2b)表达
图24:a)γ-氨基丁酸a受体2(gabaa2),b)γ-氨基丁酸b受体1(gababr1)和c)多巴胺受体1(drd1)的海马表达的变化
图25:杏仁核受体表达的变化–a)催产素受体,b)加压素受体,c)糖皮质激素受体和d)盐皮质激素受体
图26:a)脑源性神经营养因子(bdnf),b)toll样受体4(tlr-4),c)促肾上腺皮质激素释放激素受体1(crfr1)和d)促肾上腺皮质激素释放激素受体2(crfr2)的杏仁核表达的变化
图27:a)整联蛋白αm(cd11b),b)白介素6(il-6),c)谷氨酸离子型受体nmda型亚基2a(grin2a)和d)谷氨酸离子型受体nmda型亚基2b(grin2b)的杏仁核表达的变化
图28:a)gaba-a受体α2亚基(gabra2),b)gaba-ab型受体1亚基(gabbr1)和c)多巴胺受体1(drd1)的杏仁核表达的变化
图29:a)催产素受体,b)脑源性神经营养因子(bdnf),c)盐皮质激素受体和d)糖皮质激素受体的前额叶皮层表达的变化
图30:a)toll样受体4(tlr-4),b)促肾上腺皮质激素释放激素受体1(crfr1),c)促肾上腺皮质激素释放激素受体2(crfr2)和整联蛋白αm(cd11b)的前额叶皮层表达的变化
图31:a)白介素6(il-6),b)谷氨酸离子型受体nmda型亚基2a(grin2a),c)谷氨酸离子型受体nmda型亚基2b(grin2b)和d)gaba-a受体α2亚基(gabra2)的前额叶皮层表达的变化
图32:a)gaba-a受体b型受体亚基1(gabbr1)和b)多巴胺受体1(drd1)的前额叶皮层表达的变化
图33:a)色氨酸羟化酶-1(tph1)和b)吲哚胺2,3-双加氧酶-1(ido1)的结肠表达的变化
图34:a)色氨酸羟化酶-1(tph1)和b)吲哚胺2,3-双加氧酶-1(ido1)的回肠表达的变化
图35:循环色氨酸代谢物水平a)犬尿氨酸,b)色氨酸和c)犬尿氨酸/色氨酸代谢指数的变化
图36:对用mrx0005和mrx0029喂养的小鼠的小鼠脾细胞的干扰素-γ产生的影响
图37:对脾细胞的白介素-1β产生的影响
图38:对脾细胞的白介素-6产生的影响
图39:对脾细胞的肿瘤坏死因子产生的影响
图40:对脾细胞的白介素-10产生的影响
图41:对脾细胞的化学引诱剂cxcl1产生的影响
图42:盲肠短链脂肪酸水平的变化
图43:mrx0029和mrx005诱导的肌动蛋白、绒毛蛋白、闭合蛋白tjp1、tjp2、map2、drd2、gabrb3、syp、pink1、park7和nse的基因表达水平的变化。
图44:由mrx0005和mrx0029诱导的shsy5y细胞分化。(a-c)用鬼笔环肽和map2免疫标记的细胞的代表性图像。(d—f)a-c与dapi图像合并的图像。(g—i)β3微管蛋白免疫标记细胞。(j-l)与dapi图像合并。放大率x630。j-k)mrx0005和mrx0029处理对shsy5y细胞影响的蛋白质印迹分析。蛋白质印迹膜用针对map2(m)和b3微管蛋白(n)的抗体探测。肌动蛋白用作上样对照。下图:六个独立实验中一个的代表性印迹;上图:相对光密度强度。
具体实施方式
细菌菌株
本发明的组合物包含副拟杆菌属的细菌菌株。实施例证明此属的细菌可用于治疗或预防神经退行性障碍。优选的细菌菌株是狄氏副拟杆菌菌种。
用于本发明的副拟杆菌菌种的实例包括狄氏副拟杆菌、古氏副拟杆菌(parabacteroidesgoldsteinii)、粪副拟杆菌(parabacteroidesmerdae)和约氏副拟杆菌(parabacteroidesjohnsonii)。副拟杆菌类似于拟杆菌,并且是革兰氏阴性、专性厌氧、非孢子形成、无运动性且棒状的,并且大小为0.8–1.6×1.2–12μm。狄氏副拟杆菌是人粪便中最常见的菌种之一。狄氏副拟杆菌的菌株类型是jcm5825t(=ccug4941t=dsm20701t=atcc8503t)。狄氏副拟杆菌菌株jcm5825t、jcm13400、jcm13401、jcm13402、jcm13403和jcm13404以及粪副拟杆菌菌株jcm9497t和jcm13405的16srrna基因序列的genbank/embl/ddbj登录号分别是ab238922–ab238929(在本文中公开为seqidno:1-8)。示例性菌株还描述于[22]中。
在实施例中测试了以登录号ncimb42382保藏的狄氏副拟杆菌,并且在本文中也称为菌株755或mrx0005。seqidno:9中提供了所测试的755菌株的16srrna序列。菌株755在2015年3月12日以“副拟杆菌属755”由gtbiologics有限公司(lifesciencesinnovationbuilding,aberdeen,ab252zs,苏格兰)保藏于国际保藏机构ncimb有限公司(fergusonbuilding,aberdeen,ab219ya,苏格兰)并指定登录号为ncimb42382。gtbiologics有限公司随后更名为4dpharmaresearch有限公司。
wo2016/203220描述了将菌株755施用于小鼠,并且显示它可以影响肠道外部的疾病过程(诸如哮喘和关节炎)。菌株755还影响肠道外部的疾病过程以治疗本文所述的神经退行性障碍。
菌株755的基因组序列提供在seqidno:10中。使用pacbiorsii平台生成此序列。
还预期与实施例中测试的菌株紧密相关的细菌菌株有效治疗或预防神经退行性障碍。在某些实施方案中,用于本发明的细菌菌株具有与狄氏副拟杆菌的细菌菌株的16srrna序列具有至少95%、96%、97%、98%、99%、99.5%或99.9%同一性的16srrna序列。优选地,用于本发明的细菌菌株具有与seqidno:1、2、3、4、5、6、7、8或9具有至少95%、96%、97%、98%、99%、99.5%或99.9%同一性的16srrna序列。优选地,序列同一性是针对seqidno:9。优选地,用于本发明的细菌菌株具有由seqidno:9表示的16srrna序列。
还预期作为以登录号42382保藏的细菌的生物型的细菌菌株有效治疗或预防神经退行性障碍。生物型是具有相同或非常相似的生理和生物化学特征的紧密相关的菌株。
作为以登录号ncimb42382保藏的细菌的生物型并且适用于本发明的菌株可以通过对以登录号ncimb42382保藏的细菌的其他核苷酸序列进行测序来鉴定。例如,基本上可以对全基因组进行测序,并且用于本发明的生物型菌株可以具有跨其全基因组的至少80%(例如,跨至少85%、90%、95%或99%,或跨其全基因组)的至少95%、96%、97%、98%、99%、99.5%或99.9%序列同一性。用于鉴定生物型菌株的其他合适的序列可包括hsp60或重复序列,诸如box、eric、(gtg)5或rep或[23]。生物型菌株可以具有与以登录号ncimb42382保藏的细菌的对应序列具有至少95%、96%、97%、98%、99%、99.5%或99.9%序列同一性的序列。
在某些实施方案中,用于本发明的细菌菌株具有与seqidno:10具有序列同一性的基因组。在优选的实施方案中,用于本发明的细菌菌株具有跨seqidno:10的至少60%(例如,至少65%、70%、75%、80%、85%、95%、96%、97%、98%、99%或100%)与seqidno:10具有至少90%序列同一性(例如,至少92%、94%、95%、96%、97%、98%、99%或100%序列同一性)的基因组。例如,用于本发明的细菌菌株可以具有基因组,所述基因组跨seqidno:10的70%与seqidno:10具有至少90%序列同一性,或者跨seqidno:10的80%与seqidno:10具有至少90%序列同一性,或者跨seqidno:10的90%与seqidno:10具有至少90%序列同一性,或者跨seqidno:10的100%与seqidno:10具有至少90%序列同一性,或者seqidno:10的70%与seqidno:10具有至少95%序列同一性,或者跨seqidno:10的80%与seqidno:10具有至少95%序列同一性,或者跨seqidno:10的90%与seqidno:10具有至少95%序列同一性,或者跨seqidno:10的100%与seqidno:10具有至少95%序列同一性,或者跨seqidno:10的70%与seqidno:10具有至少98%序列同一性,或者跨seqidno:10的80%与seqidno:10具有至少98%序列同一性,或者跨seqidno:10的90%与seqidno:10具有至少98%序列同一性,或者跨seqidno:10的100%与seqidno:10具有至少98%序列同一性。
可替代地,可以通过使用登录号ncimb42382保藏物和限制性片段分析和/或pcr分析,例如通过使用荧光扩增片段长度多态性(faflp)和重复dna元件(rep)-pcr指纹分析或蛋白质分析或部分16s或23srdna测序,来鉴定作为以登录号ncimb42382保藏的细菌的生物型并适用于本发明的菌株。在优选的实施方案中,此类技术可以用于鉴定其他狄氏副拟杆菌菌株。
在某些实施方案中,作为以登录号ncimb42382保藏的细菌的生物型并且适用于本发明的菌株是当通过扩增核糖体dna限制性分析(ardra),例如当使用sau3ai限制性酶(例如参见例如[24]的方法和指导)分析时提供与以保藏号ncimb42382保藏的细菌相同的模式的菌株。可替代地,生物型菌株被鉴定为与以保藏号ncimb42382保藏的细菌具有相同的碳水化合物发酵模式的菌株。
可用于本发明的组合物和方法的其他副拟杆菌菌株(诸如以登录号ncimb42382保藏的细菌的生物型)可以使用任何适当的方法或策略(包括实施例中所述的测定)来鉴定。例如,可以通过与神经母细胞瘤细胞一起培养,然后评定细胞因子水平和神经保护或神经增殖水平来鉴定用于本发明的菌株。具体地,与以登录号ncimb42382保藏的细菌具有相似的生长模式、代谢类型和/或表面抗原的细菌菌株可以用于本发明。可用的菌株与ncimb42382菌株具有相当的免疫调节活性。具体地,与实施例中显示的作用相比,生物型菌株将在神经退行性疾病模型上引起相当的作用,并且在细胞因子水平上引起相当的作用,这可以通过使用实施例中描述的培养和施用方案来鉴定。
本发明的特别优选的菌株是以登录号ncimb42382保藏的狄氏副拟杆菌菌株。这是在实施例中测试的示例性755菌株,并且显示出对治疗疾病有效。因此,本发明提供了一种以登录号ncimb42382保藏的狄氏副拟杆菌菌株或其衍生物的细胞诸如分离的细胞。本发明还提供了一种组合物,其包含以登录号ncimb42382保藏的狄氏副拟杆菌菌株或其衍生物的细胞。本发明还提供了一种以登录号ncimb42382保藏的狄氏副拟杆菌菌株的生物学纯培养物。本发明还提供了一种以登录号ncimb42382保藏的狄氏副拟杆菌菌株或其衍生物的细胞,其用于治疗,特别是用于本文所述疾病的治疗。
以登录号ncimb42382保藏的菌株的衍生物可以是子代菌株(后代)或从原体培养的菌株(亚克隆)。本发明的菌株的衍生物可以在不损失生物活性的情况下例如在基因水平下进行修饰。具体地,本发明的衍生物菌株是治疗学上有效的。衍生物菌株与原始ncimb42382菌株具有相当的免疫调节活性。具体地,与实施例中显示的作用相比,衍生物菌株将在神经退行性疾病模型上引起相当的作用,并且在细胞因子水平上引起相当的作用,这可以通过使用实施例中描述的培养和施用方案来鉴定。ncimb42382菌株的衍生物通常是ncimb42382菌株的生物型。
对以登录号ncimb42382保藏的狄氏副拟杆菌的细胞的引用涵盖与以登录号ncimb42382保藏的菌株具有相同的安全性和治疗功效特征的任何细胞,并且本发明涵盖此类细胞。
在优选的实施方案中,本发明的组合物中的细菌菌株是可存活的并且能够部分地或完全地在肠定居。
发明人已发现,狄氏副拟杆菌菌株减少促炎细胞因子诸如il-6和il-8的分泌。il-8与髓鞘形成有关。il-6诱导的慢性炎症最终会导致细胞死亡。因此,本发明的细菌菌株在治疗或预防神经退行性障碍中是特别有用的。在一些实施方案中,细菌菌株可用于治疗以il-6活化增强为特征的病状。在一些实施方案中,本发明的组合物用于治疗或预防以脱髓鞘为特征的神经退行性疾病。许多神经退行性疾病以脱髓鞘为特征。脱髓鞘阻碍神经元内动作电位的传播,从而损害神经系统内的有效通信。il-8已被证明能对髓鞘形成和修复具有积极作用。mrx0029本身增加il-8的分泌。因此,本发明的组合物特别有益于治疗或预防以脱髓鞘为特征的神经退行性障碍。
发明人还发现本发明的细菌菌株增加了bdnf的活化。bdnf是一种神经营养生长因子,其已被证明能增强神经元的分化和存活。因此,本发明的组合物可以用于增强神经细胞存活以治疗或预防神经退行性疾病的方法中。
可以用于本发明的组合物中的另一种细菌是马氏巨球菌(megasphaeramassiliensis)菌种。实施例证明,狄氏副拟杆菌和马氏巨球菌都具有神经保护活性,但是产生不同的代谢物,并且可能具有不同的作用机制和特定的神经保护活性。因此,这些菌种在组合使用时可以是特别有效的。在优选的实施方案中,所述组合物包含狄氏副拟杆菌菌种的菌株和马氏巨球菌菌种的菌株。
在实施例中测试了以登录号ncimb42382保藏的狄氏副拟杆菌,并且在本文中也称为菌株mrx0005。mrx0005、mrx005、mrx005和mrx0005在本文中可互换使用。seqidno:9中提供了所测试的mrx0005菌株的16srrna序列。菌株mrx0005在2015年3月12日以“副拟杆菌属755”由gtbiologics有限公司(lifesciencesinnovationbuilding,aberdeen,ab252zs,苏格兰)保藏于国际保藏机构ncimb有限公司(fergusonbuilding,aberdeen,ab219ya,苏格兰)并指定登录号为ncimb42382。gtbiologics有限公司随后更名为4dpharmaresearch有限公司。
以登录号ncimb42787保藏的马氏巨球菌菌株是在实施例中测试的示例性mrx0029菌株,并且显示有效治疗疾病。菌株ncimb42787在2017年7月13日以“马氏巨球菌mrx0029”由4dpharmaresearch有限公司(lifesciencesinnovationbuilding,aberdeen,ab252zs,苏格兰)保藏于国际保藏机构ncimb有限公司(fergusonbuilding,aberdeen,ab219ya,苏格兰)并指定登录号为ncimb42787。因此,本发明提供了一种以登录号ncimb42787保藏的马氏巨球菌菌株或其衍生物的细胞诸如分离的细胞。本发明还提供了一种组合物,其包含以登录号ncimb42787保藏的马氏巨球菌菌株或其衍生物的细胞。本发明还提供了一种以登录号ncimb42787保藏的马氏巨球菌菌株的生物学纯培养物。本发明还提供了一种以登录号ncimb42787保藏的马氏巨球菌菌株或其衍生物的细胞,其用于治疗,特别是用于本文所述疾病的治疗。
在一些实施方案中,本发明提供了一种组合物,其包含以登录号ncimb42787保藏在ncimb的菌株,或其衍生物或生物型,以及以登录号ncimb42382保藏在ncimb的菌株,或其衍生物或生物型,其优选地用于治疗,优选地用于治疗神经退行性疾病,诸如帕金森氏病。
治疗性用途
如实施例证明,本发明的细菌组合物有效地治疗神经退行性障碍。具体地,用本发明的组合物进行的治疗增加了神经增殖并且对破坏多巴胺能神经元的药剂起神经保护剂作用。因此,本发明的组合物可以用于治疗或预防由神经元死亡引起的神经退行性障碍。
本发明的组合物可以减少nfκb启动子的活化,nfκb启动子的活化引起细胞因子产生,例如il-1β、il-1α、il-18、tnfα和il-6。用突变体α-突触核蛋白处理细胞是家族性帕金森氏病的模型。在53位的从腺嘌呤到苏氨酸的点突变导致α-突触核蛋白错误折叠。不正确折叠的α-突触核蛋白随后聚集成不溶性原纤维,其形成路易体。因此,本发明的组合物可以用于治疗或预防由神经发炎、蛋白质错误折叠和/或环境暴露引起的神经退行性障碍。本发明的组合物可以用于治疗家族性帕金森氏病。nfκb启动子的活化是通过tlr4配体介导的。已知tl4在模拟帕金森氏病的小鼠模型mptp中介导细胞死亡。本发明的组合物可以用于抑制tlr4信号传导活化nfκb启动子的能力。与pd特别相关的是,pd患者的大脑中tlr2和tlr4均被上调[25]。此外,已将α-突触核蛋白描述为tlr2的配体[26],并且我们已经证明,α-突触核蛋白使用hek-tlr4细胞也作为tlr4的配体。
本发明的组合物减少了可以由脂多糖(lps)诱导的促炎细胞因子诸如il-6的分泌。用lps处理细胞可以模拟环境因素引起的帕金森氏病。本发明的组合物可以用于减少il-6分泌。本发明的组合物可以用于治疗环境帕金森氏病。
除它们的白细胞的定向迁移的基本作用之外,假设趋化因子在中枢神经系统(cns)中具有重要功能。在鼠少突胶质细胞前体样细胞系中,趋化因子mcp-1不增加少突胶质细胞前体增殖。在原代髓鞘培养物中,mcp-1不增强此系统中的髓鞘片断形成。发明人已发现mrx0005提升mcp-1水平。在某些实施方案中,本发明的组合物用于增加mcp-1水平以治疗疾病。
用本发明的组合物治疗的神经退行性疾病的实例包括:帕金森氏病,包括进行性核上性麻痹、进行性核上性麻痹、steele-richardson-olszewski综合征、正常压力脑积水、血管或动脉硬化性帕金森病和药物诱发的帕金森病;阿尔茨海默氏病,包括本森氏综合症(benson'ssyndrome);多发性硬化症;亨廷顿氏病;肌萎缩性侧索硬化症;卢·格里格病(lougehrig'sdisease);运动神经元疾病;朊病毒病;脊髓小脑共济失调;脊髓性肌萎缩;痴呆,包括路易体、血管和额颞痴呆;原发性进行性失语;轻度认知损害;hiv相关的认知损害和皮质基底节变性。用本发明的组合物治疗的其他神经退行性疾病是进行性炎性神经病。
在某些实施方案中,本发明的组合物可以有效治疗在年长患者中发生的神经退行性障碍。实施例显示,本发明的组合物可以治疗主要在年龄超过65岁的患者中诊断出的帕金森氏病。在优选的实施方案中,本发明的组合物用于治疗65岁或更年长的患者。在其他某些实施方案中,患者年龄在40岁至65岁之间。在其他实施方案中,患者年龄大于40岁。在某些实施方案中,本发明的组合物用于治疗与老龄有关的疾病,例如50岁年龄之后诊断出的疾病。
在某些实施方案中,本发明的组合物用于治疗由蛋白质(特别是错误折叠蛋白)的积累介导或表征的神经退行性障碍。
在某些实施方案中,本发明的组合物用于治疗与灰质神经元损失有关的神经退行性障碍。在某些实施方案中,本发明的组合物用于治疗不与白质损伤有关的神经退行性障碍。
在某些实施方案中,本发明的组合物用于治疗与永久性症状有关的神经退行性障碍。
在某些实施方案中,本发明的组合物用于治疗不是自身免疫病症的神经退行性障碍。在某些实施方案中,本发明的组合物用于治疗不是多发性硬化症的神经退行性障碍。
在某些实施方案中,本发明的组合物用于减少神经元死亡,特别是用于治疗神经退行性障碍。在某些实施方案中,本发明的组合物用于保护神经元,特别是用于治疗神经退行性障碍。
如实施例所示,本发明的组合物的神经保护特效意味着所述组合物对于预防或延迟神经退行性障碍的发作或进展可以是特别有效的。在某些实施方案中,本发明的组合物用于延迟神经退行性障碍的发作或进展。
本发明的组合物可以增加il-8的分泌。il-8已被证明能在神经元髓鞘形成中起作用。在一些实施方案中,本发明的组合物可以用于增加il-8分泌。
本发明的治疗组合物可以增加bdnf的活化。bdnf作用于中枢神经系统的某些神经元,以支持现有神经元的存活并帮助新神经元和突触的生长和发育。bdnf在海马、皮层和基底前脑中具有活性,并对于长期记忆是重要的。因此,本发明的组合物可以用于增加bdnf的分泌。因此,所述组合物可以用于治疗与长期记忆障碍有关的神经退行性疾病。本发明的组合物可以用于改善长期记忆,特别是用于改善被神经退行性疾病损害的长期记忆。
在某些实施方案中,本发明的组合物增加神经元细胞中的线粒体代谢活性。
微生物群-肠-脑轴的调节
肠道与大脑之间的通信(微生物群-肠-脑轴)通过双向神经体液通信系统进行。最近的证据显示,存在于肠道中的微生物群可以通过微生物群-肠-脑轴来调节大脑发育并产生行为表型。实际上,许多综述表明,微生物群-肠-脑轴在维持中枢神经系统功能中的作用,并暗示微生物群-肠-脑轴在中枢神经系统障碍和病状的发展中的功能障碍[16-27]。
大脑与肠道之间的双向通信(即,肠-脑轴)包括中枢神经系统、神经内分泌和神经免疫系统,包括下丘脑-垂体-肾上腺(hpa)轴,自主神经系统(ans)的交感和副交感臂,包括肠神经系统(ens)和迷走神经,以及肠道微生物群。
如实施例所证明,本发明的组合物可以调节微生物群-肠-脑轴并减少与神经退行性障碍有关的细胞死亡。因此,本发明的组合物可以用于治疗或预防神经退行性障碍,特别是与微生物群-肠-脑轴的功能障碍有关的那些障碍和病状。
在特定实施方案中,本发明的组合物可以用于治疗或预防选自由以下组成的组的疾病或病状:帕金森氏病,包括进行性核上性麻痹、进行性核上性麻痹、steele-richardson-olszewski综合征、正常压力脑积水、血管或动脉硬化性帕金森病和药物诱发的帕金森病;阿尔茨海默氏病,包括本森氏综合症(benson'ssyndrome);多发性硬化症;亨廷顿氏病;肌萎缩性侧索硬化症;卢·格里格病(lougehrig'sdisease);运动神经元疾病;朊病毒病;脊髓小脑共济失调;脊髓性肌萎缩;痴呆;包括路易体;血管和额颞痴呆;原发性进行性失语;轻度认知损害;hiv相关的认知损害和皮质基底节变性。
本发明的组合物可以特别用于治疗或预防慢性疾病,治疗或预防对其他疗法(诸如利用左旋多巴、多巴胺激动剂、mao-b抑制剂、comt抑制剂、谷氨酸拮抗剂、和/或抗胆碱药物治疗)无反应的患者的疾病,和/或治疗或预防与微生物群-肠-脑轴的功能障碍有关的组织损伤和症状。
在某些实施方案中,本发明的组合物调节cns。在一些实施方案中,本发明的组合物调节自主神经系统(ans)。在一些实施方案中,本发明的组合物调节肠神经系统(ens)。在一些实施方案中,本发明的组合物调节下丘脑、垂体、肾上腺(hpa)轴。在一些实施方案中,本发明的组合物调节神经内分泌途径。在一些实施方案中,本发明的组合物调节神经免疫途径。在一些实施方案中,本发明的组合物调节cns、ans、ens、hpa轴和/或神经内分泌和神经免疫途径。在某些实施方案中,本发明的组合物调节受试者的共生代谢物的水平和/或胃肠通透性。在某些实施方案中,本发明的组合物可以用于调节多巴胺能系统。
微生物群-肠-脑轴的信号传导由神经系统调节。因此,在一些实施方案中,本发明的组合物调节神经系统中的信号传导。在某些实施方案中,本发明的组合物调节中枢神经系统的信号传导。在一些实施方案中,本发明的组合物调节感觉神经元中的信号传导。在其他实施方案中,本发明的组合物调节运动神经元中的信号传导。在一些实施方案中,本发明的组合物调节ans中的信号传导。在一些实施方案中,ans是副交感神经系统。在优选的实施方案中,本发明的组合物调节迷走神经的信号传导。在其他实施方案中,ans是交感神经系统。在其他实施方案中,本发明的组合物调节肠神经系统中的信号传导。在某些实施方案中,ans和ens神经元的信号传导直接响应于胃肠道的腔内容物。在其他实施方案中,ans和ens神经元的信号传导间接响应于由腔细菌产生的神经化学物质。在其他实施方案中,ans和ens神经元的信号传导响应于由腔细菌或肠内分泌细胞产生的神经化学物质。在某些优选的实施方案中,ens的神经元活化影响cns功能的迷走神经传入。在一些实施方案中,本发明的组合物调控肠嗜铬细胞的活性。
神经退行性疾病
tau蛋白病是与tau蛋白在人脑中神经原纤维或胶质原纤维缠结中的病理性聚集有关的神经退行性疾病。阿尔茨海默氏病是tau蛋白病变的实例。突触核蛋白病(也称为α-突触核蛋白病)是特征在于α-突触核蛋白的聚集体在神经元、神经纤维或神经胶质细胞中的异常积累的神经退行性疾病。帕金森氏病是突触核蛋白病的实例。
这两种病理学之间存在临床和病理重叠。帕金森氏病患者常常患有痴呆,并且阿尔茨海默氏病患者经常表现出帕金森病[28]。例如,进行性核上性麻痹(还称为steele-richardson-olszewski综合征)具有tau蛋白病变,但是也导致明显的帕金森病[29]。已知导致帕金森病的lrrk2中的突变与突触核蛋白、tau蛋白或两种蛋白质的积累有关[30]。
路易体病(lbd)是一种神经退行性疾病,其为老年人中的痴呆的最常见病因之一。lbd例证了tau蛋白病变与突触核蛋白病变之间存在连续性。lbd与帕金森氏病、帕金森氏病痴呆和阿尔茨海默氏病共享临床和病理特征[28]。
在特定实施方案中,本发明的组合物可以用于治疗或预防tau蛋白病和/或突触核蛋白病。在特定实施方案中,本发明的组合物可以用于治疗或预防tau蛋白病。在特定实施方案中,本发明的组合物可以用于治疗或预防突触核蛋白病。在某些实施方案中,本发明的组合物可以用于治疗或预防选自由以下组成的组的疾病或病状:帕金森氏病,包括进行性核上性麻痹、进行性核上性麻痹、steele-richardson-olszewski综合征、正常压力脑积水、血管或动脉硬化性帕金森病和药物诱发的帕金森病;阿尔茨海默氏病,包括本森氏综合症(benson'ssyndrome);以及痴呆;包括路易体;血管和额颞痴呆。
在优选的实施方案中,本发明的组合物可以用于治疗或预防帕金森氏病,包括进行性核上性麻痹、进行性核上性麻痹、steele-richardson-olszewski综合征、正常压力脑积水、血管或动脉硬化性帕金森病和药物诱发的帕金森病。在优选的实施方案中,本发明的组合物可以用于治疗或预防阿尔茨海默氏病,包括本森氏综合症。在另外优选的实施方案中,本发明的组合物可以用于治疗或预防痴呆;包括路易体;血管和额颞痴呆。
帕金森氏病
帕金森氏病是一种常见的神经退行性疾病,其在神经病理学上特征是神经细胞(产生多巴胺的细胞)的异质性群体的变性。帕金森氏病的临床诊断需要运动迟缓和以下至少一种核心症状:静息性震颤;肌肉僵硬和姿势反射障碍。在疾病进展过程中可能出现或发展的其他体征和症状是自主神经障碍(流涎、皮脂溢、便秘、排尿障碍、性功能、体位性低血压、多汗症)、睡眠障碍以及嗅觉或温度感觉的障碍。帕金森氏病是一种神经退行性疾病,其可能由于微生物群-肠-脑轴的功能障碍而发展或持续。因此,在优选的实施方案中,本发明的组合物用于治疗或预防受试者的帕金森氏病。
在另外优选的实施方案中,本发明提供了一种包含副拟杆菌属的细菌菌株的组合物,其用于治疗或预防帕金森氏病的方法。包含副拟杆菌属的细菌菌株的组合物可以改善帕金森氏病模型中的运动和认知功能。用副拟杆菌菌株进行的治疗可以调节中枢、自主神经和肠神经系统中的信号传导;可以调节hpa轴途径的活性;可以调节神经内分泌和/或神经免疫途径;并可以调节受试者的共生代谢物、炎症标记物和/或胃肠道通透性的水平,所有这些都与帕金森氏病的神经病理学有关。在优选的实施方案中,本发明提供了一种包含狄氏副拟杆菌菌种的细菌菌株的组合物,其用于治疗或预防帕金森氏病的方法。使用狄氏副拟杆菌的组合物对治疗帕金森氏病可以是特别有效的。
在优选的实施方案中,本发明的组合物预防、减少或减轻受试者中帕金森氏病的一种或多种症状。在优选的实施方案中,本发明的组合物预防、减少或减轻受试者中帕金森氏病的一种或多种核心症状。在某些实施方案中,本发明的组合物预防、减少或减轻受试者的运动迟缓。在某些实施方案中,本发明的组合物预防、减少或减轻受试者的静息性震颤;肌肉僵硬和/或姿势反射障碍。在某些实施方案中,本发明的组合物预防、减少或减轻与帕金森氏病进展有关的一种或多种症状,所述症状选自自主神经障碍(流涎、皮脂溢、便秘、排尿障碍、性功能、体位性低血压、多汗症)、睡眠障碍以及嗅觉或温度感觉的障碍。
在优选的实施方案中,本发明的组合物预防、减少或减轻与帕金森氏病并存的抑郁症状。在某些实施方案中,本发明的组合物改善了言语记忆和/或执行功能。在某些实施方案中,本发明的组合物改善注意力、工作记忆、言语流畅性和/或焦虑感。
在其他优选的实施方案中,本发明的组合物预防、减少或减轻与帕金森氏病并存的认知功能障碍。
在某些实施方案中,本发明的组合物预防、减少或减轻帕金森氏病的进展。在某些实施方案中,本发明的组合物预防、减少或减轻后期的运动并发症。在某些实施方案中,本发明的组合物预防、减少或减轻后期的运动波动。在某些实施方案中,本发明的组合物预防、减少或减轻神经元损失。在某些实施方案中,本发明的组合物改善帕金森氏病痴呆(pdd)的症状。在某些实施方案中,本发明的组合物预防、减少或减轻执行功能、注意力和/或工作记忆的障碍。在某些实施方案中,本发明的组合物改善多巴胺能神经传递。在某些实施方案中,本发明的组合物预防、减少或减轻受损的多巴胺能神经传递。
在一些实施方案中,根据症状或诊断量表,本发明的组合物改善帕金森氏病的症状。在某些实施方案中,用于评定帕金森氏病的运动功能的症状改善的测试是统一帕金森氏病评分量表。具体地,updrsii考虑了日常生活活动,并且updrsiii考虑了运动检查。
在一些实施方案中,根据症状或诊断测试和/或量表,本发明的组合物改善与pdd有关的症状。在某些实施方案中,所述测试或量表选自霍普金斯语言学习测试-修订版(hvlt-r);delis-kaplan执行功能系统(d-kefs)色词干扰测试;汉密尔顿抑郁评分量表(ham-d17;抑郁);汉密尔顿焦虑评分量表(ham-a;焦虑)和统一帕金森氏病评分量表(updrs;pd症状严重程度)。
在一些实施方案中,本发明的组合物改善了用于评定精神障碍和神经障碍的临床总体印象–总体改善(cgi-i)量表。在一些实施方案中,本发明的组合物对患有帕金森氏病的受试者的整体社交和职业损伤显示出积极作用。
阿尔茨海默氏病和痴呆
在dsm-5中,将术语痴呆用术语严重神经认知障碍和轻度神经认知障碍替换。神经认知障碍是异质类的精神疾病。最常见的神经认知障碍是阿尔茨海默氏病,其次是血管性痴呆或两者的混合形式。其他形式的神经退行性障碍(例如,路易体病、额颞痴呆、帕金森氏痴呆、克-雅病(creutzfeldt-jakobdisease)、亨廷顿氏病和韦-柯二氏综合征(wernicke-korsakoffsyndrome))伴有痴呆。
阿尔茨海默氏病和痴呆还以神经元损失为特征,因此,本发明组合物的实施例中所示的神经保护作用和神经增殖作用表明它们可以用于治疗或预防这些病状。
在dsm-5下的痴呆症状标准是在一个或多个选自以下的认知领域中认知从先前的表现水平明显下降的证据:学习和记忆;语言;执行功能;复杂的注意力;知觉运动和社会认知。认知缺陷一定会干扰日常活动的独立性。此外,认知缺陷并非仅在谵妄的情况下发生,也不能通过另一种精神障碍(例如mdd或精神分裂症)更好地解释。
除了主要症状外,患有神经退行性障碍的受试者还表现出行为和精神症状,包括躁动、攻击、抑郁、焦虑、冷漠、精神病和睡眠-觉醒周期紊乱。
神经退行性障碍可能由于微生物群-肠-脑轴的功能障碍而发展或持续。因此,在优选的实施方案中,本发明的组合物用于治疗或预防受试者的神经退行性障碍。在优选的实施方案中,神经退行性障碍是阿尔茨海默氏病。在其他实施方案中,所述神经退行性障碍选自血管性痴呆;混合型阿尔茨海默氏病和血管性痴呆;路易体病;额颞痴呆;帕金森氏痴呆;克-雅病;亨廷顿氏病;和韦-柯二氏综合征。
在优选的实施方案中,本发明的组合物预防、减少或减轻受试者的神经退行性障碍的一种或多种症状。在某些实施方案中,本发明的组合物预防、减少或减轻受试者认知功能减退的发生。在某些实施方案中,本发明的组合物在一个或多个选自以下的认知领域中改善患有神经退行性障碍的受试者的表现水平:学习和记忆;语言;执行功能;复杂的注意力;知觉运动和社会认知。在一些实施方案中,本发明的组合物预防、减少或减轻与选自以下的神经退行性障碍有关的一种或多种行为和精神症状的发生:躁动、攻击、抑郁、焦虑、冷漠、精神病和睡眠-觉醒周期紊乱。
在某些实施方案中,本发明的组合物通过在临床前阶段干预可疑的致病机制来预防、减少或减轻症状性疾病。在某些实施方案中,本发明的组合物通过减慢或停止症状进展来改善疾病纠正。在一些实施方案中,症状进展的减慢或停止与延迟潜在的神经病理学过程的证据相关。在优选的实施方案中,本发明的组合物改善神经退行性障碍的症状,包括增强的认知和功能改善。在优选的实施方案中,本发明的组合物改善痴呆的行为和精神症状(bpsd)。在优选的实施方案中,本发明的组合物改善患有神经退行性障碍的受试者进行日常活动的能力。
在优选的实施方案中,本发明的组合物改善患有阿尔茨海默氏病的受试者的认知和功能二者。在一些实施方案中,本发明的组合物改善患有阿尔茨海默氏病的受试者的认知终点。在一些实施方案中,本发明的组合物改善患有阿尔茨海默氏病的受试者的功能终点。在优选的实施方案中,本发明的组合物改善患有阿尔茨海默氏病的受试者的认知终点和功能终点。在另外的优选实施方案中,本发明的组合物改善患有阿尔茨海默氏病的受试者的总体临床反应(整体终点)。
在一些实施方案中,根据症状或诊断测试,本发明的组合物改善神经退行性障碍的症状。在某些实施方案中,用于评定阿尔茨海默氏病(和其他神经退行性障碍)的症状改善的测试选自客观认知、日常生活活动、变化的总体评定、健康相关的生活质量测试以及评定神经退行性障碍的行为和精神症状的测试。
在某些实施方案中,用于评定症状改善的客观认知测试使用阿尔茨海默氏病评定量表认知子量表(adas-cog)和经典adas量表。在某些实施方案中,使用用于阿尔茨海默氏病的神经生理学测试组合(ntb)评定认知的症状改善。
在一些实施方案中,变化的总体评定测试使用临床总体印象–总体改善(cgi-i)量表来评定精神障碍和神经障碍。在一些实施方案中,总体量表是临床医生基于面试的变化印象加(cibic-plus)。在一些实施方案中,总体量表是阿尔茨海默氏病合作研究单位临床医生的总体变化印象(adcs-cgic)。
在某些实施方案中,健康相关的生活质量量度是阿尔茨海默氏病相关的qol(adrql)和qol-阿尔茨海默氏病(qol-ad)。
在某些实施方案中,评定神经退行性障碍的行为和精神症状的测试选自以下中的行为病理学:阿尔茨海默氏病评分量表(behave-ad);痴呆的行为评分量表(brsd);神经精神病学调查表(npi);以及cohen-mansfield激越调查表(cmai)。
在一些实施方案中,本发明的组合物在与另一种用于治疗神经退行性障碍的疗法组合使用时,在预防、减少或减轻神经退行性障碍方面是特别有效的。在某些实施方案中,此类疗法包括乙酰胆碱酯酶抑制剂,包括多奈哌齐
多发性硬化症
多发性硬化症(ms)是一种脱髓鞘疾病,其中大脑和脊髓中神经元周围的髓鞘受到破坏。ms的确切根本原因尚不清楚,但认为因人而异。某些形式的ms是遗传的。环境因素也被认为是ms的原因。在一些个体中,遗传因素和环境因素二者的组合可能会触发ms的发作。
与ms相关的症状多种多样。受试者可能表现出几乎任何与自主神经、视觉、运动或感觉控制障碍有关的神经系统症状。确切的症状将根据神经元损伤/脱髓鞘的部位而变化。
il-8与髓鞘的形成有关。因此,本发明的组合物可以用于患有ms的受试者的神经元的髓鞘再生。本发明的组合物还可以用于保护神经元免于脱髓鞘。换句话说,本发明的组合物可以用于通过恢复或预防神经元髓鞘的损失来治疗或预防多发性硬化症的方法。
在一些实施方案中,本发明的组合物预防、减少或减轻受试者中ms的一种或多种症状。在一些实施方案中,本发明的组合物预防、减少或减轻受试者的疲劳。在某些实施方案中,本发明的组合物预防、减少或减轻受试者的静息性震颤、肌肉无力、肌肉痉挛、肌肉僵硬、感觉异常和/或共济失调。在某些实施方案中,本发明的组合物预防、减少或减轻与ms进展有关的一种或多种症状,所述症状选自由以下组成的列表:自主神经障碍:便秘、排尿障碍、性功能、吞咽困难、构音困难、晕厥、眩晕和/或头晕;睡眠障碍;以及嗅觉或温度感觉的障碍。在一些实施方案中,本发明的组合物预防、减少或减轻与ms有关的一种或多种眼部症状。在一些实施方案中,眼部症状选自由以下组成的列表:受试者的视力丧失、眼痛、色盲、复视和/或不自主的眼球运动。
在一些实施方案中,本发明的组合物预防、减少或减轻头晕、眩晕、神经性疼痛、肌肉骨骼疼痛、认知功能障碍、大便失禁、吞咽困难、构音困难或其任何组合。
在一些实施方案中,本发明的组合物预防、减少或减轻与ms并存的抑郁症状或焦虑症。
在一些实施方案中,使用2017年诊断ms的mcdonald准则确定症状改善。
在某些实施方案中,用本发明的组合物进行的治疗引起ms发病率或ms严重性的降低。在某些实施方案中,本发明的组合物用于降低复发率或复发严重性。在某些实施方案中,用本发明的组合物进行的治疗可以预防运动功能下降或引起与ms有关的运动功能的改善。在某些实施方案中,本发明的组合物用于预防运动功能的下降或用于改善运动功能以治疗ms。在某些实施方案中,用本发明的组合物进行的治疗可预防ms中麻痹的发展。在某些实施方案中,本发明的组合物用于预防麻痹以治疗ms。
在某些实施方案中,本发明的组合物用于预防已被鉴定为具有多发性硬化症的风险或已被诊断为患有早期多发性硬化症或“复发-缓解型”多发性硬化症的患者中的多发性硬化症。本发明的组合物可以用于预防ms的发展。本发明的组合物可以用于预防ms的进展。在某些实施方案中,本发明的组合物用于被鉴定为对ms具有遗传倾向性的患者,诸如主要组织相容性复合物(mhc)ii类表型、人白细胞抗原(hla)-dr2或hla-dr4。
本发明的组合物可以用于控制或减轻多发性硬化症。本发明的组合物对于减少与多发性硬化症有关的症状可以是特别有用的。多发性硬化症的治疗或预防可以是指例如症状严重性的减轻或对于患者是问题的触发物的加剧频率或范围的降低。在某些实施方案中,本发明的组合物减慢或停止疾病的进展。
在某些实施方案中,本发明的组合物用于治疗复发-缓解型ms。在替代性实施方案中,本发明的组合物用于治疗进展性ms,诸如继发性进展性ms(spms),其在诊断出rrms后随时间发展;原发性进展性ms(ppms),其表现出逐渐的连续神经系统恶化;和进展性复发ms(prms),其与ppms相似,但具有复发重叠。
在某些实施方案中,本发明的组合物用于治疗一种或多种ms症状,所述ms症状选自由以下组成的组:疲劳、视力问题、麻木、刺痛、肌肉痉挛、肌肉僵硬、肌肉无力、活动性问题、疼痛、思考、学习和计划问题、抑郁和焦虑、性问题、膀胱问题、肠问题、言语和吞咽困难。
神经化学因子、神经肽和神经递质以及微生物群-肠-脑轴
如上所述,微生物群-肠-脑轴由许多不同的生理系统调节。微生物群-肠-脑轴受到许多信号传导分子的调节。这些信号传导分子水平的改变会导致神经退行性疾病。发明人进行的实验表明,施用副拟杆菌菌种,特别是狄氏副拟杆菌,可以调节吲哚和犬尿氨酸的水平。这些代谢物的失调可能导致神经退行性疾病,诸如帕金森氏病。
在某些实施方案中,本发明的组合物调节脑单胺及其代谢物的水平。在优选的实施方案中,代谢物是犬尿氨酸。在某些实施方案中,本发明的组合物调节犬尿氨酸,其是色氨酸代谢的主要途径,所述途径充当烟酰胺腺嘌呤二核苷酸(nad+)产生途径。犬尿氨酸可以代谢为神经活性化合物,诸如犬尿喹啉酸(kyna)和3-羟基-1-犬尿氨酸(3-oh-1-kyn),并在进一步的步骤中代谢为喹啉酸(quin)。犬尿氨酸途径的失调可能导致免疫系统的活化和潜在的神经毒性化合物的积累。犬尿氨酸代谢的改变可能参与帕金森氏病的发展。已证明pd患者的额叶皮层、壳核和黑质致密部中犬尿氨酸水平降低[31]。因此,在某些实施方案中,本发明的组合物用于增加犬尿氨酸的水平以治疗帕金森氏病。
在本发明的某些实施方案中,本发明的组合物可以增加犬尿氨酸的水平。在人多巴胺能神经母细胞瘤细胞系中,增加的犬尿氨酸水平已被证明能在体外减轻mpp+诱导的神经元细胞死亡[32]。在某些实施方案中,犬尿氨酸和犬尿喹啉酸可以活化gi芳基烃受体(ahr)和gpr35受体。ahr受体的活化诱导il-22产生,其可以抑制局部炎症。gpr35的活化诱导三磷酸肌醇的产生和ca2+动员。
在某些实施方案中,本发明的组合物调节吲哚的水平。在优选的实施方案中,代谢物是犬尿氨酸。在某些实施方案中,本发明的组合物调节犬尿氨酸途径,其是色氨酸代谢的主要途径。
微生物群-肠-脑轴的信号传导受神经化学因子、神经肽和神经递质水平的调节。因此,在某些实施方案中,本发明的组合物调节神经化学因子、神经肽和神经递质的水平。因此,在某些优选的实施方案中,本发明的组合物直接改变cns生物化学。
微生物群-肠-脑轴的信号传导受γ-氨基丁酸(gaba)水平的调节。因此,在优选的实施方案中,本发明的组合物调节gaba的水平。gaba是一种抑制性神经递质,其降低神经元兴奋性。在某些实施方案中,本发明的组合物增加了gaba的水平。在某些实施方案中,本发明的组合物降低了gaba的水平。在某些实施方案中,本发明的组合物改变gaba能神经传递。在某些实施方案中,本发明的组合物调节中枢神经系统不同区域中的gaba转录水平。在某些实施方案中,共生来源的gaba穿过血脑屏障并直接影响神经传递。在某些实施方案中,本发明的组合物导致海马、杏仁核和/或蓝斑中gaba的减少。在某些实施方案中,本发明的组合物导致皮质区域中gaba的增加。
免疫应答
微生物群-肠-脑轴的信号传导通过免疫应答和炎性因子及标记物的改变来调节。因此,在某些实施方案中,本发明的组合物可以调节免疫应答。在某些实施方案中,本发明的组合物调节循环神经免疫信号传导分子的全身水平。在某些优选的实施方案中,本发明的组合物调节促炎细胞因子的产生和炎症。在某些实施方案中,本发明的组合物调节炎性状态。在某些实施方案中,本发明的组合物降低il-6的产生和分泌。在某些实施方案中,本发明的组合物降低nfκb启动子的活化。在某些实施方案中,本发明的组合物能够调节通过有效的促炎性内毒素脂多糖(lps)进行的il-6产生的活化。在某些实施方案中,本发明的组合物能够调节通过lps和α-突触核蛋白突变体蛋白诸如a53t进行的nfκb启动子的活化。细胞因子循环水平的增加与各种神经退行性障碍密切相关,包括帕金森氏病、痴呆和阿尔茨海默氏病。在某些实施方案中,本发明的组合物用于降低il-6水平和/或nfκb水平以治疗神经退行性障碍。
在一些实施方案中,本发明的组合物增加il-8的分泌。il-8已被证明能诱导髓鞘形成并恢复或维持有效的神经元通信。因此,在一些实施方案中,本发明的组合物用于诱导髓鞘形成以治疗神经退行性疾病。在一些实施方案中,本发明的组合物用于恢复神经元通信。在一些实施方案中,本发明的组合物用于维持神经元通信。
微生物群-肠-脑轴的信号传导通过共生代谢物的水平调节。因此,在某些实施方案中,本发明的组合物调节微生物群代谢物的全身水平。在某些优选的实施方案中,本发明的组合物调节短链脂肪酸(scfa)的水平。在某些实施方案中,scfa的水平增加或降低。在一些实施方案中,scfa是丁酸(ba)(或丁酸盐)。在一些实施方案中,scfa是丙酸(ppa)。在一些实施方案中,scfa是乙酸。在某些实施方案中,本发明的组合物调节scfa穿过血脑屏障的能力。
组蛋白乙酰化和脱乙酰化是基因表达的重要表观遗传调控因子。组蛋白乙酰化和脱乙酰化的不平衡可能导致细胞凋亡。此类组蛋白乙酰转移酶的失调涉及与年龄相关的神经退行性疾病相关的发病机理,诸如帕金森氏病、亨廷顿氏病、阿尔茨海默氏病、肌萎缩性侧索硬化症和认知功能减退[33]。因此,在某些实施方案中,本发明的组合物可以调节组蛋白脱乙酰酶活性。在某些实施方案中,本发明的组合物可以降低组蛋白脱乙酰酶活性。在某些实施方案中,本发明的组合物可以降低组蛋白乙酰酶活性。
患有神经退行性疾病(包括帕金森氏病、亨廷顿氏病、阿尔茨海默氏病和肌萎缩性侧索硬化症)的患者表现出高水平的脂质过氧化。脂质很容易被活性氧氧化,大脑富含多不饱和脂肪酸。因此,在某些实施方案中,本发明的组合物可以调节脂质过氧化。在某些实施方案中,本发明的组合物可以减少脂质过氧化。减少由活性氧引起的氧化损伤可以用于靶向神经退行性疾病的早期阶段。因此,在某些实施方案中,本发明的组合物用于治疗早期神经变性。同样因此,在某些实施方案中,本发明的组合物用于预防神经退行性障碍的发展。在此类实施方案中,本发明的组合物可以用于已经被鉴定为具有发展神经退行性障碍风险的患者。
微生物群-肠-脑轴的信号传导通过胃肠道通透性水平调节。因此,在一些实施方案中,本发明的组合物改变了胃肠道上皮的完整性。在某些实施方案中,本发明的组合物调节胃肠道的通透性。在某些实施方案中,本发明的组合物调节胃肠道的屏障功能和完整性。在某些实施方案中,本发明的组合物调节胃肠道运动性。在某些实施方案中,本发明的组合物调节共生代谢物和炎性信号传导分子从胃肠道管腔转运到血流中。
微生物群-肠-脑轴的信号传导通过胃肠道中的微生物组组成调节。因此,在某些实施方案中,本发明的组合物调节胃肠道的微生物组组成。在某些实施方案中,本发明的组合物防止微生物组生态失调和相关的毒性代谢物(例如lps)增加。在某些实施方案中,本发明的组合物调节胃肠道中梭菌的水平。在优选的实施方案中,本发明的组合物降低胃肠道中梭菌的水平。在某些实施方案中,本发明的组合物降低空肠弯曲菌的水平。在某些实施方案中,本发明的组合物调节有害厌氧细菌的增殖和由这些细菌产生的神经毒素的产生。在某些实施方案中,本发明的组合物调节乳杆菌和/或双歧杆菌的微生物组水平。在某些实施方案中,本发明的组合物调节萨特氏菌属、普雷沃菌属、瘤胃球菌属和/或产碱杆菌科的微生物组水平。在某些实施方案中,本发明的组合物增加植物乳杆菌和/或布拉酵母菌(saccharomycesboulardii)的水平。
脑损伤
实施例证明,本发明的组合物具有神经保护作用并且具有hdac抑制活性。hdac2是从中风中功能恢复的关键靶标[34],并且hdac抑制可以防止白质损伤[35],因此本发明的组合物可以用于治疗脑损伤。
在某些实施方案中,本发明的组合物用于治疗脑损伤。在一些实施方案中,脑损伤是创伤性脑损伤。在一些实施方案中,脑损伤是获得性脑损伤。在一些实施方案中,本发明的组合物用于治疗由创伤引起的脑损伤。在一些实施方案中,本发明的组合物用于治疗由肿瘤引起的脑损伤。在一些实施方案中,本发明的组合物用于治疗由中风引起的脑损伤。在一些实施方案中,本发明的组合物用于治疗由脑出血引起的脑损伤。在一些实施方案中,本发明的组合物用于治疗由脑炎引起的脑损伤。在一些实施方案中,本发明的组合物用于治疗由脑缺氧引起的脑损伤。在一些实施方案中,本发明的组合物用于治疗由脑缺氧作用引起的脑损伤。
在优选的实施方案中,本发明的组合物用于治疗中风。实施例中显示的效果与中风的治疗特别相关。当流向大脑至少一部分的血液中断时,就会发生中风。如果没有足够的血液供应来为脑组织提供氧气和营养,并从脑组织中清除废物,脑细胞就会迅速开始死亡。中风的症状取决于受血流量不足影响的大脑区域。症状包括麻痹、肌肉麻木或无力、失去平衡、头晕、突然剧烈头痛、语言障碍、记忆力减退、推理能力丧失、突然混乱、视力障碍、昏迷或甚至死亡。中风也称为脑部发作或脑血管意外(cva)。如果在短时间内恢复足够的血流,中风的症状可能很短暂。但是,如果血流量不足持续了很长一段时间,则症状可能是永久的。
在一些实施方案中,中风是脑缺血。当没有足够的血液流向大脑组织以满足代谢需求时,就会导致脑缺血。在一些实施方案中,脑缺血是局灶性脑缺血,即,局限于脑的特定区域。在一些实施方案中,脑缺血是全脑缺血,即,涵盖脑组织的广泛区域。局灶性脑缺血通常在脑血管被部分或完全阻塞,从而减少流向大脑特定区域的血液时才发生。在一些实施方案中,局灶性脑缺血是缺血性中风。在一些实施方案中,缺血性中风是血栓性的,即由血栓或血凝块引起的,其在脑血管中发展并限制或阻塞血流。在一些实施方案中,缺血性中风是血栓性中风。在一些实施方案中,缺血性中风是栓塞性的,即由栓子或行进通过血流并在远离其起源点的位置限制或阻塞血流的未附着的块体引起。在一些实施方案中,缺血性中风是栓塞性中风。全脑缺血通常在流向大脑的血流整体上受阻或减少时才发生。在一些实施方案中,全脑缺血由灌注不足引起,即由于休克引起。在一些实施方案中,全脑缺血是心脏骤停的结果。
在一些实施方案中,被诊断患有脑损伤的受试者患有脑缺血。在一些实施方案中,被诊断患有脑损伤的受试者患有局灶性脑缺血。在一些实施方案中,被诊断患有脑损伤的受试者患有缺血性中风。在一些实施方案中,被诊断患有脑损伤的受试者患有血栓性中风。在一些实施方案中,被诊断患有脑损伤的受试者患有栓塞性中风。在一些实施方案中,被诊断患有脑损伤的受试者患有全脑缺血。在一些实施方案中,被诊断患有脑损伤的受试者患有灌注不足。在一些实施方案中,被诊断患有脑损伤的受试者患有心脏骤停。
在一些实施方案中,本发明的组合物用于治疗脑缺血。在一些实施方案中,本发明的组合物用于治疗局灶性脑缺血。在一些实施方案中,本发明的组合物用于治疗缺血性中风。在一些实施方案中,本发明的组合物用于治疗血栓性中风。在一些实施方案中,本发明的组合物用于治疗栓塞性中风。在一些实施方案中,本发明的组合物用于治疗全脑缺血。在一些实施方案中,本发明的组合物用于治疗灌注不足。
在一些实施方案中,中风是出血性中风。出血性中风是由脑内或周围出血,导致肿胀、压力以及对脑细胞和组织的损伤而引起的。出血性中风通常是弱化血管破裂并渗入周围脑部的结果。在一些实施方案中,出血性中风是脑出血,即由脑组织本身内的出血引起。在一些实施方案中,脑出血是由脑实质出血引起的。在一些实施方案中,脑出血是由脑室出血引起的。在一些实施方案中,出血性中风是蛛网膜下腔出血,即发生在脑组织外部但仍在颅骨内的出血。在一些实施方案中,出血性中风是脑淀粉样血管病的结果。在一些实施方案中,出血性中风是脑动脉瘤的结果。在一些实施方案中,出血性中风是脑动静脉畸形(avm)的结果。
在一些实施方案中,被诊断患有脑损伤的受试者患有出血性中风。在一些实施方案中,被诊断患有脑损伤的受试者患有脑出血。在一些实施方案中,被诊断患有脑损伤的受试者患有脑实质出血。在一些实施方案中,被诊断患有脑损伤的受试者患有脑室出血。在一些实施方案中,被诊断患有脑损伤的受试者患有蛛网膜下腔出血。在一些实施方案中,被诊断患有脑损伤的受试者患有脑淀粉样血管病。在一些实施方案中,被诊断患有脑损伤的受试者患有脑动脉瘤。在一些实施方案中,被诊断患有脑损伤的受试者患有脑avm。
在一些实施方案中,本发明的组合物用于治疗出血性中风。在一些实施方案中,本发明的组合物用于治疗脑出血。在一些实施方案中,本发明的组合物用于治疗脑实质出血。在一些实施方案中,本发明的组合物用于治疗脑室出血。在一些实施方案中,本发明的组合物用于治疗蛛网膜下腔出血。在一些实施方案中,本发明的组合物用于治疗脑淀粉样血管病。在一些实施方案中,本发明的组合物用于治疗脑动脉瘤。在一些实施方案中,本发明的组合物用于治疗脑avm。
经过一段时间的中断后,恢复到大脑的足够血流虽然可以有效减轻与中风有关的症状,但反而会导致对脑组织的进一步损伤。在中断期间,受影响的组织会缺乏氧和营养,并且血流的突然恢复会通过诱发氧化应激而导致炎症和氧化损伤。这被称为再灌注损伤,不仅在中风后,而且在缺血或缺氧一段时间后血液供应返回组织时,心脏病发作或其他组织损伤后也有充分的文献记载。在一些实施方案中,被诊断患有脑损伤的受试者由于中风而遭受了再灌注损伤。在一些实施方案中,本发明的组合物用于治疗中风引起的再灌注损伤。
短暂性脑缺血发作(tia)(通常称为小中风)是公认的更严重中风的警告信号。因此,患有一种或多种tia的受试者罹患中风的风险更高。在一些实施方案中,被诊断患有脑损伤的受试者患有tia。在一些实施方案中,本发明的组合物用于治疗tia。在一些实施方案中,本发明的组合物用于治疗患有tia的受试者的脑损伤。
高血压、高血脂、中风家族史、心脏病、糖尿病、脑动脉瘤、动静脉畸形、镰状细胞病、血管炎、出血性病症、使用非甾体抗炎药(nsaid)、吸烟、大量饮酒、非法吸毒、肥胖、缺乏体育锻炼和不健康饮食均被视为中风的危险因素。具体地,已经证明降低血压能预防缺血性和出血性中风二者[36,37]。在一些实施方案中,本发明的组合物用于治疗具有至少一种中风风险因素的受试者的脑损伤。在一些实施方案中,受试者具有中风的两个风险因素。在一些实施方案中,受试者具有中风的三个风险因素。在一些实施方案中,受试者具有中风的四个风险因素。在一些实施方案中,受试者具有中风的多于四个风险因素。在一些实施方案中,受试者患有高血压。在一些实施方案中,受试者患有高血胆固醇。在一些实施方案中,受试者具有中风家族史。在一些实施方案中,受试者患有心脏病。在一些实施方案中,受试者患有糖尿病。在一些实施方案中,受试者患有脑动脉瘤。在一些实施方案中,受试者患有动静脉畸形。在一些实施方案中,受试者患有血管炎。在一些实施方案中,受试者患有镰状细胞病。在一些实施方案中,受试者患有出血性病症。在一些实施方案中,受试者具有使用非甾体抗炎药(nsaid)的历史。在一些实施方案中,受试者吸烟。在一些实施方案中,受试者大量饮酒。在一些实施方案中,受试者非法吸毒。在一些实施方案中,受试者是肥胖的。在一些实施方案中,受试者超重。在一些实施方案中,受试者缺乏体育锻炼。在一些实施方案中,受试者饮食不健康。
实施例表明,本发明的组合物在损伤事件发生之前施用时可以用于治疗脑损伤和帮助恢复。因此,当施用于有脑损伤风险(诸如中风)的受试者时,本发明的组合物可以特别用于治疗脑损伤。
在某些实施方案中,本发明的组合物用于减少由潜在的脑损伤,优选中风引起的损伤。组合物在潜在的脑损伤发生之前施用时,特别是当向被鉴定为有脑损伤风险的患者施用时,可以减少所造成的损伤。
实施例表明,本发明的组合物在损伤事件发生后施用时可以用于治疗脑损伤和帮助恢复。因此,在脑损伤诸如中风后施用于受试者时,本发明的组合物可以特别用于治疗脑损伤。
在一些实施方案中,本发明的组合物通过减少运动损伤来治疗脑损伤。在一些实施方案中,本发明的组合物通过改善运动功能来治疗脑损伤。在一些实施方案中,本发明的组合物通过改善肌肉强度来治疗脑损伤。在一些实施方案中,本发明的组合物通过改善记忆来治疗脑损伤。在一些实施方案中,本发明的组合物通过改善社交认可来治疗脑损伤。在一些实施方案中,本发明的组合物通过改善神经功能来治疗脑损伤。
脑损伤的治疗可以指例如减轻症状的严重性。脑损伤的治疗还可以指减少中风后的神经障碍。可以将用于治疗中风的本发明的组合物在中风发作之前,例如在被鉴定为具有中风风险的患者中提供给受试者。可以在中风发生后,例如在恢复期间提供用于治疗中风的本发明的组合物。可以在急性恢复期(即,中风后至多一周)提供用于治疗中风的本发明的组合物。可以在亚急性恢复期(即,中风后一周至三个月)提供用于治疗中风的本发明的组合物。可以在慢性恢复期(中风后三个月)提供用于治疗中风的本发明的组合物。
在某些实施方案中,本发明的组合物用于与第二活性剂组合使用。在某些实施方案中,本发明的组合物用于与阿司匹林或组织纤溶酶原激活剂(tpa)组合使用。其他第二药剂包括其他抗血小板药物(诸如氯吡格雷)、抗凝剂(诸如肝素、华法林、阿哌沙班、达比加群、依多沙班或利伐沙班)、降压药(诸如利尿剂、ace抑制剂、钙通道阻滞剂、β阻滞剂或α阻滞剂)或他汀类药物。本发明的组合物可以改善患者对第二活性剂的反应。
在某些实施方案中,本发明的组合物减少缺血对组织的影响。在某些实施方案中,本发明的组合物减少由缺血引起的对组织的损伤量。在某些实施方案中,由缺血损伤的组织是脑组织。在某些实施方案中,本发明的组合物减少坏死或坏死细胞的数量。在某些实施方案中,本发明的组合物减少凋亡或凋亡细胞的数量。在某些实施方案中,本发明的组合物减少坏死和凋亡细胞的数量。在某些实施方案中,本发明的组合物防止细胞因坏死和/或凋亡而死亡。在某些实施方案中,本发明的组合物防止细胞因缺血引起的坏死和/或凋亡而死亡。在某些实施方案中,本发明的组合物改善因缺血而损伤的组织的恢复。在某些实施方案中,本发明的组合物提高坏死细胞和/或凋亡细胞的清除速度。在某些实施方案中,本发明的组合物改善坏死细胞和/或凋亡细胞的清除功效。在某些实施方案中,本发明的组合物改善组织内细胞的更换和/或再生。在某些实施方案中,本发明的组合物改善因缺血而损伤的组织内细胞的更换和/或再生。在某些实施方案中,本发明的组合物改善组织的整体组织学(例如,在活检时)。
施用方式
优选地,本发明的组合物施用到胃肠道以便允许本发明的细菌菌株递送到肠和/或本发明的细菌菌株部分或完全定居在肠。通常,本发明的组合物口服施用,或者它们可以直肠、鼻内或通过口腔或舌下途径施用。
在某些实施方案中,本发明的组合物可以作为泡沫、作为喷雾剂或凝胶施用。
在某些实施方案中,本发明的组合物可以作为栓剂诸如直肠栓剂,例如呈可可油(可可脂)、合成硬脂(例如,suppocire、witepsol)、甘油-明胶、聚乙二醇或皂甘油组合物的形式施用。
在某些实施方案中,本发明的组合物通过管(诸如鼻胃管、口胃管、胃管、空肠造瘘管(j管)、经皮内窥镜胃造口术(peg))或端口(诸如提供到胃的路径的胸壁端口、空肠或其他合适的路径端口)来施用到胃肠道。
本发明的组合物可以施用一次,或者它们可以作为治疗方案的一部分顺序地施用。在某些实施方案中,本发明的组合物每天施用。
在本发明的某些实施方案中,根据本发明的治疗伴随对患者的肠道微生物群的评定。如果未实现本发明的菌株的递送和/或本发明的菌株的部分或完全定居而使得未观察到功效,则可以重复治疗,或者如果递送和/或部分或完全定居成功并且观察到功效,则可以停止治疗。
在某些实施方案中,可以将本发明的组合物施用于怀孕动物,例如哺乳动物,例如人,以防止子宫内和/或出生后的孩子体内发生炎性或自身免疫性疾病。
可以将本发明的组合物施用于已被诊断患有神经退行性疾病或已被鉴定为具有神经退行性疾病风险的患者。所述组合物也可以作为预防措施施用,以防止健康患者中发生神经退行性疾病。
本发明的组合物可以施用给已鉴定为具有异常的肠道微生物群的患者。例如,所述患者可以具有减少的或没有副拟杆菌,特别是狄氏副拟杆菌进行的定居。
本发明的组合物可以作为食物产品诸如营养补充剂施用。
通常,本发明的组合物用于治疗人类,虽然它们可以用于治疗动物,包括单胃哺乳动物,诸如家禽、猪、猫、狗、马或兔。本发明的组合物可以用于增强动物的生长和性能。如果施用给动物,则可以使用口服管饲法。
组合物
通常,本发明的组合物包含细菌。在本发明的优选的实施方案中,所述组合物以冻干形式配制。例如,本发明的组合物可以包含颗粒或明胶胶囊,例如例如硬明胶胶囊,其包含本发明的细菌菌株。
优选地,本发明的组合物包含冻干的细菌。细菌的冻干是建立完善的程序,并且相关指导可见于例如参考文献[38-40]。
可替代地,本发明的组合物可以包含活的有效的细菌培养物。
在一些实施方案中,本发明的组合物中的细菌菌株未被灭活,例如未被热灭活。在一些实施方案中,本发明的组合物中的细菌菌株未被杀死,例如未被热杀死。在一些实施方案中,本发明的组合物中的细菌菌株未被减毒,例如未被热减毒。例如,在一些实施方案中,本发明的组合物中的细菌菌株未被杀死、灭活和/或减毒。例如,在一些实施方案中,本发明的组合物中的细菌菌株是活的。例如,在一些实施方案中,本发明的组合物中的细菌菌株是可存活的。例如,在一些实施方案中,本发明的组合物中的细菌菌株能够部分地或完全地在肠定居。例如,在一些实施方案中,本发明的组合物中的细菌菌株是可存活的并且能够部分地或完全地在肠定居。
在一些实施方案中,所述组合物包含活细菌菌株和已被杀死的细菌菌株的混合物。
在优选的实施方案中,本发明的组合物被封装以允许将细菌菌株递送到肠。封装保护组合物不被降解,直至通过例如用化学或物理刺激(诸如压力、酶活性或可以通过ph变化触发的物理崩解)破裂来递送在目标位置。可以使用任何适当的封装方法。示例性封装技术包括包埋在多孔基质内、附着或吸附在固体载体表面上、通过絮凝自聚集或与交联剂聚集、以及机械包含在微孔膜或微胶囊之后。关于可以用于制备本发明的组合物的封装的指导可见于例如参考文献[41]和[42]。
所述组合物可以口服施用并且可以呈片剂、胶囊或粉末的形式。封装的产品是优选的,因为副拟杆菌是厌氧菌。可以包括其他成分(例如像维生素c)作为氧清除剂和益生菌底物以改善体内递送和/或部分或完全定居和存活。可替代地,本发明的益生菌组合物可以作为食物或营养产品(诸如基于奶或乳清的发酵乳制品)或作为药物产品口服施用。
所述组合物可以配制为益生菌。
本发明的组合物包含治疗有效量的本发明的细菌菌株。治疗有效量的细菌菌株足以对患者发挥有益作用。治疗有效量的细菌菌株可以足以产生对患者的肠的递送和/或受试者的肠的部分或完全定居。
例如,对于成年人,细菌的合适的日剂量可以是约1x103至约1x1011个菌落形成单位(cfu);例如,约1x107至约1x1010个cfu;在另一个实例中,约1x106至约1x1010个cfu。
在某些实施方案中,所述组合物包含相对于组合物的重量的约1x106至约1x1011个cfu/g的量的细菌菌株;例如约1x108至约1x1010个cfu/g。所述剂量可以是例如1g、3g、5g和10g。
通常,益生菌(诸如本发明的组合物)任选地与至少一种合适的益生菌化合物组合。益生菌化合物通常是不易消化的碳水化合物,诸如寡糖或多糖或者糖醇,其在上消化道中不被降解或吸收。已知的益生菌包括商业产品诸如菊粉和半乳糖-寡糖。
在某些实施方案中,本发明的益生菌组合物包含相对于总重量组成的约1至约30重量%(例如,约5至20重量%)的量的益生菌化合物。碳水化合物可选自由以下组成的组:果糖-寡糖(或fos)、短链果糖-寡糖、菊粉、异麦芽糖醇-寡糖、果胶、木寡糖(或xos)、壳聚糖-寡糖(或cos)、β-葡聚糖、改性的阿拉伯树胶和抗性淀粉、聚糊精、d-塔格糖、金合欢纤维、角豆树、燕麦、以及柑橘纤维。在一方面,益生菌是短链果糖-寡糖(为了简单起见,以下在本文中示为fos-c.c);所述fos-c.c.是不易消化的碳水化合物,通常通过甜菜糖的转化获得并且包含三个葡萄糖分子所结合的蔗糖分子。
在某些实施方案中,本发明的组合物与另一种治疗化合物组合使用以治疗或预防神经退行性障碍。在一些实施方案中,将本发明的组合物与调节神经保护或神经增殖的营养补充剂一起施用。在优选的实施方案中,营养补充剂包含营养维生素或由营养维生素组成。在某些实施方案中,维生素是维生素b6、镁、二甲基甘氨酸(维生素b16)和维生素c。在某些实施方案中,将本发明的组合物与另一种益生菌组合施用。
在某些实施方案中,本发明的组合物用于增强第二药剂对神经退行性疾病的作用。本发明的组合物的免疫调节作用可以使大脑对常规疗法更敏感,所述常规疗法诸如左旋多巴、多巴胺激动剂、mao-b抑制剂、comt抑制剂、谷氨酸拮抗剂或抗胆碱药物,它们是与本发明组合物组合施用(顺序地或同时地)的示例性第二药剂。
本发明的组合物可以包含药学上可接受的赋形剂或载体。此类合适的赋形剂的实例可见于参考文献[43]。用于治疗性用途的可接受的载体或稀释剂在制药领域是熟知的,并且例如在参考文献[44]中描述。合适的载体的实例包括乳糖、淀粉、葡萄糖、甲基纤维素、硬脂酸镁、甘露糖醇、山梨醇等。合适的稀释剂的实例包括乙醇、甘油和水。药物载体、赋形剂或稀释剂的选择可以考虑预期的施用途径和标准药学实践来选择。所述药物组合物除载体、赋形剂或稀释剂之外可以包含任何合适的粘合剂、润滑剂、悬浮剂、包衣剂、增溶剂。合适的粘合剂的实例包括淀粉;明胶;天然糖,诸如葡萄糖、无水乳糖、自由流动的乳糖、β-乳糖;玉米甜味剂;天然和合成胶,诸如阿拉伯树胶、黄蓍胶或藻酸钠、羧甲基纤维素和聚乙二醇。合适的润滑剂的实例包括油酸钠、硬脂酸钠、硬脂酸镁、苯甲酸钠、乙酸钠、氯化钠等。在所述药物组合物中可以提供防腐剂、稳定剂、染料以及甚至调味剂。防腐剂的实例包括苯甲酸钠、山梨酸以及对羟基苯甲酸的酯。还可以使用抗氧化剂和悬浮剂。
本发明的组合物可以配制为食物产品。例如,食物产品可以提供除本发明的治疗性作用之外的营养益处,诸如呈营养补充剂的形式。相似地,可以配制食物产品以增强本发明的组合物的口味或通过与普通食品而非与药物组合物更相似来使得组合物对于消费者更具吸引力。在某些实施方案中,本发明的组合物被配制为基于奶的产品。术语“基于奶的产品”意指具有变化的脂肪含量的任何液体或半固体的基于奶或乳清的产品。基于奶的产品可以是例如牛奶、山羊奶、绵羊奶、脱脂奶、全脂奶、由奶粉和乳清重组而没有任何加工的奶、或加工产品,诸如酸乳酪、凝固奶、凝乳、酸奶、酸化全脂奶、黄油乳以及其他酸奶产品。另一个重要的组包括奶饮料诸如乳清饮料、发酵奶、炼乳、婴儿或幼儿奶;调味奶、冰淇淋;含奶食物诸如糖。
在一些实施方案中,本发明的组合物包含一种或多种副拟杆菌属的细菌菌株,并且不包含来自任何其他属的细菌,或者其仅包含微少的或生物非相关的量的来自另一属的细菌。因此,在一些实施方案中,本发明提供了一种用于治疗的包含一种或多种副拟杆菌属的细菌菌株的组合物,其不包含来自任何其他属的细菌,或者其仅包含微少的或生物非相关的量的来自另一属的细菌。
在一些实施方案中,本发明的组合物包含一种或多种狄氏副拟杆菌菌种的细菌菌株,并且不包含来自任何其他菌种的细菌,或者其仅包含微少的或生物非相关的量的来自另一菌种的细菌。因此,在一些实施方案中,本发明提供了一种用于治疗的包含一种或多种狄氏副拟杆菌菌种的细菌菌株的组合物,其不包含来自任何其他菌种的细菌,或者其仅包含微少的或生物非相关的量的来自另一菌种的细菌。
在一些实施方案中,本发明的组合物包含一种或多种狄氏副拟杆菌菌种的细菌菌株,并且不包含来自任何其他副拟杆菌菌种的细菌,或者其仅包含微少的或生物非相关的量的来自另一副拟杆菌菌种的细菌。因此,在一些实施方案中,本发明提供了一种用于治疗的包含一种或多种狄氏副拟杆菌菌种的细菌菌株的组合物,其不包含来自任何其他副拟杆菌菌种的细菌,或者其仅包含微少的或生物非相关的量的来自另一副拟杆菌菌种的细菌。
在某些实施方案中,本发明的组合物包含单一细菌菌株或菌种并且不含任何其他细菌菌株或菌种。此类组合物可以仅包含微少的或生物非相关的量的其他细菌菌株或菌种。此类组合物可以是基本上不含其他种类的生物体的培养物。
在一些实施方案中,本发明提供了一种用于治疗的包含副拟杆菌属的单一细菌菌株的组合物,其不包含来自任何其他菌株的细菌,或者其仅包含微少的或生物非相关的量的来自另一菌株的细菌。
在一些实施方案中,本发明提供了一种用于治疗的包含狄氏副拟杆菌菌种的单一细菌菌株的组合物,其不包含来自任何其他菌株的细菌,或者其仅包含微少的或生物非相关的量的来自另一菌株的细菌。
在一些实施方案中,本发明的组合物包含多于一种的细菌菌株。例如,在一些实施方案中,本发明的组合物包含多于一种来自同一菌种内的菌株(例如,多于1、2、3、4、5、6、7、8、9、10、15、20、25、30、35、40或45种菌株),并且任选地不含来自任何其他菌种的细菌。在一些实施方案中,本发明的组合物包含少于50种来自同一菌种内的菌株(例如,少于45、40、35、30、25、20、15、12、10、9、8、7、6、5、4或3种菌株),并且任选地不含来自任何其他菌种的细菌。在一些实施方案中,本发明的组合物包含1-40、1-30、1-20、1-19、1-18、1-15、1-10、1-9、1-8、1-7、1-6、1-5、1-4、1-3、1-2、2-50、2-40、2-30、2-20、2-15、2-10、2-5、6-30、6-15、16-25或31-50种来自同一菌种内的菌株,并且任选地不含来自任何其他菌种的细菌。本发明包括前述内容的任何组合。
在一些实施方案中,所述组合物包含微生物聚生体。例如,在一些实施方案中,所述组合物包含副拟杆菌细菌菌株作为微生物聚生体的一部分。例如,在一些实施方案中,副拟杆菌细菌菌株与一种或多种(例如,至少2、3、4、5、10、15或20种)来自其他属的其他细菌菌株组合存在,副拟杆菌细菌菌株可以与所述其他细菌菌株在体内在肠中以共生方式存活。例如,在一些实施方案中,所述组合物包含与来自不同属的细菌菌株组合的副拟杆菌的细菌菌株。在一些实施方案中,微生物聚生体包含从单一生物体例如人类的粪便样品获得的两种或更多种细菌菌株。在一些实施方案中,微生物聚生体在自然界中发现不在一起。例如,在一些实施方案中,微生物聚生体包含从至少两个不同的生物体的粪便样品获得的细菌菌株。在一些实施方案中,两个不同的生物体来自同一物种,例如两个不同的人类。在一些实施方案中,两个不同的生物体是婴儿人类和成人人类。在一些实施方案中,两个不同的生物体是人类和非人类哺乳动物。
在一些实施方案中,本发明的组合物另外包含具有与菌株mrx005相同的安全性和治疗功效特征的细菌菌株,但其不是mrx005或不是狄氏副拟杆菌。
在本发明的组合物包含多于一种细菌菌株、菌种或属的一些实施方案中,各个细菌菌株、菌种或属可以用于单独、同时或顺序施用。例如,所述组合物可以包含所述多于一种细菌菌株、菌种或属中的全部,或者所述细菌菌株、菌种或属可以单独保存并且单独、同时或顺序施用。在一些实施方案中,所述多于一种细菌菌株、菌种或属单独保存但是在使用之前混合在一起。
在一些实施方案中,用于本发明的细菌菌株从成人粪便获得。在本发明的组合物包含多于一种细菌菌株的一些实施方案中,所有细菌菌株均从成人粪便获得,或者如果存在其他细菌菌株,它们仅以微少的量存在。细菌可以在从成人粪便获得并且用于本发明的组合物之后进行培养。
在一些实施方案中,用于本发明的细菌菌株从婴儿粪便获得。在本发明的组合物包含多于一种细菌菌株的一些实施方案中,所有细菌菌株均从婴儿粪便获得,或者如果存在其他细菌菌株,它们仅以微少的量存在。细菌可以在从婴儿粪便获得并且用于本发明的组合物之后进行培养。
如上所述,在一些实施方案中,一种或多种副拟杆菌细菌菌株是本发明组合物中的唯一治疗活性剂。在一些实施方案中,组合物中的细菌菌株是本发明的组合物中的唯一的治疗活性剂。
用于根据本发明使用的组合物可能需要或可能不需要市场批准。
在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株被冻干。在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株进行喷雾干燥。在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株被冻干或进行喷雾干燥并且其中它是活的。在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株被冻干或进行喷雾干燥并且其中它是可存活的。在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株被冻干或进行喷雾干燥并且其中它能够部分地或完全地在肠定居。在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株被冻干或进行喷雾干燥并且其中它是可存活的并且能够部分地或完全地在肠定居。
在一些情况下,冻干的细菌菌株在施用之前进行重构。在一些情况下,所述重构通过使用本文所述的稀释剂进行。
本发明的组合物可以包含药学上可接受的赋形剂、稀释剂或载体。
在某些实施方案中,本发明提供一种药物组合物,其包含:本发明的细菌菌株;以及药学上可接受的赋形剂、载体或稀释剂;其中所述细菌菌株的量当施用于有需要的受试者时足以治疗神经退行性障碍。
在某些实施方案中,本发明提供一种药物组合物,其包含:本发明的细菌菌株;以及药学上可接受的赋形剂、载体或稀释剂;其中所述细菌菌株的量足以治疗或预防神经退行性障碍。
在某些实施方案中,本发明提供以上的药物组合物,其中细菌菌株的量是相对于组合物的重量的约1×103至约1×1011个菌落形成单位/克。
在某些实施方案中,本发明提供以上的药物组合物,其中所述组合物在1g、3g、5g或10g的剂量下施用。
在某些实施方案中,本发明提供以上的药物组合物,其中所述组合物通过选自由以下组成的组的方法施用:口服、直肠、皮下、鼻腔、口腔以及舌下。
在某些实施方案中,本发明提供以上的药物组合物,其包含选自由以下组成的组的载体:乳糖、淀粉、葡萄糖、甲基纤维素、硬脂酸镁、甘露糖醇以及山梨醇。
在某些实施方案中,本发明提供以上的药物组合物,其包含选自由以下组成的组的稀释剂:乙醇、甘油和水。
在某些实施方案中,本发明提供以上的药物组合物,其包含选自由以下组成的组的赋形剂:淀粉、明胶、葡萄糖、无水乳糖、自由流动的乳糖、β-乳糖、玉米甜味剂、阿拉伯树胶、黄蓍胶、藻酸钠、羧甲基纤维素、聚乙二醇、油酸钠、硬脂酸钠、硬脂酸镁、苯甲酸钠、乙酸钠以及氯化钠。
在某些实施方案中,本发明提供以上的药物组合物,其还包含防腐剂、抗氧化剂和稳定剂中的至少一种。
在某些实施方案中,本发明提供以上的药物组合物,其包含选自由以下组成的组的防腐剂:苯甲酸钠、山梨酸以及对羟基苯甲酸的酯。
在某些实施方案中,本发明提供以上的药物组合物,其中所述细菌菌株被冻干。
在某些实施方案中,本发明提供以上的药物组合物,其中当所述组合物保存在约4℃或约25℃下的密封容器中并且所述容器置于具有50%相对湿度的气氛中时,如以菌落形成单位测量的细菌菌株的至少80%在至少约以下的时间段之后仍保留:1月、3月、6月、1年、1.5年、2年、2.5年或3年。
在一些实施方案中,本发明的组合物在包含如本文所述的组合物的密封容器中提供。在一些实施方案中,密封容器是小袋或瓶。在一些实施方案中,本发明的组合物在包含如本文所述的组合物的注射器中提供。
在一些实施方案中,本发明的组合物提供为药物制剂。例如,所述组合物可提供为片剂或胶囊。在一些实施方案中,所述胶囊是明胶胶囊(“凝胶套”)。
在一些实施方案中,本发明的组合物口服施用。口服施用可涉及吞咽,使得化合物进入胃肠道,和/或涉及口腔、舌或舌下施用,通过所述施用,化合物直接从口进入血管。
适用于口服施用的药物制剂包括固体填料、固体微颗粒、半固体和液体(包括多相或分散系统),诸如片剂;含有多颗粒或纳米颗粒、液体(例如,含水溶液)、乳液或粉末的软胶囊或硬胶囊;糖锭(包括液体填充);咀嚼剂;凝胶;快速分散剂型;膜;卵形体;喷雾剂;以及口腔/粘膜粘附贴片。
在一些实施方案中,所述药物制剂是肠溶性制剂,即适于通过口服施用将本发明的组合物递送到肠的胃耐受性制剂(例如,耐受胃ph)。当所述组合物的细菌或另一种组分是酸敏感的,例如易于在酸条件下降解时,肠溶性制剂可以是特别有用的。
在一些实施方案中,所述肠溶性制剂包含肠溶性包衣。在一些实施方案中,所述制剂是肠溶包衣剂型。例如,所述制剂可以是肠溶包衣片剂或肠溶包衣胶囊等。肠溶性包衣可以是常规的肠溶性包衣,例如,用于口服递送的片剂、胶囊等的常规包衣。所述制剂可以包括膜包衣,例如,肠溶性聚合物例如酸不可溶的聚合物的薄膜层。
在一些实施方案中,肠溶性制剂是本质上肠溶性的,例如胃耐受性的而不需要肠溶性包衣。因此,在一些实施方案中,所述制剂是不包括肠溶性包衣的肠溶性制剂。在一些实施方案中,所述制剂是由热胶凝化材料制成的胶囊。在一些实施方案中,热胶凝化材料是纤维素材料,诸如甲基纤维素、羟甲基纤维素或羟丙基甲基纤维素(hpmc)。在一些实施方案中,所述胶囊包括不含有任何成膜聚合物的壳体。在一些实施方案中,所述胶囊包括壳体并且所述壳体包含羟丙基甲基纤维素并且不包含任何成膜聚合物(例如,参见[45])。在一些实施方案中,所述制剂是本质上肠溶性的胶囊(例如,来自capsugel公司的
在一些实施方案中,所述制剂是软胶囊。软胶囊是由于存在于胶囊壳体中的软化剂例如像甘油、山梨醇、麦芽糖醇以及聚乙二醇的添加而可以具有某种弹性和柔软性的胶囊。软胶囊可以例如基于明胶或淀粉来产生。基于明胶的软胶囊可从各种供应商商购获得。基于施用方法例如像口服或直肠方式,软胶囊可以具有各种形状,它们可以是例如圆形、卵形、椭圆形或鱼雷形。软胶囊可通过常规方法例如像通过scherer法、accogel法或微滴或喷吹法产生。
培养方法
用于本发明的细菌菌株可使用如在例如参考文献[46-48]中详述的标准微生物技术来培养。
用于培养的固体或液体培养基可以是ycfa琼脂或ycfa培养基。ycfa培养基可包含(每100ml,大约值):酪胨(1.0g)、酵母提取物(0.25g)、nahco3(0.4g)、半胱氨酸(0.1g)、k2hpo4(0.045g)、kh2po4(0.045g)、nacl(0.09g)、(nh4)2so4(0.09g)、mgso4·7h2o(0.009g)、cacl2(0.009g)、刃天青(0.1mg)、氯化血红素(1mg)、生物素(1μg)、钴胺素(1μg)、对氨基苯甲酸(3μg)、叶酸(5μg)以及吡哆胺(15μg)。
用于疫苗组合物的细菌菌株
发明人已确定,本发明的细菌菌株可用于治疗或预防神经退行性障碍。这可能是本发明的细菌菌株对于宿主免疫系统所具有的作用产生的结果。因此,当作为疫苗组合物施用时,本发明的组合物还可以用于预防神经退行性障碍。在某些此类实施方案中,本发明的细菌菌株可以被杀死、灭活或减毒。在某些此类实施方案中,所述组合物可以包含疫苗佐剂。在某些实施方案中,所述组合物用于通过注射诸如通过皮下注射进行施用。
总则
除非另外指示,否则本发明的实践将采用本领域的技术内的化学、生物化学、分子生物学、免疫学以及药学的常规方法。此类技术在文献中充分地说明。参见,例如参考文献[49]和[50-56]等。
术语“包含”涵盖“包括”以及“由……组成”,例如“包含”x的组合物可以仅由x组成或者可以包括另外的事物,例如x+y。
与数值x相关的术语“约”是任选的并且是平均值,例如x±10%。
单词“基本上”不排除例如“完全”,例如“基本上不含”y的组合物可以完全不含y。必要时,可以从本发明的定义中省略单词“基本上”。
两个核苷酸序列之间的百分比序列同一性的引用意指当对齐时,比较两个序列的核苷酸的百分比是相同的。此比对和百分比同源性或序列同一性可以使用本领域已知的软件程序,例如参考文献[57]的7.7.18章节中描述的那些来确定。优选的比对通过smith-waterman同源性搜索算法使用仿射间隔搜索的具有间隔开放罚分(gapopenpenalty)为12,间隔延伸罚分(gapextensionpenalty)为2,blosum矩阵为62来确定。smith-waterman同源性搜索算法在参考文献[58]中公开。
除非明确地声明,否则包括多个步骤的工艺或方法可在方法开始或结束时包括另外的步骤或者可包括另外的插入步骤。另外,在适当的情况下,步骤可以组合、省略或以可替代的顺序执行。
本发明的各种实施方案在本文中描述。应理解,在每个实施方案中指定的特征可以与其他指定的特征组合以提供另外的实施方案。具体地,在本文中突出显示为合适的、典型的或优选的实施方案可以彼此组合(当它们相互排斥时除外)。
用于实施本发明的方式
实施例1–细菌接种物充当神经保护剂的功效
概述
用包含根据本发明的细菌菌株的组合物处理神经母细胞瘤细胞。所使用的sh-sy5y神经母细胞瘤细胞可产生多巴胺,并且已被确立为研究神经退行性疾病的体外模型。观察到细菌菌株增加神经增殖的能力。还用多巴胺能神经毒素1-甲基-4-苯基吡啶鎓(mpp)处理神经母细胞瘤细胞,其在神经母细胞瘤细胞中诱发帕金森氏病的永久症状。研究了细菌菌株充当针对mpp的神经保护剂的能力。
材料和方法
细菌菌株
755:狄氏副拟杆菌,马氏巨球菌mrx0029
细胞系
sh-sy5y神经母细胞瘤细胞购自eccacc(目录号:94030304),并在补充有营养混合物f-12ham(sigmaaldrich,目录号n4888)的mem(sigmaaldrich,目录号m2279)中生长。
方法
一旦生长,将sh-sy5y神经母细胞瘤细胞以11,000个细胞/孔接种在96孔板上,并孵育2天。然后将细胞转移至分化培养基(其包含1%fbs)和10um视黄酸(sigmaaldrich,目录号r2625-100mg)。每隔一天更换一次分化培养基,并在分化的第7天收获细胞。用或不用mpp(sigmaaldrich,目录号d048-1g)将细胞预处理8小时。随后,将细胞用10%细菌上清液处理并孵育过夜。通过使用cck-8试剂(sigmaaldrich,细胞计数试剂盒–8,目录号96992-3000tests-f)测量细胞活力,并在450nm波长下读取。
结果
这些实验的结果在图1中示出。用mrx0005或mrx0029处理神经母细胞瘤细胞会导致神经元增殖增加。与仅用mpp处理的细胞相比(其具有降低的活力),用mpp和细菌菌株一起处理的神经母细胞瘤细胞具有增加的细胞活力。这些数据表明细菌菌株可以充当神经保护剂。
实施例2a–细菌接种物减少il-6分泌的功效。
概述
促炎细胞因子的活化与神经退行性疾病中的神经元损伤有关。脂多糖(lps)是促炎细胞因子il-6的已知刺激物。用包含根据本发明的细菌菌株和lps组合的组合物处理人胶质母细胞瘤星形细胞瘤细胞,以观察其调节il-6水平的能力。
材料和方法
细菌菌株
755:狄氏副拟杆菌
细胞系
mgu373是源自恶性肿瘤的人胶质母细胞瘤星形细胞瘤,并购自sigma-aldrich(目录号08061901-1vl)。将mgu373人胶质母细胞瘤星形细胞瘤细胞在补充有10%fbs、1%青霉素链霉素、4mml-glut、1xmem非必需氨基酸溶液和1x丙酮酸钠的mem(sigmaaldrich,目录号m-2279)中生长。
方法
一旦生长,将mgu373细胞以100,000个细胞/孔接种在24孔板上。将细胞单独用lps(1ug/ml)或用10%mrx0005细菌上清液处理24h。还进行了对照,其中将细胞在未处理的培养基中孵育。之后,收集不含细胞的上清液,在10,000g下于4℃下离心3min。根据制造商说明书使用来自peprotech的人il-6elisa试剂盒(目录号#900-k16)测量il-6。
结果
这些实验的结果在图2a中示出。用lps和细菌菌株处理神经母细胞瘤细胞导致分泌的il-6水平降低。
实施例2b–细菌接种物调节il-8分泌的功效。
概述
由于神经炎症在神经退行性疾病中起关键作用,并且il-8已被证明具有神经积极作用,因此评定了包含本发明的细菌菌株和lps的组合物对il-8活化的作用。用包含根据本发明的细菌菌株和lps组合的组合物处理人胶质母细胞瘤星形细胞瘤细胞,以观察其调节il-8水平的能力。
材料和方法
细菌菌株
马氏巨球菌mrx0029;狄氏副拟杆菌mrx0005
细胞系
mgu373是源自恶性肿瘤的人胶质母细胞瘤星形细胞瘤,并购自sigma-aldrich(目录号08061901-1vl)。将mgu373人胶质母细胞瘤星形细胞瘤细胞在补充有10%fbs、1%青霉素链霉素、4mml-glut、1xmem非必需氨基酸溶液和1x丙酮酸钠的mem(sigmaaldrich,目录号m-2279)中生长。
方法
一旦生长,将mgu373细胞以100,000个细胞/孔接种在24孔板上。将细胞单独用lps(1ug/ml)或用10%mrx0029细菌上清液处理24h。之后,收集不含细胞的上清液,在10,000g下于4℃下离心3min。根据制造商说明书使用来自peprotech的人il-8elisa试剂盒(目录号#900-k18)测量il-8。
结果
这些实验的结果在图2b中示出。
实施例2c–细菌接种物减少α-突触核蛋白诱导的炎症的功效。
概述
神经炎症在帕金森氏病中起关键作用,并且α-突触核蛋白已被证明能在体内诱导神经炎症。因此,评定了本发明的细菌菌株抑制α-突触核蛋白诱导的神经炎症的能力。将人胶质母细胞瘤星形细胞瘤细胞和神经母细胞瘤细胞的共培养物暴露于野生型α-突触核蛋白和突变体同工型e46k和a53t,并用包含根据本发明的细菌菌株的组合物处理。然后测试了细菌菌株抑制α-突触核蛋白诱导的il-6分泌的能力。
材料和方法
细菌菌株
马氏巨球菌mrx0029;狄氏副拟杆菌mrx0005
细胞系
mgu373是源自恶性肿瘤的人胶质母细胞瘤星形细胞瘤,并购自sigma-aldrich(目录号08061901-1vl)。将mgu373人胶质母细胞瘤星形细胞瘤细胞在补充有10%fbs、1%青霉素链霉素、4mml-glut、1xmem非必需氨基酸溶液和1x丙酮酸钠的mem(sigmaaldrich,目录号m-2279)中生长。
sh-sy5y是源自恶性神经母细胞瘤的人神经母细胞瘤细胞系,并且可以购自sigma-aldrich(目录号94030304-1vl)。使细胞在补充有2mml-谷氨酰胺、10%热灭活的fbs、100u/ml青霉素、100μg/ml链霉素的50%mem和50%营养混合物f-12ham培养基中生长。将生长培养基上的细胞以11,000个细胞/孔接种在96孔板上,并置于培养箱中。2天后,将培养基替换为分化培养基(含有1%fbs的生长培养基)和10μm视黄酸。每隔一天更换一次分化培养基,并在分化7天后使用细胞。
方法
将shsy5y细胞以50,000个细胞/孔的密度接种在12孔板上。使细胞在补充有2mml-谷氨酰胺、10%热灭活的fbs、100u/ml青霉素、100μg/ml链霉素的50%mem和50%营养混合物f-12ham培养基中生长。将生长培养基上的细胞以11,000个细胞/孔接种在96孔板上,并置于培养箱中。2天后,将培养基替换为分化培养基(含有1%fbs的生长培养基)和10μm视黄酸。每隔一天更换一次分化培养基,并在分化7天后使用细胞。将u373以50,000个细胞/孔的密度接种在12transwell板(0.4μm聚酯膜,costar)上,持续72小时。在分化培养基(含有1%fbs而无视黄酸的生长培养基)中处理之前,将细胞一起共同培养24小时。
此后,在10%细菌上清液存在或不存在下,用25μg/mlα-突触核蛋白(wt,a53t,e46k)处理细胞48小时。收集不含细胞的上清液,在4℃下以10000g离心分离3min,等分并保存在-80℃下。如上所述测量人il-6和il-8。
结果
这些实验的结果在图3中示出。用野生型α-突触核蛋白和突变体同工型e46k和a53t处理细胞诱导il-6的适度分泌。在用细菌菌株处理的细胞中,α-突触核蛋白诱导的il-6分泌受到抑制。
实施例3–细菌接种物减少nfκb活化的功效
概述
nfκb启动子的活化导致促炎细胞因子的产生,包括il-1β、il-1α、il-18、tnfα和il-6。nfκb启动子可以通过刺激tlr4配体被α-突触核蛋白和lps活化。α-突触核蛋白的突变(诸如α-突触核蛋白a53t)与家族性帕金森氏病有关。用lps处理神经元细胞模拟环境因素引起的帕金森氏病。研究了包含根据本发明的细菌菌株的组合物抑制nfκb启动子活化的能力。
材料和方法
细菌菌株
755:狄氏副拟杆菌
细胞系
人hekbluetlr4购自invivogen(目录号hkb-htlr4)。将人hekbluetlr4在补充有10%fbs、1%青霉素链霉素、4mml-glut、normocin和1xhekblue选择溶液的dmem高葡萄糖(sigmaaldrich,目录号d-6171)中生长。
方法
一旦生长,将人hekblue细胞以25,000个细胞/孔接种于96孔板中,重复4次。将一组细胞单独用α-突触核蛋白a53t(1ug/ml)或用10%mrx0005细菌上清液处理22h。将第二组细胞单独用lps(10ng/ml,来自鼠伤寒沙门氏菌血清型,sigmaaldrich,目录号l6143)或10%mrx0005细菌上清液处理22h。随后离心分离细胞,并将20ul上清液与200ulquantiblue试剂(invivogen,目录号rep-qb2)混合,孵育2h并在655nm下读取吸光度。
结果
这些实验的结果在图4和图5中示出。图4显示,mrx0005抑制了α-突触核蛋白对nfκb启动子的活化。图5显示,mrx0005抑制了lps对nfκb启动子的活化。
实施例4–细菌接种物改变抗氧化能力的功效
概述
包含根据本发明的细菌菌株的组合物改变抗氧化能力的能力。使用众所周知的abts(2,2'-连氮基-双(3-乙基苯并噻唑啉-6-磺酸))测定法确定细菌菌株的抗氧化能力。
细菌菌株
755:狄氏副拟杆菌
方法
收集细菌细胞(106个或更多)并离心。将它们重悬于测定缓冲液中(使用三倍沉淀体积)。将悬浮液在冰上超声处理5分钟,然后以12,000xg离心分离10分钟。根据制造商的说明,取出上清液,并使用sigmaaldrich生产的abts测定试剂盒(代码cs0790)进行测量。
结果
这些实验的结果在图6中示出。图6表明,与trolox相比,mrx0005的抗氧化能力为大约0.5mm。
实施例5–细菌接种物改变脂质过氧化水平的功效
概述
研究了包含根据本发明的细菌菌株的组合物改变脂质过氧化水平的能力。硫代巴比妥酸反应物测定法(tbar)用于测量脂质过氧化的副产物。
材料和方法
细菌菌株
755:狄氏副拟杆菌
方法
收集细菌细胞(106个或更多)并离心,用等渗盐水进行洗涤步骤,然后将沉淀重悬浮在氯化钾测定缓冲液中。将悬浮液在冰上超声处理10分钟,然后以10,000xg离心分离10分钟。除去上清液,并使用硫代巴比妥酸反应物测定法评估脂质过氧化的水平。
结果
实验结果在图7中示出。图7显示了,mrx0005能够使脂质过氧化抑制大约20%,这比阳性对照丁基化羟基甲苯(1%w/v)具有更高的抗氧化能力。
实施例6–细菌接种物对组蛋白脱乙酰酶活性的作用
概述
研究了包含根据本发明的细菌菌株的组合物改变组蛋白脱乙酰酶活性的能力。组蛋白脱乙酰酶的失调涉及与年龄相关的神经退行性疾病相关的发病机理。
材料和方法
细菌菌株
755:狄氏副拟杆菌
细胞系
使用细胞系ht-29,因为存在组蛋白脱乙酰酶。
方法
通过离心并在0.22um过滤器中过滤来分离固定相细菌培养物的无细胞上清液。汇合后3天使用ht-29细胞,并在实验开始前24小时加入1mldts。用在dts中稀释的10%无细胞上清液攻击ht-29细胞,并将其孵育48小时。然后使用sigmaaldrich核酸酶提取试剂盒提取核酸酶蛋白,并在hdac活性测量之前将样品速冻。使用sigmaaldrich(uk)试剂盒对hdac活性进行荧光评定。
结果
实验结果在图8中示出。图8表明mrx0005能够降低组蛋白脱乙酰酶活性水平。
实施例7–细菌中吲哚的产生水平
概述
研究了本发明的细菌产生吲哚的能力。吲哚与减轻炎症和氧化应激有关。
材料和方法
细菌菌株
755:狄氏副拟杆菌
atcc11775是已知产生吲哚的细菌参考菌株。
方法
将固定相中完整的细菌细胞与6mm色氨酸一起孵育48小时。具有色氨酸酶的细菌菌种利用色氨酸作为底物来产生吲哚。孵育48小时后,将上清液移出并添加到kovac试剂中,以定量吲哚。使用内部验证的标准化方法制备标准品、储备溶液和试剂。
结果
实验结果在图9中示出。图9表明,mrx0005具有从色氨酸产生吲哚的能力,浓度为大约0.2mm。
实施例8–细菌中犬尿氨酸的产生水平
概述
研究了本发明的细菌产生犬尿氨酸的能力。犬尿氨酸途径的失调可能导致免疫系统的活化和潜在的神经毒性化合物的积累。犬尿氨酸代谢的改变可能参与帕金森氏病的发展。
细菌菌株
755:狄氏副拟杆菌
dsm17136是已知产生犬尿氨酸的bacteroidescopricola菌株。
方法
通过离心并在0.22um过滤器中过滤来分离固定相细菌培养物的无细胞上清液,并冷冻直至使用。使用内部验证的标准化方法来制备犬尿氨酸标准品、储备溶液和试剂。将样品用三氯乙酸处理,并在10,000xg下于4℃离心10分钟。收集上清液并分配到96孔板中。将ehrlich试剂用于犬尿氨酸检测,并以1:1的比例添加。
结果
实验结果在图10中示出。图10显示,mrx0005具有产生犬尿氨酸的能力,浓度为大约70μm。
实施例9–神经保护
将ra分化的shsy-5y细胞用mpp+(mptp的活性代谢物)处理,mptp是一种广泛用于在体外和体内模拟一些pd病理学特征的化学物质。用线粒体呼吸速率测量细胞活力(图11)。mrx0005和mrx0029均显示出显著的作用,并本身促进shsy-5y细胞中线粒体代谢活性的增加。与ycfa-mpp+处理的样品相比,mrx0005的保护作用为约20%,与槲皮素阳性对照所观察到的保护作用大致相同(图11)。
实施例10–代谢物的产生–脑中的代谢物
背景
细菌上清液中存在的代谢物可以直接影响宿主对氧化应激、细胞间通信和神经保护的反应。在离体筛查期间,在喂养mrx0005和mrx0029的小鼠的脑组织中,测量了在神经系统过程中起关键作用的代谢物。
方法
动物
将balbc(envigo,英国)成年雄性小鼠在12h的明暗循环下分组饲养;随意提供标准的啮齿动物食物和水。经过考克大学动物伦理实验委员会(universitycollegecorkanimalethicsexperimentationcommittee)的批准,所有实验均按照欧洲指南进行。在实验开始时,动物为8周龄。
研究设计
进入动物单位后,允许动物在其饲养室中适应一周。在15:00与17:00之间,它们以1x109个cfu的剂量接受活体生物疗法的口服管饲(200μl剂量),连续进行6天。在第7天,将动物断头,并收集组织进行实验。
组织收集
对于治疗和测试条件,以随机方式处死动物;采样在上午9点至下午1:00之间进行。将躯干血收集在edta钾(乙二胺四乙酸)管中,并以4000g离心15min。分离血浆并将其保存在-80℃下以进行进一步分析。快速切除大脑,解剖,并且将每个大脑区域在干冰上快速冷冻并保存在-80℃下以进行进一步分析。取出脾脏并剔除后立即处理以进行离体免疫刺激。将肠组织(切除最靠近盲肠的2cm回肠和结肠段,并使用距盲肠最远的1cm组织)安装到ussing室中以进行肠通透性测定。取出盲肠,称重并保存在-80℃下以进行scfa分析。
单胺分析
通过hplc对脑干样品上的神经递质浓度进行分析。简而言之,将脑干组织在加有4ng/40μln-甲基5-ht(sigmachemicalco.,英国)作为内标的500μl冷冻流动相中进行超声处理。流动相含有0.1m柠檬酸、5.6mm辛烷-1-磺酸(sigma)、0.1m磷酸二氢钠、0.01mmedta(alkem/reagecon,cork)和9%(v/v)甲醇(alkem/reagecon),并使用4n氢氧化钠(alkem/reagecon)将其调节至ph2.8。然后将均质液在4℃下以22,000×g离心15min,并将40μl上清液注入hplc系统,所述系统由scl10-avp系统控制器、lecd6a电化学检测器(shimadzu)、lc-10as泵、cto-10a烘箱、sil-10a自动进样器(样品冷却器保持在40℃)和在线gastorr脱气器(iss,英国)组成。使用保持在30℃下的反相柱(kinetex2.6uc18100×4.6mm,phenomenex)进行分离(流速0.9ml/min)。玻碳工作电极与ag/agcl参比电极(shimdazu)组合使用,工作电压为+0.8v,并使用class-vp5软件(shimadzu)分析所产生的色谱图。通过标准进样确定的特征性保留时间来鉴定神经递质,这些标准进样在样品分析过程中以定期间隔进行。测量分析物与内标的峰高之比,并与标准进样进行比较。结果表示为ng神经递质/g鲜重组织。
代谢物分析
对于gc代谢物分析,使用由smart等人(doi:10.1038/nprot.2010.108)所述方案的稍加修改版本,将细菌上清液样品用氯甲酸甲酯衍生化。所有样品均按随机顺序进行分析。使用与四极检测器(59977b,agilent)偶联的gc(7890b,agilent)进行分析。所述系统由chemstation(agilent)控制。使用chemstation(agilent)将原始数据转换为netcdf格式,然后使用由johnsen等人(doi:10.1016/j.chroma.2017.04.052)所述的paradise软件在matlabr2014b(mathworks,inc.)中将数据导入并处理。
对于脂肪酸分析,使用盐酸将样品酸化,并添加氘标记的内标。所有样品均按随机顺序进行分析。使用安装在与四极检测器(59977b,agilent)偶联的gc(7890b,agilent)中的高极性色谱柱(zebrontmzb-ffap,gc毛细管色谱柱30mx0.25mmx0.25μm)进行分析。所述系统由chemstation(agilent)控制。使用chemstation(agilent)将原始数据转换为netcdf格式,然后使用由johnsen等人(doi:10.1016/j.chroma.2017.04.052)所述的paradise软件在matlabr2014b(mathworks,inc.)中将数据导入并处理。
结果–神经递质的产生
结果在图12中示出,所述图显示在用mrx0029喂养的小鼠的大脑中,去甲肾上腺素水平升高(p=0.0507),同时血清素和5-hiaa略有升高。这些数据支持下面列出的代谢物分析,这表明mrx00029是4-羟基苯基乙酸(一种已知的抗氧化剂)的主要生产物(weon等人,2016)。更重要的是,4-羟基苯基乙酸是多巴胺和去甲肾上腺素的合成中间体并且是重要的生物活性分子(huot等人,parkinson’sdisese2015)。实际上,在pd中,变性变化超出了多巴胺能系统,同样影响了血清素能和去甲肾上腺素能系统,进而导致纹状体和纹状体外结构的血清素(5-羟色胺,5-ht)和去甲肾上腺素(去甲肾上腺素)水平降低(scattonb,javoy-agidf,rouquierl,duboisb,agidybrainres.1983年9月26日;275(2):321-8.)。l-dopa主要靶向pd的多巴胺相关特征,但是它不能解决5-ht和去甲肾上腺素二者的降低。此外,l-dopa处理的持续时间越长,一系列运动和非运动并发症(例如运动障碍、精神症状)越明显(helyma,morrisjg,reidwg,trafficanter,movdisord.2005年2月;20(2):190-9.)因此,这些数据证明产生有机酸(诸如4-羟基苯基乙酸或琥珀酸)的细菌可以用于治疗,特别是用于治疗神经退行性疾病。
结果–代谢物的产生
细菌上清液中存在的代谢物可以具体地直接影响宿主对氧化应激、细胞间通信和神经保护的反应。分析了mrx0029和mrx0005培养物上清液中的代谢物,并且结果在图13中示出。
几种代谢物显示了所分析的两种菌株之间的显著差异。在mrx0005中,琥珀酸的浓度特别升高。有趣的是,在mrx0029中,4-羟基苯基乙酸的样品/培养基比率显著更高(图13)。
上清液中的脂肪酸分析显示出两种菌株之间存在有趣的分歧:mrx0005主要产生乙酸和丙酸,而mrx0029产生直链和支链形式的丁酸、戊酸和己酸(图14b)。两种菌株看起来非常不同,并且具体地,值得注意的是,mrx0005和mrx0029分别产生琥珀酸和4-羟基苯基乙酸(图14a)。此外,mrx0005似乎产生更多的c2和c3短链脂肪酸,而mrx00029产生更多的c4(丁酸盐)以及直链和支链中链脂肪酸,包括己酸。
琥珀酸是参与氧化磷酸化的克雷布斯循环(krebscycle)代谢物。氧化磷酸化复合物是将蛋白质和囊泡突触运输到近端和远端区域的关键步骤(buddslandnichols,1998)。在神经退行性障碍中已报道其功能障碍,包括阿尔茨海默氏病、帕金森氏病和脊髓小脑性共济失调1型(manczakm等人2004;ebadi等人,2001)。这些发现特别有趣,因为琥珀酸可以增强线粒体活性并支持包括pd在内的与错误折叠蛋白有关的神经退行性疾病中的脆弱神经元(ferroet等人,plosone,2017)。bdnf和琥珀酸不仅在神经变性方面而且在诸如抑郁症和焦虑症的精神障碍中均具有相似的保护活性,所述精神障碍在诊断为pd或ad的患者中是非常普遍的。
图14b还证明了mrx0029是丁酸盐(丁酸)的生产物。这可能是重要的,因为丁酸盐具有已知的作用,减少血脑屏障的不可渗透性,具有神经保护作用[59]。mrx0029(和其他神经保护细菌)的这种特性可能有助于其功效。
实施例11-紧密连接蛋白的mrna表达的调节
由于最近的证据表明肠功能障碍和炎症是与pd相关的非运动症状,所以研究了本发明细菌菌株引起任何肠屏障功能障碍的能力。将ht29-mtx上皮产生粘蛋白的细胞单层(gagnon等人,jmicrobiologicalmethods,2013)作为体外模型,以评估用mrx0005和mrx0029处理后的肠道屏障破坏和免疫刺激。暴露于佛波醇12-肉豆蔻酸酯-13-乙酸酯(pma)的分化的ht29-mtx细胞分泌了大量的il-8;相比之下,与未处理和ycfa处理的细胞相比,用mrx005和mrx0029细菌上清液处理24h,诱导的il-8分泌甚至更低(图14a)。
然后研究了mrx0005和mrx0029通过修饰参与肠道屏障形成的蛋白质的表达和定位所涉及的细胞内信号转导来调控上皮通透性的能力。
分离rna并进行定量rt-pcr(qrt-pcr)分析,以表征与mrx0005和mrx0029孵育期间紧密连接蛋白的基因表达的变化。孵育2h后,施用mrx0029增强了闭合蛋白、绒毛蛋白、紧密连接蛋白1和2(分别为tjp1和tjp2)mrna的表达(图14b)。相比之下,暴露于mrx0005不改变紧密连接蛋白的基因表达,这表明这两种菌株对肠屏障的作用不同。
将体外结果与用mrx0005和mrx0029喂养的小鼠肠道的离体平行分析数据进行比较。定量结肠和回肠中tjp2和闭合蛋白的基因表达。由于mrx0029能够显著上调鼠肠结肠区域的tjp1和闭合蛋白(p=0.073),因此离体数据完全反映了体外数据(图14c+14d)。mrx0029还能够降低同一小鼠结肠的通透性功能(图14e+14f)。
材料和方法-rna提取和qpcr分析
根据制造商的说明书,使用rneasy微型试剂盒(qiagen,manchester,juk)提取总rna,并使用分光光度计(nano-dropnd-1000;thermoscientific,wilmington,de)通过260/280nm的吸光度确定rna浓度。对于mrna表达分析,根据制造商的说明书,使用高容量cdna逆转录试剂盒(thermofisher,loughborough),从2000ng的总rna中制备cdna。逆转录反应在热循环器(biometra,德国)中在25℃下进行10min,在37℃下进行120min,在85℃下进行5min。通过sybr-greenpcr测定法一式两份扩增得到的cdna,并在quantstudio7实时pcr机器(appliedbiosystems,英国)上使用标准化谱图(95℃初始变性10分钟,随后95℃下变性10秒,60℃下退火/延伸30秒,循环40次)检测产物。在40次循环后添加解离阶段,以生成熔解曲线。使用appliedbiosystemsquantstudio实时pcr软件v1.2进行分析。序列表中提供了肌动蛋白、绒毛蛋白、闭合蛋白tjp1和tjp2的引物序列。
实施例12–shsy-5y细胞中bdnf分泌的水平
背景
脑源性神经营养因子(bdnf)是大脑中与神经发育、神经保护和神经再生相关的普遍存在的分子。bdnf不仅预防神经变性,还预防精神障碍如抑郁症和焦虑症,这种精神障碍在被诊断患有pd或ad的患者中是很常见的。
方法
将sh-sy5-sy以60,000个细胞/孔的密度接种在24孔板中,并置于培养箱中。24h后,将培养基替换为分化培养基(含有1%fbs的生长培养基)和10μm视黄酸。每隔一天更换一次分化培养基,并在分化的第10天使用细胞。为了进行处理,除去分化培养基,并用450ul完全生长培养基更换,将50μl细菌sn添加到处理过的孔中,或添加ycfa+作为阴性对照。
结果
结果在图15中示出,其显示施用mrx0005与视黄酸组合增加了bdnf从分化的神经母细胞瘤细胞中的分泌。
实施例13–细菌接种物降低细胞氧化水平的功效
背景
活性氧的产生有助于神经退行性疾病的病理。研究了细菌菌株保护分化的shsy-5y和u373细胞免受通过叔丁基过氧化氢(tbhp)处理而产生的活性氧(ros)的能力。
材料和方法
细菌菌株
马氏巨球菌mrx0029
方法
将shsy-5y细胞以5000个细胞/孔的密度接种在黑色平底96孔板中,并置于co2培养箱中。24h后,将培养基替换为分化培养基(含有1%fbs的生长培养基)和10μm视黄酸。每隔一天更换一次分化培养基。在第10天,除去分化培养基,并用预热的pbs洗涤细胞,并在含1%fbs的生长培养基中用10umdcfda分子探针染色20min。然后,再次用预热的pbs洗涤细胞,并在10%细菌上清液存在或不存在下,用100umtbhp处理2h。使用tecan平板读数器在ex/em485/530nm下测量荧光强度。
结果
实验结果在图16中示出。图16b显示,mrx0005能够抑制分化的shsy-5y神经母细胞瘤细胞中ros的产生。mrx0005还减少星形胶质母细胞瘤细胞中ros的生成(图16a)。这显示mrx0005具有一般抗氧化活性。
实施例14-稳定性测试
含有本文所述的至少一种细菌菌株的本文所述的组合物保存在25℃或4℃下的密封容器中,并且所述容器置于具有30%、40%、50%、60%、70%、75%、80%、90%或95%相对湿度的气氛中。在1月、2月、3月、6月、1年、1.5年、2年、2.5年或3年之后,至少50%、60%、70%、80%或90%的细菌菌株仍保留,如通过标准方案以菌落形成单位所测量的。
实施例15
方法
动物
所使用的动物和研究设计与实施例10相同。
细菌菌株
·755:狄氏副拟杆菌(mrx005)
·马氏巨球菌(mrx0029)
组织收集
对于治疗和测试条件,以随机方式处死动物;采样在上午9点至下午2:30之间进行。将躯干血收集在edta钾(乙二胺四乙酸)管中,并以4000g离心15min。分离血浆并将其保存在-80℃下以进行进一步分析。快速切除大脑,解剖,并且将每个大脑区域在干冰上快速冷冻并保存在-80℃下以进行进一步分析。取出脾脏,收集在5mlrpmi培养基中(含l-谷氨酰胺和碳酸氢钠,r8758sigma+10%fbs(f7524,sigma)+1%青霉素链霉素(p4333,sigma)),并且在剔除后立即处理以进行离体免疫刺激。将肠组织(切除最靠近盲肠的23cm回肠和结肠段,并使用距盲肠最远的1cm2cm组织)安装到ussing室中以进行肠通透性测定。取出盲肠,称重并保存在-80℃下以进行scfa分析。
单胺分析
如实施例10中所述分析神经递质浓度
脾细胞因子测定
处死后立即将脾脏收集在5mlrpmi培养基中并立即培养。首先将脾细胞在此rpmi培养基中均质化,然后与1mlrbc裂解缓冲液(11814389001roche,sigma)一起孵育5min。加入另外的10mlrpmi培养基,然后200g离心5min。然后通过40um过滤器过滤上清液。计数细胞并接种(4,000,000/ml培养基)。适应2.5h后,用脂多糖(lps-2μg/ml)或伴刀豆球蛋白a(cona-2.5μg/ml)刺激细胞24h。刺激后,使用用于tnfα、il-10、il-1β、干扰素γ、cxcl2和il6的促炎板1(小鼠)v-plex试剂盒(mesoscalediscovery,马里兰州,美国)收获上清液,以评定细胞因子释放。使用mesoquickplexsq120、sector成像器2400、sector成像器6000、sectors600进行分析。
基因表达分析
根据制造商的建议,使用mirvanatmmirna分离试剂盒(ambion/llife技术,佩斯利,英国)提取总rna,并用dna酶处理(turbodna-free,ambion/lifetechnologies)。根据制造商的说明书,使用nanodroptm分光光度计(thermofisherscientificinc.,威尔明顿,特拉华州,美国)对rna进行定量。根据制造商的程序,使用agilent生物分析仪(agilent,斯托克波特,英国)评定rna质量,并计算rna完整性计数(rin)。将rin值>7的rna用于后续实验。根据制造商的说明书,使用appliedbiosystems高容量cdna试剂盒(appliedbiosystems,沃林顿,英国)将rna逆转录为cdna。简而言之,作为rt主混合物的一部分加入multiscribe逆转录酶(50u/μl)(1)(2)(1)(10),在25℃下孵育10min,在37℃下孵育2h,在85℃下孵育5min,并保存在4℃下。使用appliedbiosystems设计的针对小鼠特异性靶向基因的探针(6-羧基荧光素-fam)进行定量pcr,同时使用β-肌动蛋白作为内源性对照。扩增反应包含1μlcdna,5μl2xpcr主混合物(roche),900nm每种引物,并通过添加不含rna酶的水加至总计10μl。所有反应均在
盲肠内容物中短链脂肪酸分析
将盲肠内容物混合并与milliq水涡旋混合,然后在室温下孵育10min。通过离心(10000g,5min,4℃)沉淀细菌和其他固体,并通过0.2μm过滤,获得上清液。将其转移到透明的gc小瓶中,并使用2-乙基丁酸(sigma)作为内标。使用配备有zb-ffap色谱柱(30mx0.32mmx0.25mm;phenomenex)的varian3500gc火焰电离系统分析scfa的浓度。用不同浓度的标准混合物建立标准曲线,所述标准混合物包含乙酸盐、丙酸盐、异丁酸盐、正丁酸盐、异戊酸盐和戊酸盐(sigma)。通过使用varianstarchromatographyworkstation6.0版软件对峰进行积分。所有scfa数据均以μmol/g表示。
统计分析
将正态分布数据表示为平均值±sem;将非参数数据集表示为四分位数间距的中位数。使用非配对的两尾t检验来分析参数数据,并且将mann-whitney检验用于非参数数据。将spearman秩相关系数用于合并数据集中的相关分析。在所有情况下,p值<0.05被认为是显著的。
结果–神经递质的产生
图17中的结果显示了mrx005处理对小鼠大脑中神经递质浓度的影响。最值得注意的是,用mrx005进行的处理导致多巴胺减少。
结果–基因表达
分析了海马、杏仁核和前额叶皮层的脑组织中神经递质受体[血清素受体1a(5-htr1a),多巴胺d1受体,gaba受体亚基b1,gabaa受体,nmda2a(grin2a)和nmda2b(grin2b)受体]、炎性标记物[il-1β、il6、cd11b、tnfα和tlr4]和内分泌标记物[皮质酮释放因子(crf)、皮质酮释放因子受体1和2(crfr1,crfr2)、脑源性神经营养因子(bdnf)、血管加压素受体、催产素受体、糖皮质激素受体和盐皮质激素受体]的基因表达。
图18至图32显示了mrx005或mrx0029处理后海马、杏仁核和前额叶皮层中基因表达的变化。用mrx0029进行的处理导致杏仁核中糖皮质激素受体表达增加(图25c)。图26a显示,mrx005显著增加杏仁核中bdnf的表达,而用mrx0029进行的处理显著增加杏仁核中tlr4的表达(图26b)。
mrx005和mrx0029均可以增加杏仁核中cd11b的表达(图27a),而mrx005处理后il-6、grin2a和grin2b的表达降低(图27b至图33d)。此外,mrx005和mrx0029在杏仁核中显著增加了gabra2的表达并增加了gabbr1的表达。
用mrx005进行的处理导致前额叶皮层中bdnf表达的显著增加(图29b)。
论述
mrx005和mrx0029施用引起基因表达的变化,尤其是在杏仁核中。
结果–对tph1和ido-1表达的影响
图33显示,mrx0029可以显著增加结肠中色氨酸羟化酶-1(tph1)的表达,并且mrx005处理可以增加结肠中ido-1的表达。用mrx005进行的处理增加回肠中tph1和ido1的表达,而mrx029对于回肠中这些基因的表达没有影响(图34)。
吲哚胺-吡咯2,3-双加氧酶-1(ido-1)是色氨酸/犬尿氨酸途径中的第一个限速酶,而色氨酸羟化酶1(tph1)是色氨酸羟化酶的同工型,负责合成血清素。这些数据表明,mrx0029和mrx005可能影响血清素水平和色氨酸/犬尿氨酸途径。
结果–对色氨酸代谢物水平的影响
图35显示了用mrx005进行的处理对循环犬尿氨酸和色氨酸水平的影响。
结果–对脾细胞中细胞因子表达的影响
离体脾细胞测定涉及用细菌或病毒模拟攻击对脾细胞(从脾脏分离的细胞-一种参与免疫防御的主要器官)进行攻击。
用lps攻击后,mrx005显著降低了脾细胞中干扰素-γ的水平(图36)。此外,在用lps攻击后,mrx005降低了白介素-6和肿瘤坏死因子的水平(分别为图38和图39)。用lps攻击后,用mrx0029进行的处理导致干扰素-γ、白介素-1β和白介素-6降低(分别为图36、图37和图38)。
用mrx005和mrx0029进行的处理导致化学引诱剂cxcl1的水平增加(图41)。
结果–对盲肠短链脂肪酸水平的影响
当饮食中不可消化的纤维被肠道细菌发酵时,产生了短链脂肪酸(scfa)。mrx005施用的作用在图42中示出。
实施例16-mrx029和mrx005的基因表达水平变化的进一步分析
方法
细胞系
sh-sy5y细胞
细菌菌株
·755:狄氏副拟杆菌(mrx005)
·马氏巨球菌(mrx0029)
qpcr
将sh-sy5y接种在10cm皮氏培养皿中,密度为2x106个细胞。24h后,将细胞在含有10%细菌上清液或ycfa+、10umra、200um己酸或200um丙戊酸的分化培养基(含有1%fbs而无ra的生长培养基)中处理17小时。之后,使用相差evosxl核心显微镜以40x/0.65的放大率拍摄代表性图像。收集细胞,并根据rneasy微型试剂盒方案(qiagen)分离总rna。使用高容量cdna逆转录试剂盒(appliedbiosystems)制备cdna。使用qpcr测量基因表达。将gapdh用作内部对照。根据2(-δδct)方法计算倍数变化。map2、drd2、gabrb3、syp、pink1、park7和nse的引物序列提供在序列表中。
免疫标记和细胞成像
将细胞以5x104个细胞/孔接种到8孔腔室载玻片(marienfeldlaboratoryglassware)上过夜,并用10%细菌上清液处理24h。为了分化,将细胞用10nmra处理5天,然后用无细胞细菌上清液处理24h。然后在室温(rt)下,用pbs中的4%多聚甲醛的固定细胞20分钟。用pbs洗涤固定的细胞,并用pbs中的1%tritonx-100透化10分钟。用pbs洗涤后,将载玻片与封闭缓冲液(4%bsa/pbs)在rt下孵育1小时,然后加入在1%bsa/pbs中稀释的抗map2抗体或β3-微管蛋白(分别为sc-74421和sc-80005,santacruzbiotechnologyinc),在4℃下孵育12h。然后将它们用pbs洗涤两次,然后与alexaflour488缀合的抗小鼠(molecularprobesinc)和alexaflour594缀合的鬼笔环肽(ab176757,abcam)在rt下孵育1h。用pbs洗涤3次后,将载玻片用dapi染色并用
免疫印迹
在上述指示条件下培养sh-sy5y细胞,用mrx0005和mrx0029处理24h,然后在含有蛋白酶抑制剂(rochediagnostics,英国)混合物的ripa缓冲液中裂解。使用bca蛋白测定试剂盒(piercebiotechnology,罗克福德,伊利诺州)估计蛋白质浓度,通过sds-page分离并转移至pvdf膜上。然后将膜用5%脱脂干奶粉或5%bsa封闭,并与一抗(分别为map2和β3-微管蛋白)在4℃下孵育过夜。然后将印迹与适当的辣根过氧化物酶(hrp)缀合的二抗一起孵育,并通过化学发光检测试剂盒(piercebiotechnology,罗克福德,伊利诺州)检测蛋白质。对于map2和β3-微管蛋白二者,β-肌动蛋白充当对照来监测样品中蛋白质的负载变化。
结果和讨论
基因表达
图43显示了mrx0029和mrx005诱导的肌动蛋白、绒毛蛋白、闭合蛋白tjp1、tjp2、map2、drd2、gabrb3、syp、pink1、park7和nse表达水平的变化。
结果–显微镜和免疫印迹
图44显示了通过共焦显微镜确定的shsy5y细胞中map2表达水平的变化。map2和b3-微管蛋白的表达水平也通过免疫印迹分析定量。图44m和图44n中显示的结果表明,mrx029诱导了map2水平表达的增加。
序列
用于qpcr的额外引物(括号中为seqidno)
序列
seqidno:1(16s核糖体rna的狄氏副拟杆菌基因,部分序列,菌株:jcm5825-ab238922)
seqidno:2(16s核糖体rna的狄氏副拟杆菌基因,部分序列,菌株:jcm13400-ab238923)
seqidno:3(16s核糖体rna的狄氏副拟杆菌基因,部分序列,菌株:jcm13401-ab238924)
seqidno:4(16s核糖体rna的狄氏副拟杆菌基因,部分序列,菌株:jcm13402-ab238925)
seqidno:5(16s核糖体rna的狄氏副拟杆菌基因,部分序列,菌株:jcm13403-ab238926)
seqidno:6(16s核糖体rna的狄氏副拟杆菌基因,部分序列,菌株:jcm13404-ab238927)
seqidno:7(16s核糖体rna的粪副拟杆菌基因,部分序列,菌株:jcm9497-ab238928)
seqidno:8(16s核糖体rna的粪副拟杆菌基因,部分序列,菌株:jcm13405-ab238929)
seqidno:9(狄氏副拟杆菌菌株755的共有16srrna序列)
seqidno:10(菌株755基因组序列)–参见电子序列表。
seqidno:11(马氏巨球菌菌株mrx0029的共有16srrna序列)
用于qpcr的引物(括号中为seqidno)
参考文献
[1]sporetal.(2011)na,revmicrobiol.9(4):279-90.
[2]eckburgetal(2005)science.10;308(5728):1635-8.
[3]macphersonetal.(2001)microbesinfect.3(12):1021-35
[4]macphersonetal.(2002)cellmollifesci.59(12):2088-96.
[5]mazmanianetal.(2005)cell15;122(1):107-18.
[6]franketal.(2007)pnas104(34):13780-5.
[7]scanlanetal.(2006)jclinmicrobiol.44(11):3980-8.
[8]kangetal.(2010)inflammboweldis.16(12):2034-42.
[9]machiclsetal.(2013)gut.63(8):1275-83.
[10]wo2013/050792
[11]wo03/046580
[12]wo2013/008039
[13]wo2014/167338
[14]goldinandgorbach(2008)clininfectdis.46suppl2:s96-100.
[15]azadetal.(2013)bmj.347:f6471.
[16]mayeretal(2014)thejournalofneuroscience34(46):15490-15496
[17]cryananddinan(2015)neuropsychopharmacology,40:241-2.
[18]zhouandfoster(2015)neuropsychiatricdiseaseandtreatment11:715-723.
[19]wangandkasper(2014)brainbehavimmun.38:1-12.
[20]wo2016/203220
[21]chapter38-nonsteroidalanti-inflammatorydrugsexposureandthecentralnervoussystem(2014)handbookofclinicalneurology119,577-584
[22]sakamotoandbenno(2006)intjsystevolmicrobiol.56(pt7):1599-605.
[23]mascoetal.(2003)systematicandappliedmicrobiology,26:557-563.
[24]
[25]palretal,neurolres2016,38(12):1111-1122
[26]danielesgetal,scisignal2015,8(376):ra45
[27]wangetal(2016)jneurogastroenterolmotil22:589-605.
[28]foguem&manckoundia(2018)currentneurologyandneurosciencereports,18:24
[29]ludolphetal.(2009)eurjneurol.16(3):297-309.
[30]galpern&lang(2006)neurologicalprogress59(3)449-458
[31]zadorietal(2012)journalofneuraltransmission,119,2,275-283
[32]leeeta1(2008)europeanj.cellbiology87:389-397
[33]piroozniaandelefant(2013)frontcellneurosci.7:30.
[34]tang,etal.(2017)jamheartassoc,6(10).
[35]wangetal.(2015)pnas112(9):2583-2858
[36]psatyetal.(2003)jama,289(19):2534-44
[37]lancet.(1995)346(8991-8992):1647-53
[38]miyamoto-shinoharaetal.(2008)j.gen.appl.microbiol.,54,9-24.
[39]cryopreservationandfreeze-dryingprotocols,ed.bydayandmclellan,humanapress.
[40]leslieetal.(1995)appl.environ.microbiol.61,3592-3597.
[41]mitropoulouetal.(2013)jnutrmetab.(2013)716861.
[42]kailasapathyetal.(2002)currissuesintestmicrobiol.3(2):39-48.
[43]handbookofpharmaceuticalexcipients,2ndedition,(1994),editedbyawadeandpjweller
[44]remington′spharmaceuticalsciences,mackpublishingco.(a.r.gennaroedit.1985)
[45]us2016/0067188
[46]handbookofmicrobiologicalmedia,fourthedition(2010)ronaldatlas,crcpress.
[47]maintainingculturesforbiotechnologandindustry(1996)jenniec.hunter-cevera,academicpress
[48]strobel(2009)methodsmolbiol.581:247-61.
[49]gennaro(2000)remington:thescienceandpracticeofpharmacy20thedition,isbn:0683306472.
[50]molecularbiologytechniques:anintensivelaboratorycourse,(reametal,eds.,1998,academicpress).
[51]methodsinenzymology(s.colowickandn.kaplan,eds.,academicpress,inc.)
[52]handbookofexperimentalimmunology,vols.i-iv(d.m.weirandc.c.blackwell,eds,1986,blackwellscientificpublications)
[53]sambrooketal.(2001)molecularcloningalaboratorymanual,3rdedition(coldspringharborlaboratorypress).
[54]handbookofsurfaceandcolloidalchemistry(birdi,k.s.ed.,crcpress,1997)
[55]ausubeletal.(eds)(2002)shortprotocolsinmolecularbiology,5thedition(currentprotocols).
[56]pcr(introductiontobiotechniquesseries),2nded.(newton&grahameds.,1997,sprmgerverlag)
[57]currentprotocolsinmolecularbiology(f.m.ausubeletal.,eds.,1987)supplement30
[58]smith&waterman(1981)adv.appl.math.2:482-489.
[59]michelandprat(2016)anntranslmed.4(1):15.
打印(电子版原件)
(此页不是也不算为国际申请的页)
由受理局填写
打印(电子版原件)
(此页不是也不算为国际申请的页)
由国际局填写
- 还没有人留言评论。精彩留言会获得点赞!