诱导使药物进入癌细胞内的声孔效应的系统及其方法与流程
本发明涉及一种系统,该系统用于诱导使药物进入肿瘤癌细胞内的声孔效应,以提高靶标(即肿瘤)对药物的摄入。本发明还涉及一种控制超声波的方法,以这种方式,诱导使药物进入癌细胞内的声孔效应,从而改善靶标对药物的摄入。
背景技术:
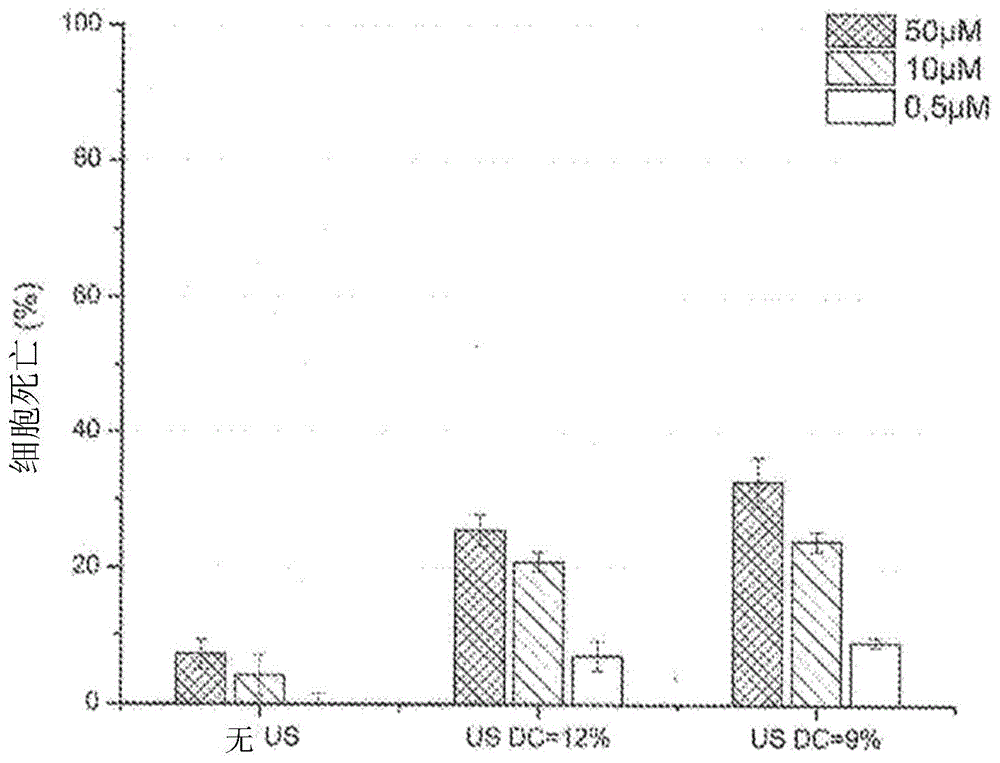
:继循环系统疾病之后,癌症成为了当今世界上第二大常见的死亡原因。国际癌症研究机构估计,由于人口老龄化,预计到2030年,癌症病例将增加约2170万,具有1300万人的死亡率。已知的肿瘤疗法是基于化学疗法和/或放射疗法和/或肿瘤块的手术切除。传统化学疗法尤其受缺乏对癌细胞选择性之苦,可在全身和局部水平上引起副作用。此外,肿瘤经常发展出对所给予的化疗药物的抗性。由于这些原因,在最近的几十年中,开发了几种技术,通过使用被称为脂质体的专用脂质结构,来改善药物递送的选择性。脂质体是纳米载体,通常包括封闭的脂质液滴,脂质液滴具有核心(通常是水性核心),容纳药物(例如化学治疗剂、抗炎药、细胞毒性剂等)。特别地,用于封装化疗药物的脂质体通常设计成具有一结构,该结构允许脂质体自身在血液中的持久循环时间,从而也允许脂质体所含药物在血液中的持久循环时间。在血液中的延长寿命允许脂质体与靶标(即肿瘤)更长时间的相互作用,因为更大量的血液通过肿瘤改善高渗透长滞留(epr)效果。因此,增强了肿瘤对药物的整体吸收,并且显著改善了运输药物的治疗指数[deshpandep.p.,biswass.,andv.ptorchilinv.p.,"currenttrendsintheuseofliposomesfortumortargeting"nanomedicine2013september;8(9)],[torchilinv.p."targetedpharmaceutical5nanocarriersforcancertherapyandimaging".aapsj.2007;9(2):128-147]。然而,即使使用了化疗药物的脂质体制剂,利用在脂质体自然降解后,进行自发释放而获得的选择性水平和治疗功效,仍不能完全令人满意。由于这些原因,即使当前被批准用于临床的纳米药物自发地释放药物,也已经实验测试了多种技术,利用外部施加的刺激来触发这种释放。已经确认,使用高强度聚焦超声可以改善对药物释放的控制,其中高强度聚焦超声除了利用局部升高温度刺激药物释放外,自身还引起细胞毒性作用,诱发肿瘤和周围组织的凝集性坏死(ep1774989b1)。冲击波还用于进行医学治疗,旨于将物质推入人体、组织或细胞内,因此用于提供疫苗、麻醉剂、抗生素等(us2009/281464a1)。为了避免与局部加热,和肿瘤细胞坏死后癌物质扩散相关的可能的毒副作用,最近采用了脉冲低强度非聚焦超声(plinfu)。plinfu能够进行脂质体的“受声波作用(insonation)”和细胞膜的“声孔效应(sonoporation)”。术语“受声波作用”,特别指诱导药物从脂质体内部向外部释放。而术语“声孔效应”是指,在细胞膜上产生瞬时非致命性穿孔,以帮助脂质体进入细胞。已经显示,与高强度聚焦超声不同,与plinfu相关的低能量(<3w/cm2)产生了最小热效应[rizzitellis.,giustettop.,falettod.,dellicastellid.,aimes.,terrenoe."thereleaseofdoxorubicinfromliposomesmonitoredbymriandtriggeredbyacombinationofusstimuliledtoacompletetumorregressioninabreastcancermousemodel",jcontrolrelease,2016;230:57-63.]。如果与脉冲低强度聚焦超声或plifu(如w02016/196741所记载的方法和系统中采用的那些)进行比较,plinfu的特征是在相同的频率、压电直径和激发周期数下,具有不同的超声分布场。由于生成plinfu的压电换能器的平坦几何形状,plinfu具有比plifu更规则的几何分布。另外,与plifu可声致穿孔的体积相比,这种平坦的几何形状允许声致穿孔更大的体积,plifu是由来自两个或更多个压电换能器的超声波束的会聚来生成。此外,在至少两个超声波束的会聚点上,可能发生干扰现象,而无法估计由此引起的失真。现有技术中,plifu系统采用能减少这种现象的方法,但是超声所穿过的介质或生物组织的不均匀性,会引起其他不可预测的干扰。由于这些原因,仅可能使用plinfu,来确保用于产生声孔效应的超声波以设定的频率和设定的占空比(dutycycle),到达靶细胞。实际上,声孔效应仅在特定的频率和占空比值的情况下,才产生纳米级的生物物理现象,而该特定的频率和占空比值取决于要进行声致穿孔的细胞类型,以及要进入该细胞膜的药物的类型。实际上,脉冲超声由发射周期(开启(on)周期)和静止周期(关闭(off)周期)交替组成。在off周期使发射周期中断,并与on周期交替进行。更特别地,on周期应取决于包含药物的载体的特性和细胞膜的特性;来自载体共振效应的振动与细胞膜相互作用,有利于孔的打开,并保护细胞免受超声的直接影响。off周期的持续时间被确定为细胞孔的打开和关闭特性的函数。off周期具有的功能是:一旦孔被打开,就不再进一步刺激细胞膜,从而有利于载体在这些孔关闭的同时,进入细胞室。如果长时间采用on周期而没有off周期,结果将是细胞膜受到持续且延长的压力,这除了干扰药物在细胞内的正确积累之外,还会在细胞上引起过大的压力水平,并产生进出细胞的现象,这同时导致药物的进入和退出。此外,延长刺激可能导致细胞死亡,其结果会使细胞质内容物(包括药物)的渗漏,具有将其通过血流输送到其他不期望的部位的风险。由于上述原因,只有具有特定频率和占空比的值的超声波束,才能通过生成振动脉冲或声子,在晶格水平上与膜相互作用。后者由于声子脉冲频率的值和膜磷脂运动频率的值相当,得以通过晶格点传播,从而引起膜组分发生位错,触发膜的瞬时开孔现象。如果使用非聚焦光束(即plinfu),则在构成发射光束的超声波之间,不会存在相长或相消干涉;这确保了所有组成光束都可以遵循,根据待治疗的所有组织特征和所用药物建立的脉冲。声子脉冲的传播,以及由此触发的膜孔瞬时打开,还受到声流效应的影响。后者被定义为在振动结构(例如细胞膜)附近小规模的流体涡流;已知这种现象会影响扩散速率和膜的渗透性,尤其是减少有用的路径,即超声波束在不与因声压本身而发生变形的组织相互作用的情况下,可以传播的路径。[nowickia.,kowalewskit.,secomskiw.,wojcikj.,"estimationofacousticalstreaming:theoreticalmodel,dopplermeasurementsandopticalvisualization",europeanjournalofultrasound1998,7:73-81]。如果应用了plifu或plinfu,则声流效果是不同的。在plifu的情况中,除了减少有用的路径之外,还可能发生从组织回到压电换能器的信号失真。这种失真不是待声致穿孔的组织所特有和特征性的,因此,这是预测到达靶细胞的超声波束的频率和占空比中,又一不确定性来源。因此,甚至更难以确保用于声孔效应的超声波,以与膜产生最佳相互作用的最优化的频率和占空比,到达目标细胞。技术实现要素:本发明的目的是提供:一种系统,所述系统能改善药物的选择性,以及癌细胞对该药物的摄取。这是由本发明的系统实现的,本发明的系统施用plinfu,通过生成声子振动来诱导细胞声孔效应。本发明的另一个目的是提供:一种控制超声波,以诱导使药物进入癌细胞内的声孔效应的方法。如以下实施例所证明的,通过声孔效应治疗所实现的细胞死亡百分比,取决于所用的药物类型和所治疗的肿瘤类型的组合。更具体地,对于下面列出的人类癌细胞的体外实验结果表明,为了达到重要的细胞死亡百分比,应根据药物和癌细胞的类型来调节plinfu的占空比。plinfu施用的持续时间,即操作时间,对于保证细胞膜孔的打开和关闭的正确时机也很重要。基于这些结果,本发明提供了一种系统和相关方法,用于根据操作者输入的配置数据,来控制诱导声孔效应的plinfu的频率和占空比,该配置数据至少包括肿瘤类型和药物类型。为了本说明书的目的,词语“低强度超声”是指功率密度低于3w/cm2的超声波,而词语“肿瘤类型”是一名称,其表示肿瘤所在部位的组织学类型和器官。因此,“肿瘤类型”的非限制性实例是“人类乳腺导管癌”、“人类胰腺癌”、“雌激素非依赖性人类乳腺癌”、“人类粘膜黑素瘤”、“人类结节性黑素瘤”、“肝细胞癌”等。另外,出于本说明书的目的,词语“药物”旨在表示,当吸入、注射、抽吸、消耗、经由皮肤上的贴剂吸收或在舌下溶解时,在体内导致暂时的生理(和/或心理)变化的任何物质,以及在医学成像中,可用于增强组织和/或结构的对比度和可见性的任何物质(即造影剂)。显然,出于本发明的目的,术语“药物”不仅用于指单一的物质或试剂,而且还指两种或更多种物质或试剂的溶液、组合物或混合物。尽管本发明的优选实施方式是,用于诱导使化疗脂质体进入癌细胞的声孔效应的系统,但是在此指出,这一系统也可以用于未封装在脂质体中的化疗药物,以及任何细胞毒性剂(即,能够杀死靶细胞的试剂)或细胞生长抑制剂(即,具有阻止靶细胞生长或细胞分裂的能力的试剂)。而且,本发明的系统可以用于除化疗药物以外的任何药物(例如抗炎药)的声孔效应,和除肿瘤病理学之外的任何病理学。在后一种情况中,词语“肿瘤类型”可以替换成词语“病理学类型”,其表示受病理学影响的组织学类型和器官。本发明通过提供一种系统来实现上述目的,所述系统包括:-发生器,所述发生器被配置为以超声频率提供电能;-至少一个超声探头,所述超声探头电连接到所述发生器,并被配置为将所述电能转换成由操作参数限定的低强度非聚焦脉冲超声波,所述操作参数包括超声波的频率和占空比;其特征在于,所述系统还包括:-输入装置,所述输入装置使操作者能够输入配置数据,该配置数据包括肿瘤类型和药物类型;和-处理器,所述处理器被配置为:基于输入的配置数据确定所述操作参数的值,其中所述频率的值至少基于肿瘤类型来确定,并且所述占空比的值至少基于药物类型和肿瘤类型来确定;以及控制所述发生器和所述超声探头,以根据所确定的值进行操作。更具体地,所述处理器通过以下步骤,基于所输入的配置数据,确定操作参数的值:-为肿瘤类型分配频率的值;以及-为若干配置数据分配占空比的值,该配置数据包括肿瘤类型和药物类型。为此,所述系统包括计算机可读存储器,其存储频率值的列表和占空比值的列表。在本发明的系统中,药物类型优选地选自由紫杉醇、紫杉醇白蛋白、阿霉素、脂质体阿霉素,伊立替康和脂质体伊立替康,以及氟尿嘧啶组成的组,并且所确定的占空比的值优选为12%以下。本发明还通过提供一种方法来实现上述目的,该方法包括:-读取操作者输入的配置数据,该配置数据包括肿瘤类型、药物类型、肿瘤等级和人体测量值;-基于至少肿瘤类型和药物类型,来确定超声波的操作参数的值,该参数包括频率和占空比;-根据所确定的值,控制至少一个超声探头进行操作,所述至少一个探头电连接到发生器,并被配置为将电能转换为超声波;利用处理器,进行读取、确定和控制的操作。本发明还涉及:一种计算机程序,其包括适用于执行上述方法的代码部分;和,一种存储计算机程序代码的计算机可读介质,当在计算机上运行时,用于执行上述方法。尽管频率的值至少应基于肿瘤类型来确定,但已经考虑到,对于那些不是表层的并且位于特定身体区域(例如腹部)中的肿瘤类型,还必须考虑其他配置数据。实际上,已知超声波的穿透深度受超声频率的影响,频率越低,穿透深度越大。例如,在软组织中,如果超声频率为1mhz,则平均穿透深度(即,超声强度相对于初始强度降低50%的深度)为4~5cm,如果频率为3mhz,则平均穿透深度为1.5cm。而如果超声频率为1mhz,则在软组织中的最大穿透深度为10~12cm,而如果超声频率为3mhz,则在软组织中的最大穿透深度为3~4cm。参考本发明,通过表明频率取决于肿瘤类型,来隐含地考虑穿透深度对频率的依赖性。实际上,如果肿瘤类型例如是黑素瘤之一,则肿瘤在体表上,而如果肿瘤类型是乳腺导管癌,则肿瘤在体表下的一定深度。由于这些原因,表明频率是考虑到肿瘤类型而确定的,这通常意味着,还要考虑与肿瘤在体表下的深度有关的信息,来确定频率。但是,有些类型的肿瘤(例如胰腺癌)位于人体区域中,其尺寸在个体之间可能存在很大差异。在这些情况中,个体之间的身体差异(例如腹围)会显著地影响,对于确保超声到达肿瘤所需频率的确定。因此,还应基于患者的人体测量值,来确定超声频率的值。更具体地,对于人类胰腺癌,此类人体测量值的一些实例可以是腹围、体重指数和体脂率。对于人类乳腺导管癌和雌激素非依赖性人类乳腺癌,此类人体测量值的一些实例可以是乳围(breastcircumference)、体重指数、体脂率、胸围(thoraxcircumference)。因此,在本发明的系统中,配置数据可以进一步包括癌细胞所属患者的人体测量值,选自由腹围、体重指数、乳围、胸围和体脂率组成的组中的所述人体测量值,以及频率值,也可以基于人体测量值来确定。在本发明的系统中,所确定的频率的值在0.6mhz和3mh之间。尽管占空比的值至少应基于肿瘤类型和药物类型来确定,但考虑到,当肿瘤是转移瘤或继发性肿瘤时,其定位可能与“肿瘤类型”命名中指示的定位不同,因此,细胞与相应原始肿瘤的细胞不同,因为它们属于与肿瘤所起源的器官不同的器官。如以下实施例所详细描述的,由于占空比必须根据期望诱导声孔效应的细胞类型而发生变化,因此占空比必须根据最终继发性肿瘤的定位而变化。由于这些原因,在本发明的系统中,配置数据可以进一步包括肿瘤的等级,并且如果肿瘤是转移瘤,则配置数据可包括该转移瘤的定位。与使药物有效进入癌细胞的声孔效应有关的另一操作参数是操作时间,即施用超声的时间间隔。如以下实施例中详细解释的那样,操作时间的值也是相关的,以确保有效的声孔效应使药物进入细胞。因此,在本发明的系统中,操作参数可以包括操作时间,所述操作时间的值至少基于肿瘤类型和药物类型来确定。本发明的系统还被配置为,自动地调谐超声探头的频率和振幅,以补偿由在探头和癌细胞之间的任何介质所引起的超声波的衰减。此外,频率和幅度的自动调谐与占空比同步发生。借助于下文对本发明的优选实施方式的详细描述,这些和其他特征将变得更加清楚,其将作为所要求保护的更一般原理的非限制性实施例。附图说明本文涉及附图,其中:图1a示出了通过体外向人类乳腺导管癌细胞给药紫杉醇,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度下(50μm、10μm、0,5μm)获得的结果;图1b示出了通过体外向人类乳腺导管癌细胞给药紫杉醇白蛋白,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度下(50μm、10μm、0,5μm)获得的结果;图2a示出了通过体外向人类乳腺导管癌细胞给药阿霉素,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(1000μg/ml、500μg/ml、100μg/ml)下获得的结果;图2b示出了通过体外向人类乳腺导管癌细胞给药脂质体阿霉素,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(1000μg/ml、500μg/ml、100μg/ml)下获得的结果;图3a示出了通过体外向雌激素非依赖性人类乳腺癌细胞给药紫杉醇,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(50μm、10μm、0,5μm)下获得的结果;图3b示出了通过体外向雌激素非依赖性人类乳腺癌细胞给药紫杉醇白蛋白,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(50μm、10μm、0,5μm)下获得的结果;图4a示出了通过体外向雌激素非依赖性人类乳腺癌细胞给药阿霉素,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(1000μg/ml、500μg/ml、100μg/ml)下获得的结果;图4b示出了通过体外向雌激素非依赖性人类乳腺癌细胞给药脂质体阿霉素,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(1000μg/ml、500μg/ml、100μg/ml)下获得的结果;图5a示出了通过体外向雌激素非依赖性人类乳腺癌细胞给药紫杉醇,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(50μm、10μm、0,5μm)下获得的结果;图5b示出了通过体外向人类胰腺癌细胞给药紫杉醇白蛋白,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了使用不同的总浓度(50μm、10μm、0,5μm)下获得的结果;图6a示出了通过体外向人类胰腺癌细胞给药伊立替康,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同总浓度(50μm、10μm、0,05μm)下获得的结果;图6b示出了通过体外向人类胰腺癌细胞给药脂质体伊立替康和氟尿嘧啶,获得的细胞死亡百分比,所述给药与超声波施用同时进行。该图示出了在不同的总浓度(50μm、10μm、0,05μm)下获得的结果;图7示出了相对于荧光素胺(fa)内化在癌细胞中的实验结果。图7特别示出了在5种实验条件下,fa被摄入到人类胰腺癌细胞中,所述条件是特别设计的,以研究超声施用的效果;图8a示出了fa被摄入到人类胰腺癌细胞中的共聚焦激光扫描显微镜(clsm)图像,所述fa单独给药,即没有施用超声和任何药物;图8b示出了fa被摄入到人类胰腺癌细胞中的共聚焦激光扫描显微镜(clsm)图像,所述fa与脂质体伊立替康一起给药,但没有施用超声;图8c示出了fa被摄入到人胰腺癌细胞中的共聚焦激光扫描显微镜(clsm)图像,所述fa与脂质体伊立替康一起给药,同时施用占空比为12%的脉冲超声;图8d示出了fa被摄入到人胰腺癌细胞中的共聚焦激光扫描显微镜(clsm)图像,在施用占空比为1%的脉冲超声后,所述fa与脂质体伊立替康一起给药;以及图8e示出了fa被摄入到人胰腺癌细胞中的共聚焦激光扫描显微镜(clsm)图像,所述fa与脂质体伊立替康一起给药,同时施用占空比为1%的脉冲超声;图9a示出了用钆特醇(prohance)(gd3+)的细胞膜孔关闭的动力学;图9b示出了用prohance和脂质体的细胞膜孔关闭的动力学;图9c示出了用四聚体(tetramer)的细胞膜孔关闭的动力学;以及图9d示出了用tetramer和脂质体的细胞膜孔关闭的动力学。具体实施方式本发明系统的优选实施方式包括:-发生器,其被配置为以超声频率提供电能;-超声探头,其电连接到发生器并被配置为:将电能转换为由操作参数限定的低强度非聚焦脉冲超声波,所述操作参数包括超声波的频率、占空比和操作时间;-输入设备,其使操作者能够输入配置数据,该配置数据包括肿瘤类型、药物类型、癌细胞所属患者的人体测量值和肿瘤等级;以及-处理器,其被配置为:·基于输入的配置数据,确定所述操作参数的值,其中频率的值基于肿瘤类型和人体测量值来确定,占空比的值基于至少药物类型和肿瘤类型来确定;以及·根据所述确定的值,控制发生器和超声探头进行操作。更具体地,本发明的系统包括计算机可读存储器,该计算机可读存储器存储频率值列表和占空比值列表,因此处理器被配置为:-为肿瘤类型分配频率的值;和-为若干配置数据分配占空比的值,该配置数据包括肿瘤类型和药物类型。该系统的优选实施方式生成的超声波的功率密度小于3w/cm2。输入装置优选地是与系统集成的触摸屏。输入装置的其他实施例是笔记本电脑、平板电脑和智能手机。在本发明的优选实施方式中,要求操作者输入的第一配置数据是药物类型。药物类型选自由紫杉醇、紫杉醇白蛋白、阿霉素、脂质体阿霉素、伊立替康、脂质体伊立替康和氟尿嘧啶组成的组。从菜单列表中选择或通过键入药物类型输入后,可以要求操作者选择肿瘤类型。肿瘤类型选自由人类乳腺导管癌、雌激素非依赖性人类乳腺癌和人类胰腺癌组成的组。然后必须通过选择以下两个选项,来输入肿瘤等级:原发性肿瘤(即原始肿瘤)和继发性肿瘤(即转移瘤)。如果选择的肿瘤等级是:-原发性肿瘤,基于药物类型和肿瘤类型确定占空比。-继发性肿瘤,操作者还必须输入继发性肿瘤的定位。在这种情况下,基于药物类型、肿瘤类型和继发性肿瘤的定位,确定占空比。在这种情况下,处理器被配置为,为一组配置数据分配占空比的值,该组配置数据包括肿瘤类型、药物类型、肿瘤等级,以及最终地,继发性肿瘤的定位。例如,如果输入的肿瘤等级为原发性,输入的肿瘤类型为人类乳腺导管癌或雌激素非依赖性人类乳腺癌,输入的药物类型为紫杉醇或紫杉醇白蛋白或阿霉素或脂质体阿霉素,则分配的占空比为9%。例如,如果输入的肿瘤等级是原发性,输入的肿瘤类型是人类胰腺癌,输入的药物类型是紫杉醇或紫杉醇白蛋白或伊立替康或脂质体伊立替康或氟尿嘧啶,则分配的占空比为1%。选择肿瘤等级后,必须输入人体测量值。如果肿瘤等级是原发性肿瘤,则操作者必须指定的人体测量值根据肿瘤类型而不同;如果肿瘤等级是继发性肿瘤,则操作者必须指定的人体测量值根据继发性肿瘤的定位而不同。例如,如果肿瘤类型是人类胰腺癌,则人体测量值可以包括腹围;如果肿瘤类型是人类乳腺导管癌,则人体测量值可以包括乳围。然后基于这些人体测量值,来确定频率。在这种情况下,处理器因此被配置为,为一组配置数据分配频率值,所述该组配置数据包括肿瘤类型,和选自由腹围、体重指数、乳围、胸围和体脂率组成的组中的至少一个人体测量值。如果肿瘤扩展到不同的深度,则本发明的系统还可包括两个探头,这两个探头以对应于不同深度的不同频率进行操作。在完成上述配置数据的输入之后,还向操作者提供了选择相对于另一肿瘤的另一组参数的可能性。例如,如果第一组配置数据涉及原发性肿瘤,则还可以设置相对于所述原发性肿瘤的转移瘤的配置数据。实际上,本发明的系统可以提供两个探头,用于原发性肿瘤的第一探头,和用于转移瘤的第二探头。由第一探头发射的超声波将具有取决于药物类型和原发性肿瘤类型的占空比,而由第二探头发射的超声波将具有取决于药物类型、原发性肿瘤类型和第二肿瘤定位的占空比。各探头的操作时间还将基于输入的配置数据来确定。更具体地,根据肿瘤类型和药物类型,操作时间可包括:-一个时间窗口,在其中施用超声;或者-两个或更多个施用超声的时间窗口,所述时间窗口被一个不施用超声的时间窗口间隔开。要求操作者接受该最小操作时间,或输入另一配置数据,该配置数据包括与最小操作时间相乘的整数,从而得到操作时间。在这种情况下,处理器被配置为,为若干配置数据分配操作时间的值,该配置数据包括:肿瘤类型和药物类型。最后,在本发明的系统的优选实施方式中,所述探头可以包括多个超声换能器,所述超声换能器的第一子集被配置为超声发射器,用于将电能转换成超声波以诱导声孔效应,并且所述超声换能器的第二子集被配置为超声接收器,用于将所置入的任何介质反射的超声波转换为处理器可读的电信号,该处理器被编程为:-计算由换能器的第一子集发射的超声波,与换能器的第二子集接收的超声波之间的频率和振幅的差值;以及-调整所发射的超声的振幅和频率的值,以这种方式补偿所述差值。换能器的第一和第二子集也可以重叠为仅一个换能器。在这种情况下,探头包括一个超声换能器,其被配置为:超声发射器,用于将电能转换为超声波以诱导声孔效应;和,超声波接收器,用于将所置入的任何介质反射的超声波,转换为处理器可读的电信号,该处理器被编程为:-计算所述换能器发射的超声波,与所述换能器接收的超声波之间的频率和振幅的差值;以及-调整发射的超声的振幅和频率的值,以这种方式补偿所述差值。实施例使用两种人类乳腺癌细胞系和一种人类胰腺癌细胞系,在体外测试了本发明的系统。具体是采用了以下细胞系:-mcf-7:人类乳腺导管癌;-mda-mb-231:雌激素非依赖性人类乳腺癌;-miapaca-2:人类胰腺癌。下表总结了细胞系和药物类型的测试组合;细胞系肿瘤类型药物类型mcf-7人类乳腺导管癌紫杉醇mcf-7人类乳腺导管癌紫杉醇白蛋白mcf-7人类乳腺导管癌阿霉素mcf-7人类乳腺导管癌脂质体阿霉素mda-mb-231雌激素非依赖性人类乳腺癌紫杉醇mda-mb-231雌激素非依赖性人类乳腺癌紫杉醇白蛋白mda-mb-231雌激素非依赖性人类乳腺癌阿霉素mda-mb-231雌激素非依赖性人类乳腺癌脂质体阿霉素miapaca-2人类胰腺癌紫杉醇miapaca-2人类胰腺癌紫杉醇白蛋白miapaca-2人类胰腺癌伊立替康miapaca-2人类胰腺癌脂质体伊立替康+氟尿嘧啶对于每种结合,在三种主要实验条件下,测量了细胞死亡百分比:-药物给药(以下称为“无-us”条件);-药物给药,同时施用频率为1mhz、周期为1秒的非聚焦脉冲低强度超声,所述药物以单剂量(uniquedose)进行给药;-施用频率为1mhz、周期为1秒的非聚焦脉冲低强度超声,然后用药物进行给药;以及-药物给药,同时施用频率为1mhz、周期为1秒的非聚焦脉冲低强度超声,所述药物以相等浓度的两次剂量进行给药(以下称为“us-dc”条件)。对于不同的占空比的值,复制了除无-us以外的所有实验条件,并为三种不同的总药物浓度,复制了每一实验条件。还针对每种细胞系和每种药物类型,测试了若干操作时间。在us-dc条件下,通过第一次给药第一剂量的药物,同时施用20秒超声,然后第二次给药第二剂量的药物,同时再施用20秒超声,获得了更好的结果。结果列在下面的表格中,并在示于图1a、1b、2a、2b、3a、3b、4a、4b、5a、5b、6a、6b中。表格具体总结了,对于上面列出的三种不同药物总浓度,在us条件和us-dc条件下获得的结果。对于后一种条件,选择两个占空比的值,以显示为治疗效果更好的代表。特别地,对于细胞系mcf-7和mda-mb-231,示出了对于以下占空比值的结果:-占空比=12%(us-dc=12%)-占空比=9%(us-dc=9%)对于细胞系miapaca-2,示出了对于以下占空比值的结果:-占空比=12%(us-dc=12%)-占空比=1%(us-dc=1%)。实施例1在下表中,报告了在三种条件下,向mcf-7细胞给药三种不同浓度的紫杉醇,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇进行第一次给药,但不施用超声(无-us),然后用第二剂量的紫杉醇进行第二次给药;-us-dc=12%:用第一剂量的紫杉醇进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的紫杉醇进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的紫杉醇进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的紫杉醇进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图1a中。实施例2在下表中,报告了在三种条件下,向mcf-7细胞给药三种不同浓度的紫杉醇白蛋白,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇白蛋白进行第一次给药,但不施用超声(无-us),然后用第二剂量的紫杉醇白蛋白进行第二次给药;-us-dc=12%:用第一剂量的紫杉醇白蛋白进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的紫杉醇白蛋白进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的紫杉醇白蛋白进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的紫杉醇白蛋白进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图1b中。实施例3在下表中,报告了在三种条件下,向mcf-7细胞给药三种不同浓度的阿霉素,细胞死亡的百分比:-无-us:用第一剂量的阿霉素进行第一次给药,但不施用超声(无-us),然后用第二剂量的阿霉素进行第二次给药;-us-dc=12%:用第一剂量的阿霉素进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的阿霉素进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的阿霉素进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的阿霉素进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图2a中。实施例4在下表中,报告了在三种条件下,向mcf-7细胞给药三种不同浓度的脂质体阿霉素,细胞死亡的百分比:-无-us:用第一剂量的脂质体阿霉素进行第一次给药,但不施用超声(无-us),然后用第二剂量的脂质体阿霉素进行第二次给药;-us-dc=12%:用第一剂量的脂质体阿霉素进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的脂质体阿霉素进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的脂质体阿霉素进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的脂质体阿霉素进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图2b中。实施例5在下表中,报告了在三种条件下,向mda-mb-231细胞给药三种不同浓度的紫杉醇,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇进行第一次给药,但不施用超声(无-us),然后用第二剂量的紫杉醇进行第二次给药;-us-dc=12%:用第一剂量的紫杉醇进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的紫杉醇进行第二次给药,同时再施用plinfu20秒。-us-dc=9%:用第一剂量的紫杉醇进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的紫杉醇进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图3a中。实施例6在下表中,报告了在三种条件下,向mda-mb-231细胞给药三种不同浓度的紫杉醇白蛋白,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇进行第一次给药,但不施用超声(无-us),然后用第二剂量的紫杉醇白蛋白进行第二次给药;-us-dc=12%:用第一剂量的紫杉醇白蛋白进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的紫杉醇白蛋白进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的紫杉醇白蛋白进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的紫杉醇白蛋白进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图3b中。实施例7在下表中,报告了在三种条件下,向mda-mb-231细胞给药三种不同浓度的阿霉素,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇进行第一次给药,但不施用超声(无-us),然后用第二剂量的阿霉素进行第二次给药;-us-dc=12%:用第一剂量的阿霉素进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的阿霉素进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的阿霉素进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的阿霉素进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图4a中。实施例8在下表中,报告了在三种条件下,向mda-mb-231细胞给药三种不同浓度的脂质体阿霉素进行给药,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇进行第一次给药,但不施用超声(无-us),然后用第二剂量的脂质体阿霉素进行第二次给药;-us-dc=12%:用第一剂量的脂质体阿霉素进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的脂质体阿霉素进行第二次给药,同时再施用plinfu20秒;-us-dc=9%:用第一剂量的阿霉素脂质体进行第一次给药,同时施用plinfu(具有占空比=9%)20秒,然后用第二剂量的脂质体阿霉素进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图4b中。实施例9在下表中,报告了在三种条件下,向miapaca2细胞给药三种不同浓度的紫杉醇,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇进行第一次给药,但不施用超声(无-us),然后用第二剂量的紫杉醇进行第二次给药;-us-dc=12%:用第一剂量的紫杉醇进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的紫杉醇进行第二次给药,同时再施用plinfu20秒;-us-dc=1%:用第一剂量的紫杉醇进行第一次给药,同时施用plinfu(具有占空比=1%)20秒,然后用第二剂量的紫杉醇进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图5a中。实施例10在下表中,报告了在三种条件下,向miapaca2细胞给药三种不同浓度的紫杉醇白蛋白,细胞死亡的百分比:-无-us:用第一剂量的紫杉醇白蛋白进行第一次给药,但不施用超声(无-us),然后用第二剂量的紫杉醇白蛋白进行第二次给药;-us-dc=12%:用第一剂量的紫杉醇白蛋白进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的紫杉醇白蛋白进行第二次给药,同时再施用plinfu20秒;-us-dc=1%:用第一剂量的紫杉醇白蛋白进行第一次给药,同时施用plinfu(具有占空比=1%)20秒,然后用第二剂量的紫杉醇白蛋白进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图5b中。实施例11在下表中,报告了在三种条件下,向miapaca2细胞给药三种不同浓度的伊立替康,细胞死亡的百分比:-无-us:用第一剂量的伊立替康进行第一次给药,但不施用超声(无-us),然后用第二剂量的伊立替康进行第二次给药;-us-dc=12%:用第一剂量的伊立替康的进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的伊立替康进行第二次给药,同时再施用plinfu20秒;us-dc=1%:用第一剂量的伊立替康进行第一次给药,同时施用plinfu(具有占空比=1%)20秒,然后用第二剂量的伊立替康进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图6a中。实施例12在下表中,报告了在三种条件下,向miapaca2细胞给药三种不同浓度的脂质体伊立替康和氟尿嘧啶(fu),细胞死亡的百分比:-无-us:用第一剂量的含脂质体伊立替康和氟尿嘧啶的溶液进行第一次给药,但不施用超声(无-us),然后用第二剂量的含有脂质体伊立替康和氟尿嘧啶的溶液进行第二次给药;-us-dc=12%:用第一剂量的含脂质体伊立替康和氟尿嘧啶的溶液进行第一次给药,同时施用plinfu(具有占空比=12%)20秒,然后用第二剂量的含脂质体伊立替康和氟尿嘧啶的溶液进行第二次给药,同时再施用plinfu20秒;-us-dc=1%:用第一剂量的含脂质体伊立替康和氟尿嘧啶的溶液进行第一次给药,同时施用plinfu(具有占空比=1%)20秒,然后用第二剂量的含脂质体伊立替康和氟尿嘧啶的溶液进行第二次给药,同时再施用plinfu20秒。上表的结果以图形方式表示在图6b中。实施例13本实施例与荧光素胺(fa)的内化实验有关。图7具体示出了在五种实验条件下,fa摄入人类胰腺癌细胞中,所述条件经特别设计,以便比较施用超声的效果。测试的实验条件是:-fa-无-us-无-药物:单独给药fa,不给药任何药物,也不施用超声;-fa-li-无-us:给药fa和伊立替康脂质体(li),不施用超声;-us-dc=12%:给药fa和伊立替康脂质体(li),同时施用占空比为12%的plinfu;-us-pre-dc=1%:施用占空比为1%的plinfu,随后给药fa和脂质体伊立替康(li);-us-dc=1%:给药fa和脂质体伊立替康(li),同时施用占空比为1%的plinfu。在图7中,以图形表示了fa内化(%),即,从细胞培养孔中除去表面活性剂液体后测得的fa百分比,即在细胞内的fa的百分比。孵育2小时后,还通过共聚焦激光扫描显微镜(clsm)分析了本实施例的实验结果。图8a、8b、8c、8d、8e示出了在上述五种实验条件下,fa摄入到人类胰腺癌细胞中的情况。从图7可以推断出,在us-dc=1%的条件下,获得较高的fa内化%。从这些图像中可以看到,单独fa(以白色表示)如何没有在细胞中积累(以灰色表示)(图8a)。当fa与脂质体伊立替康一起进行给药时(图8b),观察到更高的荧光密度,但仅在细胞外膜周水平上。可以解释为,脂质体膜的聚乙二醇的聚合物链与fa之间存在更大的化学相互作用。在图8c和图8d中(分别为us-dc=12%和us-pre-dc=1%),fa在细胞内的存在变得明显,并且最高水平的fa内化示于图8e中,对应于us-dc=1%条件。在us-pre-dc=1%的条件下,实现了一定程度的fa内化,这可能是由于在施用超声后,细胞膜需要数十秒,才能恢复到声孔效应之前的渗透性。实施例14本实施例关于对乳腺癌细胞中的孔的打开和关闭的研究。对于图形(图9a、9b、9c、9d)的每个点,样品是经声孔效应处理的。所有样品都包含相同数量的细胞。在x轴上,报告了从细胞声孔效应结束,到物质添加之间的时间,其中必须在细胞中测量该物质的内化。内化的实验如下:-0分钟时:1分钟的声孔效应完成之后,立即将固定量的prohance(磁共振的造影剂)添加到细胞培养物中;1分钟后,分离细胞。-1分钟时:1分钟的声孔效应,然后在1分钟后,将固定量的prohance添加到细胞培养物中,再过一分钟后,分离细胞。-n分钟时:1分钟的声孔效应,然后在n分钟后,将固定量的prohance添加到细胞培养物中;再过一分钟后,分离细胞。除了对其他类型的细胞进行的测试以外,这些测试还表明,细胞孔的关闭时间取决于:-细胞类型;-药物分子的类型(prohance和tetramer模拟了不同组成和尺寸的药物分子的存在);-载体试剂(脂质体)的存在或缺失。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1