使用电化学传感器对分析物进行无校正的体内测量的制作方法
相关申请的交叉引用
本申请要求享有2017年10月30日递交的、序列号为62/578,665、标题为“使用电化学传感器对分析物进行无校正的体内测量”的美国临时专利申请的优先权,其内容通过引用合并于此。
关于联邦政府赞助的研究或开发的声明
本发明是在美国陆军研究办公室授予的基金号码w91lnf-09-0001美国陆军研究办公室的政府支持下完成的。政府拥有本发明的某些权利。
背景技术:
用于检测目标物分子的各种类型的电化学传感器是已知的。许多这样的传感器产生电流输出,其中电流输出的大小响应于目标物分子的结合而变化。基于电化学适体的(ea-b)传感器使用氧化还原报告分子修饰的、电极结合的适体,其中适体中结合诱导的构象变化导致氧化还原报告分子和电极之间的电子流量发生可测量的变化。ea-b传感器为本领域提供了用于测量复杂样品中目标物分析物的多功能平台。甚至已证明ea-b传感器在体内可以实时检测流动的全血中的药物和其他目标物种。但是,尽管该平台具有巨大潜力,但e-ab传感器仍存在某些限制了其临床部署的缺点。
具体地说,ea-b传感器像所有复杂的设备一样,在制造过程中也存在不一致的地方,其中即使在同一批次中制造,单个传感器上也会存在不同数量的识别元件。这种传感器之间的物理可变性意味着,从相同设计的不同传感器获得的输出可能会发生明显变化。此外,当部署在复杂的样品环境(例如全血)中时,即使是最佳的e-ab也会发生漂移,其中适体与样品中分子的复杂混合物之间的非特异性相互作用会导致随时间变化的读数。这些因素表明必须执行校正步骤或信号校正措施以解释传感器输出。在体内植入传感器的情况下,校正是不实际的或通常是不可能的,上述的误差来源给临床实施带来了严重的障碍。
因此,在本领域中仍然需要能够实现无校正测量的新颖的电化学传感器系统和操作这种传感器的方法。此外,在本领域中仍然需要一种在体内准确地测量分析物而不会被信号漂移所混淆的方法。在本领域中仍然需要改善现有传感平台的性能和效率。
技术实现要素:
现有技术的电化学传感方法依赖于电流输出(即,绝对电流值)的测量(例如swv峰值),来确定目标物浓度,这种测量受到传感器到传感器的可变性和传感器漂移的强烈影响。本公开的发明人已经有利地发现,电化学传感器的信号输出动力学的某些方面,特别是电流衰减动力学,对传感器之间的可变性和传感器漂移不敏感。像绝对电流一样,这些电流衰减动力学参数以浓度依赖的方式响应目标物结合,但是与绝对电流不同,它们在给定类别的传感器之间稳定,并且随时间稳定,从而提供一种避免在绝对电流中观察到的可变性的方法。
本公开的发明人已经有利地开发了操作电化学传感器和解释传感器输出的新颖方法,使得由不同传感器或在不同时间产生的信号能够与样品中的目标物浓度精确地相关。本发明的方法使得一类传感器(例如,采用相同的识别元件)能够被先验地有效地校正,并且被部署用于复杂的环境(例如体内全血)中对目标物物种进行扩展的、无需校正的测量。
在第一方面,本发明的范围包括获得和解释传感器输出以提供目标物分析物浓度的准确测量的方法。在另一方面,本发明的范围包括可以无漂移或无校正测量来操作的传感器系统。在另一方面,本发明的范围包括给定类别的电化学传感器,其中传感器的输出通过在该类别的所有传感器上稳定的关系与目标物浓度相关。在另一方面,本发明的范围包括使得能够获取和解释电化学传感器输出以测量目标物浓度的计算机程序、软件和操作。
附图说明
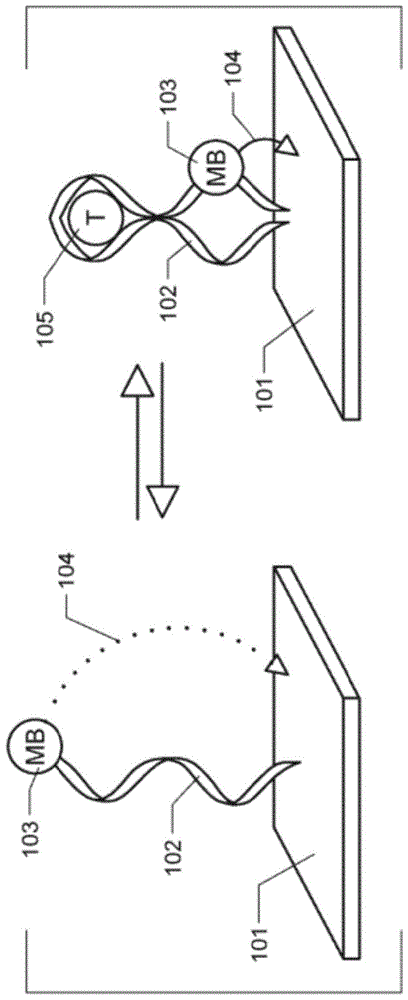
图1a和1b图1a描绘了e-ab传感平台的基本操作,其中结合至电极底物(101)的适体(102)用亚甲基蓝氧化还原报告分子(103)修饰。在没有目标物的情况下,亚甲基蓝与底物之间的电子(104)流动缓慢。当目标物(105)与适体结合时,所得到的构象变化改变了报告分子(103)与底物(101)的接近度,从而增加了电子(104)转移速率。图1b描绘了用于这种类型的e-ab传感器的代表性方波伏安曲线,其中在有目标物时的峰值电流比在没有目标物时的峰值电流高。
图2a和2b图2a描绘了使用妥布霉素作为目标物的一组六个氨基糖苷检测传感器的swv滴定曲线。使用swv产生的绝对峰值电流不仅取决于目标物分子的浓度,还取决于传感器表面上氧化还原报告分子修饰探针的数量。由于工作电极的有效面积以及包装在其上的适体探针的密度的变化,这些绝对峰值电流会因传感器不同而明显不同,从而导致原始(未校正)传感器输出出现较大变化。图2b描绘了当通过执行校正步骤而归一化的图2a的传感器输出。
图3图3描绘了通过流动的全血中结合氨基糖苷的e-ab传感器的计时电流分析法测量的时间对平均电流的电流瞬变对数-对数图。电流衰减很好地描述为两个指数相的总和。从左到右,垂直虚线左侧的第一相是双层充电电流的衰减,其中传感器对目标物不敏感。在垂直线的右边,电流瞬变高度依赖于目标物。在没有目标物的情况下获得的瞬变中,观察到法拉第电流的指数衰减较慢。在存在目标物(此处为妥布霉素)的情况下,平均电流寿命会大大缩短。通过将电位从-0.1v步进到-0.3v(报告的所有电位与ag/agcl的关系)并每10μs采样所得电流来记录所示的瞬变。实线是实验数据的多指数拟合。
图4a、4b和4c图4a描绘了结合氨基糖苷的e-ab传感器(以妥布霉素为目标物)的平均计时电流分析法测量的电流瞬变,其电流瞬变衰减,其寿命随着目标物浓度的增加而降低。实线表示两个电流瞬变的单指数拟合。图4b描绘了针对一组结合氨基糖苷的e-ab传感器建立的当前寿命与缓冲液和全血中目标物浓度之间的关系。两种样品类型之间的寿命差异可能是由于影响了亚甲基蓝的电子转移的粘度和电解质成分的变化。图4c描绘了由与用于产生图4b的标准曲线的相同类别的五个传感器测量的妥布霉素浓度,但是未用于产生标准曲线。使用这些独立的传感器通过为传感器类别生成的曲线估算流动的全血中妥布霉素的浓度,无需校正单个传感器即可在广泛的浓度范围内获得准确而精确的妥布霉素浓度的测量值。当在未稀释的全血中挑战时,在1μm至1mm范围内,测得的浓度值在妥布霉素的实际(加标)浓度的10%以内。在图4b和图4c中,误差带(其很小以至于在图4b中难以看到)代表标准偏差。
图5a和5b图5a描绘了在流动的全血(此处缺乏目标物)中的e-ab传感器输出,其中从swv记录的平均峰值电流在几个小时的过程中发生了明显漂移(未校正的信号)。应用于测量的动力学差分测量校正技术可提供校正信号。图4b描绘了随着时间的流逝,部署在全血(缺少目标物)中的相同传感器的平均电流振幅和平均电流寿命。在测试期间,计时电流的衰减振幅相当明显。但是,与此相反,电流寿命在整个时间范围内都是稳定的,并且在测试期间不会漂移。
图6a、6b、6c和6d图6a描绘了在活的、麻醉的大鼠的颈静脉中的传感器放置。将传感器装入22口径的导管中以提供结构支撑,并在2cm的深度处放置在颈静脉内。在另一侧植入输液管线以进行药物注射。图6b描绘了通过计时电流分析法产生的电流瞬变的实时非线性回归分析,以提取电流寿命并将其实时转换为目标物浓度。轨迹是20点的滚动平均值。虚线框描绘了妥布霉素注射的时间范围。图6c描绘了在每个时间点300ms时的寿命与时间的关系曲线(滚动平均值为20点),其中此方法的时间分辨率不仅足以监视药物的注射,而且还足以监视与循环系统内的药物均质化相关的随后的几十秒“混合”相。该面板对应于图6b中以虚线标记的缩放区域。图6d描绘了平均浓度与时间的关系,其中空前的时间分辨率使得可测量具有超过1,000个实验点的药物的微小尺度分布相,进而产生相关药代动力学参数的超高精度估计。
具体实施方式
操作原理本文公开的发明是通过对某些输出对传感器制造可变性和信号漂移不敏感的发现以及电化学传感器操作的广泛研究而得出的。在标准电化学传感器的实施中,电流通过目标物结合而改变,并通过伏安法评估,包括循环伏安法、交流伏安法和方波伏安法。这些方法测量峰值电流,该峰值电流与结合的、氧化还原报告分子修饰的识别元件的小部分有关,但也高度依赖于传感器上激活并存在的识别元件(例如,适体)的总数。
本公开的发明人已经开发了用于监测由目标物结合引起的电子转移的变化的替代方法。除了测量与依赖于结合的电子转移动力学间接相关的伏安峰值电流,还可以直接测量电子转移动力学,并且有利地,本公开的发明人已经发现这些值对影响峰值电流测量的误差源不敏感。本公开的发明人已经确定,通过计时电流衰减测量的电子转移动力学在很大程度上取决于目标物结合,与峰值电流不同,它与每个传感器上的激活的识别单元的数量无关。因此,可以针对选定的传感器配置确定目标物浓度与电子转移动力学之间的关系,且该关系将是稳定的,并适用于在相似条件下运行的所有相似传感器。此外,这种预测关系对于长时间运行的单个传感器也是稳定的。
本发明的这种新颖的操作原理不再需要校正单个传感器,并提供了在用于如体内的挑战性环境中无漂移操作的方法。还可以在非常精细的时标上获得测量值,从而可以通过电化学传感器在毫秒的时标上解析生物过程。
接下来描述本发明的各种元件。
电化学传感器本发明的各个实施例涉及使用电化学传感器的方法。如本文所用,电化学传感器是能够测量样品中目标物种的浓度的任何传感器,其中目标物种与传感器的识别元件的结合引起传感元件输出的电流的可测量变化,例如传感器的输出可用于估计样品中目标物的浓度。
eab传感器在第一实施方式中,在本发明的方法中使用的电化学传感器包括e-ab传感器。可以使用本领域中已知的任何e-ab传感器设计或配置。如本领域中已知的,在e-ab传感器中,识别元件包括适体。所述适体可以包含dna适体、rna适体或包含非天然核酸的适体,以及前述的杂合体。e-ab概念的变型,其中识别元件不是核酸,例如使用蛋白质、化学物质和其他分子的传感器,也在本发明的范围内。
在e-ab传感器中,工作电极的一个或多个选定的部分被适体功能化。适体可以通过任何适当的化学方法例如通过共价键合、化学吸附或吸附而与电极表面结合或以其他方式与电极表面缀合。链烷硫醇单层可用于将适体缀合到电极表面,特别适用于金电极表面。
每个适体均被一个或多个氧化还原报告分子功能化。目标物种的结合导致适体改变其构型,从而使一个或多个氧化还原报告分子的位置(或电极的可及性)被可检测地改变。氧化还原物种可以包括与电极相互作用的任何物质组成,以使得其对电极的可接近性或接近性的改变引起电子转移动力学的改变。示例性的氧化还原物种包括亚甲蓝、二茂铁、紫罗、蒽醌或任何其他醌、溴化乙锭、道诺霉素、有机金属氧化还原标记、例如卟啉配合物或冠醚循环或线性醚、钌、双吡啶、三吡啶、双咪唑、对苯二甲酸-金属络合物、细胞色素c、质体蓝蛋白和细胞色素c'。
在一些实施方式中,e-ab传感器是信号开启型传感器,使得目标物结合增强信号,并且在其他实施方式中,e-ab传感器可以包括信号关闭配置。在一个实施例中,e-ab是双链传感器,其中氧化还原物种存在于单独的链上,其一部分与适体的一部分互补或以其他方式能够可逆地结合至适体的一部分。在目标物种的存在下,氧化还原物质的链从适体中释放出来,从而使目标物种结合到适体上,并使氧化还原物质接触或接近电极。
传感器组件电化学传感器将包括一个或多个工作电极,多个识别元件结合到该工作电极上(例如,密度为0.1x1011至1x1013分子/cm2)。工作电极可以包括用于电化学传感的任何合适的电极材料,包括例如:与硫醇或胺形成键的任何金属表面、金、任何镀金金属(例如钛、钨、铂、碳、铝、铜等)、裸钯电极、碳电极等。
工作电极可以被配置成任何期望的形状或尺寸。例如,可以使用桨状电极、矩形电极、线状电极、电极阵列、丝网印刷电极和其他构造。对于体内测量,细线构造是有利的,因为低轮廓线可以插入静脉、动脉、组织或器官中,并且不会阻碍血管中的血流或对组织造成实质性损害。例如,可以使用直径为1-500μm的电线,例如100μm的电线。
本发明的电化学传感系统还包括辅助或对电极,例如铂辅助电极。电化学传感元件可以与参比电极(例如ag/agcl电极,或本领域已知的其他参比电极)一起使用。本发明的电化学传感器可以被配置在两电极或三电极系统中,其被适当地配置用于执行计时电流的测量。包含电极的电池系统可以包括混合室或其他容器,其中存在电极并与样品接触。
传感器和电极系统可以包括当部署在样品中或暴露于样品时用于获得法拉第电流测量值的组件。该组件可以包括外壳。例如,为了放置在生物体内,外壳可以包括针、导管或其他可植入结构。对于离体应用,外壳可以包括孔、微流体容器或其他结构,例如在芯片实验室设备中发现的其他结构。
本发明的电化学传感器将与适当的组件功能连接,以执行计时电流分析法测量。计时电流分析法组件可以包括彼此电连接和/或网络连接的两个或更多个设备,或者可以包括单个集成设备。
用于执行计时电流分析法测量的第一组件包括可以将期望的振幅、频率和波形的激励电压脉冲传递到传感元件的设备或设备组合。计时电流分析法组件可以包括稳压器或其他电压源以及用于将电压阶跃施加到工作电极上的电压控制器。
用于执行计时电流分析法测量的第二组件包括可以从传感元件获取时间分辨的法拉第电流输出的设备或设备组合。这些组件将包括用于读取传感器输出并存储此类输出或将输出路由到其他设备的电路,这些设备包括如模数转换器、放大器和存储介质的组件。对于大多数传感器系统中的电流衰减动力学而言,非常精细的时标分辨率是必不可少的,例如,微秒到毫秒的时标。
其他传感器类型本发明的范围不限于e-ab传感器。本发明的范围还包括任何电化学传感器,其中目标物与识别元件的结合在可通过传感元件测量的电子传递速率上产生可测量的变化。一方面,可以使用采用非介导的电化学传感的传感器,包括使用直接电子转移和氧化还原平衡作为产生信号的方式。这些生化传感器包括例如检测属于氧化还原对的物种的消耗或产生的传感器。其他传感器可以采用介导的电化学分析,即使用氧化还原物种介体进行电子转移并建立氧化还原平衡。介导的和非介导的传感器的例子可以在2015年,sander等人的“areviewofnonmediatedandmediatedapproaches”(environ.sci.technol.49:5862-5878)中找到。
其他传感器类型包括化学修饰的电极、免疫传感器、基于寡肽的传感器以及利用细胞器(例如叶绿体、线粒体)、动植物组织、微生物、酶、组织切片、肽和抗体的传感器。
其他传感器类型包括测量来自溶液相氧化还原报告分子的电子转移变化的传感器,例如,2000年,katayama等人在“thedesignofcyclicamp-recognizingoligopeptidesandevaluationofitscapabilityforcyclicamprecognitionusinganelectrochemicalsystem”(analchem.2000;72(19):4671-4)中所述的亚铁酸盐/铁氰化物氧化还原与特异性识别环状amp的17mer肽偶联。
可以使用的另一种传感器体系结构是聚合物传感器,例如2006年,lefloch在“label-freeelectrochemicaldetectionofproteinbasedonaferrocene-bearingcationicpolythiopheneandaptamer”(analchem.2006;78(13):4727-31.doi:10.1021/ac0521955)中所述的使用带有二茂铁取代基的阳离子聚噻吩作为适体系统中的介质的传感器。
可以使用的另一种传感器类型是基于由于目标物结合诱导的配体置换而引起的电子转移变化的传感器,例如,2004年,prasad在“theroleofliganddisplacementinsm(ii)-hmpa-basedreductions”(jamchemsoc.2004;126(22):6891-4.)中所述的六甲基磷酰胺与碘化钐(ii)。
另一示例性传感器类型基于氧化还原报告分子重组能量的变化,例如,2003年,plumb在“interactionofaferrocenoyl-modifiedpeptidewithpapain:towardprotein-sensitiveelectrochemicalprobes”(bioconjchem.2003;14(3):601-6.doi:10.1021/bc0256446)中所述的二茂铁-肽;或例如2012年,feld在“trinuclearrutheniumclustersasbivalentelectrochemicalprobesforligand-receptorbindinginteractions.langmuir”(2012;28(l):939-49.doi:10.1021/la202882k)中所述的三核钌簇。
可以使用的另一种传感器类型是基于空间感应的效率变化的传感器,其通过附有支架的氧化还原报告分子接近下面的电极表面来实现,例如,2010年,ge在“arobustelectronicswitchmadeofimmobilizedduplex/quadruplexdna”(angewcheminted2010;49(51):9965-7.doi:10.1002/anie.201004946)中所述的双链dna、四链dna和dna纳米开关,或2009年,cash在“anelectrochemicalsensorforthedetectionofprotein-smallmoleculeinteractionsdirectlyinserumandothercomplexmatrices”(jamchemsoc.2009;131(20):6955-7.doi:10.1021/ja9011595)中所述的含有dna的小分子识别元件。
传感器类别本发明的各种方法是基于以下发现:在给定类型的传感器中某些传感器的输出即电流衰减动力学是稳定的。如本文所使用的,一类是指具有一个或多个共享特性的多个传感器。传感器特性可能包括多种因素,包括:电极的构造和材料、待分析样品的类型、识别元件的类型、氧化还原报告分子的类型及其位置、工作电极上识别元件的堆积密度、电极功能化化学物质以及其他影响传感器输出的传感器参数。另一个类别参数可以是传感器的制造批次,其中某一个类别中的传感器是以相同份额制造的那些传感器。
在一个实施例中,一类别传感器包括多个传感器,这些传感器具有基本相同的传感器架构、相同的识别元件和氧化还原报告分子元件、用于将识别元件附接到工作电极的相同化学物质、相同的制造方法,以及相似的识别元件堆积密度(例如,按每平方厘米探针的摩尔数计算,批次内各传感器的填充密度相差1-20%)。
目标物种在本发明的方法中采用的传感器针对目标物种的检测。目标物种可以包含任何无机或有机分子,例如:小分子药物、代谢物、激素、肽、蛋白质、碳水化合物、核酸、脂质、激素、代谢物、生长因子神经递质或营养素。目标物可以包括污染物或致污物。目标物可包含毒素。目标物可包含病原体诱导的或病原体衍生的因子,或病毒或细胞。在一些实施例中,目标物种包括具有明显副作用的药物,例如化学治疗药物或具有狭窄治疗指数的药物,其中准确测量血药浓度对于确保安全剂量或最小副作用至关重要。
操作条件在选定的操作条件下利用传感器,这些条件涵盖了检测过程的各个方面。操作条件可能包含影响传感器操作和输出的因素的任何组合。
在第一方面,操作条件包括要分析的样品类型。在样品中评估本发明的目标物种。样品将包含液体。样品可能包含全血、血清、唾液、尿液、汗液、组织液、脊髓液、脑液、组织渗出液、浸软组织样本、细胞溶液、细胞内隔室、水、洗涤水、废水、地下水、食物、饮料,或其他生物和环境样品。在一些实施例中,样品源自受试者,例如人类患者或非人类动物,例如兽医的受试者或测试动物。在一个实施例中,样品包括流动的全血,即,由包括植入在受试者的活体(例如,在循环系统中)中的传感器的传感系统采样的血液。在替代实施例中,该方法用于测量气体中的目标物种,其中气体已经与液体样品平衡。
在一个实施例中,样品在测量之前被处理。处理的示例包括过滤、稀释、缓冲、离心以及在分析之前将其他材料或处理应用于样品。在一些实施例中,在执行测量之前不对样品进行处理,例如,样品未稀释、未过滤或未浓缩。
在第二方面,操作条件包括测定条件。一般的测定条件是指测定的反应条件,例如样品量、温度、ph等。
在第三方面,可以通过用于获得传感器测量值的操作参数来定义操作条件。例如,所施加的电压波形的形状和频率、电压阶跃值和采样间隔是构成操作参数的一些变量。
通过电流衰减测量目标物浓度在第一方面,本发明包括通过使用电化学传感器来测量样品中目标物种的浓度的通用方法。该方法包括以下通用步骤:
(a)确定在选定的一组操作条件下操作的选定类别的电化学传感器的选定的电流衰减量度与目标物浓度之间的数学关系;
(b)在选定的操作条件下,将选定类别的电化学传感器部署在目标物浓度未知的样品中,并获取选定的电流衰减量度值;以及
(c)应用在步骤(a)中建立的电流衰减与浓度之间的关系,可将在步骤(b)中观察到的电流衰减值用于确定样品中目标物种的浓度。
例如,在一个实施例中,本发明包括通过使用电化学传感器来测量样品中目标物种的浓度的方法,该方法包括以下步骤:
部署电化学传感器,使其暴露于样品中,其中所述电化学传感器的输出是法拉第电流,该法拉第电流以浓度依赖的方式变化到相当于样品中目标物种的浓度;
向电化学传感器施加一个或多个激励脉冲,其中通过每个脉冲产生与时间有关的法拉第电流输出;
在一个或多个激励脉冲的每一个之后,获取时间分辨的法拉第电流数据;
通过所获取的时间分辨的拉第电流数据,计算出选定的电流衰减量度值;
通过计算出的电流衰减量度值,通过应用选定的电流衰减量度与样品中目标物种浓度之间的数学关系,计算目标物种的浓度。
电流衰减量度本公开的发明人已经有利地确定,响应于激励刺激而产生的电流瞬变的衰减率与目标物种的浓度有关,并且在相同类别的传感器之间是稳定的。因此,本发明的方法依赖于电流衰减的测量值、电流衰减率与目标物浓度之间的关系以及类似传感器之间和随时间的这种关系的显着稳定性。计时电流衰减的寿命仅取决于结合和未结合识别元件(例如适体)的相对种群,而不取决于结合和未结合识别元件的绝对数量,因此提供了一种测量目标物浓度的方法,该方法与在同一类别的各个传感器之间可能发生明显变化的因素无关。
例如,在电化学传感器包括通过多个识别元件功能化的电极底物的情况下,其中每个识别元件都通过一个或多个氧化还原报告分子功能化,该氧化还原报告分子的电激励将在电极底物和氧化还原报告分子和电极底物之间引起暂时的电流流动(或在电极底物和氧化还原报告分子之间,取决于系统的配置)。在步进工作电极(例如e-ab传感器的底物)的电压时,工作电极将成为更强的还原剂(在步进到更大的负电位的情况下)或更强的氧化剂(在步进到更大的正电位的情况下)。在适当的范围内(例如,在氧化还原报告分子的氧化还原电位附近或之上),该电压阶跃将在传感器识别元件的氧化还原报告分子和电极底物之间引起法拉第电流流动。随着电流的流动,由激励移动的电子池将耗尽,并且电流将随传感器识别元件的结合状态的速率和振幅呈指数(或多指数)衰减,其中目标物结合例如通过改变氧化还原报告分子与工作电极的接近来诱导电流的更快或更慢的转移。因此,目标物结合的识别元件与未被目标物结合的识别元件的比率与样品中目标物种的浓度成比例,它将确定整个传感器的观察到的电流衰减率和振幅。
如本文所用,“电流”将指由已经部署在样品中的传感器测量的电子流。例如,电流可以包括从氧化还原报告分子到电极的电子流,或者可以包括从电极到氧化还原报告分子的电子流。本文所用的“电流衰减”是指响应于将激励刺激施加到传感器或样品上,传感器随时间测量的电流瞬变行为。
如本领域中已知的,可以使用计时电流分析的方法来实现电流衰减的测量。可以通过对传感器和/或样品施加激励并在激励之后的一段时间内测量电流响应来测量衰减参数。因此,衰减参数的测量需要与以下组件相关的样品环境或传感器:(1)传递所需电压、频率和波形的激励脉冲;(2)在与电流瞬变持续时间相对应的时间范围内测量电流响应。
激励脉冲可以是引起电流瞬变的任何类型的刺激,例如,将传感器电极的电位步进到其中氧化还原报告分子将被充分(例如,完全)氧化或还原的值。如本领域中已知的,可以选择合适的激励波形。例如,可以采用重复频率为1至10,000hz(例如5hz、10hz、20hz、50hz、100hz和在1到10,000hz之间的中间值)、+/-0.1v至0.5v范围内的电压阶跃。
通常将需要在微秒到毫秒的时标上获取时间分辨的电流测量结果。典型的电流瞬变的持续时间在10-100ms的范围内,可以通过以较短的时间间隔进行采样来解决,例如,每1μs、2μs、3μs、5μs或10μs。
一旦获取了时间分辨的电流数据,就可以对这些数据进行分析,以得出描述电流衰减动力学的许多数学参数。选定的衰减量度可以是电流瞬变的任何参数,该参数以浓度依赖的方式随样品中目标物种的浓度而变化。可以将选定的电流衰减量度评估为衰减动力学的任何量度,例如速率常数、寿命、半衰期或电流衰减的任何其他量。例如,在一个实施例中,如下所述,通过将整个衰减曲线拟合为一个函数并对该衰减曲线采用寿命(逆速率常数)或半衰期,可以得出衰减的量度。在另一个实施例中,如下所述,通过将时间分辨的数据拟合得到一个函数来得出衰减,该函数导出两个或更多指数的和,并采用相对振幅或指数分量的类似量度。
将选定的数学分析应用于所获取的时间分辨的当前数据,以得出选定的衰减量度。可以应用任何回归分析来得出选定的电流衰减量度,以解决结合的和未结合的识别元件的同时电子转移。在一个实施例中,使用对传感器电流迹线的单指数拟合来导出电流衰减的量度。在一个实施例中,使用多指数拟合来导出电流衰减的量度。在一个实施例中,使用双指数拟合来导出电流衰减的量度。在一个实施例中,使用三指数拟合来导出电流衰减的量度。可以通过单个数据点或通过对多个数据点求平均值来评估当前衰减值。例如,采样的衰减值可以包括在1-100个周期(例如5、10、20、50、75或100个周期或其中间值)之间的选定数量的激励-衰减周期上观察到的平均值。
在某些传感器系统中,识别元件的束缚状态和未束缚状态之间的相互转换动力学比传感器测得的电子转移事件要快。因此,观察到的电流瞬变反映了结合状态和未结合状态的总体加权平均值。这可以通过使用例如图4a中的单指数拟合来近似电流衰减寿命来分析。此“最佳拟合”单指数的寿命与目标物浓度单调相关。换句话说,可以最好地描述为两个指数过程之和)的电流衰减轨迹(束缚衰减和未束缚衰减)可以与单指数曲线拟合,该曲线的参数(例如,衰减常数、半衰期等)提供确定目标物浓度的方法。
在一个实施例中,通过将时间分辨的电流数据拟合到导出两个指数之和的函数并将指数分量的相对振幅用作目标物结合的量度,来得出选定的衰减量度。例如,由于观察到的电流衰减是结合和未结合衰减的组合,因此可以使用双指数拟合来描述衰减曲线,其中更快的相表示目标物结合衰减,而较慢的相表示未结合衰减。任一衰减的相对振幅,即,其相对于两相的总振幅的振幅或两相的振幅之比,可被用作目标物结合识别元件比例的量度。在替代实施方式中,可以用三个或更多指数,例如三指数拟合等来描述衰减。
例如,kamman等人在“multi-exponentialrelaxationanalysiswithmrimagingandmrspectroscopyusingfat-watersystems”(inmagneticresonanceimaging,volume5,issue5,1987,pages381-392)描述的利用指数拟合的示例性方法。
例如,在一种实现方式中,来自传感器的计时电流衰减在log-i(电流)-log-t(时间)图中进行绘制,并使用以下公式进行非线性回归分析:
对于单指数系统,通过公式1:
(公式1)
对于双指数系统,通过公式2:
(公式2)
对于三指数系统,通过公式(3):
(公式3)
其中,对于公式1-3,t是激励之后的时间,τ是时间常数,i是电流,c是恒定背景电流(如果有)。
相对振幅被计算为一个选定振幅与所有振幅之和的比值。例如,对于双指数拟合:
公式4:相对振幅
公式5:相对振幅
图3提供了电化学传感器电流衰减动力学的图示。在此示例中,将脉冲电压施加到包含亚甲基蓝氧化还原报告分子的e-ab传感器,并在脉冲之后测量电流。呈现了两条曲线,第一条曲线描绘了不包含目标物的样品的电流动力学,第二条曲线描绘了包含饱和浓度的目标物的样品的电流动力学(即,传感器的所有识别元件适体都被目标物结合)。在足够负电位下施加电压阶跃后,可实现所有亚甲基蓝报告分子的完全还原。在脉冲结束后,随时间测量这些电子的流量。在第一相中,通常是在水溶液中施加脉冲后约0.1ms,衰减很快。该相归因于在该电位偏置下在电极表面上形成的双电层的充电(即,具有微秒级的水离子的迁移)。双电层充电衰减对样品中的目标物浓度非常不敏感,通常对预测目标物浓度没有作用。在该相之后,观察到第二相,其中衰减动力学与目标物结合强烈相关,这对应于报告分子的法拉第还原,例如,亚甲基蓝到还原亚甲基蓝。在图2中,对于目标物饱和的识别元件,观察到电流快速指数衰减,寿命为100±30μ0。对于无目标物样品中的识别元件,观察到较慢的衰减,寿命为6.5±0.5ms。寿命减少约5倍(当将饱和样品与不含目标物的样品进行比较时)对应于氧化还原报告分子与电极表面的接近度变化,并反映了目标物结合的适体的数量比无目标物适体更快地转移电子。
类别校正在一个方面,本发明的范围涉及一种借助于类别中的传感器的代表性子集来校正类别的传感器的方法。校正步骤的目的是生成标准曲线,以解释该类别中所有传感器的传感器输出。因此,给定类别的传感器的校正是使用相同设计的代表性传感器,在与将要部署传感器的那些条件类似和/或代表的操作条件下测定代表性样品来进行的。一旦使用代表性子集执行了此类别校正,则可以使用该类别中的其他传感器在相似的操作条件下对目标物种执行无校正测量。
通过在选定的操作条件下为代表性样品中的选定的传感器类型建立“衰减-浓度关系”来实现类校正。衰减-浓度关系是样品中目标物浓度与由于工作电极上的电压阶跃产生的观察到的电流衰减值之间的预测关系。可以使用任何适当的回归分析来计算衰减-浓度关系。由于信号输出是结合和未结合衰减的总和,因此基于两个指数衰减曲线之和来估计单调函数的模型将非常适合计算步骤。例如,如果电流寿命是电流衰减的选定量度,则确定电流寿命与浓度之间的关系。在另一个实施例中,校正数据被拟合以提取多个指数过程,并且针对每个指数相计算的相对振幅用作衰减的量度,从而建立相对振幅与浓度之间的关系。
用于建立步骤(a)中关系的校正测量值是使用一组各种已知目标物浓度的标准液进行的。应在传感器的动态范围内对目标物浓度范围进行测量,例如,从零目标物到饱和目标物水平,例如使用加标样品。可以生成任意数量的数据点,例如可以采样2至1,000个数据点以生成校正数据。例如,可以在校正中使用25-100个数据点,例如50-75个数据点。
类别校正过程将采用一组代表性的传感器。一组代表性的传感器将包括足够数量的传感器,以提供可准确预测该类别中其他传感器的校正曲线。代表组中的传感器的数量可以例如通过本领域已知的用于基于子样本值确定样本平均值的方法来建立。代表性的组可以包括例如1、3、5、10、20、50、100或更多个传感器,以及中间的值。
图3b示出了本发明的校正曲线。对于五个e-ab氨基糖苷检测传感器,评估了全血和缓冲液中各种浓度下的当前寿命。通过寿命对langmuir等温线的浓度的非线性回归,“最佳拟合”单指数与目标物浓度单调相关。这些结果说明了不同操作条件对传感器输出的影响,其中血液和缓冲液的校正曲线不同。
在相似的工作条件下运行的给定类别的传感器将具有足够相似的衰减输出,以能够使用针对该类别的所有传感器生成的标准曲线来预测目标物。同类传感器可能具有衰减输出,当暴露于包含给定的目标物浓度的类似样品时,其具有选定的电流衰减量度的值,其相差小于20%、小于15%、小于10%、小于5%或小于1%,取决于制造的严格程度、系统固有的信噪比以及其他变量。
在一个实施例中,本发明的范围涵盖了一种类别校正的传感器。类别校正的传感器是指选定类别的传感器,例如具有选定的识别元件、选定的氧化还原报告分子、选定的电极附着化学物质、选定的电极配置以及其他定义传感器性能的参数,其中,对于该类别的传感器,选定的电流衰减量度与选定的目标物浓度之间的衰减浓度关系是已知的。在一个实施例中,类别校正传感器是基于适体的电化学传感器。
无校正测量一方面,本发明的范围包括一种无校正测量目标物物种浓度的方法。如本文所用,无校正操作是指选定类别的电化学传感器的操作,其中通过使用用于选定的传感器的特定的校正曲线将传感器输出(例如,电流衰减寿命或相对振幅)直接转换为目标物浓度值。在无校正操作中,不必在测量之前、之中或之后对传感器进行校正。
无漂移操作一方面,本发明的范围包括电化学传感器的无漂移操作,其中该传感器运行了较长的一段时间,例如数小时、数天、数月或更长时间。如图5a所示,当通过方波伏安法将传感器输出测量为振幅时,直接部署在流动的全血中的e-ab传感器将具有很大地漂移的输出。相反,如图5b所示,消除了这种严重的基线漂移,测量了电流寿命,其中电流寿命在8小时内保持稳定,而绝对传感器输出在测试期间漂移很大。
亚秒级时间分辨率本发明的方法能够直接在体内进行无校正的、亚秒分辨的分子测量。如示例中所述,通过本发明的方法,例如以100-500ms的时标,可以实时分辨血液或其他身体隔室内的目标物浓度。这种方法空前的时间分辨率使得能够在生理事件(例如药物吸收和分布、激素和神经递质释放以及在短时间范围内发生的其他生理事件)期间测量快速波动的目标物动态。通过计时电流分析法实现的精细的时标分辨率使得本发明的方法特别适合于药代动力学分析。在一个实施例中,本发明包括通过药物、代谢产物、排泄产物或其他参与药物代谢的物质的无校正测量来实时计算药代动力学参数。
传感器部署和操作在相似的操作条件下操作的一类传感器之间的电子转移动力学的固有稳定性使得能够在各种情况下使用电化学传感器。在各种实施方式中,本发明的方法使传感器在部署在不可能、繁重或昂贵的条件下时能够进行准确的测量。本发明的无校正和无漂移的方法特别适合于体内测量。例如,传感系统的传感元件或外壳可以被插入、植入或以其他方式放置在活生物体内。传感系统的传感元件可以被植入循环系统中、皮下、腹膜内、器官内或其他体室内,其中,该传感元件被暴露于体内流体中,例如间质液、血液,例如,流动的全血。本发明的植入式传感系统可以包括与人体外部的部件(例如,通过导线、电线或无线通信装置)连接的植入式传感元件,其中,外部部件执行脉冲生成、数据获取或处理。可替代地,传感元件的一个或多个辅助部件,或者甚至本发明的整个传感系统,可以被植入到体内,并且与用于数据收集的外部设备进行通信(例如,通过导线、电线或无线通信设备)。
在一个实施例中,如本领域已知的,在反馈控制的剂量系统中执行本发明的方法,其中施用药物以将血液浓度维持在治疗指数或安全指数内。例如,在这样的方法和系统中,本发明的方法是使用植入受试者中的电化学传感元件来测量目标物种的浓度的,其中目标物种是药物、药物的代谢产物或指示应服用该药物的生物标志物。当检测到的目标物种水平表明受试者需要给药物或其他药剂时,植入泵或其他药剂输送装置将按一定剂量计量的药物或药剂给药,以将药物或药剂的浓度保持在所需的范围。
在其他情况下,本发明的传感器用于例如在河流、海洋、水处理厂、工业设施、食品加工设施等中的环境或工业场所的长期和/或连续监测。
本发明的传感器也可以用于体外诊断应用中。在一个实施例中,本发明的方法包括以下步骤:从活生物体中提取样品,并通过无校正测量来测量样品中目标物种的浓度。在一个实施例中,本发明的传感器被用于即时检验系统。例如,在一个实施例中,样品是血液样品,例如自抽取的针刺或手指刺血液样品,或尿液、汗液或唾液样品。在这样的实施例中,电化学传感器可以被部署在如孔、载玻片、芯片实验室、微流体室或其他设备的外壳中。
带有校正的计时电流分析法本发明的范围不限于免校正计时电流分析法。在一种实现中,通过执行计时电流分析法的电化学传感器所获得的浓度测量的准确性通过一个或多个校正步骤的执行得以提高,即,其中将部署的传感器暴露于一个或多个已知目标物浓度的样品中,以便检查观察到的浓度值与预期的浓度值之间的偏差并校正任何此类偏差。相对于已建立的用于解调此类传感器的电化学方法,该实施例仍然带来了改进的时间分辨率计时电流分析法。
在另一个实施例中,通过校正来建立用于部署的传感器的衰减-浓度关系。可以将部署的传感器暴露于已知目标物浓度的一个或多个样品中,以便为传感器在其当前工作条件下建立衰减-浓度关系。
计算机进程和程序本发明的范围涵盖包括软件、计算机程序和编程设备的各种实施例。在一个实施例中,本发明的范围涵盖其上存储有数据和/或使得计算机执行一系列操作的编码程序的非暂时性计算机可读记录介质。该计算机可以包括任何通用计算机、处理器、嵌入式处理器、移动设备或其他计算设备。该计算机可以包含硬件元件,该硬件元件包括如键盘、鼠标、触摸屏和其他输入之类的输入设备。该计算机可以包括用于数据的输出、存储或显示的硬件元件,包括图形用户界面、显示器和存储设备。
在一个实施例中,本发明包括一种非暂时性计算机可读记录介质,其上存储有使计算机执行一系列操作的数据和/或编码程序,其中数据和/或一系列操作使电化学传感系统的操作影响本发明的方法。在各种实施例中,非暂时性计算机可读记录介质可以实现如以下的操作:控制稳压器或等效设备以将一系列步进电压脉冲传递到部署的电化学传感器;控制数据收集设备,以在传递电压脉冲后记录传感器电流输出;控制处理器执行从传感器输出数据中导出电流衰减的一个或多个选定量度的计算;存储将选定的电流衰减量度与目标物浓度相关联的校正曲线;控制处理器基于传感器输出和存储的校正曲线计算目标物浓度;存储用于执行本发明的方法的指令;以及本发明的其他操作。
在一个实施例中,本发明的范围涵盖一种被编程为执行本发明的操作的设备,例如,一种包括上述非暂时性计算机可读介质或与之相关联(例如,网络连接)的设备。
套件和系统本发明的范围扩展到被配置为执行本发明的分析物浓度测量的组件的集合。在各种实施例中,本发明的范围涵盖包括用于执行本发明的方法的两个或更多个项目的集合,另外两个组件选自由以下各项组成的组:一类别的电化学传感器,其中,传感器在选定的运行条件下获得的衰减量度与目标物浓度之间的关系是已知的;传感器外壳,用于将传感器部署到选定的样品类型;稳压器及其控制器,可以传递电信号以产生电流瞬变;数据采集和计算机可读存储介质和/或用于根据传感器电流数据计算选定的电流衰减量度的处理装置;用于从电流衰减数据计算目标物浓度的处理装置和/或计算机可读存储介质;以及用于执行本发明的方法的指令。
示例性实施例。
在一个实施例中,本发明是一种通过使用电化学传感器来测量样品中目标物种的浓度的方法,该方法包括以下步骤:
部署电化学传感器,使其暴露于样品中,其中电化学传感器的输出是法拉第电流,法拉第电流以浓度依赖的方式变化到相当于样品中目标物种的浓度;
向电化学传感器施加一个或多个激励脉冲,其中通过每个脉冲产生法拉第电流输出;
在一个或多个激励脉冲的每一个之后,获取时间分辨的法拉第电流数据;
通过获取的时间分辨的拉第电流数据,计算出选定的电流衰减量度值;
通过计算出的电流衰减量度值,通过应用选定的电流衰减量度与样品中目标物种的浓度之间的数学关系,计算目标物种的浓度。
在一个实施例中,电化学传感器包括通过多个识别元件功能化的电极,识别元件在与目标物结合后发生构象变化,其中每个识别元件都通过一个或多个氧化还原报告分子功能化。在一个实施例中,识别元件包括适体。
在一个实施例中,样品从全血、血清、唾液、尿液、汗液、组织间液、脊髓液、脑液、组织渗出液、浸渍组织样本、细胞溶液、细胞内隔间、水、洗涤水、废水、地下水、食物和饮料中选择。在一个实施例中,测量前样品未被处理。
在一个实施例中,目标物种从小分子药物、代谢物、激素、肽、蛋白质、碳水化合物、核酸、脂质、激素、代谢物、生长因子、神经递质、营养物和污染物、病原体诱导的或病原体衍生的因子、病原体或细胞中选择。
在一个实施例中,选定的目标物衰减量度是从衰减常数、平均寿命、半衰期和相对振幅中选择的。在一个实施例中,选定的目标物衰减量度是从时间分辨的电流数据的指数拟合得出的。在一个实施例中,选定的电流衰减量度是从时间分辨的电流数据的单指数拟合得出的。在一个实施例中,选定的电流衰减量度是从时间分辨的电流数据的双指数拟合得出的。
在一个实施例中,对于与已部署的电化学传感器相同类别的传感器,已经得到了选定的电流衰减量度与目标物浓度之间的数学关系。
在一个实施例中,在测量之前或之后不执行校正步骤。在一个实施例中,在较长的时间内将获得重复的测量结果。
在一个实施例中,电化学传感器部署在体内。在一个实施例中,电化学传感器部署在人类受试者中。在一个实施例中,电化学传感器部署在非人类动物中。在一个实施例中,电化学传感器部署在体外。在一个实施例中,体外部署是在即时护理系统中。
在一个实施例中,其中,电化学传感器被配置为使得当其被部署在样品中时,传感器的输出是法拉第电流,法拉第电流以浓度依赖的方式变化到相当于样品中目标物种的浓度;以及其中,对于电化学传感器所属类别的传感器,与法拉第电流衰减量度和目标物浓度相关的稳定数学关系是已知的。
在一个实施例中,电化学传感器包括用多个识别元件功能化的电极,识别元件在与目标物结合后发生构象变化,并且其中,每个识别元件都用一个或多个氧化还原报告分子功能化。在一个实施例中,类别的传感器包括具有相同识别元件类型、相同氧化还原报告分子类型和相同用于与电极共轭的附着化学物质的传感器。在一个实施例中,识别元件包括适体。
在一个实施例中,本发明是一种传感系统,包括:电化学传感器,其中,电化学系统被配置为使得当将其部署在样品中时,传感器的输出是法拉第电流,法拉第电流以浓度依赖的方式变化到相当于样品中目标物种的浓度;
硬件组件,包括用于将激励脉冲施加到电化学传感器并在每个脉冲施加之后从电化学传感器获取时间分辨法拉第电流衰减的设备;以及
非暂时性计算机可读介质,其上存储有数据和计算机程序,其能够通过电化学传感器和硬件组件来执行本文所述的方法。在一个实施例中,电化学传感器包括通过多个识别元件功能化的电极,识别元件在与目标物结合后发生构象变化,并且其中,每个识别元件都通过一个或多个氧化还原报告分子功能化。在一个实施例中,识别元件包括适体。在一个实施例中,通过本文公开的方法,将电化学传感系统编程为执行计时电流衰减分析,以得出样品中目标物种的浓度。在一个实施例中,传感系统的传感器元件被植入动物体内并且与离体硬件组件无线或有线通信。在一个实施例中,传感器中植入了用于传递电压脉冲、收集时间分辨的电流数据以及计算目标物浓度的一个或多个辅助硬件元件。在一个实施例中,除了电源(例如,电池)之外,传感器和辅助元件(包括用于传送电压脉冲的元件以及用于收集和分析时间分辨的电流数据的元件)被植入动植物体内。在一个实施例中,该系统还包括用于响应于通过本发明的方法检测到的目标物种的阈值水平而向动物施用药剂的药物递送装置,或发出需要进行药物管理的警报的装置。在一个实施例中,药物递送装置是泵。在一个实施例中,用于发出需要进行药物管理的警报的装置包括与植入的传感器系统组件有线或无线连接的可穿戴或移动设备。
在一个实施例中,本发明包括一种非暂时性存储介质,其上具有计算机可读指令,该计算机可读指令用于通过本文公开的系统和方法来操作计时电流电化学传感系统以执行计时电流衰减分析以得出样品中目标物种的浓度。
示例。示例1.使用计时电流分析法解调的e-ab传感器,可以直接在活体内实时、亚秒级地测量特定分子。
电化学的、基于适体的传感器提供了一种模块化的方法,可以连续、实时地测量特定分子目标物,而不管其化学反应性如何。该平台由适体“探针”修饰,该适体“探针”被氧化还原活性“报告分子”修饰并连接到解调电极(图1a),通过结合诱导的构象变化的信号改变了报告分子的电子转移,导致进而获得易于测量的电化学输出(图1b)。由于它们的信号传导机制模仿体内自然发生的受体采用的构象相关信号转导,因此e-ab传感器对非特异性结合特别不敏感,可轻松地支持直接在流动的未稀释血清中进行连续、延长的测量。并且,尽管当在未稀释的全血中挑战时,e-ab传感器通常表现出明显的漂移,但是本发明的发明人最近表明,当与保护膜、改进的表面钝化化学成分和/或主动漂移校正机制结合使用时,e-ab传感器可在数小时的过程中支持对全血甚至活体原位中的特定分子进行连续、实时的测量。
e-ab信号传导是由结合物诱导的适体结合的氧化还原报告分子的电子转移动力学变化所驱动。以前,循环电流、交流电或方波伏安法已用于通过观察峰值电流来“读出”此变化。这些中最常用的方波伏安法(swv)通过使传感器经受一系列电位脉冲并在由方波频率定义的延迟之后对所得法拉第电流进行采样来实现此转换。因此,观察到的电流的大小取决于电子转移速率(电子转移速率定义了到测量时电流衰减了多少),而电子转移速率又定量地取决于目标物的浓度。具体而言,当swv解调e-ab传感器时,产生的峰值电流随目标物浓度的升高而单调上升(或下降)(取决于方波频率)(图1b)。这种结合诱导的变化的相对振幅(即信号增益)取决于传感器中采用的适体,并且可以通过优化方波频率和振幅来最大化。
尽管已证明swv是将结合诱导的电子转移动力学变化转换为易于测量的输出的特别方便和可靠的方法,但这种方法并非没有局限性。首先,swv产生的峰值电流(以安培为单位)不仅取决于目标物的存在与否,还取决于传感器表面上氧化还原报告分子修饰的适体的数量,由于制造上的变化该数量会随设备与设备之间的不同而明显波动(图2a)。以前,通过在使用前校正已知(通常为零)目标物浓度的参考样品中的每个设备来解决此变化,该方法虽然有效(图2b),却增加了复杂性。其次,虽然被swv解调的e-ab传感器具有足够的选择性,可以直接部署在未稀释的血清中,但是当在体外或在体内全血中部署时,它们都显示出明显的漂移,这是以前已经使用各种漂移校正和避免漂移机制来克服的问题。最后,由于扫描swv所需的几百毫伏电位窗口所需的时间,其时间分辨率限制为几秒钟。本文证明,通过用直接测量电子转移速率的变化的计时电流分析法代替间接测量电子转移速率的变化的安培法,克服了这些限制,实现了对活体中特定分子的无校正、亚秒级分辨测量。
结果与讨论与将电子转移速率的变化转换为峰值电流的变化从而间接报告转移动力学的swv不同,计时电流分析法则直接测量电子转移动力学。通过确定响应于电极电位阶跃到氧化还原报告分子将被完全氧化或还原的值而产生的电流瞬变的寿命,可以做到这一点。对于与氨基糖苷类抗生素结合的e-ab传感器,施加足够的负电位以驱动所有亚甲基蓝报告分子完全还原,并测量合成电流(图3)。观察到的电流衰减轨迹最好描述为两个指数过程的总和。例如,在没有目标物的情况下,这些传感器表现出一个快速的指数相,寿命为100±30μs(贯穿本手稿,误差代表来自5个独立制造的传感器的标准差),而速度较慢的一个传感器的寿命为6.5±0.5ms。更快的相归因于在该电位偏置下电极表面上形成的双层充电(即时标为μs的水离子迁移)仍然对目标物浓度的变化不敏感。相反,较慢的相对应于将法拉第还原法从亚甲基蓝还原为还原亚甲基蓝。添加饱和目标物浓度后,第二相变得更快,寿命为1.20±0.01ms。寿命减少约5倍(与不含目标物的样品相比)与氧化还原报告分子到电极表面的接近度变化相符,并且可能反映了目标物结合的适体的数量,该适体比无目标物适体更快地转移电子。
从理论上讲,如果氨基糖苷结合适体的构象动力学服从两态模型,则指数相的相对振幅(反映结合的和未结合的适体的数量)将随目标物浓度单调变化。但是,二态模型假设两个指数相可以独立测量。但是,这里不是这种情况,因为在任何给定的目标物浓度下,两个指数相的寿命都非常相似,因此很难以足够的精度提取其振幅。换句话说,当适体的结合态和非结合态之间的相互转化动力学快于电子转移事件时(例如此处的情况),则构象平衡不能作为离散的静态种群进行采样。反而是,测得的寿命反映出结合状态和未结合状态的总体加权平均值。通过使用单指数拟合来近似电流衰减寿命来克服此限制(图4a)。
e-ab传感器的计时电流寿命与其目标物浓度之间的单调关系为执行e-ab测量提供了无需校正的方法。也就是说,与绝对swv峰值电流(取决于传感器上适体的总数)不同,计时电流衰减的寿命仅取决于结合和未结合适体的相对数量。因此,一旦建立了给定类型的传感器,寿命-浓度关系就可以用于确定目标物浓度,而无需校正每个单独的传感器。当用于在体外流动全血中检测妥布霉素时,寿命-浓度与氨基糖苷检测e-ab传感器之间建立了关系。具体地,对langmuir等温线进行寿命对浓度的非线性回归(图4b中的红线)并求解浓度。一批五个新的e-ab传感器(即不在初始训练组的传感器)在全血中接受妥布霉素的攻击,并使用先前确定的langmuir等温线将观测到的计时电流寿命转换为估计浓度(图4c)。这成功地确定的药物浓度在1μ定至1000μ0范围内的精确度和准确度均优于10%。
除了无需校正外,使用计时电流分析法确定的电流衰减寿命作为定义目标物浓度的一种方法,还可以防止漂移。再次,尽管被swv解调的e-ab传感器具有足够的选择性,可以在未稀释的血清中表现良好,但当直接部署在流动的全血中时,它们通常会出现严重的基线漂移(图5a)。以前,这已经使用方波伏安法进行了纠正,该方波伏安法涉及在多个频率下进行的测量(图5a)。相比之下,计时电流寿命测量固有地抵抗这种漂移。如上所述,尽管电流瞬变的总振幅明显漂移(大概是由于单分子层22的表面重组),但其指数衰减的寿命与振幅无关,因此基本上没有漂移(图5b)。
计时电流分析法解调的e-ab传感器的抗漂移性足以支持在活体动物血液中直接进行连续的、实时测量。将结合氨基糖苷的e-ab在直径为75μ5的金微丝上制成传感器,装在22号导管中以提供结构支撑,并直接部署在活大鼠的颈静脉中(图6a)。静脉注射30mg/kg后,通过进行连续两小时的连续计时电流测量来监测抗生素妥布霉素的血浆药代动力学。通过在-0.1v和-0.3v之间连续脉冲e-ab传感器的电位来实现连续测量,每个脉冲的持续时间仅为100ms。然后,对在-0.3v处产生的电流瞬变进行非线性回归分析,以实时提取电流衰减寿命,并使用先前确定的langmuir等温线将这些寿命转换为浓度(图6c)。在300ms的时间分辨率下(受适体-目标物结合动力学、数据采集和计算时间的限制),计时电流测量不仅可以解析药物注射的持续时间,还可以解析注射结束后药物“混合”并在血流中达到均一所需的时间(图6c)。
计时电流分析法解调的e-ab传感器的亚秒级时间分辨率以前所未有的精度测量药物的药代动力学。通过将体内数据拟合到两室药代动力学模型,确定妥布霉素的分布、α、消除、β、寿命。计时电流分析法解调的e-ab传感器的300ms时间分辨率支持药物的分配相的确定,α=3.74±0.04min,具有1000多个测量点以及拟合计算出的标准误差为1%。同样,药物的消除相被确定为β=69±2min,具有1.4万个测量点,将拟合的标准误差降至仅3%,这种小偏差中的很大一部分可能是由于在实验过程中动物体内的代谢波动引起的(即,β不是真正的常数)。与以前使用方波伏安法进行的体内e-ab测量相比,此精度提高了一个数量级,与先前使用抽血和离体分析的测量结果相比,这是一个很大的提高。
本文中,e-ab传感器的计时电流分析解调被用于直接在体内实现特定小分子的免校正,亚秒分辨率的测量。这种方法空前的时间分辨率表明它可以增进我们对迅速波动的生理事件的理解,例如药物吸收、激素和神经递质的释放以及中枢神经系统内药物和代谢物的运动。在从治疗药物监测到长期反馈控制药物递送等各种应用中,实时执行人体中特定分子的无校正测量的能力还可以提高给药剂量的效率和准确性。
e-ab传感器并不是唯一依靠结合诱导的电子转移动力学变化来检测分析物的生物传感器。其他示例包括用于测量溶液相氧化还原报告分子的电子转移变化、由于结合诱导的配体置换的电子转移变化、报告分子的重组能变化或与支架连接的氧化还原报告分子接近下面的电极表面在空间上引起的效率变化的传感器。从这个角度出发,我们假设计时电流分析法直接测量电子转移动力学的能力也可能在这些其他平台的研究中证明其价值。
方法。e-ab传感器的制造如下:将纯金(长度为12cm)、铂(11.5)和银(11cm)的线段切割成传感器。使用手术刀将这些电线两端的绝缘层(约2cm)去除,以实现电接触。然后将它们分别使用60%锡/40%铅松香芯焊料(直径为0.8mm)焊接到连接器电缆的三个末端之一,然后通过加热围绕电主体的可收缩管将它们连接在一起,除了在每条电线的边缘大约有5mm的小窗口。电线以分层的方式连接,首先将金线单独绝缘,然后将金线和铂线同时绝缘,最后将所有三根线绝缘在一起。这种三层厚的绝缘层的目的是为可延展探针的主体提供机械强度。为了防止电线之间的电气短路,如上所述,每根电线使用不同的长度。将金线中的传感器窗口(即,没有绝缘的区域)切成大约3mm的长度。首先将银线浸入漂白剂中过夜以形成氯化银膜,以此作为参比电极。为了增加金工作电极的表面积(以获得更大的峰值电流),传感器表面通过浸入0.5m硫酸中进行电化学粗糙化,然后将电位在einitial=0.0v至ehigh=2.0v之间对ag/agcl来回步进持续16,000个脉冲。每个潜在步骤的持续时间为20ms,没有“安静时间”。为了制造传感器,将dna构建体的等分试样在室温下用1000倍摩尔过量的三(2-羧乙基)膦还原30分钟。然后将刚刚粗糙的探针在去离子水中冲洗,然后在室温下浸入pbs中200nm的还原型dna构建体溶液中1h。此后,将传感器在4℃下于pbs中的20mm6-巯基-1-己醇中浸泡12小时,以覆盖剩余的金表面。此后,将传感器用去离子水冲洗并储存在pbs中。
对于swv测量,使用50mv的振幅,1-5mv的电位步长和10hz至500hz的变化频率,传感器相对于ag/agcl的电压为0.0v至-0.5v。所有swv测量均使用三电极设置和ch仪器(tm)电化学工作站(德克萨斯州奥斯汀(austin,tx),型号660d)进行,其中使用填充有饱和kcl溶液的商用ag/agcl参比电极和铂对电极。对于计时电流分析法,传感器的电位从-0.1v连续步进到-0.3v,每步持续100ms。对于体外测量,每10μs进行一次电流采样,对于体内测量,每100μs进行一次电流采样(以减少实验点的数量并加快数据采集的速度)。使用上述三电极e-ab传感器进行所有计时电流测量,并用gamrytmreference600+稳压器/恒流器/zra(宾夕法尼亚州沃明斯特(warminster,pa))记录。
为了研究计时电流衰减的行为,测量适体亲和力并使信号增益与目标物浓度相关,通过方波伏安法或计时电流分析法解调传感器,首先在流动的pbs中,然后在随着相应目标物浓度的增加的流动的肝素化牛血中。这些实验是在密闭系统中进行的,该系统旨在模拟在静脉中发现的血液运输类型。使用电磁齿轮泵实现血流,将流速设置为1-10mlmin-1,该流速通过流量计测量。为了构建结合曲线(适体与目标物的滴定),在分别在pbs缓冲液或血液中测量之前,新鲜制备妥布霉素的储备溶液。验证无校准行为的传感器挑战是通过挑战一批新的氨基糖苷结合e-ab传感器对抗由妥布霉素参考标准品制成的库存溶液来完成的。
在麻醉的大鼠中进行体内测量,其中将硅橡胶导管插入进行注射,或者将e-ab传感器放置在颈静脉中进行测量。使用三电极装置进行所有体内测量,其中参考电极是如上所述的涂有氯化银膜的银线,而对电极是铂线。记录长达3小时,每300ms采样一次。为了从我们的实时数据中获得药代动力学特征,使用两室模型进行非线性回归分析以适应静脉注射。回归中使用的公式如下:
cp=ae-t/α-be-t/β
其中cp是测得的血浆浓度,a和b是每个药代动力学室对最大浓度的贡献a+b=cmax,α是药物分布的一级时间常数,β是药物消除时间常数。在回归分析期间,所有变量都是浮动的,因此,通过最小化平方误差来确定最佳拟合。
在本说明书中引用的所有专利、专利申请和出版物都以相同的程度通过引用并入本文,就像每个独立的专利申请或出版物被具体地和单独地指出通过引用并入一样。呈现所公开的实施例是出于说明而非限制的目的。尽管已经参照所描述的实施例描述了本发明,但是本领域技术人员将理解,可以在不脱离本发明的整体精神和范围的情况下对本发明的结构和元件进行修改。
- 还没有人留言评论。精彩留言会获得点赞!