一种白羽肉鸡呼肠孤病毒四价灭活疫苗的制作方法
本发明属于禽类疫苗制备技术领域,具体涉及一种白羽肉鸡呼肠孤病毒四价灭活疫苗。
背景技术:
近年来白羽肉鸡呼肠孤病毒在我国某些地区的白羽肉鸡养殖场中呈区域性流行,引起的临床表现与传统的的呼肠孤病毒(白羽肉鸡呼肠孤病毒典型株s1133鸡病毒性关节炎病毒)感染有一定差异。主要表现为病鸡瘫痪、不愿走动,腱鞘炎、腓肠肌腱断裂,跗关节肿大、出血、发青直至形成黄白色纤维样干酪物,严重影响鸡群生产成绩,给我国的养鸡业造成重大损失。
现有疫苗的免疫效果下降,可能与呼肠孤病毒发生变异有关。呼肠孤病毒属于双链rna病毒,点突变的快速积累是rna病毒的一个代表性特征,由基因突变和重组而引起的抗原漂移在呼肠孤病毒中时有发生,最终导致新的毒株出现和疫苗失效。目前鸡病毒性关节炎由经典ⅰ群s1133类血清型疫苗防控,这些疫苗在世界上大部分地区已被证明是有效的。然而,针对抗原性上有差异的鸡呼肠孤病毒不同分离株,s1133类血清型疫苗只能提供部分保护。由于活疫苗的研制周期较长并且很难达到预期的效果,因此,筛选变异的新型鸡呼肠孤病毒并制备疫苗对于白羽肉鸡呼肠孤病毒病的防控具有重大意义。
技术实现要素:
本发明提供一种白羽肉鸡呼肠孤病毒四价灭活疫苗,从而弥补现有鸡呼肠孤病毒疫苗的不足。
本发明提供一种白羽肉鸡呼肠孤病毒四价灭活疫苗,包含有灭活的四种病毒株抗原和疫苗佐剂,其中抗原为保藏编号为cctccno:v201908的bb18株、保藏编号为cctccno:v201909的heb18株和保藏编号为cctccno:v201910的sd18株和s1133株;
其中四种病毒株的病毒含量不低于4×107.0tcid50/0.1ml;
其中病毒株是使用甲醛溶液进行灭活。
所述的疫苗佐剂为油相佐剂,其一种组成是94份兽用白油,1份硬脂酸铝、5份司本-80。
本发明的四价灭活疫苗,其制备方法如下:
1)病毒增殖及收获:将bb18株、heb18株、sd18株和s1133株在鸡胚成纤维细胞cef上进行病毒繁殖,获得病毒液;
2)病毒的浓缩:将收获的4种病毒液在2~8℃条件下,用超滤浓缩机浓缩,浓缩的病毒液准备进行灭活;
3)病毒灭活:将浓缩的病毒液导入灭活罐内,计量加入10%甲醛溶液,充分混合,甲醛溶液的最终浓度为0.1%;37℃摇床内,200rpm震荡灭活20小时后取出,放2~8℃保存;
4)油相制备:取兽用白油95份,硬脂酸铝1份,置于油相制备罐中加热至80℃后,再加司本-805份,至温度达到115℃时,维持30min,冷却后备用;
5)水相制备将步骤3)灭活的鸡呼肠孤病毒sd18株、bb18株、heb株和s1133株抗原液各96份分别与灭菌后的4份吐温-80混合,在水相制备罐中搅拌至吐温-80完全溶解;
6)乳化:取油相2份放于高速剪切机内,开动电机慢速转动搅拌,同时徐徐加入水相1份,以10000r/min进行乳化制成疫苗。
本发明所提供的四价灭活疫苗能够对我国白羽肉鸡呼肠孤病毒不同血清型的分离株提供完全保护,从而减少养殖业的损失。
附图说明
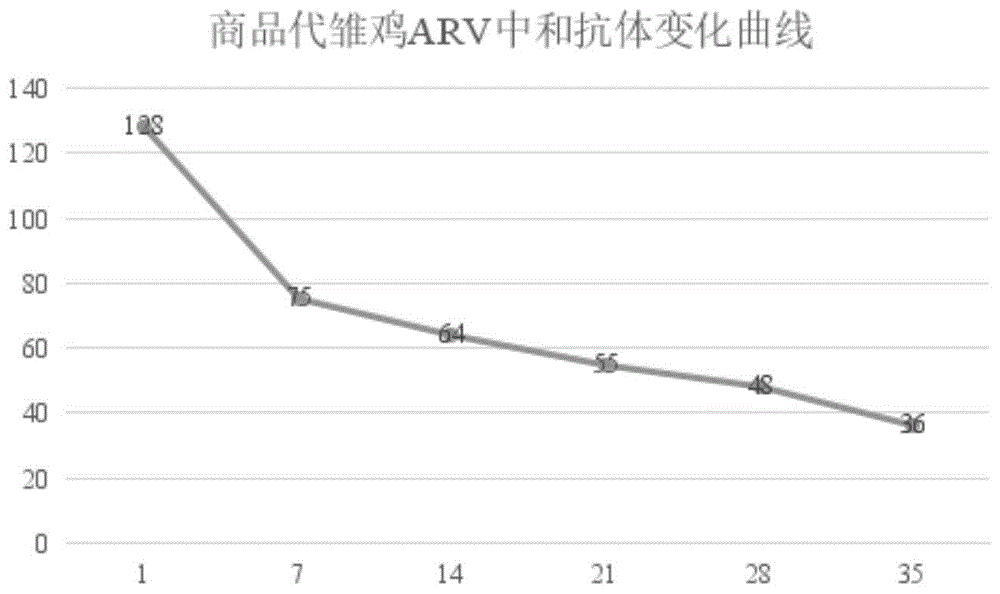
图1:免疫鸡呼肠孤病毒疫苗的父母代种鸡所产雏鸡母源抗体的中和抗体滴度变化规律图;其中横坐标是雏鸡日龄,纵坐标是中和抗体滴度。
具体实施方式
下面结合实施例对本发明进行详细的描述。
实施例1:病毒株的分离及鉴定
申请人筛选获得了3株白羽肉鸡呼肠孤病毒,在对应的发病鸡群的父母代种鸡均免疫过鸡病毒性关节炎活苗s1133株和油苗s1133株+1733株+2408株,经测定父母代种鸡开产前血清呼肠孤病毒抗体以及它们的商品代白羽肉鸡1日龄血清呼肠孤病毒母源抗体抗体均为强阳性(有效中和抗体效价≥5.0log2),理论上,此中和抗体水平完全可以阻断对型经典ⅰ群s1133类毒株野毒的攻击,从而使鸡群不发病,但是临床上不同日龄的父母代和商品代鸡群仍然发生鸡呼肠孤病毒感染,说明鸡病毒性关节炎经典毒株疫苗s1133株、1733株和2408株产生的抗体不能够对目前的肉鸡呼肠孤病毒变异株提供完全保护作用。
最终从患有瘫痪的白羽肉鸡病鸡病例中成功分离鉴定并纯化到3株白羽肉鸡呼肠孤病毒,分别命名为bb18株、heb18株、sd18株,经鉴定分别定义为鸡呼肠孤病毒ⅱ、ⅲ、ⅴ群,与传统的ⅰ群鸡呼肠孤病毒s1133在基因序列、抗原性和致病性上存在很大差异,尤其在抗原性上,血清交叉中和试验表明不同毒株之间存在明显的差异,分属于不同的血清型。使用分离到的白羽肉鸡呼肠孤病毒和经典株s1133株来制备四价灭活疫苗。
鸡呼肠孤病毒bb18株已于2019年2月20日保藏于中国武汉、武汉大学的中国典型培养物保藏中心,保藏编号为保藏编号为cctccno:v201908;
鸡呼肠孤病毒heb18株已于2019年2月20日保藏于中国武汉、武汉大学的中国典型培养物保藏中心,保藏编号为保藏编号为cctccno:v201909;
鸡呼肠孤病毒sd18株已于2019年2月20日保藏于中国武汉、武汉大学的中国典型培养物保藏中心,保藏编号为保藏编号为cctccno:v201910.
鸡呼肠孤病毒s1133购自中国兽医药品监察所。
实施例2:疫苗的制备及检测
1、疫苗的制备
1.1鸡胚成纤维细胞(cef)的制备:取9日龄spf鸡胚,用碘酒消毒气室部位蛋壳,再用75%酒精脱碘消毒,剪碎气室部位蛋壳,取出鸡胚,剪断鸡胚与卵黄连接的脐带,将鸡胚放置干净的平皿上。倒入适量微温的pbs液,除去头、翅膀、腿和胚体内脏器官,将剩余胴体用pbs液清洗3次。用剪刀将组织剪成1mm3左右的小块,用pbs液洗涤3次。加入适量37℃水浴加热的0.25%胰酶溶液,水浴锅中消化25~30min。时间到后,加入10%血清的dmem培养基终止消化,离心去掉上清,加入无血清的dmem溶液来回吹打,使细胞散开,将组织细胞悬液经200目和400目细胞筛后,收集过筛液,1500rpm离心10min,弃掉上清,用8%血清的dmem培养基将沉淀的细胞重悬,按照1×106/ml的细胞密度接种于细胞培养瓶中,在37℃、5%co2条件下进行培养。
1.2病毒增殖及收获:将本实验室先前成功分离鉴定并纯化到3株白羽肉鸡呼肠孤病毒(bb18株、heb18株、sd18株)以及经典s1133株在鸡胚成纤维细胞(cef)上进行病毒繁殖,以获得足量滴度高且纯净的病毒液。将制备的cef细胞培养过夜后,待细胞密度达到85%左右,倒掉瓶内细胞培养液,用无血清的dmem培养基洗涤三次,按照1%剂量接种病毒,37℃吸附1h,期间每隔10min轻轻摇摆细胞瓶,以使病毒吸附完全,吸附完毕后倒掉接毒液,加入1%胎牛血清的dmem培养基连续培养并观察,48h-60h后细胞病变达到80%-90%左右进行收毒,将细胞瓶放入-80℃超低温冰箱,反复冻融三次,使病毒完全从细胞内释放出来,4℃离心机内5000rpm离心30min,小心的将上清液转移至无菌瓶内。同时按现行《中国兽药典》进行无菌检验。标记好编号sd18株、bb18株、heb18株、s1133株,4℃保存备用。
1.3病毒的浓缩:将收获的4种病毒液在2~8℃条件下,用超滤浓缩机浓缩,浓缩4倍,留样,进行半成品检验,其余病毒液随即进行灭活。
1.4病毒灭活将鸡呼肠孤病毒液导入灭活罐内,计量加入10%甲醛溶液,充分混合,甲醛溶液的最终浓度为0.1%。37℃摇床内,200rpm震荡灭活20小时后取出,放2~8℃保存。
1.5半成品检验
(1)无菌检验按现行的《中国兽药典》附录中的方法进行无菌检验,确定制备的病毒液无细菌感染。
(2)病毒含量测定将收获的病毒液(灭活前取样)用灭菌生理盐水作10倍系列稀释,取10-5、10-6、10-7、10-8、10-95个稀释度,将稀释好的样品加到制备好的已长成cef细胞单层(一般24h即可)的96孔细胞板上,每个稀释度6孔,100μl/孔。同时设立正常细胞对照6孔。加样顺序应按照先加正常细胞对照,再由高稀释度到低稀释度加入细胞板。细胞培养板置37℃、5%co2培养箱中吸附1h后,补加2%胎牛血清的dmem细胞培养液100μl,置37℃、5%co2培养箱中培养,连续观察至第7日,判定结果。记录每块96孔细胞培养板中细胞的病变情况,并计算tcid50,四种病毒的病毒含量应不低于4×107.0tcid50/0.1ml。
(3)灭活检验准备9日龄的单层cef细胞3瓶,接种灭活的病毒液0.2ml,连续观察7日,同时收取细胞液再盲传2代,观察7日,观察并记录细胞病变情况。结果灭活彻底,细胞无病变。
1.6灭活疫苗的制备:经过检验合格后的半成品抗原进行疫苗制备(以下配制中各液体成分按体积比计)。
(1)油相制备取兽用白油95份,硬脂酸铝1份,置于油相制备罐中加热至80℃后,再加司本-805份,至温度达到115℃时,维持30min,冷却后备用。
(2)水相制备将灭活的鸡呼肠孤病毒sd18株、bb18株、heb18株和s1133株抗原液各96份分别与灭菌后的吐温-804份混合,在水相制备罐中搅拌至吐温-80完全溶解。
(3)乳化取油相2份放于高速剪切机内,开动电机慢速转动搅拌,同时徐徐加入水相1份,以10000r/min,乳化5分钟。乳化后,取10ml,以3000r/min离心15分钟,管底析出的水相不超过0.5ml。
(4)配苗将经过以上步骤制成鸡呼肠孤病毒sd18株、bb18株、heb株和s1133株单品油苗按照1:1:1:1的比例进行再次乳化,进行两两乳化(例如sd18株与bb18株、heb18株与s1133株)最后将sd18+bb18与heb18+s1133乳化,乳化过程中要少量多次混合乳化,以使四种抗原乳滴分布均匀。
1.7疫苗成品检验
1.7.1性状
外观:制备的疫苗为乳白色乳剂,无杂质。
剂型:为油包水型。取一清洁吸管,吸取少量疫苗滴入冷水中,除第1滴外,均不扩散。
稳定性:吸取疫苗10ml加入离心管中,以3000r/min离心15分钟,管底析出的水相不超过0.5ml。
黏度:按现行《中国兽药典》附录进行检测,符合相应的规定。
1.7.2无菌检验:按现行《中国兽药典》附录进行,结果符合规定。
1.7.3安全检验:用7日龄spf鸡10只,每只颈部皮下注射二联疫苗1.0ml,同时设对照5只,在相同的条件下饲养,连续观察14日,记录试验鸡采食、饮水及临床情况。应不出现由疫苗引起的任何局部和全身不良反应。结果表明,试验组和对照组鸡只发育正常,精神状态良好,剖检试验组发现注射部位疫苗吸收良好,无红肿、组织坏死等炎症反应。说明试制疫苗安全无害,对动物生长无影响。
1.7.4效力检验
用21日龄spf鸡10只,每只颈部皮下注射鸡呼肠孤病毒疫苗,0.3ml/只,另取5只同日龄鸡不免疫作对照,免后21日,采血分离血清,分别测定抗体。免疫组的抗体效价不低于5.0log2vn抗体。对照组应均为阴性。
2、病毒中和试验及中和抗体临界值试验
将鸡呼肠孤病毒sd18株、bb18株、heb18株和s1133株,经继代和纯化按上述方法制成灭活疫苗,分别免疫21日龄spf鸡,免疫剂量0.5ml/只,每隔2周免疫一次,共免疫3次,三免后2周进行采血分离血清。将sd18株、bb18株、heb18株和s1133株病毒液分别稀释至200eld50/0.1ml,逐一与sd18株、bb18株、heb18株和s1133株的阳性血清等体积混合,37℃震荡中和1小时后,每个中和组接种10日龄spf鸡胚5枚,0.2ml/枚,每隔24h照胚一次,弃掉24h以内死亡的鸡胚,连续观察至168小时。结果发现用sd18株阳性血清与sd18株病毒中和后接种的5枚spf鸡胚均无死亡;用bb18株阳性血清与bb18株病毒中和后接种的5枚spf鸡胚均无死亡;用heb18株阳性血清与heb18株病毒中和后接种的5枚spf鸡胚均无死亡;用s1133株阳性血清与s1133株病毒中和后接种的5枚spf鸡胚均无死亡;用s1133株的阳性血清与sd18株、bb18株和heb18株病毒中和后鸡胚出现死亡。
同上,sd18株、bb18株和heb18株的阳性血清与非本毒中和后,鸡胚均出现了死亡。这表明鸡呼肠孤病毒经典s1133株与本发明所使用的sd18株、bb18株、heb18株的交叉中和能力均很差,它们的抗体只能对本毒产生很好的中和能力,而对非本毒的中和能力很则差,四种毒株的中和谱均很窄,没有广谱性,可能与病毒本身的特性有很大关系。
表3:鸡呼肠孤病毒sd18株、bb18株、heb18株与s1133株的交叉中和试验
注:“√”表示完全中和,“×”表示不能中和。
在96孔微量细胞培养板上,用稀释液将血清作一系列倍比稀释,使其稀释度分别为原学清的1:2、1:4、1:8、1:16、1:32、1:64、1:128、1:256,每个稀释度做3~4个平行孔。以生理盐水将病毒稀释到200eld50/100μl,将每个稀释度的血清加入等体积的病毒液混合,轻轻混匀病毒-血清混合物,37℃5%co2培养箱中孵育2h。将混合液接种9日龄spf鸡胚绒毛尿囊膜,0.2ml/枚,每个稀释度接种5枚,37℃培养箱中培养,连续观察7天,以能保护50%鸡胚不死亡的最高血清稀释度的倒数作为中和终点。试验中设定鸡胚对照(不接种任何液体)、阴性对照(200eld50病毒+阴性血清)和空白对照(200eld50病毒),每个对照接种spf鸡胚5枚,0.2ml/枚。
结果判定和计算:在各对照成立的情况下,实验组若出现鸡胚死亡,则表明血清未能中和病毒,若鸡胚未出现死亡,则表明血清能够中和病毒。用reed-muench法计算固定病毒-稀释血清法中和抗体效价,结果如表4所示。
表4:分离株接种spf鸡胚死亡率统计表
eld50=-6+1/6×(-0.3)=-6.05,即1:106.05的血清稀释可以保护50%的鸡胚不发生死亡,该sd18株血清的中和抗体效价为1:106.05。用同样的方法,计算出bb18株、heb18株和s1133株血清中和抗体效价分别为1:106.35,1:106.15,1:106.0。因此,将四种毒株对应血清中和抗体的临界保护值定为1:24(即抗体在该临界值以上可以完全中和病毒),该临界值大于疫苗效力5.0log2vn,即只要鸡只血清鸡呼肠孤病毒中和抗体效价不低于1:24,鸡群就不发生病毒性关节炎疾病。
3攻毒保护试验
将鸡呼肠孤病毒s1133株、sd18株、bb18株和heb18株在9日龄spf鸡胚成纤维细胞单层上进行培养,并进行tcid50的测定,各毒株抗原含量为10-7.0tcid50/0.1ml,用终浓度1.5‰的甲醛37℃灭活20h,按照油相:水相=2:1的比例制备成灭活疫苗,并与市售的默沙东新支法关(s1133株+1733株)商品疫苗进行试验比较。将180只7日龄的spf鸡分为4大组(免疫组),30只/组,每组鸡分别胸肌注射s1133株、sd18株、bb18株、heb18株和新支法关(s1133株+1733株)鸡呼肠孤病毒灭活疫苗,0.5ml/只,并设对照组(不做任何处理),2周后进行第二次免疫0.5ml/只,二免后第3周采血分离血清并用s1133株、sd18株、bb18株、heb18株鸡呼肠孤病毒尿囊膜毒脚垫攻毒,并设正常spf鸡胚尿囊膜研磨液为攻毒对照,剂量为0.1ml/只。每日观察鸡群精神状态、采食及发病情况,尤其是鸡只脚垫在攻毒前后的变化,持续20天,并记录试验数据。
表5:攻毒前各组鸡呼肠孤病毒reo抗体s/p值(elisa法)
表6:鸡呼肠孤病毒s1133株、sd18株、bb18株、heb18株与新支法关s1133+1733之间的攻毒保护试验结果表
注:表示保护数/攻毒总数,攻毒对照组鸡脚垫均无肿胀现象。
攻毒保护试验结果表明,鸡只免疫呼肠孤病毒s1133株、sd18株、bb18株和heb18株灭活疫苗能对s1133株、sd18株、bb18株和heb18株本毒提供完全的保护,这四组攻本毒鸡只未表现任何临床症状,也无死亡现象,而对非本毒只能够提供部分保护,攻非本毒组发病鸡只关节肿胀、跛行,跗关节发热,划破后流出血红色液体,其中夹杂着血凝块,与临床发病病例剖检完全一致。这说明肉鸡呼肠孤病毒s1133株、sd18株、bb18株和heb18株之间的攻毒保护性很差,也说明本发明所使用的鸡呼肠孤病毒毒株(sd18株、bb18株、heb18株)为经典毒株s1133的变异株,它们与经典毒株在攻毒保护上有着显著的差异,因此对于现阶段我国鸡呼肠孤病毒的疫苗预防中,应添加经典毒s1133株、sd18株、bb18株和heb18株四个血清型的病毒株作为疫苗抗原,方能对目前流行的白羽肉鸡病毒性关节炎疾病起到很好的预防和保护作用。而且市售的商品疫苗新支法关对s1133毒株、sd18毒株、bb18株和heb18株均不能提供完全的保护作用,从二免后的血清抗体水平来看,商品疫苗新支法关组鸡群抗体水平明显低于单苗s1133组、sd18组、bb18组和heb18组,这可能与商品疫苗新支法关疫苗中鸡呼肠孤病毒的抗原含量偏低有很大关系,由于四联疫苗要求的疫苗工艺比较高,需要将鸡呼肠孤病毒高度浓缩,抗原含量方能达标,使之与单苗的抗原含量一致才能激发足够高的血清循环抗体水平,从而产生很好的保护作用。因此,必须改善商品疫苗的生产工艺,提高四联疫苗或四价疫苗中单个抗原的病毒含量,才能保证疫苗的质量和使用效果。
4疫苗的免疫持续期及雏鸡母源抗体的监测和攻毒保护试验
将健康的aa+父母代种鸡分为两组,分别注射商品疫苗新支法关(s1133+1733)(a组)和鸡病毒性关节炎四价灭活疫苗(sd18+bb18+heb18+s1133),90日龄和145日龄各一针,0.5ml/次,收集免后4-8周的种蛋各100枚,在孵化箱中孵化出雏,将这100只雏鸡在隔离器中饲养至35日龄,期间每周采血测定中和抗体滴度,然后随机分为5组,用s1133、sd18、bb18、heb18毒株脚垫攻毒,攻毒剂量为10-6.5eld50/0.1ml,并设对照组(注射生理盐水)。观察并记录攻毒后鸡只脚垫、跗关节有无肿胀、红肿发生(图1)。
表7:鸡呼肠孤病毒在商品代雏鸡上的攻毒保护试验表
经过两次免疫的两组种鸡,a组鸡群开产前(185日龄)血清鸡呼肠孤病毒中和抗体达到最高,越往后中和抗体开始逐渐下降,大约有30%比例的鸡只中和抗体水平不达标(低于5.0log2vn),到第250天以后,90%以上鸡只中和抗体水平降到保护线以下;而b组鸡群从开产一直到350日龄血清中和抗体滴度均在保护线以上,350天以后开始逐渐平缓下降,整个生产周期能够保证80%以上的鸡群血清中和抗体水平不低于5.0log2vn,疫苗的抗体产生快且高,免疫持续时间长,能够对鸡群产生持久的保护力。攻毒后,a组商品代雏鸡均有发病情况,脚垫肿胀,跗关节和跟腱肿胀,瘫痪、瘸腿,有的歪曲变形,鸡群精神状态差,羽毛逆立,生长发育受阻,参差不齐;而b组商品代雏鸡均正常,没有出现异常情况。说明该四价灭活疫苗能够对商品代雏鸡提供完全的保护作用,而商品化的新支法关免疫效果很差。
- 还没有人留言评论。精彩留言会获得点赞!