一种植物复合抗敏剂的制备方法及其应用与流程
本发明属于日化添加剂领域,更具体地说,它涉及一种植物复合抗敏剂的制备方法及其应用。
背景技术:
化妆品不良反应和化妆品皮肤病是困扰化妆品研发人员和品牌商的一大持续性难题,也是消费者的噩梦,伴随着功能性护肤时代的来临,化妆品不良反应出现的频率和次数将持续攀升。其中,化妆品不良反应包括有过敏、瘙痒、干燥、刺痛、红疹、溃烂、泛红、起屑、红肿、长痘等现象。
解决这些现象的核心一共有两点:一是远离过敏原,减少过敏原的添加;二是在配方中添加抗敏成分,以提高抗过敏的效率。
但是因为化妆品中每个用到的成分,都因人而异有一定的过敏率,因此在配方中添加抗敏成分是目前一种普遍做法。
目前抗敏剂以植物来源的接受度最高,相对最为安全。但是依然有极少数人对植物来源的抗敏剂本身有一定的过敏率,其原因包括农残、化肥残留、植物本身的精油成分及色素变质等,如何进一步提高植物抗敏剂的功效,降低其过敏率,是业内研发的持续追求,具有现实的指导意义。
技术实现要素:
针对现有技术存在的不足,本发明的目的在于提供一种植物复合抗敏剂的制备方法,提供了一种通过植物组合和配比来实现抗敏高效协同作用,提高抗敏效果,降低了使用风险。
为实现上述目的,本发明提供了如下技术方案:一种植物复合抗敏剂的制备方法,植物复合抗敏剂所用的药材包括如下质量份数的组分:金银花10~20份,蒲公英5~15份,锦葵15~20份,芦荟10~20份,白芍10~20份,紫花地丁10~20份,母菊5~20份;
其制备工艺包括:药材于提取罐内与提取溶剂一起进行自循环提取,得到提取液;然后切换阀门提取液进入精制罐,同时提取和精制,形成提取精制大循环,提取精制结束后减压浓缩,得到精制液。
进一步的,其中锦葵可以用欧锦葵代替。
进一步的,芦荟的品种可以是库拉索芦荟,或者木立芦荟。
本发明配方通过金银花、白芍、紫花地丁协同杀菌抑菌,净化肌肤的微生物环境;通过母菊、白芍、金银花、蒲公英协同抗炎消肿;通过芦荟、锦葵协同加强和修复屏障功能;通过白芍和蒲公英协同止痒镇痛舒缓;通过金银花、母菊、紫花地丁协同清除自由基,改善肌肤环境;通过锦葵、蒲公英、芦荟、紫花地丁、白芍富含的钙离子,促进皮肤的增生,加快屏障的修复。由此通过上述多种植物组合物复配的方式,实现了抗敏复配的协同作用,提高了整个复合抗敏剂的抗敏效果,降低了在使用过程中人员过敏的风险发生。
另外其制备工艺,首次进行提取,将药材(植物)放置在提取罐中,在提取溶剂的作用下浸泡循环(自循环方式),直至药材中的有效成分能够进入到提取溶剂中,得到含有多种药物成分的提取液。接着将上述提取液经由泵抽到精制罐中,此时再由提取精制大循环,此时不仅有利于杂质的去除,还因为杂质减少后提取液中总溶质下降,提高有效成分的提取效率,此时在日化学品中添加较少的复合抗敏剂即可达抗敏的效果,大大提高了抗敏的效果。
进一步的,所述提取溶剂为水、丁二醇、丙二醇中的一种或多种;所述提取溶剂的用量为药材质量的10~15倍。
通过采用上述技术方案,水、丁二醇、丙二醇均是常用的溶剂,具有良好的溶解性能,适合药材(植物作为原材料)的提取,为下一步精制做好了准备。
进一步的,提取温度为50~80℃,自循环时间为20~40min,循环速度6~10溶剂质量/h。
通过采用上述技术方案,不仅操作方便,节约能源,而且提取的效率高。
进一步的,精制器内填充有至少一层的填料层,所述填料层选自碳纤维层、沸石层、硅藻土层或高岭土层。
进一步的,精制器内从上到下依次填充有碳纤维层、沸石层、硅藻土层、高岭土层和硅藻土层。
进一步的,在精制器内,碳纤维层的用量为0.1~0.2m2/kg的药材,沸石层中沸石的用量为0.5~1kg/kg的药材,高岭土层中的高岭土的用量为0.1~0.3kg/kg的药材,硅藻土层中的硅藻土的用量为0.2~0.5%kg/kg的药材。
通过采用上述技术方案,多层填料层的设置提高了精制器的精制效率,可以同时除去色素、精油、农药残留、氨氮、微生物、固体杂质等,同步完成澄清度、除杂、灭菌的效果。
进一步的,多层填料层上的滤孔呈阶梯式分布。
通过采用上述技术方案,阶梯式孔径分布增加了提取液在精制器内的停留时间和流动的路径,由此有利于提高过滤的速度。
进一步的,所述精制器内安装有一个用于分散所述提取液的分布器,所述分布器的进料口与所述精制器的上端进料管连通。
通过采用上述技术方案,分布器的设置,提高了提取液在精制器内的分散程度,使得提取液能够均匀地分布在精制器内,提高了精制器的精制效率,同时也避免了大量提取液集中堆集在一起而影响过滤效率的情况发生。
进一步的,所述精制器下方设有金属孔板支撑层,所述填料层位于金属孔板支撑层的上方,金属孔板支撑层的下端外壁抵接在精制器靠近其出料管口的内壁上。
通过采用上述技术方案,金属孔板支撑层的设置,提高了精制器对填料层的支撑作用,使得填料层能够稳定的位于精制器内,且不会随着提取液的流动而发生移动。
进一步的,所述填料层与金属孔板支撑层之间设有陶瓷膜层,所述陶瓷膜层的孔径为0.22微米。
通过采用上述技术方案,陶瓷膜层的设置,减少了填料层内的物质直接随着精制循环过程流失,设置流入到导管内堵塞导管的现象发生,由此提高了精制器的稳定性,以及填料层填充的稳定性。
进一步的,在精制器的进料管处安装有换热器一,所述换热器一内提取液的温度控制在30~40℃,所述精制器的出料管口处设有换热器二,所述换热器二的另一端连接在提取罐的进料口上;提取精制大循环的速度为3~6溶剂质量/h,时间为2~3h。
通过采用上述技术方案,换热器一和换热器二的设置,有效的控制了提取液和精制液的温度,有助于降低体系内温度的变化对精制反应的影响,以及提取反应内温度变化的影响,从而提高了反应的效率。
本发明的一种植物复合抗敏剂在日化领域上的应用,尤其是在护肤品、化妆品上的应用。
优化的,本发明的一种植物复合抗敏剂在霜、面膜、乳液、凝胶上的应用。
综上所述,本发明具有以下有益效果:
1、本发明提供了一种通过植物组合和配比来实现抗敏高效协同作用,提高抗敏效果,降低了使用风险;
2、优化的,阶梯式孔径分布增加了提取液在精制器内的停留时间和流动的路径,由此有利于提高过滤的速度;
3、本发明的制备工艺,首次进行提取,将药材(植物)放置在提取罐中,在提取溶剂的作用下浸泡循环(自循环方式),直至药材中的有效成分能够进入到提取溶剂中,得到含有多种药物成分的提取液。接着将上述提取液经由泵抽到精制罐中,此时再由提取精制大循环,此时不仅有利于杂质的去除,还因为杂质减少后提取液中总溶质下降,提高有效成分的提取效率,此时在日化学品中添加较少的复合抗敏剂即可达抗敏的效果,大大提高了抗敏的效果。
附图说明
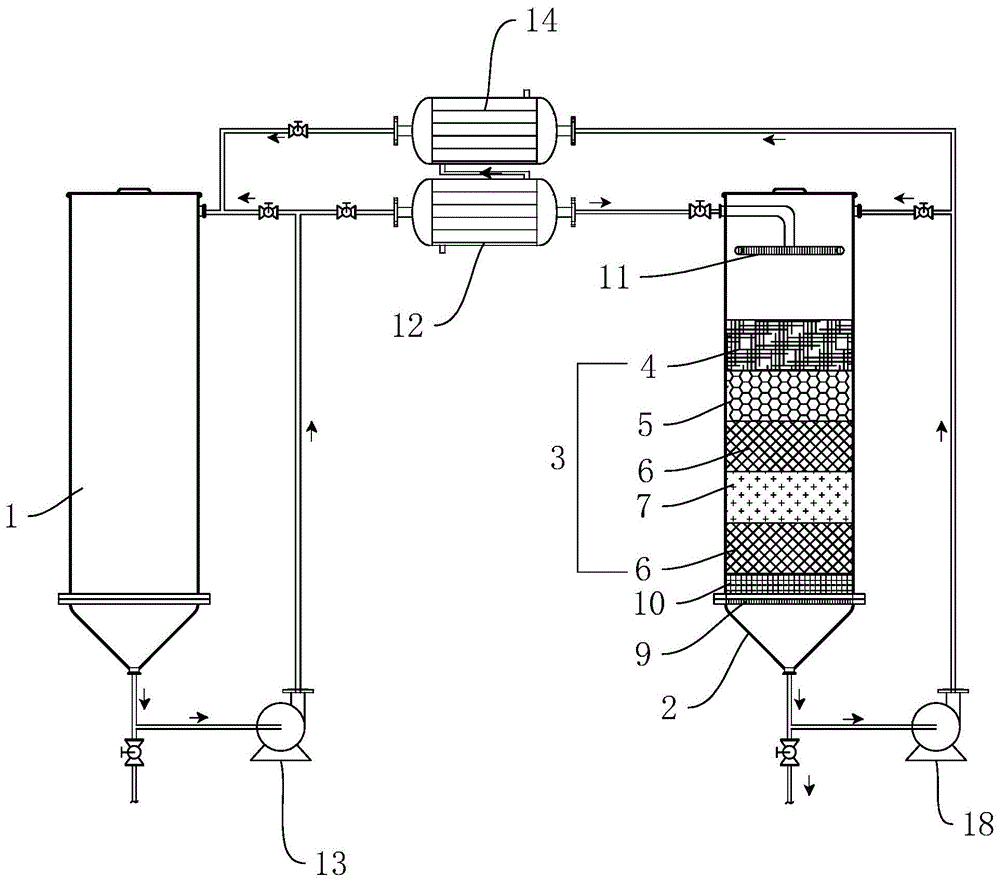
图1为一种用于制备植物复合抗敏剂的装置中实施例1的结构示意图。
附图说明:1、提取罐;2、精制器;3、填料层;4、碳纤维层;5、沸石层;6、硅藻土层;7、高岭土层;9、金属孔板支撑层;10、陶瓷膜层;11、分布器;12、换热器一;13、提升泵一;14、换热器二;15、挡板;16、空腔;17、筛盘;18、提升泵二。
具体实施方式
以下结合各实施例和附图对本发明作进一步详细说明。
一种用于制备植物复合抗敏剂的装置,如图1所示,按照工艺流程的方向依次包括提取罐1、换热器一12、精制器2、换热器二14。提取罐1上的出料口处设有具有阀门一的管道一,管道一的另一端安装有提升泵一13,在提升泵一13的另一端安装有具有阀门二的管道二,管道二的另一端连接在提取罐1的进料口处,此时打开提升泵一13、阀门一和阀门二,此时开启了提取小循环(即自循环提取过程)。
如图1所示,在提升泵一13和阀门二之间的管道二上连通有一个具有阀门三的导管三,导管三的另一端连接有换热器一12,并与换热器一12的进液口连通,同时换热器一12的出液口上连接有一个具有阀门四的导管四,导管四的另一端通入到上端具有分布器11的精制器2内,并通过精制器2内的分布器11进行均匀分散。
为了提高过滤效率,如图1所示,在精制器2内从上到下依次填充有碳纤维层4、沸石层5、硅藻土层6、高岭土层7和硅藻土层6。其中,碳纤维层4的用量为0.1-0.2m2/kg的药材,沸石层5中沸石的用量为0.5-1kg/kg的药材,高岭土层7中的高岭土的用量为0.1-0.3kg/kg的药材,硅藻土层6中的硅藻土的用量为0.2-0.5%kg/kg的药材。上述碳纤维层4、沸石层5、硅藻土层6、高岭土层7和硅藻土层6填料层3的设置,提高了精制器2的精制效率,可以同时除去色素、精油、农药残留、氨氮、微生物、固体杂质等,同步完成澄清度、除杂、灭菌的效果。同时,碳纤维层4、沸石层5、硅藻土层6、高岭土层7和硅藻土层6上的滤孔呈阶梯式分布,由此增加了提取液在精制器2内的停留时间和流动的路径,由此有利于提高过滤的速度。
为了提高支撑强度,如图1所示,在精制器2下方设有金属孔板支撑层9,上述金属孔板支撑层9为不锈钢材质支撑的网筛板,上述碳纤维层4、沸石层5、硅藻土层6、高岭土层7和硅藻土层6等填料层3位于金属孔板支撑层9的上方,并且金属孔板支撑层9的下端外壁抵接在精制器2靠近其出料管口的内壁上,由此可使填料层3能够稳定的位于精制器2内,且不会随着提取液的流动而发生移动。
如图1所示,为了精制器2的稳定性,在填料层3与金属孔板支撑层9之间设有陶瓷膜层10,上述陶瓷膜层10的孔径为0.22微米。上述陶瓷膜层10的存在大大减少了填料层3内的物质直接随着精制循环过程流失,设置流入到导管内堵塞导管的现象发生,由此提高了精制器2的稳定性。
另外如图1所示,精制器2的下端的出料管口处设有具有阀门五的管道五,管道五的另一端连接有一个提升泵二18,提升泵二18的另一端安装有具有阀门六的管道六,管道六的另一端连接在精制器2的上端进料口处,此时开启了精制过滤小循环,可以用于精制液的质量。
如图1所示,在提升泵二18和阀门六之间的管道六上连通有一个具有阀门七的管道七,管道七的另一端连接有换热器二14,并与换热器二14的进液口连通,同时换热器二14的出液口上一个具有阀门八的导管八,导管八的另一端连接在提取罐1的进料口处,以上构成了提取精制大循环,通过大循环过程,不仅有利于杂质的去除,还因为杂质减少后提取液中总溶质下降,提高有效成分的提取效率。
一、实施例1-3
实施例1:一种植物复合抗敏剂所用的药材,包括金银花10份,蒲公英5份,锦葵15份,芦荟20份,白芍20份,花地丁20份,母菊10份。
同时,上述实施例1的植物复合抗敏剂的制备方法,包括如下步骤:称取药材加入提取罐中,加15倍的纯化水,在提取温度70℃,8倍溶剂质量/h的循环速度下,自循环30min后进行大循环,其中大循环的速度为5倍溶剂质量/h,时间为2.5h。同时在精制器中,碳纤维用量为0.2m2/kg的药材,沸石用量为0.5kg/kg的药材,高岭土0.2kg/kg的药材,硅藻土0.4%kg/kg的药材,结束后提取液减压浓缩至0.5g药材/ml。
实施例2:一种植物复合抗敏剂所用的药材,包括金银花20份,蒲公英15份,锦葵15份,芦荟15份,白芍15份,紫花地丁15份,母菊5份。
同时,上述实施例2的植物复合抗敏剂的制备方法,包括如下步骤:称取药材加入提取罐中,加10倍的30wt%的丙二醇溶液,在提取温度50℃,6倍溶剂质量/h循环速度下,自循环40min后进行大循环,大循环的速度为3倍溶剂质量/h,时间为3h。同时在精制器中,碳纤维用量为0.1m2/kg的药材,沸石用量为1kg/kg的药材,高岭土0.1kg/kg的药材,硅藻土0.5%kg/kg的药材,结束后提取液减压浓缩至0.5g药材/ml。
实施例3:一种植物复合抗敏剂所用的药材,包括金银花15份,蒲公英15份,锦葵20份,芦荟10份,白芍10份,紫花地丁10份,母菊20份。
同时,上述实施例3的植物复合抗敏剂的制备方法,包括如下步骤:称取药材加入提取罐中,加12倍的30wt%的丁二醇溶液,在提取温度80℃,10倍溶剂质量/h循环速度下,自循环20min后进行大循环,大循环的速速为6倍溶剂质量/h,时间为2h。同时在精制器中,碳纤维用量为0.15m2/kg的药材,沸石用量为0.75kg/kg的药材,高岭土0.3kg/kg的药材,硅藻土0.2%kg/kg的药材,结束后提取液减压浓缩至0.5g药材/ml。
二、对比例1-3
对比例1:一种植物复合抗敏剂所用的药材,包括金银花5份,蒲公英20份,锦葵10份,芦荟24份,白芍8份,紫花地丁8份,母菊25份。
同时,上述对比例1的植物复合抗敏剂的制备方法,包括如下步骤:称取药材加入提取罐中,加15倍的纯化水,在提取温度70℃,8倍溶剂质量/h循环速度下,自循环30min后进行大循环,大循环的速速为5倍溶剂质量/h,时间为2.5h。同时在精制器中,碳纤维用量为0.2m2/kg的药材,沸石用量为0.5kg/kg的药材,高岭土0.2kg/kg的药材,硅藻土0.4%kg/kg的药材,结束后提取液减压浓缩至0.5g药材/ml
对比例2:一种植物复合抗敏剂所用的药材,包括金银花10份,蒲公英5份,锦葵15份,芦荟20份,白芍20份,紫花地丁20份,母菊10份。
同时,上述对比例2的植物复合抗敏剂的制备方法,包括如下步骤:称取药材加入提取罐中,加20倍的纯化水,在提取温度90℃,5倍溶剂质量/h循环速度下,自循环50min后进行大循环,大循环的速速为8倍溶剂质量/h,时间为4h。同时在精制器中,碳纤维用量为0.3m2/kg的药材,沸石用量为0.3kg/kg的药材,高岭土0.4kg/kg的药材,硅藻土0.1%kg/kg的药材,结束后提取液减压浓缩至0.5g药材/ml。
对比例3:一种植物复合抗敏剂所用的药材,包括金银花10份,蒲公英5份,锦葵15份,芦荟20份,白芍20份,紫花地丁20份,母菊10份。
同时,上述对比例3的植物复合抗敏剂的制备方法,包括如下步骤:称取药材加入提取罐中,加15倍的纯化水,在提取温度70℃,8倍溶剂质量/h循环速度下,自循环提取3h后过滤,滤液减压浓缩至0.5g药材/ml。
三、检测数据
试验一、理化指标检测数据
试验对象:实施例1-3制作得到的植物复合抗敏剂作为试验样品1-3;对比例1-3制作得到的植物复合抗敏剂作为对照样品1-3。
检测方法:
①氮检测方法:hj535-2009水质氨氮的测定(纳氏试剂分光光度法);
②精油类成分含量测定:5倍质量的环己烷萃取提取液m1,分液,重复2次,合并环己烷层,常温减压浓缩除去环己烷,得m2精油;
精油类成分含量=m2÷m1*106ppm
③活性物含量=(m总黄酮+m总糖+m总皂苷+m钙)÷m提取液*100%,其中总黄酮用亚硝酸钠-硝酸铝法,总糖用苯酚-硫酸法,总皂苷用香草醛-冰醋酸-高氯酸法;
④含量测定:gb5009.92-2016食品安全国家标准-食品中钙的测定;
⑤定性考察:分别在4℃、48℃、常温光照、-18~48℃交替,考察的指标为颜色、澄明度、ph值、气味,并登记在表1中。
试验结果:由表1可以看出,本配方和工艺下,试验样品1-3做出的提取液颜色较浅,颜色为浅黄,而对照样品做出的提取液的颜色3为棕黑、对照样品做出的提取液的颜色为浅棕,由此可知试验样品1-3的稳定性相比于对照样品2-3而言有极大的提升。试验样品1-3的总活性物含量和钙含量维持在2.7-2.9%;对照样品1-2的总活性物含量和钙含量维持在1.9-2.2%,由此可知试验样品1-3的总活性物含量和钙含量都比对照样品1-2要高。试验样品1-3与对照样品2-3而言,试验样品1-3对安全性有隐患的氨氮和精油类成分则大幅度的降低,由此实现了产品安全、高效、美观、稳定性好的优点。
表1试验样品1-3以及对照样品1-3的理化指标汇总
试验二、植物复合抗敏剂的安全性和功效性测试
试验对象:实施例1-3制作得到的植物复合抗敏剂作为试验样品1-3;对比例1-3制作得到的植物复合抗敏剂作为对照样品1-3。
阳性对照:b、c组为曲安奈德软膏,e组为芦丁,f组为乙基己基甘油。
试样方法:
a、刺激性:按《化妆品安全技术规范》2015年版,进行豚鼠皮肤多次刺激性实验,统计刺激强度。
b、抗敏止痒:组胺耐受测试
取豚鼠分组:实验组、醋酸曲安奈德尿素软膏组及蒸馏水阴性对照组,脱毛后各组分别涂抹所试药物4次,每日2次,每次0.025ml,面积约1.1cm2,自然成膜后用纱布包裹,胶布固定,提取物给药组局部贴敷1.2cm2,然后包扎,并固定。第3日将右后足背部脱毛处皮肤用细砂纸轻轻摩擦使之发红,但以不出血为度,然后再向创面涂抹所试药物0.2ml,40min后轻轻除去所试药物,每隔3min依次由低浓度到高浓度向每只豚鼠足背部涂抹组胺0.03ml,当豚鼠出现瘙痒反应时,累积每只豚鼠所给予的组胺量,即为该豚鼠耐受组胺的量。
c、抗炎:二甲苯致小鼠耳廓肿胀实验
在小鼠右耳涂相应各组药物,0.2ml/只,每天一次,连续3天,末次给药后30min,在小鼠右耳的前后两面涂100%二甲苯致炎液0.02ml/只,左耳不作任何处理,4小时后处死动物,立即剪下双耳,用8mm打孔器取相同部位耳片,在分析天平上称重,以右耳片重量减去左耳片重量为肿胀度,以(右耳重-左耳重)/左耳重×100%为肿胀率。
d、皮肤屏障功能测试
30名身体健康干性皮肤志愿者,测试仪器为corneometer(ck),测定tewl值(经皮水分丢失),测试时间点为样品使用前记作a0,样品使用后的4w记作a1,4周tewl值降低率=(a1-a0)÷a0*100%。
e、dpph·自由基的清除测试
用移液器取90μl浓度为2×10-4mol/ldpph加入到96孔板中,再分别加入10μl不同浓度的芦丁标准品或待测药物,每个浓度设置三个平行;设置control组和空白组,control组加无水乙醇不足体积,空白组加90μldpph溶液和10μl乙醇溶液。室温反应30min,反应后迅速在md酶标仪517nm下测定吸光度。
dpph自由基清除率/%=[1-ai/ao]×100%
a0-(空白对照扣掉control组吸光值);ai-(药物组扣掉control组吸光值)
至少测定3个浓度下的dpph自由基清除能力,计算出ic50,即dpph的抑制率为50%时的样品溶液浓度,ic50越小,抗氧化能力越强。
f、抑菌测试——最低抑菌浓度(mic值)的测定
试验菌株为金黄色葡萄球菌(atcc6538),采用微孔板法。在微孔中加入金黄色葡萄球菌100μl和药液100μl,同时设不加菌的阴性对照和不加药液的正常生长对照,每种药做3个平行,取平均值。含金黄色葡萄球菌样品置35℃培养箱孵育,24h后观察结果。采用肉眼观察直接法读取数据。结果判断的前提是生长对照良好,空白对照无菌生长清晰,其它孔随药物浓度梯度升高而菌的生长受到抑制。
试验结果:如表2中a组实验对比可以看出,试验样品1-3的刺激为0,对照样品2的刺激性为0.1;对照样品3的刺激性为0.3,由此可知工艺技术对安全性的影响比较大;同时结合表1,主要体现在氨氮和精油类物质的残留上,试验样品1-3对安全性有隐患的氨氮和精油类成分明显低于对照样品2-3,由此可知,试验样品1-3具有降低刺激性的作用。另外在bcdef组中,由试验样品1-3和对照样品1可以看出,在抗敏止痒、屏障加强、净化自由基以及抑菌的方面,试验样品1-3在0.5%溶液豚鼠组胺耐受度在29.4-31.4μg,其明显大于对照样品1-3的胺耐受度;试验样品1-3在20%溶液小鼠耳肿胀度(即左耳片重量在1.7-2.0mg),其明显大于对照样品1-3的左耳片重量。试验样品1-3在1%溶液人体4周tewl值降低率在29.4-30.7%,其明显大于对照样品1-3的tewl值降低率。试验样品1-3的金黄色葡萄球菌mic值在0.2%,阳性对照组的金黄色葡萄球菌mic值在0.156%
,对照样品1-3的金黄色葡萄球菌mic值为0.78%,其数值与阳性对照组接近,且明显小于对照样品1-3的金黄色葡萄球菌mic值。因此试验样品1-3的组方比例有明显的功效协同作用。
综上由试验样品1-3和对照样品1-3可以看出,本工艺条件下的组方的功效明显优于其他条件和传统工艺。
表2安全性和功效性测试
四、应用例1-3
应用例1:一种霜,包括如表3所示的组分及其含量。
表3应用例1的一种霜的组分及其含量
上述霜的制作方法,包括如下操作步骤:
步骤1.预混物1的制备:先将丁二醇与透明质酸钠按照表3中的用量以300r/min的速度下混合搅拌均匀,15min后得到预混物1。
步骤2.预混物2的制备:将鲸蜡硬脂醇、硬脂醇聚醚-21、硬脂酰谷氨酸钠、丁羟甲苯、角鲨烷、辛酸/癸酸甘油三酯、异壬酸异壬酯,以及牛油果树果脂按照表3中的用量以300r/min的速度下混合均匀,20min后得到预混物2。
步骤3.预混物3的制备:在反应锅内加入总量为1.00w/w%的的环五聚二甲基硅氧烷和环己硅氧烷混合物(环五聚二甲基硅氧烷和环己硅氧烷的比例为1:1)按照300r/min的速度搅拌,然后再在上述反应锅内继续加入总量为1.5w/w%的聚二甲基硅氧烷和聚二甲基硅氧烷醇混合物(聚二甲基硅氧烷和聚二甲基硅氧烷醇的比例为1:1),搅拌30min后得到预混物3。
步骤4.在预混物1中加入甘油、羟苯甲酯和去离子水,在300r/min的速度下搅拌混合均匀,15min后得到a相混合物。
步骤5.接着将a相混合物在300r/min的搅拌速度下依次加入主锅,并升温至85℃。
步骤6.将预混物2加入油锅,升温搅拌至85℃至完全溶解,加入丙烯酸羟乙酯/丙烯酰二甲基牛磺酸钠共聚物,按照300r/min的速度搅拌分散均匀后加入主锅,中速均质6~10次/秒,3min后加入预混物3,继续均质3-5min,得到b相混合物。
步骤7.将总量为0.50w/w%的苯氧乙醇、氯苯甘醚混合物(苯氧乙醇、氯苯甘醚之间的比例为1:1),以及表3所示的玫瑰香精加入到1.00w/w%的实施例3中植物抗敏剂中按照300r/min的搅拌速度下,搅拌20min后得到c相混合物。
步骤8.将步骤6中得到的b相混合物降温至45℃加入c相混合物,按照300r/min搅拌至分散均匀出料,得到霜。
应用例2:一种凝胶,包括如表4所示的组分及其含量。
表4应用例2的一种凝胶的组分及其含量
上述凝胶的制备方法,包括如下操作步骤:
步骤1.预混物1的制备:将甘油、丁二醇、透明质酸钠以及羟苯甲酯,以表4的用量在450r/min的速度下混合搅拌均匀,15min后得到预混物1。
步骤2.预混物2的制备:将茉莉花香精和peg-40氢化蓖麻油按照表4中的用量,在500r/min的速度下混合搅拌均匀,15min后得到预混物2。
步骤3.制备c相混合物:将总量为0.5w/w%的水,燕麦(avenasativa)β-葡聚糖的混合物(其中水,燕麦(avenasativa)β-葡聚糖的比例为1:0.5:0.5),以及0.20w/w%的泛醇、1.00w/w%的实施例3中植物抗敏剂中按照500r/min的搅拌速度下,搅拌20min后得到c相混合物。
步骤4.将主锅内的丙烯酸酯/c10-30烷基丙烯酸酯交链共聚物加入去离子水润湿后,按照500r/min的速度搅拌15min,然后升温至80℃后再按照表4中的用量加入水,然后在500r/min的速度下搅拌至溶解。
步骤5.将温度降至60℃,加入10%氢氧化钠,500r/min的速度下搅拌至分散完全,之后加入步骤3中的c相混合物,按照500r/min的速度下搅拌至溶解完全,得到凝胶。
应用例3:一种面膜,包括如表4所示的组分及其含量。
表4应用例1的一种面膜液的组分及其含量
上述面膜液的制备方法,包括如下操作步骤:
步骤1.预混物1的制备:将甘油、丁二醇、黄原胶、透明质酸钠以及羟苯甲酯,以表4的用量在450r/min的速度下混合搅拌均匀,15min后得到预混物1。
步骤2.制备c相混合物:将总量为0.5w/w%的水,燕麦(avenasativa)β-葡聚糖的混合物(其中水,燕麦(avenasativa)β-葡聚糖的比例为1:0.5:0.5),以及0.2w/w%的泛醇、1.00w/w%的实施例3中植物抗敏剂中按照500r/min的搅拌速度下,搅拌20min后得到c相混合物。
步骤3.将主锅内的丙烯酸酯/c10-30烷基丙烯酸酯交链共聚物加入去离子水润湿后,按照450r/min的速度搅拌15min,然后升温至80℃后再按照表4中的用量加入a相剩余原料(水、氯苯甘醚),然后在500r/min的速度下搅拌至溶解。
步骤4.将温度降至60℃,加入10%氢氧化钠,500r/min的速度下搅拌至分散完全,之后加入步骤3中的c相混合物,按照500r/min的速度下搅拌至溶解完全,得到凝胶。
具体实施例仅仅是对本发明的解释,其并不是对本发明的限制,本领域技术人员在阅读完本说明书后可以根据需要对本实施例做出没有创造性贡献的修改,但只要在本发明的权利要求范围内都受到专利法的保护。
- 还没有人留言评论。精彩留言会获得点赞!