一种丹参提取物、其制备方法及应用与流程
本公开属于抗氧化物提取技术领域,具体涉及一种具有良好抗氧化活性的丹参提取物、该提取物的制备方法及应用。
背景技术:
公开该背景技术部分的信息仅仅旨在增加对本公开的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
氧化应激与多种疾病,如心血管疾病、糖尿病、癌症、神经退行性疾病及自身免疫疾病等的发生、发展密切相关。因此,寻找安全、高效经济的天然抗氧化剂对于多种疾病的治疗具有重要的意义。丹参,唇形科植物丹参(salviamiltiorrhizabge.)的干燥根和根茎,具有具有去淤止痛,活血通经,清心除烦等功能,在对700多种中草药进行的抗氧化筛选中,丹参表现出很强的抗氧化活性,是一种很有开发前途的抗氧化剂。
丹参的有效成分主要包括脂溶性和水溶性两类,脂溶性成分多为丹参酮类,如丹参酮ⅱa、隐丹参酮等;水溶性成分主要为丹酚酸类,如丹酚酸b、丹参素、阿魏酸等丹。2015年版《中华人民共和国药典》(一部)要求以丹参酮ⅱa和丹酚酸b为指标,对丹参药材进行质量控制。说明丹参酮ⅱa和丹酚酸b在丹参的药效中发挥重要作用。研究表明,丹参酮ⅱa和丹酚酸b均有抗心肌缺血、防治冠心病等方面的作用。在体内外,丹参酮ⅱa和丹酚酸b都表现出较好的抗氧化活性。而且,丹参酮ⅱa和丹酚酸b有协同作用,可以更显著地降低氧化应激指标。
技术实现要素:
基于上述现有技术,获取一种集成提取丹参酮ⅱa和丹酚酸b的提取物对于开关相关抗氧化药物具有重要的意义。由于丹参酮ⅱa为脂溶性成分,而丹酚酸b为水溶性成分,两者极性不同,对提取溶剂的要求也不相同。提供一种高效、同时提取上述两种成分的方法对于工业生产具有重要的意义。
基于此,本公开以丹参酮ⅱa和丹酚酸b为指标,应用响应面法对丹参的提取工艺展开了研究,提供了一种制备方法简单、同时兼顾脂溶性的丹参酮ⅱa和水溶性的丹酚酸b含量的提取方法。研究表明,该方法获取的丹参提取物能够有效的提取丹参中的抗氧化成分,总体具有较强的抗氧化活性;并且该提取物可兼顾丹参酮ⅱa和丹酚酸b的提取,为后续纯化获取丹参酮ⅱa和丹酚酸b纯品提供了便利。
为了实现上述技术目的,本公开提供以下技术方案:
本公开第一方面,提供一种丹参提取物的制备方法,所述制备方法包括向丹参中加入乙醇溶液进行提取,所述乙醇溶液的浓度为65~85%。
现有技术中针对丹参中提取物研究多采用正交实验优化提取参数,本公开采用响应面法对丹参提取物的制备方法进行了研究,响应面法研究结果与实际实验拟合情况良好,实验误差较小,能较好地反映丹参酮ⅱa和丹酚酸b的提取情况。
进一步的,所述乙醇提取浓度为67%。
优选的,所述乙醇溶液的量为丹参质量的8~15倍。
进一步的,所述乙醇溶液的最佳量为丹参的12倍量。
优选的,所述提取时间为30~60min。
进一步的,所述提取时间为48min。
本公开第二方面,提供第一方面所述制备方法得到的丹参提取物。
本公开第三方面,提供第二方面所述丹参提取物在制备抗氧化应激药物/保健品中的应用。
优选的,所述抗氧化应急药物包括但不限于防治心血管疾病、糖尿病、癌症、神经退行性疾病及自身免疫疾病等方面的药物。
与现有技术相比,本公开的有益效果是:
1.丹参酮ⅱa和丹酚酸b是丹参中具有代表性的抗氧化及抗心血管疾病成分,还具有协同作用。作为极性不同的两种成分,采用同一溶剂对其进行提取具有一定的难度,本公开提供了一种可以兼顾两种成分的提取方法,可同时实现丹参酮ⅱa和丹酚酸b的共同提取。
2.本领域公知,药用植物中的成分繁多,不同提取条件下溶出的物质都不尽相同。本公开的研究表明,该提取条件下获取的丹参提取物是一种不仅能够兼顾丹参酮ⅱa和丹酚酸b的提取效率,还能够实现丹参中前抗氧化活性成分的溶出,该提取物抗氧化活性优于同等浓度的维生素c,可剂量依赖性地清除dpph和abts自由基。
附图说明
构成本公开的一部分的说明书附图用来提供对本公开的进一步理解,本公开的示意性实施例及其说明用于解释本公开,并不构成对本公开的不当限定。
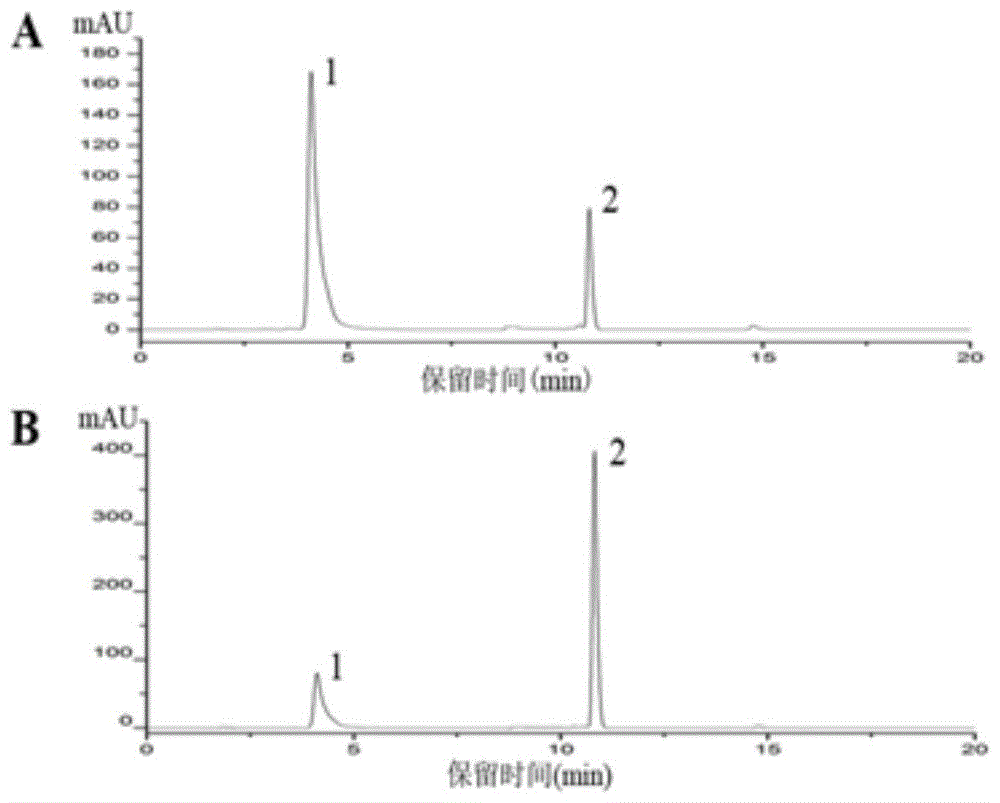
图1为实施例1中标准品高效液相色谱图;
其中,图1a为286nm波长下标准品高效液相色谱图;
图1b为270nm波长下标准品高校液相色谱图;峰1代表丹酚酸b,峰2代表丹参酮ⅱa。
图2为实施例1中样品高效液相色谱图;
其中,图2a为286nm波长下样品高效液相色谱图;
图2b为270nm波长下样品高校液相色谱图;峰1代表丹酚酸b,峰2代表丹参酮ⅱa。
图3为实施例1中两因素交互作用对丹参酮ⅱa提取影响的响应面图;
其中,图3(a)为乙醇浓度-提取时间响应面图;
图3(b)为乙醇浓度-料液比响应面图;
图3(c)为提取时间-料液比响应面图。
图4为实施例1中两因素交互作用对丹参酸b提取影响的响应面图;
其中,图4(a)为乙醇浓度-提取时间响应面图;
图4(b)为乙醇浓度-料液比响应面图;
图4(c)为提取时间-料液比响应面图。
图5为实施例1中丹参提取物对dpph自由基的清除率折线图;
图6为实施例1中丹参提取物对abts自由基的清除率折线图。
具体实施方式
应该指出,以下详细说明都是例示性的,旨在对本公开提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本公开所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本公开的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
正如背景技术所介绍的,丹参中的丹参酮ⅱa和丹酚酸b具有良好的抗氧化活性及抗心血管疾病活性。但上述两种成分极性不同,提供一种同时提取上述两种成分的方法对丹参加工生产具有重要的意义。本公开提供了一种丹参提取物的制备方法及丹参提取物,在兼顾丹参酮ⅱa和丹酚酸b提取的同时,可以获得一种具有强抗氧化性能的提取物。
为了使得本领域技术人员能够更加清楚地了解本公开的技术方案,以下将结合具体的实施例与对比例详细说明本公开的技术方案。
实施例1
1材料和仪器
1.1药材
丹参饮片购买自北京同仁堂(济南)药店有限公司。
1.2仪器
电子天平,高效液相色谱仪(型号agilent1260),hypersilods2色谱柱5μm(4.6mm×150mm),微孔滤膜0.22μm。
1.3试剂
乙腈(色谱纯),甲醇(色谱纯),购自默克股份两合公司,丹参酮ⅱa标准品(批号y20j8c40264hplc>98%),丹酚酸b标准品(批号p18j9f65817hplc>98%),水(哇哈哈纯净水),dpph(1,1-二苯基-2-三硝基苦肼)购于美国sigma公司,其余试剂均为分析纯。
2方法
2.1丹参样品溶液提取方法
将丹参饮片打粉后,用电子天平准确称取丹参粉末10.00g,置于100ml圆底烧瓶中,加入一定量的一定浓度的乙醇,然后冷凝回流一段时间,放冷后,先过滤再抽滤,得到滤液。再在滤渣中加入与第一次等量的同浓度乙醇,冷凝回流同样时间,冷却后同样先过滤再抽滤,得到第二次滤液。兼并两次滤液,用等浓度乙醇定容至200ml,然后用0.22μm滤膜滤过,得到样品溶液。
2.2丹参标准品溶液的配制
用电子天平准确称取丹参酮ⅱa标准品10.00mg,以甲醇溶解并定容至10ml,制成1000μg/ml的储备液,用0.22μm滤膜滤过后,得到丹参酮ⅱa标准品母液。重复以上步骤可得500μg/ml的丹酚酸b标准品母液。准确吸取丹参酮ⅱa的储备液1ml于10ml的容量瓶中,以甲醇稀释并定容至刻度,配成100μg/ml的使用液。
分别取100μg/ml丹参酮ⅱa标准使用溶液125μl、250μl、500μl、1000μl、2000μl,丹酚酸b160μl、320μl、640μl、1280μl、2560μl;以甲醇定容至5ml,得到丹参酮ⅱa和丹酚酸b混合标准系列溶液,则混合标准系列溶液中丹参酮ⅱa的浓度分别为2.5μg/ml、5μg/ml、10μg/ml、20μg/ml、40μg/ml,丹酚酸b的浓度分别为16μg/ml、32μg/ml、64μg/ml、128μg/ml、256μg/ml。
2.3高效液相色谱条件
色谱柱:hypersilods2(4.6mm×150mm);流动相:a:0.1%磷酸溶液,b:乙腈;流速:1.0ml/min:柱温30℃;进样量10μl;梯度洗脱方法:0~6min28%b;6~7min72→95%b;7~12min95%b;12~13min5→28%b;13~20min28%b。检测波长:286nm和270nm。
2.4单因素实验
分别以乙醇浓度、液料比、提取时间3个因素为自变量,以丹参酮ⅱa和丹酚酸b的峰面积为因变量,分别固定其中3个因素条件,变化某一因素条件,进行单因素试验,考察某一因素对丹参酮ⅱa和丹酚酸b提取的影响
2.5响应面法优化提取条件
综合各单因素试验结果,确定3个因素的3个水平,建立中心组合试验设计,对丹参酮ⅱa和丹酚酸b的集成提取条件进行优化,如下表1所示。
表1响应面实验因素与水平表
2.6体外抗氧化活性的研究
2.6.1dpph自由基清除能力测定
采用95%乙醇作为溶剂,配制成0.1mmol/l的dpph自由基溶剂,丹参提取物溶于75%的乙醇溶液稀释为不同浓度,以vc作为阳性对照。将不同浓度的丹参提取物100μl与dpph溶液100μl混合于96孔板,对照组以75%乙醇代替丹参提取物,避光反应30min,使用酶标仪于波长517nm处测定吸光度。按以下公式计算dpph自由基的清除率。重复实验三次,结果取平均值。
dpph自由基清除率(%)=(1-(as-ab)/ac)*100,式中:as为测定样品组的吸光度,ab为本底组的吸光度,ac为空白组的吸光度。
2.6.2abts+·自由基清除能力测定
用95%乙醇配制135μg/ml的abts工作液,将丹参提取物用乙醇稀释成一系列不同浓度的测试液,以vc作为阳性对照。将不同浓度的丹参提取物50μl与abts工作液100μl混合于96孔板,对照组用75%乙醇代替丹参提取物,避光反应6min,使用酶标仪于波长734nm处测定吸光度,计算公式与dpph相同。
3结果与分析
3.1标准品线性关系考察
按2.3部分的液相条件对标准溶液和样品进行分析,丹参酮ⅱa在270nm有最大吸收,丹酚酸b在286nm有最大吸收,所以选择检测波长为270nm和286nm。在该色谱条件下标准溶液和样品均能达到较好的分离(图1、图2)。
将“2.2”中配制的标准系列溶液在所建立的色谱条件下进行测定,并以浓度(x,mg/ml)对峰面积(y,mau*s)进行线性回归分析,得到丹参酮ⅱa回归方程:y=40.581x-35.788,r2=0.9995;丹酚酸b回归方程:y=5.7085x-168.17,r2=0.9992。说明丹参酮ⅱa在2.5-80μg/ml,丹酚酸b在16-512μg/ml的浓度范围内线性关系良好。
3.2单因素实验结果
3.2.1乙醇浓度的考察
乙醇浓度对丹参酮ⅱa和丹酚酸b的提取都有很大影响,但是,之前的研究乙醇浓度的跨度都很大,特别是在60%-90%之间变化趋势不是很确定,因此,本实施例首先选取了乙醇浓度为60%、65%、70%、75%、80%、85%、90%等7种不同浓度,参照2.2的方法进行提取,料液比均为1:8,两次提取时间均为60min,得到溶液后,进行液相分析得到峰面积。
表2乙醇浓度及其峰面积表
表2显示,85%乙醇提取时丹参酮ⅱa的峰面积最大,但是丹酚酸b的峰面积最大时用65%乙醇提取,两者不能同时兼顾,故本实施例选取65%、75%、85%的乙醇作为乙醇用量的三个因素。
3.2.2提取时间的考察
在提取时间上,本实施例选择了30min、45min、60min这三个量,同样参照2.2的方法,用70%的乙醇,料液比均为1:8,提取两次,得到样品溶液后进行液相分析。
表3提取时间及其峰面积表
从表中看,丹参酮ⅱa和丹酚酸b的最大峰面积都出现在45min,所以在这个影响因素上选择30min、45min、60min这三个因素进行响应面考察。
3.2.3料液比因素的确定
料液比的选择上,本实施例选择了1:8、1:10、1:12、1:15这四个量,用70%的乙醇参照2.2的方法进行两次提取,每次提取60min,得到溶液后同样进行液相分析。
表4料液比及其峰面积表
根据表三,料液比为1:12时,丹参酮ⅱa和丹酚酸b的峰面积都是最大的;同时还发现,料液比为1:15时,两者的峰面积都是最小的,舍弃1:15这个选择,所以在料液比这个因素上,本实施例选取前三个因素8倍、10倍、12倍进行响应面考察。
3.3响应面法优化丹参有效成分的集成提取工艺
3.3.1响应面分析实验结果
结合单因素试验结果,根据box-behnken试验原理,以丹参酮ⅱa和丹酚酸b的峰面积为响应值,对集成提取的工艺参数(提取时间、乙醇浓度、料液比)进行优化,响应面实验条件及结果如下表5所示。
表5响应面试验条件及结果
应用design-expert7.0软件对得到的数据进行回归分析,由此得到丹参酮ⅱa色谱峰与三因素乙醇浓度a、提取时间b、料液比c的二次多项回归方程为:y=-4255.49047+95.70373a+7.42811b+246.44112c+0.041427ab-3.36460ac-0.52294bc-0.43887a2-0.048724b2+1.88331c2;丹酚酸b色谱峰与三因素乙醇浓度a、提取时间b、料液比c的二次多项回归方程为:y=-11061.13828+293.95809a-16.92395b+540.49669c+0.24770ab-4.76770ac+1.41964bc-1.80206a2-0.14880b2-10.22999c2。
3.3.2回归方程方差分析
对回归方程式进行方差分析,丹参酮ⅱa和丹酚酸b的方差分析表分别见表6和表7。
由表6可以看出,对于丹参酮ⅱa,该模型的p值小于0.05,有显著性差异,失拟差p=0.6799>0.55,表明不显著,说明方程模型与实验实际拟合良好,实验误差较小,能较好地反映丹参酮ⅱa的提取。3个要素与响应值不是简略的线性关系,由3个要素方差分析的f值可以得到结论:本实施例所选的3个因素对丹参酮ⅱa的提取影响大小的排序为a(乙醇浓度)>c(料液比)>b(提取时间)。
表6丹参酮ⅱa的方差分析表
由表7可以看出,对于丹参酸b,该模型的p值小于0.05,有显著性差异,失拟差p=0.6590>0.55,表明不显著,说明方程模型与实验实际拟合良好,实验误差较小,能较好地反映丹参酸b的提取。3个要素与响应值不是简略的线性关系,由3个要素方差分析的f值可以得到结论:本实施例所选的3个因素对丹参酮酸b的提取影响大小的排序为a(乙醇浓度)>c(料液比)>b(提取时间)。
表7丹酚酸b的方差分析表
3.3.3响应图及等高线分析
根据拟合模型绘制不同因素对丹参酮ⅱa和丹酚酸b的响应面的三维图,可更直观地反应响应面的最高点及因素间的相互作用对响应值的影响。分别见图3和图4。
经分析得回归模型的最大值点,即乙醇浓度为67%,液料比为1:12,提取时间为48min。丹参酮ⅱa和丹酚酸b峰面积的理论值分别为785.05和2187.57mau*s。
3.3.4最佳提取工艺的验证
取丹参药材100g,以响应面法得到的最佳工艺为条件进行了三次平行实验,以验证其重复性和试验的准确性。三次实验的峰面积平均值为丹参酮ⅱa785.033mau*s,丹酚酸b2187.62mau*s,与预测值非常吻合,说明此条件实际应用价值较高,可用于丹参集成提取工艺。
3.4丹参提取物抗氧化活性分析
3.4.1丹参提取物对dpph自由基清除能力的测定
采用最佳提取工艺制得的丹参集成提取物进行dpph清除活性测试。结果表明,丹参提取物对dpph自由基有较强的清除效果,随着溶液浓度的增加,清除率不断增加,表现出明显的浓度依赖性,而且其清除效果优于阳性药vc。大多数文献报道的醇提都采用85%的乙醇,所以本实施例也对这两种工艺得到的提取物抗氧化活性进行了比较。从图中亦可以看出,采用此工艺得到的提取物与85%醇提相比,相同浓度下,其对dpph自由基的清除能力更高。
3.4.2丹参提取物对abts自由基清除能力的测定
采用最佳提取工艺制得的丹参集成提取物进行abts自由基清除能力测试。结果表明,丹参提取物对abts自由基有较强的清除效果,随着溶液浓度的增加,清除率不断增加,表现出明显的浓度依赖性,而且其清除效果优于阳性药vc。此外,与85%醇提相比,同样浓度下,其清除率更高。
以上两个自由基清除实验结果表明,此工艺得到的丹参提取物有强烈的抗氧化活性,值得进一步研究和利用。
以上所述仅为本公开的优选实施例而已,并不用于限制本公开,对于本领域的技术人员来说,本公开可以有各种更改和变化。凡在本公开的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本公开的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!