小檗碱联合芒柄花黄素在制备抗肿瘤药物中的应用的制作方法
本发明属于医药领域,具体涉及小檗碱和芒柄花黄素作为治疗肿瘤的药物及其应用,更具体涉及鼻咽癌的治疗药物。
背景技术:
鼻咽癌(nasopharyngealcarcinoma,npc)是一种上皮源性恶性肿瘤,约80%的鼻咽癌发生在我国,占我国头颈部肿瘤的首位。其发病机理尚未完全明了,目前认为其发生与遗传因素、微生物感染(eb病毒等)、环境、饮食及社会因素密切相关。鼻咽癌诊断主要依靠常规的影像学检查与病理检查,缺乏可靠的早期诊断指标和手段。因此,患者前来就医时,已有70%-80%的病人存在颈淋巴结转移,75%的病人在确诊时已属ⅲ期或ⅳ期肿瘤。
由于鼻咽腔位置深且狭小,其邻近部位有许多重要血管、神经、淋巴组织等要害结构,手术治疗非常困难,故现今鼻咽癌的治疗方式仍以放疗为主,但放疗仅针对局部病变,不能防止远处转移,且95%以上的的鼻咽癌为低分化或未分化癌,恶性程度高,生长快,易出现局部区域复发,淋巴道或血行转移,这也是放疗失败的主要原因,使放疗后5年生存率仅40%-60%。其中,远处转移是导致病情进一步恶化的突出因素。据统计,鼻咽癌患者5年累积复发率为19.8%-36.0%,远处转移率为21.2%-41.8%。寻找治疗鼻咽癌的有效药仍是鼻咽癌治疗领域亟待解决的问题。
目前常见治疗鼻咽癌的化学药物有顺铂、5-氟尿嘧啶、奈达铂等,这些药物都具有一定的细胞毒性,单用容易产生耐药性,而这种放疗联合化疗的毒副作用比较大,副作用使患者的生存质量显著下降。鼻咽癌根据不同的分期需要诱导化疗,同步放化疗,辅助化疗等,一般情况下应用紫杉类加铂类药物化疗,部分患者选择口服替吉奥,卡培他滨等药物治疗。放疗出现的副作用表现为全身反应和局部反应。全身反应表现为一系列的功能紊乱与失调,如精神不振,食欲下降,身体衰弱,疲乏,恶心呕吐,食后胀满等。局部反应,干性皮肤表现为皮肤瘙痒,色素沉着及脱皮,能产生永久性浅褐色斑;湿性皮肤表现为照射部位湿疹、水泡,严重时可造成糜烂、破溃。还有口腔黏膜反应,口腔及咽部的粘膜如果位于放疗区内,多数会出现急性的口腔及咽喉粘膜反应,通常表现为口腔粘膜的红肿、溃疡、味觉改变、疼痛、咽下困难等病症。放疗的副作用,对于身体较差的患者,多半不能承受。化疗的副作用表现为贫血,白细胞减少,血小板减少,抵抗力减弱;神经毒性反应如手脚麻木等;胃肠道反应,多数患者恶心呕吐,食欲减退;患者容易口腔溃疡;可能出现脱发;可能引起化疗药物过敏等。
中医药治疗具有多环节、多靶点、多途径等特点,其临床应用可以有效控制肿瘤,不但对于放化疗起到减毒增效的作用,而且在肿瘤的康复治疗中发挥重要作用。鉴于中医药的治疗特点,从中医药中寻找治疗鼻咽癌的有效中药或部位群或单体,对提高鼻咽癌疗效及改善预后有重要作用。因此寻找低毒、高效、天然的新型抗癌药物,开发联合用药方案是当前鼻咽癌研究的热点。
小檗碱是中药黄连的主要成分,可抑制卵巢癌、宫颈癌、乳腺癌、肺癌、肝癌、结直肠癌、胃癌、肾癌、膀胱癌、前列腺癌等多种肿瘤细胞的生长,芒柄花黄素是中药黄芪的主要有效成分之一,可抑制乳腺癌、宫颈癌、子宫内膜癌、卵巢癌、前列腺癌、膀胱癌、结直肠癌、肝癌、胃癌、肺癌、骨肉瘤和黑色素瘤细胞的生长,它们的作用主要与抑制细胞增殖、干扰细胞周期、诱导细胞凋亡、增加化疗药物敏感性等有关。针对鼻咽癌,小檗碱能提高放疗敏感性,抑制鼻咽癌细胞增殖、成瘤能力和细胞迁移能力;芒柄花黄素能抑制鼻咽癌细胞增殖和诱导凋亡,也有报道芒柄花黄素促进鼻咽癌细胞增殖,到底是抗鼻咽癌还是促鼻咽癌,存在一定分歧。尚无小檗碱联合芒柄花黄素具有抗肿瘤协同效应的报道。
技术实现要素:
本发明的目的是针对现有肿瘤治疗技术中的不足,提供一种小檗碱联合芒柄花黄素在制备抗肿瘤药物中的应用。
为实现上述目的,本发明提供一种抗肿瘤药物组合物,其特征在于,其有效成分是小檗碱和芒柄花黄素。
所述抗肿瘤是抑制肿瘤细胞增殖、诱导肿瘤细胞凋亡、抑制肿瘤细胞迁移。
所述药物还包括药学上可接受的一种或多种辅料。
所述抗肿瘤药物剂型为胶囊剂、片剂、口服制剂、微囊制剂、注射剂。所述的抗肿瘤药物给药方式为注射、口服、胃肠外、吸入式喷雾或透皮给药。
本发明针对的所述的肿瘤为实体肿瘤,更优选为原发性或继发性实体肿瘤,更具体为鼻咽癌。
在一个实施方式中,按下述剂量制备成相应的药物,小檗碱剂量为5mg/kg-20mg/kg,芒柄花黄素剂量为5mg/kg-30mg/kg,且两者用量满足1:0.5至1:2的比例。
另一方面,一种治疗鼻咽癌的药盒,其特征在于,其包括独立包装的小檗碱和芒柄花黄素制剂。优选地,药盒中小檗碱和芒柄花黄素两者的药物有效量满足1:0.5至1:2的比例。
再一方面,本发明还提供小檗碱和芒柄花黄素作为有效成分在制备治疗鼻咽癌的药物中应用。
本发明采取的技术方案是:小檗碱联合芒柄花黄素在制备抗肿瘤药物中的应用。两者联合的最佳配伍:小檗碱剂量为5mg/kg-20mg/kg,芒柄花黄素剂量为5mg/kg-30mg/kg按照1:1、1:2、2:1配比使用。优选地,所述小檗碱和芒柄花黄素的有效治疗量为10mg/kg,可以按照1:1、1:2、2:1配比,适当提高2-3倍的使用剂量,临床应用中,可以按照动物与人剂量换算公式进行计算。
本发明基于研究发现小檗碱和芒柄花黄素两者的协同作用突出而完成。两者的协同作用在最佳配比下可达到,ci值可低至0.0022,很是超出预料的范围。因而在相同的剂量下,两者联合使用治疗效应显著好于单独使用的小檗碱或芒柄花黄素。并且实验中观察了各药物的副作用,发现两药联合使用,基本无副反应。本发明人通过实验进一步证明小檗碱和芒柄花黄素单用均可通过线粒体-细胞色素c途径和内质网途径诱导鼻咽癌cne2细胞凋亡,两药配伍通过线粒体-细胞色素c途径和内质网途径诱导鼻咽癌cne2细胞凋亡,同时使用,引起的凋亡效应更强,如果只需得到单用药物的相同效应,可以降低两药浓度。加之两药物有不同作用机制,比如芒柄花黄素除了直接的抗肿瘤效应,还可以提高机体的固有免疫功能,抑制脾细胞凋亡并提高其转化率,从而发挥间接的抗肿瘤效应;另外芒柄花黄素可以通过减少自由基生成,增强抗氧化酶活性、调节能量代谢发挥抗疲劳作用。小檗碱除了直接抗肿瘤的作用,也可通过抑制th1、th17细胞分化,调节th1/th2平衡,抑制t细胞增殖,诱导树突状细胞、巨噬细胞凋亡,抑制促炎性因子和抗体生成,保护上皮屏障功能等机制发挥免疫调节作用,从而产生间接抗肿瘤效应。两药通过不同分子机制从不同方面发挥作用,最终协同发挥出很强的抗肿瘤效应,协同效应比预期的更强。
附图说明
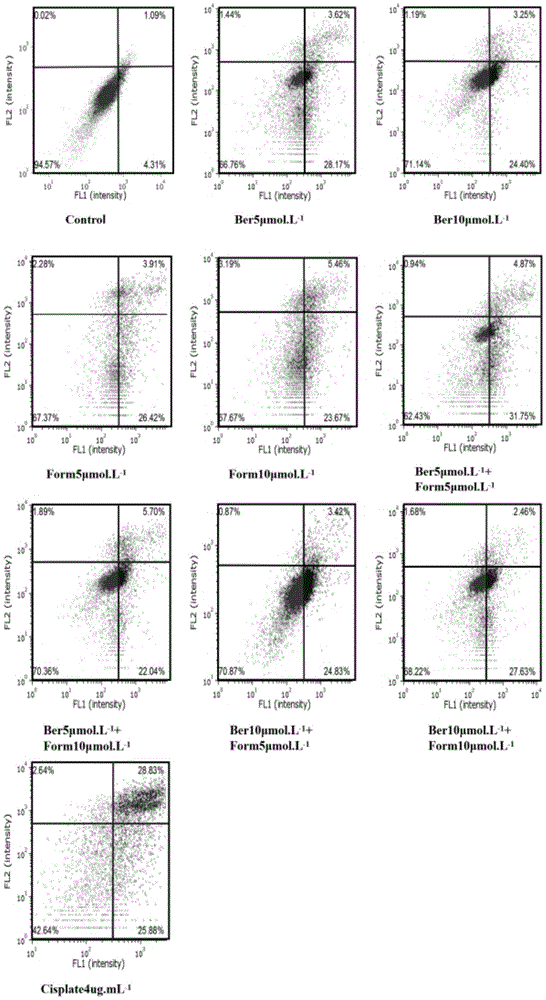
图1小檗碱联合芒柄花黄素对鼻咽癌细胞凋亡的诱导效应及联合指数;
图2小檗碱联合芒柄花黄素对鼻咽癌细胞核的影响;
其中,a.control;b.ber5μm;c.ber10μm;d.form5μm;e.form10μm;f.ber10μm+form10μm;g.ber10μm+form5μm;h.ber5μm+form10μm;i.ber5μm+form5μm;j.顺铂4.0μg.ml-1;
图3小檗碱联合芒柄花黄素对鼻咽癌细胞线粒体膜电位的影响;
其中,与control组比较,**p<0.01;
图4小檗碱联合芒柄花黄素对鼻咽癌细胞迁移的抑制作用(划痕法);
图5小檗碱联合芒柄花黄素对鼻咽癌细胞迁移的抑制作用(transwell小室法);
其中,a:control;b:ber5μm;c:ber10μm;d:form5μm;e:form10μm;f:ber5μm+form5μm;g:ber5μm+form10μm;h:ber10μm+form5μm;i:ber10μm+form10μm;j:5-fu2μg·ml-1;
图6小檗碱联合人芒柄花黄素抑制鼻咽癌裸鼠移植瘤生长(n=5);
其中,con:与实验组等体积的生理盐水;ber:10mg/kg小檗碱;form:10mg/kg芒柄花黄素;ber+form:10mg/kg小檗碱+10mg/kg芒柄花黄素;cis:3mg/kg顺铂;
与control组比较,*p<0.05与ber+form组比较,#p<0.05;
图7tunel法检测移植瘤组织细胞凋亡情况(n=5);
其中,con:与实验组等体积的生理盐水;ber:10mg/kg小檗碱;form:10mg/kg芒柄花黄素;ber+form:10mg/kg小檗碱+10mg/kg芒柄花黄素;cis:3mg/kg顺铂;与control组比较,*p<0.05;,与ber+form组比较,#p<0.05;
图8小檗碱联合芒柄花黄素对裸鼠体重的影响;
其中,con:与实验组等体积的生理盐水;ber:10mg/kg小檗碱;form:10mg/kg芒柄花黄素;ber+form:10mg/kg小檗碱+10mg/kg芒柄花黄素;cis:3mg/kg顺铂。图9小檗碱联合人参皂苷rg3对裸鼠肝、肾系数的影响;
图9小檗碱联合芒柄花黄素对裸鼠肝系数和肾系数的影响;
其中,(a)肝系数,与control组比较,*p<0.05;与cis组比较,#p<0.05,n=5.(b)肾系数,与control组比较,*p<0.05;与cis组比较,#p<0.05,n=5;
con:与实验组等体积的生理盐水;ber:10mg/kg小檗碱;form:10mg/kg芒柄花黄素;ber+form:10mg/kg小檗碱+10mg/kg芒柄花黄素;cis:3mg/kg顺铂;
图10小檗碱联合芒柄花黄素协同对鼻咽癌cne2细胞生存、凋亡及凋亡途径相关蛋白表达的影响;
与溶剂对照组比较,**p<0.01;联用组与单用组比较,#p<0.05,##p<0.01;
图11加入抑制剂后对鼻咽癌cne2细胞线粒体途径及内质网途径相关蛋白表达的影响与溶剂对照组比较,**p<0.01;药物加抑制剂组与联用组比较,#p<0.05,##p<0.01;
图12加入抑制剂后对鼻咽癌cne2细胞凋亡率的影响;
其中,与溶剂对照组比较,**p<0.01;药物加抑制剂组与联用组比较,##p<0.01。
具体实施方式
下面通过具体实施方式的详细描述,以更清楚的理解本发明,但不构成对本发明的限制。
实施例1:小檗碱联合芒柄花黄素抑制鼻咽癌细胞增殖的协同效应实验
1、单用小檗碱对鼻咽癌细胞的抑制效应
单用小檗碱(ber)处理cne2鼻咽癌细胞,在24小时、36小时、48小时、72小时均能显著抑制鼻咽癌细胞增殖,抑制率见表1。
表1小檗碱对鼻咽癌细胞增殖的抑制效应(
2、单用芒柄花黄素对鼻咽癌细胞的抑制效应
单用芒柄花黄素(form)处理cne2鼻咽癌细胞,在24小时、36小时、48小时、72小时均能显著抑制鼻咽癌细胞增殖,抑制率见表2。
表2芒柄花黄素对鼻咽癌细胞增殖的抑制效应(
3、小檗碱联合芒柄花黄素抑制鼻咽癌细胞增殖的效应
分别用不同浓度小檗碱与不同浓度芒柄花黄素配伍,观察对鼻咽癌细胞增殖的影响。
小檗碱(ber)与芒柄花黄素(form)不同剂量配伍使用,根据计算出联合指数(combinationindex,ci)来反应两药配伍的效应,ci>1为拮抗效应、ci=1为叠加效应,ci<1为协同效应。ci小于1后,ci值越小表明协同效应越强,即两药联合应用的协同效应越好。结果见表3。
药物作用24小时,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)、(ber10+form20)、(ber20+form20)组ci值分别为0.18、0.02、0.0022、0.067、0.011、0.0088;药物作用36小时,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)、(ber10+form20)、(ber20+form20)组ci值分别为0.26、0.26、0.0598、0.41、0.21、0.20;药物作用48小时,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)、(ber10+form20)、(ber20+form20)组ci值分别为0.32、0.16、0.0196、0.29、0.12、0.09,药物作用72小时,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)、(ber10+form20)、(ber20+form20)组ci值分别为0.759、0.469、0.07577、0.53308、0.47703、0.179,这些组别ci值均小于1,表现为协同效应,且协同效应很强,特别是药物联合作用24小时,ci值均远小于1,表现为非常强的协同效应,而(ber10+form5)组在各时间点均表现出非常强的协同效应。
表3小檗碱联合芒柄花黄素对鼻咽癌细胞增殖的抑制效应及联合指数(
实施例2:小檗碱联合芒柄花黄素诱导鼻咽癌细胞凋亡具有协同效应
根据实施例1的结果,采用析因设计,选择0、5μm、10μm不同浓度小檗碱(ber)联合0、5μm、10μm不同浓度芒柄花黄素(form)分为9个组:0(control,溶剂对照组)、ber5、ber10、form5、form10、(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10),另设置阳性对照顺铂组(浓度为4.0μg.ml-1)。观察两药联用对鼻咽癌细胞凋亡的影响。
1、流式细胞术检测小檗碱联合芒柄花黄素诱导鼻咽癌细胞凋亡的效应
采用流式细胞术进一步检测药物对鼻咽癌细胞凋亡的影响。分别用0、5μm、10μm小檗碱与0、5μm、10μm芒柄花黄素配伍,观察其对鼻咽癌细胞凋亡的影响,并计算联合用药指数。根据药物配伍使用效应的分析方法,联合指数ci>1为拮抗效应、ci=1为叠加效应,ci<1为协同效应。ci值小于1后,ci值越小表明协同效应越强,即两药联合应用的效应越好。药物处理36小时后,结果见图1,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)组ci值分别为0.06087、0.03191、0.12777、0.05164,ci远小于1,两药联合应用协同效应非常强。
2、hoechst33342染色观察小檗碱联合芒柄花黄素对鼻咽癌细胞形态的影响
采用hoechst33342染色观察药物配伍处理36小时后对cne2鼻咽癌细胞形态的影响。药物处理36小时后,hoechst33342染色(图2)显示,未加药组细胞的细胞核呈均匀一致的淡蓝色(a),药物处理组细胞明显出现凋亡特征,即部分细胞核呈颗粒状亮蓝色,同时伴有细胞核的边集、碎裂、皱缩等,且(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)联合组荧光强度较单用组强(b-h)。提示药物联用诱导凋亡效应强。
3、小檗碱联合芒柄花黄素对鼻咽癌细胞线粒体膜电位的影响
通过线粒体膜电位检测试剂盒(jc-10)检测药物处理后的鼻咽癌细胞,数据和荧光图像表明小檗碱、芒柄花黄素单用和联合应用都可以显著影响鼻咽癌细胞线粒体膜电位,破坏线粒体膜完整性,间接反映药物引起线粒体凋亡,见图3。红色为正常细胞,绿色为凋亡细胞。
实施例3:小檗碱联合芒柄花黄素抑制鼻咽癌细胞迁移具有协同效应
1、划痕实验观察小檗碱联合芒柄花黄素抑制鼻咽癌细胞迁移的效应
分别用0、5μm、10μm小檗碱与0、5μm、10μm芒柄花黄素配伍,采用划痕实验观察其对鼻咽癌细胞迁移的影响,并计算联合用药指数。根据药物配伍使用效应的分析方法,联合指数ci>1为拮抗效应、ci=1为叠加效应,ci<1为协同效应。ci值小于1后,ci值越小表明协同效应越强,即两药联合应用的效应越好。结果见图4和表4。根据迁移抑制率,各用药组都能显著抑制鼻咽癌细胞迁移,且(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)组迁移抑制率显著高于单用药物组,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)组联合指数分别为0.44、0.02、0.72、0.40,均远小于1,两药联合具有强的协同抑制效应。
表4小檗碱联合芒柄花黄素对鼻咽癌细胞迁移的抑制作用及联合指数(划痕法)
2、transwell实验观察小檗碱联合芒柄花黄素抑制鼻咽癌细胞迁移的效应
分别用0、5μm、10μm小檗碱与0、5μm、10μm芒柄花黄素配伍,采用transwell实验观察其对鼻咽癌细胞迁移的影响,并计算联合用药指数。根据药物配伍使用效应的分析方法,联合指数ci>1为拮抗效应、ci=1为叠加效应,ci<1为协同效应。ci值小于1后,ci值越小表明协同效应越强,即两药联合应用的效应越好。结果见图5和表5,根据迁移抑制率,各用药组都能显著抑制鼻咽癌细胞迁移,且(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)组迁移抑制率显著高于单用药物组,(ber5+form5)、(ber5+form10)、(ber10+form5)、(ber10+form10)组联合指数分别为0.71、0.71、0.98、0.87,均小于1,两药联合具有协同抑制效应。
表5小檗碱联合芒柄花黄素对鼻咽癌细胞迁移的抑制作用及联合指数(transwell法)
实施例4:小檗碱联合芒柄花黄素协同抑制鼻咽癌移植瘤生长
构建鼻咽癌裸鼠移植瘤模型,10mg/kg小檗碱联合10mg/kg芒柄花黄素经腹腔给药作用于移植瘤裸鼠,治疗18天后,称量移植瘤的重量,计算各用药组肿瘤重量与溶剂对照组(即未用药物组)的比值,得出相对重量,小檗碱单用组、芒柄花黄素单用组、小檗碱联合芒柄花黄素组移植瘤平均重量分别是溶剂对照组的63.8%、75.2%、29.4%,小檗碱单用组、芒柄花黄素组平均瘤重分别是联合用药组平均瘤重的2.17倍、2.56倍,见图6,联合用药组平均瘤重显著低于单药组(p<0.05),且经统计分析,药物间有交互作用(p<0.05),说明有协同抑制鼻咽癌移植瘤生长的效应。
实施例5:小檗碱联合芒柄花黄素诱导鼻咽癌移植瘤瘤细胞凋亡
构建鼻咽癌裸鼠移植瘤模型,以3mg/kg顺铂为阳性对照药,10mg/kg小檗碱联合10mg/kg芒柄花黄素经腹腔给药作用于移植瘤裸鼠,药物处理18天后,tunel法检测移植瘤瘤细胞凋亡情况。结果见图7,溶剂对照组、小檗碱单用组、芒柄花黄素单用组、小檗碱联合芒柄花黄素组移植瘤平均凋亡率分别是13.2%、38.5%、29.1%、79.5%,小檗碱单用组、芒柄花黄素组平均凋亡率分别是联合用药组的48.4%、36.6%,联合用药组平均凋亡率显著高于单药组(p<0.05),且经统计分析,药物间有交互作用(p<0.05),说明小檗碱联合芒柄花黄素有协同诱导鼻咽癌移植瘤细胞凋亡的效应。
实施例6:小檗碱联合芒柄花黄素对裸鼠毒副作用研究
构建鼻咽癌裸鼠移植瘤模型,10mg/kg小檗碱联合10mg/kg芒柄花黄素经腹腔给药作用于移植瘤裸鼠,药物处理18天后,观察裸鼠的状态、体重,he染色检测药物作用后肿瘤组织、肝及肾的病理变化,分析小檗碱联合芒柄花黄素对裸鼠肝、肾的影响。
实验期间,顺铂组裸鼠给药后期体重下降,而溶剂对照组及其它给药组裸鼠体重、进食、排便、活动以及精神状态无明显变化(图8)。给药结束后摘取裸鼠肝脏和肾脏组织,称取重量,计算各组肝/肾系数,结果显示顺铂组肝系数增加,肾系数降低,其他各组肝肾系数均无显著性差异(图9)。he染色发现顺铂组肝索细胞排列不是很整齐,其他各组肝小叶结构均存在,肝细胞无明显肿胀、坏死,汇管区无纤维组织增生。各组肾皮髓质结构清楚,肾小球细胞及肾小管上皮细胞无明显肿胀或变性坏死。以上结果表明小檗碱和芒柄花黄素对裸鼠没有明显的毒性。说明多用一种药物,并没有增加毒性。并且,与阳性对照组顺铂比较,毒性低。
实施例7:小檗碱联合芒柄花黄素抗肿瘤分子机制研究
实施例2和实施5只是用来说明药物的部分作用机制,即药物通过协同诱导细胞凋亡来发挥抗鼻咽癌的作用。这部分是进一步说明药物作用的分子机制,即小檗碱联合芒柄花黄素协同诱导鼻咽癌细胞凋亡的机制。
1、小檗碱联合芒柄花黄素协同对鼻咽癌cne2细胞生存、凋亡及凋亡途径相关蛋白表达的影响
westornblot结果显示,药物处理36h后,与control组相比,相关蛋白的表达量均有变化,具体表现为细胞生存蛋白survivin、抗凋亡蛋白bcl-2表达有下降趋势,促凋亡蛋白bax表达上升;且联合组较单用组趋势更明显;各凋亡途径相关蛋白的表达量与control组相比也有相应的变化,具体为cleavedcaspase-3、cleavedcaspase-7表达量上升,线粒体-细胞色素c途径的相关蛋白cleavedcaspase-9、内质网途径的相关蛋白cleavedcaspase-12表达上升,死亡受体途径的相关蛋白cleavedcaspase-8各组之间表达量无明显差异(p>0.05)。见图10。故初步判断小檗碱联合芒柄花黄素是通过线粒体-细胞色素c途径和内质网途径诱导鼻咽癌cne2细胞凋亡的。
2、线粒体凋亡途径及内质网凋亡途径在小檗碱联合芒柄花黄素协同促进鼻咽癌cne2细胞凋亡中的作用
为进一步验证线粒体凋亡途径及内质网凋亡途径在促进cne2细胞凋亡中的作用,单独或联合加入caspase-9抑制剂(z-lehd-fmk)和caspase-12抑制剂(z-atad-fmk),分别检测细胞中相关凋亡蛋白的表达水平和细胞凋亡率,见图11和图12。westernblot结果(图11)显示,与联合用药组比较,单用或联合用caspase-9抑制剂(z-lehd-fmk)或caspase-12抑制剂(z-atad-fmk)再用药物处理的三个组cleavedcaspase-3、cleavedcaspase-7表达量显著降低(均p值<0.01),同时加两种抑制剂组的cleavedcaspase-3、cleavedcaspase-7表达量降低更显著,与只加一种抑制剂组之间有统计学差异(均p值<0.01),且同时加入两种抑制剂组表达量与control组无明显差异(p>0.05),cleavedcaspase-9和cleavedcaspase-12在相对应的抑制剂组别中表达量明显降低,与control组相比,差异无统计学意义(p>0.05),即抑制cleavedcaspase-9和cleavedcaspase-12的活性后,蛋白表达量降低,说明抑制剂发挥了相应的作用。荧光双染流式细胞术结果显示:control组的细胞凋亡率为1.805±0.064%,ber5μmol·l-1组凋亡率为24.5±1.813%,form5μmol·l-1组凋亡率为21.797±1.951%,ber5μmol·l-1+form5μmol·l-1组凋亡率为28.437±1.274%,ber5μmol·l-1+form5μmol·l-1+z-lehd-fmk组凋亡率为12.447±0.451%,ber5μmol·l-1+form5μmol·l-1+z-atad-fmk组凋亡率为11.387±0.473%,ber5μmol·l-1+form5μmol·l-1+z-lehd-fmk+z-atad-fmk组凋亡率为2.983±0.075%。由数据可知,在分别加入z-lehd-fmk或z-atad-fmk后,药物诱导细胞的凋亡率相对降低(均p<0.01),但仍有诱导凋亡的效应,与control组相比,差异仍具有统计学意义(p<0.01);同时加入两种抑制剂处理后,药物诱导细胞的凋亡率显著降低(均p<0.01),且与control组之间无明显差异(p>0.05),见图12。凋亡率的变化与蛋白变化一致,即caspase-9抑制剂(z-lehd-fmk)和caspase-12抑制剂(z-atad-fmk)均削弱了小檗碱联和芒柄花黄素诱导凋亡的效应,抑制剂联合应用的效应更强,由此进一步证明,小檗碱联合芒柄花黄素通过线粒体-细胞色素c途径和内质网途径诱导鼻咽癌cne2细胞凋亡。
- 还没有人留言评论。精彩留言会获得点赞!