具有稳定的Fc受体表达的IL-2依赖性NK-92细胞的制作方法
相关申请本申请要求2018年11月26日提交的美国临时申请第62/771,479号的权益。出于所有目的,所述临时申请的内容通过引用整体并入本文。
背景技术:
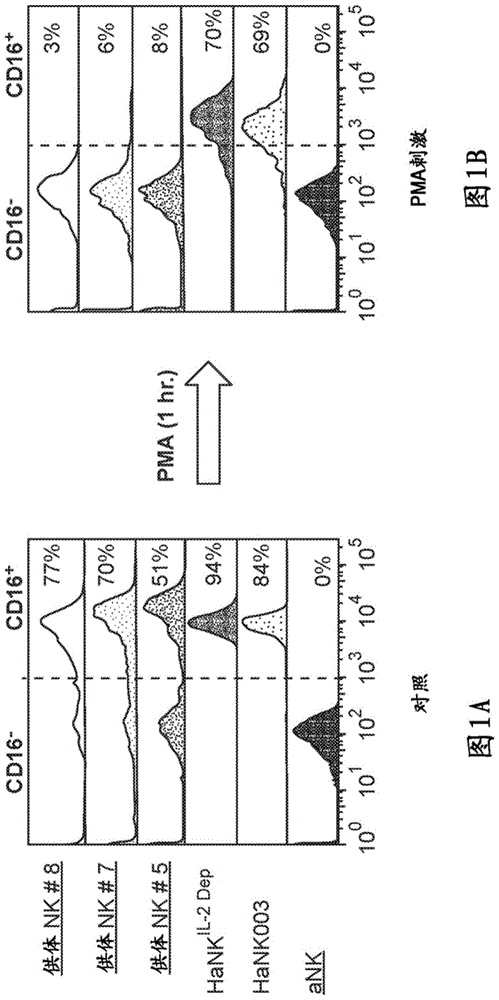
:用单克隆抗体进行的抗癌治疗显著改善了癌症患者的临床结果。治疗性抗体的主要作用机制之一是通过抗体依赖性细胞介导的细胞毒性(adcc)。自然杀伤细胞可用作用于基于细胞的免疫疗法的细胞毒性效应细胞,因为它们是adcc的主要效应细胞。本文中称为的是在患有非霍奇金淋巴瘤的受试者的血液中发现的,且然后离体永生化的细胞溶解性癌细胞系。细胞来源于nk细胞,但缺乏正常nk细胞呈现的主要抑制性受体,而同时保留了大多数激活性受体。然而,细胞不攻击正常细胞,也不在人体内引发不可接受的免疫排斥反应。细胞系的表征在wo1998/49268和美国专利申请公开号2002-0068044中公开。细胞也被评估为治疗某些癌症的潜在治疗剂。尽管细胞保留了与nk细胞相关的几乎所有激活性受体和细胞溶解途径,但其在细胞表面上不表达cd16。cd16是识别并结合抗体的fc部分以激活nk细胞用于adcc效应机制的fc受体。由于其缺乏cd16受体,未修饰的细胞不能通过adcc机制来裂解靶细胞。天然的nk细胞表达cd16,但是当nk细胞被各种刺激激活时,cd16易于受到adam17介导的蛋白水解切割。例如,已知nk细胞与k562肿瘤细胞共培养刺激cd16切割蛋白酶,其导致nk细胞中cd16表面表达的脱落。激活后,nk细胞中cd16的这种快速下调严重损害了nk细胞的adcc活性。技术实现要素:本文提供了修饰的细胞群体、包含该细胞的组合物和试剂盒以及制备和使用该细胞群体的方法。修饰的细胞表达cd16(例如,fc受体cd16的高亲和力变体),而不表达il-2。这些修饰的细胞表现出高水平的cd16表达,并且在通过刺激剂、靶细胞结合或adcc激活期间和/或之后保持该表达水平。cd16的这种稳定表达使得修饰的细胞能够在和/或adcc期间实现靶细胞的连续杀伤。从修饰的细胞排除il-2转基因使il-2转基因的负面影响最小化,并允许灵活引入可赋予修饰的所需性质的另外的转基因。例如,il-2可能因细胞泄漏或细胞死亡而在体内释放。il-2可促进treg的募集和扩增,从而导致免疫抑制。高剂量的il-2已被证明在患者中诱导强烈的副作用,例如增加的感染、瘀斑和出血、疲劳等的风险。参见https://www.cancerresearchuk.org/about-cancer/cancer-in-general/treatment/cancer-drugs/drugs/aldesleukin/side-effects。从细胞省略il-2将避免这些不良作用。上述修饰的细胞在本文中被称为“il2依赖性cd16阳性细胞”或“il2依赖性细胞”。在一些实施方案中,本公开提供了表达cd16(seqidno:1)的修饰的细胞群体,其中修饰的细胞不表达il-2,并且其中该群体包含一个或多个修饰的细胞。修饰的细胞可包含cd16的核酸(seqidno:2)。在一些实施方案中,修饰的细胞具有adcc。在一些实施方案中,与激活前细胞上的cd16表达水平相比,当细胞被激活时修饰的细胞的cd16表达水平降低不超过20%。在一些实施方案中,与接触前的细胞相比,在细胞与靶细胞接触后对cd16阳性的细胞的百分比降低不超过10%。在一些实施方案中,修饰的细胞在激活后未表现出cd16表达减少或cd16表达减少不超过20%,并且其中修饰的细胞在激活开始后保持细胞毒性稳态至少5小时。在一些实施方案中,该细胞表达的cd16水平高于来自供体的nk细胞。在一些实施方案中,通过流式细胞术测量cd16的表达。在一些实施方案中,与激活前的细胞相比,细胞激活后对cd16阳性的细胞的百分比降低不超过20%。在一些实施方案中,细胞通过一种或多种选自pma、离子霉素和lps的化合物激活。在一些实施方案中,修饰的细胞通过植物血凝素(pha)、通过与k562细胞共孵育的先天途径或者通过与利妥昔单抗和dohh共孵育的adcc激活。在一些实施方案中,修饰的细胞群体通过接触靶肿瘤细胞而被激活。靶肿瘤细胞可以是选自k562细胞和skbr-3细胞的细胞。在一些实施方案中,与激活前的修饰细胞相比,已激活的修饰细胞群体的cd16表达降低不超过10%。在一些实施方案中,与激活前的修饰细胞上的cd16表达水平相比,已激活的细胞上的cd16表达水平降低不超过5%。在一些实施方案中,修饰的细胞群体通过接触抗体和靶细胞而被激活,其中孵育导致adcc。在一些实施方案中,抗体是抗cd20抗体,且靶细胞是dohh-2细胞。在一些实施方案中,抗体是抗her2抗体,且靶细胞是skbr3细胞。在一些实施方案中,修饰的细胞数与靶细胞数的比率在1:1至1:10的范围内,包括端点。在一些实施方案中,权利要求1-18中任一项的修饰的细胞群体,其中当细胞毒性试验的效应-靶比率为5:1时,修饰的细胞具有至少60%的直接细胞毒性。在一些实施方案中,修饰的细胞具有至少40%的adcc活性。在一些实施方案中,修饰的细胞另外表达嵌合抗原受体。在一些实施方案中,修饰的细胞另外表达自杀基因。在一些实施方案中,自杀基因选自胸苷激酶(tk)基因、胞嘧啶脱氨酶、细胞色素p450和icas9。在一些实施方案中,本公开提供了一种产生能够在激活过程中维持cd16表达的修饰的细胞群体的方法,其中该方法包括将cd16(seqidno:2)而非il-2引入细胞中,其中在激活的修饰的细胞上的cd16表达不低于激活前修饰的细胞上cd16表达的80%。在一些实施方案中,cd16引入是通过慢病毒感染。在一些实施方案中,本公开还提供了包含上述任何实施方案的细胞群体的试剂盒。在一些实施方案中,试剂盒进一步包含抗体。在一些实施方案中,本公开还提供了包含上述任何实施方案的细胞群体和药学上可接受的赋形剂的药物组合物。在一些实施方案中,本公开提供了一种治疗受试者的方法,包括向受试者施用本文所述的药物组合物。附图说明图1a和1b显示了在pma/离子霉素处理之前(图1a)和之后(图1b)对“hank003细胞”(表达cd16的非il-2依赖性细胞)、il2依赖性细胞和供体nk细胞上的cd16表达的流式细胞术分析的结果。图2a-2c显示了对hank003细胞、il2依赖性细胞和供体nk细胞上的cd16表达的流式细胞分析的结果。图2a显示了与k562细胞共培养之前细胞上的cd16表达,图2b显示了与k562细胞共培养4小时后的cd16表达,和图2c显示了共培养24小时后的cd16表达。图3a和3b显示了adcc后hank003细胞和il2依赖性细胞中的cd16表达水平。adcc通过在1μg/ml利妥昔单抗存在下以1:0(仅效应物)至1:4的e:t比率共培养和dohh细胞4小时来进行,然后通过流式细胞术测量4小时和24小时的cd16表达水平。图3a显示了adcc以及对照(e:t=1:0)后的hank-003和il2依赖性中cd16表达水平的流式细胞术分析。图3b显示了4小时和24小时后cd16表达的中值荧光强度(mfi)。图4显示了在anktm细胞用携带cd16转基因的慢病毒感染后24周时间内的各个不同时间点,hank003细胞和il2依赖性克隆(h2、h7、h20、p74、p82和p110)的cd16表面染色的中值荧光强度(mfi)。图5a和图5b显示了当细胞与k562细胞以不同的效应-靶比率混合时,通过anktm细胞、hank003细胞和il2依赖性细胞的k562细胞裂解。图6a和图6b显示了在赫赛汀存在下以10:1的效应-靶比率,il2依赖细胞(图6a:h克隆和图6b:p克隆)对skbr-3细胞的抗体依赖性细胞介导的细胞毒性(adcc)。y轴值通过从在相同条件下赫赛汀存在的情况下由il2依赖性细胞裂解的skbr-3细胞的百分比减去在同种型对照抗体存在下由il2依赖性细胞裂解的skbr-3细胞的百分比来确定。具体实施方式本文提供了修饰的细胞,即il2依赖性细胞,其表达fc受体cd16的高亲和力变体,并因此能够实现cd16靶向的抗体依赖性细胞介导的细胞毒性(adcc)。本申请中公开的il2依赖性细胞不表达白介素2(il-2),例如人il-2(genbanktm登录号:aah70338.1)或包含il-2的氨基酸序列的任何多肽。adcc经由cd16fc受体通过识别靶结合的抗体(igg)的fc片段而介导,其激活修饰的细胞进行靶向杀伤。adcc对于许多治疗性应用是重要的。例如,il2依赖性细胞的adcc可通过cd16受体结合靶细胞结合的igg的fc片段来引发,以激活il2依赖性细胞进行靶向杀伤。响应于某些刺激,cd16在靠近细胞膜处被切割,导致受体的细胞外部分的释放和在激活后表达的下调(参见jing等,plosone,10(3):e0121788doi:10.1371/journal.pone.0121788(2015))。在正常情况下,这一机制有助于控制nk细胞的细胞毒性,但在肿瘤环境中,这可能降低adcc效能和癌细胞杀伤。有利的是,本公开中提供的il2依赖性细胞显示出针对癌细胞的优异adcc活性,理论上这可能是且不限于cd16的表达水平在adcc期间和/或之后被维持的事实。就本文公开的修饰的细胞而言,adcc活性指通过adcc杀死靶细胞的能力。在一个示例性实施方案中,adcc活性可通过下式确定:[在mab存在下的e+t反应中的%杀伤-在mab不存在下的e+t反应中的%杀伤]/[100-在mab不存在下的e+t反应中的%杀伤],其中e指修饰的细胞,t指靶细胞,mab指目的抗体,并且%杀伤指在反应中裂解的细胞的百分比。本公开中提供的il2依赖性细胞是通过用含有cd16,高亲和力fc-γ受体(fcγriiia/cd16a),seqidno:1的序列的质粒稳定转染细胞而产生的。il2依赖性细胞不表达il-2。因此,本公开提供了具有抗体依赖性细胞介导的细胞毒性(adcc)的修饰的细胞群体,即il2依赖性细胞,其包含含有cd16(seqidno:2)的核酸分子。任选地,修饰的细胞包含与seqidno:2具有70%、80%、90%或95%同一性的核酸序列。任选地,修饰的细胞包含与seqidno:2具有90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的核酸序列。任选地,修饰的细胞包含与seqidno:1具有70%、80%、90%或95%同一性的多肽。任选地,修饰的细胞包含与seqidno:1具有90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的多肽。术语本文所用的核酸指脱氧核糖核苷酸或核糖核苷酸及其聚合物和互补物。该术语包括单链或双链形式的脱氧核糖核苷酸或核糖核苷酸。该术语包括含有已知的核苷酸类似物或修饰的主链残基或连接(其为合成的、天然存在的和非天然存在的)的核酸,其具有与参考核酸相似的结合性质,并且其以与参考核苷酸相似的方式代谢。这些类似物的例子包括但不限于硫代磷酸酯、氨基磷酸酯、甲基膦酸酯、手性甲基膦酸酯、2-o-甲基核糖核苷酸、肽核酸(pnas)。除非另有说明,核酸序列的保守修饰变体(例如简并密码子替换)和互补序列可用于替代本文所述的特定核酸序列。具体而言,简并密码子替换可通过生成其中一个或多个选定的(或全部)密码子的第三位被混合碱基和/或脱氧肌苷残基替换的序列来实现(batzer等,nucleicacidres.19:5081(1991);ohtsuka等,j.biol.chem.260:2605-2608(1985);rossolini等,mol.cell.probes8:91-98(1994))。术语“核酸”可与基因、cdna、mrna、寡核苷酸和多核苷酸互换使用。当一个核酸与另一个核酸序列形成功能性关系时,该核酸可操作地连接。例如,如果编码前序列或分泌前导序列的dna作为参与多肽分泌的前蛋白被表达、则其与编码多肽的dna可操作地连接;如果启动子或增强子影响编码序列的转录,则其可操作地连接至该编码序列;或者核糖体结合位点的定位使得其促进翻译,则其可操作地连接到编码序列(如果其被定位以便于翻译)。一般地,可操作地连接指被连接的dna序列彼此接近,并且在分泌前导序列的情况下,是连续的且处于阅读相中。但是,增强子不必是连续的。例如,与第二核酸序列可操作地连接的核酸序列直接或间接地与这种第二序列共价连接,尽管任何有效的三维缔合都是可接受的。单个核酸序列可与多个其他序列可操作地连接。例如,单个启动子可以指导多个rna种类的转录。连接可以通过在方便的限制性位点处接合来完成。如果不存在这类位点,则按照常规做法使用合成的寡核苷酸衔接子或接头。本文中使用的术语“多肽”通常具有本领域公认的至少三个氨基酸的聚合物的含义,并且旨在包括肽和蛋白质。然而,该术语也用于指特定功能性多肽类别,例如去饱和酶、延伸酶等。对于每一个这种类别,本公开提供了这类多肽的已知序列的几个例子。然而,本领域普通技术人员将理解,术语“多肽”旨在足够宽泛以不仅包括具有本文(或在本文特别提及的参考文献或数据库中)所述的完整序列的多肽,而且包括代表这种完整多肽的功能性片段(即,保留至少一种活性的片段)的多肽。此外,本领域技术人员应理解,蛋白质序列通常容忍某些置换而不破坏活性。因此,任何保持活性并与相同类别的另一多肽共有至少约30-40%的总体序列同一性(通常大于约50%、60%、70%或80%,并且通常进一步包括至少一个具有高得多的同一性的区域,通常在一个或多个高度保守区域(通常包含至少3-4个且通常最多20个或更多个氨基酸)中大于90%或甚至95%、96%、97%、98%或99%)的多肽包含在本发明所用的相关术语“多肽”内。本领域技术人员可以通过分析本文所述各种多肽的序列来确定其他相似性和/或同一性的区域。如本领域技术人员所知,多种策略是已知的,并且可以使用工具来进行氨基酸或核苷酸序列的比较以评估同一性和/或相似性的程度。这些策略包括例如人工比对、计算机辅助的序列比对及其组合。用于执行序列比对的多种算法(其通常是由计算机执行的)是广泛可得的,或者可以由本领域技术人员产生。代表性的算法包括例如smith和waterman(adv.appl.math.,1981,2:482)的局部同源性算法;needleman和wunsch(j.mol.biol.,1970,48:443)的同源性比对算法;pearson和lipman(proc.natl.acad.sci.(usa),1988,85:2444)的相似性检索方法;和/或这些算法的计算机化实施(例如,wisconsingeneticssoftwarepackagerelease7.0中的gap、bestfit、fasta和tfasta,geneticscomputergroup,575sciencedr.,madison,wis.)。整合这些算法的容易获得的计算机程序包括,例如,blastn、blastp、gappedblast、pileup、clustalw等。当使用blast和gappedblast程序时,可以使用相应程序的默认参数。或者,实施者可根据其实验和/或其他要求使用非默认参数(例如,参见网址为www.ncbi.nlm.nih.gov的网站)。本文中使用的术语“转化”指通过其将外源或异源核酸分子(例如,载体或重组核酸分子)引入受体细胞或微生物中的过程。外源或异源核酸分子可以整合或不整合到(即,共价连接至)构成宿主细胞或微生物基因组的染色体dna中。例如,外源或异源多聚核苷酸可以保持在游离体元件如质粒上。可选地或另外地,外源或异源多聚核苷酸可以变成整合到染色体中,从而通过染色体复制被子细胞遗传。用于转化的方法包括但不限于磷酸钙沉淀;受体细胞与含有重组核酸的细菌原生质体融合;用含有重组核酸的脂质体处理受体细胞;deae葡聚糖;使用聚乙二醇(peg)融合;电穿孔;磁穿孔;基因枪递送;逆转录病毒感染;脂质转染;以及直接将dna微注射到细胞中。术语“转化的”,如在提及细胞时所使用的,指已经经历如本文所述的转化的细胞,使得细胞携带外源或异源遗传物质(例如,重组核酸)。术语“转化的”也可以或替代地用于指含有外源或异源遗传物质的微生物、微生物株、组织、生物体等。当提及细胞、核酸、多肽、载体等使用时,术语“修饰的”和“重组的”表示该细胞、核酸、多肽、载体等已经通过实验室方法进行了修饰或者是实验室方法的结果,并且是非天然存在的。因此,例如,修饰的细胞包括通过实验室方法(例如,用于将核酸引入细胞中的转化方法)产生或修饰的细胞。修饰的细胞可包括在细胞的天然(非重组)形式中未发现的核酸序列,或可包括已被改变的核酸序列,例如与非天然启动子连接的核酸序列。如本文所用,术语“效应-靶比率”指用于评估效应细胞对靶细胞的细胞毒性的分析中使用的效应细胞(例如,细胞,如il2依赖性细胞)的数量与靶细胞(例如,肿瘤细胞)的数量的比率。如本文所用,“自然杀伤(nk)细胞”是指在没有特定抗原性刺激的情况下杀死靶细胞的免疫系统细胞,且没有根据主要组织相容性复合物(mhc)类别的限制。靶细胞可以是癌细胞或肿瘤细胞。nk细胞特征在于cd56表面标志物的存在和cd3表面标志物的不存在。如本文所用,“细胞”指从如gong等(1994)所描述的高效力独特细胞系衍生的自然杀伤细胞,其权利为nantkwest所有。为本发明之目的且除非另有说明,术语或“nk92”意指原始细胞系以及已被修饰(例如通过引入外源基因)的细胞系、细胞的克隆和细胞。细胞及其示例性和非限制性的修饰描述于美国专利第7,618,817;8,034,332;8,313,943;9,181,322;9,150,636号;和公开的美国申请10/008,955号中,其全部通过引用整体并入本文,且包括野生型和细胞为本领域技术人员所知,且对于本领域技术人员来说其可从nantkwest,inc.方便地获得。如本文所用,术语“anktm细胞”指从gong等(1994)中所描述的高效力独特细胞系衍生的未修饰的自然杀伤细胞,其权利为nantkwest所有。如本文所用,术语“细胞”指衍生于gong等(1994)中所描述的高效力独特细胞系的自然杀伤细胞,其权利为nantkwest所有,其经修饰以在细胞表面上表达cd16(以下,“cd16阳性细胞”或“细胞”)。因此,细胞的例子包括il2依赖性细胞(“hank003细胞”)和il2依赖性细胞—前者另外表达重组il-2,而后者不表达。本文使用的术语“nk细胞”指a)供体来源的nk细胞,b)nk-92.176v-cd16.eril2细胞(即,非il2依赖性细胞)和c)nk-92.176v-cd16细胞(即,il2依赖性细胞)。如本文所公开的,供体来源的nk细胞在激活时表现出快速和深度的cd16表达降低,其中在过夜恢复后仅具有边际的表达恢复,细胞(il2依赖性和非依赖性类似的)在维持峰值细胞毒性效力的同时表现出很少或没有cd16表达的降低。术语“fc受体”指在某些细胞(例如,自然杀伤细胞)表面上发现的蛋白质,其通过结合于称为fc区的抗体部分而造成免疫细胞的保护功能。抗体的fc区与细胞的fc受体(fcr)的结合通过抗体介导的吞噬作用或抗体依赖性细胞介导的细胞毒性(adcc)刺激细胞的吞噬或细胞毒性活性。fcr根据其识别的抗体类型进行分类。例如,fc-γ受体(fcγr)与抗体的igg类结合。fcγriii-a(也称为cd16)是一种低亲和力的fc受体,其结合igg抗体并激活adcc。fcγriii-a通常存在于nk细胞上。细胞不表达fcγriii-a。编码cd16的代表性氨基酸序列显示于seqidno:1中。编码cd16的代表性多核苷酸序列显示于seqidno:2中。cd16的完整序列可在swissprot数据库中作为条目p08637找到。本文所用术语“激活”涉及本文所公开的修饰的细胞或nk细胞时指的是通过接触一种或多种激活剂(刺激剂)而刺激nk细胞以发挥细胞毒性功能的现象。这些细胞毒性功能可包括释放胞质蛋白质,例如穿孔素和称为颗粒酶的蛋白酶,以诱导紧密邻近细胞的凋亡或裂解。这些激活剂包括但不限于各种细胞因子(例如,干扰素或巨噬细胞衍生的细胞因子)、植物凝集素(例如,植物血凝素(pha)、伴刀豆球蛋白a(cona)和美洲商陆丝裂原(pwm))、脂多糖(lps)、pma(佛波醇12-肉豆蔻酸13-乙酸酯)/离子霉素、结核菌素的纯化蛋白质衍生物(ppd)。激活可以指a)pha刺激,b)通过与k562共孵育的先天途径激活,或c)通过与利妥昔单抗和dohh共孵育的adcc激活。在一些实施方案中,激活剂可以是肿瘤细胞。在一些实施方案中,激活剂为具有配体(例如,ulbp和mica/b)的肿瘤细胞,该配体可被nk细胞或修饰的细胞上的受体(例如nkg2d、nkp46、nkp30和dnam-1)识别。这种相互作用激活nk细胞,其使肿瘤细胞溶解。在一些实施方案中,激活nk细胞或修饰的细胞的肿瘤细胞为k562细胞。nk细胞或修饰的细胞也可通过接触一种或多种包含抗体及其靶细胞的激活剂而被激活。在nk细胞或修饰的细胞上表达的fc受体cd16识别靶结合的抗体的fc片段并与其相互作用,且这种相互作用激活nk细胞以裂解靶细胞,这是称为adcc的过程。术语“表达”指基因产物的产生。当提及表达时,术语“稳定”指多核苷酸被整合到细胞的基因组中并表达。如本文所用,术语“抗体”指免疫球蛋白或其片段。抗体可以是任何类型的(例如,igg、iga、igm、ige或igd)。优选地,抗体为igg。抗体可以是非人的(例如,来自小鼠、山羊或任何其他动物)、全人的、人源化的或嵌合的。抗体可以是多克隆的或单克隆的。任选地,该抗体是单克隆的。如本文所用,术语“癌症”指在哺乳动物中发现的所有类型的癌症、赘生物或恶性肿瘤,包括白血病、癌瘤和肉瘤。示例性癌症包括脑癌、乳腺癌、子宫颈癌、结肠癌、头颈癌、肝癌、肾癌、肺癌、非小细胞肺癌、黑色素瘤、间皮瘤、卵巢癌、肉瘤、胃癌、子宫癌和髓母细胞瘤。另外的实例包括霍奇金病、非霍奇金淋巴瘤、多发性骨髓瘤、神经母细胞瘤、卵巢癌、横纹肌肉瘤、原发性血小板增多症、原发性巨球蛋白血症、原发性脑瘤、癌症、恶性胰腺胰岛瘤、恶性类癌、膀胱癌、癌前皮肤病变、睾丸癌、淋巴瘤、甲状腺癌、神经母细胞瘤、食道癌、泌尿生殖道癌、恶性高钙血症、子宫内膜癌、肾上腺皮质癌、内分泌和外分泌腺的肿瘤和前列腺癌。细胞细胞系是发现在存在白介素2(il-2)的情况下增殖的独特细胞系。gong等,leukemia8:652-658(1994)。这些细胞对多种癌症具有高的细胞溶解活性。细胞是具有广泛的抗肿瘤细胞毒性的同源癌性nk细胞群体,在扩增后具有可预期的结果。一期临床试验已确认其安全性特征。在患有非霍奇金淋巴瘤的受试者的血液中发现,且然后离体永生化。细胞源自nk细胞,但缺乏正常nk细胞呈现的主要抑制性受体,同时保留了大多数激活性受体。然而,细胞不攻击正常细胞,也不会在人体内引发不可接受的免疫排斥反应。细胞系的表征在wo1998/49268和美国专利申请公开号2002-0068044中公开。据发现细胞系呈现cd56bright、cd2、cd7、cd11a、cd28、cd45和cd54表面标志物。此外,它不显示cd1、cd3、cd4、cd5、cd8、cd10、cd14、cd16、cd19、cd20、cd23和cd34标志物。细胞在培养物中的生长依赖于重组白介素2(ril-2)的存在,低至1iu/ml的剂量足以维持增殖。il-7和il-12不支持长期生长,其他测试的细胞因子也不支持,包括il-1α、il-6、肿瘤坏死因子α、干扰素α和干扰素γ。即使以1:1的低效应:靶(e:t)比率,仍具有高细胞毒性。gong等,同上。细胞保藏于美国典型培养物保藏中心(atcc),命名为crl-2407。虽然细胞保留了与nk细胞相关的几乎所有激活性受体和细胞溶解途径,但其在细胞表面上不表达cd16。cd16是识别并结合抗体的fc部分以激活nk细胞的抗体依赖性细胞毒性(adcc)的fc受体。由于不存在cd16受体,细胞无法通过adcc机制裂解靶细胞,并因此不能增强内源性或外源性抗体(即利妥昔单抗和赫赛汀)的抗肿瘤作用。对内源性nk细胞的研究表明,il-2(1000iu/ml)对运输过程中nk细胞的激活至关重要,但细胞无需维持在37℃和5%的二氧化碳下。koepsell等,transfusion53:398-403(2013)。然而,内源性nk细胞与细胞显著不同,这在很大程度上是因为其明显不同的起源:是衍生自癌症的细胞系,而内源性nk细胞是从供体(或患者)收获并处理用于输注入患者体内。内源性nk细胞制备物是异质细胞群体,而细胞是同质的克隆细胞系。细胞在培养中容易地增殖而同时保持细胞毒性,而内源性nk细胞则不能。另外,内源性的nk细胞异质群体不以高密度聚集。此外,内源性nk细胞表达fc受体,包括细胞不表达的cd-16受体。产生il2依赖性细胞本申请中公开的il2依赖性细胞是通过引入高亲和力fcγ受体(fcγriiia/cd16a)基因进行修饰的细胞。该形式的cd16在氨基酸176处具有缬氨酸,其对抗体的fc片段具有高亲和力且因此促进了adcc的提高。可以通过本领域技术人员已知的任何机制将cd16转基因工程化到表达载体中。在一些实施方案中,载体允许将转基因整合到细胞的基因组中。在一些实施方案中,载体具有正向选择标记。正向选择标记包括允许细胞在杀死不表达该基因的细胞的条件下生长的任何基因。非限制性实例包括抗生素抗性,例如遗传霉素(来自tn5的neo基因)。多种载体均可用于表达本文公开的fc受体。在一些实施方案中,载体是质粒。在一个实施方案中,载体是病毒载体。病毒载体包括但不限于慢病毒载体、逆转录病毒载体、腺病毒载体、腺相关病毒载体、单纯疱疹病毒载体、痘病毒载体等。可以使用本领域已知的任何转染方法将转基因引入细胞中,包括但不限于感染、电穿孔、脂质转染、核转染或“基因枪法”。在一些实施方案中,通过慢病毒将cd16转基因引入细胞中。通常,包含cd16转基因的病毒构建体首先与包装慢病毒所需的其他质粒一起被引入到细胞系中。这些质粒可包括至少一个慢病毒包装质粒,例如pcmv-δr8.2,和包膜质粒,例如pcmv-vsv-g。转染后,病毒颗粒在培养物上清液中形成。收集上清液并用于感染细胞以产生表达cd16的il2依赖性细胞。在一些实施方案中,表达cd16的细胞在通过有限稀释进行铺板前被富集。然后可以选择表达cd-16的细胞的单个克隆进行扩增,和然后进行表型和功能分析。因此,本公开中提供了表达cd16(seqidno:1)的修饰的细胞(即il2依赖性细胞)的群体,其中修饰的细胞不表达il-2,并且其中该群体包含一个或多个修饰的细胞。在一些实施方案中,修饰的细胞包含cd16的核酸(seqidno:2)。在一些实施方案中,该修饰的细胞具有抗体依赖性细胞介导的细胞毒性(adcc)。另一类型的细胞,即hank003细胞,通过用含有编码cd16(seqidno:1)和il-2(seqidno:3)的序列的基于双顺反子质粒的载体对细胞进行电穿孔的稳定转染来产生。申请号62/468,890中公开了产生hank003的方法,该申请的全部内容通过引用结合于此。测量il2依赖性细胞上的cd16表达与激活时丧失cd16表达的nk细胞不同,本公开中提供的il2依赖性细胞能够在激活期间和/或之后维持高水平的cd16表达。一般地,尽管缺乏il-2表达,il2依赖性细胞仍保持高水平的cd16表达,表明il-2表达对细胞的cd16稳定性无不利影响。细胞(例如il2依赖性hank细胞)上的cd16表达水平可通过本领域已知测量蛋白质表达的任何方法(例如免疫印迹、elisa和流式细胞术)进行测量。在一些实施方案中,通过流式细胞术测量cd16表达。通过流式细胞术检测cd16表达通常包括将细胞样品与偶联于荧光染料的抗cd16抗体一起孵育。然后在流式细胞仪上分析样品以检测结合的抗体,并且来自结合的抗体的荧光染料的强度,例如平均荧光强度,对应于细胞上cd16表达的量。在一些实施方案中,通过与pma和离子霉素一起孵育激活细胞,例如il2依赖性细胞,并测量激活前和激活后的cd16表达水平。在一些实施方案中,孵育持续0.5-4小时,例如0.5-2小时,或约1小时。在一些实施方案中,用于激活细胞的pma为10-80nm,例如20-60nm,或约40nm。在一些实施方案中,用于激活hanktm细胞的离子霉素为200-1000nm,例如300-800nm、400-700nm或约669nm。在一些实施方案中,与激活前细胞上的cd16表达水平相比,hanktm细胞上的cd16表达水平降低不超过20%,例如不超过40%、不超过30%、不超过25%。在一些实施方案中,与激活前的细胞相比,在激活后对cd16呈阳性的细胞的百分比降低不超过20%或不超过18%。在一些实施方案中,在激活后对cd16呈阳性的细胞的百分比未降低。在一些实施方案中,与激活前的cd16表达水平相比,已激活的细胞(例如,il-2依赖性细胞)表现出0-20%、0-10%或0-5%范围内的cd16表达减少。在一些实施方案中,可以通过将细胞与对nk细胞敏感的靶细胞(例如,肿瘤细胞)共培养来激活细胞,例如,il2依赖性细胞。在一些实施方案中,肿瘤细胞为k562细胞。k562细胞是人慢性髓系白血病细胞。如本公开中使用的,效应-靶比率指相对于靶细胞的数量的效应细胞(例如细胞,包括il2依赖性细胞)数量。在一些实施方案中,效应-靶比率在0.5:1至2:1之间,例如约1:1。孵育期的长度通常足以实现靶细胞的完全细胞毒性杀伤。在一些实施方案中,孵育期为约2至8小时,例如约4小时。在一些实施方案中,在孵育期后,允许细胞在培养基中恢复。在一些实施方案中,恢复期持续12-48小时,例如约20-28小时或约24小时。在一些实施方案中,i)在细胞与靶细胞(例如,靶肿瘤细胞)接触之前的时间和ii)在孵育期结束时和/或恢复期结束时监测细胞上的cd16表达水平。在一些实施方案中,与激活前的细胞相比,细胞群体在与靶细胞接触后(例如,在孵育期结束时或恢复期结束时)的cd16表达下降不超过20%、不超过10%、不超过5%、不超过3%。在一些实施方案中,与接触靶细胞之前的细胞相比,在孵育期结束时或恢复期结束时对cd16呈阳性的细胞的百分比降低不超过20%、不超过10%。在一些实施方案中,细胞也可以通过接触抗体及其靶细胞被激活,其中接触导致adcc。在一些实施方案中,抗体为利妥昔单抗(抗cd20抗体),和靶细胞为dohh-2细胞。在一些实施方案中,抗体为赫赛汀(抗her2抗体),和靶细胞为skbr3细胞。在一些实施方案中,效应-靶比率在1:1至1:10的范围内,例如1:1、1:2或1:4。在一些实施方案中,与adcc前的hank003细胞相比,在adcc后细胞(例如il2依赖性细胞)上的cd16表达降低不超过50%,例如不超过40%、不超过30%、不超过25%、不超过20%、不超过10%。在一些实施方案中,与adcc之前的群体中的细胞相比,在cd16阳性的群体中的细胞(例如,il2依赖性细胞)的百分比降低不超过20%或不超过10%。因此,本公开还提供了产生能够在激活期间维持cd16表达的修饰的细胞群体的方法,其中该方法包括将cd16(seqidno:2)而非il-2引入细胞中,其中在激活的修饰细胞上的cd16表达不低于激活前修饰的细胞上cd16表达的50%。在一些实施方案中,已激活的细胞(例如,il-2依赖性细胞)从激活开始保持细胞毒性的稳态至少24小时。细胞的细胞毒性可使用本领域公知的方法进行测量。在一些实施方案中,细胞毒性是直接细胞毒性。在一些实施方案中,细胞毒性为adcc。在一段时间内保持细胞毒性的稳态是指细胞裂解靶细胞的能力在参考时间段内基本保持相同。在某些情况下,维持细胞毒性的稳态反映为在相同的测定条件下,在参考时间段结束时被效应细胞裂解的靶细胞的百分比为在参考时间段开始时效应细胞裂解的靶细胞百分比的至少70%,例如至少75%、至少80%、至少85%、至少90%或至少95%。另外的转基因在一些实施方案中,修饰的细胞,例如il2依赖性细胞,进一步工程化以在细胞表面上表达嵌合抗原受体(car)。任选地,car对肿瘤特异性抗原具有特异性。在us2013/0189268;wo1999024566a1;us7098008和wo2000020460a1中以非限制性实例的方式描述了肿瘤特异性抗原;其每一篇通过引用整体结合于此。肿瘤特异性抗原包括但不限于nkg2d、cs1、gd2、cd138、epcam、ebna3c、gpa7、cd244、ca-125、eta、mage、cage、bage、hage、lage、page、ny-seo-1、gage、cea、cd52、cd30、muc5ac、c-met、egfr、fab、wt-1、psma、ny-eso1、afp、cea、ctag1b、cd19和cd33。另外的非限制性肿瘤相关抗原及与之相关的恶性肿瘤可见表1中。表1:肿瘤特异性抗原和相关恶性肿瘤在一些实施方案中,car靶向cd19、cd33或pd-l1。在实例中,使用本领域已知的方法制备变体多肽,如寡核苷酸介导的(定点)诱变、丙氨酸扫描和pcr诱变。定点诱变(carter,1986;zoller和smith,1987)、盒式诱变、限制选择诱变(wells等,1985)或其他已知技术可以对克隆的dna进行以产生cd16变体(ausubel,2002;sambrook和russell,2001)。任选地,car靶向与特定癌症类型相关的抗原。任选地,癌症选自白血病(包括急性白血病(例如,急性淋巴细胞性白血病、急性髓细胞性白血病(包括成髓细胞性、早幼粒细胞性、髓单核细胞性、单核细胞性和红白血病))和慢性白血病(例如,慢性髓细胞性(粒细胞性)白血病和慢性淋巴细胞性白血病)、真性红细胞增多症、淋巴瘤(例如,霍奇金病和非霍奇金病)、多发性骨髓瘤、瓦尔登斯特伦巨球蛋白血症、重链病、实体肿瘤,包括但不限于肉瘤和癌瘤如纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、成骨性肉瘤、脊索瘤、血管肉瘤、内皮肉瘤、淋巴管肉瘤、淋巴管内皮肉瘤、滑膜瘤、间皮瘤、尤因氏瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、胰腺癌、乳腺癌、卵巢癌、前列腺癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、囊腺癌、髓样癌、支气管源性癌、肾细胞癌、肝细胞瘤、胆管癌、绒毛膜癌、精原细胞瘤、胚胎癌、肾母细胞瘤、子宫颈癌、睾丸肿瘤、肺癌、小细胞肺癌、膀胱癌、上皮癌、神经胶质瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质瘤、脑膜血管瘤、黑色素瘤、神经母细胞瘤和视网膜母细胞瘤。在一些实施方案中,编码car的多核苷酸经突变以改变编码car的氨基酸序列而不改变car的功能。例如,可在以上公开的car中进行导致“非必需”氨基酸残基处的氨基酸置换的多核苷酸置换。car可以按照例如专利公开号wo2014039523;us20140242701;us20140274909;us20130280285和wo2014099671中所述工程化,其每一篇通过引用整体结合于此。任选地,car为cd19car、cd33car或cspg-4car。另外的修饰-自杀基因在一些实施方案中,修饰的细胞,例如il2依赖性细胞,进一步工程化以引入自杀基因。术语“自杀基因”是允许对细胞进行负向选择的基因。自杀基因被用作安全系统,从而允许表达该基因的细胞通过引入选择试剂而被杀死。这在重组基因引起导致不受控制的细胞生长的突变的情况下是需要的。已确认了多种自杀基因系统,包括单纯疱疹病毒胸苷激酶(tk)基因、胞嘧啶脱氨酶基因、水痘-带状疱疹病毒胸苷激酶基因、硝基还原酶基因、大肠杆菌gpt基因和大肠杆菌deo基因(也参见,例如yazawak,fisherwe,brunicardifc:currentprogressinsuicidegenetherapyforcancer.worldj.surg.2002july;26(7):783-9)。如本文所用,自杀基因在细胞中具有活性。通常,自杀基因编码的蛋白质对细胞无任何不良影响,但在特定化合物存在时杀死细胞。因此,自杀基因通常是系统的一部分。在一个实施方案中,自杀基因是胸苷激酶(tk)基因。tk基因可以是野生型或突变体tk基因(例如,tk30、tk75、sr39tk)。表达tk蛋白的细胞可以用更昔洛韦杀死。在另一实施方案中,自杀基因是胞嘧啶脱氨酶,其在5-氟胞嘧啶存在下对细胞是毒性的。garcia-sanchez等,"cytosinedeaminaseadenoviralvectorand5-fluorocytosineselectivelyreducebreastcancercells1million-foldwhentheycontaminatehematopoieticcells:apotentialpurgingmethodforautologoustransplantation."blood1998jul15;92(2):672-82。在另一实施方案中,自杀基因是细胞色素p450,其在异环磷酰胺或环磷酰胺存在下是毒性的。参见,例如,touati等,"asuicidegenetherapycombiningtheimprovementofcyclophosphamidetumorcytotoxicityandthedevelopmentofananti-tumorimmuneresponse."currgenether.2014;14(3):236-46。在另一实施方案中,自杀基因是icas9。distasi,(2011)"inducibleapoptosisasasafetyswitchforadoptivecelltherapy."nengljmed365:1673-1683。也参见morgan,"liveandletdie:anewsuicidegenetherapymovestotheclinic"moleculartherapy(2012);20:11-13。icas9蛋白在小分子ap1903存在下诱导细胞凋亡。ap1903是生物学惰性小分子,其在临床研究中表明具有良好的耐受性,并已用于过继细胞治疗的情况中。与上述公开的cd19转基因一样,这些另外的转基因(例如,cd19car)可通过本领域技术人员已知的任何机制工程化到表达载体中。这些另外的转基因可工程化到与cd19转基因相同的表达载体或不同的表达载体中。在优选实施方案中,该转基因被工程化到相同的载体中。使用il2依赖性细胞的治疗方法还提供了用修饰的细胞(例如本文所述的il2依赖性细胞)治疗受试者的方法。任选地,受试者用修饰的细胞和抗体治疗。修饰的细胞,例如il2依赖性细胞,例如il2依赖性细胞,可以按照细胞的绝对数量施用于受试者,例如,所述受试者可以施用约1000个细胞/注射至高达约100亿个细胞/注射,例如大约、至少约或至多约1×1010、1×109、1×108、1×107、5×107、1×106、5×106、1×105、5×105、1×104、5×104、1×103、5×103(等等)个修饰的细胞,例如il2依赖性细胞/注射,或任意两个数字之间的任何范围(包括端点)。任选地,受试者施用1×108至1×1010个细胞。任选地,每周施用细胞一次或多次,持续一周或多周。任选地,每周施用细胞一次或两次,持续1、2、3、4、5、6、7、8、9、10周或更多周。任选地,受试者施用约1000个细胞/注射/m2至高达约100亿个细胞/注射/m2,例如约、至少约或至多约1×108/m2、1×107/m2、5×107/m2、1×106/m2、5×106/m2、1×105/m2、5×105/m2、1×104/m2、5×104/m2、1×103/m2、5×103/m2(等等)个修饰的细胞,例如il2依赖性细胞/注射,或任意两个数字之间的任何范围(包括端点)。任选地,修饰的细胞,例如il2依赖性细胞可按照细胞的相对数量施用于这种个体,例如,所述个体可施用约1000个细胞至高达约100亿个细胞/千克个体,例如约、至少约或至多约1×108、1×107、5×107、1×106、5×106、1×105、5×105、1×104、5×104、1×103、5×103(等等)个修饰的细胞,例如il2依赖性细胞/千克个体,或任意两个数字之间的任何范围(包括端点)。任选地,总剂量可按体表面积的m2计算,包括约1×1011、1×1010、1×109、1×108、1×107/m2,或任意两个数值之间的任何范围(包括端点)。任选地,向患者施用约10亿至约30亿个修饰的细胞,例如il2依赖性细胞。任选地,每剂量注射的修饰的细胞(例如,il2依赖性细胞)的量可以按体表面积的m2计算,包括1×1011、1×1010、1×109、1×108、1×107/m2。修饰的细胞(例如,il2依赖性细胞)和任选地其他抗癌剂可对癌症患者施用一次,可施用多次,例如在治疗期间每1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22或23小时一次,或每1、2、3、4、5、6或7天一次,或每1、2、3、4、5、6、7、8、9、10周或更多周一次,或任意两个数值之间的任何范围(包括端点)。在一个实施方案中,修饰的细胞,例如il2依赖性细胞,在施用于患者之前被辐射。例如,在美国专利号8,034,332中描述了对修饰的细胞(例如il2依赖性细胞)的辐射,该专利通过引用整体并入本文。在一个实施方案中,辐射未经工程化以表达自杀基因的修饰的细胞,例如il2依赖性细胞。任选地,修饰的细胞(例如,il2依赖性细胞)在包含修饰的细胞(例如,il2依赖性细胞)和介质(例如,人血清或其等同物)的组合物中施用。任选地,该介质包含人血清清蛋白。任选地,介质包含人血浆。任选地,介质包含约1%至约15%的人血清或人血清等同物。任选地,介质包含约1%至约10%的人血清或人血清等同物。任选地,介质包含约1%至约5%的人血清或人血清等同物。任选地,介质包含约2.5%的人血清或人血清等同物。任选地,血清为人ab血清。任选地,使用可接受用于人类治疗剂中的血清替代物代替人血清。该类血清替代物在本领域中可能是已知的。任选地,修饰的细胞(例如,il2依赖性细胞)在包含修饰的细胞(例如,il2依赖性细胞)和支持细胞活力的等渗液体溶液的组合物中施用。任选地,修饰的细胞(例如,il2依赖性细胞)在从冷冻保存的样品重构的组合物中施用。根据本文提供的方法,受试者施用有效量的一种或多种本文提供的药剂。术语有效量和有效剂量可互换使用。术语有效量被定义为产生所需生理反应(例如炎症减轻)所需的任何量。用于施用药剂的有效量和时间表可由本领域技术人员根据经验确定。用于施用的剂量范围是足够大以产生其中疾病或障碍的一种或多种症状受到影响(例如减轻或延迟)的所需效果的那些。剂量不应过大以至于引起实质的不良反应,如不必要的交叉反应、过敏反应等。一般地,剂量随年龄、状况、性别、疾病类型、疾病或障碍的程度、施用途径或方案中是否包含其他药物而变化,并且可由本领域技术人员确定。在任何禁忌症的情况中,个体医生可调整剂量。剂量可以变化,并且可以每天以一个或多个剂量施用来给药,持续一天或几天。在文献中可以找到给定类别药品的适当剂量的指导。例如,对于给定参数,有效量将显示至少5%、10%、15%、20%、25%、40%、50%、60%、75%、80%、90%或至少100%的提高或降低。功效也可以表示为“倍数”提高或降低。例如,与对照相比,治疗有效量可具有至少1.2倍、1.5倍、2倍、5倍或更高的效果。准确的剂量和制剂取决于治疗目的,并且由本领域技术人员使用已知技术确定(例如参见lieberman,pharmaceuticaldosageforms(vols.1-3,1992);lloyd,theart,scienceandtechnologyofpharmaceuticalcompounding(1999);remington:thescienceandpracticeofpharmacy,22ndedition,gennaro,editor(2012)和pickar,dosagecalculations(1999))。药学上可接受的组合物可包括多种载体和赋形剂。可以使用多种水性载体,例如缓冲盐水等。这些溶液是无菌的,且通常不含不需要的物质。合适的载体和赋型剂及其制剂描述于remington:thescienceandpracticeofpharmacy,21stedition,davidb.troy,ed.,lippicottwilliams&wilkins(2005)中。药学上可接受的载体是指在生物学上或其他方面不是不希望的材料,即该材料施用于受试者而不会引起不希望的生物学效应或以有害的方式与包含该材料的药物组合物的其他组分相互作用。如果施用于受试者,载体可任选地选择为使活性成分的降解最小化并使受试者中的不良副作用最小化。如本文所用,术语“药学上可接受的”与“生理上可接受的”和“药理上可接受的”同义使用。根据给药途径,药物组合物通常包含用于缓冲和储存中防腐的试剂,并且可包括用于适当递送的缓冲剂和载体。组合物可包含近似生理条件所需的可接受的辅助物质,例如ph调节剂和缓冲剂、毒性调节剂等,例如乙酸钠、氯化钠、氯化钾、氯化钙、乳酸钠等。这些制剂中的细胞和/或其他试剂的浓度可以变化,并且主要基于流体体积、粘度、体重等根据所选择的特定施用模式和受试者的需求进行选择。任选地,修饰的细胞(例如,il2依赖性细胞)与一种或多种用于所治疗的癌症的其他治疗联合施用于受试者。不受理论的约束,据信受试者用修饰的细胞(例如,il2依赖性细胞)和另一种癌症疗法共同治疗允许修饰的细胞(例如,il2依赖性细胞)和替代治疗能够给予内源性免疫系统清除之前压倒该内源性作用的癌症的可能。任选地,用于正在治疗的癌症的两种或更多种其他治疗包括,例如,抗体、放射、化学治疗、干细胞移植或激素治疗。任选地,抗体与修饰的细胞(例如,il2依赖性hank细胞)结合施用于患者。任选地,修饰的细胞(例如,il2依赖性细胞)和抗体一起(例如,在相同的制剂中);单独地(例如在单独的制剂中)同时施用于受试者;或者可以单独施用,例如按照不同的给药方案或在一天的不同时间。当单独施用时,抗体可通过任何合适的途径施用,例如静脉内或口服施用。任选地,抗体可用于靶向癌细胞或表达癌症相关标志物的细胞。许多抗体已被批准单独用于治疗癌症。表2.fda批准的示例的治疗性单克隆抗体抗体可以通过多种机制治疗癌症。当免疫细胞(如nk细胞)与通过fc受体(如cd16)结合靶细胞的抗体结合时,发生adcc。因此,表达cd16的细胞与有效量的至少一种针对特定癌症相关蛋白的单克隆抗体一起施用于受试者,例如阿仑单抗、贝伐单抗、替伊莫单抗、奥法木单抗、利妥昔单抗和曲妥珠单抗。任选地,单克隆抗体为裸单克隆抗体、偶联单克隆抗体或双特异性单克隆抗体。任选地,可以使用结合癌细胞并且还结合存在于细胞表面上的细胞表面蛋白的双特异性抗体。癌症特异性抗体与在癌细胞表面上表达的特定蛋白质抗原结合。细胞可以被修饰,使得抗体与细胞表面相结合。任选地,该抗体对癌症具有特异性。通过这种方式,细胞可以特异性地靶向癌症。中和抗体也可以被分离。例如,分泌的糖蛋白ykl-40在多种类型的晚期人类癌症中升高。设想抗ykl-40的抗体可用于抑制肿瘤生长、血管生成和/或转移。参见faibish等,(2011)mol.cancerther.10(5):742-751。针对癌症的抗体可从商业上可获得的来源购买,或可通过本领域已知的任何方法产生。例如,可通过从先前一名或多名受癌症感染并在取样时已恢复或正在恢复的患者获得b细胞、骨髓或其他样品来产生抗体。从这些样品鉴定、筛选和生长抗体(例如单克隆抗体)的方法是已知的。例如,可以通过从目标样品或细胞分离rna、从分离的rna制备cdna、针对重链和/或轻链cdna富集cdna,并使用噬菌体展示载体创建文库来制备噬菌体展示文库。例如,可以如maruyama等中所述制备和筛选文库,该文献在此全文引入作为参考。抗体可以通过重组方法或任何其他方法制备。beerli等,pnas(2008)105(38):14336-14341中也描述了人单克隆抗体的分离、筛选、表征和产生,该文献在此全文引入作为参考。药剂或组合物的组合可以伴随(例如作为混合物)、单独但同时(例如通过单独的静脉内管线)或顺序(例如首先施用一种药剂,然后施用第二药剂)来施用。因此,术语组合用于指伴随、同时或顺序施用两种或更多种药剂或组合物。根据受试者的具体特征和所选择的治疗类型,治疗过程最好是对于个体逐个确定。治疗(例如本文所公开的那些)可每日、每日两次、每两周、每月或以治疗有效的任何适用的方式施用于受试者。治疗可以单独施用或与本文公开的或本领域已知的任何其他治疗联合施用。另外的治疗可以与第一治疗同时、在不同的时间或按照完全不同的治疗方案施用(例如,第一治疗可以是每日施用,而另外的治疗是每周施用)。试剂盒还公开了包含所提供的il2依赖性细胞的试剂盒。任选地,试剂盒进一步包括一种或多种另外的药剂,如抗体。试剂盒的组分可包含在一个或不同的容器中,例如一个或多个小瓶。抗体可以是液体或固体形式(例如,冷冻干燥后)以增加保质期。如果是液体形式,组分可包含添加剂(如稳定剂和/或防腐剂(如脯氨酸、甘氨酸或蔗糖)或其他增加保质期的添加剂)。任选地,试剂盒可包含另外的化合物,例如在施用il2依赖性细胞和抗体之前、同时或之后施用的治疗活性化合物或药物。这类化合物的例子包括维生素、矿物质、氟氢化可松、布洛芬、利多卡因、奎尼丁、化学治疗剂等。任选地,试剂盒的使用说明包括在癌症治疗中使用试剂盒组分的说明。说明书还可包含关于如何制备(例如,在冷冻干燥的蛋白质的情况下,稀释或重构)抗体和il2依赖性细胞(例如,解冻和/或培养)的信息。说明书还可包括关于施用剂量和频率的指导。公开了可用于所公开的方法和组合物、可与所公开的方法和组合物结合使用、可用于制备所公开的方法和组合物或为所公开的方法和组合物的产物的材料、组合物和组分。本文公开了这些和其他材料,并且应当理解,当公开这些材料的组合、子集、相互作用、组等时,尽管可能未明确公开对这些化合物的各种单独和集体组合和排列各自的具体引用,但在本文中对其每一种都具体的考虑和描述。例如,如果公开和讨论了一种方法,并且讨论了可以对包括该方法在内的多个分子进行的多种修改,则该方法和可能的修改的各种和每一种组合和排列都是特别考虑的,除非特别指出相反的情况。同样,也特别地考虑和公开了这些的任何子集或组合。该概念适用于本公开的所有方面,包括但不限于使用所公开组合物的方法中的步骤。因此,如果存在可执行的多个另外的步骤,则应理解这些另外步骤中的每一个可通过所公开方法的任何特定方法步骤或方法步骤的组合来执行,并且每一个这样的组合或组合的子集被具体考虑并应被视为已公开。本文引用的公开出版物及对于其所引用的材料在此具体地通过引用整体并入。以下实施例旨在进一步说明本文所述方法和组合物的某些方面,而非旨在限制权利要求的范围。实施例实施例1.材料实施例中所描述的细胞表面蛋白的细胞荧光分析通过使用特定的荧光团偶联抗体或上表中所列的相应同种型对照的直接免疫染色来进行。简而言之,10e5个细胞在100μl流式细胞染色缓冲液(pbs,1%bsa)中于4℃下在黑暗中用制造商推荐的抗体量染色30分钟。细胞用流式细胞染色缓冲液洗涤两次,并重悬于200μl流式细胞染色缓冲液中。样品在10流式细胞仪(miltenyibiotec)上进行处理,并使用flowjo软件分析数据。实施例中使用的抗体如表3中所示:表3.抗体实施例2.il2依赖性hank细胞的产生通过用pcl20c-v176-cd16慢病毒构建体稳定转染anktm细胞对细胞进行遗传修饰来产生il2依赖性细胞。该构建体编码在氨基酸176(从全长蛋白质的起始密码子开始计算)具有缬氨酸,而非天然cd16多肽中的苯丙氨酸,的cd16序列,这使得adcc增加。pcl20c-v176-cd16构建体基于pcl20c-mp-cd19car-ires-gfp(seqidno:6)产生,其为8928bp且包含2917-4380bp位的cd19-car、4381-4980bp位的ires和4981-5700bp位的gfp。质粒用kpni消化,其在2906、4852和5729位切割以去除cd19-car和gfp。限制性消化生成三个以下大小的片段:6015(骨架)、1946和877bp。对骨架片段进行纯化,并将包含顶链(seqidno:7)和底链(seqidno:8)的双链寡聚体连接到上述产生的骨架上。这一寡核苷酸的添加引入了ecori、sphi和noti位点,它们在cd16序列中是非切割体(non-cutter)。cd16基因使用pcr引物seqidno:9和seqidno:10克隆。扩增的cd16多核苷酸在末端含有kpni位点和noti位点,并通过用这两种酶消化骨架和扩增的cd16并连接而克隆到工程化骨架片段中。pcl20c-v176-cd16质粒的全核苷酸序列显示于seqidno:11中。简而言之,pcl20c-v176-cd16慢病毒原种随后通过用以下量的质粒转染每10cm皮氏培养皿的7x10e6个293t细胞产生:7.5μgpcl20c-v176-cd16、5μgpcmv-δr8.2和2.5μgpcmv-vsv.g。后两种质粒在naldini等,scienceapr.12;272(5259):263-7(1996)和zufferey等,nat.biotechnol.1997sep;15(9):871-5中描述。按照制造商的说明,使用lipofectamine3000(lifetechnologies,目录#l3000-008)进行转染。转染后48小时收集病毒上清液,并使用来自systembiosciences的peg-it病毒沉淀溶液(目录号lv810a-1)浓缩10倍。在transdux(systembiosciences,目录号lv850a-1)存在下,在24孔板的1ml最终培养基中通过旋转培养(840g,35℃下99分钟)用100μl浓缩病毒感染5x10e5个anktm细胞。根据制造商的说明,使用纯化的抗人cd16抗体(biolegend,目录号302002)和来自miltenyi的抗小鼠iggmicrobeads(目录号130-048-401)对表达v176-cd16的细胞进行富集。富集后,通过有限稀释对细胞进行铺板。在补充5%热灭活人ab血清和500iu/mlil-2的x-vivo10培养基中生长15天后,选择单个克隆h2、h7和h20(“h克隆”)以及p74、p82和p110(“p克隆”)。使用与apc-cy7偶联的针对cd16的抗体(biolegend,目录#302018)通过流式细胞术测试细胞的cd16表达。通过流式细胞术监测这些单个克隆在感染后24周生长期期间的cd16表达,且结果见图4。实施例3.hank003细胞的产生hank003通过用含有cd16和il-2两者的序列的基于双顺反子的质粒载体电穿孔anktm细胞而产生。il-2序列用内质网保留信号kdel标记以防止il-2蛋白从内质网(er)分泌,其称为eril-2,具有seqidno:3的氨基酸序列。编码用内质网保留信号标记的il-2的多核苷酸具有seqidno:4的核苷酸序列。转染质粒根据提供的规格由geneartag构建质粒。合成基因pneukv1_fcril2(seqidno:5)由合成的寡核苷酸和pcr产物组装。使用ecori和noti限制性位点将片段克隆到pneukv1_o059载体主链中。pneukv1_o059是合成载体,含有氨苄青霉素抗性盒。用于表达转基因的启动子是具有sv40聚腺苷酸序列的ef-1α。所得质粒长度为5,491个碱基对(bp),且包含cd16和il-2的人源序列。cd16和il-2均无任何转化性质。从转化的细菌纯化质粒dna,并通过uv光谱测定其浓度。通过测序验证最终构建体。所用限制性位点内的序列一致性(sequencecongruence)为100%。质粒在无tse的生产条件下制备。pneukv1_fcril2质粒的全核苷酸序列见seqidno:5。为了产生hank003细胞系,将小瓶的(anktm)mastercellbanktm(mcb)(anktmcoa)和250mgpneukv1_fcril2质粒发送至eufetsgmbh。eufets将mcb瓶解冻,并将细胞培养至足以用质粒转染的数量。在转染后的前两天,转染的细胞在具有il-2、x-vivo10和5%热灭活人ab血清的培养基中生长。两天后,不再向生长介质中添加il-2,并且任何被转染并产生足够量的il-2的细胞继续生长。通过有限稀释分离多个克隆,并初步筛选表型和fc受体表达。表现出良好生存力(>70%)、可接受的倍增时间、预期的表型和阳性fc受体表达的六(6)个克隆被发送至德国红十字会gmp测试实验室(grc)进行更深度的筛选并最终选择单个克隆。在grc处,测试所有克隆的表型(包括fc受体表达)、adcc、细胞因子谱、生长特性和放射敏感性。选定的细胞系hank003用于生成主细胞库。对所选克隆进行的全基因组测序证实,质粒插入位点位于17号染色体上15,654,977-15,661,403位的单一位置处。通过一轮有限稀释选择anktm细胞电穿孔产生的多个克隆。单个克隆用于建立gmp主细胞库hank003。实施例4.评估pma/离子霉素激活后il2依赖性细胞上的cd16表达将如上所述产生的hank003细胞和il2依赖性细胞以及来自三个供体(#5、#7和#8)的nk细胞与40nm的pma和669nm的离子霉素一起孵育1小时。通过将刺激前的细胞和刺激后的细胞与cd16特异性的荧光染料偶联的抗体孵育并通过流式细胞术检测结合的抗体来监测cd16表达。表4总结了表达cd16的细胞的百分比,且图1a(pma刺激前)和图1b(pma刺激后)中显示了代表性的图形表示。表4.pma/离子霉素激活后cd16的表达结果表明,pma/离子霉素处理导致供体nk细胞中cd16表达90%±0.06的下调,而该处理在hank003细胞和hank-lite细胞中仅导致25.5%±0.04的下调,即cd16下调比供体nk细胞低三倍。实施例5.评估与靶细胞孵育后il2依赖性细胞上的cd16表达从researchbloodcomponentsllc(boston,ma)获得来自外周血的供体nk细胞。ms柱(目录号130-042-201)和cd56微珠(目录号130-050-401)从miltenyibiotec(sandiego,ca)获得。如上所述产生hank003细胞和il2依赖性细胞。供体nk细胞、hank003细胞和il2依赖性细胞与k562细胞(美国典型培养物保藏中心(“atcc”),manassas,va)在正常共培养条件(即补充5%人ab血清的x-vivo10培养基,37℃下在5%二氧化碳培养箱中4小时,效应-靶比率1:1)下培养4小时,以允许对靶细胞的完全细胞毒性杀伤。首先在4小时孵育完成时分析cd16表达,并在使细胞恢复另外20小时后再次分析,即在24小时孵育完成时分析细胞。结果总结于表5中,且代表性图表见图2。表5.通过接触k562细胞激活后cd16的表达结果表明,与k562共培养4小时后,供体nk细胞的cd16表达下降61%±0.09,细胞下降4.9%±2.57。在过夜恢复(24小时共培养)后,供体nk中的cd16下调为约57%,而il2依赖性细胞中的cd16下调仅约1%,即接近原始的cd16水平(图2)。该结果表明,il2依赖性细胞中的cd16表达d与k562细胞共培养后是稳定的。实施例6.评估抗体依赖性细胞介导的细胞毒性(adcc)后il2依赖性细胞上的cd16表达在抗体依赖性细胞介导的细胞毒性(adcc)后,检查了hank003和il2依赖的细胞中的cd16表达水平。通过将细胞与dohh-2(来自atcc的cd20+人淋巴瘤b细胞系)在1μg/ml利妥昔单抗(从biogenidec和genentech获得的cd20指导细胞溶解性单克隆抗体)存在下以效应-靶比率1:0(仅效应细胞)或1:4孵育4小时来进行adcc。然后,首先在4小时孵育结束时和然后在另外20小时孵育结束时,通过流式细胞术测量cd16表达。结果表明,在adcc后(4小时共培养完成时),细胞中的cd16表达下调少于10%。参见图3a,比较cd16+细胞的百分比与不存在靶细胞的组(即e:t=1:0)中cd16+细胞的百分比。图3b显示了在4小时共培养期后和在adcc后的20小时恢复(24小时共培养期)后,anktm、hank003和il2依赖性细胞上的cd16平均荧光强度(mfi)。结果显示,即使在adcc之后,cd16在il2依赖性细胞中仍大量存在,表明细胞中的cd16表达在il2依赖性细胞中是高度稳定的。实施例7.表型分型进行流式细胞术分析以测量各种nk细胞特异性标志物的表面表达,包括il2依赖性克隆的cd3、cd56、cd16、cd337、cd54和nkg2d。结果见表6。表6.nk细胞特异性标志物的表面表达cd3cd56cd16cd337cd54nkg2dank-0.18%97.5%0.36%62.7%96.9%93.5%hank-003-0.01%96.8%96.8%70.9%95.0%88.4%克隆h2-0.13%98.3%89.1%21.9%98.4%83.4%克隆h7-0.34%96.9%86.8%58.9%96.2%96.2%克隆h20-0.51%95.5%91.7%84.5%98.3%97.0%克隆p740.19%90.2%73.6%70.6%92.2%87.4%克隆p820.27%91.8%83.9%79.3%95.3%95.6%克隆p1102.20%90.0%74.3%81.4%84.8%85.6%结果显示,与hank-003细胞一样,il2依赖性克隆显示cd56、cd54和nkg2d的阳性表达,这与anktm细胞的表达基本相似。所有il2依赖性克隆表达显著水平的cd16。除克隆h2外,所有克隆均显示显著水平的cd337表达。实施例8.生长特性anktm细胞、hank003细胞、il2依赖性细胞的p和h克隆在补充5%热灭活人ab血清和500iu/mlil-2的x-vivo10培养基中生长。细胞以10e5细胞/ml接种,并在第3、5和7天通过台盼蓝排除法测量细胞数量。倍增时间基于每组四次实验的平均值确定,且结果见下表7。表7.生长特性倍增时间(小时)ank34.8±3.9hank00337.5±4.6克隆h234.4±3.9克隆h729.2±0.6克隆h2035.8±1.4克隆p7433.4±4.6克隆p8236.5±3.5克隆p11037.6±5.2结果显示,il2依赖性克隆与hank-003细胞或anktm细胞相比具有基本相似的生长速率(例如克隆h2、h20、p74、p82和p110)或更快的生长速率(例如克隆h7)。实施例9.直接细胞毒性k562细胞在补充10%热灭活fbs(gibco/thermofisher)的rpmi-1640培养基(gibco/thermofisher)中生长。k562细胞和效应细胞,hank-003细胞或hanklite细胞,在96孔平板(falconbd,franklinlakes,nj)中以不同的效应-靶比率组合,短暂离心,并在补充5%人ab血清的x-vivo10培养基中于37℃下在5%二氧化碳培养箱中孵育4小时。孵育后,细胞在1%bsa/pbs缓冲液中用碘化丙锭(pi,sigma-aldrich)以5g/ml进行染色,并立即通过流式细胞术进行分析。样品在10流式细胞仪(miltenyibiotec)上进行处理,并使用flowjo软件分析数据。死亡的靶细胞,即k562细胞,被鉴定为pkh67-gl和pi双重阳性的。靶细胞和效应细胞也分别用pi染色以评估自发细胞裂解。死亡细胞的百分比通过pkh67+靶细胞群体中pi+的百分比确定。%杀伤计算如下=[样品中的%死亡靶细胞-%自发死亡靶细胞]/[100-%自发死亡靶细胞]。图5a(p克隆)和图5b(h克隆)显示了被il2依赖性克隆裂解的k562细胞的百分比。结果表明,当il2依赖性细胞与靶细胞以相同的效应-靶比率一起孵育时,其表现出与anktm细胞基本相似或更高的细胞毒性。在一些情况下,这些il2依赖性克隆表现出比il2依赖性细胞更高的细胞毒性。实施例10.adcc根据实施例9中所述的方法分析了il2依赖性细胞对skbr-3细胞(atcc,manassas,va)的抗体依赖性细胞介导的细胞毒性(adcc),除了在与效应细胞共孵育前,将染色的靶细胞与不同浓度(0.001-1微克/毫升)的单克隆抗体,赫赛汀或同种型对照抗体("igg")预孵育的额外步骤。adcc计算如下=[在mab存在下e+t反应中的%杀伤-在mab不存在下e+t反应中的%杀伤]/[100-在mab不存在下e+t反应中的%杀伤],(e=效应细胞,t=靶细胞)。skbr-3细胞在与效应细胞混合前,在补充10%热灭活fbs(gibco/thermofisher)的rpmi-1640培养基(gibco/thermofisher)中生长。如图6a和图6b中所示,il2依赖性克隆表现出高的adcc活性,并且在一些情况下高于hank-003细胞。例如,当赫赛汀以100ng/ml存在时,h7克隆的adcc活性比hank-003细胞高40%。说明性序列seqidno:1高亲和力变体免疫球蛋白gammafc区受体iii-a氨基酸序列(全长形式)。176位的val加下划线。序列开头的加下划线部分代表信号肽。seqidno:2高亲和力变体免疫球蛋白gammafc区受体iii-a核酸序列(全长形式)。seqidno:3eril-2(er保留信号加下划线)氨基酸序列seqidno:4eril-2核酸序列seqidno:5pneukv1_fcril2质粒seqidno:6pcl20c-mp-cd19car-ires-gfp质粒seqidno:7用于向pcl20mcs骨架添加另外的ecori、sphi和noti限制性位点的寡核苷酸的顶链。5’cgtaactaccgtgaattcatctacaagcatgcattgtagtagcggccgcatcgatgccgtataccgtac3’seqidno:8用于向pcl20mcs骨架添加另外的ecori、sphi和noti限制性位点的寡核苷酸的底链。5’ggtatacggcatcgatgcggccgctactacaatgcatgcttgtagatgaattcacggtagttacggtac3’seqidno:9用于克隆cd16的正向引物5’acttcaggtaccggtgccaccatgtggcagctgctgctg3’seqidno:10用于克隆cd16的反向引物5’taggttgcggccgctcacttgtcctgggggtccttc3’seqidno:11pcl20c-v176-cd16质粒的核苷酸序列权利要求书(按照条约第19条的修改)1.一种表达cd16(seqidno:1)的修饰的nk-细胞群体,其中所述修饰的nk-细胞不表达il-2,并且其中所述群体包含一个或多个所述修饰的nk-细胞,其中与激活前所述细胞上的cd16表达水平相比,当所述细胞被激活时所述cd16表达水平降低不超过20%。2.根据权利要求1所述的修饰的nk-细胞群体,其中所述修饰的nk-细胞包含cd16的核酸(seqidno:2)。3.根据权利要求1所述的修饰的nk-细胞群体,其中所述修饰的nk-细胞具有抗体依赖性细胞介导的细胞毒性(adcc)。4.根据权利要求1所述的修饰的nk-细胞群体,其中所述nk-细胞群体在激活后未表现出cd16表达的降低或cd16表达降低不超过20%,并且其中所述修饰的nk-细胞在激活开始后保持细胞毒性稳态至少5小时。5.根据权利要求1-3中任一项所述的修饰的nk-细胞群体,其中所述细胞比来自供体的nk细胞表达更高水平的cd16。6.所述修饰的nk-细胞群体,其中与激活前的所述细胞相比,在所述细胞激活后对cd16阳性的细胞的百分比降低不超过20%。7.根据权利要求1所述的修饰的nk-细胞群体,其中所述cd16表达通过流式细胞术测量。8.根据权利要求1所述的群体,其中所述激活为pha刺激、通过与k562细胞共孵育的先天途径激活或通过与利妥昔单抗和dohh共孵育的adcc激活。9.根据权利要求1所述的群体,其中所述细胞通过选自pma、离子霉素和lps的一种或多种化合物激活。10.根据权利要求1所述的修饰的nk-细胞群体,其中所述细胞通过接触靶肿瘤细胞被被激活。11.根据权利要求10所述的修饰的nk-细胞群体,其中所述靶肿瘤细胞选自k562细胞和skbr-3细胞。12.根据权利要求10所述的修饰的nk-细胞群体,其中与所述激活前的所述修饰的nk-细胞相比,所述cd16表达降低不超过10%,或其中。13.根据权利要求10所述的修饰的nk-细胞群体,其中与所述激活前的所述修饰的nk-细胞相比,所述cd16表达降低不超过5%。14.根据权利要求10所述的修饰的nk-细胞群体,其中与接触所述靶细胞之前的所述细胞相比,在所述细胞接触所述靶细胞后对cd16阳性的细胞的百分比降低不超过10%。15.根据权利要求1所述的修饰的nk-细胞群体,其中所述nk-细胞通过接触抗体和靶细胞而被激活,其中所述孵育导致adcc。16.根据权利要求15所述的修饰的nk-细胞群体,其中所述抗体为抗cd20抗体,且所述靶细胞为dohh-2细胞。17.根据权利要求15所述的修饰的nk-细胞群体,其中所述抗体为抗her2抗体,且所述靶细胞为skbr3细胞。18.根据权利要求15所述的修饰的nk-细胞群体,其中所述效应-靶比率为1:1至1:10。19.根据权利要求1所述的修饰的nk-细胞群体,其中所述修饰的nk-细胞另外表达嵌合抗原受体。20.根据权利要求1-3和5-19中任一项所述的修饰的nk-细胞群体,其中当所述效应-靶比率为5:1时,所述修饰的nk-细胞具有至少60%的直接细胞毒性。21.根据权利要求1-3和5-19中任一项所述的修饰的nk-细胞群体,其中所述修饰的nk-细胞具有至少40%的adcc活性。22.一种产生能够在激活过程中保持cd16表达的修饰的nk-细胞群体的方法,其中该方法包括将cd16(seqidno:2)而非il-2引入nk-细胞中,其中在所述激活的修饰的nk-细胞上的cd16表达不低于所述激活前所述修饰的nk-细胞上的cd16表达的50%。23.根据权利要求22所述的方法,其中所述cd16的引入是通过慢病毒感染。24.一种包括权利要求1-3和5-21中任一项的细胞群体的试剂盒。25.根据权利要求24所述的试剂盒,其中所述试剂盒进一步包括抗体。26.一种药物组合物,其包含权利要求1-3和5-21中任一项的细胞群体和药学上可接受的赋形剂。27.一种治疗受试者的方法,包括向所述受试者施用权利要求26的药物组合物。28.根据权利要求1所述的修饰的nk-细胞群体,其中所述修饰的nk-细胞进一步表达自杀基因。29.根据权利要求28所述的修饰的nk-细胞群体,其中所述自杀基因选自胸苷激酶(tk)基因、胞嘧啶脱氨酶、细胞色素p450和icas9。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1