针对CLL-1的单结构域抗体的制作方法
针对cll
‑
1的单结构域抗体
1.相关申请的交叉引用
2.本技术要求保护2018年11月30日提交的美国临时申请第62/774,025号和2018年12月14日提交的美国临时申请第62/780,092号的权益,这两个申请的内容通过引用整体并入本文。
背景技术:
3.c型凝集素样分子1(cll
‑
1,也称为micl,和clec12a)在急性髓系白血病(aml)细胞上和在癌症干细胞(csc)上表达,所述癌症干细胞是可以产生额外癌细胞的细胞。aml仍然是主要的治疗挑战和血液肿瘤学中未满足的需求。aml是导致未成熟髓系胚细胞在骨髓和外周血中不可控地积累的疾病,并且所述疾病具有多种亚型,其导致了开发涵盖性靶向疗法的挑战。尽管对所述疾病的分子遗传学的了解越来越多,但批准用于aml的新型疗法相对较少。因此,仍然需要用于aml的新型治疗剂,诸如靶向cll
‑
1的治疗剂。
技术实现要素:
4.在一个方面,本公开尤其提供结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段、可用于结合cll
‑
1的组合物和用于治疗疾病的方法,所述方法包括施用此类抗体或其抗原结合片段。在一些实施方案中,本公开提供一种包含本文所述的vhh的抗体或其抗原结合片段。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列或其片段。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seqid no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。在一些实施方案中,本公开提供一种结合
(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的任一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh包含seq id no:3
‑
25中的任一个中所绘的至少一个cdr(例如,cdr1、cdr2和/或cdr3)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh包含与seq id no:3
‑
25中的任一个中所绘的cdr(例如,cdr1、cdr2和/或cdr3)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的至少一个cdr。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh包含表1a和/或表1b中所绘的组1
‑
13中的任一组的cdr1、cdr2和/或cdr3。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh包含表1a和/或表1b中所绘的组1
‑
13中的任一组的(i)cdr1和cdr2;(ii)cdr2和cdr3;(iii)cdr1和cdr3;或(iv)cdr1、cdr2和cdr3。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体或其抗原结合片段,其包含vhh或由vhh组成,所述vhh包含表1a和/或表1b中所绘的组1的cdr1、cdr2和cdr3;组2的cdr1、cdr2和cdr3;组3的cdr1、cdr2和cdr3;组4的cdr1、cdr2和cdr3;组5的cdr1、cdr2和cdr3;组6的cdr1、cdr2和cdr3;组7的cdr1、cdr2和cdr3;组8的cdr1、cdr2和cdr3;组9的cdr1、cdr2和cdr3;组10的cdr1、cdr2和cdr3;组11的cdr1、cdr2和cdr3;组12的cdr1、cdr2和cdr3;或组13的cdr1、cdr2和cdr3。
5.在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如由seq id no:28的最后50、40或30个c
‑
末端氨基酸组成或包含所述c
‑
末端氨基酸的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在
例如由seq id no:28的氨基酸243至275组成或包含所述氨基酸的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如由seq id no:28的氨基酸248至262组成或包含所述氨基酸的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如由seq id no:28的氨基酸251至260组成或包含所述氨基酸的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其结合(例如,选择性结合)cll
‑
1且不与sc02
‑
357抗体(例如,由seq id no:26组成或包含seq id no:26)竞争结合。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其结合(例如,选择性结合)cll
‑
1且与本文所述的抗体或抗原结合片段(例如,包含选自seq id no:3至seq id no:25的序列或由所述序列组成)竞争结合cll
‑
1。
6.在一些实施方案中,本公开提供一种编码本文所述的抗体或其抗原结合片段的核酸序列。在一些实施方案中,本公开提供一种包含编码本文所述的抗体或其抗原结合片段的核酸序列的载体。在一些实施方案中,本公开提供一种包含编码本文所述的抗体或其抗原结合片段的核酸序列的宿主细胞。在一些实施方案中,本公开提供一种包含载体的宿主细胞,所述载体包含编码本文所述的抗体或其抗原结合片段的核酸序列。在一些实施方案中,本公开提供一种产生抗体或其抗原结合片段的方法,其包括在适于表达抗体或其抗原结合片段的条件下培养宿主细胞,例如包含编码本文所述的抗体或其抗原结合片段的核酸的宿主细胞。在一些实施方案中,本公开提供一种治疗cll
‑
1相关疾病或病症的方法,所述方法包括向有需要的受试者施用有效量的本文所述的抗体或其抗原结合片段,例如施用包含有效量的本文所述的抗体或其抗原结合片段的组合物(例如,药物组合物)。
7.本公开的其他特征、目的和优点在以下具体实施方式中是明显的。然而,应当理解,尽管具体实施方式指出了本发明的实施方案,但其仅以举例说明的方式给出,而非限制。根据具体实施方式,在本发明范围内的各种变化和修改对本领域技术人员而言将是明显的。
8.定义
9.一个或一种:冠词“一个”和“一种”在本文中用以指代冠词的语法对象中的一个/种或多于一个/种(即,至少一个/种)。举例而言,“一种要素”意指一种要素或多于一种要素。
10.亲和力:如本文所用,术语“亲和力”是指抗原结合部分(例如,本文所述的单结构域抗体)和抗原靶标(例如,cll
‑
1)之间的结合相互作用的特征并且指示结合相互作用的强度。在一些实施方案中,亲和力的量度表示为解离常数(k
d
)。在一些实施方案中,抗原结合部分对抗原靶标具有高亲和力(例如,k
d
小于约10
‑7m、小于约10
‑8m或小于约10
‑9m)。
11.大约或约:如本文所用,术语“大约”或“约”在应用于一个或多个所关注值时,是指与所述参考值相似的值。在某些实施方案中,除非另有说明或从上下文中另外显而易见,否则术语“大约”或“约”是指落在所述参考值的任一方向(大于或小于)的25%、20%、19%、18%、17%、16%、15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%或更少以内的一系列值(除非这个数字将超过可能值的100%)。
12.抗体:如本文所用,术语“抗体”是指多肽,其包括至少一个免疫球蛋白可变区,例如提供免疫球蛋白可变结构域或免疫球蛋白可变结构域序列的氨基酸序列。例如,抗体可
包括重(h)链可变区(本文缩写为vh)和轻(l)链可变区(本文缩写为vl)。在另一实例中,抗体包括两个重(h)链可变区和两个轻(l)链可变区。术语“抗体”包括抗体的抗原结合结构域或片段(例如,单结构域抗体、单链抗体、fab、f(ab')2、fd、fv、dab片段)以及完整抗体,例如iga、igg、ige、igd、igm型(以及其亚型)的完整免疫球蛋白。免疫球蛋白的轻链可为κ型或λ型。
13.抗原靶标:如本文所用,“抗原靶标”是由本文所述的抗体的抗原结合部分特异性结合的任何分子。在一些实施方案中,抗原靶标为cll
‑
1。
14.恒定区:如本文所用,术语“恒定区”是指对应于或来源于抗体的一个或多个恒定区免疫球蛋白结构域的多肽。恒定区可包括以下免疫球蛋白结构域中的任一个或全部:ch1结构域、铰链区、ch2结构域、ch3结构域(来源于iga、igd、igg、ige或igm)和ch4结构域(来源于ige或igm)。
15.fc区:如本文所用,术语“fc区”是指两个“fc多肽”的二聚体,每个“fc多肽”包含抗体的恒定区,不包括第一恒定区免疫球蛋白结构域。在一些实施方案中,“fc区”包括通过一个或多个二硫键、化学接头或肽接头连接的两个fc多肽。“fc多肽”是指iga、igd和igg的最后两个恒定区免疫球蛋白结构域,和ige和igm的最后三个恒定区免疫球蛋白结构域,并且还可包括这些结构域的柔性铰链n
‑
末端的部分或全部。对于igg,“fc多肽”包含免疫球蛋白结构域c伽马2(cγ2)和c伽马3(cγ3)以及c伽马1(cγ1)和cγ2之间的铰链的下部。尽管fc多肽的边界可以变化,但是人igg重链fc多肽通常被定义为包含在t223或c226或p230处开始到其羧基端的残基,其中编号是根据如kabat等人(1991,nih出版物91
‑
3242,national technical information services,springfield,va)中的eu索引。对于iga,fc多肽包含免疫球蛋白结构域c阿尔法2(cα2)和c阿尔法3(cα3)以及c阿尔法1(cα1)和cα2之间的铰链的下部。fc区可为合成的、重组的或由诸如ivig的天然来源产生。
16.同一性:如本文所用,术语“同一性”是指核酸分子(例如,dna分子和/或rna分子)之间和/或多肽之间的整体相关性。在一些实施方案中,如果核酸或多肽的序列至少25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%或99%相同,则所述核酸或多肽被认为彼此“基本上相同”。计算两个核酸或多肽序列的同一性百分比例如可出于最优比较目的通过比对这两个序列来执行(例如,为了最优比对,可在第一序列和第二序列中的一个或两个中引入缺口并且出于比较目的可忽略非相同的序列)。在某些实施方案中,出于比较目的而比对的序列的长度为参考序列长度的至少30%、至少40%、至少50%、至少60%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%、至少99%或基本上100%。然后比较对应位置处的核苷酸。当第一序列中的位置被与第二序列中的对应位置处相同的残基(例如,核苷酸或氨基酸)占据时,则在此位置处分子是相同的。两个序列之间的同一性百分比随着由序列共享的相同位置的数目而变化,考虑到为了最优比对两个序列而需要引入的缺口的数目和每个缺口的长度。两个序列之间的序列比较和同一性百分比确定可使用数学算法来完成。例如,两个核苷酸序列之间的同一性百分比可使用meyers和miller,1989的算法确定,所述算法已经并入align程序(2.0版)。在一些示例性实施方案中,用align程序进行的核酸序列比较使用pam120权重残基表、缺口长度罚分为12和缺口罚分为4。或者,两个核苷酸序列之间的同一性百分比可使用gcg软件包中的gap程序、使用nwsgapdna.cmp矩阵来确定。
17.免疫球蛋白单可变结构域:如本文所用,术语“免疫球蛋白单可变结构域”或“单可变结构域”意指能够特异性结合抗原的表位而不与额外的可变免疫球蛋白结构域配对的免疫球蛋白可变结构域。免疫球蛋白单可变结构域在本公开的含义中的一个实例是“结构域抗体”,诸如免疫球蛋白单可变结构域vh和vl(vh结构域和vl结构域)。免疫球蛋白单可变结构域的另一实例是来自骆驼科动物的“vhh结构域”(或简称为“vhh”),如本文所述。
18.免疫球蛋白可变结构域:如本文所用,术语“免疫球蛋白可变结构域”或“可变结构域”意指如下免疫球蛋白结构域,其为或包括四个“框架区”(在本领域中和本文中分别称为“框架区1”或“fr1”;称为“框架区2”或“fr2”;称为“框架区3”或“fr3”;和称为“框架区4”或“fr4”);所述构架区被三个“互补决定区”或“cdr”(在本领域中和本文中分别称为“互补决定区1”或“cdr1”;称为“互补决定区2”或“cdr2”;和称为“互补决定区3”或“cdr3”)中断。在一些实施方案中,免疫球蛋白可变结构域的一般结构或序列可表示如下:fr1
‑
cdr1
‑
fr2
‑
cdr2
‑
fr3
‑
cdr3
‑
fr4。
19.k
a
:如本文所用,“k
a”是指特定抗原结合部分与抗原靶标形成抗原结合部分/抗原靶标复合物的缔合速率。
20.k
d
:如本文所用,“k
d”是指特定抗原结合部分/抗原靶标复合物的解离速率。
21.k
d
:如本文所用,“k
d”是指解离常数,其由k
d
与k
a
的比率(即,k
d
/k
a
)获得并且表示为摩尔浓度(m)。k
d
值可使用本领域中已经充分证实的方法,例如通过使用表面等离子体共振,或使用诸如系统的生物传感器系统确定。
22.选择性结合:如本文所用,就抗原结合部分和抗原靶标而言,“选择性结合”、“选择性地结合”、“特异性结合”或“特异性地结合”是指抗原结合部分优先与抗原靶标缔合,而不与不是抗原靶标的实体缔合。在抗原结合部分与非靶标之间可能发生一定程度的非特异性结合。在一些实施方案中,如果抗原结合部分和抗原靶标之间的结合与抗原结合部分和非靶标的结合相比大2倍、大5倍、大10倍或大100倍,则所述抗原结合部分选择性地结合所述抗原靶标。在一些实施方案中,如果结合亲和力小于约10
‑5m、小于约10
‑6m、小于约10
‑7m、小于约10
‑8m或小于约10
‑9m,则抗原结合部分选择性地结合抗原靶标。
23.受试者:如本文所用,术语“受试者”意指期望对其进行诊断、预后或治疗的任何受试者。例如,受试者可为哺乳动物,例如,人或非人灵长类动物(诸如猿、猴、猩猩或黑猩猩)、犬、猫、豚鼠、兔、大鼠、小鼠、马、牛或奶牛。
24.治疗有效量:如本文所用,术语“治疗有效量”是指以适于任何医学治疗的合理的效益/风险比赋予所治疗的受试者治疗效果的本文所述的抗体或组合物的量。治疗效果可为客观性的(即,可由一些试验或标志物测量)或主观性的(即,受试者给出效果指示或感受到效果)。特定地,“治疗有效量”是指抗体或组合物诸如通过改善与疾病相关的症状,预防或延迟疾病的发作,和/或还减轻疾病症状的严重性或频率有效治疗、改善或预防特定疾病或病况,或表现出可检测的治疗或预防效果的量。治疗有效量可以可包含多个单位剂量的给药方案来施用。对于任何特定的抗体或组合物,治疗有效量(和/或有效给药方案内的适当单位剂量)可例如取决于施用途径、与其他药剂的组合而变化。此外,对于任何特定受试者的具体治疗有效量(和/或单位剂量)可取决于多种因素,所述因素包括所治疗的病症和病症的严重性;所用的具体药剂的活性;所用的具体组合物;受试者的年龄、体重、一般健康状况、性别和饮食;所用的具体治疗分子的施用时间、施用途径和/或排泄或代谢的速率;治
疗的持续时间;以及医学领域众所周知的类似因素。
25.治疗:如本文所用,术语“治疗(treatment)”(还有“治疗(treat)”或“治疗(treating)”)是指部分或完全地缓解、改善、减轻、抑制特定疾病、病症和/或病况的一种或多种症状或特征、延迟其发作、降低其严重性和/或降低其发生率的本文所述的抗体或组合物的任何施用。这种治疗可用于未表现出相关疾病、病症和/或病况的征兆的受试者,和/或仅表现出疾病、病症和/或病况的早期征兆的受试者。或者或另外,这种治疗可用于表现出相关疾病、病症和/或病况的一种或多种已确立征兆的受试者。
附图说明
26.图1示出某些vhh克隆与clec12a的结合。
27.图2a至图2c示出u937细胞通过某些vhh克隆结合。
28.图3a至图3c示出某些vhh克隆的ec50的确定。
29.图4a和图4b示出u937细胞通过某些vhh克隆结合。
30.图5a至图5d示出u937细胞通过某些vhh克隆结合。
31.图6a至图6c示出u937细胞通过某些vhh克隆结合。
32.图7a至图7d示出在某些vhh克隆之间不同或相似表位的确定。
33.图8证实vhh克隆1h1结合clec12a的线性表位。
34.图9证实抗clec12a scfv和某些vhh克隆之间的表位差异。
35.图10a和图10b证实vhh克隆2h3识别重组clec12a蛋白的能力。
36.图11a和图11b证实质谱鉴定的抗clec12a scfv和vhh克隆2h3的表位(注意:图中的氨基酸编号仅基于胞外结构域氨基酸(即,全长序列的200个氨基酸65
‑
25)。
37.图12示出vhh克隆2h3特异性结合clec12a。
具体实施方式
38.本公开部分地基于选择性结合cll
‑
1/clec12a的单结构域抗体的发现。本公开还涉及编码所述抗体或其抗原结合片段的核酸、包含此类核酸的细胞及使用方法。
39.单结构域抗体
40.单结构域抗体是其互补决定区是单结构域多肽的一部分的抗体。实例包括但不限于重链抗体、天然缺乏轻链的抗体、来源于常规4
‑
链抗体的单结构域抗体、工程化抗体和除来源于抗体的那些外的单结构域支架。单结构域抗体可为本领域已知的任何单结构域抗体或任何未来的单结构域抗体。单结构域抗体可来源于任何物种,包括但不限于小鼠、人、骆驼、美洲驼、山羊、兔、牛。根据本公开的一个方面,如本文所用的单结构域抗体是天然存在的单结构域抗体,称为缺乏轻链的重链抗体。此类单结构域抗体公开在例如wo 94/04678中。来源于天然缺乏轻链的重链抗体的此类可变结构域在本文中称为“vhh”或“纳米抗体”。
41.这样的vhh可来源于在骆驼科物种中,例如在骆驼、单峰骆驼、美洲驼、骆马、羊驼和原驼中产生的抗体。除骆驼科之外的其他物种可产生天然缺乏轻链的重链抗体;此类vhh在本公开的范围内。来自骆驼科动物的vhh结构域的氨基酸残基根据kabat等人,“sequence of proteins of immunological interest”,us public health services,nih(bethesda,md),出版号91
‑
3242(1991);还参见riechmann等人,j.immunol.methods 231:
25
‑
38(1999)给出的vh结构域的通用编号进行编号。根据此编号,fr1包含在位置1
‑
30的氨基酸残基,cdr1包含在位置31
‑
35的氨基酸残基,fr2包含在位置36
‑
49的氨基酸,cdr2包含在位置50
‑
65的氨基酸残基,fr3包含在位置66
‑
94的氨基酸残基,cdr3包含在位置95
‑
102的氨基酸残基,且fr4包含在位置103
‑
113的氨基酸残基。
42.然而,应注意(如本领域对于vh结构域和vhh结构域所众所周知的),cdr中的每一个中的氨基酸残基的总数目可变化,并且可不对应于由kabat编号指示的氨基酸残基的总数目(即,根据kabat编号的一个或多个位置在实际序列中可能未被占据,或实际序列可含有比kabat编号允许的数目更多的氨基酸残基)。这意味着,通常,根据kabat的编号可对应于或可不对应于实际序列中氨基酸残基的实际编号。
43.本领域中已知用于对vh结构域的氨基酸残基进行编号的替代方法,所述方法也可以类似方式应用于vhh结构域。然而,在本公开、权利要求书和附图中,除非另外指出,否则将遵循根据kabat并应用于如上所述的vhh结构域的编号。
44.在一些实施方案中,本公开提供一种cll
‑
1结合抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列或其片段(例如,其cll
‑
1结合片段)。如本文提供的序列表中所指示,seq id no:3
‑
25中的每一个包括在n
‑
末端的vhh氨基酸,和在c
‑
末端的以下氨基酸:(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少(i)
‑
(v)中的一个或多个(和/或缺少(i)
‑
(v)中的一个或多个的一部分)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas的一个或多个。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部。
45.在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少(i)
‑
(v)中的一个或多个(和/或缺少(i)
‑
(v)中的一个或多个的一部分),并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸(即,除(i)
‑
(v)中包括的氨基酸外)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分),其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸
tsgpggqgaeqkliseedlgahhhhhhgas中的全部,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。
46.在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少(i)
‑
(v)中的一个或多个(和/或缺少(i)
‑
(v)中的一个或多个的一部分)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的每一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部。
47.在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少(i)
‑
(v)中的一个或多个(和/或缺少(i)
‑
(v)中的一个或多个的一部分),并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸(即,除(i)
‑
(v)中包括的氨基酸外)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的任一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的一个或多个,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh具有与seq id no:3
‑
25中的任一个的氨基酸序列的一部分(例如,cll
‑
1结合部分)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的任一个中所绘的c
‑
末端氨基酸tsgpggqgaeqkliseedlgahhhhhhgas中的全部,并且其中所述部分缺少一个或多个(例如,1、2、3、4、5个或更多个)额外的氨基酸。
48.在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含在seq id no:3
‑
25中的任一个中所绘的至少一个cdr(例如,cdr1、cdr2和/或cdr3)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含seq id no:3
‑
25中的任一个中所绘的至少一个cdr(例如,cdr1、cdr2和/或cdr3)的一部分,其中所述部分缺少seq id no:3
‑
25中的任一个中所绘的cdr的1、2、3、4、5个或更多个氨基酸。在一些实施方案中,本公开提供一种结合(例
如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含与seq id no:3
‑
25中的任一个中所绘的cdr(例如,cdr1、cdr2和/或cdr3)至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的至少一个cdr。在一些实施方案中,本公开提供一种结合(例如,选择性地结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含与seq id no:3
‑
25中的任一个中所绘的至少一个cdr(例如,cdr1、cdr2和/或cdr3)的一部分至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,其中所述部分缺少seq id no:3
‑
25中的任一个中所绘的cdr的1、2、3、4、5个或更多个氨基酸。
49.在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含表1a和/或表1b中所绘的组1
‑
13中的任一组的cdr1、cdr2和/或cdr3。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含表1a和/或表1b中所绘的组1
‑
13中的任一组的(i)cdr1和cdr2;(ii)cdr2和cdr3;(iii)cdr1和cdr3;或(iv)cdr1、cdr2和cdr3(例如,其中cdr来自一个特定组,或其中cdr选自两个或更多个不同组)。在一些实施方案中,本公开提供一种结合(例如,选择性结合)cll
‑
1的抗体,其为vhh或包括vhh,所述vhh包含如表1a和/或表1b中所绘的组1的cdr1、cdr2和cdr3;组2的cdr1、cdr2和cdr3;组3的cdr1、cdr2和cdr3;组4的cdr1、cdr2和cdr3;组5的cdr1、cdr2和cdr3;组6的cdr1、cdr2和cdr3;组7的cdr1、cdr2和cdr3;组8的cdr1、cdr2和cdr3;组9的cdr1、cdr2和cdr3;组10的cdr1、cdr2和cdr3;组11的cdr1、cdr2和cdr3;组12的cdr1、cdr2和cdr3;或组13的cdr1、cdr2和cdr3。
50.表1a:
51.组cdr1cdr2cdr31caasgsifaineivaacasdgntydansrgnyy2cvvsgdtrsivaacasdgntydansrgnyy3cvasgsirsivaacasdgntydansrgnyy4caasgftfnsyawvsdinsgggstnatelrgsdyyrgpireyay5caasgltfsnyaainwsggttdaasyrlritvvvtpdeyhy6caasgfafddyawvssiswngggtyvklvdsgwysaydy7cvvsgatsnvnalvaaissggstsaaqdwategyeydy8cvvsgtmfsgkdvatvssdggtdhflwgrhy9cvasgndisgsavavdaprerpfgpslrtfhgrewyrppwfts10caasgsifsinavavvsrfgettnarirgnygsridy11cvvsgnmldlntlvaalgistyardynfes12gsdrsinvitsggttkadtrwggmy13grtidngainwsggatasrrgvdlrrnsyeydy
52.表1b:如基于imgt编号和anarci软件(http://opig.stats.ox.ac.uk/webapps/sabdab
‑
sabpred/anarci.php)鉴定的cdr
53.组cdr1cdr2cdr31gsifaineinlcasdgntdansrgnyy2gdtrsinlcasdgntdansrgnyy
3gsirsinvcasdgntdansrgnyy4gftfnsyainsgggstatelrgsdyyrgpireyay5gltfsnyainwsggttaasyrlritvvvtpdeyhy6gfafddyaiswngggtvklvdsgwysaydy7gatsnvnaissggstaaqdwategyeydy8gtmfsgkdvssdggthflwgrhy9gndisgsavdaprerpgpslrtfhgrewyrppwfts10gsifsinavsrfgetnarirgnygsridy11gnmldlntlgistardynfes12gsdrsinvitsggttkadtrwggmy13grtidngainwsggatasrrgvdlrrnsyeydy
54.在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如在seq id no:28的最后50、40或30个氨基酸中的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如在seq id no:28的氨基酸243至275内的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如在seq id no:28的氨基酸248至262内的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其在例如在seq id no:28的氨基酸251至260内的表位处结合(例如,选择性结合)cll
‑
1。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其结合(例如,选择性结合)cll
‑
1且不与sc02
‑
357竞争结合。在一些实施方案中,本公开提供一种抗体或其抗原结合片段,其结合(例如,选择性结合)cll
‑
1且与本文所述的抗体或抗原结合片段(例如,包含选自seq id no:3至seq id no:25的序列)竞争结合cll
‑
1。
55.如本领域技术人员将理解,任何这样的cdr序列都可容易地例如使用分子生物学技术与本文提供的或本领域中以其他方式已知的任何其他多肽(例如,抗体)序列或结构域组合,所述多肽序列或结构域包括如本文公开的或本领域中以其他方式已知的任何框架区、cdr或恒定结构域或其部分,如可能存在于如本文公开的或本领域中以其他方式已知的任何格式的抗体或结合分子中。
56.抗体或片段可通过本领域已知的用于合成抗体的任何方法(参见,例如harlow等人,antibodies:a laboratory manual,(cold spring harbor laboratory press,第2版,1988);brinkman等人,1995,j.immunol.methods 182:41
‑
50;wo 92/22324;wo 98/46645)产生。嵌合抗体可使用在例如morrison,1985,science 229:1202中描述的方法产生,并且人源化抗体可使用在例如美国专利号6,180,370中描述的方法产生。
57.本文所述的组合物和方法的额外抗体是双特异性抗体和多价抗体,如在例如segal等人,j.immunol.methods 248:1
‑
6(2001);和tutt等人,j.immunol.147:60(1991)中所述。
58.融合蛋白和缀合物
59.在一些实施方案中,本公开提供融合蛋白,其包含(i)一种或多种本文所述的单结构域抗体或其抗原结合片段(例如,一种或多种本文所述的cdr),和(ii)一种或多种额外的多肽。例如,融合蛋白可包含一种或多种本文所述的单结构域抗体和本文所述的恒定区或
fc区。在一些实施方案中,一种或多种本文所述的单结构域抗体或其抗原结合片段(例如,一种或多种本文所述的cdr)可非共价或共价缀合如融合到抗原(例如,细胞治疗剂的抗原靶标,例如car
‑
t细胞或抗体药物缀合物),如在例如wo2017/075537、wo2017/075533、wo2018156802和wo2018156791中所述。
60.在一些实施方案中,本公开提供一种包含一种或多种如本文所述的vhh和一种或多种额外的多肽的融合蛋白。在一些实施方案中,额外的多肽包含额外的抗体或其片段。额外的抗体包括,例如完整的igg、ige和igm、双或多特异性抗体(例如,等)、单链fv、多肽
‑
fc融合物、fab、骆驼状抗体、遮蔽抗体(例如,)、small modular immunopharmaceuticals(小型模块化免疫药物)(“smipstm”)、单链或串联双价抗体vhh(包括但不限于本公开描述的那些)、vhh(包括但不限于本公开描述的那些)、微型抗体、锚蛋白(ankyrin)重复蛋白或锚蛋白(ankyrin)重复蛋白或dart、tcr样抗体、dart、tcr样抗体、dart、tcr样抗体、dart、tcr样抗体、dart、tcr样抗体、微量蛋白(microprotein)、(microprotein)、和示例性的额外抗体列于表4中。在一些实施方案中,额外抗体靶向pd
‑
1、tim
‑
3、lag
‑
3、ido、a2ar、tgfβ、cd47或参与免疫抑制途径的其他蛋白质。
61.表4:
62.63.[0064][0065]
在一些实施方案中,额外的多肽包含肿瘤相关抗原(taa)或肿瘤特异性抗原(tsa)的全部或一部分或由其组成。tsa或taa抗原的非限制性实例包括分化抗原,诸如mart
‑
1/melana(mart
‑
i)、gp100(pmel 17)、酪氨酸酶、trp
‑
1、trp
‑
2,和肿瘤特异性多谱系抗原,诸
如mage
‑
1、mage
‑
3、bage、gage
‑
1、gage
‑
2、p15;过表达的胚胎抗原,诸如cea;过表达的癌基因和突变的肿瘤抑制基因,诸如p53、ras、her
‑
2/neu;由染色体易位产生的独特肿瘤抗原,诸如bcr
‑
abl、e2a
‑
prl、h4
‑
ret、igh
‑
igk、myl
‑
rar;和病毒抗原,诸如艾巴氏病毒抗原ebva和人乳头瘤病毒(hpv)抗原e6和e7。其他肿瘤抗原包括tsp
‑
180、mage
‑
4、mage
‑
5、mage
‑
6、rage、ny
‑
eso、erbb、p185erbb2、p180erbb
‑
3、c
‑
met、nm
‑
23h1、psa、tag
‑
72、ca 19
‑
9、ca 72
‑
4、cam 17.1、numa、k
‑
ras、β连环蛋白(beta
‑
catenin)、cdk4、mum
‑
1、p 15、p 16、43
‑
9f、5t4、791tgp72、甲胎蛋白(alpha
‑
fetoprotein)、β
‑
hcg、bca225、btaa、ca 125、ca 15
‑
3\ca 27.29\bcaa、ca 195、ca 242、ca
‑
50、cam43、cd68\p1、co
‑
029、fgf
‑
5、g250、ga733\epcam、htgp
‑
175、m344、ma
‑
50、mg7
‑
ag、mov18、nb/70k、ny
‑
co
‑
1、rcas1、sdccag16、ta
‑
90\mac
‑
2结合蛋白\亲环素c相关蛋白、taal6、tag72、tlp、muc16、il13rα2、frα、vegfr2、lewis y、fap、epha2、ceacam5、egfr、ca6、ca9、gpnmb、egp1、folr1、内皮受体、steap1、slc44a4、(nectin
‑
4)粘连蛋白
‑
4、ags
‑
16、鸟苷酸环化酶c(guanalylcyclase c)、muc
‑
1、cfc1b、整联蛋白α3链(a3b1的整联蛋白α3链,层粘连蛋白受体链)和tps。
[0066]
在一些实施方案中,额外的多肽包含选自以下的肿瘤抗原的全部或一部分或由其组成:cd19、cd20、cd22、cd30、cd72、cd180、cd171(l1cam)、cd123、cd133、cd138、cd37、cd70、cd79a、cd79b、cd56、cd74、cd166、cd71、cll
‑
1/cleck12a、ror1、磷脂酰肌醇蛋白聚糖3(glypican 3)(gpc3)、间皮素(mesothelin)、cd33/il3ra、c
‑
met、psca、psma、糖脂f77(glycolipid f77)、egfrviii、gd
‑
2、my
‑
eso
‑
1和mage a3。
[0067]
在一些实施方案中,额外的多肽包含选自cd19、cd20、cd21、cd22、cd23、cd24、cd40、cd72、cd180、ror1、bcma、cd79a和cd79b的b细胞特异性标志物的全部或一部分或由其组成(参见,例如lebien等人,blood 112:1570
‑
1580(2008))。
[0068]
在一些实施方案中,本公开提供与治疗部分缀合的抗体,所述治疗部分诸如细胞毒素、生物活性蛋白(例如,一种或多种肽或一种或多种细胞因子)或放射性同位素放射毒素(radioisotoperadiotoxin)。此类缀合物在本文中称为“免疫缀合物”。包括一种或多种细胞毒素的免疫缀合物被称为“免疫毒素”。细胞毒素或细胞毒性剂包括对细胞有害(例如,杀死细胞)的任何剂。实例包括紫杉醇(taxol)、松胞菌素b(cytochalasin b)、短杆菌肽d(gramicidin d)、溴化乙锭、依米丁(emetine)、丝裂霉素、依托泊苷、替诺泊苷、长春新碱、长春碱、秋水仙素、多柔比星、道诺霉素、二羟基炭疽菌素二酮(dihydroxy anthracin dione)、米托蒽醌、光神霉素、放线菌素d、1
‑
脱氢睾酮、糖皮质激素、普鲁卡因、丁卡因、利多卡因、普萘洛尔和嘌呤霉素及其类似物或同系物。
[0069]
可被缀合的治疗剂还包括例如抗代谢物(例如,甲氨蝶呤、6
‑
巯基嘌呤、6
‑
硫代鸟嘌呤、阿糖胞苷、5
‑
氟尿嘧啶达卡巴嗪(decarbazine))、烷化剂(例如,氮芥、塞替派苯丁酸氮芥、美法仑、卡莫司汀(bsnu)和洛莫司汀(ccnu)、环磷酰胺、白消安、二溴甘露糖醇、链脲霉素、丝裂霉素c和顺
‑
二氯二胺合铂(ii)(ddp)顺铂)、蒽环类(例如,道诺霉素(daunorubicin)(以前是正定霉素(daunomycin))和多柔比星)、抗生素(例如,更生霉素(dactinomycin)(以前是放线菌素(actinomycin))、博来霉素、光神霉素和蒽霉素(amc))和抗有丝分裂剂(例如,长春新碱和长春碱)。
[0070]
可与本文所述的抗体缀合的治疗性细胞毒素的其他优选实例包括倍癌霉素(duocarmycin)、卡奇霉素(calicheamicin)、美登素(maytansine)和澳瑞他汀
(auristatin)及其衍生物。
[0071]
细胞毒素可使用本领域可用的接头技术与抗体缀合。已经用于将细胞毒素缀合到抗体的接头类型的实例包括但不限于腙、硫醚、酯、二硫化物和含肽接头。可选择例如对溶酶体区室内的低ph值的切割敏感或对蛋白酶的切割敏感的接头,所述蛋白酶诸如优先在肿瘤组织中表达的蛋白酶,诸如组织蛋白酶(例如,组织蛋白酶b、c、d)。
[0072]
关于细胞毒素类型、用于将治疗剂缀合到抗体的接头和方法的进一步讨论,也参见saito,g.等人,(2003)adv.drug deliv.rev.55:199
‑
215;trail,p.a.等人(2003)cancer immunol.immunother.52:328
‑
337;payne,g.(2003)cancer cell 3:207
‑
212;allen,t.m.(2002)nat.rev.cancer 2:750
‑
763;pastan,i.和kreitman,r.j.(2002)curr.opin.investig.drugs 3:1089
‑
1091;senter,p.d.和springer,c j.(2001)adv.drug deliv.rev.53:247
‑
264。
[0073]
本文所述的抗体还可缀合到放射性同位素以产生细胞毒性放射性药物,也称为放射免疫缀合物。可与抗体缀合用于诊断或治疗的放射性同位素的实例包括但不限于碘
131
、铟
111
、钇
90
和镥
177
。本领域已建立了用于制备放射免疫缀合物的方法。放射免疫缀合物的实例是可商购获得的,包括zevalin
tm
(spectrum pharmaceuticals)和bexxar
tm
(以前由glaxosmithkline销售),并且相似的方法可用于使用本文所述的抗体制备放射免疫缀合物。
[0074]
核苷酸序列
[0075]
本公开包括编码一种或多种本文所述的抗体(例如,本文所述的vhh)或其部分(例如,一种或多种本文所述的cdr)和/或一种或多种本文所述的融合蛋白的核苷酸序列。在各种情况下,此类核苷酸序列可存在于载体中。在各种情况下,此类核苷酸可存在于细胞的基因组中,例如需要治疗的受试者的细胞或用于产生抗体的细胞,例如用于产生抗体的哺乳动物细胞。
[0076]
cll
‑1[0077]
人c型凝集素样分子
‑
1(cll
‑
1),也称为micl或clec12a,是ii型跨膜糖蛋白和参与免疫调节的c型凝集素样受体大家族的成员。cll
‑
1先前已经从髓系源性细胞中得到鉴定。cll
‑
1的胞内结构域含有基于免疫酪氨酸的抑制基序(itim)和yxxm基序。各种细胞上的含itim受体的磷酸化通过募集蛋白质酪氨酸磷酸酶shp
‑
1、shp
‑
2和ship导致激活途径的抑制。yxxm基序具有pi
‑
3激酶13的p85亚基的潜在sh2结构域结合位点,其涉及细胞活化途径,揭示了cll
‑
1作为髓系细胞上的抑制和活化分子的潜在双重作用。事实上,在经转染的和髓系源性细胞系中已经以实验方式证实了cll
‑
1与shp
‑
1和shp
‑
2的关联。
[0078]
cll
‑
1在造血细胞中的表达模式受到限制。其特别是在源自外周血和骨髓的髓系细胞中,以及在大多数aml胚细胞中见到。最近的研究说明cll
‑
1也存在于aml中的cd34+/cd38
‑
区室中的大多数白血病干细胞上,但不存在于正常骨髓和再生骨髓对照中的cd34+/cd38
‑
细胞,其有助于区分正常干细胞和白血病干细胞。(参见,例如zhao等人,haematologica 95:71
‑
78(2010);bakker等人,cancer res.64:8443
‑
8450(2004))。
[0079]
cll
‑
1的核苷酸和蛋白质序列对于许多物种是已知的。例如,人序列可在genbank登录号af247788.1(编码序列示于seq id no:1中)和uniprot登录号q5qgz9(seq id no:2)中见到。对于如seq id no:2所示的人cll
‑
1蛋白,胞外结构域包含大约氨基酸65
‑
265,跨膜
结构域包含大约氨基酸44
‑
64,且胞质结构域包含大约氨基酸1
‑
43。人cll
‑
1的茎结构域跨越氨基酸65
‑
139,且c凝集素结构域跨越氨基酸140
‑
249,两者均参考seq id no:2中所示的序列。普通技术人员将理解可最佳比对cll
‑
1变体(例如,物种同系物、等位基因变体等),例如用于鉴定保守残基和结构域。
[0080]
cll
‑
1相关病症
[0081]
本公开的抗体和/或融合蛋白可用于例如检测和/或治疗cll
‑
1相关病症,即与在标准对照(例如,正常、非疾病、非癌细胞)中的cll
‑
1表达相比cll
‑
1的细胞表面表达升高或降低相关的疾病。cll
‑
1表达通常限于髓系谱系细胞,例如外周血和脾中的树突细胞、粒细胞和单核细胞。在一些情况下,cll
‑
1水平升高与癌症相关,特别是在造血csc(例如,lsc)中,和在骨髓增生性病症中,包括白血病如aml(急性骨髓性或骨髓增生性白血病)、mds(骨髓增生异常综合征)、骨髓纤维化、cmml(慢性骨髓单核细胞白血病)、多发性骨髓瘤、浆细胞瘤和cml(慢性骨髓性或骨髓增生性白血病)。参见,例如morsink等人,blood rev.2018年11月1日.pii:s0268
‑
960x(18)30072
‑
9.doi:10.1016/j.blre.2018.10.003.[epub];bakker等人,cancer res.64:8443
‑
8450(2004);van rhenen等人,blood 110:2659
‑
66(2007);zhao等人,haematologica 95:71
‑
78(2010);van rhenen等人,leukemia21:1700
‑
7(2007);和herrmann等人,haematologica 97:219
‑
26(2012)。
[0082]
通过检测细胞表面标志物表达,可对aml细胞进行表征并将其与其他细胞区分开来。除了cll
‑
1+之外,aml细胞可为cd33+(尽管一些是cd33
‑
)、cd45+和cdw52+。aml胚细胞(包括lsc)通常是cd34+cd38
‑
。hsc和lsc的特征可在于cd34的表达,但前者不表达cll
‑
1。mds细胞的特征可在于cds、cd7、cd13和cd34的表达。cml细胞的特征可在于7
‑
add、cd33、cd34和cd38的表达。
[0083]
骨髓增生异常综合征(mds)包括一组密切相关的血液形成病症,其中骨髓显示出暗示白血病前期过程的定性和定量变化,但具有不一定终止为急性白血病的慢性病程。许多术语,包括白血病前期、难治性贫血、难治性骨髓细胞生成障碍性贫血(refractory dysmyelopoietic anemia)、郁积型(smoldering)或亚急性白血病、骨髓细胞生成障碍综合征(dmps)和骨髓发育不良(myelodysplasia),都用于描述mds。这些病况的特征可在于成熟受损(骨髓细胞生成障碍)和血细胞数量减少的细胞骨髓。dmps的特征可在于存在巨成红血细胞样细胞(megablastoid)、巨核细胞发育异常(megarkaryocyte dysplasia)和异常胚细胞数量增加,反映了粒细胞成熟过程增强。dmps患者通常显示与在急性髓系白血病中见到的那些相似的染色体异常,并且在某些部分的患病患者中发展为急性髓系白血病。
[0084]
慢性骨髓增生性病症是一系列病况,其特征可在于成熟和未成熟的粒细胞、红细胞和血小板的数量增加。慢性骨髓增生性疾病可转变为此组中的其他形式,具有终止于急性髓系白血病的趋势。此组内的特定疾病包括真性红细胞增多症、慢性髓系白血病、原因不明的髓系白血病、原发性血小板增多症和慢性中性粒细胞性白血病。
[0085]
骨髓纤维化的特征可在于骨髓的瘢痕形成,其可导致红细胞和白细胞以及血小板的数量减少。骨髓纤维化瘢痕形成可由白血病引起,但可具有其他原因,诸如血小板增多症或药物副作用。
[0086]
在各种情况下,本文所述的抗体和/或融合蛋白治疗、减轻cll
‑
1相关病症的一种或多种症状或生物标志物,或降低其患病率,降低其频率,或降低其水平或量。具体的症状
和症状的进展在受试者之间不同。因此,在一些实施方案中,将本文所述的抗体和/或融合蛋白施用到有需要的受试者,例如患有cll
‑
1相关病症的受试者。
[0087]
在各种情况下,施用本文所述的抗体和/或融合蛋白导致cll
‑
1相关病症的一种或多种症状或生物标志物的患病率、频率、水平和/或量降低,例如与所述受试者中的先前测量值相比或与参考值相比,一种或多种症状或生物标志物降低至少3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%、45%、50%、60%、70%、80%、90%、95%、99%或100%。
[0088]
在一些实施方案中,如本文所述的抗体和/或融合蛋白的有效剂量可为例如小于1,000mg/剂,例如小于900mg/剂、800mg/剂、700mg/剂、600mg/剂、500mg/剂、550mg/剂、400mg/剂、350mg/剂、300mg/剂、200mg/剂、100mg/剂、50mg/剂、25mg/剂或更少。替代如本文公开的剂量或与如本文公开的剂量组合,如本文所述的抗体和/或融合蛋白可以小于每周一次,例如小于每周、2周、3周、4周、5周、6周、7周、8周,9周、10周、11周、12周、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月或一年一次的频率有效或有用地施用。
[0089]
在一些实施方案中,本文所述的抗体和/或融合蛋白可用于许多诊断和/或治疗应用。例如,如本文所述的抗体的经可检测标记的版本可用于检测样品(例如,生物样品)中cll
‑
1的存在或量的测定。本文所述的抗体和/或融合蛋白可用于研究cll
‑
1活性抑制的体外测定。在一些实施方案中,本文所述的抗体和/或融合蛋白可在设计用于鉴定抑制cll
‑
1或另外可用于治疗cll
‑
1相关病症的额外新型化合物的测定中用作阳性对照。
[0090]
本文所述的抗体和/或融合蛋白可用于监测受试者,例如患有、怀疑患有、有风险发展一种或多种cll
‑
1相关病症或在一种或多种cll
‑
1相关病症的治疗中的受试者。监测可包括确定受试者中,例如受试者的血清中cll
‑
1的量或活性。在一些实施方案中,评估在施用如本文所述的抗体和/或融合蛋白之后至少一(1)小时,例如至少2、4、6、8、12、24或48小时,或至少1天、2天、4天、10天、13天、20天或更多天,或至少1周、2周、4周、10周、13周、20周或更多周进行。受试者可在一个或多个下列时期进行评估:在开始治疗之前;在治疗期间;或在已经施用治疗的一种或多种要素之后。评估可包括评估对进一步治疗的需要,例如评估是否应当改变施用剂量、施用频率或治疗持续时间。其还可包括评估增加或减少选定的治疗方式的需要,例如增加或减少本文所述的cll
‑
1相关病症的任何治疗。
[0091]
测量抗体和cll
‑
1的相互作用
[0092]
本文所述的抗体与cll
‑
1的结合性质可通过本领域已知的方法,例如以下方法之一来测量:biacore分析、酶联免疫吸附测定(elisa)、x
‑
射线晶体学、序列分析和扫描诱变。可使用表面等离子体共振(spr)分析抗体和cll
‑
1的结合相互作用。spr或生物分子相互作用分析(bia)实时检测生物特异性相互作用,而无需对任何相互作用物进行标记。bia芯片的结合表面处质量的变化(指示结合事件)导致表面附近光的折射率的改变。折射率的变化产生可检测的信号,其被测量为生物分子之间的实时反应的指示。使用spr的方法描述于例如美国专利号5,641,640;raether(1988)surface plasmons springer verlag;sjolander和urbaniczky(1991)anal.chem.63:2338
‑
2345;szabo等人,(1995)curr.opin.struct.biol.5:699
‑
705和由biacore international ab(uppsala,sweden)提供的在线资源)中。额外地,还可使用可从sapidyne instruments(boise,id.)得到的(kinetic exclusion assay)测定。
[0093]
来自spr的信息可用于提供抗体与cll
‑
1的结合的平衡解离常数(k
d
)和动力学参数(包括k
on
和k
off
)的准确和定量测量。此类数据可用于比较不同的分子。来自spr的信息也可用于开发结构
‑
活性关系(sar)。可鉴定给定位置处的变体氨基酸,其与例如高亲和力的特定结合参数相关。
[0094]
在某些实施方案中,本文所述的抗体表现出对cll
‑
1结合的高亲和力。在各种实施方案中,如本文所述的抗体对cll
‑
1的kd小于约10
‑4m、10
‑5m、10
‑6m、10
‑7m、10
‑8m、10
‑9m、10
‑
10
m、10
‑
11
m、10
‑
12
m、10
‑
13
m、10
‑
14
m或10
‑
15
m。在某些实施方案中,如本文所述的抗体对cll
‑
1的k
d
在0.001nm和1nm之间,例如0.001nm、0.005nm、0.01nm、0.05nm、0.1nm、0.5nm或1nm。
[0095]
配制和施用
[0096]
本公开包括组合物,例如,药物组合物,其含有与药学上可接受的载剂一起配制的一种或多种本文所述的抗体和/或融合蛋白。本领域中众所周知的制备制剂的方法例如在“remington:the science and practice of pharmacy”(第20版,a.r.gennaro a r.编,2000,lippincott williams&wilkins,philadelphia,pa.)中见到。如本文所用,“药学上可接受的载剂”包括生理上相容的任何和所有溶剂、分散介质、包衣、抗细菌和抗真菌剂、等渗剂和吸收延迟剂等。例如,载剂可适于静脉内、肌肉内、皮下、胃肠外、脊柱或表皮施用(例如,通过注射或输注)。取决于施用途径,抗体可包被在材料中以保护化合物免受酸的作用和其他可能使化合物失活的自然条件的影响。
[0097]
药物组合物可包含药学上可接受的抗氧化剂。药学上可接受的抗氧化剂的实例包括:(1)水溶性抗氧化剂,诸如抗坏血酸、盐酸半胱氨酸、硫酸氢钠、焦亚硫酸钠、亚硫酸钠等;(2)油溶性抗氧化剂,诸如抗坏血酸棕榈酸酯、丁基化羟基苯甲醚(bha)、丁基化羟基甲苯(bht)、卵磷脂、没食子酸丙酯、α
‑
生育酚等;和(3)金属螯合剂,诸如柠檬酸、乙二胺四乙酸(edta)、山梨醇、酒石酸、磷酸等。这些组合物还可含有佐剂,诸如防腐剂、润湿剂、乳化剂和分散剂。
[0098]
通过上文的灭菌方法和通过包含各种抗细菌剂和抗真菌剂,例如对羟基苯甲酸酯、氯丁醇、苯酚山梨酸等,可以确保防止微生物的存在。还可希望将诸如糖、氯化钠等的等渗剂包含在组合物中。另外,可注射药物形式的延长吸收可通过包含诸如单硬脂酸铝和明胶的延迟吸收的剂来实现。
[0099]
药学上可接受的载剂包括无菌水溶液或分散体和用于临时制备无菌可注射溶液或分散体的无菌粉末。用于药学活性物质的此类介质和剂的使用是本领域中是已知的。除非任何常规介质或剂与活性化合物不相容,否则预期将其用于本发明的药物组合物中。补充活性化合物也可掺入组合物中。
[0100]
治疗组合物通常在制造和储存的条件下必须是无菌且稳定的。组合物可配制成溶液、微乳液、脂质体或其他适于高药物浓度的有序结构。载剂可为溶剂或分散介质,所述溶剂或分散介质含有例如水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇等)及其合适的混合物。可例如通过使用诸如卵磷脂的包衣、在分散体的情况下通过保持所需粒度以及通过使用表面活性剂来维持适当的流动性。
[0101]
无菌可注射溶液可通过将所需量的抗体与(根据需要)上文所列成分中的一种或成分的组合掺入适当溶剂中,随后进行灭菌微滤来制备。通常,通过将活性化合物掺入含有碱性分散介质和来自上文所列的所需其他成分的无菌媒介物中来制备分散体。在用于制备
无菌可注射溶液的无菌粉末的情况下,优选的制备方法是真空干燥和冷冻干燥(冻干),所述方法从其先前无菌过滤的溶液产生活性成分加上任何额外所需成分的粉末。
[0102]
可与载剂材料组合以产生单一剂型的抗体和/或融合蛋白的量将取决于被治疗的受试者和特定施用方式而变化。可与载剂材料组合以产生单一剂型的抗体和/或融合蛋白的量通常是产生治疗效果的组合物的量。通常,在百分百之中,此量将在约0.01%至约99%,优选约0.1%至约70%,最优选约1%至约30%的与药学上可接受的载剂组合的抗体的范围内。
[0103]
调整剂量方案以提供最佳的所需反应(例如,治疗反应)。例如,可以施用单个药丸(bolus),可以随时间的推移施用若干分次剂量,或者可以如由治疗情况的急迫性所指示将剂量成比例地减少或增加。为了易于施用和剂量均一性而按剂量单位形式来配制胃肠外组合物是特别有利的。如本文所用的剂量单位形式是指适合以单位剂量用于待治疗的受试者的物理离散单元;各单元含有预定量的抗体,经计算与所需药学载剂联合产生所需治疗效果。剂量单位形式的规格决定于且直接取决于(a)抗体的独特特性和待实现的特定治疗效果和(b)混配用于治疗个体的敏感性的这种抗体的领域中固有的限制。
[0104]
对于本文公开的抗体和/或融合蛋白的施用,剂量范围为约0.0001至100mg/kg受试者体重,且更通常为0.01至5mg/kg受试者体重。例如,剂量可为0.3mg/kg体重、1mg/kg体重、3mg/kg体重、5mg/kg体重、10mg/kg体重或20mg/kg体重或在1mg/kg至20mg/kg的范围内。示例性治疗方案需要每周一次、每两周一次、每三周一次、每四周一次、每月一次、每3个月一次或每3至6个月一次施用,或在开始时以短的施用间隔(诸如,每周一次至每三周一次),然后是延长的间隔(诸如,每月一次至每3至6个月一次)施用。
[0105]
或者,抗体和/或融合蛋白可作为缓释制剂施用,在这种情况下,需要较少频率的施用。剂量和频率取决于抗体和/或融合蛋白在患者中的半衰期而变化。通常,人抗体显示最长的半衰期,随后是人源化抗体、嵌合抗体和非人抗体。施用的剂量和频率可取决于治疗是预防性的还是治疗性的而变化。在预防性应用中,在较长的时间内以相对不频繁的间隔施用相对低的剂量。一些患者在他们的余生继续接受治疗。在治疗性应用中,有时需要相对短间隔的相对高的剂量,直到疾病的进展减少或终止,并且优选直到患者显示疾病症状的部分或完全改善。此后,可对患者施用预防性方案。
[0106]
本公开的药物组合物中的抗体和/或融合蛋白的实际剂量水平可以变化,以便获得对于特定患者、组合物和施用方式有效实现所需治疗反应而对患者无毒的抗体和/或融合蛋白的量。选定的剂量水平将取决于多种药代动力学因素,包括所用的本发明的特定组合物或其酯、盐或酰胺的活性,施用途径,施用时间,所用的特定化合物的排泄速率,治疗持续时间,与所用的特定组合物组合使用的其他药物、化合物和/或材料,所治疗患者的年龄、性别、体重、病情、一般健康状况和先前病史,以及医学领域中众所周知的类似因素。
[0107]
本公开的组合物可使用本领域中已知的多种方法中的一种或多种经由一种或多种施用途径施用。如本领域技术人员所理解,施用途径和/或方式将取决于所需结果而变化。优选的施用途径包括静脉内、肌肉内、皮内、腹膜内、皮下、脊柱或其他胃肠外施用途径,例如通过注射或输注。如本文所用的短语“胃肠外施用”是指除了肠内和局部施用之外的施用方式,通常通过注射进行,并且包括但不限于静脉内、肌肉内、动脉内、鞘内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、脊柱内、硬膜外和胸骨
内注射和输注。
[0108]
或者,组合物可通过非胃肠外途径,诸如局部、表皮或粘膜施用途径,例如经鼻内、口服、阴道、直肠、舌下或局部施用。
[0109]
抗体和/或融合蛋白可用将防止快速释放的载剂制备,诸如控释制剂,包括植入物、透皮贴剂和微囊化递送系统。可使用可生物降解的生物相容性聚合物,诸如乙烯乙酸乙烯酯、聚酸酐、聚乙醇酸、胶原蛋白、聚原酸酯和聚乳酸。许多制备此类制剂的方法已获得专利,或者通常是本领域技术人员众所周知的。参见,例如sustained and controlled release drug delivery systems,j.r.robinson编,marcel dekker,inc.,new york,1978。
[0110]
治疗组合物可用本领域已知的医疗装置施用。例如,在一个优选的实施方案中,本公开的治疗组合物可用无针皮下注射装置施用,所述装置诸如美国专利号5,399,163;5,383,851;5,312,335;5,064,413;4,941,880;4,790,824或4,596,556中公开的装置。可用于本公开的众所周知的植入物和模块的实例包括:美国专利号4,487,603,其公开了用于以受控速率分配药物的可植入微型输注泵;美国专利号4,486,194,其公开了用于通过皮肤施用药物的治疗装置;美国专利号4,447,233,其公开了用于以精确的输注速率递送药物的药物输注泵;美国专利号4,447,224,其公开了用于连续药物递送的可变流量可植入输注设备;美国专利号4,439,196,其公开了具有多室区室的渗透药物递送系统;和美国专利号4,475,196,其公开了渗透药物递送系统。许多其他此类植入物、递送系统和模块是本领域技术人员已知的。
[0111]
在一些实施方案中,可使用例如病毒载体的载体,例如使用已知方法将所述抗体和/或融合蛋白施用到受试者。在一些实施方案中,病毒载体可用于将抗体和/或融合蛋白引入癌细胞(例如,肿瘤细胞)中。引入这样的抗体和/或融合蛋白可增加对受试者的免疫系统和/或一种或多种额外治疗剂的易感性(参见,例如wo2017/075533)。
[0112]
可将编码本文所述的抗体和/或融合蛋白的核酸序列克隆到多种类型的载体中。例如,可将核酸克隆到质粒、噬菌粒、噬菌体衍生物、动物病毒和粘粒中。其他载体可包括表达载体、复制载体、探针产生载体、测序载体和病毒载体。在其他实例中,载体可为泡沫病毒(fv)载体,即一种由泡沫病毒(spumavirus)制备的逆转录病毒载体。病毒载体设计和技术是本领域中众所周知的,如sambrook等人(molecular cloning:a laboratory manual,2001)和其他病毒学和分子生物学手册中所述。
[0113]
已经开发了许多基于病毒的系统用于将基因转移到哺乳动物细胞中。病毒载体的实例包括但不限于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒、慢病毒、痘病毒、单纯疱疹1病毒、疱疹病毒、肿瘤病毒(例如,鼠白血病病毒)等。通常,合适的载体含有在至少一种生物体中有功能的复制起点、启动子序列、方便的限制性内切核酸酶位点和一个或多个可选择标志物(例如,wo 01/96584;wo 01/29058;和美国专利号6,326,193)。慢病毒和逆转录病毒的转导可通过添加聚凝胺(santacruz sc
‑
134220;millipore tr
‑
1003
‑
g;sigma 107689)来增强,聚凝胺是一种阳离子聚合物(也称为海美溴铵(hexamehtrine bromide)),用于增加逆转录病毒转导的效率。
[0114]
逆转录病毒是属于逆转录病毒科的包膜病毒。一旦进入宿主细胞,病毒通过使用病毒逆转录酶将其rna转录成dna进行复制。逆转录病毒dna作为宿主基因组的一部分复制,
并且被称为原病毒(provirus)。可使用本领域已知的技术将选定的基因插入载体并包装在逆转录病毒颗粒中。然后可分离重组病毒并将其体内递送到受试者的细胞。许多逆转录病毒系统是本领域中已知的(参见,例如美国专利号5,994,136、6,165,782和6,428,953)。
[0115]
逆转录病毒包括α逆转录病毒属(例如,禽白血病病毒);β逆转录病毒属(例如,小鼠乳腺肿瘤病毒);δ逆转录病毒属(例如,牛白血病病毒和人t
‑
嗜淋巴细胞病毒);ε逆转录病毒属(例如,大眼梭鲈皮肤肉瘤病毒(walleye dermal sarcoma virus));和慢病毒属。在一些实施方案中,逆转录病毒是慢病毒,即一种逆转录病毒科的病毒属,例如,其特征在于孵育期长。慢病毒在逆转录病毒之中是独特的,能够感染非分裂细胞;它们可将显著量的遗传信息递送到宿主细胞的dna中,因此可用作有效的基因递送载体。在一些实例中,慢病毒可为但不限于人免疫缺陷病毒(hiv
‑
1和hiv
‑
2)、猿猴免疫缺陷病毒(s1v)、猫免疫缺陷病毒(fiv)、马传染性贫血(eia)和绵羊髓鞘脱落病毒(visna virus)。来源于慢病毒的载体提供在体内实现显著水平的基因转移的手段。
[0116]
在一些实施方案中,载体是腺病毒载体。腺病毒是一个含有双链dna的大病毒科。它们复制宿主细胞的dna,同时使用宿主的细胞机器合成病毒rna dna和蛋白质。腺病毒是本领域中已知的,其影响复制细胞和非复制细胞两者,以适应大的转基因,并编码蛋白而不整合到宿主细胞基因组中。
[0117]
在一些实施方案中,使用aavp载体。aavp载体是原核载体
‑
真核载体的杂合体,其是重组腺相关病毒和噬菌体的遗传顺式元件的嵌合体。aavp组合了噬菌体和aav载体系统两者的选定元件,从而提供了一种易于在细菌中产生且几乎没有或没有包装限制的载体,同时允许感染哺乳动物细胞并整合到宿主染色体中。含有许多适当元件的载体是可商购获得的,并且可通过标准方法进一步修饰以包括必要的序列。其中,aavp不需要辅助病毒或反式作用因子。另外,aav对哺乳动物细胞的天然向性被消除,因为没有aav衣壳形成。其他方法和细节在美国专利8,470,528和hajitou a.等人,cell,125:358
‑
398中。
[0118]
在一些实施方案中,使用人乳头瘤(hpv)假病毒。dna质粒可包装到乳头瘤病毒l1和l2衣壳蛋白中以产生可有效递送dna的假病毒粒子(pseudovirion)。包封可保护dna免受核酸酶的影响,并提供具有高稳定性水平的靶向递送。使用hpv假病毒可减轻许多与使用病毒载体相关的安全问题。其他方法和实例在hung,c.等人,plos one,7:7(e40983);2012;美国专利8,394,411;和kines,r.等人,int j of cancer,2015中。
[0119]
在一些实施方案中,使用溶瘤病毒。溶瘤病毒疗法可在癌细胞中选择性地复制病毒,并且随后可在肿瘤内扩散,例如,而不影响正常组织。或者,溶瘤病毒可优先感染和杀死细胞而不引起对正常组织的损伤。溶瘤病毒还可有效地诱导对自身以及对感染的肿瘤细胞的免疫反应。通常,溶瘤病毒分为两类:(i)在癌细胞中天然优先复制并且在人体内非致病性的病毒。示例性的(i)类溶瘤病毒包括自主性细小病毒、粘液瘤病毒(痘病毒)、新城疫病毒(ndv;副粘液病毒)、呼肠孤病毒和塞内加谷(seneca valley)病毒(小核糖核酸病毒)。第二类(ii)包括经遗传操作用作疫苗载体的病毒,包括麻疹病毒(副粘病毒)、脊髓灰质炎病毒(小核糖核酸病毒)和痘苗病毒(痘病毒)。另外,溶瘤病毒可包括在正常细胞中而不是在癌细胞中复制所需的基因中用突变/缺失基因工程化的那些病毒,包括腺病毒、单纯疱疹病毒和水泡性口炎病毒。溶瘤病毒由于其低遗传抗性可能性而可用作病毒转导方法,因为它们可靶向多个途径且以肿瘤选择性方法复制。肿瘤内的病毒剂量可由于原位病毒扩增而随
时间增加(与随时间减少的小分子疗法相比),并且可内建安全特征(即,药物和免疫敏感性)。
[0120]
组合疗法
[0121]
在各种实施方案中,如本文所述的抗体和/或融合蛋白可包括在进一步包括向受试者施用至少一种额外剂的治疗过程中。在各种情况下,与如本文所述的抗体和/或融合蛋白组合施用的额外剂可为阿糖胞苷(胞嘧啶阿拉伯糖苷或ara
‑
c)和/或蒽环类药物,诸如多柔比星、道诺霉素、正定霉素、伊达比星和米托蒽醌;其他化疗药物,诸如羟基脲(hydroxyurea)地西他滨(decitabine)克拉屈滨(cladribine)(2
‑
cda)、氟达拉滨(fludarabine)cda)、氟达拉滨(fludarabine)拓扑替康(topotecan)、依托泊苷(etoposide)(vp
‑
16)、6
‑
硫代鸟嘌呤(6
‑
tg)、皮质类固醇药物如泼尼松或地塞米松甲氨蝶呤(mtx)、6
‑
巯基嘌呤(6
‑
mp)或阿扎胞苷(azacitidine)全反式维甲酸(all
‑
trans
‑
retinoic acid)(atra)、维甲酸(tretinoin)或acid)(atra)、维甲酸(tretinoin)或和三氧化二砷(ato,)。在一些实施方案中,本文所述的融合蛋白(例如,由一种或多种vhh和一种或多种肿瘤抗原组成或包含一种或多种vhh和一种或多种肿瘤抗原的融合蛋白)与结合至这样的一种或多种肿瘤抗原的细胞治疗剂(例如,car
‑
t细胞)或抗体药物缀合物组合施用,如在例如wo2017/075537、wo2017/075533、wo2018156802和wo2018156791中所述。
[0122]
在各种情况下,与如本文所述的抗体和/或融合蛋白组合施用的额外剂可与抗体和/或融合蛋白同时施用,与抗体和/或融合蛋白在同一天施用,或与抗体和/或融合蛋白在同一周施用。在各种情况下,与如本文所述的抗体和/或融合蛋白组合施用的额外剂可与抗体和/或融合蛋白一起在单一制剂中施用。在某些实施方案中,以与如本文所述的抗体和/或融合蛋白的施用在时间上分开的方式施用额外剂,例如,在抗体和/或融合蛋白的施用之前或之后一个或多个小时,在抗体和/或融合蛋白的施用之前或之后一天或多天,在抗体和/或融合蛋白的施用之前或之后一周或多周,或在抗体和/或融合蛋白的施用之前或之后一个月或多个月施用额外剂。在各种实施方案中,一种或多种额外剂的施用频率可与如本文所述的抗体和/或融合蛋白的施用频率相同、相似或不同。
[0123]
当组合物将与第二活性剂组合使用时,组合物可与第二剂共同配制,或者组合物可与第二活性剂制剂分开配制。例如,相应的药物组合物可例如在临施用前混合,且一起施用,或者可例如在相同或不同的时间单独施用。
[0124]
在一些实施方案中,本文所述的抗体和/或融合蛋白与额外剂的组合施用导致病况或其症状的改善,其改善程度大于由单独的抗体(或融合蛋白)或额外剂产生的改善程度。组合效果与每种剂单独的效果之间的差异可为统计学显著差异。在一些实施方案中,组合施用本文所述的抗体和/或融合蛋白与额外剂允许与例如批准用于额外剂的标准给药方案的额外剂给药方案相比,以减少的剂量、减少的剂量数目和/或减少的给药频率施用额外剂。
[0125]
试剂盒
[0126]
本文所述的抗体或其抗原结合片段和/或融合物(例如,包含抗体或抗原结合片段
和/或融合蛋白的药物组合物)可提供在试剂盒中。在一些情况下,所述试剂盒包括(a)含有本文所述的抗体和/或融合蛋白(例如,包含本文所述的抗体和/或融合蛋白的药物组合物)的容器,和任选地(b)信息材料。所述信息材料可为描述性的、指导性的、营销性的或其他涉及本文所述的方法和/或抗体和/或融合蛋白例如用于治疗益处的用途的材料。
[0127]
试剂盒的信息材料在其形式上不受限制。在一些情况下,信息材料可包括关于抗体和/或融合蛋白的生产、抗体和/或融合蛋白的氨基酸、编码抗体和/或融合蛋白的核酸、抗体和/或融合蛋白的分子量、浓度、有效期、批次或生产地点信息等的信息。在其他情况下,信息材料涉及例如以合适的施用量、方式或施用方式(例如,本文所述的剂量、剂型或施用方式)施用抗体和/或融合蛋白的方法。所述方法可为治疗患有cll
‑
1相关病症的受试者的方法。
[0128]
在一些情况下,信息材料,例如说明书,以印刷品,例如印刷文本、图画和/或照片,例如标签或印刷片材提供。信息材料也可以其他格式,诸如盲文、计算机可读材料、视频记录或音频记录提供。在其他情况下,试剂盒的信息材料为联系信息,例如实际地址、电子邮件地址、网站或电话号码,其中试剂盒的使用者可获得关于其中的抗体和/或它们在本文所述的方法中的用途的实质性信息。信息材料也可以任何格式的组合提供。
[0129]
除了本文所述的抗体和/或融合蛋白之外,试剂盒还可包括其他成分,诸如溶剂或缓冲液、稳定剂或防腐剂。试剂盒还可包括其他剂,例如第二剂或第三剂,例如其他治疗剂。所述组分可以例如液体、干燥或冻干形式的任何形式提供。所述组分可为基本上纯的(尽管它们可组合在一起或彼此分开递送)和/或无菌的。当组分以液体溶液提供时,液体溶液可为水溶液,诸如无菌水溶液。当组分以干燥形式提供时,通常通过添加合适的溶剂进行重构。例如无菌水或缓冲液的溶剂可任选地提供在试剂盒中。
[0130]
试剂盒可包括一个或多个用于抗体(和/或融合蛋白)和/或其他剂的容器。在一些情况下,试剂盒含有用于抗体和/或融合蛋白和信息材料的单独容器、分隔物或隔室。例如,抗体和/或融合蛋白可包含在瓶、小瓶或注射器中,而信息材料可包含在塑料套或包装中。在其他情况下,试剂盒的单独元件包含在单个未分开的容器内。例如,抗体和/或融合蛋白可包含在瓶、小瓶或注射器中,所述瓶、小瓶或注射器具有附着于其上的标签形式的信息材料。在一些情况下,试剂盒可包括多个(例如,一包)单独的容器,每个容器含有一个或多个单位剂型(例如,本文所述的剂型)的抗体和/或融合蛋白。容器可包括单位剂量,例如,包括抗体和/或融合蛋白的单位。例如,试剂盒可包括多个注射器、安瓿、箔包装、泡罩包装或医疗装置,例如,各自含有单位剂量。试剂盒的容器可为气密的、防水的(例如,对水分的变化或蒸发是不可渗透的)和/或不透光的。
[0131]
试剂盒可任选地包括适于施用抗体和/或融合蛋白的装置,例如注射器或其他合适的递送装置。可提供预装载有例如以单位剂量的抗体和/或融合蛋白,或者所述装置可为空的,但适于装载。
[0132]
重组基因技术
[0133]
根据本公开,可使用本领域技术内的常规分子生物学、微生物学和重组dna技术。此类技术描述于文献中(参见,例如,sambrook,fritsch&maniatis,molecular cloning:a laboratory manual,第二版(1989)cold spring harbor laboratory press,cold spring harbor,n.y.;dna cloning:a practical approach,第i期和第ii期(d.n.glover编,
1985);oligonucleotide synthesis(m.j.gait编,1984);nucleic acid hybridization(b.d.hames&s.j.higgins编,(1985));transcription and translation(b.d.hames&s.j.higgins编,(1984));animal cell culture(r.i.freshney编,(1986));immobilized cells and enzymes(irl press,(1986));b.perbal,a practical guide to molecular cloning(1984);f.m.ausubel等人(编),current protocols in molecular biology,john wiley&sons,inc.(1994)。
[0134]
基因,诸如编码多肽如本文所述的抗体的核酸的重组表达可包括构建含有编码所述多肽的核酸的表达载体。一旦获得多核苷酸,就可使用本领域已知的技术通过重组dna技术生产用于产生多肽的载体。已知的方法可用于构建含有多肽编码序列和适当转录与翻译控制信号的表达载体。这些方法包括,例如,体外重组dna技术、合成技术和体内遗传重组。
[0135]
表达载体可通过常规技术转移到宿主细胞中,然后转染的细胞可通过常规技术培养以产生多肽。已经开发了许多基于病毒的系统用于将基因转移到哺乳动物细胞中。病毒载体的实例包括但不限于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒、慢病毒、痘病毒、单纯疱疹2病毒、疱疹病毒、肿瘤病毒(例如,鼠白血病病毒、痘苗病毒)等。通常,合适的载体含有在至少一种生物体中有功能的复制起点、启动子序列、方便的限制性内切核酸酶位点和一个或多个可选择标志物(例如,wo 01/96584;wo 01/29058;和美国专利号6,326,193)。例如,可使用慢病毒或逆转录病毒载体转导淋巴细胞(例如,t细胞)。溶瘤病毒载体(例如,腺病毒、痘苗病毒、aav)可用于转导肿瘤细胞(例如,其可分泌本文所述的抗体)。参见,例如wo2017/075533。
[0136]
本文中提到的所有出版物、专利申请、专利和其他参考文献都通过引用整体并入本文。另外,所述材料、方法和实施例仅是说明性的,而并非旨在是限制性的。除非另外定义,否则本文使用的所有技术和科学术语均具有与本发明所属领域的普通技术人员通常所理解相同的含义。虽然在本发明的实践或测试中可使用与本文所述的那些方法和材料相似或等效的方法和材料,但本文描述了合适的方法和材料。
[0137]
实施例
[0138]
以下实施例描述了制备和实施本发明的一些优选方式。然而,应理解,这些实施例仅出于说明性目的且并非意在限制本发明的范围。此外,除非在实施例中的描述是以过去时态呈现,否则文本,如说明书的其余部分,并非意欲暗示实际上执行了实验或实际上获得了数据。
[0139]
实施例1
‑
vhh抗体的评定
[0140]
实施例中所述的克隆具有表2中提到的氨基酸序列。
[0141]
表2:
[0142][0143][0144]
通过elisa筛选约184个sdab样品与涂覆在板上的clec12a(也称为cll
‑
1)的结合。将板用在pbs中的1μg/ml人clec12a(o/n4c)涂覆,然后用5%乳/pbst封闭(2小时,室温);在封闭状态中添加以1:1稀释的细菌表达的sdab(1小时),用pbst洗涤5次,用小鼠抗myc
‑
标签单克隆抗体(mab)检测1小时,然后用山羊抗小鼠igg
‑
hrp检测(1小时),二者均在封闭状态中,在抗体之间用pbst洗涤5次,且使板显色30分钟。每个板包括4个对照/92个样品/板。约32%筛选的sdab为elisa阳性。图1示出某些克隆的结合数据。
[0145]
评定了vhh克隆对u937细胞的结合。简言之,方法包括:在室温下将u937细胞(2.5x10^5)fc阻断(人fc阻断,bd目录号bdb564220)10分钟,然后通过在500g下旋转2分钟用facs缓冲液(pbs+1%bsa+0.1%叠氮化钠)洗涤一次;将在facs缓冲液中的vhh克隆(3μg/ml作为最终浓度)添加到细胞沉淀中且在4℃下孵育30分钟,然后通过在500g下旋转2分钟用facs缓冲液洗涤两次;将抗his
‑
pe(r&d systems,目录号ic050p)添加到细胞中;将混合物在4℃下孵育30分钟且通过在500g下旋转2分钟用facs缓冲液洗涤两次;将在pbs中的1%pfa(多聚甲醛)添加到细胞沉淀中以固定细胞,然后进行facs分析。测试的vhh克隆:1b5:储备液=1.6mg/ml;1h1:储备液=1.9mg/ml;1g6:储备液=1.1mg/ml;2f3:储备液=1.45mg/ml;2f5:储备液=0.5mg/ml;2h3:储备液=2mg/ml。如图2a至图2c中所示,用抗his
‑
pe检测克隆1h1、1g6、2f5和2h3与u937细胞的结合;通过抗his
‑
pe可检测到克隆1b5和2f3与u937细
胞的非常少的结合。
[0146]
vhh克隆对u937细胞的结合使用不同剂量进行评定以确定ec50。简言之,方法包括:将facs缓冲液中的vhh克隆(3ug/ml作为起始浓度/测试,3x连续稀释)添加到fc封闭的u937或293t
‑
cll1细胞(2.5x10^5)中,将混合物在4℃下孵育30分钟,然后通过在500g下旋转2分钟用facs缓冲液稀释两次;将抗his
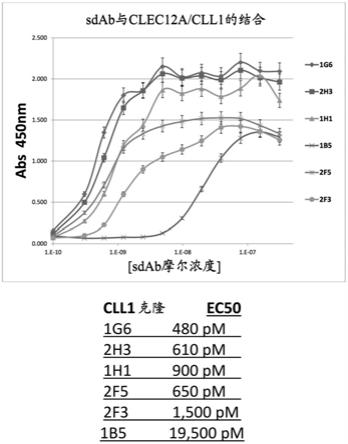
‑
pe添加到细胞中,然后将混合物在4℃下孵育30分钟且通过在500g下旋转2分钟用facs缓冲液洗涤两次;将在pbs中的1%pfa(多聚甲醛)添加到细胞沉淀中以固定细胞,然后进行facs分析。测试的vhh克隆:1b5:储备液=1.6mg/ml;1h1:储备液=1.9mg/ml;1g6:储备液=1.1mg/ml;2f3:储备液=1.45mg/ml;2f5:储备液=0.5mg/ml;2h3:储备液=2mg/ml。如图3a至图3c中所示,u937细胞上的克隆的ec50为:1g6=0.49nm,2f5=0.47nm,2h3=0.35nm和1h1=81nm。
[0147]
评定额外vhh克隆与u937的结合。简言之,将facs缓冲液中的vhh克隆(3μg/ml作为最终浓度/测试)添加到fc封闭的u937细胞(2.5x10^5)中,将混合物在4℃下孵育30分钟,然后通过在500g下旋转2分钟用facs缓冲液稀释两次;将抗cmyc(novus,目录号nbp2
‑
37822)添加到细胞中,将混合物在4℃下孵育30分钟且通过在500g下旋转2分钟用facs缓冲液稀释两次;然后将抗msigg
‑
pe(jackson immunoresearch,目录号115
‑
116—146)添加到细胞中,将混合物在4℃下孵育30分钟且通过在500g下旋转2分钟用facs缓冲液稀释两次,将在pbs中的1%pfa(多聚甲醛)添加到细胞沉淀中以固定细胞,然后进行facs分析。测试的克隆:1a10:储备液=0.9mg/ml;1b1:储备液=0.9mg/ml;1c6:储备液=1.5mg/ml;2c8:储备液=0.9mg/ml;1d2:储备液=0.06mg/ml。作为对照的先前克隆2f5:储备液=0.5mg/ml。如图4a和图4b中所示,通过a
‑
cmyc检测,四个克隆在u937上显示99%的结合。
[0148]
对于克隆与u937细胞的结合筛选另一板。简言之,将10μl的克隆裂解物添加到90μl的在facs缓冲液中的fc封闭的u937(2.5x10^5)中,在4℃下孵育30分钟,通过在500g下旋转2分钟用facs缓冲液稀释两次,将a
‑
cmyc
‑
pe(novus,目录号nb200
‑
108pe,1:200稀释)添加到细胞中,在4℃下孵育30分钟,通过在500g下旋转2分钟用facs缓冲液稀释两次,用在pbs中的1%pfa固定,然后通过流式细胞术分析。如图5a至图5d中所示,从96个裂解物中鉴定出31个抗cll1阳性克隆。
[0149]
对于克隆与u937细胞的结合筛选额外板。简言之,将10μl的克隆裂解物添加到90μl的在facs缓冲液中的fc封闭的u937(2.5x10^5)中,在4℃下孵育30分钟,通过在500g下旋转2分钟用facs缓冲液稀释两次,添加a
‑
cmyc
‑
pe(1:200稀释),在4℃下孵育30分钟,通过在500g下旋转2分钟用facs缓冲液稀释两次,用在pbs中的1%pfa固定,然后通过流式细胞术分析。如图5a至图5d中所示,从第一板中从96个裂解物中鉴定出31个抗cll1阳性克隆。如图6a至图6c中所示,从第二板中从96个裂解物中鉴定出28个抗cll1阳性克隆。
[0150]
结合的总结提供于表3中:
[0151]
表3:
[0152][0153][0154]
使用elisa确定vhh克隆是否识别不同或相似的表位。在4c下用在0.1m碳酸盐缓冲液(ph 9.5,o/n)中的0.1ug/ml可溶的clec12a
‑
his(sino biological#11896
‑
h07h)涂覆96孔板(pierce目录号15041)过夜(o/n)。在室温下将板用在tbs中的0.3%脱脂乳(200ul/孔)封闭1小时。将板用1xtbst(0.1m tris、0.5m nacl和0.05%tween
‑
20)洗涤3次。将测试抗clec12a vhh以10ug/ml水平地添加到整个板上,每孔100ul且孵育1小时。在不洗涤的情况下,将测试抗clec12a生物素化vhh以0.2ug/ml竖直地沿着板添加,每孔100ul,且孵育1小时。在用1xtbst洗涤3次后,以1:2000(100ul/孔)添加hrp缀合的链霉亲和素(pierce#21130),然后在室温下暗处孵育1小时。为了检测,每孔以100ul添加1
‑
step ultra tmb
‑
elisa试剂(thermo fisher#34028)且在450nm处读数。作图结果显示,除了1h1和可能的2c2之外,大多数抗clec12a vhh识别相同的表位。这说明来自1b1、ig6和2f5的vhh识别与来自cdr1不同的克隆(即,1a10和2h3)的vhh相同的表位。ih1 vhh与这些不同,且2c2是中间的。结果描绘在图7a至图7d中。
[0155]
实施例2
‑
表位作图
[0156]
使用下列方法中的一种或多种来定义每种抗体的结合表位。表位是线性的或构象
的。线性表位由序列中不形成3维结构的氨基酸的线性延伸组成。构象表位是需要三级折叠以产生适当结合区的表位。表位作图技术用于鉴定线性表位或构象表位。然而,线性技术不能定位构象表位。线性技术包括肽阵列扫描、扫描诱变、肽文库噬菌体展示和限定线性表位中见到的氨基酸的相关技术。这些线性技术用于定位可结合抗原的非构象部分的抗体的表位,例如,如已知的可结合其构象已被破坏的变性蛋白的抗体。大多数表位是构象的,并且通过使用一种或多种技术来定义,所述技术包括x射线共结晶学;可用展示在噬菌体表面上的大肽进行的构象肽扫描;诱变技术,由此使抗原的具体氨基酸残基突变或改变(通常变成丙氨酸)并检测复合物的存在(通常用荧光,例如在fret测定中);可为自动化的技术,即,当使用计算机以文库格式产生许多质粒克隆以进行数据库的统计学计算时;交联结合质谱法,其中抗体和抗原用质量标记的化学交联剂加标签。使用高质量maldi检测来确认抗体/抗原复合物。一旦产生,抗体/抗原复合物是极其稳定的,并且对复合物应用各种酶和消化条件以提供许多不同的重叠肽。使用高分辨率质谱和ms/ms技术进行这些肽的鉴定。交联肽的鉴定使用与交联试剂连接的质量标签来确定。在ms/ms片段化和使用具体相互作用软件的数据分析后,在同一实验中确定表位和互补位两者。在另一种技术氢氘交换(hdx)中,测量蛋白质结构主链中氢分子的可用性。在分析期间,未结合的抗原和结合的抗体
‑
抗原复合物两者都在氘化水中孵育,以便交换来自蛋白质主链的暴露氨基酸的任何氢。通过比较未结合的抗原与结合的抗体
‑
抗原复合物,确定表位的残基。这些技术中的一种或多种用于鉴定本发明的vhh抗体的线性表位和构象表位。
[0157]
线性表位
[0158]
为了评估是否有任何鉴定的vhh克隆结合clec12a上的线性表位,在sds
‑
page后通过蛋白质印迹(western blot)评估克隆结合变性的clec12a的能力。为了测试vhh克隆对clec12a的识别,在还原条件下在4
‑
12%梯度sds凝胶(invitrogen,np0321)上运行0.5μg的clec12a
‑
his(sino biological,11896
‑
h07h)。印迹法后,使用iblot 2系统(invitrogen,ib23002),将膜在tris缓冲盐水(tbs)中的5%脱脂乳中封闭1小时。接着,将一半印迹与约1ug/ml myc加标签的抗clec12a vhh的蛋白质上清液孵育2小时,然后在洗涤缓冲液(1x tbst:0.1m tris、0.5m nacl、0.05%tween 20)中洗涤3次。然后将印迹与1:2000hrp
‑
抗myc(rockland/fisher,50
‑
105
‑
8097)再孵育1小时且用洗涤缓冲液洗涤3次,然后使用supersignal west femto maximum sensitivity substrate(thermo fisher,34095)展开。将印迹的另一半用1:2000hrp
‑
抗his(biolegend/fisher,652504)以0.1μg/ml直接孵育1小时,且展开作为在印迹上存在clec12a的阳性对照。通过蛋白质印迹发现仅一个克隆,vhh克隆1h1,结合变性的clec12a。结果描绘在图8中。
[0159]
实施例3
‑
vhh克隆识别与先前报道的抗clec12a scfv不同的表位
[0160]
为了进一步阐明由vhh克隆结合的表位,测试了几个vhh克隆与已知抗clec12a scfv竞争结合的能力。将包含美国专利7741443中所述的抗clec12a scfv sc02
‑
357(本文包括为seq id no:26)的融合蛋白固定在塑料板上,然后结合重组clec12a。然后评估三个生物素化vhh克隆,1a10、1b1和2h3,每个来自相同的表位簇,和生物素化clec12a的阴性对照(道1)的结合。这三个克隆中的每一个都能够结合与抗clec12a scfv预结合的clec12a。此结果(图9)证实由抗clec12a scfv识别的表位与由vhh克隆识别的表位不同。
[0161]
实施例4:vhh克隆与clec12a变体的结合
[0162]
vhh克隆识别可商购获得的重组clec12a蛋白的能力通过elisa测试。简言之,在4℃下将96孔板(pierce,15041)用在0.1m碳酸盐,ph9.5中的2.0ug/ml clec12a(sino biological,11896
‑
h07h或abclonal,rp01018)涂覆过夜。在室温(rt)下将板用在tris缓冲盐水(tbs)中的200μl/孔0.3%脱脂乳封闭1小时。然后,用洗涤缓冲液(1x tbst:0.1m tris、0.5m nacl、0.05%tween 20)将板洗涤3次。接着,添加100μl的2h3 vhh
‑
myc
‑
his(seq id no:15,通过prosci纯化),以5μg/ml开始,稀释3倍,且在室温下孵育1小时。将板用洗涤缓冲液洗涤3次且每孔添加100μl的1ug/ml抗myc抗体(novus/fisher,nbp2
‑
37822)。将板在室温下孵育1小时,然后用洗涤缓冲液洗涤3次。在洗涤步骤后,每孔添加100μl的1:2000稀释的hrp
‑
抗migg(jackson immunoresearch,115
‑
035
‑
062)且在室温下暗处孵育1小时。为了检测,每孔添加100μl来自thermo fisher,34028的1
‑
step ultra tmb
‑
elisa,然后在显色时在405nm处读板。重复此实验两次。每个实验的图表使用softmax软件产生,且示于图10a中。
[0163]
在第二elisa中,用如上的clec12a蛋白涂覆板,但不是用2h3 vhh探测,添加2h3 vhh
‑
g4sx4
‑
cd19
‑
his融合蛋白,以5μg/ml开始,稀释3倍。同样,代替抗myc试剂,添加1μg/ml浓度的抗cd19 ab fmc63。洗涤后,如上进行使用hrp抗migg试剂的方案。图表使用softmax软件产生,且示于图10b中。
[0164]
应理解,可商购获得的重组clec12a蛋白具有添加的六组氨酸标签以便于分析。来自sino biological的clec12a在n
‑
末端具有his标签,而来自abclonal的clec12a在c
‑
末端具有his标签。我们发现vhh克隆2h3结合固定的sino biological clec12a,但不结合固定的abclonal clec12a(参见图10a)。含有2h3的vhh簇的表位可能靠近c
‑
末端结合,即添加的c
‑
末端his标签可能干扰结合。应当注意,clec12a是ii型膜蛋白,即c
‑
末端是细胞外的。为了消除clec12a直接结合到塑料的潜在问题(图4a),还使用预先固定在塑料板上的抗clec12a抗体固定来自每个来源的clec12a,这产生相似的结果(图10b)。
[0165]
为了进一步研究所观察的结合差异是否是由c
‑
末端his标签干扰克隆2h3的结合引起的,我们回顾了这两种重组clec12a蛋白的氨基酸序列。我们发现存在两种形式的clec12a,在此区域中具有单个氨基酸差异。规范序列(uniprot;q5qgz9
‑
1)含有赖氨酸(k以粗下划线表示;seq id no:27)。
[0166][0167]
然而,sino biological序列(genbank:eaw96132.1)代之以谷氨酰胺(q以粗下划线表示;seq id no:28)。
[0168][0169]
在评估与其他clec12a序列的结合后,我们发现vhh克隆2h3不结合来自abclonal的clec12a(ncbi参考序列:np_001193939.1,同工型3)或来自genscript的cdna,二者在氨基酸254处都含有赖氨酸残基。这表明k/q氨基酸在2h3表位内或附近,并且与2h3表位接近c
‑
末端一致。相反,scfv与两种蛋白质变体结合。
[0170]
实施例5
‑
基于质谱的表位鉴定
[0171]
为了进一步定义scfv和vhh 2h3的表位,我们使用可商购获得的方法(covalx),其将结合物共价交联到靶标,然后使用质谱确定结合位点。通过将含有非共价相互作用的蛋白质样品与特定开发的交联混合物混合(bich,c等人,anal.chem.,2010,82(1),第172
‑
179页),可以高敏感性特异性地检测非共价复合物。产生的共价结合允许相互作用的物质在样品制备过程和maldi电离中存活。一种特殊的高质量检测系统允许在高质量范围内表征相互作用。图11a示出在2h3和clec12a之间交联的氨基酸,其限定2h3表位的区域。氨基酸251(t);252(y);和260(k)(基于全长clec12a seq id no 28)被鉴定为交联的。表位跨越含有k/q变体的区域,与此区域中电荷的变化完全一致(k对q),如实施例3所示破坏2h3表位。图11b示出sc02
‑
357scfv的表位。同样,其在c
‑
末端附近的存在与所有其他结果一致,即,与2h3不同的表位,而是在clec12a的最后50aa内。
[0172]
实施例6
‑
结合的特异性
[0173]
为了检测与clec12a相关蛋白的结合,确定了具有最高同源性程度的家族成员。clec1a和clec12b在它们的胞外结构域中的同一性最相关,分别为36%和32%。c末端flag加标签的clec12a(ohu09814d)、clec12b(ohu13983b)和clec1a(ohu27138d)的表达质粒购自genscript。使用制造商的方案,每孔(6孔板)使用2μg质粒和10μl lipofectamine 2000(invitrogen,11668019),将它们转染到293t细胞中。48小时后,使用accutase(thermo fisher,00
‑
4555
‑
56)取出细胞,并用pbs洗涤。然后用人fc
‑
block(bd biosciences,564219)封闭细胞10分钟。将fc封闭的293t
‑
clec12a、clec12b或clec1a细胞再悬浮于50μl facs缓冲液(pbs/1%bsa/0.1%叠氮化钠)中,然后将其添加到50μl的在facs缓冲液中连续稀释的2h3vhh
‑
cd19
‑
his融合蛋白(his trap excel(ge healthcare,17
‑
3712纯化的)中,以5μg/ml开始,最终浓度。所用的2h3 vhh的序列是seq id no:15的版本,缺少在seq id 29中公开的c
‑
末端myc和his标签。以3倍阶梯进行连续稀释。将细胞和2h3vhh
‑
cd19融合蛋白在4℃下一起孵育30分钟。将样品在facs缓冲液中洗涤并在4℃以500rcf离心2分钟。重复此洗涤步骤,然后将细胞再悬浮于含有2.5μg/ml pe标记的fmc63(milliporesigma,mab1794h)的facs缓冲液中。在4℃下孵育30分钟后,将细胞如所述洗涤两次,将其再悬浮于
150μl pbs/1%多聚甲醛中以固定细胞。通过每个样品用5μl抗flag
‑
apc试剂(biolegend,637307)染色转染的细胞来验证clec受体的表达。在4℃下30分钟后,如上洗涤并固定样品。通过流式细胞术(bd accuri 6)收集细胞样品数据,并使用bd accuri 6软件分析。确定了仅含有vhh 2h3的融合蛋白与表达clec12a的细胞结合(图12)。
[0174]
其他实施方案
[0175]
虽然本文描述了本发明的许多实施方案,但是可改变本公开和实施例以提供本发明的其他方法和组合物。因此,应当理解,除了通过示例方式表示的具体实施方案外,本发明的范围将由所附权利要求限定。本文引用的所有参考文献都通过引用并入本文。
[0176]
[0177]
[0178][0179]
seq id no:3(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas))
[0180][0181]
seq id no:4(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas))
[0182][0183]
seq id no:5(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas))
[0184][0185]
seq id no:6(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0186][0187]
seq id no:7(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0188][0189]
seq id no:8(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0190][0191]
seq id no:9(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0192][0193]
seq id no:10(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0194][0195]
seq id no:11(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0196][0197]
seq id no:12(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0198][0199]
seq id no:13(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0200][0201]
seq id no:14(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0202][0203]
seq id no:15(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0204][0205]
seq id no:16(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0206][0207]
seq id no:17(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0208][0209]
seq id no:18(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0210][0211]
seq id no:19(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0212][0213]
seq id no:20(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0214][0215]
seq id no:21(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0216][0217]
seq id no:22(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0218][0219]
seq id no:23(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0220][0221]
seq id no:24(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0222][0223]
seq id no:25(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示(i)9个氨基酸的接头(tsgpggqga),(ii)myc
‑
标签(eqkliseedl),(iii)2个氨基酸的接头(ga),(iv)六组氨酸标签(hhhhhh),和(v)额外的3个氨基酸(gas)):
[0224][0225]
seq id no:29(下划线依序表示cdr1、cdr2、cdr3;c
‑
末端粗斜体表示9个氨基酸的接头(tsgpggqga)
[0226]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1