牙髓间充质干细胞在制备克罗恩病治疗药物中的用途的制作方法
本发明涉及生物技术领域,具体涉及牙髓间充质干细胞在制备克罗恩病治疗药物中的用途。
背景技术:
克罗恩病是以慢性肠道炎性病变为主要表现的全身性疾病,其病因尚未明确,可能与免疫功能紊乱有关,可并发穿孔、肠梗阻、出血、局限性腹膜炎、脓肿以及癌变等症状,临床上需要进行外科手术(手术率可达70%~100%)。肛瘘是克罗恩病最常见的一种肛周表现,也是医学领域内难治性疾病,因反复肿痛、破溃流脓,从而严重影响患者的生活质量。为治疗肛瘘,从最初的以治愈为主,逐渐过渡到以保护肛门功能为主,甚至在无法很好保护肛门功能的时候,予以不治疗,即汪建平教授提出的“带瘘生存”。弊端也随之出现:1.患者需要长期垫护垫生活,肛周皮肤长期浸泡在肛瘘分泌物中,出现潮红、瘙痒、坏死等;2.长期的炎变有发展成癌症的可能。为了在保护肛门功能的基础上更好得治愈肛瘘,国内外采用一些手术治疗:肛瘘挂线术、肛瘘切缝引流术、内口皮瓣下移缝合术、肛瘘封堵术(生物胶、生物材料)等。但是治疗肛瘘,不能单纯按照传统的肛门直肠疾病的手术方法来治疗,否则易造成手术的失败,且术后具有较大创面,瘘管迁延分布会使术后创面愈合时间长。
寻找有效的药物和治疗方法是十分必要的,而建立一种可重复性、简单、经济且与临床相接近的动物模型是研发的前提。猴是目前最好的肛瘘模型,但其价格高不便利;牧羊犬的肛肠具有特殊性,与人类存在较大差异;王琛等使用sd大鼠造模,将小条纱布置入其颈背部,造模45天后,将金黄色葡萄球菌和大肠杆菌混合菌液注射到小条纱布内,该造模法比较合适并为国内外学者研究提供实在的大鼠肛瘘模型。以上造瘘的模型均没有完完全全地模拟肛瘘状态,存在一定的人为因素。
技术实现要素:
为了解决现有技术中所存在的问题,本发明的目的在于,提供牙髓间充质干细胞在制备克罗恩病治疗药物中的用途。
本发明是通过以下技术方案实现的:
本发明的的第一方面,提供了牙髓间充质干细胞用于制备克罗恩病治疗药物的用途。
所述牙髓间充质干细胞为现有技术,可通过市购途径获得,也可由本领域技术人员根据具体需要自行制备获得。
一种实施方式中,所述克罗恩病治疗药物至少具有以下功用之一:
1)改善肠溃疡等级评分和肠溃疡面积;
2)降低肛周分泌物、大便出血及大便粘稠度;
3)降低血清中炎性细胞因子tnf-α、il-12、、il-6和il-1β的水平;
4)提高抗炎性细胞因子il-10的水平。
所述克罗恩病治疗药物必然包括牙髓间充质干细胞,并以牙髓间充质干细胞作为前述功用的有效成分。
所述克罗恩病治疗药物中,发挥前述功用的有效成分可仅为牙髓间充质干细胞亦可包含其他可起到类似功用的分子。
亦即,牙髓间充质干细胞为所述克罗恩病治疗药物的唯一有效成分或有效成分之一。
可选的,所述间充质干细胞用于制备克罗恩病导致的肛瘘的治疗药物。
所述克罗恩病治疗药物形式无特殊限制,可以为固体、液体、凝胶、半流质、气雾等各种物质形式。
所述克罗恩病治疗药物主要针对的对象为哺乳动物,如啮齿类动物、灵长类动物等。
本发明的第二方面,提供了一种治疗克罗恩病的方法,为向对象施用牙髓间充质干细胞。
所述的对象可以为哺乳动物。所述哺乳动物优选为啮齿目动物、偶蹄目动物、奇蹄目动物、兔形目动物、灵长目动物等。所述灵长目动物优选为猴、猿或人。
所述对象可以是罹患克罗恩病的患者或者期待治疗的克罗恩病的个体。
所述牙髓间充质干细胞可以在接受克罗恩病治疗前、中、后向对象施用。
一种实施方式中,可采用注射方式向对象施用牙髓间充质干细胞。
一种实施方式中,所述注射方式选自系统注射。
本发明的第三方面,提供一种克罗恩病治疗药物,包括有效剂量的牙髓间充质干细胞。
所述克罗恩病治疗药物必然包括牙髓间充质干细胞,并以牙髓间充质干细胞作为前述功用的有效成分。
所述克罗恩病治疗药物中,发挥前述功用的有效成分可仅为牙髓间充质干细胞亦可包含其他可起到类似功用的分子。
亦即,牙髓间充质干细胞为所述克罗恩病治疗药物的唯一有效成分或有效成分之一。
所述克罗恩病治疗药物形式无特殊限制,可以为固体、液体、凝胶、半流质、气雾等各种物质形式。
所述克罗恩病治疗药物主要针对的对象为哺乳动物,如啮齿类动物、灵长类动物等。
本发明的第四方面,提供一种克罗恩病联合治疗药物组合,包括有效量的牙髓间充质干细胞和至少一种其他克罗恩病治疗药物。
所述联合治疗药物组合可以是以下形式中的任意一种:
一)将牙髓间充质干细胞和其他克罗恩病治疗药物分别制成独立的制剂,制剂的剂型可相同或不同,给药途径亦可相同或不同。
当其他克罗恩病治疗药物为抗体时,一般采用胃肠外给药型。当其他克罗恩病治疗药物为化学药物时,给药形式可以比较丰富,可以是胃肠道给药亦可以是非胃肠道给药。一般推荐针对各化学药物的已知给药途径给药。
二)将牙髓间充质干细胞和其他克罗恩病治疗药物配置成复方制剂,在将牙髓间充质干细胞和其他克罗恩病治疗药物采用相同给药途径给药并同时施加时,可采用将两者配置成复方制剂的形式。
本发明的第五方面,提供了一种治疗克罗恩病的方法,为向对象施用有效量的牙髓间充质干细胞以及向对象施用有效量的其他克罗恩病治疗药物和/或向对象实施其他克罗恩病治疗手段。
可以同步地或顺序地给予有效量的牙髓间充质干细胞和至少一种有效量的其他克罗恩病治疗药物。
基于本发明通过试验研究发现,牙髓间充质干细胞可用于治疗克罗恩病,在与牙髓间充质干细胞以外的其他克罗恩病治疗药物联合用药中,至少可以起到疗效相加的效果,进一步增强对于克罗恩病的治疗作用。
本发明还提供间充质干细胞制备具有如下任一或多种作用的产品的用途:
1)改善肠溃疡等级评分和肠溃疡面积;
2)降低肛周分泌物、大便出血及大便粘稠度;
3)降低血清中炎性细胞因子tnf-α、il-12、、il-6和il-1β的水平;
4)提高抗炎性细胞因子il-10的水平。
所述间充质干细胞选自牙髓间充质干细胞。
与现有技术相比,本发明的有益效果为:
本发明通过试验首次证实了牙髓间充质干细胞系统注射对克罗恩病具有明显的治疗效果,为克罗恩病的治疗提供全新的技术方案和选择。
附图说明
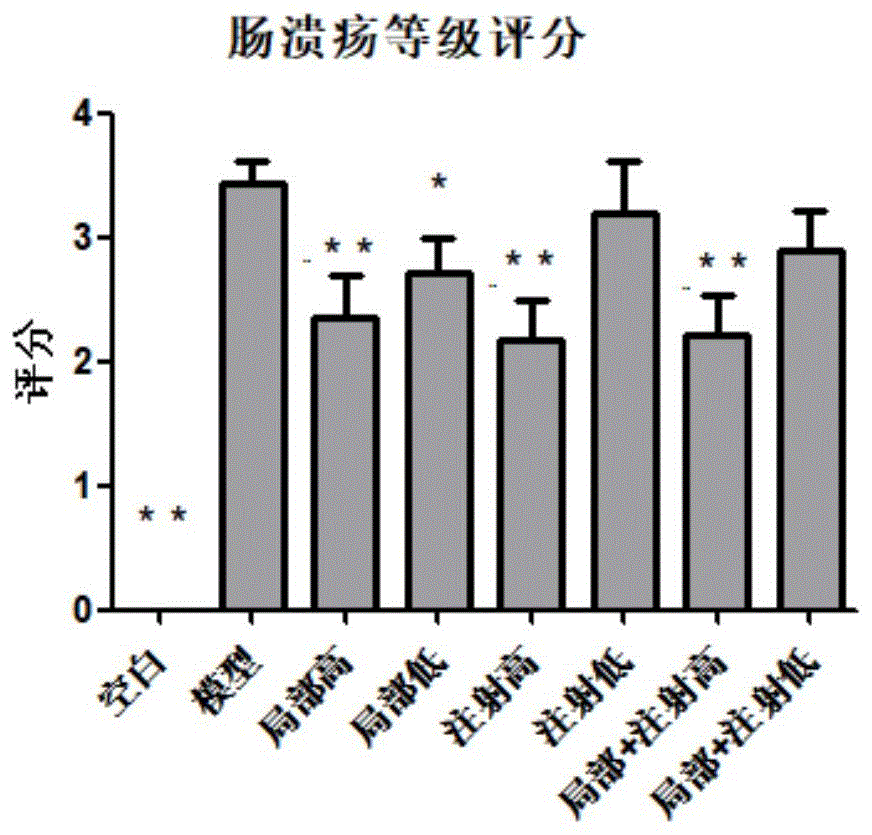
图1:治疗后肛瘘观测指标-肠溃疡等级评分。
图2:治疗后肛瘘观测指标:肠溃疡面积评分。
图3:治疗后肛瘘观测指标:肛周分泌物评分。
图4:治疗后肛瘘观测指标:大便出血等级评分。
图5:治疗后肛瘘观测指标:大便粘稠度等级评分。
图6:治疗前后细胞因子elisa检测结果。
图7:il-1β细胞因子免疫组化检测结果。
图8:il-6细胞因子免疫组化检测结果。
图9:il-10细胞因子免疫组化检测结果。
附图中,*,p<0.05;**,p<0.01;***,p<0.001。
具体实施方式
干细胞是一类具有自我复制的多潜能细胞,间充质干细胞是其中被认为最具有医学价值的干细胞种类。间充质干细胞(mesenchymalstemcells,msc)作为间质起源的非造血干细胞,其存在于多种人体组织,如骨髓(bonemarrow,bm),脐带(umbilicalcord,uc)、脐带血(umbilicalcordblood,ucb)、脂肪组织(adiposetissue,at)、牙髓(dentalpulp、dp)和皮肤。根据不同的组织来源及分离培养方法,msc由一大类特征和功能各异的细胞亚型所组成。msc对于主要组织相容性复合体(majorhistocompatibilitycomplex,mhc)i类分子的表达水平较低,并且不表达mhcii类分子和共刺激因子(cd80、cd86、cd40),因而其免疫原性低,移植排斥风险小。既往研究显示,msc可在多种炎症状态下介导免疫耐受作用。它们通过细胞间的直接接触以及分泌免疫调节分子,影响先天性和获得性免疫细胞(如t细胞、b细胞、dc、自然杀伤细胞)的发生发育和免疫功能。
牙髓组织位于牙齿内部的牙髓腔内,是牙体组织中唯一的软组织。通过对人牙髓细胞的研究,发现了一种与骨髓间充质干细胞有着极其相似的免疫表型及形成矿化结节能力的细胞,细胞中形态呈梭形,可自我更新和多向分化,有着较强的克隆能力。这些由牙髓组织中分离出的成纤维状细胞就称为牙髓干细胞(dentalpulpstemcells,dpscs)。dpscs来源于6-11岁的小孩自然脱落的牙齿和成人需要拔掉的智齿,容易大量获得细胞,易于质量控制,不会带来伦理学问题,并且dpscs具有多分化潜能,免疫原性低。因此,dpscs成为再生医学领域可靠而丰富的细胞来源。
牙髓间充质干细胞用于制备克罗恩病治疗药物
本发明通过试验研究首次证实和发现,牙髓间充质干细胞可用于治疗克罗恩病。因此,牙髓间充质干细胞可用于制备克罗恩病治疗药物。
以牙髓间充质干细胞为主要活性成分或主要活性成分之一制备药物。通常,药物中除了有效成分外,根据不同剂型的需要,还会包括一种或多种药学上可接受的载体或辅料。
“药学上可接受的”是指当分子本体和组合物适当地给予动物或人时,它们不会产生不利的、过敏的或其它不良反应。
“药学上可接受的载体或辅料”应当与牙髓间充质干细胞相容,即能与其共混而不会在通常情况下大幅度降低药物组合物的效果。可作为药学上可接受的载体或辅料的一些物质的具体例子是糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纤维素及其衍生物,如甲基纤维素钠、乙基纤维素和甲基纤维素;西黄蓍胶粉末;麦芽;明胶;滑石;固体润滑剂,如硬脂酸和硬脂酸镁;硫酸钙;植物油,如花生油、棉籽油、芝麻油、橄榄油、玉米油和可可油;多元醇,如丙二醉、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化剂,如tween;润湿剂,如月桂基硫酸钠;着色剂;调味剂;压片剂、稳定剂;抗氧化剂;防腐剂;无热原水;等渗盐溶液;和磷酸盐缓冲液等。这些物质根据需要用于帮助配方的稳定性或有助于提高活性或它的生物有效性或在口服的情况下产生可接受的口感或气味。
本发明中,除非特别说明,药物剂型并无特别限定,可以被制成注射剂、针剂、口服液、片剂、胶囊、滴丸、喷剂等剂型,可通过常规方法进行制备。药物剂型的选择应与给药方式相匹配。
牙髓间充质干细胞联合治疗药物组合和施用方法
所述联合治疗药物组合可以是以下形式中的任意一种:
一)将牙髓间充质干细胞和其他克罗恩病治疗药物分别制成独立的制剂,制剂的剂型可相同或不同,给药途径亦可相同或不同。使用时,可几种药同时使用,也可几种药先后使用。先后给药时,应当在先用药物仍对机体有效的期间内向机体施加其他药物。
二)将牙髓间充质干细胞和其他克罗恩病治疗药物配置成复方制剂,在将牙髓间充质干细胞和其他克罗恩病治疗药物采用相同给药途径给药并同时施加时,可采用将两者配置成复方制剂的形式。
抗体常用的用药方法为静脉注射、静脉滴注或动脉灌注。其用法用量可参考现有技术。
小分子化合物常用的用药方法可以是胃肠道给药或者是胃肠外给药。sirna、shrna、抗体则一般采用胃肠外给药。可以是局部给药亦可以为全身给药。
可以同步地或顺序地给予有效量的牙髓间充质干细胞和至少一种有效量的其他克罗恩病治疗药物。
使用时,可将有效量的牙髓间充质干细胞和有效量的其他克罗恩病治疗药物同时使用,也可将有效量的牙髓间充质干细胞和有效量的其他克罗恩病治疗药物先后使用。先后给药时,应当在先用药物仍对生物体有效的期间内向生物体施加其他药物。
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围;在本发明说明书和权利要求书中,除非文中另外明确指出,单数形式“一个”、“一”和“这个”包括复数形式。
当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本技术领域技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本技术领域的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实现本发明。
除非另外说明,本发明中所公开的实验方法、检测方法、制备方法均采用本技术领域常规的分子生物学、生物化学、染色质结构和分析、分析化学、细胞培养、重组dna技术及相关领域的常规技术。
实施例1
1实验材料与仪器
1.1实验动物
选用健康sd大鼠180只,体重在200-230g之间。
1.2饲养条件
1.2.1实验室内外环境条件:
饲养环境条件标准:中华人民共和国国标gb14925-2010;
饲养环境控制系统:自动控制全新风中央空调系统
温度:20----26℃(日温差≦4℃)
湿度:相对湿度30----70%
光照:人工照明12小时明暗交替
1.2.2饲料:
给料方法:自由摄取(试验有特殊要求时除外)
营养成分检测:由饲料供应商每批提供检测报告
常规营养成分指标:粗蛋白、粗脂肪、粗纤维、粗灰分、水分、钙和磷
1.2.3饮水:
种类:实验动物饮用水(自来水高压灭菌)
供水方法:饮水瓶盛装,自由摄取
1.2.4笼具及垫料:
垫料每周至少更换2次,同时更换饲养盒,遇有异常情况随时更换饲养盒。每3天更换消毒饮水瓶和瓶塞,每两周消毒1次笼架。所有换洗的笼具清洗过后均采用高压灭菌。
1.3分组
180只大鼠分为模型组、高剂量局部给药组(简称局部高)、低剂量局部给药组(简称局部低)、高剂量局部给药+尾静脉注射组(简称局部+注射高)、低剂量局部给药+尾静脉注射组(简称局部+注射低)、高剂量尾静脉注射组(简称注射高)、低剂量尾静脉注射组(简称注射低)和空白组。各组在体重、性别、健康程度等一般资料差异无统计学意义(p>0.05),具有可比性。
2主要实验试剂
试剂厂家
水合氯醛国药
tnbssigma
医用棉签国药
医用酒精杭州欧拓普生物技术有限公司
3主要实验仪器
电子天平、肛瘘探针、曲别针、棉线
4实验方法
4.1牙髓干细胞的剂量选择:由于各实验室对干细胞的培养、扩增技术不同,给予剂量也同。在运输过程中,细胞可能已沉淀在ep管底部形成沉淀物,需要重新悬浮(通过手轻轻敲击)。避免阳光照射。
4.2主要药效学研究
(1)大鼠肛瘘模型
大鼠在麻醉前禁食12小时。腹腔注射10%的水合氯醛(0.3ml/100g体重)麻醉大鼠。术前器具需用75%的酒精擦拭以保持无菌。麻醉完成后,大鼠呈昏睡状态,剪除多余的肛周皮毛使其完全露出肛门,用医用酒精常规消毒大鼠肛门周围的皮肤,并用棉签蘸取适量润滑油使之暴露。造瘘组在截石位第3、9点位置距离肛缘1cm处用曲别针从齿状线以上肛门括约肌由内向外穿出并固定。穿刺结束后将大鼠送回饲养室,观察并监测生命体征直到大鼠苏醒。
(2)tnbs造模及注射干细胞
术后第18天去除曲别针后,初诊触及明显条索状物、硬节或肿块及使用肛瘘探针探测到瘘管表明造模成功。大鼠一侧瘘管挂线后直肠给予tnbs造模。直肠内注射tnbs18小时后,按照表1剂量给予牙髓干细胞治疗肛瘘大鼠。干细胞注射前使用生理盐水清洁瘘管,并去除任何疤痕组织。在非常靠近或贴近瘘管的状态下局部给予干细胞或尾静脉注射给予干细胞。局部注射时将一半剂量注射到瘘管内口周围的组织中,并将一半剂量注入沿瘘管的组织壁中。在瘘管通往肛门附近的皮肤上轻轻按摩20至30秒。
表1大鼠给药剂量(大鼠按220g/只计)
(3)统计观察
每日统计大鼠死亡个数,称量体重,观察并进行疾病活动指数(dai)评分,计算总体生存率、稀便率及体重变化等。
ⅰ.疾病活动指数(dai)评分
①结合患者(患病动物)的体重下降百分率(体重不变为0,1-5为1分,5-10为2分,10-15为3分,大于15为4分)
②大便黏稠度(正常为0,松散的大便为2分,腹泻为4分)
③大便出血(正常0分,隐血阳性为2分,显性出血为4分)三种情况进行综合评分将3项结果的总分除以3即得到dai值。即dai=(体重指数+大便形状+出血情况)/3。
ⅱ.肛周分泌物变化,评分标准如下
①肛门较清洁干燥无明显分泌物,记0分;
②肛门局部潮湿少许分泌物,可浸湿半根消毒棉签,记1分;
③肛门局部湿润中量分泌物,可浸湿1根消毒棉签,记2分;
④肛门局部较湿润大量分泌物,可浸湿1.5根消毒棉签,记3分;
⑤肛门局部超大量分泌物,可浸湿2根及以上消毒棉签,记4分。
(4)给予干细胞治疗5-9天,大鼠麻醉后取血、瘘管周围组织及结直肠,观察结直肠溃疡指标,瘘管组织及结直肠溃疡部位固定包埋后进行切片。溃疡观测指标如下:结直肠长度、重量、溃疡面积、瘘口愈合率及愈合程度评分。
(5)细胞因子检测
酶联免疫吸附测定(elisa)检测各组大鼠血清中炎性细胞因子tnf-α、ifn-γ、il-6、il-1β、il-10、il-12、趋化因子rantes和巨噬细胞炎症蛋白2(mip-2)的浓度。
tnf-αelisa试剂盒:生工生物,d730457-0096
ifn-γelisa试剂盒:生工生物,d730231-0096
il-6elisa试剂盒:生工生物,d730243-0096
il-1βelisa试剂盒:生工生物,d730238-0096
il-10elisa试剂盒:生工生物,d730245-0096
il-12elisa试剂盒:生工生物,d730235-0096
mip-2elisa试剂盒:生工生物,d730273-0096
检测方法参照说明书进行。
(6)he染色、炎症病理组织学评分
通过石蜡切片免疫组化观察瘘管周围组织及结肠组织的炎症及抗炎细胞因子的表达。
4.3统计学分析
运用统计软件spss、进行统计分析处理,以p<0.05为差异具有统计学意义。
5实验结果
5.1体重变化
0.047530635、0.010619326、0.010915819、0.020507733、0.007394868、-0.009765317、0.029264543、0.011007338
5.2溃疡观测指标评分和溃疡面积变化
所有观测指标均经两人重复观察,计分不一致者经再次观察确认。肠溃疡等级评分及肠溃疡面积结果如图1和2所示,表明牙髓间充质干细胞治疗后可显著改善肠溃疡相关指标;局部和静脉注射两种方式均可达到治疗效果,且高剂量组效果显著优于低剂量组(*,p<0.05;**,p<0.01;***,p<0.001)。
5.3治疗后肛瘘观测指标评分
所有观测指标均经两人重复观察,计分不一致者经再次观察确认。结果如图3、图4和图5所示,表明牙髓间充质干细胞治疗后可显著降低肛周分泌物、大便出血及大便粘稠度的评分,局部和静脉注射两种方式均可达到治疗效果(*,p<0.05;**,p<0.01;***,p<0.001)。
5.4治疗前后细胞因子elisa检测
白介素10是一种多细胞源、多功能的细胞因子,调节细胞的生长与分化,参与炎性反应和免疫反应,是目前公认的炎症与免疫抑制因子。
如图6所示,与未治疗大鼠的血清相比,牙髓干细胞治疗大鼠的血清中炎性细胞因子tnf-α、il-12、、il-6和il-1β的水平降低,抗炎性细胞因子il-10的水平升高(*p<0.05;**p<0.01;***p<0.001)。
细胞因子免疫组化检测结果如图7、图8和图9所示,与未治疗模型组相比,干细胞治疗后炎症细胞因子il-1β和il-6水平有显著降低,高剂量治疗组效果优于低剂量治疗组;抗炎因子il-10的水平在干细胞治疗后会明显升高,其作用效果在局部高剂量给药组最为明显。
以上的实施例是为了说明本发明公开的实施方案,并不能理解为对本发明的限制。此外,本文所列出的各种修改以及发明中方法、组合物的变化,在不脱离本发明的范围和精神的前提下对本领域内的技术人员来说是显而易见的。虽然已结合本发明的多种具体优选实施例对本发明进行了具体的描述,但应当理解,本发明不应仅限于这些具体实施例。事实上,各种如上所述的对本领域内的技术人员来说显而易见的修改来获取发明都应包括在本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!