一种酒精免洗凝胶的制备方法与流程
1.本发明属于免洗凝胶技术领域,具体涉及一种酒精免洗凝胶的制备方法。
背景技术:
2.自然界中存在着各种各样的微生物,尤其是在夏季及病菌高发期,细菌滋生速度增快,部分微生物进入体内会对人体体内环境产生较大的影响,甚至引起各类感染性疾病。
3.乙醇俗称酒精,是常用的消毒剂,有极强的除菌和抑菌作用,它可以凝固蛋白质并导致病原体死亡。医疗上也常用体积分数为70%~75%的乙醇作消毒剂使用,主要是过高浓度的酒精会在细菌表面形成一层保护膜,阻止其进入细菌体内,难以将细菌彻底杀死。若酒精浓度过低,虽可进入细菌,但不能将其体内的蛋白质凝固,同样也不能将细菌彻底杀死。因此,使用70%~75%的酒精,既能使组成细菌的蛋白质凝固,又不能形成包膜,能使酒精继续向内部渗透,而使其彻底消毒杀菌。
4.随着社会的发展,人们也越来越重视健康,开始使用各类消毒产品来对食物、身体、衣物等进行消毒,但大多数产品,需要用水清洗,对于水资源较为贫乏的地区,或外出的人群,较为不便,因此逐渐兴起了一系列免洗产品,其中免洗凝胶尤为受欢迎。酒精免洗凝胶使用方法中最为显著的特点就是在不用清水冲洗的前提下,还能够有效达到对手部细菌抑制和清除作用。
5.但是对于高浓度的酒精免洗凝胶在制备时很容易出现一系列问题,如产品的透明度不好,在制备时或者稳定性期间容易出现白色絮状物质进而影响产品品质。本发明的主要目的就是解决上述问题,制备出透明度高、稳定性佳的酒精免洗凝胶。
技术实现要素:
6.本发明的目的在于提供一种透明度高、稳定性好的酒精免洗凝胶的制备方法,该方法工艺简单,使用方便,且配方中不含香精及色素,对细菌能起到有效的抑制和清除作用。
7.本发明是通过以下技术方案实现的:
8.一方面,本发明提供了一种酒精免洗凝胶的制备方法,所述制备方法中需缓慢匀速地加入乙醇,所述乙醇的加入完成的总时间为2~20min,优选3~10min。
9.在一些实施例中,所述乙醇的加入完成的总时间为2~20min。
10.在一些实施例中,所述乙醇的加入完成的总时间为3~10min。
11.在一些实施例中,一种酒精免洗凝胶的制备方法,具体包括如下步骤:
12.(a)将增稠剂、保湿剂及水加热至80~85℃,搅拌溶解并保温10~15min;
13.(b)开启均质,均质速度1000~1500r/min,均质2~5min;
14.(c)开启冷却降温,待温度降至41~46℃时,在搅拌状态下缓慢匀速地加入所述乙醇,乙醇的加入速度不宜过快,否则易于出现白色絮状物质造成产品稳定不佳;
15.(d)继续搅拌,在搅拌状态下加入ph调节剂,调节体系ph在5.5~6.5之间,加水补
足至总重量的100份,搅拌均匀后即得透明的有一定粘度的酒精免洗凝胶。
16.在一些实施例中,所述乙醇的浓度大于95%。
17.在一些实施例中,所述ph调节剂是以溶于水的形式提供的。当所述ph调节剂以溶于水的形式提供时,对增稠剂进行中和时不会导致局部浓度瞬间过高,与其他组分共同配合制备的酒精免洗凝胶的稳定性及透明度更优。
18.在一些实施例中,所述ph调节剂和水的重量比为1:5~1:10。
19.另一方面,本发明提供了一种根据上述制备方法制备得到的酒精免洗凝胶,所述各原料的配比为,以重量份计,每100份重量中,由3.0~8.0份的保湿剂,0.3~0.6份的增稠剂,65~75份的乙醇,适量的ph调节剂以及余量的水组成。
20.在一些实施例中,所述各原料的配比为,以重量份计,每100份重量中,由4.0~6.0份的保湿剂,0.35~0.55份的增稠剂,68~73份的乙醇,适量的ph调节剂以及余量的水组成。
21.在一些实施例中,所述保湿剂包括甘油或丁二醇。
22.在一些实施例中,所述增稠剂包括卡波姆类中的一种或者多种的组合。
23.在一些实施例中,所述增稠剂为carbopol ultrez 20、carbopol ultrez 21、carbopol 980的一种或者多种的组合。
24.在一些实施例中,所述ph调节剂包括三乙醇胺或者氨丁三醇。
25.本发明的有益效果在于:
26.(1)本发明配方中不含香精及色素,可以适合多种人群的手部消毒,如从事食品及其它加工行业人员。
27.(2)本发明的酒精免洗凝胶无需用水冲洗,使用方便,还能够有效达到对手部细菌抑制和清除作用,易于被消费者接受。
28.(3)本发明制备方法工艺简单,制备的酒精免洗凝胶外观透明度高,且稳定性好。
29.(4)产品配方不粘手、迅速风干,并含滋润保湿成份,以保持双手肌肤的舒适清爽。
30.详细说明
31.一方面,本发明提供了一种酒精免洗凝胶的制备方法,所述制备方法中需缓慢匀速地加入乙醇,所述乙醇的加入完成的总时间为2~20min,优选3~10min。
32.在一些实施例中,所述乙醇的加入完成的总时间为2~20min。
33.在一些实施例中,所述乙醇的加入完成的总时间为3~10min。
34.在一些实施例中,一种酒精免洗凝胶的制备方法,具体包括如下步骤:
35.(a)将增稠剂、保湿剂及水加热至80~85℃,搅拌溶解并保温10~15min;
36.(b)开启均质,均质速度1000~1500r/min,均质2~5min;
37.(c)开启冷却降温,待温度降至41~46℃时,在搅拌状态下缓慢匀速地加入所述乙醇,乙醇的加入速度不宜过快,否则易于出现白色絮状物质造成产品稳定不佳;
38.(d)继续搅拌,在搅拌状态下加入ph调节剂,调节体系ph在5.5~6.5之间,加水补足至总重量的100份,搅拌均匀后即得透明的有一定粘度的酒精免洗凝胶。
39.在一些实施例中,所述乙醇的浓度大于95%。
40.在一些实施例中,所述ph调节剂是以溶于水的形式提供的。当所述ph调节剂以溶于水的形式提供时,对增稠剂进行中和时不会导致局部浓度瞬间过高,与其他组分共同配
合制备的酒精免洗凝胶的稳定性及透明度更优。
41.在一些实施例中,所述ph调节剂和水的重量比为1:5~1:10。
42.在一些实施例中,所述ph调节剂和水的重量比为1:5。
43.在一些实施例中,所述ph调节剂和水的重量比为1:8。
44.在一些实施例中,所述ph调节剂和水的重量比为1:10。
45.另一方面,本发明提供了一种根据上述制备方法制备得到的酒精免洗凝胶,所述各原料的配比为,以重量份计,每100份重量中,由3.0~8.0份的保湿剂,0.3~0.6份的增稠剂,65~75份的乙醇,适量的ph调节剂以及余量的水组成。
46.在一些实施例中,所述各原料的配比为,以重量份计,每100份重量中,由4.0~6.0份的保湿剂,0.35~0.55份的增稠剂,68~73份的乙醇,适量的ph调节剂以及余量的水组成。
47.在一些实施例中,所述各原料的配比为,以重量份计,每100份重量中,由4.0份保湿剂,0.40份增稠剂,73份乙醇,1.6份ph调节剂的水溶液(其中ph调节剂与水重量比为1:10)以及余量的水组成。
48.在一些实施例中,所述各原料的配比为,以重量份计,每100份重量中,由5.0份保湿剂,0.55份增稠剂,68份乙醇,1.5份ph调节剂的水溶液(其中ph调节剂与水重量比为1:8)以及余量的水组成。
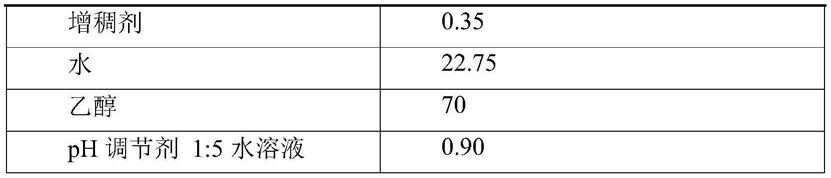
49.在一些实施例中,所述各原料的配比为,以重量份计,每100份重量中,由6.0份保湿剂,0.35份增稠剂,70份乙醇,0.9份ph调节剂的水溶液(其中ph调节剂与水重量比为1:5)以及余量的水组成。
50.在一些实施例中,所述保湿剂包括甘油或丁二醇。
51.在一些实施例中,所述增稠剂包括卡波姆类中的一种或者多种的组合。
52.在一些实施例中,所述增稠剂为carbopol ultrez 20、carbopol ultrez 21、carbopol 980的一种或者多种的组合。
53.在一些实施例中,所述ph调节剂包括三乙醇胺或者氨丁三醇。
具体实施方式
54.下面详细描述本发明的实施例。下面的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
55.下面结合具体实施例对本发明进行进一步的解释说明。
56.实施例1
57.本实施例中一种外观透明度高、稳定性好的酒精免洗凝胶,是由下列按重量份的原料制备而成,见表1:
58.表1:
59.[0060][0061]
具体操作方法:
[0062]
称取0.35份增稠剂、6.0份甘油及水加热至80℃灭菌,并搅拌溶解;开启均质,均质速度1000r/min,均质5min;开启冷却降温,待温度降至41℃时,在搅拌状态下将乙醇缓慢匀速地加入到体系中,乙醇的加入速度不宜过快,乙醇的加入完成时间为3.5min,搅拌均匀后最后加入提前溶于水配置好的ph调节剂,调节ph值,控制体系ph为6.0,搅拌均匀后即得透明的有一定粘度的酒精免洗凝胶。
[0063]
实施例2
[0064]
本实施例中一种外观透明度高、稳定性好的酒精免洗凝胶,是由下列按重量份的原料制备而成,见表2:
[0065]
表2:
[0066]
原料配比(%)甘油4.0增稠剂0.40水21乙醇73ph调节剂1:10水溶液1.6
[0067]
具体操作方法:
[0068]
称取0.40份增稠剂、4.0份甘油及水加热至85℃灭菌,并搅拌溶解;开启均质,均质速度1200r/min,均质3min;开启冷却降温,待温度降至42℃时,在搅拌状态下将乙醇缓慢匀速地加入到体系中,乙醇的加入速度不宜过快,乙醇的加入完成时间为4min,搅拌均匀后最后加入提前溶于水配置好的ph调节剂,调节ph值,控制体系ph为5.5,搅拌均匀后即得透明的有一定粘度的酒精免洗凝胶。
[0069]
实施例3
[0070]
本实施例中一种外观透明度高、稳定性好的酒精免洗凝胶,是由下列按重量份的原料制备而成,见表3:
[0071]
表3:
[0072][0073]
[0074]
具体操作方法:
[0075]
称取0.55份增稠剂、5.0份甘油及水加热至82℃灭菌,并搅拌溶解;开启均质,均质速度1500r/min,均质2min;开启冷却降温,待温度降至45℃时,在搅拌状态下将乙醇缓慢匀速地加入到体系中,乙醇的加入速度不宜过快,乙醇的加入完成时间为5min,搅拌均匀后最后加入提前配置好的ph调节剂,调节ph值,控制体系ph为6.3,搅拌均匀后即得透明的有一定粘度的酒精免洗凝胶。
[0076]
对比例1
[0077]
对比例1与实施例2的组成成分相同,只是工艺处理方式不同,具体为:称取0.40份增稠剂、4.0份甘油及水加热至85℃灭菌,并搅拌溶解;开启均质,均质速度1200r/min,均质3min;开启冷却降温,待温度降至42℃时,在搅拌状态下将乙醇于30s内一次性快速加入到体系中,搅拌均匀后最后加入提前溶于水配置好的ph调节剂,调节ph值,控制体系ph为5.5,最终得到了有白色絮状物质的酒精免洗凝胶。
[0078]
对比例2
[0079]
对比例2与实施例2的组成成分相同,只是工艺处理方式不同,具体为:称取0.40份增稠剂、4.0份甘油及水加热至85℃灭菌,并搅拌溶解;开启均质,均质速度1200r/min,均质3min;开启冷却降温,待温度降至42℃时,在搅拌状态下将乙醇缓慢匀速地加入到体系中,乙醇的加入完成时间为30min,搅拌均匀后最后加入提前溶于水配置好的ph调节剂,调节ph值,控制体系ph为5.5,最终得到了虽然透明度可以但是具有很强流动性较稀的产品。
[0080]
对比例3
[0081]
对比例3与实施例2的组成成分相同,只是工艺处理方式不同,具体为:称取0.40份增稠剂、4.0份甘油及水加热至85℃灭菌,并搅拌溶解;开启均质,均质速度1200r/min,均质3min;开启冷却降温,待温度降至42℃时,在搅拌状态下加入溶于水配置好的ph调节剂,调节体系的ph为5.5,最后在搅拌状态下将乙醇缓慢匀速地加入到体系中,乙醇的加入完成时间为4min,最终得到了外观有点朦、透明度不高的酒精免洗凝胶。
[0082]
实施例和对比例的外观和稳定性比较见表4:
[0083]
表4:
[0084][0085][0086]
将实施例2制备的酒精免洗凝胶进行如下测试:
[0087]
一、不粘手、迅速风干的效果
[0088]
将实施例2制备的酒精免洗凝胶与市面市售类似免洗产品进行如下功效实验:
[0089]
选取试验者40例;分为2组,每组20人,实验组用本发明实施例2的配方制备的产品,对照组用市面销售的类似免洗产品。取3ml免洗凝胶于掌心,均匀涂抹于手部进行彻底清洁,让受试者双手相互充分搓擦,作用时间为1min,并记录试用者使用感受和反馈。
[0090]
表5:产品风干速度和粘腻性的对比表
[0091][0092]
从结果反馈可以看出100%的试用者认为本发明的凝胶风干速度较快,在彻底清洁后的10s内已完全风干;且95%的试用者认为产品使用结束时无粘腻感。在风干速度和使用感粘腻性方面要优于市售产品。
[0093]
二、乙醇含量及稳定性测试
[0094]
检测方法如下:
[0095]
检测依据:《消毒技术规范》(2002年版)2.2.1.2.11乙醇含量的测定;《消毒技术规范》(2002年版)2.2.3消毒产品稳定性测定。
[0096]
检测条件:环境温度为22.3℃,相对湿度为62%。
[0097]
结果如下:
[0098]
保存前后稳定性测试结果见表6:
[0099]
表6:稳定性测试结果
[0100][0101]
由以上结果可以看出本发明制备的凝胶在54℃保存14天后,乙醇含量为72.5%(v/v),其稳定性试验前的乙醇含量为74.3%(v/v),乙醇含量的下降为2.4,说明本发明制备的凝胶符合《消毒技术规范》(2002年版)中有效成分含量下降率≤10%的要求,该样品贮存的有效期可至少为1年。
[0102]
三、对微生物的杀灭测试
[0103]
a:对金黄色葡萄球菌、大肠杆菌和铜绿假单胞菌的杀灭试验
[0104]
试验菌株:金黄色葡萄球菌atcc6538,大肠杆菌8099,铜绿假单胞菌atcc15422。以上菌种代数为第4代,并用0.03mol/l pbs配制菌悬液。
[0105]
中和剂:含3%吐温80的pbs溶液。
[0106]
有机干扰物:3%牛血清蛋白
[0107]
检测依据:《消毒技术规范》(2002年版)2.1.1.5中和剂鉴定试验;2.1.1.7细菌定量杀灭试验。
[0108]
菌悬液的制备:选取菌含量为1*108cfu/ml~5*108cfu/ml的菌悬液进行中和鉴定
试验。
[0109]
中和剂鉴定试验:试验菌为大肠杆菌。试验分组为:(1)消毒剂+菌片,(2)(消毒剂+菌片)+中和剂,(3)中和剂+菌片,(4)(消毒剂+中和剂)+菌片,(5)稀释液+中和剂+培养基。样品本发明的酒精免洗凝胶与中和剂同比稀释1.5倍,作用1min,试验重复3次。
[0110]
杀灭性能测试:按照载体浸泡定量杀菌试验,样品作用时间为30s、1min、1.5min、试验重复3次。试验环境温度为21℃~22℃。
[0111]
结果如下:
[0112]
(1)中和剂鉴定试验
[0113]
3次重复试验证明,第1组平均生长菌落数为无菌生长,第2组生长菌落数为1.1*102cfu/片,第3、4、5组平均生长菌落相近,三组间误差率为4.64%,第6组无菌落生长。
[0114]
具体结果见表7:
[0115]
表7:中和剂鉴定试验结果
[0116][0117]
注:阴性对照无菌生长。
[0118]
(2)对金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌的杀灭效果
[0119]
经3次重复试验的证明,样品作用30s,对金黄色葡萄球菌的杀灭对数值为>3.00,对大肠杆菌的杀灭对数值为>3.00,对铜绿假单胞菌的杀灭对数值为>3.00。具体结果见表8:
[0120]
表8:样品对金黄色葡萄球菌、大肠杆菌和铜绿假单胞菌的杀灭结果
[0121][0122]
注:阴性对照无菌生长。
[0123]
结论:以含3%吐温80的pbs为中和剂,本发明的免洗酒精凝胶作用1min,对金黄色
葡萄球菌的杀灭对数值均>3.00,对大肠杆菌的杀灭对数值为>3.00,对铜绿假单胞菌的杀灭对数值为>3.00。本发明制备的酒精免洗凝胶符合《消毒技术规范》(2002年版)的要求。
[0124]
b:对白色念珠菌的杀灭试验
[0125]
试验菌株:白色念珠菌atcc 10231。以上菌株代数为第4代,并用含0.03mol/l pbs配制菌悬液。
[0126]
中和剂:含3%吐温80的pbs溶液。
[0127]
有机干扰物:3%牛血清蛋白
[0128]
检测依据:《消毒技术规范》(2002年版)2.1.1.5中和剂鉴定试验;2.1.1.7细菌定量杀灭试验。
[0129]
菌悬液的制备:选取菌含量为1*108cfu/ml~5*108cfu/ml的菌悬液进行中和鉴定试验。
[0130]
中和剂鉴定试验:试验菌为大肠杆菌。试验分组为:(1)消毒剂+菌片,(2)(消毒剂+菌片)+中和剂,(3)中和剂+菌片,(4)(消毒剂+中和剂)+菌片,(5)稀释液+中和剂+培养基。样品本发明的酒精免洗凝胶与中和剂同比稀释1.5倍,作用1min,试验重复3次。
[0131]
杀灭性能测试:按照载体浸泡定量杀菌试验,样品作用时间为30s、1min、1.5min、试验重复3次。试验环境温度为21℃~22℃。
[0132]
结果如下:
[0133]
(1)中和剂鉴定试验
[0134]
3次重复试验证明,第1组平均生长菌落数为无菌生长,第2组生长菌落数为4.8*102cfu/片,第3、4、5组平均生长菌落相近,三组间误差率为4.04%,第6组无菌落生长。
[0135]
具体结果见表9:
[0136]
表9:中和剂鉴定试验
[0137][0138]
注:阴性对照无菌生长。
[0139]
(3)对白色念珠菌的杀灭效果
[0140]
经3次重复试验证明,样品作用30s,对白色念珠菌的杀灭对数值为>3.00。
[0141]
具体结果见表10:
[0142]
表10:样品对白色念珠菌杀灭结果
[0143][0144]
注:阴性对照无菌生长。
[0145]
结论:以含3%吐温80的pbs为中和剂,本发明的免洗酒精凝胶作用1min,对白色念珠菌的杀灭对数值均>3.00。本发明制备的酒精免洗凝胶符合《消毒技术规范》(2002年版)的要求。
[0146]
四、卫生手现场消毒实验
[0147]
中和剂:含3%吐温80的pbs溶液。
[0148]
对照采样液:0.1%吐温80pbs。
[0149]
检测依据:《消毒技术规范》(2002年版)2.1.2.6消毒剂对手消毒现场试验。
[0150]
消毒前:让受试者双手相互充分搓擦,左手指并拢,用无菌棉试在含10ml稀释液试管中浸湿,于管壁上挤干后,在五指屈面指尖至指根,往返涂擦2遍,每涂擦一遍,将棉拭转动一次。采样后,以无菌操作方式将棉拭采样端剪入中和剂试管内,作为阳性对照样本。
[0151]
根据消毒剂使用说明书的方法对右手进行消毒,设定作用时间为1min,消毒后用中和剂代替稀释液,与阳性对照组同样的方法对受试者右手上表面残留的自然菌采样一次,作为试验组样本。
[0152]
受试人数30人次。试验环境温度21℃~22℃,相对湿度58%~68%。
[0153]
具体结果见表11。
[0154]
表11:对卫生手的消毒现场试验结果
[0155][0156]
[0157]
注:阴性对照组无菌生长
[0158]
结论:经30人次试验结果显示,本发明制备的酒精免洗凝胶样品涂抹作用1min,对卫生手表面自然菌的杀灭对数值均>1.00。符合gb 27950
--
2011《手消毒剂卫生要求》的要求。卫生手消毒后残留自然菌≤100cfu/cm2。本发明制备的酒精免洗凝胶符合15982—2012《医院消毒卫生标准》的规定。
[0159]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0160]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1