使用超高射频(RF)功率在超短持续时间内消融低-中深度的消融灶的制作方法
本发明整体涉及射频(rf)消融,并且具体地涉及心脏rf消融。
背景技术:
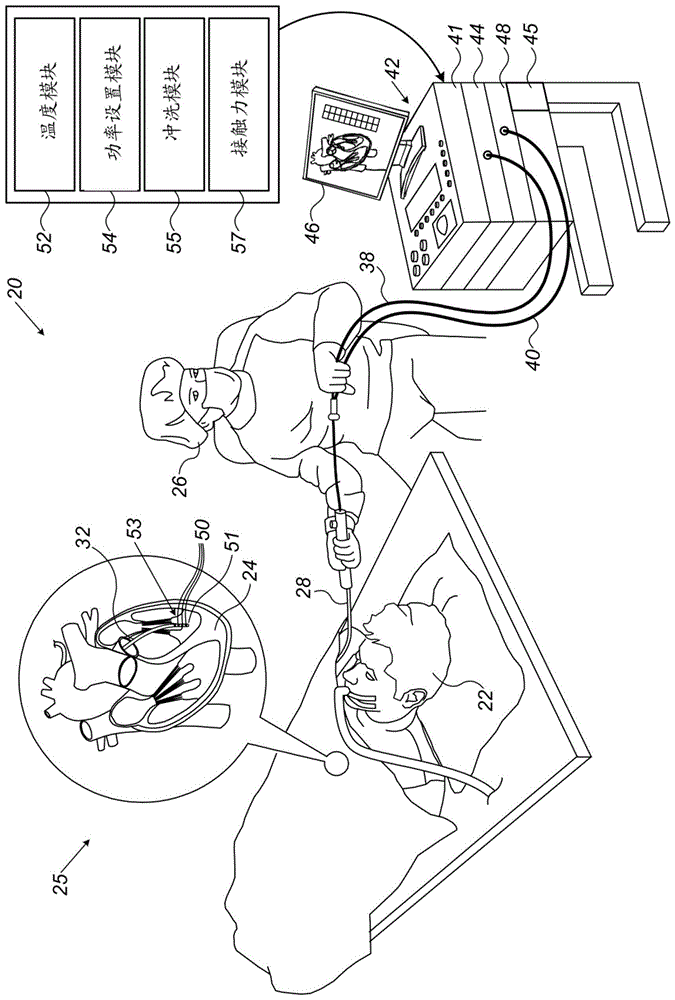
:先前在专利文献中提出了用于优化射频(rf)消融治疗的技术。例如,美国专利申请公布2009/0093802描述了用于经中隔心脏规程的系统和方法。根据具体实施方案的用于治疗患者的方法包括将穿透导丝的组织定位在心中隔附近,将能量脉冲引导到导丝,以及通过沿远侧方向以一系列离散步长移动导丝来将导丝推进到中隔内并穿过中隔。各个步长可具有在患者体外测量的预定距离。该方法还可包括在导丝已穿过中隔之后经由导丝来传送导管。又如,美国专利申请公布2004/0172110描述了一种能够烧灼心房前庭中的目标消融灶的rf加热球囊导管。rf加热球囊导管包括:能够充胀的球囊,该能够充胀的球囊能够在充胀时与目标消融灶接触;rf电极,该rf电极用作附接到受检者身体表面的表面电极的对电极并且放置在球囊的壁中或球囊内部以在表面电极与rf电极之间提供rf功率;温度传感器,该温度传感器能够感测球囊内部的温度;引导轴,该引导轴从内管的末端伸出并且能够将球囊保持在目标消融灶上;以及导丝,该导丝延伸穿过导管和引导轴。美国专利9962217描述了组织消融系统和方法,其中心脏导管结合了用于在接合消融部位时感测抵靠远侧尖端的机械力的压力检测器。控制件对压力检测器作出响应,以根据部位的接触压力、消融器的功率输出和能量施加时间之间的关系计算消融体积。该系统以某一施加时间和某一功率水平向组织施加指定剂量的能量以消融组织,其中剂量的施加时间和功率水平中的至少一者取决于机械力。技术实现要素:本发明的实施方案提供了一种身体组织消融的方法,该方法包括定义超高功率超短持续时间(upud)消融协议,超高功率超短持续时间(upud)消融协议指定具有(i)至少400瓦的目标消融功率和(ii)不超过三秒的脉冲持续时间的消融信号以用于在患者体内的组织中产生指定的消融灶。在消融探头与组织之间实现接触。使用消融探头,根据upud协议向组织施加消融信号,upud协议递送具有指定目标消融功率和持续时间的消融信号。在一些实施方案中,定义upud消融协议包括将脉冲持续时间设置为不超过一秒。在其他实施方案中,定义upud消融协议包括将脉冲持续时间设置为不超过患者的单个心跳周期。在一些实施方案中,方法还包括在消融信号的施加期间,监测组织附近的温度,并且如果所监测的温度超过预定义的最高温度,则停止消融信号。在另一个实施方案中,方法还包括在消融信号的施加期间,监测探头施加在组织上的接触力,并且如果所监测的接触力降至低于预先指定的值,则停止消融信号。根据本发明的实施方案,另外提供了一种用于身体组织消融的系统,该系统包括存储器、消融探头、超高功率超短持续时间(upud)发生器和处理器。存储器被配置为存储超高功率超短持续时间(upud)消融协议的值,超高功率超短持续时间(upud)消融协议指定具有(i)至少400瓦的目标消融功率和(ii)不超过三秒的脉冲持续时间的消融信号以用于在患者体内的组织中产生指定的消融灶。消融探头被配置为与组织实现接触。upud发生器被配置为生成消融信号。处理器被配置为控制发生器和消融探头以根据upud协议向组织施加消融信号,upud协议递送具有指定目标消融功率和持续时间的消融功率。结合附图,通过以下对本发明的实施方案的详细描述,将更全面地理解本发明,其中:附图说明图1为根据本发明的实施方案的用于超高功率超短持续时间(upud)心脏射频(rf)消融疗法的系统的示意性图解说明图;并且图2为示意性地示出根据本发明的实施方案的图1的超高功率超短持续时间(upud)rf消融系统的操作中执行的算法的步骤的流程图。具体实施方式概述心脏射频(rf)消融系统可在消融期间改变消融功率的速率,以试图实现精确的消融灶深度。一些系统可改变rf功率和冲洗速率以及消融的持续时间,同时确保消融组织的温度不超过最大值或降至低于最小值。然而,在例如薄组织的消融期间,组织可具有较差的温度响应(例如,组织温度可意外上升/下降)。因此,系统可相应地改变其施加到组织的能量的量,这可导致不受控制的消融灶深度。例如,在施加几十瓦并持续至多十秒的持续时间的典型协议中,组织中的不受控的传导加热机制可导致不受控制的消融灶深度。在一些情况下,其他控制读数诸如阻抗可能不准确,从而导致rf功率和消融持续时间的不正确调谐,诸如在过长时间内施加过少的功率,这会导致低效的消融和可能的副作用诸如血块。下文所述的本发明的实施方案以恒定的超高功率超短持续时间(upud)模式来操作消融系统。通常,本发明所公开的upud消融协议使用在超短持续时间内(例如,不超过三秒并且通常仅持续0.5-0.9秒的亚秒持续时间,这取决于目标消融灶深度)施加到组织的超高额定消融rf功率(例如,每个消融电极至少400瓦)来实现预先计划的消融灶。超短消融时间确保高功率集中在期望的消融灶区域中,以便显著地降低来自逸出期望区域的能量的附带损伤(例如由经由组织的传导加热引起的损伤)的风险。利用本发明所公开的rf消融的upud模式,所得的消融灶深度主要取决于组织的阻抗加热而非组织的传导加热,以便实现消融灶参数的高水平再现性。具体地,上述常规消融协议与本发明所公开的upud协议之间的差异是显著的,尤其是在难以保持导管的稳定位置的区域中,例如在肺静脉与心耳之间的脊处。在与单个心跳相当的持续时间内生成并且施加rf消融的能力显著地降低了对导管在长持续时间(例如,十个心跳)内保持稳定的需求。降低的需求继而减少了医师需要稳定导管来实现准确、有效的消融灶所花费的努力和时间。在一个实施方案中,rf消融持续时间被设置为不超过患者的单个心跳周期(单个心动周期)。可针对特定患者预先测量心跳周期,或者可设置适用于所有患者的通用上限。在一些实施方案中,在消融期间运行算法的处理器监测温度,并且如果温度超过容许的最高温度值(例如,预先指定的高温极限),则处理器停止消融规程。除此之外或另选地,在消融期间,处理器监测导管与组织之间的接触力,并且如果接触力降至低于导致消融效率下降的预先指定的值,则处理器停止消融规程。就多电极导管而言,本发明的实施方案能够在如上所述的亚秒范围内的典型所需持续时间内对电极中的每个电极施加大约400瓦。本发明所公开的upud消融可产生例如高度局限性的精确消融灶的环。本发明所公开的upudrf消融技术可因此改善基于导管的rf消融规程的临床结果。系统描述图1为根据本发明的实施方案的用于超高功率超短持续时间(upud)心脏射频(rf)消融疗法的系统20的示意性图解说明图。通常,系统20的存储器45存储用于不同临床场景的多个消融协议,诸如图2中描述的协议。如图所见,医师26将导管28穿过血管插入到受检者22的心脏24的腔室内,并且操纵该导管以使得导管的远侧端部32接触待治疗的区域中的心脏组织。在插图25中看到的导管28的尖端电极51包括测量电极温度的一个或多个温度传感器50。在一些实施方案中,使用该温度来估计消融组织附近的温度。尖端电极51还包括一个或多个接触力传感器53,该一个或多个接触力传感器测量由尖端电极51施加到组织上的力。用于估计由消融探头抵靠组织施加的瞬时接触力的方法在2019年5月6日提交的名称为“adaptingirrigationrateinradiofrequency(rf)ablationinresponsetocontact-forcevariation”的美国专利申请16/403865中有所描述,该专利申请被转让给本专利申请的受让人并且其公开内容以引用方式并入本文。另选地,可使用任何其他合适的技术来估计由尖端电极51施加在组织上的接触力。在将远侧端部32定位在消融部位处并且确保尖端与心脏组织接触之后,操作者26致动控制台42中的超高功率超短持续时间(upud)rf能量发生器44,以经由缆线38向远侧端部32供应rf功率。同时,冲洗泵48通过管40和导管28中的管腔向远侧端部供应冷却流体诸如生理盐水溶液。通常,在消融之前和期间,显示器46向医师26显示消融参数的值,诸如下表i-ii中所列的那些。可调节超高功率超短持续时间(upud)rf和冲洗的定时,以便在超短消融期间提供适当体积的冲洗液来冷却导管的尖端和组织,而不会向心脏加入过多的冲洗流体。为了操作系统20,处理器41包括被处理器用来操作系统的多个模块。这些模块包括温度模块52、功率设置模块54、冲洗模块55和接触力模块57,以下描述了这些模块的功能。具体地,处理器41运行如本文所公开的包括在图2中的专用算法,该专用算法使得处理器41能够执行本发明所公开的步骤,如下文进一步所述。尽管图解实施方案具体地涉及使用尖端消融装置来消融心脏组织,但本文所述的方法可另选地应用于包括多个消融电极的消融装置中,其中每个电极由处理器41独立地控制并且根据upud协议中指定的rf功率和持续时间来操作,诸如图2所述。在超短持续时间内施加超高rf功率图2为示意性地示出根据本发明的实施方案的图1的超高功率超短持续时间(upud)rf消融系统20的操作中执行的算法的步骤的流程图。该过程开始于消融参数预设步骤60,在该步骤期间,医师26预设消融功率和持续时间。步骤60可涉及生成用于不同临床场景的不同协议,并且将协议存储在例如系统20的存储器45中。在一些实施方案中,按照表i-ii所示来设置上述消融参数和其他预设参数。通常,对于每个电极的rf功率,系统的操作者仅设置超高rf功率,而出于安全原因,系统将最小rf功率自动设置为零。表i-ii提供了不同的可能设置,这些设置可用于优化消融灶深度,同时最小化附带损伤,具体取决于临床需要。参数值/范围预设消融功率水平400w预设消融时间0.5s-0.7s容许的最高温度65℃接触力的采样率5hz-70hz预设冲洗流速2ml/min-30ml/min表-i低消融灶深度参数值/范围预设消融功率水平400w预设消融时间0.8s-0.9s容许的最高温度65℃接触力的采样率5hz-70hz冲洗流速2ml/min-30ml/min表-ii中消融灶深度消融参数设置步骤60在医师26例如通过使用或修改预定义的upud消融协议来执行消融之前实施。在消融治疗开始时,在探头导入步骤62中,医师26使用结合到系统20中的导管位置跟踪系统将导管28插入到心脏24中的期望的位置中。接下来,在电极-组织接触步骤64处,医师26在电极尖端51与目标心脏组织之间实现物理接触。处理器41接收来自导管28上的传感器的接触力指示信号并且确定瞬时接触力。在rf递送步骤66处,医师26使用医师26所选择的特定消融协议来操作系统20,就该特定消融协议而言,参数值是在步骤60和62中选择的。医师26的任务是通过在超短持续时间期间施加(例如,利用电极51)目标功率来执行预设消融协议,该超短持续时间定义在例如包括表i-ii所示的消融参数的upud协议中。表i-ii中给出的值为示例值,并且任何其他合适的值可用于另选的实施方案中。一般来讲,每个电极施加的功率水平为至少400w,并且脉冲持续时间不超过三秒。在大多数实际具体实施中,脉冲持续时间不超过一秒。在一些实施方案中,脉冲持续时间被设置为不超过患者的单个心跳周期(单个心动周期)。在单个心跳中执行消融为有利的,例如,因为在该过程的持续时间内保持导管稳定为明显较容易的。在一个实施方案中,处理器41预先测量正被治疗的特定患者的心跳周期,并且确保脉冲持续时间不超过预先测量的心跳周期。另选地,脉冲持续时间可被设置为短于通常适用于所有患者的通用持续时间(例如,某个亚秒持续时间)。系统20的显示器46可被配置为通过本领域已知的方法向医师26显示rf到电极的递送的进度。进度的显示可为图形的(诸如如由消融产生的相应消融灶尺寸的模拟)和/或通过字母数字显示器。在rf递送规程期间,处理器41使用温度模块52和接触力模块57来对规程的进展执行多个检查。在一些实施方案中,检查温度(68),并且如果温度超过根据表i的容许最大值,则处理器在消融终止步骤72处结束功率的递送并停止消融规程。除此之外或另选地,检查接触力(70),并且如果接触力降至低于预先指定的值,则处理器在消融终止步骤72处结束功率的递送并停止消融规程。图2中所示的示例性流程图完全是为了概念清晰而选择的。本实施方案还包括算法的附加步骤,诸如检查冲洗流速,这些附加步骤已被有意地从本文的公开内容中省略以便提供较简化的流程图。尽管本文所述的实施方案主要涉及心脏应用,但本文所述的方法和系统也可用于消融身体的其他器官,诸如肾和前列腺消融。因此应当理解,上面描述的实施方案以举例的方式被引用,并且本发明不限于上文特定示出和描述的内容。相反,本发明的范围包括上文描述的各种特征的组合和子组合以及它们的变型和修改,本领域的技术人员在阅读上述描述时将会想到该变型和修改,并且该变型和修改并未在现有技术中公开。以引用方式并入本专利申请的文献被视为本申请的整体部分,不同的是如果这些并入的文献中限定的任何术语与本说明书中明确或隐含地给出的定义相冲突,则应仅考虑本说明书中的定义。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1