双特异性抗体CAR细胞免疫疗法的制作方法
双特异性抗体car细胞免疫疗法
1.相关申请的交叉引用本技术根据35 u.s.c.
ꢀ§ꢀ
119(e)要求2019年9月10日提交的美国临时申请第62/898,503号的优先权,其内容通过引用整体并入本技术。
2.序列表本技术包含序列表,该序列表已经以ascii格式电子提交,并通过引用整体并入本文。该ascii副本创建于2020年9月4日,命名为113086-0112_sl.txt,大小为134,417字节。
技术领域
3.本公开大体上涉及人类免疫学领域,特别是癌症免疫疗法。
4.背景仅提供以下对本发明背景的讨论以辅助本发明的技术。
5.目前的癌症治疗方案包括化学疗法、免疫调节药物
14
、单克隆抗体
15
、以及自体或异体移植。这些疗法通常会导致疾病缓解,但几乎所有患者最终都会复发并由于疾病的复发而死亡。因此,对新疗法的需求尚未得到满足,包括针对复发和/或难治性疾病的新的组合免疫疗法。本公开解决了这些限制,并且还提供了相关的优点。
技术实现要素:
6.嵌合抗原受体(chimeric antigen receptor,car)t细胞已在临床上成功用于治疗血液系统恶性肿瘤和实体瘤,最近已被美国fda批准
1-4
。双特异性抗体(bispecific antibody,bsab)也已被fda批准用于癌症治疗,并被用作car t细胞治疗的替代免疫疗法5。但是,基于car和bsab的癌症免疫疗法仍需改进,重要原因有五个。第一,在某些情况下,car t细胞无法在体内扩增,也无法存活足够长的时间来启动患者的肿瘤溶解6。据报道,car t细胞的功效与体内car t细胞存在的数量和持续时间相关
6-8
。第二,肿瘤细胞可以脱落靶抗原以逃避治疗,尤其是当仅靶向单个抗原时。第三,bsab除了昂高且制造费时外,还具有较短的半衰期,迄今为止尚未显示出有疗效
9,10
。第四,car t细胞与针对两种不同的肿瘤相关抗原的bsab联合治疗可能是一种好方法;然而,对每一种进行单独离体生产将是劳动密集型的,而且成本高昂;尚未报道过对t细胞进行工程改造以在单个构建体中同时表达car和bsab(例如,双特异性t细胞接合器,即bite,或双特异性自然杀伤细胞接合器,即bike),其中bsab结合所有溶细胞效应细胞,或尚未证明其具有累加或协同作用,或会提高t细胞的存活率。最后,目前的car免疫治疗方法主要集中于一种免疫细胞类型,即t细胞,不包括免疫系统的先天和适应性臂(arm)中的所有其他溶细胞效应细胞。nkg2d是一种c-凝集素类型的受体,其实际上在免疫系统的先天和适应性臂中的所有溶细胞效应细胞上都表达
11,12
。
7.本公开提供了一个平台,其通过对用单一载体感染的t细胞和/或自然杀伤(nk)细胞进行工程改造来部分或全部解决这些问题,所述载体递送这两种治疗模式,即产生其car靶向一种特定的肿瘤相关抗原并表达和/或分泌靶向另一种特定得肿瘤相关抗原的bsab的t细胞或nk细胞。
8.因此,在一方面,本文提供了双特异性抗体-嵌合抗原受体(bsab-car,在本文中称为bsab-car构建体或car构建体),其包括,或基本上由以下组成,或由以下组成:(1)嵌合抗原受体(car),其包括,或基本上由以下组成,或由以下组成:(a)癌症或肿瘤靶向抗体的抗原结合域;(b)铰链结构域,(c)跨膜结构域和(d)细胞内结构域;和(2)双特异性抗体,其包括,或基本上由以下组成,或由以下组成:针对在与car结合的相同癌症或肿瘤细胞上表达的癌症或肿瘤抗原的抗体的抗原结合域,和抗nkg2d抗原结合域。在一方面,细胞内结构域包括一个或多个、或两个或多个共刺激区域,其包括,或基本上由以下组成:cd28共刺激信号传导区域和/或4-1bb共刺激结构域。car的双特异性抗体部分可以进一步包括,或基本上由以下组成,或进一步由以下组成:位于抗nkg2d抗原结合结构域之前的信号结构域。本文还提供了编码这些构建体的多核苷酸和载体以及它们编码的多肽。在一方面,car和bsab由单个连续的多核苷酸表达,并且癌症或肿瘤靶向抗体在宿主细胞的细胞表面上表达,bsab组分由表达car的细胞分泌。本文进一步提供了编码这些构建体的多核苷酸以及由它们在体外或体内编码的多肽。
9.在某些实施方式中,肿瘤靶向抗体的抗原结合结构域包括任选地通过接头肽连接的重链可变区和轻链可变区、scfv片段和/或fc片段中的一个或多个,或基本上由其组成,或由其组成。在一些实施方式中,重链和/或轻链可变区包括针对b细胞成熟抗原(bcma)和/或slamf7(也称为cs1或cd319)中的任一个和/或其每一个的等效物的抗体的相关cdr区,或基本上由其组成,或由其组成。在一方面,肿瘤靶向抗体靶向bcma并且bsab包含抗cs1抗体的抗原结合片段。在一些实施方式中,重链和/或轻链可变区包括b细胞成熟抗原(bcma)和/或slamf7(也称为cs1或cd319)中的任一个和/或其每一个的等效物的抗物的抗体的氨基酸序列,或基本上由其组成,或由其组成。在一方面,所述构建体还包括信号结构域,或基本上由其组成,或由其组成。本文还提供了编码这些构建体的多核苷酸和载体以及由它们在体外或体内编码的多肽。
10.在某些实施方式中,car还包括位于重链可变区和轻链可变区和/或scfv和fc区和/或抗原结合结构域之间的接头多肽,或基本上由其组成,或由其组成。在一方面,接头多肽位于抗nkg2d和抗cs1的抗体片段之间。在某些实施方式中,接头是甘氨酸-丝氨酸接头。在进一步的实施方式中,连接多肽包括序列(甘氨酸-丝氨酸)n,其中n是1到6的整数(seq id no:110)(例如,其中n是4),或基本上由其组成,或由其组成。在另一方面,所述多核苷酸包含编码自我切割肽的序列,例如位于car和双特异性抗体之间的t2a肽,例如,在抗bcma car和抗nkg2d抗原结合域之间。在一方面,所述bsab-car还包含自我切割肽,例如位于抗nkg2d和结合癌症或肿瘤抗原(例如cs1)的第二抗原结合域(两者均与fc片段相连)之间的t2a肽。在这种情况下,可以添加“knobs-into-holes”系统,这样就不会发生nkg2d-fc或cs1-fc的同源二聚体,而使用如protein engineering, vol. 9(6):617-621 (1996)中描述的方法时,这两者的异二聚体会发生。在一方面,所述car还包括信号结构域,或基本上由其组成,或由其组成。在一方面,信号结构域,例如igg1信号肽,位于bsab-car的nkg2d肿瘤抗原部分的起始处。本领域已知其他信号肽。本文进一步提供编码这些构建体的多核苷酸和载体以及由它们在体外或体内编码的多肽。
11.在一方面,bsab-car包含图1e中部分所示的结构,即单个bsab-car,其包括(a)bcma抗原结合多肽、自我切割肽(例如t2a)、抗nkg2d scfv和fc多肽、第二自我切割肽(例如
t2a)和抗cs1 scfv和fc多肽,或基本上由其组成。在这种情况下,可以添加“knobs-into-holes”系统,这样就不会发生nkg2d-fc或cs1-fc的同源二聚体,而使用如protein engineering, vol. 9(6):617-621 (1996) 中描述的方法时,这两者的异二聚体会发生。所述car,例如抗bcma car,还可以包括铰链结构域、跨膜结构域和细胞内结构域。在一方面,所述bs-ab car构建体还包括信号结构域,或基本上由其组成,或由其组成。在一方面,所述bs-ab car构建体还包括信号肽,或基本上由其组成,或由其组成,例如igg1信号肽,任选地位于bsab-car构建体的抗nkg2d-抗肿瘤抗原部分的起始处。本领域已知其他信号肽。本文还提供了编码这些bsab-car构建体的多核苷酸和载体以及由它们在体外或体内编码的多肽。
12.在一方面,bsab-car包含图1f中部分所示的结构,即单个car,其包括(a)bcma抗原结合多肽、自我切割肽(例如t2a)、抗nkg2d scfv和fc多肽、hma多肽、抗cs1 scfv和fc多肽,或基本上由其组成。所述bcma car还可以包括铰链结构域、跨膜结构域和细胞内结构域。在一方面,所述多肽还包括信号结构域,或基本上由其组成,或由其组成。在一方面,所述构建体进一步包括信号肽,或基本上由其组成,或由其组成,例如igg1信号肽,位于bsab-car的nkg2d肿瘤抗原部分的起始处。本领域已知其他信号肽。本文还提供了编码这些bsab-car构建体的多核苷酸和载体以及由它们在体外或体内编码的多肽。
13.在一方面,bsab-car包含图1g中部分所示的结构,即单个bs-ab car,其包括(a)bcma抗原结合多肽、自我切割肽(例如t2a)、抗nkg2d scfv和fc多肽、接头(例如g4s多肽(seq id no: 134))和抗cs1 scfv和fc多肽,或基本上由其组成。bcma car还可以包括铰链结构域、跨膜结构域和细胞内结构域。在一方面,所述多肽还包括信号结构域,或基本上由其组成,或由其组成。在一方面,所述构建体还包括信号域,或基本上由其组成,或由其组成,例如igg1信号肽,位于bsab-car的nkg2d肿瘤抗原部分的起始处。本领域已知其他信号肽。本文还提供了编码这些bsab-car构建体的多核苷酸和载体以及由它们在体外或体内编码的多肽。
14.在一方面,本文提供的是:(a)car,其包括(i)结合癌症或肿瘤细胞的癌症或肿瘤靶向抗体的抗原结合域,任选的条件是所述癌症或肿瘤靶向抗体不靶向b细胞成熟抗原(bcma),(ii)铰链结构域,(iii)跨膜结构域和(iv)细胞内结构域,或基本上由其组成,或由其组成;和(b)双特异性抗体,其包括识别并结合nkg2d的抗原结合结构域和结合由car的癌症或肿瘤细胞表达的不同抗原的抗体的抗原结合结构域,或基本上由其组成,或由其组成。car与分泌的bsab的结合旨在减少对一种方式(例如car)的克隆抗性的机会。此外,通过使用nkg2d,它对肿瘤微环境(除了car)、肿瘤床(例如nk细胞)带来各种细胞溶解作用,并且申请人在本文中表明,这显著增加了肿瘤细胞的杀伤。这对于本领域技术人员的知识是出人意料的。已经报道了肿瘤特异性组合(townsend et al. (2018), j. exper. & clin. cancer res. 37:163,以及其中引用的参考文献),但迄今为止,它们尚未与nkg2d元件组合。
15.在一方面,铰链结构域包括cd8α铰链结构域,或基本上由其组成,或由其组成。在一方面,所述多核苷酸还包括编码信号结构域的多核苷酸,或基本上由其组成,或由其组成。在一方面,所述信号结构域,例如igg1信号肽,位于bsab-car的nkg2d肿瘤抗原部分的起始处。本领域已知其他信号肽。
16.在一方面,car的跨膜结构域包括cd8α跨膜结构域,或基本上由其组成,或由其组成。在另一方面,细胞内结构域包括选自cd28共刺激信号区域、4-1bb共刺激信号区域、icos共刺激信号区域或ox40共刺激区域的一个或多个、或两个或多个共刺激区域,或基本上由其组成,或由其组成。在另一方面,跨膜结构域包括cd28共刺激信号区域和/或4-1bb共刺激信号区域,或基本上由其组成,或由其组成。在另一方面,信号结构域包括cd3 ζ信号结构域,或基本上由其组成,或由其组成。
17.在一些方面,双特异性抗体包括nkg2d的配体、或抗nkg2d scfv和/或其等效物,或基本上由其组成,或由其组成。在一些方面,nkg2d的配体、抗nkg2d scfv、结合nkg2d的抗体的cdr区域和/或其各自的等效物。在一些方面,双特异性抗体包括nkg2d抗体的重链和轻链可变区,和/或其每一个的等效物,或基本上由其组成,或由其组成。在一些方面,双特异性抗体包括衍生自nkg2d抗体的单链可变片段(scfv)和/或其每一个的等效物,或基本上由其组成,或由其组成。
18.由选自结合以下靶标的抗体的car或癌症或肿瘤靶向抗体靶向的抗原的非限制性实例:cd19、间皮素、人表皮生长因子受体2(her2)、前列腺干细胞抗原(psca)、癌胚抗原(cea)、cd33、gtpase激活蛋白(gap)、神经节苷脂g2(gd2)、cd5、前列腺特异性膜抗原(psma)、受体酪氨酸激酶样孤儿受体1(ror1)、cd123、cd70、cd38、粘蛋白1(muc1)、肝配蛋白a型受体2前体(epha2)、表皮生长因子受体变体iii(egfrviii)、白细胞介素13受体α2(il13ra2)、cd133、磷脂酰肌醇蛋白聚糖3(glypican 3,gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白α(fap)、血管内皮生长因子受体2(vegfr2)、癌症/睾丸(ct)、鸟苷酸环化酶c(gucy2c)、肿瘤相关糖蛋白72(tag-72)、胸苷激酶1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖转移酶(hprt1)。本领域已知其他肿瘤靶向抗体。
19.在一方面,car识别并结合flt3且双特异性抗体结合cd123,被用于治疗aml。在另一方面,car识别并结合egfr且双特异性抗体结合il13ra2,被用于治疗胶质母细胞瘤(gbm)。
20.本文还提供了编码上述car构建体的多核苷酸以及由它们在体外或体内编码的多肽。在一方面,多核苷酸编码:(a)car,其包括(i)癌症或肿瘤靶向抗体的抗原结合结构域,条件是癌症或肿瘤靶向抗体不靶向b细胞成熟抗原(bcma);(ii)铰链结构域;(iii)跨膜结构域;(iv)和细胞内结构域,或基本上由其组成,或由其组成;和(b)编码双特异性抗体的多核苷酸,其包括识别并结合nkg2d的抗原结合结构域和识别并结合与car不同靶标的肿瘤或癌细胞上的抗原的多核苷酸,或基本上由其组成,或由其组成。在一方面,所述多核苷酸编码cd8α铰链结构域。在一方面,所述多核苷酸还包括编码信号结构域的多核苷酸,或基本上由其组成,或由其组成。
21.在一方面,所述多核苷酸还编码跨膜结构域,其包含cd8α跨膜结构域,或基本上由其组成,或由其组成。在另一方面,多核苷酸还编码细胞内结构域,其包括cd28共刺激信号区域和/或4-1bb共刺激信号区域,或基本上由其组成,或由其组成。在另一方面,所述多核苷酸还包含编码cd3ζ信号结构域的多核苷酸。
22.在一些方面,所述多核苷酸编码双特异性抗体,所述双特异性抗体包括nkg2d配体、或抗nkg2d scfv和/或其每一个的等效物,或基本上由其组成,或由其组成。在一些方面,nkg2d配体或抗nkg2d scfv包括结合nkg2d的抗体的cdr区域,和/或其每一个的等效物,
或基本上由其组成,或由其组成。在一些方面,所述多核苷酸编码双特异性抗体,所述双特异性抗体包括针对(例如识别和结合)nkg2d的抗体的重链可变区和轻链可变区,和/或其每一个的等效物,或基本上由其组成,或由其组成。在一些方面,所述多核苷酸编码双特异性抗体,所述双特异性抗体包括衍生自针对(例如识别和结合)nkg2d的抗体和/或其等效物的单链可变片段(scfv),或基本上由其组成,或由其组成。
23.由多核苷酸编码的抗体或抗原结合结构域的非限制性实例选自结合选自以下抗原的那些:flt3、egfr、cd123、il13ra2、cd19、间皮素、人表皮生长因子受体2(her2)、前列腺干细胞抗原(psca)、癌胚抗原(cea)、cd33、gtpase激活蛋白(gap)、神经节苷脂g2(gd2)、cd5、前列腺特异性膜抗原(psma)、受体酪氨酸激酶样孤儿受体1(ror1)、cd123、cd70、cd38、粘蛋白1(muc1)、肝配蛋白a型受体2前体(epha2)、表皮生长因子受体变体iii(egfrviii)、白介素13受体α2(il13ra2)、cd133、磷脂酰肌醇蛋白聚糖3(gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白α(fap)、血管内皮生长因子受体2(vegfr2)、癌症/睾丸(ct)、鸟苷酸环化酶c(gucy2c)、肿瘤相关糖蛋白72(tag-72)、胸苷激酶1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖转移酶(hprt1)。本领域已知其他肿瘤靶向抗体。
24.在一些方面,(a)和(b)的多核苷酸是连续的。这类的非限制性示例在图1e-1g和图3a中示出。
25.本公开还提供了一种载体,其包括前述多核苷酸中的任何一种,或基本上由其组成,或由其组成。在一些方面,所述多核苷酸或载体还包括驱动多核苷酸和/或car和/或双特异性抗体表达的调控元件(例如启动子和/或增强子元件),或基本上由其组成,或由其组成。在一些方面,所述载体是质粒或病毒载体,其非限制性示例选自逆转录病毒载体、慢病毒载体、腺病毒载体和腺相关病毒载体。
26.本文还提供了一种分离的细胞,其包括如本文所述的上述载体、car和/或多核苷酸中的任何一种,或基本上由其组成,或由其组成。细胞可以是原核细胞(例如细菌细胞)或真核细胞。真核细胞的非限制性示例包括但不限于:酵母细胞、动物细胞、哺乳动物细胞、牛细胞、猫细胞、狗细胞、小鼠细胞、马细胞或人类细胞。在一些方面,所述真核细胞、哺乳动物细胞或人类细胞是免疫细胞,任选地是t细胞、b细胞、nk细胞、树突状细胞、髓样细胞、单核细胞或巨噬细胞。在一些方面,所述分离的细胞表达car并分泌双特异性抗体。
27.本文还提供了包含载体和任何一种上述多核苷酸和/或任何一种上述载体和/或任何一种上述分离的细胞的组合物。在一方面,所述载体是药学上可接受的载体。
28.在一些方面,本公开涉及一种分离的复合物,其包含与癌症或肿瘤细胞结合的上述分离的细胞中的任何一种,其中所述癌症或肿瘤细胞通过抗原的抗原结合域或由编码car或bsab的多核苷酸表达的肿瘤靶向抗体与所述分离细胞结合。
29.在一些方面,本公开涉及一种产生表达car的细胞的方法,该方法包括用上述多核苷酸中的任何一种转导分离的细胞。在一些方面,表达car的细胞选自t细胞、b细胞、nk细胞、树突状细胞、髓样细胞、单核细胞或巨噬细胞。
30.在一些方面,本公开涉及一种抑制癌细胞、或表达癌症或肿瘤抗原的肿瘤、或包含癌症或肿瘤细胞的组织生长的方法,其包括使癌细胞、肿瘤或组织与上述car和双特异性抗体和/或表达car和/或双特异性抗体的分离的细胞中的任一种接触,或基本上由其组成,或由其组成。在一些方面,所述接触是体外或体内的。在一些方面,所述接触是体内的,并且所
述的分离细胞与被治疗的对象是自体的或同种异体的。在一些方面,所述接触是体内的,并且所述分离细胞与被治疗的对象是同种异体的。体内接触可通过向需要此类治疗的对象施用所述细胞来实现。如本领域技术人员显而易见的,选择肿瘤或癌症抗原的抗原结合域来结合并治疗或抑制癌症或肿瘤细胞的生长。
31.在一些方面,本公开提供了一种通过向对象施用有效量的如本文所述的car和双特异性抗体和/或表达bsab-car的宿主细胞以及上调car的抗原结合域的靶抗原的表达的细胞减少疗法或化学疗法或治疗,来抑制癌细胞、或表达癌症或肿瘤抗原的肿瘤、或包含癌症或肿瘤细胞的组织生长的方法。在一些方面,所述细胞减少疗法包括化学疗法、冷冻疗法、热疗、靶向疗法和/或放射疗法中的一种或多种,或基本上由其组成,或由其组成。
32.在一些方面,本公开提供了一种用于在有需要的对象中抑制癌症或肿瘤的生长、抑制癌症或肿瘤的转移、或治疗癌症或肿瘤中的一种或多种的方法,其包括向对象施用上述car和双特异性抗体或者表达car和双特异性抗体的分离细胞中的任何一种,或基本上由其组成,或由其组成。在一些方面,分离的细胞对有需要的对象是自体或同种异体的。在一些方面,分离的细胞对有需要的对象是同种异体的。如本领域技术人员显而易见的,car的肿瘤或癌症的抗原的抗原结合结构域被选择以结合并治疗或抑制癌症或肿瘤细胞的生长。
33.在一些方面,上述方法还包括向对象施用上调靶抗原表达的细胞减少疗法或化学疗法或治疗,或基本上由其组成,或由其组成。在一些方面,所述细胞减少疗法包括化学疗法、冷冻疗法、热疗、靶向疗法和/或放射疗法中的一种或多种,或基本上由其组成,或由其组成。
34.本文还提供了一种试剂盒,其包括如本文所公开的car、bsab-car、多核苷酸、细胞或组合物中的一种或多种,以及任选地用于制造或使用它们的说明书,或基本上由其组成,或由其组成。试剂盒任选地进一步包含用于分析患者样本中癌症或肿瘤的表型的组合物,从而可以选择适当的car或bsab-car来治疗癌症或肿瘤。
35.在进一步的方面,本文提供了在一个构建体中编码如上所述的car和双特异性抗体(“bsab car构建体”)的分离的核酸。在一方面,所述分离的核酸编码靶向bcma以外的癌症或肿瘤相关抗原和双特异性抗体的抗原结合片段,例如,一种靶向aml或gbm上的抗原(例如flt-3、egfr、cd123或il13ra2)的scfv和一种来自抗nkg2d抗体的scfv,其通过编码非免疫原性蛋白质接头(例如来自人肌肉醛缩酶(hma))的核酸连接在一起。图3中示出了示例性的bsab-car载体。所述载体任选地包含调控序列,例如启动子、增强子和病毒长末端重复序列(ltr)。
36.本公开的一些方面涉及一种产生分泌bsab的表达car的细胞或表达car的细胞的方法,该方法包括以下步骤、或基本上由以下步骤组成、或由以下步骤组成:用如本文所述的编码car和bsab的核酸序列或编码bsab-car的分离的核酸转导分离的细胞。
37.另一方面,所述方法进一步包括:选择和分离表达car或bsab-car的细胞。在另一方面,所述细胞是真核细胞,例如哺乳动物细胞,例如人细胞,例如t细胞、b细胞、nk细胞、树突状细胞、髓样细胞、单核细胞、巨噬细胞、其任何亚群或任何其他免疫细胞。可以使用如本文所述的病毒载体或使用在标题为如“用嵌合抗原受体瞬时修饰t细胞以进行过继治疗的非病毒rna转染”的riet et al. (2013) meth. mol. biol. 969:187-201中描述的技术来转导细胞。
38.在某些实施方式中,所述方法进一步包括以下步骤、或基本上由以下步骤组成、或由以下步骤组成:用分离的多核苷酸转导细胞,所述分离的多核苷酸包括编码双特异性抗体的多核苷酸、或基本上由其组成、或由其组成,该双特异性抗体任选地识别并结合nkg2d。在一些实施方式中,双特异性抗体包括任选地由密码子最优化的nkg2d配体、或基本上由其组成、或由其组成。在某些实施方式中,双特异性抗体包括针对任选地由密码子最优化的nkg2d或其每一个的等效物的抗体的相关cdr区,或基本上由其组成,或由其组成。在一些实施方式中,双特异性抗体包括针对任选地由密码子最优化的nkg2d和/或其每一个的等效物的抗体的重链和/或轻链可变区,或基本上由其组成,或由其组成。在一些实施方式中,双特异性抗体包含衍生自针对nkg2d的抗体的单链可变片段(scfv)(任选密码子优化的)和/或其每一个的等效物。可以使用本文所述的病毒载体(例如慢病毒载体)或使用在标题为“用嵌合抗原受体瞬时修饰t细胞以进行过继治疗的非病毒rna转染”的riet et al. (2013) meth. mol. biol. 969:187-201中描述的技术来转导细胞。
39.在某些实施方式中,产生表达car或bsab-car的细胞的方法进一步包括以下步骤、或基本上由以下步骤组成、或者由以下步骤组成:激活和扩增表达car的细胞的群体。本公开的某些方面涉及一种分离的、活化的细胞群,其包含car或bsab-car,或基本上由其组成,或由其组成。在某些实施方式中,所述细胞是t细胞、b细胞、nk细胞、树突状细胞、髓样细胞、单核细胞、巨噬细胞、其任何亚群或任何其他免疫细胞中的一种或多种。
40.本公开的方面涉及一种通过使肿瘤与有效量的上述分离的细胞或组合物接触来抑制表达癌症或肿瘤抗原的肿瘤生长的方法。所述接触可以是体外的或体内的。在体外接触时,所述方法可以被用来针对患者肿瘤测试个性化疗法或被用来检测联合治疗。在体内接触时,所述方法可用于抑制有需要的对象(例如患有癌症的人类患者)的肿瘤或癌细胞的生长,并且所述患者接受有效量的所述细胞。在某些实施方式中,所述肿瘤是实体肿瘤。如本文所述,有效量被单独使用或与其他疗法联合。在某些实施方式中,靶向的癌症/肿瘤是实体瘤或影响血液和/或骨髓的癌症,例如多发性骨髓瘤(multiple myeloma,mm)、急性髓系白血病(acute myeloid leukemia,aml)或胶质母细胞瘤(glioblastoma,gbm)。在某些实施方式中,分离的细胞对被治疗的对象是自体同源的。在另一方面,所述细胞对被治疗的对象是同种异体的。在另一方面,所述方法进一步包括以下步骤、或基本上由以下步骤组成、或由以下步骤组成:向对象施用有效量的细胞减少疗法。在另一方面,所述方法进一步包括以下步骤:分离待施用至对象的细胞,用有效量的如本文所述的编码car或bsab-car的分离的核酸转导细胞,培养该细胞以获得编码car或bsab-car的细胞群(其任选地被扩增和激活),然后将所述细胞施用至患者。
41.上述组合物和方法是独特的,并且克服了现有技术的局限性,因为它们提供了一种同时分泌靶向第二肿瘤相关抗原的基于nkg2d的bsab的car细胞,其中所述car的癌症或肿瘤靶向抗体不靶向b细胞成熟抗原(bcma)。所公开的基于car nkgd2d的bsab仅是示例性的。如本领域中已知的,可针对任何数量的肿瘤抗原来修改该方法,例如egfr、flt-3、il13ra2、egfrviii;cd70、间皮素、cd123、cd19、cea、cd133、her2,参见townsend et al. (2018) j. exp. & clinical cancer res. 37:163。在另一方面,car的癌症或肿瘤靶向抗体不靶向b细胞成熟抗原(bcma)、egfrviii;cd70、间皮素、cd123、cd19、cea、cd133、her2中的一种或多种。
t,红色实线)、bcma car(bcma car t,绿色实线)和bsab-bcma seq. trans. t细胞(蓝色实线)以所示的e:t比率共培养4小时,并测量靶细胞裂解(
51
cr释放)。bsab-bcma seq. trans. t与bcma car t相比,* p《0.05,** p《0.01;seq. trans. t与bsab t相比,# p《0.05,## p《0.01。k562细胞作为bcma-cs1-阴性对照。(图2c)2
ꢀ×ꢀ
105个未经修饰的t细胞(白色方形)、ev t细胞(灰色阴影方形)、bsab t细胞(红色方形)、bcma car t细胞(绿色方形)或bsab bcma seq. trans. t细胞(蓝色方形)单独培养(无靶标)或用表达不同水平的cs1和bcma的等量的mm.1s、h929或rpmi-8226 mm细胞或bcma-cs1
‑ k562细胞刺激24小时,收集上清液以通过elisa测定ifn-γ分泌。* p《0.05,** p《0.01,n.s 无显著差异。(图2d和图2e)按照(图2c)中所述地处理细胞,并通过elisa分别测定无细胞上清液中的il-2或tnf-α分泌。** p《0.01,n.s 无显著差异。
46.图3a-3h显示了在同一构建体中同时含有bcma car和抗nkg2d-抗cs1双特异性抗体(bsab)的示例性bsab-car载体的产生,以及用该构建体转导的t细胞的功能检查。(图3a)所产生的同时表达bcma car和抗nkg2d-抗cs1-bsab(以下称为bsab-car)的慢病毒载体的示意图。t2a,一种自我切割的2a基因。如本文所述,所述载体包含编码抗原结合结构域的多核苷酸,所述抗原结合结构域结合癌症或肿瘤抗原,而不是选自bmca、egfrviii;cd70、间皮素、cd123、cd19、cea、cd133或her2的抗原。(图3b)用抗6x his-标签抗体(“6x-his”如seq id no:111所示)对空载体(ev)转导的t细胞或bsab-car t细胞的上清液和细胞裂解物进行免疫印迹分析。(图3c)将
51
cr标记的mm1.s细胞(5
×
103)与未经修饰的t细胞(t,黑色实线)、空载体转导的t细胞(ev t,黑色虚线)或bsab-car t细胞(紫色线)以所示的e:t比率共培养4小时,然后测量目标裂解(
51
cr释放)。(图3d)将从健康供体中分离的未经修饰的(黑色实线)、ev(黑色虚线)、bsab(红线)、bcma car(绿色实线)或bsab-car(紫色实线)转导的cd8(+)t细胞与
51
cr标记的mm1.s mm细胞(5
×
103)以所示的e:t比率共培养4小时,并测量目标裂解(
51
cr释放)。(图3e)用mm.1s mm细胞以10:1的e:t比率进行4小时
51
cr释放测定。为了评估在不同数量的正常(未感染)人pbmc存在下的抗肿瘤作用,以mm.1s mm靶细胞的1倍、10倍、100倍和200倍量添加pbmc。(图3f)以5:1的e:t比率进行的未经修饰的t细胞(黑色方形)、ev t细胞(图案方形)、bsab t细胞(红色方形)、bcma-car t细胞(绿色方形)或bsab-car t细胞(紫色方形)针对mm.1s mm 目标细胞的
51
cr释放测定。如图所示,效应细胞和mm.1s mm 靶细胞的孵育时间对于pbmc、nk和nk t细胞为4小时(左图),对于cd3
+ t细胞、cd8
+ t细胞、vγ9vd2 t细胞或cd4
+ t细胞为16小时。* p《0.05,** p《0.01,n.s.无显著差异。(图3g)ev t细胞(gfp,绿色)和mm.1s mm 细胞(红色)共培养1小时后的对照,对突触进行共聚焦显微镜分析(比例尺10
ꢀµ
l,上图;比例尺20
ꢀµ
l,下图);即使在下图所示的更高能量下,也没有注意到突触。(图3h)bsab car t细胞(e:gfp,绿色)和mm.1s mm 细胞(t: 红色)共培养一小时;在所有方框中均观察到e/t突触并由箭头指示(s1示出了每个方框中从左向右移动的相同的共轭e/t对,s2和s3同样如此)。左上方的方框显示了亮场(bf,比例尺10
ꢀµ
l);顶部中间的方框显示了bsab car t细胞(gfp,绿色)和mm.1s mm 细胞(红色)共培养的免疫荧光图像(比例尺10
µ
l)。右上方的方框是合并的图像,带有额外的抗6x-his标签(“6x-his”如seq id no: 111所示)识别bsab(蓝色,比例尺10
ꢀµ
l)。最下面的三行显示了在放大的区域(比例尺20
ꢀµ
l)中可视化的三个单独的e/t共轭物(s1、s2和s3)。
47.图4a-4d显示,在被bsab-car t细胞识别后,k562细胞中bcma和cs1的过表达触发
增强的细胞毒性和细胞因子分泌。(图4a)用cs1(左图)或bcma(右图)或igg同种型对照(每个图上的黑色虚线)抗体染色细胞之后,过表达cs1和bcma(k562-cs1-bcma,灰色阴影)或空载体对照(k562-pcdh,黑色实线)的k562细胞的流式细胞术分析。(图4b)空载体(ev)转导的或bsab-car转导的t细胞对k562-cs1-bcma和k562-pcdh细胞的细胞毒性,通过4小时
51
cr释放测定来确定。将k562-cs1-bcma或k562-pcdh细胞与ev t细胞或bsab-car t细胞以所示的e:t比率进行孵育。** p《0.01(k562-cs1-bcma+bsab t细胞与k562-pcdh+bsab t细胞相比)。(图4c)对ev t细胞或bsab-car t细胞(1
×
105)进行单独培养,或用相等数量的k562-cs1-bcma或k562-pcdh细胞刺激。来自培养物的上清液用于通过elisa确定ifn-γ分泌。** p《0.01。(图4d)按照(图4c)中所述地处理细胞,并通过elisa测定无细胞上清液中的il-2分泌。**p《0.01。
48.图5a-5e显示分泌的抗nkg2d-抗cs1 bsab通过nkg2d信号传导增强了car t细胞的增殖。(图5a)未经修饰的t细胞(1)、2-ev t细胞(2)、bsab t细胞(3)、bcma car t细胞(4)、bsab car t细胞(5)或幼稚t细胞(6)(非增殖对照)培养后的培养基颜色显示在上方小图中。条形图提供了细胞总数的统计分析,每组包括6个独立样本。** p《0.01(第5组 vs 第1、2、4组,第3组 vs 第1、2、4组)。为了记录t细胞增殖或t细胞增殖的缺乏,使用了紫染料(violet)细胞跟踪器,并显示为v450稀释度,在下方小图中以直方图显示。(图5b)在存在或不存在来自(图5a)的bsab car t细胞的无细胞上清液的情况下,未经修饰的t细胞、ev t细胞和bcma car t细胞的五日龄培养基(分别示出为1+、2+、4+或1、2、4)。对细胞进行计数,数据以条形图显示(顶部)。** p《0.01(4+ vs 4,2+ vs 2,1+ vs 1)。紫染料细胞跟踪器显示为v450稀释度,由下方小图中的直方图显示(底部)。(图5c)显示了两日龄的培养基。1a-未经修饰t细胞、2a-ev t细胞、3a-bsab t细胞、4a-bcma car t细胞和5a-bsab car t细胞。在第0天,将nkg2d阻断抗体(20
ꢀµ
g/ml)添加到1b、2b、3b、4b和5b的培养物中,同时将非反应性同种型对照抗体(20
ꢀµ
g/ml)添加到1a、2a、3a、4a和5a)。在这些孔下面是cd3、nkg2d、f(ab)2(用“fab”表示,代表car的表达)和ki67的流式细胞术染色,以测量细胞增殖。(图5d)进行免疫印迹分析以确定akt蛋白的磷酸化(p),以及1a
‑‑‑
未经修饰的t、2a
‑‑‑
ev t、3a
‑‑‑
bsab t、4a
‑‑‑
bcma-car t和5a
‑‑‑
bsab-car t以及1b-未经修饰的t细胞+nkg2d阻断剂、2a
‑‑‑
ev t+nkg2d阻断剂、3a
‑‑‑
bsab-t+nkg2d阻断剂、4a
‑‑‑
bcma-car t+nkg2d阻断剂和5a
‑‑‑
bsab-car t+nkg2d阻断剂的总akt蛋白。(图5e)将(图5c)中所示的相同细胞(1a、2a、3a、4a和5a)也与mm.1s mm细胞共培养48小时。如上文(图5c)中所述地进行流式细胞术分析以评估细胞增殖。
49.图6a-6c显示了分泌的抗nkg2d-抗cs1 bsab体外通过nkg2d信号传导提高了car t细胞存活。(图6a)显示了1
‑‑‑
未经修饰的t+il-2、2
‑‑‑
ev t+il-2、3
‑‑‑
bsab t+il-2、4
‑‑‑
bcma-car t+il-2、5
‑‑‑
bsab car t+il-2的五日龄培养基。cd3(第1列)、f(ab)2(第2列)和ki67流式细胞术染色以观察细胞增殖(第3列),annexin v/sytox blue以观察细胞存活(第4列)。(图6b)在上方小图显示了1
‑‑‑
未经修饰的t、2
‑‑‑
ev t、3
‑‑‑
bsab t、4
‑‑‑
bcma-car t和5
‑‑‑
bsab-car t的五日龄培养基(无il-2)。cd3(第1列)和ki67(第2列)的流式细胞术染色以检测细胞增殖。包括annexin v/sytox blue以检测细胞存活(第3列)。(图6c)显示了cd3、ki67增殖细胞、annexin v(-)sytox blue(-)活细胞、annexin v(+)凋亡细胞和annexin v(+)sytox blue(+)死细胞的百分比的统计分析。多重t检验,比较各组。** p《
0.01。
50.图7a-7d显示了体内bsab-car转导的t细胞比bcma-car t细胞和对照t细胞具有更好的增殖和存活能力。(图7a)将未经修饰的t细胞、ev t细胞、bcma-car t细胞和bsab-car t细胞静脉内(i.v.)注射到免疫缺陷的nsg小鼠中(a,上图)的设计。3d直方图(下图,第1列)表示已注射的人类cd3 t细胞的百分比。蓝色直方图表示的是第-1天未注射t细胞的小鼠,橙色直方图表示注射t细胞后1天,黑色直方图表示注射t细胞后14天(红色箭头表示bsab-car t组)。等高线表示cd69表达(橙色表示静脉内注射后1天,黑色表示静脉内注射后14天)。紫色直方图(第4列)表示静脉内注射后35天经注射的cd3 t细胞的百分比。紫色等高线是4组的ki67和cd69染色的组合,以显示细胞增殖。红色等高线是sytox blue和annexin v染色的组合,以显示细胞凋亡和细胞死亡。s-/a-表示sytox blue (-)/annexin v(-),s-/a+表示sytox blue-/annexin v+,s+/a+表示sytox blue+/annexin v+。(图7b、图7c)(图7a)中显示的人cd3
+
(图7b)和cd69
+
(图7c)细胞的统计分析。未经修饰的t(空心矩形)、ev t(图案填充的矩形)、bcma-car t(灰色阴影矩形)和bsab-car t(黑色矩形)。多重t检验,比较各组。** p《0.01,n.s. 无显著差异,n=5只小鼠/组。(图7d)ki67
+
cd69
+
增殖细胞、annexin v(-) sytox blue(-)活细胞、annexin v(+)sytox blue(-)凋亡细胞和annexin v(+)sytox blue(+)死细胞百分比的统计分析。多重t检验,比较各组。** p《0.01,n.s. 无显著差异,n=5/组。
51.图8a-8c显示了bsab-car t细胞特异性地离体识别和消除表达cs1或/和bcma的人原发性多发骨髓瘤细胞。(图8a)从mm患者骨髓中分离的cd138
+
多发性骨髓瘤肿瘤细胞中cs1和bcma蛋白的流式细胞术表面染色。显示了来自8例患者的结果。八名患者的mm细胞用pe结合的抗cs1 mab 抗体(左图)或apc结合的链霉亲和素和生物素标记的抗bcma mab(右图)染色。各种颜色用于指示8名患者或同种型匹配的对照抗体(灰色阴影)中的每一个。(图8b)将5
×
103的cd138
+
多发性骨髓瘤细胞与ev t细胞(黑色虚线)、bsab t细胞(红色线)、bcma-car t细胞(绿色线)或bsab-car t细胞(紫色线)以所示的e:t比率共培养4小时,然后使用标准
51
cr释放测定法确定特异性裂解。显示了来自患者样本1和患者样本4的代表性数据。分析了八名患者的数据,并显示为每位患者的单独值(右图)。(图8c)将所示的转导的t细胞与cd138
+
多发性骨髓瘤肿瘤细胞以1:1的e:t比率共培养24小时,并通过elisa在无细胞的上清液中测量ifn-γ的分泌。
52.图9a-9c显示,bsab car t细胞在抑制体内mm生长和延长携带有mm或被肿瘤细胞再次攻击的小鼠的存活方面是优越的。(图9a)显示了来自每个所示的组的五只具有mm.1s肿瘤的代表性小鼠的生物发光成像。nsg小鼠静脉内接种表达荧光素酶的8
ꢀ×ꢀ
10
6 mm.1s细胞(第0天)。在肿瘤植入后第10、17和24天,每只小鼠分别静脉内注射生理盐水(对照组)或10
×
10
6 ev t细胞、bsab t细胞、bsma car t细胞、bsab-bcma seq. trans. t细胞或bsab car t细胞(上方小图,实验时间表)。该行的图像是在肿瘤植入后第10天,即在注入工程化t细胞或对照t细胞之前拍摄的。在小鼠已经接受了两次治疗后(第10、17天)并且就在第三次治疗之前,在第24天拍摄的中间一行的图像。最下面一行的图像显示了经过3轮治疗(第10、17和24天)的第31天的小鼠。(图9b)在肿瘤植入后第80天,从存活的小鼠(3只bcma-car t细胞治疗组小鼠、4只bcma-seq-trans.t细胞治疗组小鼠和5只bsab-car t细胞治疗组小鼠)中收集外周血(pbl)。计算了pbl的总细胞数(左图)。fitc结合的抗人cd45 mab和
apc结合的链霉亲和素与生物素标记的山羊抗小鼠(fab)2多克隆抗体或正常的多克隆山羊免疫球蛋白g(igg)抗体的流式细胞术染色。如中间图所示,计算fab(+)细胞的百分比和数量。(图9c)用各种转导的t细胞、生理盐水(黑色实线)、ev t细胞(黑色虚线)、bsab t细胞(红色线)、bcma car t细胞(绿色线)、bcma seq. trans. t细胞(蓝色线)和bsab-car t细胞(紫色虚线)处理的mm.1s荷瘤小鼠的kaplan-meier生存曲线。带有箭头的灰色虚线垂直线表示在第80天用4
×
10
6 mm.1s细胞再次攻击小鼠。
53.图10a-10d显示,在过继转移的人pbmc的存在下,bsab-car t细胞比bcma-car t细胞更有效地抑制体内mm生长并延长了mm荷瘤小鼠的存活时间。(图10a)显示了来自每个所示组的三只具有mm.1s肿瘤的代表性小鼠的生物发光成像。nsg小鼠静脉内接种表达荧光素酶的8
×
10
6 mm.1s细胞(第0天)。在肿瘤植入后第10、17和24天,每只小鼠静脉内注射生理盐水(对照组)、bsma-car t细胞或bsab-car t细胞。在肿瘤植入后第10天,将来自同一供体的骨髓细胞耗尽的pbmc静脉内注射给小鼠(上方小图,实验时间表)。就在输注工程化t细胞或对照t细胞之前,在肿瘤植入后第10天拍摄第一列图像。在小鼠已经接受了两次治疗(第10、17天)后并且就在施用第三次治疗之前,在第19天拍摄第二列中的图像。第三列中的图像显示了经过3轮治疗(第10、17和24天)的第28天的小鼠。第四列中的图像显示了第37天的小鼠。(图10b)从存活的注射了bsab-car t细胞的小鼠(n=5)和未经治疗的nsg小鼠(无,n=5)收集血液。cd19/20 (+)人浆细胞、cd56 (+)nk细胞和cd3 (+)t细胞的流式细胞术染色。设门(gate)在人cd3(+)f(ab)2(+)上的绿色等高线表示存活的人t细胞中car表达的百分比。(图10c)对人cd19/20(+)浆细胞、cd56(+)nk细胞、cd3(+)t细胞和cd3(+)f(ab)2(+)存活的car t细胞百分比的统计分析。(图10d)用生理盐水(黑色实线)、bcma-car t细胞(绿色线)或bsab-car t细胞(紫色虚线)等各种转导的t细胞处理的携带mm1s的小鼠的kaplan-meier生存曲线。p《0.0001,bsab-car t细胞与bcma-car t细胞相比。
54.图11a-11c。(图11a)3d彩虹点流式细胞术图谱(基于cd3染色,cd3阳性细胞显示黄色和绿色,cd3阴性细胞显示深蓝色和紫色)显示cd3(+)t细胞(黑色圈,黄色和绿色)、γδ t细胞(仅黄色)、nkt细胞(橙色圈,黄色和绿色)和nk细胞(蓝色圈、深蓝色和紫色)的百分比。2d等高线图显示3d图的详细信息。(图11b)t细胞、cd8
+
t细胞、pan γδ t细胞、vγ9vδ2 t细胞、nk t细胞和nk细胞中nkg2d表面表达的流式细胞术染色。所提供的数据代表了来自10名健康供体的pbmc。(图11c)(b)中nkg2d
+
细胞的百分比的统计分析。n=10。
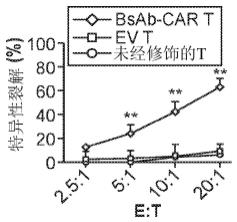
55.图12a-12b。(图12a)以10:1的e:t比率进行4小时
51
cr释放测定[e,未经修饰的t细胞(黑色实线)或ev转导的(黑色虚线)、bsab转导的(红色线)、bcma-car转导的(绿色线)或bsab-car转导的t细胞(紫色线)的效应细胞]。相对于靶细胞的1倍、10倍、100倍或200倍的不同量的人pbmc。在a中显出了三个代表性实验中的一个的特异性裂解曲线,在b中示出了三个实验的总结数据。(图12b)(a)的
51
cr释放分析结果的统计分析,多重t检验,* p《0.05,** p《0.01,n.s. 无显著差异,重复3次。
[0056]
图13a-13d。(图13a)从订购自美国红十字会的leukopack中分离出cd3(+)t细胞、cd8(+)细胞毒性t细胞、cd4(+)t细胞、γδt细胞、nk t细胞和nk细胞。初免(prime)的t细胞的黑色等高线图显示了cd3和pan αβ tcr的组合染色。棕色和绿色等高线图分别显示分选的cd8(+)和cd4(+)t细胞。(图13b)用cd3和cd56染色活化的人nk细胞。(图13c)用cd3和pan γδ tcr抗体对分选的pan γδ t细胞进行染色。通过cd3、cd56、vγ9和 vδ2的结合染色,绘
制了活化的vγ9γδ2tcr t细胞的黑色等高线图。(图13d)将新鲜的fac分选的人cd3(+)cd56(+)nkt细胞用cd3和cd56进行染色。
[0057]
图14a-14e。(图14a)未经修饰的t细胞(黑色实线)、ev t细胞(黑色虚线)、bsab t细胞(红色线)、bcma-car t细胞(绿色线)或bsab-car t细胞(紫色线)在不同时间点(包括2h、4h、8h和16h)以5:1的e:t比率的
51
cr释放测定。未添加其他pbmc。(图14b、图14c、图14d、图14e)在存在或不存在大量t细胞或单个t细胞亚群(包括初免的cd3(+)t细胞、cd8(+)t细胞、cd4(+)t细胞和vγ9vδ2 t细胞)的情况下,重复上述细胞毒性试验。对于所有实验,效应细胞与靶mm.1s 细胞的比例为 5:1。
[0058]
图15a-15j显示了bsab car t细胞(绿色)或ev t细胞(绿色)与mm.1s mm细胞(红色)共培养24小时后的共聚焦显微镜分析。(图15a-图15f)bsab-car t细胞与mm.1s mm细胞共培养24小时显示mm.1s mm 细胞消失。(图15g-图15j)ev t细胞与mm.1s mm细胞共培养24小时显示mm.1s mm细胞的持久性。bf=明场;比例尺,10 μl。
[0059]
图16显示了稳定地表达cs1和bcma基因的k562细胞的产生。左边的伪彩色流式细胞图显示未转导的k562细胞的对照。中间的伪彩色流式细胞图显示facs分选的pcdh-cs1-gfp慢病毒感染的k562细胞。第三个伪彩色流式细胞图显示facs分选的cs1(+)bcma(+) k562细胞。
[0060]
图17a-17d。(图17a)48小时的培养基。1a-未经修饰的t细胞、2a-ev t细胞、3a-bsab t细胞、4a-bcma car t细胞和5a-bsab car t细胞。cd3和nkg2d的流式细胞术染色以观察cd3 (+)群体(蓝色方框)、cd3 (+)nkg2d (+)群体(红色方框)和cd3 (+)nkg2d (-)群体(绿色方框)。(图17b)第0天,将nkg2d阻断抗体(20 μg/ml)加入(图17a)培养物中,并命名为1b、2b、3b、4b和5b。48小时后,对cd3和f(ab)2进行流式细胞术染色以观察细胞群。cd3 (+)群体(蓝色方框)。(图17c)显示了来自(图17a)的48小时的培养基。在第0天,将cs1阻断抗体(20 μg/ml)加入(图17a)培养物中,并命名为1c、2c、3c、4c和5c。48小时后,用抗cd3、抗f(ab)2、抗nkg2d和抗ki67染色细胞后进行流式细胞术分析以观察细胞增殖。将细胞设门于cd3(+)上,并示出了cd3(+)nkg2d(+)群体(红色方框)、cd3(+)nkg2d(-)群体(绿色方框)。红色点流式细胞图显示nkg2d(+)fab(+)(上方三个)或nkg2d(+)fab(-)(下方两个)细胞的增殖。绿色点流式细胞图显示nkg2d(-)fab(+)(上方三个)或nkg2d(-)fab(-)(下方两个)细胞的增殖。fab表示针对car表达的抗f(ab)2染色。(图17d)将来自(图17a)中1a、2a、3a、4a和5a的细胞与mm.1s肿瘤细胞共培养48小时。用抗cd3、抗ff(ab)2和抗nkg2d抗体对细胞染色后,进行流式细胞术分析。fab表示f(ab)2染色,其指示car表达。
[0061]
图18提供对图7中的数据的补充数据。在图7中,显示了人cd3 t细胞百分比的图3d直方图(第1列)。这些是原始的伪彩色流式细胞图。蓝色方框表示第-1天未注射t细胞的小鼠的人cd3百分比(第1列)。橙色方框表示注射t细胞后一天在小鼠中的抗人cd3(+)细胞,并在用抗f(ab)2染色后通过流式细胞术分析检测到car表达(第2、3列)。黑色方框显示在注入工程化或对照人t细胞14天小鼠中的抗人cd3(+)细胞(第4列)。紫色方框显示在注入工程化或对照人t细胞后第35天小鼠中的抗人cd3(+)细胞(第5列)。cd3(+)人类细胞的统计分析如图7所示。
[0062]
图19a-19b显示了人类健康供体的pbmc中骨髓细胞耗尽的影响,以避免将其注射到nsg小鼠体内后的gvhd。(图19a)将ficoll paque plus分离的人pbmc进行染色。数字1表
示淋巴细胞百分比,数值2表示粒细胞百分比,数值3表示单核细胞百分比。在进行facs分选前,对cd11c、cd14、cd33和cd66b进行染色以检查健康供体pbmc中骨髓细胞的百分比。(图19b)分选后,如上所述将cd11c、cd14、cd33和cd66b染色,显示伪彩色流式细胞图。
[0063]
图20提供了通过标准4h-51
cr释放测定法进行的人bsab car t细胞对自体pbmc、t细胞、nk细胞和浆细胞的细胞毒性的评估。通过ficoll-paque plus梯度离心分离pbmc。cd3(+) t细胞、cd56(+) nk细胞和cd19/20 (+)浆细胞从pbmc进行了fac分选。ev t细胞在细胞毒性试验中用作对照。
[0064]
图21a-21d。(图21a)受bsab-bcma-car(bsab-car t)慢病毒感染的健康供体的初免t细胞的不同时间点(12h、24h、48h、72h和96h)。显示了bf(亮场)gfp(绿色)的相同视图。(图21b)用抗-his标签的免疫印迹以显示bsab-car t细胞的上清液中bsab的分泌。图21b公开了“his 6x”如seq id no: 111所示。(图21c)bsab car t慢病毒感染的初免t细胞的流式细胞术染色。对gfp阳性细胞进行分选,用生物素标记的山羊抗小鼠fab特异性或同种型匹配的对照抗体对细胞进行染色,然后进行链霉亲和素和cd3抗体染色。(图21d)将
51
cr标记的h929、rpmi-8226和k562靶细胞系(5
×
103)与未经修饰的t细胞(黑色实线)、空载体转导的t细胞(ev t,黑色虚线)或bsab-car t细胞(紫色线)以所示的e:t比率共培养4小时。测量目标裂解(
51
cr释放)。bsab-car t与未经修饰的t或ev t相比,** p《0.01,重复三次。bcma(-)cs1(-)阴性k562作为阴性对照靶细胞。
[0065]
详细描述应当理解,本公开不限于所描述的特定方面,因此它们当然可以变化。还应理解,本文中使用的术语仅用于描述特定方面的目的,并无意于进行限制,因为本公开的范围将仅由所附权利要求书限定。在整个本公开中,用阿拉伯数字引用了各种技术出版物。这些出版物的完整引用可以在权利要求书的前面找到,并通过引用并入本文。
[0066]
已经显示b细胞成熟抗原(bcma)和slamf7(cs1或cd319)都是出色的mm肿瘤抗原靶点,而nkg2d是极好的免疫细胞靶点。nkg2d(一种受体)几乎在所有溶细胞免疫细胞上表达,包括nk细胞、nk t细胞、cd8(+) t细胞和gd t细胞
23
。bcma是肿瘤坏死因子受体超家族(tnfrsf17或cd269)的成员,是在浆细胞分化过程中被选择性诱导的,在幼稚和记忆b细胞中几乎不存在
24,25
。已经报道过表达抗bcma-car的t细胞的过继转移是治疗mm的有希望的新策略
26-28
。cs1是mm中另一种有吸引力的与肿瘤相关的靶抗原,因为cs1在mm细胞的表面上高度且普遍地表达
29,30
。cs1在nk细胞上和活化的cd8(+) t细胞的子集上低水平表达,但在髓样细胞和正常造血干细胞上几乎检测不到
31
。针对cs1的治疗性单克隆抗体已被fda批准用于治疗mm
32
。申请人已发表的研究表明,向cs1重定向的t细胞或nk细胞的基因修饰增强了对骨髓瘤细胞的消灭作用
29,30
。最近的一项临床前研究表明,接受cs1 car t细胞治疗的患者mm细胞被有效清除,而cs1表达水平较低的正常nk和t细胞未受影响(gogishvili, 2017 blood. 2017 dec 28;130(26):2838-2847. doi: 10.1182/blood-2017-04-778423. epub 2017 oct 31)。nkg2d是一种活化受体,如上所述在多种先天和适应性溶细胞中表达
11,33
。触发nkg2d可以导致先天和适应性细胞免疫的激活
34
。
[0067]
如本文所公开的,申请人对t细胞进行工程改造以(1)表达特异性第二代car,其结合至癌症或肿瘤抗原,其任选地结合除了bmca之外,或在另一方面,除了egfrviii;cd70、间皮素、cd123、cd19、cea、cd133或her2和(2)同时分泌抗nkg2d-bsab。先前的数据表明,这些
and sambrook eds. (2012) molecular cloning: a laboratory manual, 第四版; ausubel et al. eds. (2015) current protocols in molecular biology系列; methods in enzymology (academic press, inc., n.y.)系列; macpherson et al. (2015) pcr 1: a practical approach (irl press at oxford university press); macpherson et al. (1995) pcr 2: a practical approach; mcpherson et al. (2006) pcr: the basics (garland science); harlow and lane eds. (1999) antibodies, a laboratory manual; greenfield ed. (2014) antibodies, a laboratory manual; freshney (2010) culture of animal cells: a manual of basic technique, 第六版; gait ed. (1984) oligonucleotide synthesis;美国专利号4,683,195; hames and higgins eds. (1984) nucleic acid hybridization; anderson (1999) nucleic acid hybridization; herdewijn ed. (2005) oligonucleotide synthesis: methods and applications; hames and higgins eds. (1984) transcription and translation; buzdin and lukyanov ed. (2007) nucleic acids hybridization: modern applications; immobilized cells and enzymes (irl press (1986)); grandi ed. (2007) in vitro transcription and translation protocols, 第二版; guisan ed. (2006) immobilization of enzymes and cells; perbal (1988) a practical guide to molecular cloning, 第二版; miller and calos eds, (1987) gene transfer vectors for mammalian cells (cold spring harbor laboratory); makrides ed. (2003) gene transfer and expression in mammalian cells; mayer and walker eds. (1987) immunochemical methods in cell and molecular biology (academic press, london); lundblad and macdonald eds. (2010) handbook of biochemistry and molecular biology,第四版; 以及herzenberg et al. eds (1996) weir's handbook of experimental immunology, 第五版;以及可在提交时获得的每个版本的最新版本。
[0073]
所有数值(包括范围),例如ph、温度、时间、浓度和分子量,都是近似值,适当时可上(+)或下(-)的浮动1.0或0.1,或者变化+/-15%、或者10%、或者5%、或者2%。应当理解,尽管并非总是明确指出,但所有数值之前均带有术语“约”。还应理解,尽管并非总是明确指出,本文所述的试剂仅为示例性的,其等效物是本领域已知的。
[0074]
不需明确指出,除非另有说明,否则推定当本发明涉及多肽、蛋白质、多核苷酸或抗体时,它们的等效物或生物学等效物也预期在本发明的范围内。
[0075]
定义应当理解,本文中使用的章节或小节标题仅用于组织目的,不应被解释为限制和/或分离所述主题。
[0076]
如说明书和权利要求书中所使用的,单数形式的“一种”、“一个”和“该/所述”包括复数指代,除非上下文另有明确指出。例如,术语“一个细胞”包括多个细胞,包括其混合物。
[0077]
如本文所用,术语“包括”或“包括”旨在表示组合物和方法包括所述的元素,但不排除其他元素。“基本上由
……
组成”当被用来定义组合物和方法时,应该意为排除对于所述目的的组合来说具有任何实质性作用的其他元素。因此,如本文定义的基本上由该元素组成的组合物,将不会从分离和纯化方法中排除微量污染物和药学上可接受的载体(例如磷酸盐缓冲盐水、防腐剂等)。“由
……
组成”应当意为排除多于微量元素的其他成分和用于
施用本文公开的组合物的实质性方法步骤,或用于生产组合物或达到预期结果的工艺步骤。通过这些过渡性术语的每一个进行定义的实施方案都在本公开的范围之内。
[0078]“任选的”或“任选地”是指随后描述的情况可能发生也可能不发生,因此描述包括所述情况发生的实例和不发生的实例。
[0079]
如本文所用,“和/或”是指并涵盖相关列出项目的一个或多个的任何和所有可能的组合,以及当解释为替代的(“或”)时缺少组合。
[0080]“大体上”或“基本上”指几乎全部地或完全地,例如,某些给定数量的95%或更多。在一些实施方式中,“大体上”或“基本上”是指95%、96%、97%、98%、99%、99.5%或99.9%。
[0081]
如本文所用,术语“动物”表示活的多细胞脊椎动物生物,是包括例如哺乳动物和鸟类的类别。术语“哺乳动物”包括人类哺乳动物和非人类哺乳动物。
[0082]
术语“受试者/对象”、“宿主”、“个体”和“患者”在本文中可互换使用,是指人类和兽医学对象,例如,人类、动物、非人灵长类动物、狗、猫、羊、鼠、马和牛。在一些实施方式中,所述对象是人类。在一些实施方式中,它们指脊椎动物,优选地为哺乳动物,更优选地为人类。哺乳动物包括但不限于小鼠、大鼠、兔、猿猴、牛、绵羊、猪、犬科动物、猫科动物、农场动物、运动动物、宠物、马和灵长类动物,特别是人类。除了可用于人类治疗外,本公开还可用于伴侣哺乳动物、外来动物和家养动物(包括哺乳动物、啮齿动物)的兽医治疗。在一种实施方式中,哺乳动物包括马、狗和猫。在本公开的另一个实施方式中,人是胎儿、婴儿、青春期前对象、青少年、儿科患者或成人。一方面,所述对象是有症状前的哺乳动物或人类。另一方面,所述对象具有最小的疾病临床症状。所述对象可以是男性或女性、成人、婴儿或儿科对象。另一方面,所述对象是成年对象。在一些情况下,成年对象是成年人类,例如,超过18岁的成年人类。
[0083]
如本文所用,术语“抗体”统一指免疫球蛋白或免疫球蛋白样分子,包括但不限于,例如iga、igd、ige、igg和igm、其组合,以及在任何脊椎动物中在免疫过程期间产生的类似分子,所述脊椎动物例如是哺乳动物(例如人类、山羊、兔和小鼠)以及非哺乳动物物种(例如鲨鱼免疫球蛋白)。除非另有特别说明,否则术语“抗体”包括完整的免疫球蛋白和“抗体片段”或“抗原结合片段”,它们与感兴趣的分子(或一组高度相似的感兴趣的分子)特异性结合至基本上排除与其他分子的结合(例如,抗体和抗体片段与感兴趣的分子的结合常数相比与生物样品中的其他分子的结合常数大至少10
3 m-1
、至少10
4 m-1
或至少10
5 m-1
)。术语“抗体”还包括基因工程形式,例如嵌合抗体(例如鼠或人源化的非灵长类抗体)、异源偶联抗体(例如双特异性抗体)。另见,pierce catalog and handbook, 1994-1995 (pierce chemical co., rockford, ill.); owen et al., kuby immunology, 7th ed., w.h. freeman & co., 2013; murphy, janeway’s immunobiology, 8th ed., garland science, 2014; male et al., immunology (roitt), 8th ed., saunders, 2012; parham, the immune system, 4th ed., garland science, 2014。
[0084]
如本文所用,术语“单克隆抗体”是指由b淋巴细胞的单个克隆或由已经转染了单个抗体的轻链和重链基因的细胞产生的抗体。单克隆抗体通过本领域技术人员已知的方法产生,例如通过由骨髓瘤细胞与免疫脾细胞的融合制备杂交抗体形成细胞。单克隆抗体包括人源化单克隆抗体。
[0085]
就抗体结构而言,免疫球蛋白具有通过二硫键相互连接的重(h)链和轻(l)链。轻
链有两种类型,和k。存在决定抗体分子的功能活性的五种主要的重链类型(或同种型):igm、igd、igg、iga和ige。每条重链和轻链都包含恒定区域和可变区域(所述区域也被称为“结构域”)。结合起来,重链和轻链可变区域特异性地结合抗原。轻链和重链可变区域包含被三个高度可变区域打断的“框架”区域,所述高度可变区域也被称为“互补决定区域”或“cdr”。框架区域和cdr的范围已经被确定(参见kabat et al., sequences of proteins of immunological interest, u.s. department of health and human services, 1991,其以引用的方式合并入本文中)。kabat数据库现在在线维护。不同的轻链或重链的框架区域的序列在物种之内是相对保守的。抗体的框架区域,即组成的轻链和重链的结合的框架区域,主要采用β折叠构象,而cdr形成环,该环连接所述β折叠结构或者在一些情况中形成所述β折叠的一部分。因此,框架区域作用来形成支架,其用来通过互链、非共价相互作用将cdr定位在正确的朝向中。
[0086]
cdr主要负责结合至抗原的表位。每条链的cdr通常被称为cdr1、cdr2和cdr3,这是从n末端开始依次进行编号,并且也通常由该特定的cdr所位于的链而确定(重链区域标记为cdhr而轻链区域标记为cdlr)。因此,cdhr3是来自位于发现其的抗体重链的可变结构域的cdr3,而cdlr1是来自发现其的抗体的轻链的可变结构域的cdr1。例如,tnt抗体将具有对tnt相关抗原独特的特异性的vh区域和v
l
区域序列,并因此具有特异性的cdr序列。具有不同的特异性(即对不同抗原的不同结合位点)的抗体具有不同的cdr。虽然抗体与抗体之间不同的是cdr,但是在cdr之内只有有限数量的氨基酸位置直接涉及抗原结合。在cdr之内的这些位置称为特异性决定残基(sdr)。
[0087]
如本文所用,可结晶片段(fc)区域指稳定抗体并任选地与免疫细胞或血小板上的的fc受体相互作用(例如结合)或结合补体蛋白的抗体的尾部区域。在一些实施方式中,可使用fc突变体,例如在fc中包含人igg4 fc区域的f234a、l235a和n297q的一个或两个或所有三个突变,或者在对应于人igg4 fc区的位置的其等效物,例如,对于seq id no:81,对应的位置是seq id no:81的氨基酸(aa)16、aa 17和aa 79。
[0088]
如本文所用,术语“抗原”是指可以被特异性的体液或细胞免疫的产物(例如抗体分子或t细胞受体)特异性地结合的化合物、组合物或物质。抗原可以是任何类型的分子,包括例如半抗原、简单中间代谢物、糖(例如寡糖)、脂质和激素以及大分子(例如复合碳水化合物(例如多糖)、磷脂和蛋白质)。常见的抗原的类别包括但不限于病毒抗原、细菌抗原、真菌抗原、原生动物和其他寄生虫抗原、肿瘤抗原、涉及自身免疫疾病的抗原、过敏和移植物排斥、毒素和其他杂项抗原。
[0089]
在一些实施方式中,结合部分的抗原,例如抗体、其抗原结合片段或car,可在本文中以以下形式提供:“抗原”后跟结合部分(例如bcma car),或在抗原之前具有“抗”并在抗原之后具有结合部分(例如抗bcma抗体),或抗原后跟“的”或“针对”且之后是结合部分(例如cs1的抗体)。
[0090]
如本文所用,术语肿瘤相关抗原(taa)、癌症抗原、肿瘤抗原、癌症相关抗原和肿瘤相关抗原在本文中可互换使用,指的是癌症或肿瘤细胞的抗原物质。在一些实施方式中,taa存在于一些肿瘤或癌症细胞上以及一些正常细胞上,任选地以较低水平存在。在一些实施方式中,taa仅存在于肿瘤或癌症细胞上,而不存在于正常细胞上。在一些实施方式中,taa选自flt3、cd19、间皮素、人表皮生长因子受体2(her2)、前列腺干细胞抗原(psca)、癌胚
抗原(cea)、cd33、gtpase激活蛋白(gap)、神经节苷脂g2(gd2)、cd5、前列腺特异性膜抗原(psma)、受体酪氨酸激酶样孤儿受体1(ror1)、cd123、cd70、cd38、粘蛋白1、(muc1)、肝配蛋白a型受体2前体(epha2)、表皮生长因子受体变体iii(egfriii)、白细胞介素13受体α2(il13ra2)、cd133、磷脂酰肌醇蛋白聚糖3(gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白α(fap)、血管内皮生长因子受体2(vegfr2)、癌症/睾丸(ct)、鸟苷酰环化酶c(gucy2c),肿瘤相关糖蛋白72(tag-72)、胸苷激酶1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖转移酶(hprt1)。
[0091]
如本文所用,术语“抗原结合结构域”是指能够特异性结合到抗原靶标的任何蛋白质或多肽结构域。
[0092]
如本文所用,术语“自体”在涉及细胞时是指,被分离并且被灌注回相同的对象(受体或宿主)的细胞。“同种异体”是指非自体的细胞。
[0093]
如本文所用,术语“b细胞”是指在适应性免疫系统的体液免疫中的一类淋巴细胞。b细胞主要作用来制造抗体、用作抗原呈递细胞、释放细胞因子、以及在抗原相互作用引起的刺激之后开发记忆性b细胞。b细胞与其他淋巴细胞(例如t细胞)的不同点在于细胞表面上存在b细胞受体。b细胞可以是被分离的,也可以从商业上可获得的来源得到。商业上可获得的b细胞系的非限制性示例包括ahh-1 (atcc
®ꢀ
crl-8146
™
)、bc-1 (atcc
®ꢀ
crl-2230
™
)、bc-2 (atcc
®ꢀ
crl-2231
™
)、bc-3 (atcc
®ꢀ
crl-2277
™
)、ca46 (atcc
®ꢀ
crl-1648
™
)、dg-75 [d.g.-75] (atcc
®ꢀ
crl-2625
™
)、ds-1 (atcc
®ꢀ
crl-11102
™
)、eb-3 [eb3] (atcc
®ꢀ
ccl-85
™
)、z-138 (atcc #crl-3001)、db (atcc crl-2289)、toledo (atcc crl-2631)、pfiffer (atcc crl-2632)、sr (atcc crl-2262)、jm-1 (atcc crl-10421)、nfs-5 c-1 (atcc crl-1693)、nfs-70 c10 (atcc crl-1694)、nfs-25 c-3 (atcc crl-1695)、以及sup-b15 (atcc crl-1929)细胞系。进一步的示例包括但不限于衍生自间变性和大细胞淋巴瘤的细胞系,例如del、dl-40、fe-pd、jb6、karpas 299、ki-jk、mac-2a ply1、sr-786、su-dhl-1、-2、-4、-5、-6、-7、-8、-9、-10和-16、dohh-2、nu-dhl-1、u-937、granda519、usc-dhl-1、rl; 霍奇金淋巴瘤,例如dev、hd-70、hdlm-2、hd-myz、hkb-1、km-h2、l 428、l 540、l1236、sbh-1、sup-hd1、su/rh-hd-l。这样的商业上可获得的细胞系的非限制性示例的来源包括美国类型培养物保藏中心或atcc(http://www.atcc.org/)以及德国微生物和细胞培养物保藏中心(https://www.dsmz.de/)。
[0094]
如本文所用,“癌症”是一种疾病状态,其特征在于对象中存在表现出异常的不受控制的复制的细胞,并且在一些方面,该术语可与术语“肿瘤”互换使用。术语“癌症或肿瘤抗原”是指已知与癌细胞或肿瘤细胞或组织相关并在表面上表达的抗原,术语“癌症或肿瘤靶向抗体”是指靶向此类抗原的抗体。
[0095]
如本文所用,术语“嵌合抗原受体”(car)指这样的融合蛋白,其包含能够结合抗原的细胞外结构域、衍生自与该细胞外结构域衍生自的多肽不同的多肽的跨膜结构域、以及至少一个细胞内结构域。“嵌合抗原受体(car)”有时被称为“嵌合受体”、“t-体(t-body)”或“嵌合免疫受体(cir)”。“能够结合至抗原的细胞外结构域”是指能够结合至某个抗原的任何寡肽或多肽。“细胞内结构域”或“细胞内信号结构域”是指已知用作发送信号来引起细胞内的生物过程的激活或抑制的结构域的任何寡肽或多肽。在某些实施方式中,除了主信号结构域之外,细胞内结构域还可以包括一个或多个共刺激信号结构域、或者基本上由其组
成,或由其组成。“跨膜结构域”是指已知跨越细胞膜并且能够作用来连接细胞外结构域和信号结构域的任何寡肽或多肽。嵌合抗原受体可以任选地包含“铰链结构域”,其用作细胞外结构域和跨膜结构域之间的接头。本文提供了其非限制性示例,例如:铰链结构域:igg1重链铰链编码序列:ctcgagcccaaatcttgtgacaaaactcacacatgcccaccgtgcccg (seq id no: 112)如本领域中已知的,另外的非限制性示例包括igg4铰链区、igd和cd8结构域。
[0096]
跨膜结构域:cd28跨膜区域编码序列:ttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtg (seq id no: 113)细胞内结构域:4-1bb共刺激信号区域编码序列:aaacggggcagaaagaaactcctgtatatattcaaacaaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggaggatgtgaactg (seq id no: 114)细胞内结构域:cd28共刺激信号区域编码序列:aggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcc (seq id no: 115)细胞内结构域:cd3 ζ信号区域编码序列:agagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaa (seq id no: 116)。
[0097]
每个示例性结构域组分的其他实施方式包括具有相似生物学功能的其他蛋白质,其与由以上公开的核酸序列编码的蛋白质具有至少70%或至少80%的氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%序列同一性。此外,本文提供了此类结构域的非限制性示例。
[0098]
如本文所用,术语“cd8 α铰链结构域”是指与该名称相关的特定的蛋白质片段,以及与本文所示的cd8 α铰链结构域序列具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性,更优选地至少95%序列同一性的具有类似的生物功能的任何其他分子。在pinto, r.d. et al. (2006) vet. immunol. immunopathol. 110:169-177中提供了人类、小鼠和其他物种的cd8 α铰链结构域的示例性序列。在pinto, r.d. et al. (2006) vet. immunol. immunopathol. 110:169-177中提供了与cd8 α铰链结构域相关的序列。其非限制性示例包括:人cd8 α铰链结构域:pakptttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiy (seq id no: 117)。
[0099]
小鼠cd8 α铰链结构域:kvnstttkpvlrtpspvhptgtsqpqrpedcrprgsvkgtgldfacdiy (seq id no: 118)。
[0100]
猫cd8α铰链结构域:pvkptttpaprpptqapittsqrvslrpgtcqpsagstveasgldlscdiy (seq id no: 119)。
[0101]
如本文所用,术语“cd8 α跨膜结构域”是指与该名称相关的特定的蛋白质片段,以
及与本文所示的cd8 α跨膜结构域序列具有至少70%、或至少80%的氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%序列同一性的具有类似的生物功能的任何其他分子。与人t细胞表面糖蛋白cd8 α链(genbank登录号:np_001759.3)的183至203位氨基酸、或小鼠t细胞表面糖蛋白cd8 α链(genbank登录号:np_001074579.1)的197至217位氨基酸、以及大鼠t细胞表面糖蛋白cd8 α链(genbank登录号:np_113726.1)的190至210位氨基酸置相关的片段序列,提供了cd8 α跨膜结构域的其他示例性序列。与列出的每一个登录号相关的序列提供如下:人cd8 α跨膜结构域:iyiwaplagtcgvlllslvit (seq id no: 120)。
[0102]
小鼠cd8 α跨膜结构域:iwaplagicvalllsliitli (seq id no: 121)。
[0103]
大鼠cd8 α跨膜结构域:iwaplagicavlllslvitli (seq id no: 122)。
[0104]
如本文所用,术语“cd28跨膜结构域”是指与该名称相关的特定的蛋白质片段,以及与本文所示的cd28跨膜结构域序列具有至少70%、或至少80%氨基酸序列同一性、至少90%序列同一性、或者至少95%序列同一性的具有类似的生物功能的任何其他分子。与genbank登录号xm_006712862.2和xm_009444056.1相关的片段序列,提供了cd28跨膜结构域的其他的非限制性的示例性序列。本文提供了与每个列出的登录号相关的序列。
[0105]
如本文所用,术语“4-1bb共刺激信号区域”是指与该名称相关的特定的蛋白质片段,以及与如本文所示的4-1bb共刺激信号区域序列具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%序列同一性的具有类似的生物功能的任何其他分子。在美国公开号20130266551a1(作为美国申请号13/826,258提交)中提供了4-1bb共刺激信号区域的非限制性示例序列,例如下面提供的示例性序列:4-1bb共刺激信号区域:krgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcel (seq id no: 123)。
[0106]
如本文所用,术语“cd28共刺激信号区域”是指与该名称相关的特定的蛋白质片段,以及与本文所示的cd28共刺激信号区域序列具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%序列同一性的具有类似的生物功能的任何其他分子。在美国专利号5,686,281;geiger, t.l. et al., blood 98: 2364-2371 (2001); hombach, a. et al., j immunol 167: 6123-6131 (2001); maher, j. et al. nat biotechnol 20: 70-75 (2002); haynes, n.m. et al., j immunol 169: 5780-5786 (2002); haynes, n.m. et al., blood 100: 3155-3163 (2002)中提供了示例性的cd28共刺激信号结构域序列。非限制性的示例包括以下cd28序列的114-220残基:mlrlllalnl fpsiqvtgnk ilvkqspmlv aydnavnlsc kysynlfsre fraslhkgldsavevcvvyg nysqqlqvys ktgfncdgkl gnesvtfylq nlyvnqtdiy fckievmypppyldneksng tiihvkgkhl cpsplfpgps kpfwvlvvvg gvlacysllvtvafiifwvr skrsrllhsd ymnmtprrpg ptrkhyqpya pprdfaayrs (seq id no: 124),及其等效物。
[0107]
如本文所用,术语“icos共刺激信号区域”是指与该名称相关的特定的蛋白质片段,以及与本文所示的icos共刺激信号区域序列具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%序列同一性的具有类似的生物功能的任何其他分子。在美国公开号2015/0017141a1中提供了icos共刺激信号区域的非限制性的示例序列。示例性的多核苷酸序列提供如下:
icos共刺激信号区域编码序列:。
[0108]
如本文所用,术语“ox40共刺激信号区域”是指与该名称相关的特定的蛋白质片段,以及与本文所示的ox40共刺激信号区域序列具有至少70%、或至少80%氨基酸序列同一性、或至少90%序列同一性、或至少95%序列同一性的具有类似的生物功能的任何其他分子。在美国公开号2012/20148552a1中公开了ox40共刺激信号区域的非限制性的示例性序列,其包括以下提供的示例性序列。
[0109]
ox40共刺激信号区域编码序列:agggaccag aggctgcccc ccgatgccca caagccccct gggggaggca gtttccggac ccccatccaa gaggagcagg ccgacgccca ctccaccctg gccaagatc (seq id no: 126)及其等效物。
[0110]
如本文所用,术语“cd28共刺激信号区域”是指与该名称相关的特定的蛋白质片段,以及与本文所示的cd28共刺激信号区域序列具有至少70%、或至少80%氨基酸序列同一性、或至少90%序列同一性、或至少95%序列同一性的具有类似的生物功能的任何其他分子。在美国专利号5,686,281; geiger, t.l. et al. (2001) blood 98: 2364-2371; hombach, a. et al. (2001) j immunol 167: 6123-6131; maher, j. et al. (2002) nat biotechnol 20: 70-75; haynes, n.m. et al. (2002) j immunol 169: 5780-5786 (2002); haynes, n.m. et al. (2002) blood 100: 3155-3163中提供了示例性的cd28共刺激信号结构域序列。非限制性示例包括以下的残基114-220和编码的序列:cd28序列:mlrlllalnl fpsiqvtgnk ilvkqspmlv aydnavnlsc kysynlfsre fraslhkgldsavevcvvyg nysqqlqvys ktgfncdgkl gnesvtfylq nlyvnqtdiy fckievmypppyldneksng tiihvkgkhl cpsplfpgps kpfwvlvvvg gvlacysllvtvafiifwvr skrsrllhsd ymnmtprrpg ptrkhyqpya pprdfaayrs (seq id no: 124)及其等效物。
[0111]
如本文所用,术语“cd3ζ信号结构域”是指与该名称相关的特定的蛋白质片段,以及与如本文所示的cd3 ζ信号结构域序列具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地具有至少95%序列同一性的具有类似的生物功能的任何其他分子。在美国申请号13/826,258中提供了cd3 ζ信号结构域的非限制性示例序列,例如:rvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (seq id no: 3)。
[0112]
如本文所用,术语nkg2d是指最近引起极大关注的活化受体。已经鉴定出许多nkg2d靶配体。这些中最引人注目的是一对紧密相关的蛋白质,称为mica和micb(主要组织相容性复合体(mhc)i类链相关)。
[0113]
免疫和生物试剂(参见linscottsdirectory.com,如上所述)。
[0114]
如本文所用,术语“flt3”是指与该名称、任何其替代名称(fms相关酪氨酸激酶、干细胞酪氨酸激酶、fms样酪氨酸激酶、fl细胞因子受体、cd135抗原、ec 2.7.10.1、cd135、flk-2、stk1、flk2、生长因子受体酪氨酸激酶iii型、受体型酪氨酸蛋白激酶flt3、胎肝激酶
2、胎肝激酶、ec 2.7.10、flt-3、stk-1)或uniprot 登录号p36888相关的受体型酪氨酸蛋白激酶flt3,以及与flt3具有至少80%氨基酸序列同一性、优选地90%序列同一性、或至少95%序列同一性的具有类似的生物功能的任何其他分子及其任何变体或同种型。特异性结合flt3的单克隆抗体可从例如becton dickinson biosciences和其他商业来源获得,例如在以下网址列出的那些:biocompare.com/search-antibodies/search=flt3&said=0。本领域已知制备抗原结合片段的方法。抗原结合结构域可以来自任何适当的物种,例如绵羊或人。
[0115]
flt3的非限制性示例包括:人类flt3同种型1,mpalardggqlpllvvfsamifgtitnqdlpvikcvlinhknndssvgksssypmvsespedlgcalrpqssgtvyeaaavevdvsasitlqvlvdapgnisclwvfkhsslncqphfdlqnrgvvsmvilkmtetqageyllfiqseatnytilftvsirntllytlrrpyfrkmenqdalvcisesvpepivewvlcdsqgesckeespavvkkeekvlhelfgtdirccarnelgrectrlftidlnqtpqttlpqlflkvgeplwirckavhvnhgfgltwelenkaleegnyfemstystnrtmirilfafvssvarndtgyytcssskhpsqsalvtivekgfinatnssedyeidqyeefcfsvrfkaypqirctwtfsrksfpceqkgldngysiskfcnhkhqpgeyifhaenddaqftkmftlnirrkpqvlaeasasqascfsdgyplpswtwkkcsdkspncteeitegvwnrkanrkvfgqwvssstlnmseaikgflvkccaynslgtscetillnspgpfpfiqdnisfyatigvcllfivvltllichkykkqfryesqlqmvqvtgssdneyfyvdfreyeydlkwefprenlefgkvlgsgafgkvmnataygisktgvsiqvavkmlkekadsserealmselkmmtqlgshenivnllgactlsgpiylifeyccygdllnylrskrekfhrtwteifkehnfsfyptfqshpnssmpgsrevqihpdsdqisglhgnsfhsedeieyenqkrleeeedlnvltfedllcfayqvakgmeflefkscvhrdlaarnvlvthgkvvkicdfglardimsdsnyvvrgnarlpvkwmapeslfegiytiksdvwsygillweifslgvnpypgipvdanfykliqngfkmdqpfyateeiyiimqscwafdsrkrpsfpnltsflgcqladaeeamyqnvdgrvsecphtyqnrrpfsremdlgllspqaqveds (seq id no: 127),以及任选地其等效物。
[0116]
人类flt3同种型2:mpalardggqlpllvvfsamifgtitnqdlpvikcvlinhknndssvgksssypmvsespedlgcalrpqssgtvyeaaavevdvsasitlqvlvdapgnisclwvfkhsslncqphfdlqnrgvvsmvilkmtetqageyllfiqseatnytilftvsirntllytlrrpyfrkmenqdalvcisesvpepivewvlcdsqgesckeespavvkkeekvlhelfgtdirccarnelgrectrlftidlnqtpqttlpqlflkvgeplwirckavhvnhgfgltwelenkaleegnyfemstystnrtmirilfafvssvarndtgyytcssskhpsqsalvtivekgfinatnssedyeidqyeefcfsvrfkaypqirctwtfsrksfpceqkgldngysiskfcnhkhqpgeyifhaenddaqftkmftlnirrkpqvlaeasasqascfsdgyplpswtwkkcsdkspncteeitegvwnrkanrkvfgqwvssstlnmseaikgflvkccaynslgtscetillnspgpfpfiqdnisfyatigvcllfivvltllichkykkqfryesqlqmvqvtgssdneyfyvdfreyeydlkwefprenlefgkvlgsgafgkvmnataygisktgvsiqvavkmlkekadsserealmselkmmtqlgshenivnllgactlsgpiylifeyccygdllnylrskrekfhrtwteifkehnfsfyptfqshpnssmpgsrevqihpdsdqisglhgnsfhsedeieyenqkrleeeedlnvltfedllcfayqvakgmeflefksarlpvkwmapeslfegiytiksdvwsygillweifslgvnpypgipvdanfykliqngfkmdqpfyateeiyiimqscwafdsrkrpsfpnltsflgcqladaeeamyqnvdgrvsecphtyqnrrpfsremdlgllspqaqveds (seq id no: 128),以及任选地其等效物。
[0117]
如本文所用,术语flt3-1在一些方面是指包含具有cdr的氨基酸序列的抗体,所述cdr与下文公开的重链和轻链多核苷酸序列中编码的cdr中的任何一个(优选地以下cdr3区
中的至少一个、最优选地以下两个cdr3区)具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选至少95%序列同一性。下文还公开了所述cdr区的氨基酸序列。
[0118]
flt3-1重链可变区多核苷酸序列:caggtccaactgcagcagcctggggctgagcttgtgaagcctggggcttcattgaagctgtcctgcaagtcttccgggtacaccttcaccagctactggatgcactgggtgaggcagaggcctggacatggccttgagtggatcggagagattgatccttctgacagttataaagactacaatcagaagttcaaggacaaggccacattgactgtggacagatcctccaacacagcctacatgcacctcagcagcctgacatctgatgactctgcggtctattattgtgcaagagcgattacgacgaccccctttgacttctggggccaaggcaccactctcacagtctcctca (seq id no: 105),以及任选地其等效物。
[0119]
flt3-1轻链可变区多核苷酸序列:gatattgtgctaactcagtctccagccaccctgtctgtgactccaggagatagcgtcagtctttcctgcagggccagccagagtattagcaacaacctacactggtatcaacaaaaatcacatgagtctccaaggcttctcatcaagtatgcttcccagtccatctctgggatcccctccaggttcagtggcagtggatcagggacagatttcactctcagtatcaacagtgtggagactgaagattttggagtgtatttctgtcaacagagtaacacctggccgtacacgttcggaggggggaccaagctggaaataaaacgg (seq id no: 103),以及任选地其等效物。
[0120]
flt3-1 cdhr1: sywmh (seq id no: 21),以及任选地其等效物。
[0121]
flt3-1 cdhr2: eidpsdsykdynqkfkd (seq id no: 23),以及任选地其等效物。
[0122]
flt3-1 cdhr3: aitttpfdf (seq id no: 25),以及任选地其等效物。
[0123]
flt3-1 cdlr1: rasqsisnnlh (seq id no: 15),以及任选地其等效物。
[0124]
flt3-1 cdlr2: yasqsis (seq id no: 17),以及任选地其等效物。
[0125]
flt3-1 cdlr3: qqsntwpyt (seq id no: 19),以及任选地其等效物。
[0126]
flt3 cdr结构域氨基酸序列的其他非限制性示例描述于:美国专利申请号us20180346601的表1-4、美国专利申请号us20180037657的表v、美国专利申请号us20170037149的表10、美国专利申请号us20160272716的表v、美国专利申请号us20110091470的表1-3和美国专利申请号us20090297529的表1-3。
[0127]
flt3重链可变区和轻链可变区氨基酸序列的非限制性示例描述于:美国专利申请号us2018034601的表1和表3、美国专利申请号us20180037657的表x、美国专利申请号us20170037149的表10和美国专利申请号us20160272716的表vii。
[0128]
如本文所用,术语flt3-2是指包含具有cdr的氨基酸序列的抗体,所述cdr与在下文公开的重链和轻链多核苷酸序列中编码的cdr中的任何一个(优选地以下cdr3区中的至少一个、最优选地以下两个cdr3区)具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%序列同一性。下文还公开了所述cdr区的氨基酸序列。
[0129]
flt3-2重链可变区序列:caggtgcagctgaagcagtcaggacctggcctagtgcagccctcacagagcctgtccatcacctgcacagtctctggtttctcattaactaactatggtttacactgggttcgccagtctccaggaaagggcctggagtggctgggagtgatatggagtggtggaagcacagactataatgcagctttcatatccagactgagcatcagcaaggacaactccaagagccaagttttctttaaaatgaacagtctgcaggctgatgacacagccatatactactgtgccagaaaaggagggatctactatgctaaccattactatgctatggactactggggtcaaggaacctcagtcaccgtctcctca (seq id no: 106),以及任选地其等效物。
[0130]
flt3-2轻链可变区序列:gacattgtgatgacacagtctccatcctccctgagtgtgtcagcaggagagaaggtcactatgagctgcaagtccagtcagagtctgttaaacagtggaaatcaaaagaactatatggcctggtatcagcagaaaccagggcagcctcctaaactgttgatctacggggcatccactagggaatctggggtccctgatcgcttcacaggcagtggatctggaaccgatttcactcttaccatcagcagtgtgcaggctgaagacctggcagtttattactgtcagaatgatcatagttatccgctcacgttcggtgctgggaccaagctggagctgaaacgg (seq id no: 104),以及任选地其等效物。
[0131]
flt3-2 cdhr1: nyglh (seq id no: 22),以及任选地其等效物。
[0132]
flt3-2 cdhr2: viwsggstdynaafis (seq id no: 24),以及任选地其等效物。
[0133]
flt3-2 cdhr3: ggiyyanhyyamdy (seq id no: 26),以及任选地其等效物。
[0134]
flt3-2 cdlr1: kssqsllnsgnqknym (seq id no: 16),以及任选地其等效物。
[0135]
flt3-2 cdlr2: gastres (seq id no: 18),以及任选地其等效物。
[0136]
flt3-2 cdlr3: qndhsyplt (seq id no: 20),以及任选地其等效物。
[0137]
flt3抗体的非限制性示例包括以下序列,或基本上由其组成,或由其组成:重链可变区,其包括:cdhr1,其具有氨基酸序列(sywmh, seq id no: 21)或(nyglh, seq id no: 22)或其每一个的等效物,cdhr2,其具有氨基酸序列(eidpsdsykdynqkfkd, seq id no: 23)或(viwsggstdynaafis, seq id no: 24)或其每一个的等效物,以及cdhr3,其具有氨基酸序列(aitttpfdf, seq id no: 25)或(ggiyyanhyyamdy, seq id no: 26)或其每一个的等效物;和/或轻链可变区,其包含:cdlr1,其具有氨基酸序列(rasqsisnnlh, seq id no: 15)或(kssqsllnsgnqknym, seq id no: 16)或其每一个的等效物,cdlr2,其具有氨基酸序列(yasqsis, seq id no: 17)或(gastres, seq id no: 18)或其每一个的等效物,以及cdlr3,其具有所述氨基酸序列(qqsntwpyt, seq id no: 19)或(qndhsyplt, seq id no: 20)或其每一个的等效物。在一方面,flt3 car由ef1 α启动子ef1α驱动。
[0138]
首字母缩写“egfr”表示表皮生长因子受体。egfr也称为erbb-1和her1。它是细胞表面受体的表皮生长因子家族的细胞表面受体。术语“egfr”还指与该名称相关的特定的蛋白质片段,以及与本文所公开的egfr的任何同种型具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%氨基酸序列同一性的具有类似的生物功能的任何其他分子。同种型1为典型序列;因此,以下所有位置信息均指下文公开的氨基酸序列。
[0139]
egfr同种型1,uniprot p00533-1:mrpsgtagaallallaalcpasraleekkvcqgtsnkltqlgtfedhflslqrmfnncevvlgnleityvqrnydlsflktiqevagyvlialntveriplenlqiirgnmyyensyalavlsnydanktglkelpmrnlqeilhgavrfsnnpalcnvesiqwrdivssdflsnmsmdfqnhlgscqkcdpscpngscwgageencqkltkiicaqqcsgrcrgkspsdcchnqcaagctgpresdclvcrkfrdeatckdtcpplmlynpttyqmdvnpegkysfgatcvkkcprnyvvtdhgscvracgadsyemeedgvrkckkcegpcrkvcngigigefkdslsinatnikhfknctsisgdlhilpvafrgdsfthtppldpqeldilktvkeitgflliqawpenrtdlhafenleiirgrtkqhgqfslavvslnitslglrslkeisdgdviisgnknlcyantinwkklfgtsgqktkiisnrgensckatgqvchalcspegcwgpeprdcvscrnvsrgrecvdkcnllegeprefvenseciqchpeclpqamnitctgrgpdnciqcahyidgphcvktcpagvmgenntlvwkyadaghvchlchpnctygctgpglegcptngpkipsiatgmvgalllllvvalgiglfmrrrhivrk
rtlrrllqerelvepltpsgeapnqallrilketefkkikvlgsgafgtvykglwipegekvkipvaikelreatspkankeildeayvmasvdnphvcrllgicltstvqlitqlmpfgclldyvrehkdnigsqyllnwcvqiakgmnyledrrlvhrdlaarnvlvktpqhvkitdfglakllgaeekeyhaeggkvpikwmalesilhriythqsdvwsygvtvwelmtfgskpydgipaseissilekgerlpqppictidvymimvkcwmidadsrpkfreliiefskmardpqrylviqgdermhlpsptdsnfyralmdeedmddvvdadeylipqqgffsspstsrtpllsslsatsnnstvacidrnglqscpikedsflqryssdptgaltedsiddtflpvpeyinqsvpkrpagsvqnpvyhnqplnpapsrdphyqdphstavgnpeylntvqptcvnstfdspahwaqkgshqisldnpdyqqdffpkeakpngifkgstaenaeylrvapqssefiga (seq id no: 129)。
[0140]
结合位点包括但不限于位置745和855;活性位点包括但不限于位置837;以及其他感兴趣的位点包括但不限于位置1016。egfr同种型2(uniprot p00533-2)在位置404到405具有fl到ls取代,并且缺失了位置406到1210的区域。egfr同种型4(uniprot p00533-4)在位置628具有c到s的取代,并且缺失了位置629到1210的区域。egfr同种型3(uniprot p00533-3)位置628至705不同,并根据以下序列缺失位置706至1210的区域。
[0141]
egfr同种型3,uniprot p00533-3:mrpsgtagaallallaalcpasraleekkvcqgtsnkltqlgtfedhflslqrmfnncevvlgnleityvqrnydlsflktiqevagyvlialntveriplenlqiirgnmyyensyalavlsnydanktglkelpmrnlqeilhgavrfsnnpalcnvesiqwrdivssdflsnmsmdfqnhlgscqkcdpscpngscwgageencqkltkiicaqqcsgrcrgkspsdcchnqcaagctgpresdclvcrkfrdeatckdtcpplmlynpttyqmdvnpegkysfgatcvkkcprnyvvtdhgscvracgadsyemeedgvrkckkcegpcrkvcngigigefkdslsinatnikhfknctsisgdlhilpvafrgdsfthtppldpqeldilktvkeitgflliqawpenrtdlhafenleiirgrtkqhgqfslavvslnitslglrslkeisdgdviisgnknlcyantinwkklfgtsgqktkiisnrgensckatgqvchalcspegcwgpeprdcvscrnvsrgrecvdkcnllegeprefvenseciqchpeclpqamnitctgrgpdnciqcahyidgphcvktcpagvmgenntlvwkyadaghvchlchpnctygpgneslkamlfclfklsscnqsndgsvshqsgspaaqesclgwipsllpsefqlgwggcshlhawpsasviitassch (seq id no: 130)。
[0142]
egfrviii是egfr的一种突变体形式,据报道其在相当比例的多形性胶质母细胞瘤(gb)患者中表达。gan et al. 205350-5370报告,所述突变体形式也在其他肿瘤中表达。术语“突变体egfr”可指egfrviii或与该名称相关的特定的蛋白质片段,以及与egfrviii具有至少70%、或至少80%氨基酸序列同一性、优选地90%序列同一性、更优选地至少95%氨基酸序列同一性的具有类似的生物功能的任何其他分子,如本文所示或本文进一步定义的等效物。
[0143]
egfrviii, uniprot p00533[30-297]:mrpsgtagaa llallaalcp asraleekkv cqgtsnkltq lgtfedhfls lqrmfnncev vlgnleityv qrnydlsflk tiqevagyvl ialntveriplenlqiirgn myyensyala vlsnydankt glkelpmrnl qeilhgavrf snnpalcnve siqwrdivss dflsnmsmdf qnhlgscqkc dpscpngscwgageencqkl tkiicaqqcs grcrgkspsd cchnqcaagc tgpresdclv crkfrdeatc kdtcpplmly npttyqmdvn pegkysfgat cvkkcprnyv vtdhgscvra cgadsyemee dgvrkckkce gpcrkvcngi gigefkdsls inatnikhfk nctsisgdlh ilpvafrgds fthtppldpq eldilktvke itgflliqaw penrtdlhaf enleiirgrt kqhgqfslav vslnitslgl rslkeisdgd viisgnknlc yantinwkklfgtsgqktkiisnrgensckatgqvchalcspegcwgpeprdcvscrnvsrgrecvdkcn
llegeprefvenseciqchpeclpqamnitctgrgpdnciqcahyidgphcvktcpagvmgenntlvwkyadaghvchlchpnctygctgpglegcptngpkipsiatgmvgalllllvvalgiglfmrrrhivrkrtlrrllqerelvepltpsgeapnqallrilketefkkikvlgsgafgtvykglwipegekvkipvaikelreatspkankeildeayvmasvdnphvcrllgicltstvqlitqlmpfgclldyvrehkdnigsqyllnwcvqiakgmnyledrrlvhrdlaarnvlvktpqhvkitdfglakllgaeekeyhaeggkvpikwmalesilhriythqsdvwsygvtvwelmtfgskpydgipaseissilekgerlpqppictidvymimvkcwmidadsrpkfreliiefskmardpqrylviqgdermhlplmdeedmddvvdadeylipqqgffsspstsrtpllsslsatsnnstvacidrnglqscpikedsflqryssdptgaltedsiddtflpvpeyinqsvpkrpagsvqnpvyhnqplnpapsrdphyqdphstavgnpeylntvqptcvnstfdspahwaqkgshqisldnpdyqqdffpkeakpngifkgstaenaeylrvapqssefiga(seqidno:131)。
[0144]
术语“突变体egfr”还可指egfr的任何同种型的自然变体,包括但不限于具有以下一种或多种突变的变体:位置98的r至q、位置266的p至r、位置428的g至d、位置521的r至k、位置674的v至i、位置709的e至a、位置709的e至g、位置709的e至k、位置719的g至a、位置719的g至c、位置719的g至d、位置719的g至s、位置724的g至s、位置734的e至k、位置746至752的elreats(seqidno:172)至d、位置746至751的elreat(seqidno:173)至a、位置746至750的缺失、位置746的缺失、位置747至751的缺失、位置747至749的缺失、位置747的l至f、位置748的r至p、位置752至759的缺失、位置768的s至i、位置769的v至m、位置787的q至r、位置790的t至m、位置833的l至v、位置834的v至l、位置835的h至l、位置838的l至v、位置858的l至m、位置858的l至r、位置861的l至q、位置873处的g至e、位置962的r至g、位置988的h至p、位置1034的l至r、位置1210的a至v、和/或任一特定位置处的不同氨基酸的取代或缺失。
[0145]
在一些实施方式中,抗体的重链可变区包括以下多肽序列,或基本上由其组成,或由组成:qvqlqqsgsemarpgasvklpckasgdtftsywmhwvkqrhghgpewigniypgsggtnyaekfknkvtltvdrssrtvymhlsrltsedsavyyctrsggpyffdywgqgttltvss(seqidno:45),或其等效物,或由多核苷酸编码的多肽:gacattctaatgacccaatctccactctccctgcctgtcagtcttggagatcaagcctcctacctgcaaaggccaggccagtctccaaagctcctgatctacaaagtttccgaccgattttacctgcaaaggccaggccagtctccaaagctcctgatctacaaagtttccgaccgattttctggggtcccagacaggttcagtggcagtggatcagggacagatttcacactcaagatcagcagagtagaggctgaggatctgggaatttattactgctttcaaggttcacatattcctcccacgttcggaggggggaccaagctggaaatcaaacgtgcggcc(seqidno:132),或其等效物。
[0146]
所述多肽或其每一个的等效物可在羧基末端后跟另外的50个氨基酸、或约40个氨基酸、或约30个氨基酸、或约20个氨基酸、或约10个氨基酸、或约5个氨基酸、或约4个、或3个、或2个或1个氨基酸。
[0147]
在其他方面,lc可变区包括以下多肽序列,或基本上由其组成,或由其组成:dilmtqsplslpvslgdqasiscrssqnivhnngitylewylqrpgqspklliykvsdrfsgvpdrfsgsgsgtdftlkisrveaedlgiyycfqgshipptfgggtkleikr
aa(seqidno:43),或其等效物,或由多核苷酸编码的多肽:caggtccagctgcagcagtctgggtctgagatggcgaggcctggagcttcagtgaagctgccctgcaaggcttctggcgacacattcaccagttactggatgcactgggtgaagcagaggcatggacatggccctgagtggatcggaaatatttatccaggtagtggtggtactaactacgctgagaagttcaagaacaaggtcactctgactgtagacaggtcctcccgcacagtctacatgcacctcagcaggctgacatctgaggactctgcggtctattattgtacaagatcggggggtccctacttctttgactactggggccaaggcaccactctcacagtctcctcc(seqidno:133),或其等效物。
[0148]
所述多肽或其每一个的等效物可在羧基末端后跟另外的50个氨基酸、或约40个氨基酸、或约30个氨基酸、或约20个氨基酸、或约10个氨基酸、或约5个氨基酸、或约4个、或3个、或2个或1个氨基酸。
[0149]
其等效物包括与car具有至少80%的氨基酸同一性的多肽或由在高度严格条件下与编码car的多核苷酸的补体杂交的多核苷酸编码的多肽,其中所述高度严格条件包括约55℃至约68℃的孵育温度;约1xssc至约0.1xssc的缓冲液浓度;约55%至约75%的甲酰胺浓度;以及约1xssc、0.1xssc的洗涤液或去离子水。
[0150]
可选的实施方案包括来自lc可变区的一个或多个cdr(例如,cdr1、cdr2、cdr3)和来自其他egfr抗体cdr的适当cdr,及其每一个的等效物。因此,作为示例,来自lc可变区的cdr1和cdr2可以与另一种抗egfr抗体的lc可变区的cdr3结合,并且在一些方面,可以在羧基末端包括另外的50个氨基酸、或约40个氨基酸、或约30个氨基酸、或约20个氨基酸、或约10个氨基酸、或约5个氨基酸、或约4个、或3个、或2个或1个氨基酸。在另一方面,egfrcar是wo2016/164370中公开的car。
[0151]“组合物”通常是指活性剂(例如化合物或组合物)和天然存在或非天然存在的载体的组合,所述载体是惰性的(例如,可检测试剂或标签)或活性的(例如佐剂、稀释剂、粘合剂、稳定剂、缓冲剂、盐、亲脂性溶剂、防腐剂、佐剂等),并包括药学上可接受的载体。载体还包括药物赋形剂和添加剂蛋白质、肽、氨基酸、脂质和碳水化合物(例如糖,包括单糖、二寡糖、三寡糖、四寡糖和寡糖;衍生的糖,如糖醇、醛糖酸、酯化糖等;以及多糖或糖聚合物),其可以单独地或组合地存在,以重量或体积计单独地或组合地包括1-99.99%。示例性的蛋白质赋形剂包括血清白蛋白(例如人血清白蛋白(hsa)、重组人白蛋白(rha))、明胶、酪蛋白等。还具有缓冲能力的代表性的氨基酸/抗体组分包括丙氨酸、精氨酸、甘氨酸、精氨酸、甜菜碱、组氨酸、谷氨酸、天冬氨酸、半胱氨酸、赖氨酸、亮氨酸、异亮氨酸、缬氨酸、甲硫氨酸、苯丙氨酸、阿斯巴甜等。碳水化合物赋形剂也旨在在本技术的范围之内,其实例包括但不限于:单糖,例如果糖、麦芽糖、半乳糖、葡萄糖、d-甘露糖、山梨糖等;双糖,例如乳糖、蔗糖、海藻糖、纤维二糖等;多糖,例如棉子糖、松三糖、麦芽糖糊精、葡聚糖、淀粉等;以及糖醇,例如甘露糖醇、木糖醇、麦芽糖醇、乳糖醇、木糖醇山梨醇(葡萄糖醇)和肌醇。
[0152]
如本文所用,术语“包括/包含/含有”旨在表示组合物和方法包括所述的元素但不排除其他元素。“基本上由
……
组成”当被用来定义组合物和方法时,应该表示排除对于预期用途的组合来说具有任何实质性作用的其他元素。例如,如本文定义的基本上由该元素组成的组合物,将不会从分离和纯化方法中排除微量污染物和药学上可接受的载体(例如磷酸盐缓冲盐、防腐剂等)。“由
……
组成”应该表示排除多于微量元素的其他成分和用于施用本文公开的组合物的实质性方法步骤。通过这些过渡性术语的每一个进行定义的方面都
在本公开的范围内。
[0153]
如本文所用,术语“共有序列”是指这样的氨基酸或核酸序列,其是通过比对一系列多个序列而确定的,并定义了代表在多个序列的每个相应位置的主要氨基酸或碱基选择的理想序列。取决于一系列多个序列的序列,该系列的共有序列可以与每个序列相差零个、一个、几个或多个取代。而且,取决于一系列多个序列的序列,可以为该系列确定一个以上的共有序列。共有序列的生成已经过深入的数学分析。各种软件程序可用于确定共有序列。
[0154]
如本文所用,术语“crispr”是指依赖于聚集的规则间隔的短回文重复途径的序列特异性遗传操作技术。crispr可用于执行基因编辑和/或基因调节,以及简单地将蛋白质靶向特定的基因组位置。基因编辑是指一种基因工程,其中通过将缺失、插入或碱基取代引入多核苷酸序列来改变靶多核苷酸的核苷酸序列。在一些方面,crispr介导的基因编辑利用非同源末端连接(nhej)或同源重组的途径来进行编辑。基因调控是指增加或减少特定基因产物(如蛋白质或rna)的产生。
[0155]
如本文所用,术语“grna”或“向导rna”指用于靶向特定基因以利用crispr技术进行校正的向导rna序列。设计用于靶向特异性的grna和供体治疗性多核苷酸的技术是本领域众所周知的。例如,doench, j., et al. nature biotechnology 2014; 32(12):1262-7, mohr, s. et al. (2016) febs journal 283: 3232-38, 和graham, d., et al. genome biol. 2015; 16: 260。grna包含以下多核苷酸,或基本上由其组成,或由其组成:融合多核苷酸,其包含crispr rna(crrna)和反式激活cripsr rna(tracrrna);或多核苷酸,其包含crispr rna(crrna)和反式激活cripsr rna(tracrrna)。在一些方面,grna是合成的(kelley, m. et al. (2016) j of biotechnology 233 (2016) 74-83)。如本文所用,grna的生物学等效物包括但不限于可以将cas9或其等效物引导至特定核苷酸序列(例如细胞基因组的特定区域)的多核苷酸或靶向分子。
[0156]
如本文所用,“细胞减少疗法”包括但不限于化学疗法、冷冻疗法和放射疗法。起到减少细胞增殖作用的试剂是本领域已知的并且被广泛使用。仅在其分裂时杀死癌细胞的化学疗法药物称为细胞周期特异性药物。这些药物包括在s期起作用的药物,包括拓扑异构酶抑制剂和抗代谢物。
[0157]
拓扑异构酶抑制剂是干扰拓扑异构酶(拓扑异构酶i和ii)的作用的药物。在化学疗法过程中,拓扑异构酶控制复制所需的dna结构的操纵,因此具有细胞周期特异性。拓扑异构酶i抑制剂的示例包括如上列出的喜树碱类似物、伊立替康(irinotecan)和拓扑替康(topotecan)。拓扑异构酶ii抑制剂的示例包括安吖啶(amsacrine)、依托泊苷(etoposide)、依托泊苷磷酸和替尼泊苷(teniposide)。
[0158]
抗代谢物通常是正常代谢底物的类似物,经常会干扰染色体复制过程。它们在周期的非常特定的阶段攻击细胞。抗代谢药物包括:叶酸拮抗剂,例如甲氨蝶呤;嘧啶拮抗剂,例如5-氟尿嘧啶、氟尿苷(foxuridine)、阿糖胞苷、卡培他滨(capecitabine)和吉西他滨(gemcitabine);嘌呤拮抗剂,例如6-巯基嘌呤和6-硫鸟嘌呤;腺苷脱氨酶抑制剂,例如克拉屈滨(cladribine)、氟达拉滨(fludarabine)、奈拉滨(nelarabine)和喷司他丁(pentostatin);等等。
[0159]
植物生物碱衍生自某些类型的植物。长春花生物碱由长春花植物(catharanthus rosea)制成。紫杉烷由太平洋紫衫树(taxus)的树皮制成。长春花生物碱和紫杉烷类也被称
为抗微管剂。鬼臼毒素来自五月苹果植物。喜树碱类似物源自亚洲的“快乐树”(camptotheca acuminata)。鬼臼毒素和喜树碱类似物也被分类为拓扑异构酶抑制剂。植物生物碱通常是细胞周期特异性的。
[0160]
这些试剂的示例包括长春花生物碱,例如长春新碱(vincristine)、长春碱(vinblastine)和长春瑞滨(vinorelbine);紫杉烷类,例如紫杉醇和多西他赛(docetaxel);鬼臼毒素,例如依托泊苷和替尼索德(tenisopide);以及喜树碱类似物,例如伊立替康(irinotecan)和拓扑替康(topotecan)。
[0161]
冷冻疗法包括但不限于涉及降低温度的疗法,例如低温疗法。
[0162]
辐射疗法包括但不限于暴露于辐射,例如本领域已知的辐射,例如电离辐射、uv辐射。示例性剂量包括但不限于至少约2 gy至不超过约10 gy的电离辐射剂量和/或至少约5 j/ m2至不超过约50 j/m2(通常约10 j/ m2)的紫外辐射剂量。
[0163]“可检测的标签”、“标签”、“可检测的标记物”或“标记物”可互换使用,包括但不限于放射性同位素、荧光染料、化学发光化合物、染料和蛋白质(包括酶)。可检测的标签也可以被连接至本文所述的多核苷酸、多肽、抗体或组合物。
[0164]
如本文所用,术语“可检测的标记物”是指能够直接或间接产生可检测的信号的至少一个标记物。该标记物的非穷举性的列表包括酶,其例如通过比色、荧光、发光制造可检测的信号,例如辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、葡萄糖-6-磷酸脱氢酶、生色团(例如荧光剂、发光染料)、带有通过电子显微镜或通过其电性质(例如导电率、电流分析、伏安法、阻抗)检测的电子密度的基团、可检测的基团,例如其分子具有足够的大小来诱导其物理和/或化学性质上的可检测的修饰,此类检测可以通过光学方法(例如衍射、表面等离子体共振、表面变化、接触角变化)或物理方法(例如原子力谱、隧道效应、或放射性分子(例如
32
p、
35
s或
125
i))完成。该术语还包括与多核苷酸偶联的序列,其将在插入序列的表达时提供信号,例如绿色荧光蛋白(gfp)等。标签自身可以是可检测的(例如放射性同位素标签或荧光标签),或者在酶标签的情况下,可催化可检测的底物化合物或组合物的化学改变。标签可适用于小规模检测,或更适用于高通量筛选。因此,合适的标签包括但不限于磁活性同位素、非放射性同位素、放射性同位素、荧光染料、化学发光化合物、染料和蛋白质(包括酶)。可以简单地检测标签,也可以对其进行量化。简单地检测的反应通常包括其存在仅被确认的反应,而被量化的反应通常包括具有可量化(例如,可用数字报告的)值的反应应,例如强度、偏振和/或其他特性。在发光或荧光分析中,可直接使用与实际参与结合的分析组分相关的发光体或荧光团,或间接使用与另一个(例如,报告基因或指示剂)组分相关的发光体或荧光团,生成可检测反应。产生信号的发光标签的示例包括但不限于生物发光和化学发光。可检测的发光反应通常包括发光信号的变化或出现。本领域已知用于发光标记分析成分的合适的方法和发光体,例如如haugland, richard p. (1996) handbook of fluorescent probes and research chemicals (6th ed)中所述。发光探针的示例包括但不限于水母发光蛋白和荧光素酶。
[0165]
如本文所用,术语“免疫偶联物”包括与第二试剂(例如细胞毒性试剂、可检测试剂、放射性试剂、靶向试剂、人类抗体、人源化抗体、嵌合抗体、合成抗体、半合成抗体或多特异性抗体)相关或连接的抗体或抗体衍生物。
[0166]
合适的荧光标签的示例包括但不限于荧光素、罗丹明、四甲基罗丹明、曙红、赤藓
红、香豆素、甲基香豆素、芘、孔雀石绿、二苯乙烯、路西法黄、cascade蓝
™
, 还有德克萨斯红。其他合适的光学染料如haugland, richard p. (1996) handbook of fluorescent probes and research chemicals (6th ed.)中所述。
[0167]
在另一方面,荧光标签被官能化以促进与细胞或组织表面中或表面上存在的细胞成分(例如细胞表面标记物)的共价连接。合适的官能团包括但不限于异硫氰酸酯基、氨基、卤代乙酰基、马来酰亚胺、琥珀酰亚胺酯和磺酰卤化物,所有这些都可以被用于将荧光标签连接到第二分子。荧光标签的官能团的选择取决于接头、试剂、标记物或第二标签试剂的连接位点。
[0168]“有效量”或“有效的量”是指该量的试剂或合并的量的两种或更多种试剂在被施用来治疗哺乳动物或其他对象时,足以影响对疾病的这种治疗。“有效量”将会根据试剂、疾病及其严重程度以及待治疗对象的年龄、体重等而发生变化。
[0169]
在一些实施方式中,组分名称中的术语“第一”、“第二”、“第三”、“第四”或类似术语用于区分和识别在其名称中共享特定标识的多个组分。例如,在整个说明书中使用“第一taa”和“第二taa”来区分两种taa,并且在一些实施方式中,第一taa是由本文公开的car识别并结合的taa,而第二taa是由本文公开的双特异性抗体识别并结合的taa。
[0170]
术语“编码”在被应用至核酸序列时是指,被陈述来“编码”多肽的多核苷酸,以其天然状态或者在通过本领域技术人员熟知的方法操作时,可以被转录和/或翻译来产生用于该多肽和/或其片段的mrna。反义链是这种核酸的互补序列,并且编码序列可以由此推导出。
[0171]
如本文所用,术语“增强子”,是指不管其相对于要被表达的核酸序列的位置和方向,都增强、改善或改良核酸序列的转录的序列元件。增强子可以增强来自单一启动子的转录,或者同时增强来自一个以上的启动子的转录。只要保留或基本上保留该改善转录的功能(例如至少70%、至少80%、至少90%或至少95%的野生型活性,即全长序列的活性),则野生型增强子序列的任何截断的、突变的或以其他方式修饰的变体也在上述定义范围内。
[0172]
一个方面,术语抗体的“等效物”或“生物等效物”是指抗体如通过elisa或其他合适的方法测定地选择性结合其表位蛋白质或其片段的能力。生物等效的抗体包括但不限于与参考抗体结合到相同的表位的抗体、肽、抗体片段、抗体变体、抗体衍生物和抗体模拟物。
[0173]
在没有明确描述的情况下应该推断、并且除非另有说明,否则当本公开涉及多肽、蛋白质、多核苷酸或抗体时,这样的等效物或生物等效物旨在落入本公开的范围内。如本文所用,当提及参考蛋白质、抗体、多肽或核酸时,术语“其生物等效物”旨在与“其等效物”是同义的,是指具有最小的同源性,同时仍然保持期望的结构或功能。除非本文具体说明,否则可以预期的是,本文提及的任何多核苷酸、多肽或蛋白质还包括其等效物。例如,等效物是指与参考蛋白质、多肽或核酸具有至少约70%同源性或同一性、或至少80%同源性或同一性、或至少约85%、或至少约90%、或至少约95%、或98%百分比同源性或同一性并且表现出基本上等效的生物活性。替代地,当提及多核苷酸时,其等效物是在严格条件下与参考多核苷酸或其互补序列杂交的多核苷酸。
[0174]
多核苷酸或多核苷酸区域(或多肽或多肽区域)与另一个序列具有一定百分比(例如,80%、85%、90%或95%)的“序列同一性”意味着,当对齐时,该百分比的碱基(或氨基酸)在两个序列的比较中是相同的。可以使用本领域已知的软件程序来确定对齐和同源性或序列
spupdate + pir。这些程序的详细信息可以在以下网址找到:ncbi.nlm.nih.gov/cgi-bin/blast。术语“同源性”或“相同的”、
ꢀ“
同一性”或“相似性”百分比还表示、或者可以被应用至测试序列的互补序列。所述术语还包括具有缺失和/或插入、以及具有取代的序列。如本文所述,优选的算法可以解释间隙等。优选地,在长度至少为约25个氨基酸或核苷酸的区域上、或者更优选地在长度至少为50-100个氨基酸或核苷酸的区域上存在同一性。“不相关的”或“非同源的”序列与本文所公开的序列中的一个具有小于40%的同一性、或者小于25%的同一性。
[0181]“杂交”是指其中一个或多个多核苷酸反应来形成复合物,并且该复合物通过核苷酸残基的碱基之间的氢键结合而被稳定的反应。可以通过watson-crick碱基配对、hoogstein结合或通过任何其他序列特异性的方式发生氢键结合。所述复合物可以包括形成双螺旋结构的两条链、形成多链复合物的三条或更多条链、单一的自我杂交的链、或这些的任何组合。杂交反应可以由在更广泛的过程中的步骤组成,例如pcr过程的起始步骤、或者通过核酶进行的多核苷酸的酶切步骤。
[0182]
严格杂交条件的示例包括:约25℃至约37℃的孵育温度;约6x ssc至约10x ssc的杂交缓冲液浓度;约0%至25%的甲酰胺浓度;以及约4x ssc至约8x ssc 的洗涤溶液。中等杂交条件的示例包括:约40℃至约50℃的孵育温度;约9x ssc至约2x ssc的缓冲液浓度;约30%至50%的甲酰胺浓度;以及约5x ssc至2x ssc的洗涤溶液。高严格条件的示例包括:约55℃至约68℃的孵育温度;约1x ssc至约0.1x ssc的缓冲液浓度;约55%至75%的甲酰胺浓度;以及约1x ssc、0.1x ssc的洗涤溶液、或去离子水。一般来说,杂交孵育时间为5分钟至24小时,具有1、2或更多个洗涤步骤,洗涤孵育时间为约1、2或15分钟。ssc是0.15 m nacl和15 mm柠檬酸盐缓冲液。应该理解的是,可以采用使用其他缓冲系统的ssc的等效物。
[0183]
如本文所用,术语“分离的”是指,分子或生物体或细胞材料基本上不含其他材料。在一方面,术语“分离的”是指,核酸(例如dna或rna)或蛋白质或多肽(例如抗体或其衍生物)或细胞或细胞器、或组织或器官与存在于自然来源中的其他dna或rna、或蛋白质或多肽、或细胞或细胞器、或组织或器官分离。术语“分离的”还指,核酸或肽基本上不含细胞材料、病毒材料、或培养基(当通过重组dna技术生产时)、或化学前体或其他化学品(当化学合成时)。再者,“分离的核酸”旨在包括天然地不形成为片段并且不会在天然状态下发现的核酸片段。术语“分离的”在本文中还被用来指从其他细胞蛋白质分离的多肽,并且旨在包括纯化的和重组的多肽。术语“分离的”在本文中还被用来指从其他细胞分离的细胞或组织,并且旨在包括培养的和工程化的细胞或组织。
[0184]
如本文所用,术语“分离的细胞”通常是指基本上与组织的其他细胞分离的细胞。
[0185]
在一些实施方式中,术语“工程化的”或“重组的”是指具有至少一种通常在参考物种的天然存在的蛋白质、多肽、多核苷酸、菌株、野生型菌株或亲本宿主菌株中不存在的修饰。在一些实施方式中,术语“工程化的”或“重组的”是指通过人类干预合成的。
[0186]“免疫细胞”包括衍生自在骨髓中产生的造血干细胞(hsc)的白血细胞(白细胞)、淋巴细胞(t细胞、b细胞、自然杀伤(nk)细胞)和骨髓来源的细胞(嗜中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、单核细胞、巨噬细胞、树突状细胞)。
[0187]
如本文所用,术语“接头序列”、“接头肽”和“接头多肽”可互换使用,是指任何这样的氨基酸序列,其包含可以被重复1至10、或至约8、或至约6、或至约5、或4、或3、或2次的1至
10个、或8个氨基酸、或6个氨基酸、或5个氨基酸。例如,接头可以包含由重复三次的五肽组成的多达15个氨基酸残基。在一方面,接头序列是包括gly-gly-gly-gly-ser(seqidno:134)的三个拷贝的(甘氨酸4丝氨酸)3(seqidno:14)柔性多肽接头。
[0188]“对应于肿瘤组织类型的正常细胞”是指来自与肿瘤组织相同组织类型的正常细胞。非限制性示例是患有肺肿瘤的患者的正常肺细胞、或没有患有肺癌的患者的肺组织、或患有结肠肿瘤的患者的正常结肠细胞。
[0189]
如本文所用,术语“t细胞”是指在胸腺中成熟的一种淋巴细胞。t细胞在细胞介导的免疫中起重要作用,并且与其他淋巴细胞(例如b细胞)的不同点在于细胞表面上存在t细胞受体。t细胞可以是被分离的,也可以从商业上可获得的来源得到。“t细胞”包括表达cd3的所有类型的免疫细胞,包括t辅助细胞(cd4+细胞)、细胞毒性t细胞(cd8+细胞)、自然杀伤t细胞、t调节细胞(treg)和γ-δt细胞。“细胞毒性细胞”包括cd8+t细胞、自然杀伤(nk)细胞和嗜中性粒细胞,这些细胞能够介导细胞毒性反应。商业上可获得的t细胞系的非限制性示例包括bcl2(aaa)jurkat(atcc
®
crl-2902
™
)、bcl2(s70a)jurkat(atcc
®
crl-2900
™
)、bcl2(s87a)jurkat(atcc
®
crl-2901
™
)、bcl2jurkat(atcc
®
crl-2899
™
)、neojurkat(atcc
®
crl-2898
™
)、tall-104细胞毒性人类t细胞系(atcc#crl-11386)细胞系。进一步的示例包括但不限于成熟的t细胞系,例如deglis、ebt-8、hpb-mlp-w、hut78、hut102、karpas384、ki225、my-la、se-ax、skw-3、smz-1和t34;以及未成熟的t细胞系,例如all-sil、be13、ccrf-cem、cml-t1、dnd-41、du.528、eu-9、hd-mar、hpb-all、h-sb2、ht-1、jk-t1、jurkat、karpas45、ke-37、kopt-k1、k-t1、l-kaw、loucy、mat、molt-1、molt3、molt-4、molt13、molt-16、mt-1、mt-all、p12/ichikawa、peer、per0117、per-255、pf-382、pfi-285、rpmi-8402、st-4、sup-t1至t14、tall-1、tall-101、tall-103/2、tall-104、tall-105、tall-106、tall-107、tall-197、tk-6、tlbr-1、-2、-3和-4、ccrf-hsb-2(ccl-120.1)、j.rt3-t3.5(atcctib-153)、j45.01(atcccrl-1990)、j.cam1.6(atcccrl-2063)、rs4;11(atcccrl-1873)、ccrf-cem(atcccrm-ccl-119);和皮肤t细胞淋巴瘤细胞系,例如hut78(atcccrm-tib-161)、mj[g11](atcccrl-8294)、hut102(atcctib-162)。无白血病(nullleukemia)细胞系,包括但不限于reh、nall-1、km-3、l92-221,是免疫细胞的另一种商业上可获得的来源,同样的是衍生自其他白血病和淋巴瘤的细胞系,例如k562红白血病、thp-1单核细胞白血病、u937淋巴瘤、hel红白血病、hl60白血病、hmc-1白血病、kg-1白血病、u266骨髓瘤。这样的商业上可获得的细胞系的非限制性示例性来源包括美国类型培养保藏中心或atcc(http://www.atcc.org/)以及德国微生物和细胞培养物保藏中心(https://www.dsmz.de/)。
[0190]
如本文所用,术语“nk细胞”(也被称为自然杀伤细胞)是指起源于骨髓并且在先天免疫系统中起重要作用的一类淋巴细胞。nk细胞提供针对病毒感染的细胞、肿瘤细胞或其他应激细胞的快速免疫反应,即使是在细胞表面上不存在抗体和主要组织相容性复合体。nk细胞可以是被分离的,也可以从商业上可获得的来源得到。商业性的nk细胞系的非限制性示例包括nk-92(atcc
®
crl-2407
™
)、nk-92mi(atcc
®
crl-2408
™
)细胞系。进一步的示例包括但不限于hank1、khyg-1、nkl、nk-ys、noi-90和ytnk细胞系。这样的商业上可获得的细胞系的非限制性示例性来源包括美国类型培养保藏中心或atcc(http://www.atcc.org/)以及德国微生物和细胞培养物保藏中心(https://www.dsmz.de/)。
[0191]
如本文所用,涉及调控性多核苷酸,术语“可操作地连接”是指调节性多核苷酸和其所连接的多核苷酸序列之间的连接,使得当特定蛋白质结合至调节性多核苷酸时,连接的多核苷酸被转录。
[0192]
如本文所用,相对于细胞、组织或器官的术语“过表达”表示蛋白质的量大于对照细胞、对照组织或器官中产生的量。过表达的蛋白质可以是宿主细胞内源的或宿主细胞外源的。
[0193]
术语“多核苷酸”和“寡核苷酸”被可互换地使用,并且指任何长度的核苷酸的聚合形式、是脱氧核糖核苷酸或核糖核苷酸或其类似物。多核苷酸可以具有任意的三维结构并且可以进行已知或未知的任何作用。以下是多核苷酸的非限制性示例:基因或基因片段(例如探针、引物、est或sage标签)、外显子、内含子、信使rna(mrna)、转运rna、核糖体rna、rnai、核酶、cdna、重组多核苷酸、支链多核苷酸、质粒、载体、分离的任何序列的dna、分离的任何序列的rna、核酸探针和引物。多核苷酸可以包含经修饰的核苷酸,例如甲基化核苷酸和核苷酸类似物。如果存在,则对核苷酸结构的修饰可以被施加在多核苷酸的组装之前或之后。核苷酸的序列可以被非核苷酸成分打断。多核苷酸可以在聚合之后被进一步修饰,例如与标签组分偶联。该术语还指双链分子和单链分子。除非另有说明或者需要,否则本技术的涉及多核苷酸任何方面都包括双链形式以及已知或预测形成双链形式的两个互补的单链形式中的每一个。
[0194]
如本文所用,术语“核酸序列”和“多核苷酸”被可互换地使用以指任何长度的核苷酸的聚合形式,核糖核苷酸或脱氧核糖核苷酸。因此,该术语包括但不限于单链、双链或多链dna或rna、基因组dna、cdna、dna-rna杂交体、或包含嘌呤和嘧啶碱基或其他天然的、化学的或生物化学修饰的、非天然的或衍生的核苷酸碱基的聚合物。
[0195]
在一些实施方式中,参考核酸、多核苷酸或寡核苷酸的等效物编码由参考核酸编码的相同序列。在一些实施方式中,任选地在高度严格性条件下,参考核酸、多核苷酸或寡核苷酸的等效物与参考、互补参考、反向参考和/或反向互补参考杂交。另外地或可选地,等效核酸、多核苷酸或寡核苷酸与参考核酸、多核苷酸或寡核苷酸具有至少70%、或至少75%、或至少80%序列同一性、或至少85%序列同一性、或至少90%序列同一性、或至少92%序列同一性、或至少95%序列同一性、或至少97%序列同一性,或至少98%序列同一性,或者等效核酸在高度严格条件下与参考多核苷酸或其互补序列杂交。在一方面,等效物必须编码任选地可通过本文所述的一种或多种测定来识别的功能性蛋白质。在另一方面,等效物具有与参考核酸、多核苷酸或寡核苷酸具有至少70%、或至少75%、或至少80%序列同一性、或至少85%序列同一性、或至少90%序列同一性、或至少92%序列同一性、或至少95%序列同一性、或至少97%序列同一性,或至少98%序列同一性,或者等效核酸在高度严格条件下与参考多核苷酸或其互补序列杂交。
[0196]
如本文所用,术语“启动子”是指调节编码序列(例如基因)的表达的任何序列。启动子可以例如是组成型的、可诱导的、可抑制的或组织特异性的。“启动子”是这样的控制序列,它是多核苷酸序列的一个区域,在此控制转录的起始和速率。它可以包含遗传元件,在此调节蛋白和分子可以结合例如rna聚合酶和其他转录因子。启动子的非限制性示例包括ef1α启动子和cmv启动子。ef1α序列是本领域已知的(参见,例如addgene.org/11154/sequences/; ncbi.nlm.nih.gov/nuccore/j04617,每个最后访问时间为2019年3月13日,
以及zheng and baum (2014) int’l. j. med. sci. 11(5):404-408)。cmv启动子序列是本领域已知的(参见,例如snapgene.com/resources/plasmid-files/set=basic_cloning_vectors&plasmid=cmv_promoter,最后访问时间为2019年3月13日,以及zheng and baum (2014), 同上)。示例是:ef1α启动子序列:aaggatctgcgatcgctccggtgcccgtcagtgggcagagcgcacatcgcccacagtccccgagaagttggggggaggggtcggcaattgaacgggtgcctagagaaggtggcgcggggtaaactgggaaagtgatgtcgtgtactggctccgcctttttcccgagggtgggggagaaccgtatataagtgcagtagtcgccgtgaacgttctttttcgcaacgggtttgccgccagaacacagctgaagcttcgaggggctcgcatctctccttcacgcgcccgccgccctacctgaggccgccatccacgccggttgagtcgcgttctgccgcctcccgcctgtggtgcctcctgaactgcgtccgccgtctaggtaagtttaaagctcaggtcgagaccgggcctttgtccggcgctcccttggagcctacctagactcagccggctctccacgctttgcctgaccctgcttgctcaactctacgtctttgtttcgttttctgttctgcgccgttacagatccaagctgtgaccggcgcctac (seq id no: 148),以及任选地其等效物。
[0197]
如本文所用,术语“t2a”和“2a肽”可互换使用,是指任何2a肽或其片段、任何2a样肽或其片段、或在包含共有多肽基序d-v/i-e-x-n-p-g-p (seq id no: 174)的相对较短的肽序列中包含必需氨基酸的人工肽(长度约为20个氨基酸,取决于病毒来源),其中x指一般认为是自我切割的任何氨基酸。
[0198]
il3rα(il3rα)或cd123是一种在几种血液系统恶性肿瘤中过度表达的表面受体。使用天然配体il-3进行il3r的初始靶向。cd123 car细胞对小鼠和人类的aml细胞具有强大的细胞毒性。townsend et al. (2018) j. exper. & clin. cancer res. 37:163,以及其中引用的参考文献。因此,car-able cd123结合肽和多核苷酸是本领域已知的。
[0199]
il3rα2(il13rα2)是一种在胶质母细胞瘤细胞上表达的细胞标记物。它是一种il-13受体,其充当诱饵通过直接与il-13rα1受体竞争来诱导下游stat信号。townsend et al. (2018),同上。基于scfv的cars已经过测试并证明是成功的。townsend et al. (2018),同上。
[0200]
术语“蛋白质”、“肽”和“多肽”可以互换使用,并且以其最广泛的意义来指两个或更多个氨基酸、氨基酸类似物或肽模拟物子单元的化合物。所述子单元可以通过肽键而被连接。在另一方面,所述子单元可以通过其他键(例如酯键、醚键等)而被连接。蛋白质或肽必须包含至少两个氨基酸,并且对于可以组成蛋白质或肽的序列的氨基酸的最大数目没有限制。如本文所用,术语“氨基酸”是指天然的和/或非天然的或合成的氨基酸,包括甘氨酸以及d和l光学异构体、氨基酸类似物和肽模拟物。
[0201]
术语等效物和生物等效物可以互换使用,例如,当提及蛋白质或多肽作为参考时。在一些实施方式中,等效蛋白质或多肽与参考蛋白质或多肽具有至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%、或至少约95%、至少约96%、至少约97%、至少约98%或至少约99%序列同一性。在一些实施方式中,等效蛋白质或多肽与本文所公开的多肽或蛋白质具有至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%或至少约95%、至少约96%、至少约97%、至少约98%或至少约99%序列同一性。在一些实施方式中,等效蛋白质或多肽与本文所述的等效多核苷酸编码的多肽或蛋白质具有至少约60%、至少约70%、至少约80%、至
少约85%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%或至少约95%、至少约96%、至少约97%、至少约98%或至少约99%序列同一性。另外地或可选地,多核苷酸的等效物将编码与参考或亲本多核苷酸具有相同或类似功能的蛋白质或多肽。在一些实施方式中,等效物是任选地可通过本文所述的一种或多种测定识别的功能性蛋白质。在另一方面,等效物与参考蛋白质或多肽具有至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%或至少约95%、至少约96%、至少约97%、至少约98%或至少约99%序列同一性。
[0202]
如本文所用,“对应于”参考序列中的识别位置的感兴趣的序列中的氨基酸(aa)或核苷酸(nt)残基位置是指在感兴趣序列和参考序列之间的序列比对中,与识别位置对齐的残基位置。有多种程序可用于执行此类序列比对,例如clustal omega和blast。
[0203]
如本文所用,术语“纯化的”不要求绝对的纯度;相反,它旨在作为相对性的术语。因此,例如,纯化的核酸、肽、蛋白质、生物复合物或其他活性化合物是整体地或部分地与蛋白质或其他污染物分离的。一般而言,用于在本发明中使用的基本上纯化的肽、蛋白质、生物复合物或其他活性化合物,在该肽、蛋白质、生物复合物或其他活性化合物与药物载体、赋形剂、缓冲剂、吸收促进剂、稳定剂、防腐剂、佐剂或其他辅助成分在用于治疗性给药的完整的药物制剂中混合或制备之前,包括多于80%的存在于制剂中的所有大分子种类。更一般地,在与其他制剂成分混合之前,所述肽、蛋白质、生物复合物或其他活性化合物被纯化,以代表大于90%、通常大于95%的存在于纯化制剂中的所有大分子种类。在其他情况下,纯化的制剂可以是基本上均质的,其中其他大分子种类不能通过常规技术而被检测到。
[0204]
如本文所用,术语“纯化标记物”是指可用于纯化或鉴定的至少一个标记物。该标记物的非穷举性的列表包括his、lacz、gst、麦芽糖结合蛋白、nusa、bccp、c-myc、cam、flag、gfp、yfp、樱桃、硫氧还蛋白、聚(nanp)、v5、snap、ha、几丁质结合蛋白、softag 1、softag 3、strep或s蛋白。合适的直接或间接荧光标记物包括flag、gfp、yfp、rfp、dtomato、樱桃、cy3、cy5、cy5.5、cy7、dnp、amca、生物素、地高辛、tamra、德克萨斯红、罗丹明、alexa荧光、fitc、tritc或任何其他荧光染料或半抗原。在一些实施方式中,纯化标记物是ha标签,任选地包含ypydvpdya (seq id no: 84),或基本上由其组成,或由其组成。
[0205]
如本文所用,术语“重组蛋白”是指通过重组dna技术制造的多肽,其中通常编码该多肽的dna备插入进合适的表达载体,该表达载体被用来转化宿主细胞以产生异源蛋白。
[0206]
如本文所用,术语“特异性结合”是指抗体与抗原之间的接触具有的结合亲和力以至少10-6 m。在一些方面,抗体结合具有的亲和力为至少约10-7 m,并且优选10-8 m、10-9 m、10-10 m、10-11 m或10-12 m。
[0207]“实体瘤”是通常不包括囊肿或液体区域的异常的组织块。实体肿瘤可以是良性的或恶性的、转移性或非转移性的。不同类型的实体瘤以形成它们的细胞的类型命名。实体肿瘤的示例包括肉瘤、癌和淋巴瘤。
[0208]
如本文所用,术语“自杀基因”是能够诱导细胞凋亡的基因;非限制性示例包括hsv-tk(单纯疱疹病毒胸苷激酶)、胞嘧啶脱氨酶、硝基还原酶、羧酸酯酶、细胞色素p450或pnp(嘌呤核苷磷酸化酶)、截短的egfr、或诱导型半胱天冬酶(“icasp”)。自杀基因可以通过多种途径发挥作用,并且在某些情况下,可以由诱导剂(小分子)诱导。例如,icasp自杀基因包含与优化地结合诱导剂的蛋白质可操作地连接的半胱天冬酶蛋白的一部分;将诱导剂引
入包含自杀基因的细胞中导致半胱天冬酶的活化和随后所述细胞的凋亡。
[0209]
术语“转换”或“转导”在其被应用至生产嵌合抗原受体细胞时是指,外来核苷酸序列被引入细胞中的过程。在一些实施方式中,所述转导是通过载体完成的。
[0210]
如本文所用,“处理”或“治疗”对象等的疾病在本文中用于表示获得期望的药理学和/或生理学效果。“治疗”的示例包括但不限于:防止疾病在预先有疾病倾向的但尚未被诊断为患有疾病的对象中发生;抑制疾病,即阻止其发展;和/或缓解或改善疾病症状。在一方面,治疗是阻止疾病或病症症状的发展,例如癌症。在一些实施方式中,它是指(1)防止症状或疾病在预先有倾向的或尚未显示疾病症状的对象中发生;(2)抑制疾病或阻止其发展;或者(3)改善或消退疾病或疾病的症状。如本领域所理解的,“治疗”是用于获得有益的或期望的结果(包括临床结果)的方法。对于本技术的目的,有益的或期望的结果可以包括但不限于以下中的一种或多种:一种或多种症状的缓解或改善、病症(包括疾病)的程度的降低、病症(包括疾病)的稳定化(即不恶化)状态、病症(包括疾病)的延迟或减缓、病症(包括疾病)、状态和缓解(无论是部分还是全部)的进展、改善或缓解,无论是可检测的还是不可检测的。含有所公开的组合物和方法的治疗可以是一线、二线、三线、四线、五线治疗,并且旨在用作单独疗法或与其他合适的疗法组合。当所述疾病是癌症时,以下临床终点是治疗的非限制性示例:减轻肿瘤负担、减缓肿瘤生长、延长总生存期、延长肿瘤进展时间、抑制转移或减少肿瘤转移。在一方面,术语“处理”或“治疗”不包括防范或预防。
[0211]
在一种实施方式中,如本文所用的术语“疾病”或“病症”是指癌症或肿瘤(可互换使用)、被诊断患有此类疾病的状态、被怀疑患有此类疾病的状态或处于患此类疾病的高风险的状态。
[0212]
在整个治疗过程中,细胞或载体或其他制剂及含有它们的组合物的“施用”或“递送”可以一剂、连续或间歇的方式进行。本领域技术人员已知确定最有效的给药方式和剂量的方法,并且会随着用于治疗的组合物、治疗目的、治疗的靶细胞和治疗的对象而变化。可以进行单次或多次给药,剂量水平和模式由治疗医师选择,或者对于动物,由治疗兽医选择。本领域已知合适剂量的制剂和施用方法。还可以确定给药途径,并且确定最有效给药途径的方法是本领域技术人员已知的,并且将随着用于治疗的组合物、治疗目的、被治疗对象的健康状况或疾病阶段以及靶细胞或组织而变化。给药途径的非限制性示例包括口服给药、腹腔内给药、输注、鼻腔给药、吸入、注射和局部应用。
[0213]“药物组合物”旨在包括活性多肽、多核苷酸或抗体与惰性或活性载体(例如固体载体)的组合,使得该组合物适于体外、体内或离体的诊断或治疗用途。
[0214]
如本文所用,术语“药学上可接受的载体(carrier)”包括任何标准医药载体,例如磷酸盐缓冲盐溶液、水和乳液(例如油/水或水/油乳液)、以及各种类型的润湿剂。所述组合物还可以包括稳定剂和防腐剂。关于载体、稳定剂和佐剂的示例,参见martin (1975) remington’s pharm. sci., 15th ed. (mack publ. co., easton)。
[0215]
如本文所用,术语“载体(vector)”是指设计用于在不同宿主之间转运的核酸构建体,包括但不限于质粒、病毒、粘粒、噬菌体、bac、yac等。在一些实施方式中,所述质粒载体可从市售载体制备。在其他实施方式中,根据本领域已知的技术,所述病毒载体可由杆状病毒、逆转录病毒、腺病毒、aav等产生。在一种实施方式中,所述病毒载体是慢病毒载体。
[0216]“病毒载体”定义为重组产生的病毒或病毒颗粒,其包含将在体内、体外或离体递
送到宿主细胞的多核苷酸。病毒载体的实例包括逆转录病毒载体、慢病毒载体、腺病毒载体、腺相关病毒载体、甲病毒载体等。甲病毒载体,如基于semliki forest病毒的载体和基于sindbis病毒的载体,也已被开发用于基因治疗和免疫治疗。参见schlesinger and dubensky (1999) curr. opin. biotechnol. 5:434-439和ying, et al. (1999) nat. med. 5(7):823-827。
[0217]
在基因转移由慢病毒载体介导的方面,载体构建体是指包含慢病毒基因组或其部分的多核苷酸和治疗基因。如本文所用,“慢病毒介导的基因转移”或“慢病毒转导”具有相同的含义,指通过病毒进入细胞并将其基因组整合到宿主细胞基因组中,使基因或核酸序列稳定转移到宿主细胞中的过程。病毒可以通过其正常的感染机制进入宿主细胞,或者经过修饰使其与不同的宿主细胞表面受体或配体结合以进入细胞。逆转录病毒以rna的形式携带基因信息;然而,一旦病毒感染细胞,rna就会被反转录成dna形式,并整合到受感染细胞的基因组dna中。整合的dna形式被称为前病毒。如本文所用,慢病毒载体指能够通过病毒或病毒样进入机制将外源核酸引入细胞的病毒颗粒。“慢病毒载体”是本领域众所周知的一种逆转录病毒载体,与其他逆转录病毒载体相比,其在转导非分裂细胞方面具有某些优势。参见trono d. (2002) lentiviral vectors, new york: spring-verlag berlin heidelberg。
[0218]
本公开的慢病毒载体基于或源自肿瘤逆转录病毒(含mlv的逆转录病毒亚组)和慢病毒(含hiv的逆转录病毒亚组)。示例包括aslv、snv和rsv,所有这些病毒都被分为用于慢病毒载体颗粒生产系统的包装和载体组件。根据本公开的慢病毒载体颗粒可以基于特定逆转录病毒的基因或其他方式(例如通过特定选择的包装细胞系统)改变形式。
[0219]
根据本公开的载体颗粒“基于”特定逆转录病毒是指该载体源自该特定逆转录病毒。载体颗粒的基因组包含来自该逆转录病毒的成分作为骨架。载体颗粒包含与rna基因组兼容的基本载体成分,包括逆转录和整合系统。通常包括衍生自特定逆转录病毒的gag和pol蛋白。因此,载体颗粒的大多数结构成分通常来自该逆转录病毒,尽管它们可能已通过基因或其他方式改变以提供所需的有用特性。然而,某些结构成分,尤其是env蛋白,可能来自不同的病毒。通过在载体颗粒产生系统中使用不同的env基因,可以改变感染或转导的载体宿主范围和细胞类型,从而赋予载体颗粒不同的特异性。
[0220]
如本文所用,术语“腺相关病毒”或“aav”是指与该名称相关并属于parvoviridae科dependoparvovirus属病毒类别中的一员。已知这种病毒的多种血清型适合基因传递;所有已知血清型都能感染各种组织类型的细胞。本领域已知至少11个顺序编号的aav血清型。可用于本文所公开的方法的非限制性示例性血清型包括11种血清型中的任何一种,例如aav2、aav8、aav9,或变体或合成血清型,例如aav-dj和aav-php.b。所述aav颗粒包括三种主要病毒蛋白:vp1、vp2和vp3,或基本上由其组成,或由其组成。在一种实施方式中,aav指血清型aav1、aav2、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aav13、aav php.b或aav rh74中的一种。这些载体是可市售的、或已在专利或技术文献中描述。
[0221]
当用于描述本文所公开的任何组分、范围、剂型等的选择时,术语或“可接受的”、“有效的”或“充分的”是指所述组分、范围、剂型等适用于本公开的目的。
[0222]
本文使用的术语“调控序列”、“表达控制元件”或“启动子”是指与要被转录和/或复制的靶多核苷酸操作性连接,并促进靶多核苷酸的表达和/或复制的多核苷酸。启动子是
表达控制元件或调控序列的一个示例。启动子可以位于为调控基因转录提供控制点的基因或其他多核苷酸的5'或上游。聚合酶ii和iii是启动子的示例。下面提供了mndu3启动子的序列和示例性cmv启动子的序列。
[0223]
如本文所用,信号肽是指(有时称为信号序列、靶向信号、定位信号、定位序列、转运肽、先导序列或先导肽)存在于大多数新合成蛋白质的n端的短肽(通常为16-30个氨基酸长),其目的地为分泌途径。在一些实施方式中,信号肽是分泌信号,例如il 2信号肽。参见,例如seq id no:4。在一些实施方式中,信号肽引导蛋白质或多肽(例如跨膜蛋白质)定位于细胞膜中,例如在细胞表面上。其中一个示例是igg1信号肽。参见,例如seq id no:5。
[0224]
分泌信号是指分泌信号肽,其允许蛋白质从胞液运输到分泌途径。蛋白质可以表现出不同水平的成功分泌,通常某些信号肽在与特定蛋白质结合时会导致更低或更高水平的分泌。在真核生物中,信号肽是由真核细胞胞液中的信号识别颗粒(srp)识别的疏水性氨基酸串。信号肽由mrna核糖体复合物产生后,srp与肽结合并停止蛋白质翻译。然后,srp将mrna/核糖体复合物运送到粗内质网,在那里蛋白质被翻译到内质网的腔中。然后,然后将信号肽从蛋白质上切割下来,在内质网中产生可溶性或膜标记(如果也存在跨膜区域)蛋白质。这些在本领域中是已知的,并且可从供应商例如 oxford genetics 市售获得。
[0225]
如本文所用,可裂解肽(也称为可裂解接头)是指可被例如酶裂解的肽。包含这种可裂解肽的一种翻译多肽可产生两种最终产物,因此,允许由一个开放阅读框表达一种以上的多肽。可裂解肽的一个示例是自裂解肽,例如2a自裂解肽。2a自裂解肽是一类18-22 aa长的肽,可诱导细胞内重组蛋白的裂解。在一些实施方式中,2a自裂解肽选自p2a、t2a、e2a、f2a和bmcpv2a。参见,例如wang y, et al. 2a self-cleaving peptide-based multi-gene expression system in the silkworm bombyx mori. sci rep. 2015;5:16273,公开于2015年11月5日。
[0226]
如本文所用,“多能细胞”定义了一种分化程度较低的细胞,其可产生至少两种不同的(基因型和/或表型)进一步分化的子代细胞。另一方面,“多能细胞”包括诱导多能干细胞(ipsc),其是人工衍生的来自非多能细胞的干细胞,通常是成体体细胞,其在历史上通过诱导一个或多个干细胞特异性基因的表达而产生。此类干细胞特异性基因包括但不限于八聚体转录因子家族,即oct-3/4;sox基因家族,即sox1、sox2、sox3、sox 15和sox 18;klf基因家族,即klf1、klf2、klf4和klf5;myc基因家族,即c-myc和l-myc;nanog基因家族,即oct4、nanog和rex1;或者lin28。ipsc的示例如takahashi et al. (2007) cell advance online publication 20 november 2007; takahashi & yamanaka (2006) cell 126:663
–
76; okita et al. (2007) nature 448:260-262; yu et al. (2007) science advance online publication 20 november 2007; 以及nakagawa et al. (2007) nat. biotechnol. advance online publication 30 november 2007中所述。
[0227]“诱导多能细胞”是指从成年细胞重新编程为未成熟表型的胚胎样细胞。本领域已知多种方法,例如"a simple new way to induce pluripotency: acid." nature, 29 january 2014且可在sciencedaily.com/releases/2014/01/140129184445获得,最后访问日期为2014年2月5日,和美国专利申请公开号2010/0041054。人类ipsc也表达干细胞标记物,并且能够产生具有所有三个胚层特征的细胞。
[0228]
如本文所用,造血干细胞(hsc)是产生所有类型血细胞(包括但不限于白细胞、红
细胞和血小板)的细胞(例如干细胞)。造血干细胞可以在外周血和骨髓中找到。
[0229]
术语药学上可接受的载体(或培养基)可与术语生物相容性载体或培养基互换使用,是指试剂、细胞、化合物、材料、组合物和/或剂型,其不仅与待进行治疗施用的细胞和其他药剂相容,而且在合理的医学判断范围内,适合与人类和动物的组织接触使用,无过度的毒性、刺激、过敏反应或其他符合合理效益/风险比的并发症。适用于本公开中使用的药学上可接受的载体包括液体、半固体(例如凝胶)和固体材料(例如细胞支架和基质、管板和其他此类材料,如本领域已知并在本文中更详细描述的其他此类材料)。这些半固体和固体材料可设计为抵抗体内降解(不可生物降解)或可设计为可在体内降解(能进行生物降解的、可生物降解的)。生物可降解的材料还可以是生物可吸收或生物可再吸收的,即它可以溶解并吸收到体液中(水溶性植入物就是一个例子),或者通过转化为其他材料或通过自然途径分解和消除、降解并最终从体内消除。
[0230]
细胞群是指一个以上细胞的集合,这些细胞在表型和/或基因型上相同(克隆)或不相同。如本文所述,所述群体可以是纯化的、高度纯化的、基本上同质的或异质的。
[0231]“基本同质”描述了一个细胞群,其中超过50%、或超过60%、或超过70%、或超过75%、或超过80%、或超过85%、或超过90%、或超过95%的细胞具有相同或相似的表型。表型可以通过预先选择的细胞表面标记或其他标记来确定。
[0232]
如本文所用,术语“nkg2d”是指属于c型凝集素样受体的cd94/nkg2家族的跨膜蛋白,其由位于nk基因复合物和/或其生物等效物中的基因klrk1基因编码。所述蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc12m011728, hgnc: 18788, entrez gene: 22914, ensembl: ensg00000213809, omim: 611817和uniprotkb: p26718下找到,其通过引用并入本文。
[0233]
如本文所用,术语“bcma”和“b细胞成熟抗原
”ꢀ
可互换使用,指代属于识别b细胞激活因子(baff)并由tnfrsf17基因编码的tnf超家族的蛋白质。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc16p012058, hgnc: 11913, entrez gene: 608, ensembl: ensg00000048462, omim: 109545和uniprotkb: q02223下找到,其通过引用并入本文。
[0234]
如本文所用,术语“slamf7”、“cs1”和“cd319
”ꢀ
可互换使用,指代已知为多发性骨髓瘤中正常浆细胞和恶性浆细胞的稳健标记并由slamf7基因编码的蛋白质。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc01p160709, hgnc: 21394, entrez gene: 57823, ensembl: ensg00000026751, omim: 606625和uniprotkb: q9nq25下找到,其通过引用并入本文。
[0235]
如本文所用,术语“cd19”和“b淋巴细胞抗原cd19
”ꢀ
可互换使用,指代已知为人体内由基因cd19编码的跨膜蛋白的蛋白质。在人类中,cd19 在所有 b 系细胞(浆细胞除外)和滤泡树突状细胞中表达。由于其存在于所有b细胞上,是b淋巴细胞发育的生物标志物,淋巴瘤诊断可用作白血病免疫治疗的靶点。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc16po28943, hgnc: 1633, entrez gene: 930, ensembl: ensg00000177455, omim: 107265和uniprotkb: p15391下找到,其通过引用并入本文。
[0236]
如本文所用,术语“her2”、“her2/neu”、“cd340”和“erbb2
”ꢀ
可互换使用,指代已知为人类表皮生长因子受体(her/egfr/erbb)家族成员的蛋白质。这种癌基因的扩增或过表
达已被证明在某些侵袭性乳腺癌的发展和进程中起着重要作用。该蛋白已成为许多乳腺癌患者的重要生物标志物和治疗靶点。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc17p039687, hgnc: 3430, entrez gene: 2064, ensembl: ensg000000141736, omim: 164870和uniprotkb: p04626下找到,其通过引用并入本文。
[0237]
如本文所用,术语“间皮素”和“msln
”ꢀ
可互换使用,指代在人体内由msln基因编码的蛋白质。间皮素是一种在间皮细胞中表达的40 kda的蛋白质。间皮素在多种类型的肿瘤中过表达,包括间皮瘤、卵巢癌、胰腺癌、肺腺癌和胆管癌。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc16p001100, hgnc: 7371, entrez gene: 10232, ensembl: ensg000000102854, omim: 601051和uniprotkb: q13421下找到,其通过引用并入本文。
[0238]
如本文所用,术语“psca”和“前列腺干细胞抗原
”ꢀ
可互换使用,指代在人体内由psca基因编码的蛋白质。psca是一种糖基磷脂酰肌醇锚定的细胞膜糖蛋白,在前列腺中高度表达。psca也在膀胱、胎盘、结肠、肾脏和胃中表达。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc08p142670, hgnc: 9500, entrez gene: 8000, ensembl: ensg000000167653, omim: 602470和uniprotkb: o43653下找到,其通过引用并入本文。
[0239]
如本文所用,术语“cea”和“癌胚抗原
”ꢀ
可互换使用,指代参与细胞粘附的一组高度相关的糖蛋白。健康成年人血液中的cea水平通常很低;然而,在某些类型的癌症中,其血清水平会升高,这表明其可以在临床试验中用作肿瘤标记物。在免疫学上,cea糖蛋白被表征为cd66分化簇的成员;所述蛋白质包括cd66a、cd66b、cd66c、cd66d和cd66e。
[0240]
cd66a(也称为癌胚抗原相关细胞粘附分子1)或基础基因的非限制性示例性序列可在gene cards id: gc19m042507, hgnc: 1814, entrez gene: 634, ensembl: ensg000000079385, omim: 109770和uniprotkb: p13688下找到,其通过引用并入本文。
[0241]
cd66b(也称为癌胚抗原相关细胞粘附分子8)或基础基因的非限制性示例性序列可在gene cards id: gc19m042580, hgnc: 1820, entrez gene: 1088, ensembl: ensg00000124469, omim: 615747和uniprotkb: p31997下找到,其通过引用并入本文。
[0242]
cd66c(也称为癌胚抗原相关细胞粘附分子6)或基础基因的非限制性示例性序列可在gene cards id: gc19p04150, hgnc: 1818, entrez gene: 4680, ensembl: ensg00000086548, omim: 163980, and 和uniprotkb: p40199下找到,其通过引用并入本文。
[0243]
cd66d(也称为癌胚抗原相关细胞粘附分子3)或基础基因的非限制性示例性序列可在gene cards id: gc19p041796, hgnc: 1815, entrez gene: 1084, ensembl: ensg00000170956, omim: 609142和uniprotkb: p40198下找到,其通过引用并入本文。
[0244]
cd66e(也称为癌胚抗原相关细胞粘附分子5)或基础基因的非限制性示例性序列可在gene cards id: gc19p041709, hgnc: 1817, entrez gene: 1048, ensembl: ensg00000105388, omim: 114890和uniprotkb: p06731下找到,其通过引用并入本文。
[0245]
如本文所用,术语“gtp酶激活蛋白”、“gap”和“ras p21蛋白激活剂1
”ꢀ
可互换使用,指代作为gtp酶激活蛋白的gap1家族成员的细胞质蛋白。该蛋白刺激正常ras p21的gtpase活性,但不刺激其致癌对应物。作为ras功能的抑制剂,该蛋白增强了ras蛋白微弱的内在gtpase活性,导致ras的非活性gdp结合形式,从而控制细胞增殖和分化。导致任一蛋白
结合位点改变的突变与基底细胞癌有关。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc05p087267, hgnc: 9871, entrez gene: 5921, ensembl: ensg000000145715, omim: 139150和uniprotkb: p20936下找到,其通过引用并入本文。
[0246]
如本文所用,术语“gd2”、“神经节苷脂g2”和“神经节苷脂gd2”可互换使用,指代在人体中在各种类型恶性细胞的质膜上表达的化学物质。gd2的iupac名称为(2r,4r,5s,6s)-2-[3-[(2s,3s,4r,6s)-6-[(2s,3r,4r,5s,6r)-5-[(2s,3r,4r,5r,6r)
‑ꢀ
3-乙酰胺基-4,5-二羟基-6-(羟甲基)恶烷(oxan)-2-基]氧基-2-[(2r,3s,4r,5r,6r)-4,5-二羟基-2-(羟甲基)-6-[(e)-3-羟基-2-(十八烷基氨基)十八烷基-4-烯氧基]恶烷-3-基]氧基-3-羟基-6-(羟甲基)恶烷-4-基]氧基-3-氨基-6-羧基-4-羟基恶烷-2-基]-2,3-二羟基丙氧基]-5-氨基-4-羟基-6-(1,2,3-三羟丙基)恶烷-2-甲酸。
[0247]
如本文所用,术语“cd5”和“t细胞表面糖蛋白cd5
”ꢀ
可互换使用,指代人体中在t细胞表面上表达的蛋白质。据报道,t细胞肿瘤可能表达cd5,在慢性淋巴细胞白血病和套细胞淋巴瘤中也有发现。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc11p061118, hgnc: 1685, entrez gene: 921, ensembl: ensg00000110448, omim: 153340和uniprotkb: p06127下找到,其通过引用并入本文。
[0248]
如本文所用,术语“前列腺特异性膜抗原”、“psma”、“叶酸水解酶1”和“folh1
”ꢀ
可互换使用,指代属于m28肽酶家族的ii型跨膜糖蛋白的蛋白质。在前列腺中,该蛋白质在癌细胞中上调,并被用作前列腺癌的有效诊断和预后指标。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc11m056090, hgnc: 3788, entrez gene: 2346, ensembl: ensg00000086205, omim: 600934和uniprotkb: q04609下找到,其通过引用并入本文。
[0249]
如本文所用,术语“受体酪氨酸激酶样孤儿受体1”和“ror1
”ꢀ
可互换使用,指代调节中枢神经系统中神经轴突生长的蛋白质。表达的增加与b细胞慢性淋巴细胞白血病有关。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc01p063774, hgnc: 10256, entrez gene: 4919, ensembl: ensg00000185483, omim: 602336和uniprotkb: q01973下找到,其通过引用并入本文。
[0250]
如本文所用,术语“cd123”、“白介素3受体亚基α”和“il-3ra
”ꢀ
可互换使用,指代异源二聚体细胞因子受体的白介素3特异性亚基。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc0xp001336, hgnc: 6012, entrez gene: 3563, ensembl: ensg00000185291, omim: 430000和uniprotkb: p26951下找到,其通过引用并入本文。
[0251]
如本文所用,术语“cd70”和“肿瘤坏死因子配体超家族成员7
”ꢀ
可互换使用,指代属于肿瘤坏死因子配体家族的细胞因子。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc19m006583, hgnc: 11937, entrez gene: 970, ensembl: ensg00000125726, omim: 602840, and 和uniprotkb: p32970下找到,其通过引用并入本文。
[0252]
如本文所用,术语“cd38”和“adp核糖环化酶1
”ꢀ
可互换使用,指代非谱系限制的ii型跨膜糖蛋白,其合成水解环腺苷酸5'-二磷酸核糖(一种细胞内钙离子动员信使)。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc04p015779, hgnc: 1667, entrez gene: 952, ensembl: ensg0000004468, omim: 107270和uniprotkb: p28907下
找到,其通过引用并入本文。
[0253]
如本文所用,术语“粘蛋白1”和“粘蛋白1
”ꢀ
可互换使用,指代作为粘蛋白家族成员的膜结合蛋白。这种蛋白的过表达、细胞内异常定位和糖基化变化与癌症有关。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc01m155158, hgnc: 7508, entrez gene: 4582, ensembl: ensg00000185499, omim: 158340和uniprotkb: p15941下找到,其通过引用并入本文。
[0254]
如本文所用,术语“epha2”和“ephrin a型受体2
”ꢀ
可互换使用,指代结合ephrin a配体的蛋白质。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc01m016196, hgnc: 3386, entrez gene: 1969, ensembl: ensg00000142627, omim: 176946和uniprotkb: p29317下找到,其通过引用并入本文。
[0255]
如本文所用,术语“egfrviii”和“表皮生长因子变异体iii
”ꢀ
可互换使用,指代表皮生长因子变异体(viii),它是最常见的egfr突变,发生在高达30%的高级胶质瘤(尤其是多形性胶质母细胞瘤)中。egfrviii源于外显子2-7的缺失,导致形成不能与任何已知配体结合的组成性激活突变受体。
[0256]
如本文所用,术语“il13ra2”和“白介素13受体亚基α2
”ꢀ
可互换使用,指代白介素13受体复合物的亚基。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc0xm115003, hgnc: 5975, entrez gene: 3598, ensembl: ensg00000123496, omim: 300130和uniprotkb: q14627下找到,其通过引用并入本文。
[0257]
如本文所用,术语“cd133”和“prominin 1
”ꢀ
可互换使用,指代一种五跨跨膜糖蛋白。这种蛋白质定位于膜突起,通常在成人干细胞上表达,人们认为它通过抑制分化来维持干细胞的特性。这种蛋白质与几种类型的癌症有关。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc04m015965, hgnc: 9454, entrez gene: 8842, ensembl: ensg00000007062, omim: 604365和uniprotkb: o43490下找到,其通过引用并入本文。
[0258]
如本文所用,术语“gpc3”和“glypican 3
”ꢀ
可互换使用,指代细胞表面硫酸肝素蛋白聚糖,其由被可变数量的硫酸肝素链取代的膜相关蛋白核心组成。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc0xm133535, hgnc: 4451, entrez gene: 2719, ensembl: ensg00000147257, omim: 300037和uniprotkb: p51654下找到,其通过引用并入本文。
[0259]
如本文所用,术语“epcam”和“上皮细胞粘附分子
”ꢀ
可互换使用,指代癌相关抗原,其是包括至少两种i型膜蛋白的家族成员。这种抗原在大多数正常上皮细胞和胃肠道癌中表达,并作为一种同种型钙非依赖性粘附分子发挥作用。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc02p047345, hgnc: 11529, entrez gene: 4072, ensembl: ensg00000119888, omim: 18553和uniprotkb: p16422下找到,其通过引用并入本文。
[0260]
如本文所用,术语“fap”和“成纤维细胞活化蛋白α
”ꢀ
可互换使用,指代属于丝氨酸蛋白酶家族的同二聚体整膜明胶酶。其在上皮癌的反应性基质成纤维细胞、愈合伤口的肉芽组织、骨和软组织肉瘤的恶性细胞中选择性表达。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc02m162170, hgnc: 3590, entrez gene: 2191, ensembl: ensg00000078098, omim: 600403和uniprotkb: q12884下找到,其通过引用并入本文。
[0261]
如本文所用,术语“vegfr2”、“血管内皮生长因子受体2”和“激酶插入域受体
”ꢀ
可互换使用,指代作为vegf诱导的内皮细胞增殖、存活、迁移、管状形态发生和发芽的主要介质的蛋白质。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc04m055078, hgnc: 6307, entrez gene: 3791, ensembl: ensg00000128052, omim: 191306和uniprotkb: p35968下找到,其通过引用并入本文。
[0262]
如本文所用,术语“癌症/睾丸抗原”和“ct抗原
”ꢀ
可互换使用,指代正常表达仅限于睾丸中雄性生殖细胞但不在成人体细胞组织中的一类肿瘤抗原。在恶性肿瘤中,多种肿瘤可能表达ct抗原。ct抗原的非限制性示例性包括:ctag1b、ctag2、ct45a2、ct45a5、ct45a6、ct45a3、ct45a1、ct47b1、ct47a11、ct47a6、ct47a7、ct45a7、ctg1a、at45a8、ct45a9、ct47a1、ct47a2、ct47a3、ct47a4和ct47a8。
[0263]
如本文所用,术语“gucy2c”和“鸟苷酸环化酶2c
”ꢀ
可互换使用,指代作为内源性肽鸟苷酸和尿鸟苷酸受体的跨膜蛋白。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc12m014612, hgnc: 4688, entrez gene: 2984, ensembl: ensg00000070019, omim: 601330和 uniprotkb: p25092下找到,其通过引用并入本文。
[0264]
如本文所用,术语“tag72”、“cd247”和“肿瘤相关糖蛋白-72
”ꢀ
可互换使用,指代t细胞受体ζ。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc01m167399, hgnc: 1677, entrez gene: 919, ensembl: ensg00000198821, omim: 186780和uniprotkb: p20963下找到,其通过引用并入本文。
[0265]
如本文所用,术语“tk1”和“胸腺嘧啶核苷激酶1
”ꢀ
可互换使用,指代催化向胸腺嘧啶核苷中添加γ-磷酸基团的胞液酶。高水平的这种蛋白质已被用作诊断和分类多种癌症的生物标志物。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc12m014612, hgnc: 4688, entrez gene: 2984, ensembl: ensg00000070019, omim: 601330和uniprotkb: p25092下找到,其通过引用并入本文。
[0266]
如本文所用,术语“hprt1”和“次黄嘌呤磷酸核糖转移酶1
”ꢀ
可互换使用,指代通过5-磷酸核糖基1-焦磷酸转移5-磷酸核糖基,催化次黄嘌呤转化为肌苷单磷酸和鸟嘌呤转化为鸟苷单磷酸的转移酶。该蛋白质或基础基因的非限制性示例性序列可在gene cards id: gc0xp134460, hgnc: 5157, entrez gene: 3251, ensembl: ensg00000165704, omim: 308000和uniprotkb: p00492下找到,其通过引用并入本文。
[0267]
将与上述每个登录号和参考文献相关的序列通过引用并入本文。
[0268]
实施本公开的方式免疫调节分子施用被视为癌症疗法。然而,由于与全身施用相关的严重副作用(giovarelli, m. et al. (2000) j immunol. 164:3200-3206; lasek, w. et al. (2014) cancer immunol immunother. 63:419-435),在相关肿瘤中获得高浓度的这些免疫调节分子以实现有效的免疫应答一直是困难的。
[0269]
由于最近使用基因工程嵌合抗原受体(car)t细胞自体疗法治疗b细胞淋巴瘤和白血病取得了前所未有的结果(maude, s.l. et al. (2014) new engl. j. med. 371:1507-1517; porter, d.l. et al. (2011) new engl. j. med. 365:725-733),许多实验室已经开始将这种方法应用于实体肿瘤,包括卵巢癌、前列腺癌和胰腺肿瘤。car修饰的t细胞将单克隆抗体的hla非依赖性靶向特异性与活化t细胞的细胞溶解活性、增殖和归位特性
结合,但不响应检查点抑制。由于car t细胞能够直接杀死抗原表达靶点,因此对任何抗原阳性细胞或组织都具有高度毒性,因此需要构建具有高度肿瘤特异性抗体的car。迄今为止,已经针对α-叶酸受体、间皮素、muc-cd、psma和其他靶点构建了用于人类实体瘤的car修饰t细胞,但大多数在正常组织中有一些抗原的非靶点表达。这些构建体没有在患者中显示出相同的异常结果,强调需要进行额外研究以确定可用于治疗实体瘤car t细胞构建的新靶点和方法。
[0270]
因此,本发明提供了一种嵌合抗原受体(car),其包含特定于癌症或肿瘤抗原的结合域,在一些方面,该结合域是除抗bcma抗体之外的抗原的抗原结合域,本发明还提供一种双特异性抗体(例如bite或 bike)或其片段、编码bsab car构建体的多核苷酸或载体、靶向肿瘤或癌症抗原并分泌可溶性抗体片段的bsab-car表达细胞,以及与其用途和生产相关的方法和组合物。
[0271]
嵌合抗原受体及其用途组分本公开提供了与癌症或肿瘤抗原结合的嵌合抗原受体(car),所述car包含,或基本上由以下组成,或由以下组成:包括细胞外、跨膜和细胞内结构域(在本文中也称为细胞质结构域)的细胞活化部分。胞外结构域包含靶标特异性结合元件,或者称为抗原结合域。胞内结构域或细胞质结构域包括一个或多个共刺激信号区和信号域,例如cd3 ζ链部分。car可任选地进一步包含多达300个氨基酸、优选地10至100个氨基酸、更优选地25至50个氨基酸的间隔域。
[0272]
另外或可选地,本文所公开的car包含,或基本上由以下组成,或由以下组成:识别并结合癌细胞上的肿瘤相关抗原(taa)的抗原结合域、铰链结构域、跨膜结构域和细胞内/细胞质结构域。在一些实施方式中,所述taa不是b细胞成熟抗原(bcma),例如egfr(野生型或egfrviii)或flt3。在一些实施方式中,所述taa是bcma。
[0273]
间隔域。所述car可任选地进一步包含多达300个氨基酸、优选地10至100个氨基酸、更优选地25至50个氨基酸的间隔域。例如,间隔可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个氨基酸。间隔域可包括例如人fc结构域、ch3结构域或任何免疫球蛋白(例如iga、igd、ige、igg或igm或其变体)的铰链区的一部分。例如,一些实施方式可包括具有或不具有s228p、l235e和/或n297q突变(根据kabat编号)的igg4铰链。其他间隔包括但不限于cd4、cd8和cd28铰链区。
[0274]
信号肽。所述car可任选地进一步包含信号肽,任选地将car引导至car和/或bsab car表达细胞的细胞表面。在一些实施方式中,信号肽位于car的n末端,例如位于car的抗原结合域的n末端侧。在一些实施方式中,信号肽可以是任何免疫球蛋白的信号肽,例如iga、igd、ige、igg或igm。在一种实施方式中,信号肽是igg1的信号肽。在另一种实施方式中,信号肽包含seq id no:5序列或其等效物,或基本上由其组成,或由其组成。在进一步的实施方式中,seq id no:5的等效物仍然将car引导至位于car和/或bsab car表达细胞的细胞表面上。另外或可选地,seq id no:5的等效物与seq id no:5至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同。本领域技术人员可以使用检测将蛋白质引导至位于细胞表面的信号肽的方
法,例如免疫染色和对蛋白质表达细胞成像。
[0275]
抗原结合域。在某些实施方式中,本公开提供了一种car,其包含对癌症或肿瘤抗原具有特异性的抗原结合域,或基本上由其组成,或由其组成。抗原结合域可以来自任何合适的物种,例如小鼠、人类或人源化序列。
[0276]
在一些实施方式中,抗原结合域包含抗bcma抗体或结合bcma相关抗原的抗体的抗原结合域,或基本上由其组成,或由其组成。特异性结合这些抗原的单克隆抗体是可市售的。抗原结合域可以来自任何合适的物种,例如小鼠、人类或人源化序列。一方面,抗原结合域包含针对除b细胞成熟抗原(bcma)之外的癌症或肿瘤抗原的抗体的重链可变区和轻链可变区。在另一实施方式中,抗原结合域包含抗slamf7抗体(也称为抗cs1抗体或抗cd319抗体)的重链和轻链可变区,和/或其各自的等效物。在一些实施方式中,抗原结合域包含,或基本上由以下组成,或由以下组成:靶标特异性抗体(即,针对除b细胞成熟抗原(bcma)和/或slamf7(也称为cs1或cd319)以外的抗原的抗体和/或其等效物)的片段,例如scfv。scfv区可包括用短接头肽连接的免疫球蛋白重链(vh)和轻链(v
l
)的可变区。接头肽的长度可以是1到50个氨基酸,例如,1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、38、39、40、41、42、43、45、46、47、48、49或50个氨基酸。在一些实施方式中,接头富含甘氨酸,尽管它也可能含有丝氨酸或苏氨酸。
[0277]
在本公开的一些实施方式中,抗癌或抗肿瘤抗体的抗原结合域的等效物包括以下特征中的一个或多个:(a) 轻链免疫球蛋白可变区/结构域序列包含一个或多个(例如1、2、3或更多)cdr,其与本公开的任何轻链序列的轻链可变区/结构域的cdr至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同;(b)重链免疫球蛋白可变区/结构域序列包含一个或多个(例如1、2、3或更多)cdr,其与本公开的任何重链序列的重链可变区/结构域的cdr至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同;(c) 轻链免疫球蛋白可变区/结构域序列与本公开的任何轻链序列的轻链可变区/结构域至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同;(d)重链免疫球蛋白可变区/结构域序列与本公开的任何重链序列的重链可变区/结构域至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同;(e) 轻链(lc)免疫球蛋白可变区/结构域序列与本公开的任何轻链序列的轻链可变区/结构域至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同;以及(f) 抗体结合的表位与本公开的任何序列结合的表位重叠。
[0278]
在进一步的实施方式中,(a)至(e)中的任何一项或多项仍然识别并结合本公开的参考序列的相同表位,和/或识别并结合与本公开的参考序列结合的表位重叠的表位。
[0279]
抗原结合域等效物的其他实例包括与参考肽具有至少85%、或至少90%、或至少
95%,或至少97%氨基酸同一性的肽,或者由在高度严格条件下与编码抗原结合域的多核苷酸的互补序列杂交的多核苷酸编码的多肽。在一些实施方式中,高度严格条件包括约55
°
c至约68
°
c的培养温度;约1x ssc至0.1x ssc的缓冲液浓度;约55%至75%的甲酰胺浓度;以及约1x ssc、0.1x ssc或去离子水的洗涤溶液。
[0280]
在一些实施方式中,如本文所公开的car的抗原结合域识别并结合fms样酪氨酸激酶3(flt3),即,是抗flt3抗原结合域。在一些实施方式中,抗flt3抗原结合域包含以下cdr中的一个或两个或三个或四个或五个或全部六个,或基本上由其组成,或由其组成:cdrl1,包含rasqsisnnlh (seq id no: 15)、kssqsllnsgnqknym (seq id no: 16) 或其各自的等效物,或基本上由其组成,或由其组成;cdrl2,包含yasqsis (seq id no: 17)、gastres (seq id no: 18)或其各自的等效物,或基本上由其组成,或由其组成;cdrl3,包含qqsntwpyt (seq id no: 19)、qndhsyplt (seq id no: 20)或其各自的等效物,或基本上由其组成,或由其组成;cdrh1,包含sywmh (seq id no: 21)、nyglh (seq id no: 22) 或其各自的等效物,或基本上由其组成,或由其组成;cdrh2,包含eidpsdsykdynqkfkd (seq id no: 23)、viwsggstdynaafis (seq id no: 24) 或其各自的等效物,或基本上由其组成,或由其组成;和cdrh3,包含aitttpfdf (seq id no: 25)、ggiyyanhyyamdy (seq id no: 26) 或其各自的等效物,或基本上由其组成,或由其组成。在进一步的实施方式中,其cdr等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合flt3。在一些实施方式中,抗flt3抗原结合域包含以下部分,或基本上由其组成,或由其组成:轻链可变区,其包括选自以下的序列,或基本上由其组成,或由其组成:divltqspatlsvtpgdsvslscrasqsisnnlhwyqqkshesprllikyasqsisgipsrfsgsgsgtdftlsinsvetedfgvyfcqqsntwpytfgggtkleikr (seq id no: 27)、divmtqspsslsvsagekvtmsckssqsllnsgnqknymawyqqkpgqppklliygastresgvpdrftgsgsgtdftltissvqaedlavyycqndhsypltfgagtklelkr (seq id no: 28)或其各自的等效物;和/或重链可变区,其包括选自以下的序列,或基本上由其组成,或由其组成:qvqlqqpgaelvkpgaslklsckssgytftsywmhwvrqrpghglewigeidpsdsykdynqkfkdkatltvdrssntaymhlssltsddsavyycaraitttpfdfwgqgttltvss (seq id no: 29)、qvqlkqsgpglvqpsqslsitctvsgfsltnyglhwvrqspgkglewlgviwsggstdynaafisrlsiskdnsksqvffkmnslqaddtaiyycarkggiyyanhyyamdywgqgtsvtvss (seq id no: 30)或其各自的等效物。在进一步的实施方式中,其可变区等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合flt3。
[0281]
在一些实施方式中,如本文所公开的car的抗原结合域识别并结合表皮生长因子受体(egfr),例如野生型egfr(egfrwt)和/或其变体,例如egfrviii。该抗原结合域在本文中也称为抗egfr抗原结合域。在一些实施方式中,所述抗egfr抗原结合域包含以下cdr中的一个或两个或三个或四个或五个或全部六个,或基本上由其组成,或由其组成:cdrl1,包含rssqnivhnngityle (seq id no: 31)、rasqgirnnla (seq id no: 32)或其各自的等效物,或基本上由其组成,或由其组成;cdrl2,包含kvsdrfs (seq id no: 33)、aasnlqs (seq id no: 34)或其各自的等效物,或基本上由其组成,或由其组成;cdrl3,包含fqgshippt (seq id no: 35)、lqhhsyplt (seq id no: 36)或其各自的等效物,或基本上由其组成,或由其组成;cdrh1,包含gdtftsy (seq id no: 37)、gftfssy (seq id no: 38)或其各自的等效
物,或基本上由其组成,或由其组成;cdrh2,包含ypgsgg (seq id no: 39)、sgsggs (seq id no: 40)或其各自的等效物,或基本上由其组成,或由其组成;和cdrh3,包含sggpyffdy (seq id no: 41)、ssgwsey (seq id no: 42)或其各自的等效物,或基本上由其组成,或由其组成。在进一步的实施方式中,其cdr等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合egfr。在一些实施方式中,抗egfr抗原结合域包含以下部分,或基本上由其组成,或由其组成:轻链可变区,其包括选自以下的序列,或基本上由其组成,或由其组成:dilmtqsplslpvslgdqasiscrssqnivhnngitylewylqrpgqspklliykvsdrfsgvpdrfsgsgsgtdftlkisrveaedlgiyycfqgshipptfgggtkleikraa (seq id no: 43)、diqmtqspsslsasvgdrvtitcrasqgirnnlawyqqkpgkapkrliyaasnlqsgvpsrftgsgsgteftlivsslqpedfatyyclqhhsypltsgggtkveikyahns (seq id no: 44)或其各自的等效物;和/或重链可变区,其包括选自以下的序列,或基本上由其组成,或由其组成:qvqlqqsgsemarpgasvklpckasgdtftsywmhwvkqrhghgpewigniypgsggtnyaekfknkvtltvdrssrtvymhlsrltsedsavyyctrsggpyffdywgqgttltvss (seq id no: 45)、evqvlesggglvqpggslrlscaasgftfssyamswvrqapgkglewvsaisgsggstnyadsvkgrftisrdnskntlylqmnslraedtavyycagssgwseywgqgtlvtvss (seq id no: 46)或其各自的等效物。在进一步的实施方式中,其可变区等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合egfr。
[0282]
在一些实施方式中,如本文所公开的car的抗原结合域识别并结合bcma,即抗bcma抗原结合域。在一些实施方式中,所述抗原结合域包含以下cdr中的一个或两个或三个或四个或五个或全部六个,或基本上由其组成,或由其组成:cdrl1,包含rasesvtilgshlih (seq id no: 47)、sasqdisnyln (seq id no: 48)、rasesvtilgshliy (seq id no: 49)或其各自的等效物,或基本上由其组成,或由其组成;cdrl2,包含lasnvqt (seq id no: 50)、ytsnlhs (seq id no: 51)、lasnvqt (seq id no: 52)或其各自的等效物,或基本上由其组成,或由其组成;cdrl3,包含lqsrtiprt (seq id no: 53), qqyrklpwt (seq id no: 54), lqsrtiprt (seq id no: 55)或其各自的等效物,或基本上由其组成,或由其组成;cdrh1,包含gytftdy (seq id no: 56)、ggtfsny (seq id no: 57)、gytfrhy (seq id no: 58)或其各自的等效物,或基本上由其组成,或由其组成;cdrh2,包含intetre (seq id no: 59)、yrghsd (seq id no: 60)、ntesgv (seq id no: 61)或其各自的等效物,或基本上由其组成,或由其组成;和cdrh3,包含dysyamdy (seq id no: 62)、gaiyngydvldn (seq id no: 63)、dylysldf (seq id no: 64)或其各自的等效物,或基本上由其组成,或由其组成。在进一步的实施方式中,其cdr等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合bcma。在一些实施方式中,抗bcma抗原结合域包含以下部分,或基本上由其组成,或由其组成:轻链可变区,其包括选自以下的序列,或基本上由其组成,或由其组成:divltqsppslamslgkratiscrasesvtilgshlihwyqqkpgqpptlliqlasnvqtgvparfsgsgsrtdftltidpveeddvavyyclqsrtiprtfgggtkleik (seq id no: 65)、diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapklliyytsnlhsgvpsrfsgsgsgtdftltisslqpedfatyycqqyrklpwtfgqgtkleikr (seq id no: 66)、divltqsppslamslgkratiscrasesvtilgshliywyqqk
pgqpptlliqlasnvqtgvparfsgsgsrtdftltidpveeddvavyyclqsrtiprtfgggtkleik (seq id no: 67) 或其各自的等效物;和/或重链可变区,其包括以下序列,或基本上由其组成,或由其组成:qiqlvqsgpelkkpgetvkisckasgytftdysinwvkrapgkglkwmgwintetrepayaydfrgrfafsletsastaylqinnlkyedtatyfcaldysyamdywgqgtsvtvss (seq id no: 68)、qvqlvqsgaevkkpgssvkvsckasggtfsnywmhwvrqapgqglewmgatyrghsdtyynqkfkgrvtitadkststaymelsslrsedtavyycargaiyngydvldnwgqgtlvtvss (seq id no: 69)、qiqlvqsgpelkkpgetvkisckasgytfrhysmnwvkqapgkglkwmgrintesgvpiyaddfkgrfafsvetsastaylvinnlkdedtasyfcsndylysldfwgqgtaltvss (seq id no: 70) 或其各自的等效物。在进一步的实施方式中,其可变区等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合bcma。
[0283]
在一些实施例中,如本文所公开的car的抗原结合域识别并结合cs1,即抗cs1抗原结合域。在一些实施方式中,所述抗cs1抗原结合域包含以下cdr中的一个或两个或三个或四个或五个或全部六个,或基本上由其组成,或由其组成:cdrl1,包含kasqdvitgva (seq id no: 71)或其等效物,或基本上由其组成,或由其组成;cdrl2,包含sasyryt (seq id no: 72)或其等效物,或基本上由其组成,或由其组成;cdrl3,包含qqhystplt (seq id no: 73)或其等效物,或基本上由其组成,或由其组成;cdrh1,包含gysftty (seq id no: 74)或其等效物,或基本上由其组成,或由其组成;cdrh2,包含hpsdse (seq id no: 75)或其等效物,或基本上由其组成,或由其组成;和cdrh3,包含stmiatramdy (seq id no: 76)或其等效物,或基本上由其组成,或由其组成。在进一步的实施方式中,其cdr等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合cs1。在一些实施方式中,抗cs1抗原结合域包含以下部分,或基本上由其组成,或由其组成:轻链可变区,其包括选自以下的序列,或基本上由其组成,或由其组成:sdivmtqsqksmstsvgdrvsitckasqdvitgvawyqqkpgqspklliysasyrytgvpdrftgsgsgtdftftisnvqaedlavyycqqhystpltfgagtklelk (seq id no: 77),klelktgagftlptsyhqqcyyvaldeaqvnsitftfdtgsgsgtfrdpvgtyrysasyillkpsqgpkqqywavgtivdqsakctisvrdgvstsmskqsqtmvids (seq id no: 154), divmtqsqksmstsvgdrvsitckasqdvitgvawyqqkpgqspklliysasyrytgvpdrftgsgsgtdftftisnvqaedlavyycqqhystpltfgagtklelk (seq id no: 78) 或其各自的等效物;和/或重链可变区,其包括以下序列,或基本上由其组成,或由其组成:svtvstgqgwydmartaimtsracyyvasdestpsslqmyatssskdvtltakdkfkqnlrtesdsphimgiwelgqgprqkvwnmwyttfsygsakcslkvsagprvleagpqqlqvqs (seq id no: 79), ssvtvstgqgwydmartaimtsracyyvasdestpsslqmyatssskdvtltakdkfkqnlrtesdsphimgiwelgqgprqkvwnmwyttfsygsakcslkvsagprvleagpqqlqvq (seq id no: 149),sqvqlqqpgaelvrpgasvklsckasgysfttywmnwvkqrpgqglewigmihpsdsetrlnqkfkdkatltvdkssstaymqlssptsedsavyycarstmiatramdywgqgtsvtvs (seq id no: 80), qvqlqqpgaelvrpgasvklsckasgysfttywmnwvkqrpgqglewigmihpsdsetrlnqkfkdkatltvdkssstaymqlssptsedsavyycarstmiatramdywgqgtsvtvs s (seq id no: 150) 或其各自的等效物。在
进一步的实施方式中,其可变区等效物和/或包括该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合域识别并结合cs1。
[0284]
在一些实施方式中,参考蛋白质或多肽的等效物,例如cdr、可变区、抗原结合域或抗体,与参考蛋白质或多肽至少80%、或至少85%、或至少90%、或至少95%、或至少96%、或至少97%、或至少98%、或至少99%相同。
[0285]
在一些实施方式中,参考蛋白质或多肽(例如cdr、可变区、抗原结合域或抗体)的等效物包含参考蛋白质或多肽的c端到n端的氨基酸序列,或基本上由其组成,或由其组成。例如,参考蛋白质或多肽包含kasqdvitgva (seq id no: 71),或基本上由其组成,或由其组成;其等效物包含avgtivdqsak (seq id no: 151),或基本上由其组成,或由其组成。在cdr、可变区、抗原结合域或抗体作为参考蛋白质或多肽的实施方式中,等效物仍然识别并结合参考的相同表位。
[0286]
鉴于嵌合抗原受体(car)具有不同的作用机制和安全性,治疗性抗体不能保证其在car中成功使用。即使针对同一抗原,它们也无法相互预测。抗体利用抗原结合诱导肿瘤细胞凋亡和/或fc受体结合巨噬细胞、自然杀伤(nk)细胞和中性粒细胞以诱导多方面的免疫反应。然而,car免疫细胞(例如t细胞和nk细胞)利用与肿瘤抗原的特异性结合,随后通过人工嵌合受体诱导免疫细胞激活。尽管car免疫细胞和抗体都可能具有非靶向毒性,具体而言,抗体可以诱导fc受体介导的毒性(schlothauer et al. protein eng. des. sel. 29, 457-466 (2016)),而car免疫细胞通常会导致致命的细胞因子释放综合征(crs)和神经毒性(gupta et al. j emerg med. 2020 may 27;s0736-4679(20)30352-8)。因此,本领域技术人员无法仅基于共同的抗原结合域来预测car的疗效和安全性。
[0287]
尽管在某些方面,car中的scfv可以衍生自抗体;为了发挥功能,两者都需要与肿瘤抗原结合。然而,抗体与肿瘤抗原的结合通常是可溶形式的,而car上的scfv与肿瘤抗原的结合则来自免疫细胞的表面。至少有三种差异决定了这两种类型的相互作用:1)两种环境对蛋白质或肽构象要求不同;2)在抗体设置中,由两个fab区(每个区由一部分重链和一部分轻链组成)和重链上的fc组成的全长抗体控制结合亲和力,并且由于两个fab区,结合是二价的,而对于car、scfv,其中由重链可变区(vh)和轻链活区(vl)组成的一个fab区通过接头相互连接,为单价结合;3)由于单价结合且scfv长度比相应抗体短,当小鼠scfv用于car时(这是市场上大多数car的情况),car的结合亲和力较低,而患者的免疫原性较低(dotti et al. immunol rev 257, 107-126 (2014))。因此,抗体的功能无法预测car的功能。事实上,haso et al. (blood 121, 1165-1174 (2013)最近证明,使用高亲和力抗体衍生的scfv增加car的结合亲和力,并不能增加car在体外和体内的活性(haso et al. blood 121, 1165-1174 (2013)和handgretinger et al. blood 121, 1065-1066 (2013))。
[0288]
在一些实施方式中,如本文所公开的抗原结合域还包括肽接头,例如,在两个cdr之间和/或在其轻链可变区或其等效物与其重链可变区或其等效物之间。在一种实施方式中,肽接头包含ggggsggggsggggs (seq id no: 14)或其等效物,或基本上由其组成,或由其组成。在一些实施方式中,seq id no:14的等效物可以是1到50个氨基酸长度,例如,1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、35、36、37、38、39、40、41、42、43、44、45、46、48、49或50个氨基酸。在一些实施方式中,seq id no:14的等效物富含甘氨酸,尽管它也可能含有丝氨酸或苏氨酸。在一些实施方
式中,seq id no:14的等效物包括(ggggs)n,或基本上由其组成,或由其组成,其中n可以是1、或2、或3、或4、或5、或6、或7、或8、或9、或10、或11、或12、或13、或14、或15或更多的整数(seq id no: 134-135, 14和136-147)。
[0289]
铰链结构域。铰链结构域可以来自天然或合成来源。在一些实施方式中,铰链结构域衍生自分化蛋白簇,例如cd8、cd28、cd3、cd45、cd4、cd5、cds、cd9、cd16、cd22、cd33、cd37、cd64、cd80、cd86、cd134、cd137、cd154。在一种实施方式中,铰链结构域是cd8α铰链结构域。在一些实施方式中,铰链结构域衍生自免疫球蛋白,例如iga、igd、ige、igg或igm。在一种实施方式中,铰链结构域是igg1铰链结构域。在进一步的实施方式中,igg1铰链结构域包括lepkscdkthtcppcpdpkgt (seq id no: 1)或其等效物,或基本上由其组成,或由其组成。在一些实施方式中,与seq id no:1相比,seq id no:1的等效物包含1个、或2个、或3个、或4个、或5个、或6个、或7个、或8个、或9个、或10个、或11个、或12个、或13个、或14个、或15个、或更多个突变。
[0290]
跨膜结构域。跨膜结构域可以来自天然或合成来源。如果来源是天然的,则该结构域可能来自任何膜结合或跨膜蛋白。本公开中特定用途的跨膜区可衍生自cd8、cd28、cd3、cd45、cd4、cd5、cd4、cd9、cd16、cd22、cd33、cd37、cd64、cd80、cd86、cd134、cd137、cd154和tcr。或者,跨膜结构域可以是合成的,在这种情况下,它将主要包含疏水残基,例如亮氨酸和缬氨酸。优选地,在合成跨膜结构域的每一端将发现苯丙氨酸、色氨酸和缬氨酸的三联体。任选地,长度最好在2到10个氨基酸之间的短寡肽或多肽接头可在car的跨膜结构域和细胞质信号域之间形成连接。甘氨酸-丝氨酸双链体提供了一种特别合适的接头。在一些实施方式中,所述跨膜结构域包括cd8α跨膜结构域或cd28跨膜结构域,或基本上由其组成,或由其组成。
[0291]
胞质/胞内结构域。car的细胞质结构域或细胞内结构域负责激活car所在免疫细胞的至少一种传统效应器功能。在一些实施方式中,细胞质结构域或细胞内结构域包括细胞内信号域,或基本上由其组成,或由其组成。细胞内信号结构域或在一些实施方式中的信号域是指转导效应器功能信号并引导免疫细胞执行其特定功能的蛋白质的一部分。只要截断部分足以传递效应器功能信号,就可以使用整个信号传导域或其截断部分。tcr和共受体及其衍生物或变体的细胞质序列可作为用于car的细胞内信号域发挥作用。本公开中特定用途的细胞内信号域可衍生自fcr、tcr、cd3、cds、cd22、cd79a、cd79b和cd66d。在一些实施方式中,car的信号域可包括cd3 ζ信号域,或基本上由其组成,或由其组成。在一些实施方式中,cd3 ζ信号域包括以下序列,或基本上由其组成,或由其组成rvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (seq id no: 3)或其等效物。在进一步的实施例中,与seq id no:3相比,seq id no:3的等效物可包含1个、或2个、或3个、或4个、或5个、或6个、或7个、或8个、或9个、或10个、或11个、或12个、或13个、或14个、或15个、或更多个突变,但仍然能够转导效应器功能信号并引导免疫细胞执行其与 seq id no: 3 相同的特定功能。例如在bridgeman js, et al. clin exp immunol. 2014 feb;175(2):258-67中可以找到评估这种转导的示例性方法。
[0292]
由于仅通过tcr产生的信号不足以完全激活t细胞,因此可能还需要次级或共刺激信号。因此,共刺激信号分子的细胞内区域,包括但不限于蛋白质cd27、cd28、4-ibb
(cd137)、ox40、cd30、cd40、pd-1、icos、淋巴细胞功能相关抗原-1(lfa-1)、cd2、cd7、light、nkg2c、b7-h3的细胞内结构域,或特异性结合cd83的配体,也可包括在car的细胞质结构域中。例如,除了信号域(例如,cd3ζ信号域)之外,car还可以包括一个、两个或更多个共刺激域。在一些实施方式中,细胞内结构域还包括选自cd28共刺激信号区、4-1bb共刺激信号区、icos共刺激信号区或ox40共刺激区的一个或更多或两个或更多共刺激区。
[0293]
在一些实施方式中,嵌合抗原受体的细胞激活部分是t细胞信号域,其包含一个或多个选自以下的蛋白质或其片段,或基本上由其组成,或由其组成:cd8蛋白、cd28蛋白、4-1bb蛋白、ox40、cd30、cd40、pd-1、icos、lfa-1、cd2、cd7、cd27、light、nkg2c、b7-h3、和cd3 ζ蛋白。
[0294]
在一些实施方式中,嵌合抗原受体的细胞激活部分是t细胞信号域,其包含一个或多个选自以下的蛋白质或其片段,或基本上由其组成,或由其组成:cd8蛋白、cd28蛋白、4-1bb蛋白和cd3 ζ蛋白。
[0295]
在特定的实施方式中,car包含,或基本上由以下组成,或由以下组成:癌症或肿瘤靶向抗体的抗原结合域、cd8α铰链结构域、cd8α跨膜结构域、共刺激信号区和cd3 ζ信号域组成,或由其组成。在进一步的实施方式中,共刺激信号区包括cd28共刺激信号区和4-1bb共刺激信号区之一或两者。在一些实施方式中,car包含,或基本上由以下组成,或由以下组成:cd28跨膜和细胞质结构域,其包括fwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrs (seq id no: 2)或其等效物。在进一步的实施例中,与seq id no:32相比,seq id no:2的等效物可包含1个、或2个、或3个、或4个、或5个、或6个、或7个、或8个、或9个、或10个、或11个、或12个、或13个、或14个、或15个、或更多个突变,但仍然能够作为跨膜结构域和共刺激信号区发挥作用。
[0296]
在一些实施方式中,如本文所公开的car和/或其细胞质结构域进一步包含il2rβ或其片段。在进一步的实施方式中,il2rβ的片段包含il2rβ的jak-stat活化结构域以促进免疫细胞的活化,或基本上由其组成,或由其组成。在一些实施方式中,car和/或car的细胞内结构域进一步包含il2rβ或其包含jak-stat活化结构域的片段。在一些实施方式中,jak-stat活化域包括,或基本上由以下组成,或由以下组成:jak结合域(也称为box-1基序,其允许酪氨酸激酶jak结合,例如jak1)和/或信号转导和转录激活因子(stat,例如stat3或stat5)结合基序。jak结合域的一个示例可以在ncbi refseq:np_000869.1的氨基酸编号278到286中找到。在进一步的实施方式中,细胞内结构域进一步包含内源性或外源性jak结合基序和/或内源性或外源性stat结合基序。在一些实施方式中,外源性stat3结合基序为yxxq(seq id no: 152),任选地为yrhq(seq id no: 153)。表达此类car细胞的细胞显示抗原依赖性jak-stat3/5通路激活,这在体外促进了它们的增殖并阻止了终末分化。或者,来自除il2rβ以外的蛋白质的jak-stat激活域可在此用作替代。此类蛋白质的实例可包括促红细胞生成素受体(epor)、血小板生成素受体(tpor)、粒细胞巨噬细胞集落刺激因子受体(gm-csfr)或生长激素受体(ghr)。例如,参见us20190359685a1以及kagoya et al. nat med. 2018 mar;24(3):352-359. doi: 10.1038/nm.4478. epub 2018 feb 5。
[0297]
开关机制。在一些实施方式中,car还可以包括用于控制car的表达和/或激活的开关机制。例如,car可包含,或由以下组成:细胞外、跨膜和细胞内结构域,其中细胞外结构域
包含靶标特异性结合元件,其结合标记、结合域或标签,其对靶细胞(例如癌细胞)上或由靶细胞表达的靶抗原以外的分子具有特异性。在一些实施方式中,此类标记、结合域或标签识别并结合在靶细胞上或由靶细胞表达的靶抗原。在此类实施方式中,car的特异性由第二构建体提供,其包括、或由以下组成、或基本上由以下组成:靶抗原结合域和car上的由标记、结合域或标签识别或结合的域。参见,例如,wo 2013/044225、wo 2016/000304、wo 2015/057834、wo 2015/057852、wo 2016/070061、us 9233125、us 2016/0129109。通过这种方式,可以向对象施用表达car的t细胞、nk细胞或其他免疫细胞,但在施用包含标记、结合域或标签的第二组合物(例如bcma特异性结合域)之前,其不能结合目标抗原(即bcma)。
[0298]
本发明的car可能同样需要多聚化以激活其功能(参见,例如,us 2015/0368342、us 2016/0175359、us 2015/0368360)和/或外源信号,例如小分子药物(us 2016/0166613, yung et al., science, 2015),以引发免疫细胞反应,例如t细胞反应或nk细胞反应。
[0299]
此外,所公开的car可包含“自杀开关”(也称为“自杀基因”),以在治疗后诱导car细胞死亡(buddee et al., plos one, 2013),或在与靶抗原结合后下调car的表达(wo 2016/011210)。一种非限制性的示例性自杀开关或自杀基因是icasp。在一些实施方式中,如本文所公开的car和/或其细胞质结构域进一步包含自杀基因产物。在进一步的实施方方式中,自杀基因产物选自以下中的一种或多种:hsv-tk(单纯疱疹病毒胸苷激酶)、胞嘧啶脱氨酶、硝基还原酶、羧酸酯酶、细胞色素p450或pnp(嘌呤核苷磷酸化酶)、截短型egfr或诱导型半胱天冬酶(“icasp”)。
[0300]
在一些实施方式中,car可进一步包括可检测的标记或纯化标记。另一方面,如本文所述的car包含在组合物中,例如用于诊断或治疗的药学上可接受的载体。
[0301]
在某些实施方式中,car的癌症或肿瘤靶向抗体的抗原结合域包括,或基本上由以下组成,或由以下组成:任选地由连接肽连接的重链可变区和轻链可变区。在一些实施方式中,重链和/或轻链可变区包括,或基本上由以下组成,或由以下组成:针对抗原的抗体的相关cdr区(例如b细胞成熟抗原(bcma)以外的cdr区)和/或slamf7(也称为cs1或cd319)和/或其各自的等效物。在某些实施方式中,car进一步包括,或基本上由以下组成,或由以下组成:位于重链可变区和轻链可变区之间的接头多肽。在某些实施方式中,所述接头是甘氨酸-丝氨酸接头。在进一步的实施方式中,接头多肽包括,或基本上由以下组成,或由以下组成:序列(甘氨酸丝氨酸)n,其中n是1到6的整数(seq id no:110),其中在一个方面,n是4。
[0302]
在某些实施方式中,car的癌症或肿瘤靶向抗体的抗原结合域结合任何癌症或肿瘤相关抗原,例如选自以下中的一种或多种:flt3、cd19、间皮素、人表皮生长因子受体2(her2)、前列腺干细胞抗原(psca)、癌胚抗原(cea)、gtp酶激活蛋白(gap)、神经节苷脂g2(gd2)、cd5、前列腺特异性膜抗原(psma)、受体酪氨酸激酶样孤儿受体1(ror1)、cd123、cd70、cd38、b细胞成熟抗原(bcma)、粘蛋白1(muc1)、肝配蛋白a型受体2前体(epha2)、野生型表皮生长因子受体(egfrwt)、表皮生长因子受体变异体iii(egfrviii)、白介素13受体α2(il13ra2)、cd133、glypican 3(gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白α(fap)、血管内皮生长因子受体2(vegfr2)、癌症/睾丸(ct)、鸟苷酸环化酶c(gucy2c)、肿瘤相关糖蛋白72(tag-72)、胸苷激酶1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖转移酶(hprt1)。它们可以包含抗原结合域的重链和轻链,或者包含抗原结合域的cdr,或由其组成。
[0303]
还提供了编码car构建体的多核苷酸(例如分离和/或工程化多肽)和/或分离核
酸。多核苷酸和/或核酸可进一步包含必要的调节序列,例如,在宿主细胞中表达的启动子,例如哺乳动物或人类宿主细胞,例如t细胞或nk细胞和/或增强子元件。在一些实施方式中,多核苷酸和/或核酸进一步包含指导car表达的第一调控序列。在进一步的实施方式中,调控序列包括以下中的一项或多项:启动子、内含子、增强子或多聚腺苷酸化信号。在一些实施方式中,启动子是cmv、mnd或ef1α启动子。在进一步的实施方式中,car多核苷酸和/或核酸进一步编码可检测或纯化的标记肽(例如gfp),其可由第二调控序列调控,例如位于编码多核苷酸5
′
端的启动子元件,例如cmv、mnd和ef1a启动子。在一些实施方式中,第二启动子包含ef1α启动子。正如本领域技术人员显而易见的,启动子是针对宿主表达系统选择的,并且会随着宿主和表达载体以及预期用途而变化。在一些实施方式中,多核苷酸和/或核酸进一步包含自杀基因,其编码任选自以下中的一种或多种的自杀基因产物:hsv-tk(单纯疱疹病毒胸苷激酶)、胞嘧啶脱氨酶、硝基还原酶、羧酸酯酶、细胞色素p450或pnp(嘌呤核苷磷酸化酶)、截断型egfr或诱导型半胱天冬酶(“icasp”)。在进一步的实施方式中,多核苷酸和/或核酸进一步包含指导自杀基因产物表达的第三调控序列。在一种实施方式中,任何一个或两个或三个调节序列在细胞中是可诱导的或是组成性活性的。在一种实施方式中,调节序列中的任何一个或两个或三个可以是细胞特异性或组织特异性的。
[0304]
在一些实施方式中,多核苷酸和/或核酸包含以下中的一种或多种,或基本上由其组成,或由其组成:(i)编码信号肽的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:atggggtggtcaagcattattctgtttctggtcgctaccgctacaggcgtccat (seq id no: 86), atgtacaggatgcaactcctgtcttgcattgcactaagtcttgcacttgtcacaaacagt (seq id no: 87)或其各自的等效物;(ii)编码连接肽的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:ggtgggggcggctctggtggcggtggcagcggcggaggtggcagt (seq id no: 88);(iii)编码跨膜和细胞质结构域的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:ttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcc (seq id no: 89)或其等效物;(iv)编码信号域的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:agagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgc (seq id no: 90)或其等效物;(vi)编码接头的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或
由以下组成:ccgagcggccaggcgggcgcggcggcatcggagtccctgtttgtgtcaaatcacgcctac (seq id no: 92) 或其等效物;(vii)编码抗bcma轻链可变区的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:gatattgttcttactcaatcacccccaagccttgcgatgtctcttggtaaacgagcgacaattagttgtagagcttctgaaagcgtaactattcttgggtcacatcttattcattggtatcaacaaaagccgggacaaccgcctacactcttgattcaactcgcgagcaatgttcaaacgggtgtccctgcacgcttttctgggagcggttcacgaacagattttactctcacgattgatccagtcgaagaagatgatgtcgctgtatattattgtctccaaagtaggacaataccaagaacttttggtggtggtacaaaattggaaattaaa (seq id no: 93),gacatccagatgacccagagccctagctcactgagcgccagcgtgggcgacagggtgaccattacctgctccgccagccaggacatcagcaactacctgaactggtaccagcagaagcccggcaaggcccccaagctgctgatctactacacctccaacctgcactccggcgtgcccagcaggttcagcggaagcggcagcggcaccgatttcaccctgaccatctccagcctgcagcccgaggacttcgccacctactactgccagcagtacaggaagctcccctggactttcggccagggcaccaaactggagatcaagcgt (seq id no: 94),gacatcgtgctgacccagagcccccccagcctggccatgtctctgggcaagagagccaccatcagctgccgggccagcgagagcgtgaccatcctgggcagccacctgatctactggtatcagcagaagcctggccagccccccaccctgctgatccagctggctagcaatgtgcagaccggcgtgcccgccagattcagcggcagcggcagcagaaccgacttcaccctgaccatcgaccccgtggaagaggacgacgtggccgtgtactactgcctgcagagccggaccatcccccggacctttggcggaggaacaaagctggaaatcaag (seq id no: 95),gacatcgtgctgacccagagcccccccagcctggccatgtctctgggcaagagagccaccatcagctgccgggccagcgagagcgtgaccatcctgggcagccacctgatccactggtatcagcagaagcccggccagccccccaccctgctgatccagctcgccagcaatgtgcagaccggcgtgcccgccagattcagcggcagcggcagcagaaccgacttcaccctgaccatcgaccccgtggaagaggacgacgtggccgtgtactactgcctgcagagccggaccatcccccggacctttggcggaggcaccaaactggaaatcaag (seq id no: 96)或其各自的等效物;(viii)编码抗bcma重链可变区的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:cagatccagctggtgcagtccggccccgagctgaagaagcccggcgagaccgtgaagatctcctgcaaggcctccggctacaccttcaccgactactccatcaactgggtgaagcgggcccccggcaagggcctgaagtggatgggctggatcaacaccgagacccgggagcccgcctacgcctacgacttccggggccggttcgccttctccctggagacctccgcctccaccgcctacctgcagatcaacaacctgaagtacgaggacaccgccacctacttctgcgccctggactactcctacgccatggactactggggccagggcacctccgtgaccgtgtcctcc (seq id no: 97),caggtgcagctggtccagagcggcgccgaagtgaagaagcccggcagctccgtgaaagtgagctgcaaggccagcggcggcaccttcagcaactactggatgcactgggtgaggcaggcccccggacagggcctggagtggatgggcgccacctacaggggccacagcgacacctactacaaccagaagttcaagggccgggtgaccatcaccgccgacaagagcaccagcaccgcctacatggaactgagcagcctcaggagcgaggacaccgctgtgtattactgcgccaggggcgccatctacaacggctacgacgtgctggacaactggggccagggcacactagtgaccgtgtccagc (seq id no: 98),atgggatggagctctatcatcctcttcttggtagcaacagctacaggtgtccaccagattcagctggt
gcagagcggccctgagctgaagaaacccggcgagacagtgaagatcagctgcaaggcctccggctacaccttccggcactacagcatgaactgggtgaaacaggcccctggcaagggcctgaagtggatgggccggatcaacaccgagagcggcgtgcccatctacgccgacgacttcaagggcagattcgccttcagcgtggaaaccagcgccagcaccgcctacctggtgatcaacaacctgaaggacgaggataccgccagctacttctgcagcaacgactacctgtacagcctggacttctggggccagggcaccgccctgaccgtgtccagc (seq id no: 99),或cagattcagctggtgcagagcggccctgagctgaagaaacccggcgagacagtgaagatcagctgcaaggcctccggctacaccttcaccgactacagcatcaactgggtgaaaagagcccctggcaagggcctgaagtggatgggctggatcaacaccgagacaagagagcccgcctacgcctacgacttccggggcagattcgccttcagcctggaaaccagcgccagcaccgcctacctgcagatcaacaacctgaagtacgaggacaccgccacctacttttgcgccctggactacagctacgccatggactactggggccagggcaccagcgtgaccgtgtccagc (seq id no: 100) 或其各自的等效物;(xi)编码抗flt3轻链可变区的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:gatattgtgctaactcagtctccagccaccctgtctgtgactccaggagatagcgtcagtctttcctgcagggccagccagagtattagcaacaacctacactggtatcaacaaaaatcacatgagtctccaaggcttctcatcaagtatgcttcccagtccatctctgggatcccctccaggttcagtggcagtggatcagggacagatttcactctcagtatcaacagtgtggagactgaagattttggagtgtatttctgtcaacagagtaacacctggccgtacacgttcggaggggggaccaagctggaaataaaacgg (seq id no: 103),gacattgtgatgacacagtctccatcctccctgagtgtgtcagcaggagagaaggtcactatgagctgcaagtccagtcagagtctgttaaacagtggaaatcaaaagaactatatggcctggtatcagcagaaaccagggcagcctcctaaactgttgatctacggggcatccactagggaatctggggtccctgatcgcttcacaggcagtggatctggaaccgatttcactcttaccatcagcagtgtgcaggctgaagacctggcagtttattactgtcagaatgatcatagttatccgctcacgttcggtgctgggaccaagctggagctgaaacgg (seq id no: 104) 或其各自的等效物;(xii)编码抗flt3重链可变区的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:caggtccaactgcagcagcctggggctgagcttgtgaagcctggggcttcattgaagctgtcctgcaagtcttccgggtacaccttcaccagctactggatgcactgggtgaggcagaggcctggacatggccttgagtggatcggagagattgatccttctgacagttataaagactacaatcagaagttcaaggacaaggccacattgactgtggacagatcctccaacacagcctacatgcacctcagcagcctgacatctgatgactctgcggtctattattgtgcaagagcgattacgacgaccccctttgacttctggggccaaggcaccactctcacagtctcctca (seq id no: 105),caggtgcagctgaagcagtcaggacctggcctagtgcagccctcacagagcctgtccatcacctgcacagtctctggtttctcattaactaactatggtttacactgggttcgccagtctccaggaaagggcctggagtggctgggagtgatatggagtggtggaagcacagactataatgcagctttcatatccagactgagcatcagcaaggacaactccaagagccaagttttctttaaaatgaacagtctgcaggctgatgacacagccatatactactgtgccagaaaaggagggatctactatgctaaccattactatgctatggactactggggtcaaggaacctcagtcaccgtctcctca (seq id no: 106) 或其各自的等效物;(xiii)编码抗cs1轻链可变区的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:aaacttgagt tgaagaccgg tgccggcttc accttaccga ccagttatcatcaacaatgctattacgtggccctggacgaagcacaggtgaattcaattacgtttacgtt
tgataccggctctggcagcggtacatttcgtgatcccgtgggcacttaccgctattcggcgagttatatcttgctgaaaccttcccaaggtccgaaacagcagtactgggcggttggcaccattgtagaccaatcagccaaatgtacaatctcggttcgcgatggtgtcagtacgtcgatgtctaagcagtcacagacaatggttatcgat(seqidno:107)或其等效物;(xiv)编码抗cs1重链可变区的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:agcgttaccgtgagtacaggccagggctggtatgacatggcacgtacagccatcatgacctcgcgcgcatgttactacgtcgcgtcagatgaatcgacgccttcctcgctgcaaatgtatgcaacctccagcagcaaagatgttaccctgaccgcaaaggacaagtttaaacagaatttgcgtacggagagtgactccccgcacatcatgggaatctgggagttgggtcaggggcctcgtcagaaggtatggaacatgtggtatacaactttttcgtacggctcagcaaaatgcagcttgaaagtgtcggcaggtccgcgcgtgctggaggccggtccgcagcagctgcaagtccagtct(seqidno:108)或其等效物;和(xv)编码铰链结构域的核苷酸序列,其中所述核苷酸序列包括,或基本上由以下组成,或由以下组成:ctcgagcccaaatcttgtgacaaaactcacacatgcccaccgtgcccggatcccaaaggtacc(seqidno:109)或其等效物。
[0305]
在一些实施方式中,参考核苷酸序列的等效物编码参考核苷酸序列的相同氨基酸序列。在一些实施方式中,参考核苷酸序列的等效物与参考核苷酸序列至少80%(例如至少85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少96%、至少97%、至少98%、或至少99%)相同。另外或可选地,参考核苷酸序列的等效物在高度严格条件下与参考核苷酸的互补序列杂交。在一些实施方式中,高度严格条件包括约55
°
c至约68
°
c的培养温度;约1xssc至0.1xssc的缓冲液浓度;约55%至75%的甲酰胺浓度;以及约1xssc、0.1xssc或去离子水的洗涤溶液。还提供了一种与本文所公开的多核苷酸反向、互补或反向互补的多核苷酸。在一些实施方式中,本文所公开的多核苷酸还包括可检测或纯化标记和/或编码可检测或纯化标记的序列。
[0306]
多核苷酸和/或分离的核酸可插入载体,例如表达载体,例如慢病毒载体、或逆转录病毒载体(在5'和3'ltr之间)、或腺病毒载体或任何其他可表达基因型的载体。图1a是本发明的示例性构建体。显而易见,当临床用于人类患者时,标记物或纯化标签将从构建体中省略。可使用本文所述的病毒载体或rietetal.(2013)meth.mol.biol.969:187-201entitled“nonviralrnatransfectiontotransientlymodifytcellwithchimericantigenreceptorsforadoptivetherapy”中所述的技术转导细胞。在一些实施方式中,所述载体是非病毒载体,例如质粒。在一些实施方式中,所述载体是病毒载体,任选地选自逆转录病毒载体、慢病毒载体、腺病毒载体和腺相关病毒载体。另外或可选地,载体还包括指导编码car的多核苷酸和/或分离核酸的复制和/或表达的调控序列。在进一步的实施方式中,调控序列包括以下中的一个或多个:启动子、内含子、增强子或多聚腺苷酸化信号。在一些实施方式中,所述载体还包括可检测或纯化标记。
[0307]
制备用于car构建体的抗体的过程可购买或使用本领域已知的和在本文中简要描述的方法制备用于本公开的抗体。如果发现了新的抗原,则需要制造抗体和该抗体的抗原结合结构域。它们的制造和用途是众所周知的并公开在例如harlow, e. and lane, d., antibodies: a laboratory manual, cold spring harbor laboratory press, cold spring harbor, n.y., 1999
3837 (1989);winter, g. et al., nature, 349: 293-299 (1991))。
[0315]
或者,可以使用生产单链抗体的技术。单链抗体(scfv)包含通过接头肽(通常长度约为5至25个氨基酸)相连的重链可变区和轻链可变区。在scfv中,重链和轻链的可变区可以来源于相同的抗体或不同的抗体。scfv可以使用重组技术合成,例如通过在宿主生物(例如大肠杆菌)中编码scfv的载体的表达。编码scfv的dna可以通过以下来获得:通过使用限定其两端的引物对的pcr,使用编码dna的全部或所需氨基酸序列的部分dna作为模板进行扩增,该dna选自编码上述抗体的重链或重链可变区的dna以及编码其轻链或其轻链可变区的dna,并进一步将编码多肽接头部分的dna与限定其两端的引物对组合进行扩增,以使接头的两端分别与重链和轻链连接。含有编码scfv的dna的表达载体和由该表达载体转化的宿主可以根据本领域已知的常规方法获得。
[0316]
还可以产生抗原结合片段,例如,可以通过抗体分子的胃蛋白酶消化产生f(ab')2片段,以及可以通过还原f(ab')2片段的二硫键产生fab片段。或者,可以构建fab表达文库以允许快速和轻易地鉴定出具有所需特异性的单克隆fab片段(huse et al., science, 256: 1275-1281 (1989))。
[0317]
抗体修饰。本公开的抗体可以被多聚化以增加对抗原的亲和力。被多聚化的抗体可以是一种抗体或是识别同一抗原的多个表位的多种抗体。作为抗体的多聚化的一种方法,可以例举igg ch3结构域与2个scfv分子的结合、链霉亲和素的结合、螺旋-转角-螺旋基序的导入以及类似的方法。本文公开的抗体组合物可以是这些抗体中的任何一种与另一种试剂(免疫偶联物)之间形成的偶联物的形式。在一方面,本文公开的抗体结合至放射性物质。在另一方面,本文公开的抗体可以被结合至各种类型的分子(例如聚乙二醇(peg))。
[0318]
抗体筛选。各种免疫测定可用于筛选以鉴定具有所需特异性的抗体。使用具有确定特异性的多克隆或单克隆抗体进行竞争性结合或免疫放射测定的多种方案在本领域中是众所周知的。此类免疫测定通常涉及测量相关抗原或其任何片段或寡肽与其特异性抗体之间的复合物形成。可以使用利用对两个非干扰相关抗原表位特异的单克隆抗体的双位点基于单克隆的免疫测定,也可以使用竞争性结合测定(maddox 等人,j. exp. med.,158:1211
ꢀ‑
1216 (1983))。
[0319]
抗体纯化。本文公开的抗体可以纯化至同质。可以通过采用常规的蛋白质分离和纯化方法来进行抗体的分离和纯化。
[0320]
仅为例举,抗体可以通过适当地选择和与色谱柱、过滤器、超滤、盐沉淀、透析、制备型聚丙烯酰胺凝胶电泳、等电聚焦电泳等的联合使用而被分离和纯化。蛋白质纯化和表征策略:a laboratory course manual, daniel r. marshak et al. eds., cold spring harbor laboratory press (1996);antibodies: a laboratory manual. ed harlow and david lane, cold spring harbor laboratory (1988)。
[0321]
色谱法的实例包括亲和色谱法、离子交换色谱法、疏水色谱法、凝胶过滤色谱法、反相色谱法和吸附色谱法。在一方面,色谱可以通过使用液相色谱(例如hplc或fplc)来进行。
[0322]
在一方面,蛋白a柱或蛋白g柱可用于亲和层析。其他示例性柱包括蛋白a柱、hyper d、poros、sepharosef.f.(pharmacia)等。
[0323]
双特异性抗体本文还提供了包含nkg2d或肿瘤抗原的任何抗体的双特异性抗体构建体,例如抗-nkg2d抗体的抗原结合结构域和结合cs1的抗体的肿瘤靶向抗原结合结构域。在一些实施方案中,提供了一种双特异性抗体,其包含以下,或者基本上由以下组成,或者由以下组成:识别并结合癌细胞上的taa的抗原结合结构域和识别并结合nkg2d的抗原结合结构域。在一个实施方案中,提供了一种双特异性抗体,其包含以下,或者基本上由以下组成,或者由以下组成:识别并结合cs1的抗原结合结构域(即抗-cs1抗原结合结构域)和识别并结合nkg2d的抗原结合结构域(即,抗-nkg2d抗原结合结构域)。在一些实施方案中,抗原结合结构域结合存在于car所结合的抗原结合结构域(例如,各自结合mm细胞或成胶质细胞瘤细胞)的癌症或肿瘤细胞的类型上的抗原。抗原结合结构域可以来自任何合适的物种(例如鼠、人或人源化序列)。此类的一个例子在2016年2月22日提交的pct/us2016/018955中进行了描述,该专利通过引用并入本文,特别是包括此类的多核苷酸和氨基酸序列。在本文中作为这种方法的示例描述的是一种构建体,其中两个抗原结合结构域中的至少一个对与预定的第一抗原共表达的抗原具有特异性。例如,在mm的情况下,bcma和cs1在mm上共表达,并且选择cs1来补充car构建体的bcma抗原结合结构域。或者,bcma可以补充抗-cs1car。
[0324]
在进一步的方面,抗原结合结构域包含任选地经密码子优化的scfv片段,或基本上由其组成,或由其组成。在进一步的方面,双特异性抗原结合结构域是通过肽接头连接的重链可变区和轻链可变区。通常,抗原结合结构域可以通过肽接头(例如源自人肌肉醛糖(hma)
35
的非免疫原性蛋白接头)连接在一起。图3a中提供了这样的示例,并且图1e、1f或1g中示出了双特异性组分。如这些图中所示,构建体可以进一步包含t2a、自切割2a基因、hma多肽和/或接头肽(例如g4s肽接头(seqidno:14和134至147)(“g4s"公开为seqidno:134)。
[0325]
在一些实施方案中,如本文所公开的双特异性抗体的抗-taa抗原结合结构域识别并结合任何癌症或肿瘤相关抗原,例如一种或多种选自以下的抗原:flt3、cd19、间皮素、人表皮生长因子受体2(her2)、前列腺干细胞抗原(psca)、癌胚抗原(cea)、gtp酶激活蛋白(gap)、神经节苷脂g2(gd2)、cd5、前列腺特异性膜抗原(psma)、受体酪氨酸激酶样孤儿受体1(ror1)、cd123、cd70、cd38、b细胞成熟抗原(bcma)、粘蛋白1(muc1)、肝配蛋白a型受体2前体(epha2)、野生型表皮生长因子受体(egfrwt)、表皮生长因子受体变体iii(egfrviii)、白细胞介素13受体α2(il13ra2)、cd133、磷脂酰肌醇蛋白聚糖3(glypican3,gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白α(fap)、血管内皮生长因子受体2(vegfr2)、癌症/睾丸(ct)、鸟苷酸环化酶c(gucy2c)、肿瘤相关糖蛋白72(tag-72)、胸苷激酶1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖基转移酶(hprt1)。这些可以包含抗原结合结构域的重链和轻链,或者其由抗原结合结构域的cdr组成或包含抗原结合结构域的cdr。
[0326]
在一些实施方案中,本文公开的双特异性抗体的抗-taa抗原结合结构域识别并结合fms-样酪氨酸激酶3(flt3),即,为抗-flt3抗原结合结构域。在一些实施方案中,抗-flt3抗原结合结构域包含以下cdr中的一个或两个或三个或四个或五个或所有的六个,或基本上由其组成,或由其组成:cdrl1,其包含seqidno:15、seqidno:16或其各自的等效物,或基本上由其组成,或由其组成; cdrl2,其包含seq id no: 17、seq id no: 18或其各
自的等效物,或基本上由其组成,或由其组成;cdrl3,其包含seq id no: 19、seq id no: 20或其各自的等效物,或基本上由其组成,或由其组成;cdrh1,其包含seq id no: 21、seq id no: 22或其各自的等效物,或基本上由其组成,或由其组成;cdrh2,其包含seq id no: 23、seq id no: 24或其各自的等效物,或基本上由其组成,或由其组成;和cdrh3,其包含seq id no: 25、seq id no: 26或其各自的等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,其cdr等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合flt3。在一些实施方案中,抗-flt3抗原结合结构域包含以下,或者基本上由以下组成,或由以下组成:轻链可变区,其包含选自以下的序列:seq id no: 27、seq id no: 28或其各自的等效物,或基本上由其组成,或由其组成;和/或重链可变区,其包含选自以下的序列:seq id no: 29、seq id no: 30或其各自的等效物,或者基本上由其组成,或由其组成。在进一步的实施方案中,其可变区等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合flt3。
[0327]
在一些实施方案中,本文公开的双特异性抗体的抗-taa抗原结合结构域识别并结合表皮生长因子受体(egfr)(例如野生型egfr(egfrwt)和/或其变体(例如egfrviii))。该抗原结合结构域在本文中也称为抗-egfr抗原结合结构域。在一些实施方案中,抗-egfr抗原结合结构域包含以下cdr中的一个或两个或三个或四个或五个或六个,或基本上由其组成,或由其组成:cdrl1,其包含seq id no: 31、seq id no: 32或其各自的等效物的序列,或基本上由其组成,或由其组成; cdrl2,其包含seq id no: 33、seq id no: 34或其各自的等效物,或基本上由其组成,或由其组成;cdrl3,其包含seq id no: 35、seq id no: 36或其各自的等效物的序列,或基本上由其组成,或由其组成;cdrh1,其包含seq id no: 37、seq id no: 38或其各自的等效物,或基本上由其组成,或由其组成;cdrh2,其包含seq id no: 39、seq id no: 40或其各自的等效物的序列,或基本上由其组成,或由其组成;和cdrh3,其包含seq id no: 41、seq id no: 42或其各自的等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,其cdr等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合egfr。在一些实施方案中,抗-egfr抗原结合结构域包含以下,或基本上由以下组成,或由以下组成:轻链可变区,其包含选自seq id no: 43、seq id no: 44或其各自的等效物的序列,或基本上由其组成,或由其组成,和/或重链可变区,其包含选自seq id no: 45、seq id no: 46或其各自的等效物的序列,或基本上由其组成,或由其组成。在进一步的实施方案中,其可变区等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合egfr。
[0328]
在一些实施方案中,本文公开的双特异性抗体的抗-taa抗原结合结构域识别并结合bcma,即抗-bcma抗原结合结构域。在一些实施方案中,抗原结合结构域包含以下cdr中的一个或两个或三个或四个或五个或六个,或基本上由其组成,或由其组成:cdrl1,其包含seq id no: 47、seq id no: 48、seq id no: 49或其各自的等效物,或基本上由其组成,或由其组成;cdrl2,其包含seq id no: 50、seq id no: 51、seq id no: 52或其各自的等效物,或基本上由其组成,或由其组成;cdrl3,其包含seq id no: 53、seq id no: 54、seq id no: 55或其各自的等效物,或基本上由其组成,或由其组成;cdrh1,其包含seq id no: 56、seq id no: 57、seq id no: 58或其各自的等效物,或基本上由其组成,或由其组成;cdrh2,其包含seq id no: 59、seq id no: 60、seq id no: 61或其各自的等效物,或基本
上由其组成,或由其组成;和cdrh3,其包含seq id no: 62、seq id no: 63、seq id no: 64或其各自的等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,其cdr等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合bcma。在一些实施方案中,抗-bcma抗原结合结构域包含以下,或基本上由以下组成,或由以下组成:轻链可变区,其包含选自seq id no: 65、seq id no: 66、seq id no: 67或其各自的等效物的序列,或基本上由其组成,或由其组成,和/或重链可变区,其包含选自seq id no: 68、seq id no: 69、seq id no: 70或其各自的等效物的序列,或基本上由其组成,或由其组成。在进一步的实施方案中,其可变区等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合bcma。
[0329]
在一些实施方案中,本文公开的双特异性抗体的抗-taa抗原结合结构域识别并结合cs1,即抗-cs1抗原结合结构域。在一些实施方案中,抗-cs1抗原结合结构域包含以下cdr中的一个或两个或三个或四个或五个或六个,或基本上由其组成,或由其组成:cdrl1,其包含seq id no: 71或其等效物,或基本上由其组成,或由其组成;cdrl2,其包含seq id no: 72或其等效物,或基本上由其组成,或由其组成;cdrl3,其包含seq id no: 73或其等效物,或基本上由其组成,或由其组成;cdrh1,其包含seq id no: 74或其等效物,或基本上由其组成,或由其组成;cdrh2,其包含seq id no: 75或其等效物,或基本上由其组成,或由其组成;和cdrh3,其包含seq id no:76或其等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,其cdr等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合cs1。在一些实施方案中,抗cs1抗原结合结构域包含以下,或基本上由以下组成,或由以下组成:轻链可变区,其包含选自seq id no: 77、seq id no: 154、seq id no: 78或其各自的等效物的序列,或基本上由其组成,或由其组成,和/或重链可变区,其包含选自seq id no: 79、seq id no: 149、seq id no: 80、seq id no: 150或其各自的等效物的序列,或基本上由其组成,或由其组成。在进一步的实施方案中,其可变区等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合cs1。
[0330]
在一些实施方案中,抗-nkg2d抗原结合结构域包含以下互补决定区(cdr)中的一个或两个或三个或四个或五个或所有六个,或基本上由其组成,或由其组成:轻链互补决定区1(cdrl1),其包含sgsssnignnavn(seq id no: 6)或其等效物,或基本上由其组成,或由其组成;轻链互补决定区2(cdrl2),其包含yddllps(seq id no: 7)或其等效物,或基本上由其组成,或由其组成;轻链互补决定区3(cdrl3),其包含aawddslngpv(seq id no: 8)或其等效物,或基本上由其组成,或由其组成;重链互补决定区1(cdrh1),其包含gftfssy(seq id no: 9)或其等效物,或基本上由其组成,或由其组成;重链互补决定区2(cdrh2),其包含rydgsn(seq id no: 10)或其等效物,或基本上由其组成,或由其组成;和重链互补决定区3(cdrh3),其包含drglgdgtyfdy(seq id no: 11)或其等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,其cdr等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合nkg2d。在一些实施方案中,抗-nkg2d抗原结合结构域包含以下,或者基本上由以下组成,或者由以下组成:轻链可变区,其包含qsaltqpasvsgspgqsitiscsgsssnignavnwyqqlpgkapklliyyddllpsgvsdrfsgsksgtsaflaisglqsedeadyycaawddslngpvfgggtkltvl(seq id no:12)或其等效物,或基本上由其组成,或由其
组成;和/或重链可变区,其包含qvqlvesggglvkpggslrlscaasgftfssygmhwvrqapgkglewvafirydgsnkyyadsvkgrftisrdnskntlylqmnslraedtavyycakdrglgdgtyfdywgqgttvtvss(seq id no: 13)或其等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,其可变区等效物和/或包含该等效物、或基本上由该等效物组成、或由该等效物组成的抗原结合结构域识别并结合nkg2d。
[0331]
在一些实施方案中,参考蛋白质或多肽(例如cdr、可变区、抗原结合结构域或抗体)的等效物与参考蛋白质或多肽至少80%、或至少85%、或至少90%、或至少95%、或至少 96%、或至少97%、或至少98%、或至少99%相同。
[0332]
在一些实施方案中,参考蛋白质或多肽(例如cdr、可变区、抗原结合结构域或抗体)的等效物包含参考蛋白质或多肽的c末端至n末端的氨基酸序列,或基本上其组成,或由其组成。这种等效物在本文中也称为反向序列。例如,参考蛋白质或多肽包含以下,或基本上由以下组成,或还由以下组成:kasqdvitgva(seq id no: 71),并且其等效物包含以下,或基本上由以下组成,或还由以下组成:avgtivdqsak(seq id no: 151)。在cdr、可变区、抗原结合结构域或抗体作为参考蛋白或多肽的实施方案中,等效物仍然识别并结合参考的相同表位。
[0333]
在一些实施方案中,本文公开的抗原结合结构域进一步包含肽接头,例如,在两个cdr之间和/或其轻链可变区或其等效物与其重链可变区或其等效物之间。在一个实施方案中,肽接头包含ggggsggggsggggs(seq id no: 14)或其等效物,或基本上由其组成,或由其组成。在一些实施方案中,seq id no: 14的等效物可以是1至50个氨基酸的长度,例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个氨基酸。在一些实施方案中,seq id no: 14的等效物富含甘氨酸,尽管它也可以含有丝氨酸或苏氨酸。在一些实施方案中,seq id no: 14的等效物包含(ggggs)n,或基本上由其组成,或由其组成,其中n可以是1、或2、或3、或4、或5、或6、或7、或8、或9、或10、或11、或12、或13、或14、或15或更多的整数(seq id no: 134-135、14和136-147)。
[0334]
在一些实施方案中,双特异性抗体(bsab)进一步包含任选地在其n末端的信号肽,任选地引导双特异性抗体分泌出bsab或bsab-car表达细胞和/或促进双特异性抗体、其片段或等效物的分泌。在一些实施方案中,信号肽位于双特异性抗体的n末端,例如,在双特异性抗体的两个抗原结合结构域的n末端侧。在一些实施方案中,信号肽是il2信号肽。在一些实施方案中,信号肽包含myrmqllscialslalvtns(seq id no: 4)或其等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,seq id no: 4的等效物仍然指导双特异性抗体分泌出bsab或bsab-car表达细胞和/或促进双特异性抗体、其片段或等效物的分泌。另外地或替代地,seq id no: 4的等效物与seq id no: 4至少80%(例如至少 85%、至少90%、或至少91%、或至少92%、或至少93%,或至少94%、至少95%、至少96%、至少97%、至少98%或至少99%)相同。检测信号肽是否指导蛋白质从表达bsab或bsab-car的细胞中分泌出来的方法对于本领域技术人员是可用的,例如免疫染色显示出细胞培养物上清液中的这种蛋白质。
[0335]
在一些实施方案中,双特异性抗体(bsab)进一步包含可检测或纯化标志物。在一个实施方案中,可检测标志物包含ypydvpdya(seq id no: 84),或基本上由其组成,或由其组成。
[0336]
在一些实施方案中,本文公开的抗原结合结构域进一步包含免疫球蛋白、其突变体或其等效物的片段可结晶(fc)区。在一些实施方案中,fc区或其突变体是人fc区或其突变体。在一些实施方案中,fc区或其突变体是禽类(例如鸡)、或鼠、或牛、或猪、或骆驼、或美洲驼、或鲨鱼fc区或其突变体。在一个实施方案中,fc区包含eskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no: 81)或其等效物,或基本上由其组成,或由其组成。在一些实施方案中,fc区包含eskygppcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no: 82)或在对应于seq id no: 81的氨基酸(aa)16、aa17和aa79的位置具有突变的fc等效物,或基本上由其组成,或由其组成。在进一步的实施方案中,fc等效物、变体或突变体结合在免疫细胞和/或血小板上的fc受体。另外地或替代地,fc等效物、变体或突变体结合互补蛋白。在一些实施方案中,等效物相对于其参考包含1、或2、或3、或4、或5、或6、或7、或8、或9、或10、或11、或12、或13、或14、或15个或更多的突变。
[0337]
在一些实施方案中,双特异性抗体进一步包含两个抗原结合结构域之间的肽接头。在一些实施方案中,肽接头源自人肌肉醛缩酶(hma),任选地包含psgqagaaaslfvsnhay(seq id no: 83),或基本上由其组成,或由其组成。在一个实施方案中,肽接头包含ggggsggggsggggs(seq id no: 14)或其等效物,或基本上由其组成,或由其组成。在一些实施方案中,seq id no:14的等效物可以是1至50个氨基酸的长度,例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个氨基酸。在一些实施方案中,seq id no:14的等效物富含甘氨酸,尽管它也可以含有丝氨酸或苏氨酸。在一些实施方案中,seq id no: 14的等效物包含(ggggs)n,或基本上由其组成,或由其组成,其中n可以是1、或2、或3、或4、或5、或6、或7、或8、或9、或10、或11、或12、或13、或14、或15或更多的整数(seq id no: 134-135、14和136-147)。在一些实施方案中,本文的肽接头是可切割的肽。在进一步的实施方案中,本文的肽接头是自切割肽。在更进一步的实施方案中,本文的肽接头是t2a肽,任选地包含hvgsgegrgslltcgdveenpgp(seq id no: 85)或其等效物,或基本上由其组成,或由其组成。在一些实施方案中,seq id no: 85的等效物与seq id no: 85相比包含1、或2、或3、或4、或5、或6、或7、或8、或9、或10、或11、或12、或13、或14 、或15个或更多突变,并且仍然能够自我切割,从而从单个多肽释放两种产物。评估这种自切割的方法对本领域技术人员而言是可用的,例如通过蛋白质印迹检测产物和/或多肽的分子大小。
[0338]
在一些实施方案中,双特异性抗体包含以下,或基本上由以下组成,或由以下组成:任选地从n末端到c末端,任选的信号肽、抗taa重链可变区、第一任选的肽接头、抗taa轻链可变区、任选的fc区或其突变体或其各自的等效物、第二任选的肽接头、抗-nkg2d重链可变区、第三任选的肽接头、抗-nkg2d轻链可变区、任选的fc区或其突变体或其各自的等效物。
[0339]
在一些实施方案中,双特异性抗体包含以下,或基本上由以下组成,或由以下组
成:任选地从n末端到c末端,任选的信号肽、抗-taa重链可变区、第一任选的肽接头、抗-taa轻链可变区、任选的fc区或其突变体或其各自的等效物、第二任选的肽接头、抗-nkg2d轻链可变区、第三任选的肽接头、抗-nkg2d重链可变区、任选的fc区或其突变体或其各自的等效物。
[0340]
在一些实施方案中,双特异性抗体包含以下,或者基本上由以下组成,或者由以下组成:任选地从n末端到c末端,任选的信号肽、抗-taa轻链可变区、第一任选的肽接头、抗-taa重链可变区、任选的fc区或其突变体或其各自的等效物、第二任选的肽接头、抗-nkg2d重链可变区、第三任选的肽接头、抗-nkg2d轻链可变区、任选的fc区或其突变体或其各自的等效物。
[0341]
在一些实施方案中,双特异性抗体包含以下,或者基本上由以下组成,或者由以下组成:任选地从n末端到c末端,任选的信号肽、抗-taa轻链可变区、第一任选的肽接头、抗taa重链可变区、任选的fc区或其突变体或其各自的等效物、第二任选的肽接头、抗-nkg2d轻链可变区、第三任选的肽接头、抗-nkg2d重链可变区、任选的fc区或其突变体或其各自的等效物。
[0342]
在一些实施方案中,在双特异性抗体的c末端处的抗原结合结构域的可变区包含以下,或者基本上由以下组成,或由以下组成:反向序列,即,如果存在于单特异性抗体中,则为可变区序列的c末端至n末端。在进一步的实施方案中,在双特异性抗体的n末端的抗原结合结构域进一步包含fc区或其突变体或其各自的等效物。在更进一步的实施方案中,在进一步的实施方案中,在双特异性抗体的c末端处的抗原结合结构域进一步不包含fc区或其突变体或其各自的等效物。
[0343]
还提供了编码双特异性抗体的多核苷酸(例如分离的和/或工程化的多肽)和/或分离的核酸。多核苷酸和/或核酸可以进一步包含必需的调控序列,例如,用于在宿主细胞(例如哺乳动物或人类宿主细胞(例如t细胞或nk细胞))中表达的启动子,和/或增强子。在一些实施方案中,多核苷酸和/或核酸进一步包含指导car表达的第一调控序列。在进一步的实施方案中,调控序列包含以下中的一种或多种:启动子、内含子、增强子或多聚腺苷酸化信号。在一些实施方案中,启动子是cmv或ef1α启动子。在进一步的实施方案中,多核苷酸和/或分离的核酸可进一步包含编码可检测或纯化标志物(例如gfp)的多核苷酸,其可位于bsab编码多核苷酸的下游并由单独的调节元件(第二调控序列)(例如,任选地选自ef1α启动子的启动子)调节。对本领域技术人员显而易见的是,选择启动子用于宿主表达系统。如图3a所示,构建体可以进一步包含t2a(一种自切割2a基因)。在一些实施方案中,多核苷酸和/或核酸进一步包含编码自杀基因产物的自杀基因,所述自杀基因产物任选地选自以下中的一种或多种:hsv-tk(单纯疱疹病毒胸苷激酶)、胞嘧啶脱氨酶、硝基还原酶、羧酸酯酶、细胞色素p450或pnp(嘌呤核苷磷酸化酶)、截短的egfr或诱导型半胱天冬酶(“icasp”)。在进一步的实施方案中,多核苷酸和/或核酸进一步包含指导自杀基因产物表达的第三调控序列。在一个实施方案中,调控序列中的任何一种或两种或三种在细胞中是可诱导的或组成性激活的。在一个实施方案中,调控序列中的任何一种或两种或三种可以是细胞特异性的或组织特异性的。
[0344]
在一些实施方案中,多核苷酸和/或核酸包含以下,或基本上由以下组成,或由以下组成:
(i)编码信号肽的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 86、seq id no: 87或其各自的等效物,或基本上由其组成,或由其组成;(ii)编码接头肽的核苷酸序列,并且其中该核苷酸序列包含seq id no: 88,或基本上由其组成,或由其组成;(v)编码可切割肽的核苷酸序列,并且其中所述核苷酸序列包含:cacgtgggttctggagaaggacgcggttccttgttgacgtgtggcgatgtagaggaaaatccgggtcca(seq id no: 91)或其等效物,或基本上由其组成,或由其组成;(vi)编码接头的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 92或其等效物,或基本上由其组成,或由其组成;(vii)编码抗-bcma轻链可变区的核苷酸序列,并且其中所述核苷酸序列选自:seq id no: 93、seq id no: 94、seq id no: 95、seq id no: 96或其各自的等效物;(viii)编码抗-bcma重链可变区的核苷酸序列,并且其中所述核苷酸序列选自:seq id no: 97、seq id no: 98、seq id no:99或seq id no:100或其各自的等效物;(ix)编码抗-nkg2d轻链可变区的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 101或其等效物,或基本上由其组成,或由其组成;(x)编码抗-nkg2d重链可变区的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 102或其等效物,或基本上由其组成,或由其组成;(xi)编码抗-flt3轻链可变区的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 103或seq id no: 104或其各自的等效物,或基本上由其组成,或由其组成;(xii)编码抗-flt3重链可变区的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 105、seq id no: 106或其各自的等效物,或基本上由其组成,或由其组成;(xiii)编码抗-cs1轻链可变区的核苷酸序列,并且其中所述核苷酸序列包含seq id no: 107或其等效物,或基本上由其组成,或由其组成;和(xiv)编码抗-cs1重链可变区的核苷酸序列,并且其中该核苷酸序列包含seq id no: 108或其等效物,或基本上由其组成,或由其组成。
[0345]
在一些实施方案中,参考核苷酸序列的等效物编码与所述参考相同的氨基酸序列。在一些实施方案中,参考核苷酸序列的等效物与所述参考至少80%(例如至少 85%、至少90%、或至少91%、或至少92%、或至少93%、或至少94%、至少95%、至少 96%、至少97%、至少98%或至少99%)相同。另外地或替代地,参考核苷酸序列的等效物在高度严格条件下与所述参考的互补序列杂交。在一些实施方案中,高度严格条件包括约55℃至约68℃的培养温度;约1xssc至约 0.1xssc的缓冲液浓度;约55%至约75%的甲酰胺浓度;和大约1xssc、0.1xssc或去离子水的洗涤溶液。还提供了与本文公开的多核苷酸反向、互补或反向互补的多核苷酸。在一些实施方案中,本文公开的多核苷酸进一步包含可检测或纯化标志物和/或编码可检测或纯化标志物的序列。
[0346]
多核苷酸和/或分离的核酸可以插入到载体(例如表达载体(例如位于5'和3'ltr 之间的慢病毒载体))中。图1b是本公开的示例性慢病毒载体构建体,其中在一方面,抗肿瘤或抗癌抗体的抗原结合结构域不同于抗bmca抗体。正如对于技术人员显而易见的,构建体可以不包含标志物肽或纯化标志物。在一些实施方案中,载体是非病毒载体(例如质粒)。在一些实施方案中,载体是病毒载体,任选地选自逆转录病毒载体、慢病毒载体、腺病毒载体
和腺相关病毒载体。另外地或替代地,载体还包含指导编码抗体的多核苷酸和/或分离的核酸的复制和/或表达的调控序列。在进一步的实施方案中,调控序列包含以下中的一种或多种:启动子、内含子、增强子或多聚腺苷酸化信号。在一些实施方案中,载体还包含可检测或纯化标志物。
[0347]
bsab-car构建体因此,在一方面,本文提供的bsab-car(本文也称为bsab-car构建体、bsab-car多肽或多肽)包含以下,或基本上由以下组成,或由以下组成:(a)癌症或肿瘤靶向抗体的抗原结合结构域;(b)铰链结构域;(c)跨膜结构域;(d)细胞内结构域,以及双特异性抗体,其包含以下,或基本上由以下组成,或由以下组成:作为一个元件的nkg2d抗原结合结构域和选择来结合与car的抗原结合结构域相同的细胞类型的第二抗原结合结构域。在一方面,提供了一种多肽,其包含以下,或基本上由以下组成,或由以下组成:如本文公开的car和如本文公开的双特异性抗体。在一方面,提供了一种多肽,其包含以下,或基本上由以下组成,或由以下组成:(i)嵌合抗原受体(car)的氨基酸序列,其包含以下,或基本上由以下组成,或者由以下组成:(1)识别并结合癌细胞上的第一肿瘤相关抗原(taa)的抗原结合结构域(第一抗taa抗原结合结构域),条件是第一taa不是b细胞成熟抗原(bcma);(2)铰链结构域;(3)跨膜结构域;和(4)细胞内结构域;和(ii)双特异性抗体,其包含以下,或基本上由以下组成,或由以下组成:(1)识别并结合癌细胞上的第二taa的抗原结合结构域(第二抗-taa抗原结合结构域);和(2)识别并结合nkg2d的抗原结合结构域(抗-nkg2d抗原结合结构域)。在另一方面,提供了一种多肽,其包含以下,或基本上由以下组成,或由以下组成:(i)car的氨基酸序列,其包含以下,或基本上由以下组成,或由以下组成:(1)识别并结合bcma的抗原结合结构域(抗-bcma抗原结合结构域);(2)铰链结构域;(3)跨膜结构域;和(4)细胞内结构域;和(ii)双特异性抗体,其包含以下,或基本上由以下组成,或由以下组成:(1)识别并结合nkg2d的抗原结合结构域(抗-nkg2d抗原结合结构域)和(2)识别并结合cs1的抗原结合结构域(抗-cs1抗原结合结构域)。car元件可以进一步包含信号肽。信号肽也可以位于bsab-car构建体的bsab部分之前。在一些实施方案中,细胞内结构域包含一个或多个、或两个或更多个共刺激结构域,所述共刺激结构域可包含以下,或基本上由以下组成,或由以下组成:cd28共刺激信号区和/或4-1bb共刺激结构域。在一些实施方案中,第一taa和第二taa在相同的癌症或肿瘤类型和/或细胞上表达。在某些实施方案中,肿瘤靶向抗体的抗原结合结构域包含任选地通过接头肽连接的重链可变区和轻链可变区,或基本上由其组成,或由其组成。在一些实施方案中,重链和/或轻链可变区包含以下,或基本上由以下组成,或由以下组成:b细胞成熟抗原(bcma)和/或slamf7(也称为cs1或cd319)和/或其各自的等效物的抗体的相关cdr区。在一些实施方案中,肿瘤靶向抗体靶向bcma并且双特异性抗体靶向或结合相同的细胞或肿瘤类型(例如胶质母细胞瘤、mm或aml)。在一些实施方案中,重链和/或轻链可变区包含针对任一个b细胞成熟抗原(bcma)的抗体的氨基酸序列,或者基本上由其组成,或由其组成,并且双特异性抗体包含抗slamf7抗体(也称为抗cs1或抗cd319抗体)的cdr、重链和轻链或scfv和/或fv片段和/或其各自的等效物中的一个或多个。在一些实施方案中,构建体的car部分进一步包含信号域和/或信号肽,或基本上由其组成,或由其组成。在一些实施方案中,第一taa是bcma并且第二taa是cs1。在一些实施方案中,第一taa是cs1并且第二taa是bcma。
[0348]
在一些实施方案中,bsab包含抗-flt3抗体的抗原结合结构域,并且bsab部分包含抗-nkg2d的抗原结合结构域和-抗cd123抗体的抗原结合结构域。这种bsab是用于治疗aml的疗法,并且制造和使用这种bsabcar的方法包含在本公开的范围内。将有效量的bsab给药于患有aml的患者。这些方法可以辅以适当的诊断方法来诊断aml并监测治疗过程和毒性。在一些实施方案中,第一taa是flt3并且第二taa是cd123。在一些实施方案中,第一taa是cd123并且第二taa是flt3。
[0349]
在一些实施方案中,bsab包含抗-egfr抗体的抗原结合结构域,并且bsab部分包含抗-nkg2d的抗原结合结构域和抗-il13ra2抗体的抗原结合结构域。这种bsab是用于治疗胶质母细胞瘤的疗法,并且制造和使用该bsabcar的方法包含在本公开的范围内。将有效量的bsab给药于患有胶质母细胞瘤的患者。给药可以是局部(颅内给药)或全身给药。这些方法可以辅以适当的诊断方法来诊断胶质母细胞瘤并监测治疗过程和毒性。在一些实施方案中,第一taa是egfr并且第二taa是il13ra2。在一些实施方案中,第一taa是il13ra2并且第二taa是egfr。
[0350]
在某些实施方案中,bsab-car构建体进一步包含位于重链可变区和轻链可变区之间的接头多肽,或基本上由其组成,或由其组成。在一些实施方案中,接头多肽位于ndg2d的抗体片段和其他抗原结合部分,例如抗-cs1、抗-cd123或抗-il13ra2之间。在某些实施方案中,接头是甘氨酸-丝氨酸接头。在进一步的实施方案中,接头多肽包含序列(甘氨酸-丝氨酸)n,或者基本上由其组成,或进一步由其组成,其中n是1至6的整数(seqidno:110)(例如,其中n为4)。在一些实施方案中,bsab-car包含位于结合癌症或肿瘤细胞的抗体或抗原结合片段与双特异性抗体之间(例如,位于bmcacar与nkg2d抗原结合结构域之间)的自切割肽(例如t2a肽)。在一些实施方案中,bsab-car进一步包含自切割肽,例如位于nkg2d和结合癌症或肿瘤抗原(例如cs1)的第二抗原结合结构域之间的t2a肽。在一些实施方案中,这种car元件进一步包含信号域,或基本上由其组成,或由其组成。在进一步的实施方案中,信号肽位于抗nkg2d抗体的nkg2d抗原结合结构域之前。在一些实施方案中,这种car元件进一步包含信号肽,或基本上由其组成,或由其组成。在一些实施方案中,第一taa和第二taa中的任一个或两个是或选自:flt3、cd19、间皮素、人表皮生长因子受体2(her2)、前列腺干细胞抗原(psca)、癌胚抗原(cea)、cd33、gtp酶激活蛋白(gap)、神经节苷脂g2(gd2)、cd5、前列腺特异性膜抗原(psma)、受体酪氨酸激酶样孤儿受体1(ror1)、cd123、cd70、cd38、粘蛋白1(muc1)、肝配蛋白a型受体2前体(epha2)、表皮生长因子受体变体iii(egfrviii)、白细胞介素13受体α2(il13ra2)、cd133、磷脂酰肌醇蛋白聚糖3(gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白α(fap)、血管内皮生长因子受体2(vegfr2)、癌症/睾丸(ct)、鸟苷酸环化酶c(gucy2c)、肿瘤相关糖蛋白72(tag-72)、胸苷激酶1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖基转移酶(hprt1)。
[0351]
在一些实施方案中,bsab-car构建体(本文也称为多肽)进一步包含位于以下中的任意两个之间的肽接头:car;双特异性抗体;和任选的自杀基因产物。在一些实施方案中,bsab-car构建体还包含在car和bsab之间的肽接头。在一些实施方案中,此处的肽接头是可切割的肽。在进一步的实施方案中,此处的肽接头是自切割肽。在更进一步的实施方案中,此处的肽接头是t2a肽,任选地包含hvgsgegrgslltcgdveenpgp(seqidno:85)或其等效物,或基本上由其组成,或由其组成。在一些实施方案中,seqidno:85的等效物与seqid
no:85相比包含1、或2、或3、或4、或5、或6、或7、或8、或9、或10、或11、或12、或13、或14、或15个或更多个突变,并且仍然能够自我切割,从而从单个多肽释放两种产物。评估这种自切割的方法对于本领域技术人员是可用的,例如通过蛋白质印迹检测产物和/或多肽的分子大小。
[0352]
在一些实施方案中,bsab-car构建体(本文也称为多肽)进一步包含可检测或纯化标志物。
[0353]
进一步提供了编码这些bsab-car构建体的多核苷酸和载体。
[0354]
在一些实施方案中,bsab-car包含图1e中部分所示的结构,即单个bsab-car,其包含bcmacar、自切割肽(例如t2a)、nkg2dscfv和fc多肽、第二自切割肽(例如t2a)和cs1scfv和fc多肽,或基本上由其组成。bcmacar进一步包含铰链结构域、跨膜结构域和细胞内结构域。在一些实施方案中,car组分进一步包含信号域,或基本上由其组成,或由其组成。在一些实施方案中,bsab-car构建体包含位于氨基(n)末端和/或抗-nkg2d抗原结合结构域之前的信号肽,或基本上由其组成,或由其组成。本文提供了示例性的igg1信号肽,但其他肽是本领域已知的并且可以替代该肽。进一步提供了编码这些bsab-car构建体的多核苷酸和载体。
[0355]
在一些实施方案中,bsab-car包括图1f中部分所示的结构,即单个bsab-car,其包含以下或基本上由以下组成:bcma抗原结合多肽、自切割肽(例如t2a)、nkg2dscfv和fc多肽、hma多肽以及cs1scfv和fc多肽。bcmacar进一步包含铰链结构域、跨膜结构域和细胞内结构域。在一些实施方案中,bcmacar进一步包含位于氨基(n)末端或抗nkg2d抗原结合结构域之前的信号肽,或基本上由其组成,或由其组成。本文提供了示例性的igg1信号肽,但其他肽是本领域已知的并且可以替代该肽。进一步提供了编码这些bsab-car构建体的多核苷酸和载体。
[0356]
在一些实施方案中,bsab-car包括图1g中部分所示的结构,即单个bsab-car,其包含:(a)bcma抗原结合多肽、自切割肽(例如t2a)、nkg2dscfv和fc多肽、接头(例如g4s多肽)(seqidno:134)以及cs1scfv和fc多肽,或基本上由其组成。bcma进一步包含铰链结构域、跨膜结构域和细胞内结构域,或基本上由其组成。在一些实施方案中,该多肽进一步包含位于氨基末端或抗-nkg2d抗原结合结构域之前的信号肽,或基本上由其组成,或由其组成。本文提供了示例性的igg1信号肽,但其他肽是本领域已知的并且可以替代该肽。进一步提供了编码这些bsab-car构建体的多核苷酸和载体。
[0357]
在另一方面,本文提供了多核苷酸(例如分离的和/或工程化的多肽)和/或分离的核酸,它们在一个构建体中编码如上文公开的car构建体和双特异性抗体(“bsab-car构建体”)。抗原结合结构域可以来自任何合适的物种,例如鼠、人或人源化序列。在一方面,多核苷酸和/或分离的核酸编码靶向除bcma之外的癌症或肿瘤抗原的抗原结合片段以及双特异性抗体,例如来自抗cs1抗体的一个scfv和来自抗nkg2d抗体的一个scfv通过非免疫原性蛋白质接头(例如来自人肌肉醛糖(hma))连接在一起。在一些实施方案中,编码car构建体的多核苷酸和/或核酸位于编码bsab的核酸的5'处。在进一步的实施方案中,t2a编码元件位于5'处的car多核苷酸的和3'处的bsab之间。在一些实施方案中,编码car构建体的多核苷酸和/或核酸位于编码bsab的核酸的3'处。在进一步的实施方案中,t2a编码元件位于3'处的car多核苷酸和5'处的bsab之间。多核苷酸和/或核酸可以进一步包含必需的调控序列,
例如,用于在宿主细胞(例如哺乳动物或人类宿主细胞(例如t细胞或nk细胞))中表达的启动子。在一些实施方案中,多核苷酸和/或核酸进一步包含指导bsab-car构建体表达的第一调控序列。在进一步的实施方案中,调控序列包含以下中的一种或多种:启动子、内含子、增强子或多聚腺苷酸化信号。在一些实施方案中,启动子是位于编码car的多核苷酸5'处的ef1a或cmv启动子。在进一步的实施方案中,多核苷酸和/或分离的核酸可以进一步包含可检测或纯化标志物和/或编码可检测或纯化标志物的序列,所述标志物例如是gfp,其可以在bsab多核苷酸的下游并且在分离的调控元件(第二调控序列)(例如启动子,其任选地是ef1α启动子)的控制下。对于本领域技术人员显而易见的,启动子被选择来用于宿主表达系统。在一些实施方案中,多核苷酸和/或核酸进一步包含编码自杀基因产物的自杀基因,所述自杀基因产物任选地选自以下中的一种或多种:hsv-tk(单纯疱疹病毒胸苷激酶)、胞嘧啶脱氨酶、硝基还原酶、羧酸酯酶、细胞色素p450或pnp(嘌呤核苷磷酸化酶)、截短的egfr或诱导型半胱天冬酶(“icasp”)。在进一步的实施方案中,多核苷酸和/或核酸进一步包含指导自杀基因产物表达的第三调控序列。在一个实施方案中,调控序列中的任何一种或两种或三种在细胞中是可诱导的或组成性激活的。在一个实施方案中,调控序列中的任何一种或两种或三种可以是细胞特异性的或组织特异性的。
[0358]
在一些实施方案中,多核苷酸和/或核酸包含本文公开的编码car的多核苷酸和本文公开的编码双特异性抗体的多核苷酸,或基本上由其组成,或由其组成。在一些实施方案中,编码car的多核苷酸和编码双特异性抗体的多核苷酸是连续的。在一些实施方案中,编码car的多核苷酸的和编码双特异性抗体的多核苷酸的通过编码本文公开的可切割肽的序列而连接在一起。还提供了与本文公开的多核苷酸反向的、互补的或反向互补的多核苷酸。在一些实施方案中,本文公开的多核苷酸进一步包含可检测或纯化标志物和/或编码可检测或纯化标志物的序列。
[0359]
在与本文的任何公开内容相关的一些实施方案中,调控序列包含以下中的一项或多项:启动子、内含子、增强子或聚腺苷酸化信号,或基本上由其组成,或由其组成。
[0360]
多核苷酸和/或分离的核酸可以插入到载体中,例如表达载体(例如位于5'和3'ltr之间的慢病毒载体)。图3a是本公开的示例性慢病毒载体构建体。正如对于技术人员显而易见的,构建体可以不包含标志物肽或纯化标志物。在一些实施方案中,载体是非病毒载体,例如质粒。在一些实施方案中,载体是病毒载体,任选地选自逆转录病毒载体、慢病毒载体、腺病毒载体和腺相关病毒载体。另外地或替代地,载体进一步包含指导编码bsab-car的多核苷酸和/或分离的核酸的复制和/或表达的调控序列。在进一步的实施方案中,调控序列包含以下中的一种或多种:启动子、内含子、增强子或多聚腺苷酸化信号。在一些实施方案中,载体还包含可检测或纯化标志物。
[0361]
宿主细胞和制备car的过程本公开的方面涉及一种包含car、bsab和/或bsab-car的细胞(其在本文中也称为宿主细胞)(例如分离的和/或工程化的细胞),以及生产这种细胞的方法。在一方面,提供了一种分离的或工程化的细胞,其包含以下中的一种或多种:本文公开的多肽、本文公开的多核苷酸或本文公开的载体。该细胞是原核或真核细胞。在一些实施方案中,细胞是t细胞、b细胞、nk细胞、nkt细胞、树突细胞、骨髓细胞、单核细胞、巨噬细胞、其任何亚群或任何其他免疫细胞。在一些实施方案中,细胞是免疫细胞,任选地选自t细胞、b细胞、nk细胞、nkt细
胞、树突细胞、骨髓细胞、单核细胞、巨噬细胞。在进一步的实施方案中,免疫细胞来源于造血干细胞(hsc)和/或诱导多能干细胞(ipsc)。真核细胞可以来自任何优选的物种,例如动物细胞、哺乳动物细胞(例如人、牛细胞、鼠细胞、马细胞、猫细胞或犬细胞)。细胞可以来自患者、供体或细胞系(例如那些现成可用的)。细胞对于被治疗的对象可以是自体的或同种异体的。在一些实施方案中,细胞进一步包含可检测或纯化标志物。在一些实施方案中,细胞表达本文公开的car。另外地或替代地,细胞表达本文公开的双特异性抗体。在进一步的实施方案中,细胞在细胞外分泌双特异性抗体。还提供了一种细胞群,其包含本文公开的细胞,或基本上由其组成,或由其组成。在进一步的实施方案中,细胞群是基本上同质的。
[0362]
在特定的实施方案中,分离的细胞包含以下,或基本上由以下组成,或由以下组成:外源性(例如对于细胞或细胞种类)car或bsabcar,其包含癌症或肿瘤抗体的抗原结合结构域、cd8α铰链结构域、cd8α跨膜结构域、cd28共刺激信号区和/或4-1bb共刺激信号区和cd3ζ信号区,或基本上由其组成,或由其组成。在一个单独的实施方案中,分离的细胞进一步包含如本文所公开的bsab。在又一个实施方案中,细胞包含如本文所公开的bsab。在某些实施方案中,分离的细胞是t细胞,例如动物t细胞、哺乳动物t细胞、猫t细胞、犬t细胞或人t细胞。在某些实施方案中,分离的细胞是nk细胞,例如动物nk细胞、哺乳动物nk细胞、猫nk细胞、犬nk细胞或人nk细胞。在某些实施方案中,分离的细胞是nkt细胞,例如动物nkt细胞、哺乳动物nkt细胞、猫nkt细胞、犬nkt细胞或人nkt细胞。在某些实施方案中,分离的细胞是b细胞,例如动物b细胞、哺乳动物b细胞、猫b细胞、犬b细胞或人b细胞。应当理解,对于树突细胞、骨髓细胞、单核细胞、巨噬细胞、这些细胞的任何亚群或如所述的t细胞、nk细胞、ntt细胞和b细胞和/或任何其他免疫细胞,相同或相似的实施方案都是适用的。在一方面,细胞是t细胞,其已通过基因编辑技术(例如crispr或talen)而被修饰以去除cd52表达。
[0363]
在某些实施方案中,本文公开了产生bsab、car和/或car或bsab-car表达细胞(任选地分泌bsab)的方法,该方法包含以下步骤,或基本上由以下步骤组成,或由以下步骤组成:使用编码bsab、car、bsab和car和/或bsabcar的核酸序列(例如如本文所公开的多核苷酸和/或载体)转导本文所述的细胞或本文所述的细胞群或分离的细胞群。在进一步的实施方案中,选择已经成功地用核酸序列转导的细胞亚群。在一些实施方案中,分离的细胞是t细胞、动物t细胞、哺乳动物t细胞、猫t细胞、犬t细胞或人t细胞,从而产生bsab、car、bsab和car和/或bsabcart细胞。在某些实施方案中,分离的细胞是nk细胞,例如动物nk细胞、哺乳动物nk细胞、猫nk细胞、犬nk细胞或人nk细胞,从而产生bsab、car、bsab和car和/或bsabcarnk细胞。在某些实施方案中,分离的细胞是nkt细胞,例如动物nkt细胞、哺乳动物nkt细胞、猫nkt细胞、犬nkt细胞或人nkt细胞,从而产生bsab、car、bsab和car和/或bsabcarnkt细胞。在一些实施方案中,分离的细胞是b细胞、动物b细胞、哺乳动物b细胞、猫b细胞、犬b细胞或人b细胞,从而产生bsab、car、bsab和car和/或bsabcarb细胞。应当理解,对于树突细胞、骨髓细胞、单核细胞、巨噬细胞、这些或所描述的t细胞、nk细胞和b细胞的任何亚群和/或任何其他免疫细胞,相同或相似的实施方案都是适用的。在一些实施方案中,细胞选自造血干细胞(hsc)、诱导多能干细胞(ipsc)或免疫细胞。在一些实施方案中,细胞群包含造血干细胞(hsc)、诱导多能干细胞(ipsc)或免疫细胞,或基本上由其组成,或由其组成。在一些实施方案中,免疫细胞选自t细胞、b细胞、nk细胞、nkt细胞、树突细胞、骨髓细胞、单核细胞或巨噬细胞。在一些实施方案中,免疫细胞来源于hsc和/或ipsc。在一个实施方案中,
所述细胞是t细胞,其已经使用基因编辑技术(例如crispr或talen)修饰以去除cd52表达。在一方面,细胞对于被治疗的对象是自体的或同种异体的。
[0364]
分离的细胞的来源。在本文公开的细胞的扩增和遗传修饰之前,可以从对象——例如,在涉及自体治疗的实施方案中——或市售的细胞系或培养物或干细胞(如诱导多能干细胞( ipsc))中获得细胞。
[0365]
可以从对象的多种来源获得细胞,包括对象的外周血单核细胞、骨髓、淋巴结组织、脐带血、胸腺组织、感染部位的组织、腹水、胸腔积液、脾组织和肿瘤。分离相关细胞的方法在本领域中是众所周知的并且可以很容易地适用于本技术;在下文的实施例中描述了示例性方法。与本公开相关的用于分离的方法包括但不限于life technologies dynabeads
®ꢀ
system;stemcell technologies easysep
™
、robosep
™
、rosettesep
™
、sepmate
™
; miltenyi biotec macs
™
细胞分离试剂盒和其他市售细胞分离和分隔试剂盒。免疫细胞的特定亚群可以通过使用对独特的细胞表面标志物具有特异性的珠子或此类试剂盒中可用的其他结合剂来分离。 例如,macs
™ꢀ
cd4+和cd8+微珠可用于分离cd4+和cd8+ t细胞。可根据已知技术分离的细胞的替代而非限制性实例包括大量t细胞、nk t细胞和γδt细胞。
[0366]
或者,可以通过市售的细胞培养物获得细胞,包括但不限于:对于t细胞,bcl2(aaa)jurkat(atcc
®ꢀ
crl-2902
™
)、bcl2(s70a)jurkat(atcc
®ꢀ
crl
‑ꢀ
2900
™
)、bcl2(s87a)jurkat(atcc
®ꢀ
crl-2901
™
)、bcl2 jurkat(atcc
®ꢀ
crl-2899
™
)、neo jurkat(atcc
®ꢀ
crl-2898
™
)细胞系;对于b细胞,ahh-1(atcc
®ꢀ
crl-8146
™
)、bc-1(atcc
®ꢀ
crl-2230
™
)、bc-2(atcc
®ꢀ
crl-2231
™
)、bc-3(atcc
®ꢀ
crl-2277
™
)、ca46(atcc
®ꢀ
crl-1648
™
)、dg-75 [dg-75](atcc
®ꢀ
crl-2625
™
)、ds-1(atcc
®ꢀ
crl-11102
™
)、eb-3 [eb3](atcc
ꢀ®ꢀ
ccl-85
™
)、z-138(atcc #crl-3001)、db(atcc crl-2289)、toledo(atcc crl-2631)、 pfiffer(atcc crl-2632)、sr(atcc crl-2262)、jm-1(atcc crl-10421)、nfs-5 c-1(atcc crl-1693);nfs-70 c10(atcc crl-1694)、nfs-25 c-3(atcc crl-1695)和sup-b15(atcc crl-1929)细胞系;对于nk细胞,nk-92(atcc
®ꢀ
crl-2407
™
)、nk-92mi(atcc
®ꢀ
crl-2408
™
)细胞系。其他实例包括但不限于:成熟t细胞系,例如deglis、ebt-8、hpb-mlp-w、hut 78、hut 102、karpas 384、ki 225、my-la、se-ax、skw
‑ꢀ
3、smz-1和t34;未成熟t细胞系,例如 all-sil、be13、ccrf-cem、cml-t1、dnd-41、du.528、eu-9、hd-mar、hpb-all、h-sb2、ht-1、 jk-t1、jurkat、karpas 45、ke-37、kopt-k1、k-t1、l-kaw、loucy、mat、molt-1、molt 3、molt-4、molt 13、molt-16、mt-1、mt-all、p12/ichikawa、peer、per0117、per-255、pf-382、pfi-285、rpmi-8402、st-4、sup-t1到t14、tall-1、tall-101、tall-103 /2、tall-104、tall-105、tall-106、tall-107、tall-197、tk-6、tlbr-1、-2、-3和-4、ccrf-hsb-2(ccl-120.1)、j.rt3-t3.5(atcc tib-153)、j45.01(atcc crl-1990)、j.cam1.6(atcc crl-2063)、rs4;11(atcc crl-1873)、ccrf
‑ꢀ
cem(atcc crm-ccl-119);皮肤t细胞淋巴瘤系,例如hut78(atcc crm-tib-161)、mj[g11](atcc crl-8294)、hut102(atcc tib-162);源自间变性和大细胞淋巴瘤的b细胞系,例如 del、dl-40、fe-pd、jb6、karpas 299、ki-jk、mac-2a ply1、sr-786、su-dhl-1、-2、-4、-5、-6、-7、-8、-9、-10和-16、dohh-2、nu-dhl-1、u-937、granda 519、usc-dhl-1、rl;霍奇金淋巴瘤,例如dev、hd-70、hdlm-2、hd-myz、hkb-1、km-h2、l 428、l 540、l1236、sbh-1、sup-hd1和su/rh-hd-l;和nk细胞系,例如 hank1、khyg-1、nkl、nk-ys、noi-90和yt。
无效白血病细胞系(null leukemia cell lines),包括但不限于 reh、nall-1、km-3、l92-221,是另一种可商购的免疫细胞来源,同样的是源自其他白血病和淋巴瘤的细胞系,例如k562红白血病(erythroleukemia)、thp-1单核细胞白血病、u937淋巴瘤、hel红白血病、hl60白血病、hmc-1白血病、kg-1白血病、u266骨髓瘤。此类可商购的细胞系的非限制性示例性来源包括美国典型培养物保藏中心或atcc (atcc.org/)和德国微生物和细胞培养物保藏中心( german collection of microorganisms and cell cultures)(dsmz.de/)。
[0367]
在一些实施方案中,表达所公开的car的t细胞可以被进一步修饰以减少或消除内源性tcr的表达。减少或消除内源性tcr可以减少脱靶效应并提高t细胞的有效性。可以使用多种方法产生稳定地缺乏功能性tcr表达的t细胞。t细胞将整个t细胞受体作为混合物内化、分类和降解,在静息t细胞中的半衰期约为 10小时且在受刺激的t细胞中为3小时(von essen, m. et al. 2004. j. immunol. 173:384-393)。tcr复合物的正常功能需要组成tcr复合物的蛋白质的适当化学计量比。tcr功能还需要两个具有itam基序的功能性tcrζ蛋白。tcr在与其mhc肽配体结合后的激活需要多个tcr在同一个t细胞上的结合,所有这些都必须正确地发出信号。因此,如果tcr复合物因不能正确地结合或不能以最佳方式发出信号的蛋白质而不稳定,则t细胞将不会被充分激活以开始细胞反应。
[0368]
因此,在一些实施方案中,tcr表达可以使用rna干扰(例如,shrna、sirna、mirna 等)、crispr或其他靶向编码特定tcr(例如,tcr-α和tcr-β)的核酸和/或原代t 细胞中的cd3链的方法来消除。通过阻断这些蛋白质的一种或多种的表达,t细胞将不再产生tcr复合物的关键成分中的一种或多种,从而使tcr复合物不稳定并阻止功能性tcr的细胞表面表达。即使在使用rna干扰时的一些tcr复合物可以再循环到细胞表面,但rna(例如 shrna、sirna、mirna等)会阻止tcr蛋白的新产生,从而导致整个tcr复合物的降解和去除,致使产生在功能性tcr表达中具有稳定缺陷的t细胞。
[0369]
抑制性rna(例如,shrna、sirna、mirna等)在原代t细胞中的表达可以使用任何常规表达系统(例如慢病毒表达系统)来实现。尽管慢病毒可用于靶向静息原代t细胞,但并非所有t细胞都会表达shrna。这些t细胞中的一些可能无法表达足够量的rna,从而无法充分抑制tcr表达以改变t细胞的功能活性。因此,可以去除在病毒转导后保留中至高度tcr表达的t细胞,例如,通过细胞分选或分离技术使剩余的t细胞缺乏细胞表面tcr或cd3,从而能够扩增缺乏功能性tcr或cd3 表达的分离的t细胞群。
[0370]
使用传统的crispr/cas系统可以实现crispr在原代t细胞中的表达,并引导特定于靶向tcr的rna。合适的表达系统(例如慢病毒或腺病毒表达系统)是本领域已知的。与抑制剂rna的递送类似,crispr系统可用于在car细胞疗法中特异性靶向静息原代t细胞或其他适合的免疫细胞。此外,在crispr编辑不成功的情况下,可以根据上文公开的方法选择细胞以获得成功。例如,如上文所述,在病毒转导后保留中至高度tcr表达的t细胞可以被去除,例如,通过细胞分选或分离技术,使得剩余的t细胞缺乏细胞表面tcr或cd3,从而能够扩增缺乏功能性tcr或cd3表达的分离的t细胞群。还应了解,crispr编辑构建体可用于敲除内源性tcr和敲除本文公开的car构建体。因此,应当理解,可以设计crispr系统以实现这些目的中的一个或两个。
[0371]
载体(vector)。car细胞可以使用载体来制备。本公开的方面涉及编码(i)car或(ii)编码免疫调节分子的多核苷酸的分离的核酸序列,以及载体,所述载体包括这些核酸
和/或它们各自的互补序列和/或等效物中的一种或两种,或基本上由其组成,或由其组成。
[0372]
在一些实施方案中,编码car组分的分离的核酸序列包含癌症或肿瘤靶向抗体的抗原结合结构域、cd8α铰链结构域、cd8α跨膜结构域、cd28共刺激信号区和/或4-1bb共刺激信号区和cd3ζ信号区,或基本上由其组成,或由其组成。在特定的实施方案中,分离的核酸序列包含编码以下的序列:(a)癌症或肿瘤靶向抗体的抗原结合结构域,随后是(b)cd8α铰链结构域,(c)cd8α跨膜结构域,随后是(d)cd28共刺激信号区和/或4-1bb共刺激信号区,随后是(e)cd3ζ信号区,或者基本上由其组成,或者由其组成。在一些实施方案中,编码car组分的分离的核酸序列包含编码癌症或肿瘤靶向抗体的抗原结合结构域的序列上游的kozak共有序列,或者基本上由其组成,或由其组成。在一方面,抗原结合结构域靶向bcma、flt3或egfr、或cd19、cd123或il13ra2。在一方面,抗原结合结构域靶向her2。在一方面,抗原结合结构域靶向psca。在一方面,抗原结合结构域靶向cea。在一方面,抗原结合结构域靶向gap。在一方面,抗原结合结构域靶向gd2。在一方面,抗原结合结构域靶向cd5。在一方面,抗原结合结构域靶向psma。在一方面,抗原结合结构域靶向ror1。在一方面,抗原结合结构域靶向cd123。在一方面,抗原结合结构域靶向cd70。在一方面,抗原结合结构域靶向cd38。在一方面,抗原结合结构域靶向muc1。在一方面,抗原结合结构域靶向epha2。在一方面,抗原结合结构域靶向egfrviii。在一方面,抗原结合结构域靶向il13ra2。在一方面,抗原结合结构域靶向cd133。在一方面,抗原结合结构域靶向gpc3。在一方面,抗原结合结构域靶向epcam。在一方面,抗原结合结构域靶向fap。在一方面,抗原结合结构域靶向vegfr2。在一方面,抗原结合结构域靶向癌症/睾丸抗原。在一方面,抗原结合结构域靶向gucy2c。在一方面,抗原结合结构域靶向tag-72。在一方面,抗原结合结构域靶向tk1。在一方面,抗原结合结构域靶向hprt1。
[0373]
在一些实施方案中,分离的核酸包含编码双特异性抗体的多核苷酸,或基本上由其组成,或由其组成。在某些实施方案中,双特异性抗体包含相关cdr区或scfv、或nkg2d抗体的scfv和fv、以及任选的抗slamf7(也称为cs1或cd319)的抗原结合结构域,例如任选地经密码子优化的scfv和fv或scfv多肽,或其各自的等价物,或基本上由其组成,或由其组成。在某些实施方案中,双特异性抗体包含针对nkg2d的抗体和针对slamf7(也称为cs1或cd319)的抗体(任选地经过密码子优化)的相关cdr区或其各自的等效物,或基本上由其组成,或由其组成。在一些实施方案中,双特异性抗体包含针对nkg2d的抗体和针对slamf7(也称为cs1或cd319)的抗体(任选地经过密码子优化)的重链和/或轻链可变区和/或其各自的等效物,或基本上由其组成,或由其组成。在一些实施方案中,双特异性抗体包含源自针对nkg2d的抗体的单链可变区片段(scfv)或来自针对nkg2d的抗体的scfv和fc片段,以及任选的针对slamf7(也称为cs1或cd319)的抗体(任选地经过密码子优化)的单链可变区片段(scfv)和任选的scfv和fc片段和/或其各自的等效物。在一些实施方案中,分离的核酸包含编码可操作地连接至启动子的双特异性抗体的多核苷酸序列,或基本上由其组成,或由其组成,所述启动子可根据上文公开的方法产生。
[0374]
在一些实施方案中,分离的核酸包含可检测的标记和/或赋予抗生素抗性的多核苷酸。在一方面,标记或多核苷酸可用于选择用分离的核酸成功转导的细胞。
[0375]
在一些实施方案中,分离的核酸序列包含在载体中。在某些实施方案中,载体是质粒。在其他实施方案中,载体是病毒载体。此类载体的非限制性实例包括但不限于逆转录病
毒载体、慢病毒载体、腺病毒载体和腺相关病毒载体。在特定实施方案中,载体是慢病毒载体。
[0376]
示例性载体的制备和使用所述载体的car表达细胞的产生在以下实施例中详细讨论。总体来说,编码car或免疫调节分子的天然的或合成的核酸的表达通常通过将编码car多肽或其部分的核酸可操作地连接至启动子,并将构建体掺入表达载体中来实现。类似的方法可用于构建包含编码免疫调节分子的多核苷酸的分离的核酸序列。载体可适合于在真核生物中复制和整合。用于产生包含载体和/或外源核酸的细胞的方法是本领域众所周知的。参见,例如,sambrooketal.(2001,molecularcloning:alaboratorymanual,coldspringharborlaboratory,newyork)。在一方面,术语“载体”是指一种重组载体,它保留感染和转导非分裂和/或缓慢分裂细胞并整合到靶细胞基因组中的能力。在一些方面,载体源自或基于野生型病毒。在进一步的方面,载体源自或基于野生型慢病毒。这样的例子包括但不限于人类免疫缺陷病毒(hiv)、马传染性贫血病毒(eiav)、猿免疫缺陷病毒(siv)和猫免疫缺陷病毒(fiv)。或者,可用作载体骨架的基础的其他逆转录病毒(例如鼠白血病病毒(mlv))也在预期内。显然,根据本公开的病毒载体不必局限于特定病毒的成分。病毒载体可以包含源自两种或更多种不同病毒的成分,也可以包含合成成分。可以操纵载体成分以获得所需的特征,例如靶细胞特异性。
[0377]
本公开的重组载体来源于灵长类动物和非灵长类动物。灵长类慢病毒的例子包括人类免疫缺陷病毒(hiv)、人类获得性免疫缺陷综合征(aids)的病原体和猿免疫缺陷病毒(siv)。非灵长类慢病毒组包括原型“慢发病毒”visna/maedi病毒(vmv),以及相关的山羊关节炎脑炎病毒(caev)、马传染性贫血病毒(eiav)和近期描述的猫免疫缺陷病毒(fiv)和牛免疫缺陷病毒(biv)。现有技术的重组慢病毒载体是本领域已知的,例如,参见美国专利号6,924,123;7056699;7,419,829和7,442,551,其通过引用并入本文。
[0378]
美国专利号6,924,123公开了某些逆转录病毒序列有助于整合到靶细胞基因组中。该专利教导了每个逆转录病毒基因组都包含称为gag、pol和env的基因,它们编码病毒体蛋白和酶。这些基因的两侧是被称为长末端重复(ltr)的区域。ltr负责前病毒整合和转录。它们还用作增强子-启动子序列。换句话说,ltr可以控制病毒基因的表达。逆转录病毒rna的衣壳化是通过位于病毒基因组5'端的psi序列发生的。ltr本身是相同的序列,其可以分为三个元件,称为u3、r和u5。u3来源于rna3'末端的独特序列。r来源于rna两端重复的序列,u5来源于rna5'端独有的序列。这三个元件的大小在不同的逆转录病毒中可能有很大差异。对于病毒基因组,poly(a)添加(终止)的位点位于在右侧ltr中r和u5之间的边界处。u3含有前病毒的大部分转录控制元件,其包括启动子和多个增强子序列,这些序列响应于细胞转录激活蛋白以及在某些情况下响应于病毒转录激活蛋白。关于结构基因gag、pol和env本身,gag编码病毒的内部结构蛋白。gag蛋白被蛋白水解加工成成熟蛋白ma(基质)、ca(衣壳)和nc(核衣壳)。pol基因编码逆转录酶(rt),其含有dna聚合酶、相关的rnaseh和整合酶(in),它们介导基因组的复制。对于病毒载体颗粒的生产,载体rna基因组在宿主细胞中由编码它的dna构建体来表达。不由载体基因组编码的颗粒的组分由在宿主细胞中表达的附加核酸序列(“包装系统”,其通常包括gag/pol和env基因中的一项或两者)反式提供。生产病毒载体颗粒所需的
md.))中来生产高滴度的含有重组逆转录病毒的上清液。在本公开的另一种方法中,这样瞬时转染的第一细胞群而后与哺乳动物靶细胞(例如人淋巴细胞)共培养以高效转导具有外源基因的靶细胞。在本公开的又一方法中,将来自上述瞬时转染的第一细胞群的上清液与哺乳动物靶细胞(例如人淋巴细胞或造血干细胞)一起培养以高效地用外源基因转导靶细胞。
[0384]
在另一方面,包装载体在能够产生病毒的第一哺乳动物细胞群中稳定表达,例如人胚肾细胞(例如293细胞)。逆转录病毒或慢病毒载体通过用可选择标志物共转染或用假型病毒感染来引入细胞。在这两种情况下,载体整合。或者,载体可以被引入进游离型维持质粒中。产生含有高滴度重组逆转录病毒的上清液。
[0385]
car细胞的激活和扩增。无论是在对细胞进行基因修饰以表达所需的car之前或之后,都可以使用通常已知的方法激活和扩增细胞,这些方法例如是在以下美国专利号中所描述的;6,534,055; 6,905,680;6,692,964;5,858,358;6,887,466;6,905,681;7,144,575; 7,067,318;7,172,869;7,232,566;7,175,843; 5,883,223;6,905,874; 6,797,514;6,867,041和参考文献,例如lapateva et al. (2014) crit rev oncog 19(1-2):121-32;tam et al. (2003) cytotherapy 5(3):259-72;garcia-marquez et al. (2014) cytotherapy 16(11):1537-44。用离体的肿瘤相关抗原刺激可以激活和扩增选定的car表达细胞亚群。或者,细胞可以通过与肿瘤相关抗原相互作用而在体内被激活。对于某些免疫细胞,可能需要额外的细胞群、可溶性配体和/或细胞因子或刺激剂来激活和扩增细胞。相关试剂是本领域公知的并且根据已知的免疫学原理来进行选择。例如,可溶性cd-40配体可以有助于激活和扩大某些b细胞群;类似地,辐照的饲养细胞可用于激活和扩增nk细胞的过程。
[0386]
激活相关细胞的方法在本领域中是公知的并且可以很容易地适用于本技术;在下文的实施例中描述了示例性方法。与本公开相关的用于分离的方法包括但不限于life technologies dynabeads
®ꢀ
system激活和扩增试剂盒;bd biosciences phosflow
™
激活试剂盒、miltenyi biotec macs
™ꢀ
激活/扩增试剂盒和其他特定于激活相关细胞基团的市售细胞试剂盒。特定的免疫细胞亚群可以通过使用此类试剂盒中珠子或可用的其他试剂来激活或扩增。例如,α-cd3/α-cd28 dynabeads
®
可用于激活和扩增分离的t细胞群。
[0387]
使用方法治疗应用。本公开的方法方面涉及用于在体外或体内抑制肿瘤或癌细胞(例如,mm、aml或gb细胞)的生长和/或用于治疗有需要的癌症患者的方法。在一些实施方案中,肿瘤是实体瘤。在一些实施方案中,癌症是影响血液和/或骨髓的癌症,例如mm。在一些实施方案中,癌症或肿瘤细胞表达或过表达癌症或肿瘤抗原cs1。当在体外实践时,这些方法提供了用于精准医学应用的体外测定和用于测试新组合和疗法的有用的测定。
[0388]
在一方面,提供了一种抑制表达肿瘤相关抗原(taa)的癌细胞或包含该癌细胞的组织的生长的方法。该方法包含使癌细胞或组织与可选地有效量的如本文公开的分离的或工程化的细胞或细胞群接触,或基本上由其组成,或由其组成。在一些实施方案中,该接触是体外或体内的。在一些实施方案中,该接触是在体内进行的,并且分离的细胞对于被治疗对象是自体的或同种异体的。在一些实施方案中,该接触是在体内进行的,并且分离的细胞对于被治疗对象是同种异体的。在一些实施方案中,该方法进一步包含使癌细胞或组织与
有效量的细胞减灭疗法或上调taa表达的疗法接触。在一些实施方案中,细胞减灭疗法包括化学疗法、冷冻疗法、热疗法、靶向疗法和/或放射疗法。在一些实施方案中,癌细胞表达第一taa或如本文公开的bcma。另外地或替换地,癌细胞表达第二taa或如本文所公开的cs1。
[0389]
在一方面,提供了一种用于以下中的一项或多项的方法:在有需要的对象中抑制癌症的生长、抑制癌症的转移或治疗癌症。该方法包括向有需要的对象施用例如有效量的本文公开的分离的或工程化的细胞或细胞群,或基本上由其组成,或由其组成。在一些实施方案中,分离的或工程化的细胞对于有需要的对象是自体的。在一些实施方案中,分离的或工程化的细胞对于有需要的对象是同种异体的。在一些实施方案中,通过确定以下中的一项或两项的表达来选择对象以用于疗法:如本文所公开的第一taa或bcma,和/或如本文所公开的第二taa或cs1。在进一步的实施方案中,通过使对象的样品在体外或体内与与识别和结合taa或bcma或cs1的抗原结合结构域接触,并检测样品与抗原结合结构域之间的结合来确定表达。在更进一步的实施方案中,抗原结合结构域进一步包含可检测标志物。在一些实施方案中,该方法进一步包含向对象施用有效量的细胞减灭疗法或上调taa表达的疗法。在一些实施方案中,细胞减灭疗法包含化学疗法、冷冻疗法、热疗、靶向疗法和/或放射疗法。
[0390]
在一方面,提供了一种用于治疗被选为治疗对象中的癌症的方法。该方法包含向对象施用例如有效量的本文公开的分离的或工程化的细胞或细胞群,或基本上由其组成,或由其组成。在一些实施方案中,如果对象的癌细胞表达以下中的一项或两项,则被选择为对象:如本文公开的第一taa或bcma,和/或如本文公开的第二taa或cs1。在一些实施方案中,taa表达通过使对象的样品在体外或体内与识别并结合taa或bcma或cs1的抗原结合结构域接触,并检测样品与抗原结合结构域之间的结合来确定。在进一步的实施方案中,抗原结合结构域进一步包含可检测标志物。在一些实施方案中,分离的或工程化的细胞相对于有需要的对象是自体的。在一些实施方案中,分离的或工程化的细胞相对于有需要的对象是同种异体的。
[0391]
在某些实施方案中,这些方法包含向对象或患者施用包含car的分离的细胞(例如,有效量),或基本上由其组成,或由还进一步其组成。在进一步的实施方案中,这种分离的细胞包含或表达car和/或双特异性抗体。在一些实施方案中,car的抗原结合结构域包含bcma抗体或除b细胞成熟抗原(bcma)和/或slamf7(也称为cs1或cd319)以外的抗体的相关cdr区和/或其各自的等效物,或基本上由其组成,或进一步由其组成。在一些实施方案中,car的抗原结合结构域包含除bcma和/或slamf7(也称为cs1或cd319)之外的抗原的抗体的重链和/或轻链可变区和/或其各自的等效物,或基本上由其组成,或进一步由其组成。在更进一步的实施方案中,分离的细胞是t细胞或nk细胞。在一些实施方案中,双特异性抗体包含nkg2d配体和可选地slamf7(也称为cd319或cs1)配体,或基本上由其组成,或进一步由其组成。在某些实施方案中,双特异性抗体包含nkg2d和可选地slamf7(也称为cs1或cd319)的抗体的相关cdr区,或其各自的等效物,或基本上由其组成,或进一步由其组成。在一些实施方案中,双特异性抗体包含nkg2d和可选地slamf7(也称为cs1或cd319)的抗体的重链和/或轻链可变区和/或其各自的等效物,或基本上由其组成,或进一步由其组成。在一些实施方案中,双特异性抗体包含单独的单链可变区片段(scfv)或与源自nkg2d的抗体的fc片段组合的单链可变区片段(scfv),以及可选地单独的单链可变区片段(scfv)或其与源自slamf7
(也称为cd319或cs1)的抗体的fc片段的组合和/或其各自的等效物。该方法可以与治疗医师或兽医确定的其他抗癌疗法和手术相结合。
[0392]
在一方面,本文提供了用于向有需要的对象施用包含或表达car和/或双特异性抗体的分离细胞的方法,其中bsab包含抗flt3抗体的抗原结合结构域,bsab部分包含抗-nkg2d的抗原结合结构域和抗-cd123抗体的抗原结合结构域。这种bsab是一种用于治疗aml的疗法,并且制造和使用这种bsab car的方法包含在本公开的范围内。将有效量的bsab施用至患有aml的患者。这些方法可以辅以适当的诊断方法来诊断aml并监测治疗和毒性。该方法可以与治疗医师或兽医确定的其他抗癌疗法和手术相结合。
[0393]
在另一方面,本文提供了用于向有需要的对象施用包含或表达car和/或双特异性抗体的分离细胞的方法,其中bsab包含抗-egfr抗体的抗原结合结构域,并且bsab部分包含抗-nkg2d的抗原结合结构域和抗-il13ra2抗体的抗原结合结构域。该bsab是用于治疗胶质母细胞瘤的疗法,并且制造和使用该bsab car的方法包含在本公开的范围内。将有效量的bsab施用于患有胶质母细胞瘤的患者。给药可以是局部(颅内给药)或全身给药。这些方法可以辅以适当的诊断方法来诊断胶质母细胞瘤并监测治疗和毒性。该方法可以与治疗医师或兽医确定的其他抗癌疗法和手术相结合。
[0394]
在一方面,本文提供了用于向有需要的对象施用包含或表达car和/或双特异性抗体的分离细胞的方法,其中bsab、bsab-car包含图1e中部分显示的结构,即单个bsab-car包含bcma car、自切割肽(例如t2a)、nkg2d scfv和fc多肽、第二自切割肽(例如t2a)和cs1 scfv和fc多肽,或基本上由其组成。bcma car进一步包含铰链结构域、跨膜结构域和细胞内结构域。在一方面,car组分进一步包含位于氨基末端或抗-nkg2d抗原结合结构域之前的信号结构域,或基本上由其组成,或进一步由其组成。本文提供了示例性的igg1信号肽,但其他肽是本领域已知的并且可以替代该肽。这种bsab是一种用于治疗mm的疗法,并且制造和使用这种bsab car的方法包含在本公开的范围内。将有效量的bsab施用于患有mm的患者。这些方法可以辅以适当的诊断方法来诊断mm并监测治疗和毒性。该方法可以与治疗医师或兽医确定的其他抗癌疗法和手术相结合。
[0395]
在另一方面,本文提供了用于向有需要的对象施用包含或表达car和/或双特异性抗体的分离细胞的方法,其中bsab包含图1f中部分显示的结构,即单个bsab-car包含bcma 抗原结合多肽、自切割肽(例如t2a)、nkg2d scfv和fc多肽、hma多肽和cs1 scfv 和fc多肽,或基本上由其组成。bcma car进一步包含铰链结构域、跨膜结构域和细胞内结构域。在一方面,bcma car进一步包含位于氨基末端或抗-nkg2d抗原结合结构域之前的信号结构域,或基本上由其组成,或还进一步由其组成。本文提供了示例性的igg1信号肽,但其他肽是本领域已知的并且可以替代该肽。这种bsab是一种用于治疗mm的疗法,并且制造和使用这种bsab car的方法包含在本公开的范围内。将有效量的bsab施用于患有mm的患者。这些方法可以辅以适当的诊断方法来诊断mm并监测治疗和毒性。该方法可以与治疗医师或兽医确定的其他抗癌疗法和手术相结合。
[0396]
在一方面,本文提供了用于向有需要的对象施用包含或表达car和/或双特异性抗体的分离细胞的方法,其中bsab、bsab-car包含图1g中部分显示的结构,即单个bs-ab car包含:(a)bcma抗原结合多肽、自切割肽(例如t2a)、nkg2d scfv和fc多肽、接头(如g4s多肽(seq id no:134)),以及cs1 scfv和fc多肽,或基本上由其组成。bcma进一步包含铰链结构
域、跨膜结构域和细胞内结构域,或基本上由其组成。在一方面,该多肽进一步包含位于氨基末端或抗-nkg2d抗原结合结构域之前的信号结构域,或者基本上由其组成,或进一步由其组成。本文提供了示例性的igg1信号肽,但其他肽是本领域已知的并且可以替代该肽。这种bsab是一种用于治疗mm的疗法,并且制造和使用这种bsab car的方法在本公开的范围内。将有效量的bsab施用于患有mm的患者。这些方法可以辅以适当的诊断方法来诊断mm并监测治疗和毒性。该方法可以与治疗医师或兽医确定的其他抗癌疗法和手术相结合。
[0397]
在一些实施方案中,分离的细胞对于被治疗对象或患者是自体的。在另一方面,肿瘤表达癌症或肿瘤抗原并且所述对象已通过诊断被选择用于该疗法,例如使用识别并结合car靶向的肿瘤或癌症相关抗原的抗体。所述对象是动物、哺乳动物、犬科动物、猫科动物、牛科动物、马科动物、鼠科动物或人类患者。
[0398]
本文公开的car细胞可以单独给药或可以与本文公开的双特异性抗体组合给药或者在一种细胞中给药,与如本文所述的稀释剂、已知的抗癌治疗剂和/或其他成分(如细胞因子)或其他具有免疫调节作用的细胞群组合。它们可以作为一线疗法、二线疗法、三线疗法或进一步疗法给药。附加疗法的非限制性实例包括细胞减灭疗法,例如放射疗法、冷冻疗法或化学疗法或生物制剂。其他非限制性实例包括其他相关细胞类型,例如未修饰的免疫细胞、包含表达一种或多种免疫调节分子的载体的修饰的免疫细胞,或对不同于本文所公开的抗原的抗原具有特异性的car细胞。与本公开的car细胞一样,在一些实施方案中,这些细胞可以是自体的或同种异体的。适当的治疗方案将由治疗医师或兽医确定。
[0399]
本公开的药物组合物可以以适合于待治疗或预防的疾病的方式给药。虽然适当的剂量可通过临床试验确定,但给药量和频率将取决于患者的状况、患者疾病的类型和严重程度等因素。在一方面,它们通过直接注射直接地给药或全身性给药(例如静脉注射)。本公开的方面提供了用于确定患者是否可能对car疗法有反应或不可能对car疗法有反应的示例性方法。该方法包含确定从患者中分离的肿瘤样品中是否存在坏死,并定量表达癌症或肿瘤抗原的癌症或肿瘤细胞的量。在某些实施方案中,该方法进一步包括,或基本上由以下组成,或进一步由以下组成:向被确定可能对car疗法有反应的患者施用有效量的car疗法。car疗法相对于患者可以是自体的或同种异体的,并且该患者可以是患有实体瘤的动物对象或人对象。
[0400]
用于坏死的组织学染色技术在本领域中是众所周知的。例如,苏木精和伊红染色,也称为“h&e染色”,是识别组织中(尤其是在致瘤性或癌性生长中)是否存在坏死的常用技术。细胞质h&e染色显示嗜酸性粒细胞增多,部分归因于细胞质rna的丢失,部分归因于变性的细胞质蛋白。在坏死组织染色中,由于细胞质细胞器的酶消化,细胞质常出现“虫蛀(moth eaten)”现象。髓鞘形态、钙化和吞噬其他细胞的证据也是可以通过组织学染色检测到的坏死组织的标志。坏死组织在核染色中也有特定的标志,通常表现为细胞死亡导致核溶解、固缩和核碎裂。使用显微镜手动或自动定量这些坏死标志可以确定car治疗的相关性。检测致瘤性或癌性生长或坏死组织的替代方法包括但不限于基于生物标志物或基于成像的诊断,也与确定患者是否会对某些类型的car治疗产生反应同样相关,并可据此使用。很明显,car-bsab疗法是根据患者样品中癌症或肿瘤的基因型和/或表型选择的,这样抗原结合结构域将靶向并治疗特定的癌症或肿瘤。
[0401]
载体(carrier)
本公开内容的其他方面涉及包含(或基本上由其组成,或由其组成)载体和产物中的一种或多种的组合物——例如,本文公开的细胞群、car、包含car的分离的细胞、多肽、多核苷酸、分离的核酸、载体(vector)、细胞、细胞群和含有本文公开的car和/或双特异性抗体的分离的细胞和/或编码此类的核酸。在一些实施方案中,载体是药学上可接受的载体。在进一步的方面,该组合物可以另外地包含免疫调节分子和/或包含编码双特异性抗体的多核苷酸的分离的核酸。在某些实施方案中,双特异性抗体包含抗bcma和/或nkg2d,可选地,slamf7(也称为cs1或cd319)的抗体的相关cdr区或其各自的等效物,或基本上由其组成,或进一步由其组成。在一些实施方案中,双特异性抗体包含抗nkg2d、可选地slamf7(也称为cs1或cd319)的抗体的重链和/或轻链可变区(其可选地是经密码子优化的)和/或其各自的等效物,或基本上由其组成,或进一步由其组成。在一些实施方案中,双特异性抗体包含源自nkg2d抗体的单独的单链可变区片段(scfv)或与源自nkg2d抗体的fc片段的组合、可选地源自slamf7的单独的单链可变区片段(scfv)或与源自slamf7(也称为cd319或cs1)(可选地经过密码子优化)的fc片段的组合和/或其各自的等效物。
[0402]
简言之,本公开的药物组合物包括但不限于本文所述的任何一种要求保护的组合物,及其与一种或多种药学或生理学可接受的载体、稀释剂或赋形剂的组合。此类组合物可包含缓冲剂,例如中性缓冲盐水、磷酸盐缓冲盐水等;碳水化合物,例如葡萄糖、甘露糖、蔗糖或葡聚糖、甘露醇;蛋白质;多肽或氨基酸,例如甘氨酸;抗氧化剂;螯合剂,例如edta或谷胱甘肽;佐剂(例如氢氧化铝);和防腐剂。本公开的组合物可配制来用于局部或全身给药,例如口服、静脉内、颅内、局部、肠内和/或肠胃外给药。在某些实施方案中,本公开的组合物被配制为用于静脉内给药。
[0403]
细胞或组合物的给药可以在整个治疗过程中以一剂、连续或间歇地方式进行,并以提供实现所需治疗益处的有效量进行。确定最有效的给药方式和给药剂量的方法是本领域技术人员已知的,并且会根据用于治疗的组合物、治疗的目的和被治疗对象的不同而变化。可以进行剂量水平和模式由治疗医师选择的单次或多次给药。合适的剂量制剂和给药方法是本领域已知的。在另一方面,本公开的细胞和组合物可以与其他治疗组合给药。
[0404]
使用本领域已知的和描述于例如pct/us2011/064191中的方法将细胞和细胞群施用于宿主和/或对象。可以施用本公开的细胞或组合物以产生用于实验和筛选测定的所需疾病、病症或状况的动物模型。
[0405]
还提供了一种分离的复合物,其包含以下中的一项或两项:结合癌细胞的本文公开的分离的或工程化的细胞,和/或结合到癌细胞的如本文所公开的多肽,或基本上由其中的一项或两项组成,或由其中的一项或两项组成。在一些实施方案中,癌细胞通过如本文所公开的第一抗-taa抗原结合结构域或如本文所公开的抗-bcma抗原结合结构域与分离的细胞结合。在一些实施方案中,癌细胞通过本文公开的第一抗-taa抗原结合结构域或本文公开的抗-bcma抗原结合结构域与多肽结合。另外地或替代地,癌细胞通过如本文公开的第二抗-taa抗原结合结构域或如本文公开的抗-cs1抗原结合结构域与多肽结合。
[0406]
组合疗法如本文所描述的组合物可以作为一线、二线、三线、四线或其他疗法施用并且可以与细胞减灭干预疗法组合施用。可以由治疗医师确定顺序或同时给药。在一些实施方案中,它们可以与能够上调car和/或bsab结合的肿瘤或其他抗原的表达的疗法组合。在一些实施
方案中,一些临床药物可以增加靶向抗原。例如,cs1的表面表达可以通过来那度胺(lenalidomide)来增加,来那度胺是一种经fda批准的用于多发性骨髓瘤的免疫调节剂药物,参见wangetal.(2018)clin.cancerres.jan1;24(1):106-119。另一个例子是fda批准的药物米哚妥林(midostaurin),当car-bsab靶向flt3抗原时,它会增加flt3的表达。在一些实施方案中,它们可以与癌症或肿瘤的手术切除相结合。在一些实施方案中,细胞减灭疗法包含化学疗法、冷冻疗法、热疗法、靶向疗法和/或放射疗法,或基本上由其组成,或由其组成。
[0407]
试剂盒如本文所述的,本公开提供了用于产生和施用car和/或bsabcar细胞的方法。在一个特定方面,本公开提供了用于执行这些方法的试剂盒,以及用于执行本公开的方法(例如收集细胞和/或组织,和/或执行筛选/转导/等,和/或分析结果)的说明书。
[0408]
在一方面,该试剂盒包含以下,或基本上由以下组成,或进一步由以下组成:如本文所公开的多肽、如本文所公开的多核苷酸、如本文所公开的载体、如本文所公开的分离的核酸、包含所述核酸的载体、如本文所公开的细胞(例如分离的同种异体细胞,优选t细胞或nk细胞)、如本文所公开的细胞群、如本文所公开的组合物、如本文所公开的分离的复合物和/或可选地从患者处获取到的自体细胞的说明书。这样的试剂盒还可以包含以下,或者基本上由以下组成,或者还进一步包含:适合于car和/或bsabcar表达细胞的转导和/或选择和/或活化和/或扩增的培养基和其他试剂,例如本文所公开的那些。
[0409]
在一方面,该试剂盒包含分离的car和/或bsabcar表达细胞或其细胞群,或基本上由其组成,或进一步由其组成。在一些实施方案中,该试剂盒的细胞在给药于有需要的对象之前可能需要激活和/或扩增。在进一步的实施方案中,试剂盒可以进一步包含以下、或基本上由以下组成:培养基和试剂(例如以上公开内容中涵盖的那些)以激活和/或扩增分离的car和/或bsabcar表达细胞。在一些实施方案中,该细胞将用于car疗法。在进一步的实施方案中,该试剂盒包含将分离的细胞给药于需要car治疗的患者的说明书。
[0410]
本公开的试剂盒还可包含例如缓冲剂、防腐剂或蛋白质稳定剂。该试剂盒可进一步包含检测可检测标记所必需的组分,例如酶或底物。该试剂盒还可以包含一个对照样品或一系列对照样品,其可以被分析并与测试样品进行比较。该试剂盒的每个组分都可以封装在一个单独的容器中,所有各种容器都可以放在一个包装中,并附有解释使用该试剂盒进行的化验结果的说明书。本公开的试剂盒可以在试剂盒容器上或其中包含书面产品。该书面产品描述了如何使用试剂盒中包含的试剂。
[0411]
可修改地,这些推荐的试剂盒组分可以以本领域技术人员惯用的方式来包装。例如,这些推荐的试剂盒组分可以溶液形式或作为液体分散体等来提供。
[0412]
以下实施例为可在各种情况下用于实施本公开的程序的说明。
[0413]
实施例1
–
bsabcart细胞的产生和功效嵌合抗原受体(car)t细胞和双特异性抗体(bsab)是fda批准的疗法,其显示出令人印象深刻的癌症治疗潜力。然而,在大多数情况下,两者都还未被证明具有治愈能力。这可能是部分由于治疗的持续时间,即cart细胞可能无法在体内存活足够长的时间,且bsab的半衰期非常短,制造过程昂贵且耗时,因此限制了它们的功效和广泛的应用。在本文中,申请人成功地创建了一个将cart细胞疗法与bsab疗法相结合使两者都具有持久效果的潜
力的平台。申请人在多发性骨髓瘤(mm)的环境中测试了该平台,mm是一种无法治愈的癌症,在目前fda批准的疗法后复发率很高。申请人利用两种mm靶抗原cs1和bcma验证了这一概念,并创建了一种新颖且有效的单慢病毒构建体以产生表达bcmacar并分泌可溶性抗-nkg2d-抗-cs1bsab的bsab-cart细胞,前者攻击bcma(+)mm肿瘤细胞,后者结合所有nkg2d(+)溶细胞性细胞,该溶细胞性细胞包括cd8(+)t细胞、γδt细胞、自然杀伤(nk)t细胞和nk细胞,用于促进其对cs1(+)mm的细胞毒活性。这种一体化、多方面的免疫模式同时提供两种“活的药物”,即cart细胞和bsab,其捕获了针对同一恶性群体上不同靶抗原的先天性和适应性免疫效应细胞。申请人发现,与bcmacart细胞或bsab转导的t细胞相比,bsab-cart细胞分泌更多的ifn-γ并显示出更高的脱粒能力,同时通过靶向mm肿瘤细胞(包括mm细胞系和原发性mm肿瘤细胞)在体外表现出增强的细胞毒作用。在缺乏bcma和cs1这两种抗原的内源性表达的靶细胞中的异位地强制表达增强了靶细胞的裂解。重要的是,从bcmacart细胞中分泌的抗-nkg2d-抗-cs1bsab以自分泌方式通过激活nkg2d信号分别来触发bcmacart细胞在体外的增殖以及它们在体内增强的增殖和存活。这些多管齐下的作用导致体内强大的抗肿瘤活性。总的来说,本文提供了产生下一代癌症免疫疗法的证据,该疗法能够将cart细胞疗法和抗-nkg2d双特异性抗体疗法结合到单个平台中,以增加持续的时间和增强疗效以及能够同时捕获先天性和适应性溶细胞性效应细胞的特异性抗肿瘤活性。
[0414]
细胞培养:细胞系mm.1s、h929、rpmi-8226(人多发性骨髓瘤细胞系)和k562(人红白血病细胞系)购自atcc(manassas,va,usa)。这些细胞用含有10%胎牛血清(fbs)(invitrogen,ca,usa)和1%抗生素-抗真菌剂(invitrogen)的rpmi1640培养基(sigma,st.louis,usa)培养。293t细胞系,其从atcc购买并用于慢病毒的生产,并在dmem(sigma)加与rpmi1640中相同的补充剂中培养。按照制造商的说明,通过ficoll-paqueplus(gehealthcarebio-sciences,pittsburgh,pa)密度梯度离心分离来自健康供体和mm患者的人外周血单个核细胞(pbmc)。根据制造商的说明,分别使用人nk、nkt和γδt细胞分离试剂盒(macs,miltenyibiotech,auburn,ca,usa)分离人cd56
+
nk细胞、cd3
+
cd56
+
nkt细胞和cd3
+
γδtcr
+
t细胞。原发性mm患者样本由俄勒冈州立大学综合癌症中心和詹姆斯癌症医院的白血病组织库共享资源(leukemiatissuebanksharedresourceoftheosucomprehensivecancercenterandjamescancerhospital)提供。对人类对象进行的所有工作根据俄亥俄州立大学机构审查委员会(theohiostateuniversityinstitutionalreviewboard)批准的协议。
[0415]
小鼠:6至8周大的nsg(nod.cg-prkdcscidil2rgtm1wjl/szj)小鼠购自jacksonlaboratories(barharbor,me,usa)并被用于所有体内研究。所有动物工作均根据俄亥俄州立大学动物护理和使用委员会(theohiostateuniversityanimalcareandusecommittee)批准的方案进行。密切监测mm疾病的进展,并记录生存数据。在观察到小鼠后肢麻痹、嗜睡、体重明显减轻后处死小鼠。
[0416]
bcma-car、抗-nkg2d-抗-cs1bsab和bsab-bcmacar-慢病毒构建体的产生:对于bcmacar,用于重链(vh)和轻链(vl)可变区的bcma编码结构域序列源自杂交瘤并使用接头重组。vh-接头-vl片段被结合至带有cd28-cd3ζ部分的框架。抗bcma-scfv-cd28-cd3ζ片段被亚克隆到慢病毒载体pcdh中以创建第二代pcdh-bcmacar构建体。为了制备抗-nkg2d-抗-cs1 bsab慢病毒构建体,由来自抗-cs1单克隆抗体和抗-nkg2d抗体的两个经密码子优
化的单链可变区片段(scfv)通过源自人肌肉醛糖的非免疫原性蛋白接头被连接在一起而被克隆到pcdh慢病毒载体中。对于“一体式”bsab-bcma car,将抗-bcma-scfv-cd28-cd3-t2a盒整合到pcdh抗
ꢀ‑
cs1-nkg2d bsab-ef1a-gfp以构建完整的pcdh-bcma car-t2a-bsab-ef1a-gfp慢病毒构建体。这些方法被用于产生如本文所述的bsab-car。
[0417]
t细胞的慢病毒的生产和转导:慢病毒转染和感染如先前报道的方案
36,37
所描述的来实施。
[0418]
稳定地表达cs1和bcma基因的k562细胞的生产:先前报道
30
了包含人类cs1编码序列的全长pcdh-cmv-cs1-ef1α-gfp构建体。为了产生慢病毒,使用lipofectamine
® 2000(invitrogen)将293t细胞与 pcdh-cs1质粒或pcdh空载体质粒加上包装质粒pcmv-vsvg和pcmv-dr9共转染。而后收集慢病毒上清液并使用先前公布的方案
36, 38
感染k562细胞。然后使用facs aria ii细胞分选仪(bd biosciences,san jose,ca,usa)对gfp 阳性细胞进行分选。bcma-k562是用携带全长bcma cdna的载体转导的k562细胞。使用上述方法进行慢病毒生产、感染和分选。cs1
+
bcma
+
k562细胞是通过将pcdh-cmv-bcma-ef1a-gfp慢病毒构建体转导至上述 cs1-k562细胞产生的。双转导细胞用apc抗bcma mab染色,然后分选gfp
+
bcma
+
细胞群。在用于实验之前,这些gfp
+
bcma
+
双阳性细胞在培养中传代数次以确保抗bcma mab结合细胞的缺失。
[0419]
流式细胞仪分析:如先前报道
30
的那样检测细胞表面上的car表达。本研究中使用的抗体包括:fitc和生物素-标记的山羊抗-小鼠(fab)2多克隆抗体或正常多克隆山羊免疫球蛋白g(igg)抗体(jackson immunoresearch)、别藻蓝蛋白(apc)-偶联链霉亲和素(jackson immunoresearch)、percp/cy5.5-结合链霉亲和素(biolegend)、pe、percp/cy5.5和bv421抗-人cd3(hcd3,克隆ucht1和sk7,bd biosciences)、apc和pe抗-hcd56(克隆tuly56和cmssb,ebioscience)、fitc 和pc5.5 抗-tcr pan γ/δ(克隆immu510,beckman coulter, inc. ca,usa)、pc5抗-tcr pana/b(克隆 ip26a,beckman)、fitc抗-tcr vγ9(克隆immu 360,beckman)和海洋蓝(pacific blue)抗-tcr vδ2(克隆 immu 389,beckman)、未结合及apc抗-hnkg2d(克隆 1d11bd biosciences)、pe-cy7抗-hcd8(克隆sk1,bd biosciences)、apc-cy7抗-hcd4(克隆sk3,bd biosciences)、bv421抗-人 cd1d(克隆 cd1d42,bd optibuild)、v450抗-hcd11c(克隆b-ly6,bd horizon)、apc-h7抗-hcd19(克隆 hib19,bd pharmingen)、apc-h7抗-hcd20(克隆 2h7,bd生物科学)、fitc抗-hc d45(克隆 j.33,beckman)、生物素和fitc抗
ꢀ‑
hcd14(克隆63d3和m5e2,biolegend)、生物素和pe抗-hcd33(克隆 p67.6,biolegend和wm53,bd pharmingen)、生物素抗-hcd66b (克隆 g10f5,biolegend)、未结合及pe-抗-hcs1(克隆 162,ebioscience)、apc-抗-hbcma(克隆 19f2,biolegend)、pe-抗-ki67(克隆 sola15,bd biosciences)、pe-hcd69(克隆fn50,bd biosciences)。细胞用含有4%牛血清白蛋白的pbs洗涤一次,在室温下用抗体染色20分钟,并用 lsrii流式细胞仪(bd biosciences,san jose,ca,usa)分析。
[0420]
免疫印迹:为了检测双特异性抗体的细胞内表达和分泌,使用6x-his-标记mab(“6x-his”公开为seq id no: 111)(克隆4a12e4,invitrogen)。根据申请人先前报道
30, 37
的标准免疫印迹方案进行免疫印迹。如先前报道
30, 37
的,为了检测car表达,car-转导的t细胞被裂解并且蛋白质被提取来进行免疫印迹,用小鼠抗人cd3 mab(bd pharmingen)进行探测。
[0421]
细胞毒性测定:细胞被
51
cr标记并与转导的t细胞在各种效应物下共培养:在96孔v型底板的孔中以目标比率(e:t)在37℃下4小时,然后收获上清液以使用topcount计数器(canberrapackard)测量
51
cr从靶细胞中的释放。在研究bsab与pbmc结合的能力时,从美国红十字会(americanredcross)订购的白细胞包装中分离出cd3
+
t细胞、cd8
+
细胞毒性t细胞、gdt细胞、nkt细胞和nk细胞。t细胞用dynabeads
tm
人t-activatorcd3/cd28(4
×
104/
µ
l,珠子:t=1:1)与il-2(500u/ml)和il-15(500u/ml)上述标准4小时
51
cr释放试验之前启动5-14天。在细胞毒性测定之前,人nk细胞被il-2(500u/ml)激活。分离的人cd3
+
cd56
+
nkt细胞由α-galcer(α-半乳糖神经酰胺,krn7000,enzobiocheminc.ny,usa,100ng/ml)与il-2(100u/ml)
39
激活7-10天。对于cd3
+
gdtcr
+
t细胞激活,使用带有il-2(100u/ml)
40,41
的hmbpp((e)-1-羟基-2-甲基-2-丁烯基4-焦磷酸盐,sigma.10nm)并培养14天。分离来自白细胞采集(leukopack)的这些细胞的方案得到了俄亥俄州立大学机构审查委员会的批准。
[0422]
elisa:根据制造商的方案,使用来自r&d系统(minneapolis,mn,usa)的试剂盒通过酶联免疫吸附试验(elisa)测定培养上清液中人ifn-γ的存在。还通过elisa试剂盒(thermofisherscientific,ma,usa)测定培养上清液中人il-2和tnf-α的水平。对于这些elisa分析,将来自患者的骨髓瘤细胞系或原代mm细胞的2.5
×
105细胞与96孔v底板中的2.5
×
105工程化或对照t细胞一起培养24小时。使用synergyht酶标仪(biotek,winooski,vt,usa)在450nm处读取数据。
[0423]
携带mm小鼠的体内治疗和生物发光成像:先前已经描述
30
了表达萤火虫荧光素酶基因mm.1s-gl3的mm.1s骨髓瘤细胞。为了建立异种移植原位mm模型,nsg小鼠(雄性)在第0天通过尾静脉静脉注射在200
µ
l盐水中的8
×
106个mm.1s-gl3细胞。在第10、17和24天,给予小鼠各自在200
µ
l生理盐水中的(1)载体对照(盐水)或10
×
106个效应细胞,包括(2)空载体转导的t细胞,(3)bsab转导的t细胞,(4)bcma
–
car转导的t细胞,(5)依次用bsab和bcma-car转导的t细胞,或(6)bsab-car转导的t细胞,通过尾静脉静脉注射。在接种mm.1s-gl3细胞后10天、24天、31天,将d-荧光素(150mg/kg体重;goldbiotechnology)腹膜内注射进所有小鼠。使用带有livingimage软件(perkinelmer)的体内成像系统(ivis)进行成像。在第80天,我们通过给每只小鼠尾静脉静脉注射在200l盐水中的4
×
106mm1.s细胞来挑战存活的小鼠。收集存活数据并在第140天关闭。为了研究bsab的作用,在人骨髓细胞耗竭的pbmc存在下重复上述实验。为此目的,nsg小鼠在第0天通过尾静脉静脉注射在200ml盐水中的8
×
106个mm.1s-gl3细胞。在第10天,给小鼠注射3
×
106个不同的转导t细胞,然后是3
×
106个cd33
─
cd14
─
cd66b
─
人pbmc,全部静脉注射。在第17天和第24天,小鼠通过静脉注射接受了3
×
106个由同一供体生成的工程化t细胞。在第10天、第19天、第28天和第37天,小鼠被注入d-荧光素并如上所述成像。
[0424]
由免疫荧光显微镜检测的免疫-突触:主要为了标记分泌的抗-nkg2d-抗-cs1bsab,收集来自bsabcart细胞的上清液并用6x-histagmab(“6x-his”公开为seqidno:111)(克隆4e3d10h2/e3,invitrogen)在1:500的稀释度下在37℃培养1小时,然后用alexafluor
®
350(蓝色,thermofisherscientific,ma,usa)标记。收获mm.1s细胞,并在生长条件下使用celltracker
tm
深红色染料(20
µ
m,thermofisherscientific)培养45分钟。为了观察免疫突触,将bsab-car t细胞(gfp,绿色)或空载体转导的对照t细胞(gfp,绿
8226,bsab-bcmaseq.trans.t细胞表现优于bsabt细胞,但不优于bcma-cart细胞。重要的是,单一或联合抗原靶向对阴性对照k562红白血病靶细胞系都没有活性(图2b)。值得注意的是,与bsabt细胞、evt细胞和未修饰的t细胞的作用相比,bcma-cart细胞在裂解mm靶细胞方面更有效。统计分析表明,当靶mm细胞系表达中等至高水平的cs1和bcma(即mm1.s和h929)时,用效应细胞的bsab-bcmaseq.trans.t细胞群进行的细胞毒性测定观察到协同效应,而当靶细胞表达低或中等水平的两种抗原(即rpmi-8226)时,未观察到这种效应(图2b)。
[0426]
为了进一步确定上述转导的t细胞在识别内源性表达cs1和bcma的mm细胞后的激活,申请人通过elisa在来自未修饰的t细胞、evt、bcma-cart细胞、bsabt细胞和bsab-bcmaseq.trans.t细胞的上清液中测量了ifn-g、il-2和tnf-a分泌。当与bcma
高
cs1
高
mm.1s或bcma
高
cs1
中
h929mm细胞系共培养时,来自bsab-bcmaseq.trans.t细胞的ifn-g分泌明显高于单独的bsabt细胞或bcmacart细胞。在与bcma
中
cs1
低
rpmi-8226mm细胞系共培养的条件下,来自bsab-bcmaseq.trans.t细胞的ifn-分泌显著高于bsabt细胞,但与bcmat细胞相比没有显著提高。在与cs1
─
bcma
─
k562红白血病细胞系或无肿瘤靶细胞共培养条件下,bsab-bcmaseq.trans.t细胞并不优于bsabt细胞或bcma-cart细胞的单抗原靶向(图2c)。当与mm.1s、h929或rpmi-8226mm细胞系共培养时,bsabt细胞、bcma-cart细胞或bsab-bcmaseq.trans.t细胞中产生的il-2显著高于未修饰的t细胞或evt细胞(图2d)。有趣的是,即使在与阴性对照k562红白血病细胞系或无靶细胞共培养时,bsabt细胞和bsab-bcmaseq.trans.t细胞分泌的高水平il-2显著高于在bcmacart细胞中看到的il-2分泌水平(图2d),这表明至少在这种情况下,这种效应似乎是由分泌的bsab本身的存在引起的,而不是来自mm靶细胞。tnf-α分泌与ifn-γ分泌一致(图2e)。总体而言,这些结果表明,与bsabt细胞或bcma-cart细胞相比,bsab-bcmaseq.trans.t细胞可以更特异地识别mm靶细胞,并在识别这些mm细胞后变得更加活跃。此外,与其他条件相比,申请人还注意到bsabt细胞或bsab-bcmaseq.trans.t细胞分泌的bsab无论mm细胞是否存在似乎都会引发t细胞激活,其证据是,与不表达bsab构建体的t细胞相比,它们的il-2产量非常丰富(图2d)。这表明在细胞毒性cd8(+)t细胞上表达的nkg2d受体被分泌的bsab激活。
[0427]
生成单个构建体-工程化的bsab-cart细胞以靶向mm中的bcma和cs1:申请人注意到,当与表达bcma-car或bsab的t细胞相比时,由两个单独的构建体递送的共同表达bcma-car和抗-nkg2d-抗-cs1bsab的t细胞(即bsab-bcmaseq.trans.t细胞)在杀死mm细胞方面表现更出色。表达bsab和car的单个构建体(以下称为bsab-car)在以下方面更实用:(1)在单个t细胞中产生两种构建体的有效表达;(2)降低制造成本;(3)节省时间。因此,申请人生成了一个单一的bsab-car构建体,该构建体在慢病毒载体骨架中包含由t2a连接的两个部分(图3a)。为了产生表达bsab-car的原代t细胞,申请人使用了上述相同的方法,然后确定bsab-car转导的t细胞是否被成功转导。car的表面表达通过流式细胞术分析得到证实(图21c)。在第4天,在细胞裂解物和无血清培养基中使用6x-his-taggedab(“6x-his”,seqidno:111)都成功检测到bsab融合蛋白(图3b)。此外,为了动态测量bsab分泌,申请人在第5天在无血清培养基中重新接种
bsab-cart细胞,然后在12h、24h、48h、72h和96h收集无细胞上清液。结果表明,bsab分泌是有效的,因为表达在12小时前开始并以时间依赖性方式继续增加(图21a-b)。申请人随后证明,与evt细胞和未修饰的t细胞的杀伤力相比,未分级的bsab-cart细胞对bcma
高
cs1
高
mm细胞系mm.1s的杀伤力显著优越(图3c)。对bcma
高
cs1
中
h929和bcma
中
cs1
低
rpmi-8226mm靶细胞系也获得了类似的结果,但对阴性对照k562红白血病细胞系没有杀伤(图21d)。由于大约80%的cd8
+
t细胞具有高表面密度的nkg2d表达(相对于未分级t细胞的30%;图11a),申请人用bsab-car构建体转导至高度富集的cd8
+
t细胞。或许可以预见,申请人发现这些细胞对bcma
高
cs1
高
mm.1smm细胞系的细胞毒性高于cd8
+
bsabt细胞和cd8
+
bcma-cart细胞以及高于两个阴性对照,即未修饰的t细胞和evt细胞(图3d)。cart细胞分泌的bsab需要两种抗原才能发挥作用:在肿瘤细胞上表达的cs1和在免疫细胞上表达的nkg2d。申请人首先评估了pbmc中的tcrpanα/βcd3
+
t、tcrpanγ/δcd3
+
t、cd3
+
cd56
+
nkt和cd3-cd56
+
nk细胞的百分比,其分别占pbmc的50%、1%、8%和15%(图11a)。此外,申请人证实nkg2d在大约30%的t细胞、80%的cd8
+
t细胞、70%的γ/δt细胞、60%的nkt细胞和90%的nk细胞上表达。值得注意的是,近90%的vγ9vδ2t细胞(γδt细胞的一个子集)表达nkg2d(图11b和11c)。为了确定抗-nkg2d-抗-cs1bsab是否引发nkg2d
+
免疫细胞,申请人按照10个效应细胞(转导的或未修饰的t细胞)比1个靶细胞(mm.1s)的比率进行了如上所述的4小时铬-51释放测定,但添加了不同数量的人pbmc,即1倍、10倍、100倍或200倍于肿瘤细胞。申请人假设,如果从bsabt细胞和/或bsab-cart细胞分泌的bsab将非转导的nkg2d
+
溶细胞性效应细胞募集到cs1+mm靶细胞系,则靶标的杀伤会随着来自添加未转导的pbmc的稀释度的增加而上升。为了支持他们的假设,随着非转导pbmc的增加,只有含有分泌bsab的转导t细胞(即bsabt细胞和bsab-cart细胞)的培养物显示出对bcma
高
cs1
高
mm.1smm细胞系的细胞毒性增加(图3e)。可以预见的是,对于具有比mm.1smm细胞系更低的cs1表达的bcma
高
cs1
中
h929细胞系的效果更温和,并且对于bcma
中
cs1
低
rpmi-8226mm靶细胞系没有效果(图12a、12b)。申请人接下来将pbmc的每个子集(即nk细胞、nkt细胞、cd8
+
t细胞和γ9vδ2t细胞)富集到接近98%的纯度(图13),并分别用il-2、calcer加il-2、cd3/cd28dynabeads加il-2和hmbpp加il-2启动它们,然后每个用对照或实验载体中的一种来转导,然后以e:t比为5:1对每一个进行对于bcma
高
cs1
高
mm.1smm细胞系的4h(图3f,左)或16h(图3f,右)
51
cr-释放细胞毒性测定。在4小时或更长时间的孵育中,结果显示无论t细胞亚群或激活方法如何,bsabcart细胞比用其他构建体转导的相同细胞具有显著更高的细胞毒性(图3f和14)。重要的是,在检查的bsabcart细胞群中,与对照细胞相比,活化的cd4
+
bsabcart细胞的细胞毒活性增加最少(图3f,右图和图14),可能至少部分是由于在这个细胞群上相对较低的nkg2d的表面密度表达。为了确定bsab-cart细胞分泌的bsab是否可以诱导bsab-cart细胞和mm.1smm细胞之间的突触形成,共培养一小时后进行了共聚焦显微镜分析。当观察evt细胞和mm.1smm细胞共培养的对照时,没有看到突触(图3g)。相反,在bsab-cart细胞和 mm.1s mm 细胞共培养期间观察到突触(图 3h)。
[0428]
此外,当观察bsab car-t细胞(绿色)与目标mm.1s mm 细胞(红色)的 24小时共培养物时,申请人注意到仅存在bsab car-t 细胞群(绿色)(图 15a-f);然而,在ev t 细胞和 mm.1s mm细胞的共培养物中,靶mm.1s mm 细胞和效应ev t细胞(绿色)仍然存在(图15g-m)。
[0429]
bsab-car t 细胞的功能增强的识别和激活依赖于cs1和bcma:为了证明 bsab-car t细胞增强的细胞毒性作用依赖于靶向肿瘤抗原,申请人接下来探讨了在bsab-car t细胞抗性 k562 细胞系中强制过表达 cs1 和 bcma 是否可以降低其针对该效应群体的裂解阈值。为此目的,申请人用编码人cs1和bcma的慢病毒(或空载体pcdh作为对照)依次转导k562细胞以产生异位表达cs1和bcma的k562细胞系(图16)。在确认成功生成靶细胞系后(图 4a),申请人进行了 51
cr 释放测定,结果表明cs1 和 bcma 在k562 红白血病细胞系中的过表达导致bsab-car t 细胞,与使用 ev t 细胞的细胞毒性相比,对该 k562 细胞系的细胞毒性活性显著增加(图 4b,紫色线)。申请人接下来进行了 elisa 测定,结果显示,与 ev t 细胞与 k562-cs1-bcma 细胞的共培养相比,在 bsab-car t 细胞和 k562-cs1-bcma 细胞的共培养中, ifn-γ和 il-2 分泌增加(图4c,4d)。然而,当bsab-car t 细胞和 ev t 细胞与 k562-pcdh 一起培养时,它们的细胞毒性、ifn-γ 和 il-2 的产生没有差异(图 4b-d)。总的来说,这些数据表明bsab-car t细胞对靶细胞的识别、杀伤和细胞因子分泌的增加以cs1和bcma依赖性方式发生。
[0430]
分泌的抗-nkg2d-抗-cs1 bsab 通过 nkg2d 信号传导增强体外car t 细胞增殖和体内存活和增殖:在一些患者中,由于扩增和存活能力有限,car t 细胞不能存活很长时间,这会限制这些细胞的功效
42
。出乎意料的是,申请人发现在相似的时间点,与没有bsab的其他条件相比,bsab 转导的 t 细胞和 bsab-car t 细胞的培养基酸度更高,表明细胞代谢率更高(图5a,顶部)。这一观察结果与上述数据一致,即这些bsab转导的细胞即使没有靶细胞或与bcma
─
cs1
─ 靶细胞一起能分泌更多的细胞因子(图2d)。申请人推测bsab的表达和分泌可以诱导t细胞增殖、存活和/或其活化。细胞计数证实,与其他培养条件相比,那些含有用 bsab 或 bsab-car 构建体转导的 t 细胞的群体确实含有显著更高数量的细胞(图 5a,条形图),这是由t 细胞增殖引起的,如紫色细胞跟踪器所记录的并显示为下方直方图中显示的 v450 稀释度(图 5a,直方图)。
[0431]
为了确认这些意外的结果,申请人将图 5a 中所示的 bsab-car t 细胞培养物的上清液添加到不含 bsab 的细胞培养条件中,即bcma car t 细胞、ev t 细胞和未修饰的 t 细胞。事实上,与未添加来自 bsab-car t 细胞培养基的上清液的 bcma car t 细胞、ev t 细胞和未修饰t细胞的培养物(未显示)相比,添加 bsab-car t 细胞培养物的上清液在 5 天培养后导致了细胞代谢程度显著提高,正如细胞更新中出现的培养基的黄色所证明的那样。细胞计数证实,与其他培养条件相比,那些补充有来自bsab-car t 细胞培养物的培养基确实含有显著更高数量的细胞(图 5b,顶部),这是由t 细胞增殖引起的,正如紫色细胞追踪器记录的并显示为下方直方图中显示的 v450 稀释度(图 5b,底部)。ki67 染色表明,在含有 bsab t 细胞或 bsab-car t 细胞的培养物中,绝大多数 nkg2d
+ 细胞以及近一半的 nkg2d
—
细胞正在增殖(图 5c 和图 17a),表明 bsab激活的 nkg2d
+ 细胞可以反过来激活 nkg2d
—
细胞,尽管程度较轻。此外,nkg2d 阻断抗体减轻了分泌的 bsab 的增殖作用(图5c蓝框,图17b)。进行免疫印迹分析以确定 akt 蛋白的磷酸化(p),证实分泌的 bsab
可以在 bsab t 和 bsab-car t 细胞培养条件下引发nkg2d
+ 细胞增殖和活化,因为这些条件具有更高水平的p-akt(图 5d)。
[0432]
迄今为止提供的数据支持这样一种观点,即 bsab 激活 nkg2d
+
免疫细胞是通过 nkg2d通路发生的。申请人接下来询问激活是否是通过 cs1而发生,cs1不仅在 mm 细胞上表达,而且在 nk、nkt、cd8
+ t 和b 细胞或其亚群上表达。(veillette and guo crit rev oncol hematol. 2013 oct;88(1):168-77. doi: 10.1016/j.critrevonc.2013.04.003. epub 2013 jun 2;gogishvili et al. blood. 2017 dec 28;130(26):2838-2847. doi: 10.1182/blood-2017-04-778423. epub 2017 oct 31.)为了确定分泌的bsab是否也通过其 cs1 的表达和通过 cs1
+
信号通路刺激 nkg2d
+ 免疫细胞,申请人接下来使用抗 cs1阻断抗体阻断该通路。申请人发现cs1阻断不影响免疫细胞的激活状态(图17c)。此外,申请人进行了nkg2d和cs1双重阻断,结果表明与nkg2d单阻断相比没有差异(数据未显示)。总的来说,这些数据表明分泌 bsab的免疫细胞的激活仅通过 nkg2d 信号通路发生。基于上述发现,申请人预计在 t 细胞与目标群体 mm.1s mm 细胞的共培养中,免疫激活不会严格依赖于nkg2d,也不限于t细胞的 nkg2d
+ 亚群。例如,当 bsab t和 bsab-car t细胞与 mm.1s mm 细胞共培养时,通过ki67染色测量,cd3
+ t 细胞的nkg2d
+
(图 5e 中的红色;83% 到 94%)部分和 nkg2d-(图 5e 中的绿色;79% 到 87%)部分的显示出广泛的增殖。同样,对于仅表达 bcma car(在图 5e 中表示为 fab
+
)的 cd3
+ t细胞,通过ki67染色测量,cd3
+ t细胞的nkg2d
+
(红色;90.4%)和 nkg2d-(绿色;85.8%)部分均显示广泛增殖,尽管略低于 nkg2d
+ 和 nkg2d
‑ bsab-car t 细胞。
[0433]
为了研究转导的 t 细胞在体外存活的能力,申请人在存在或不存在 il-2 的情况下培养了各种转导的 t 细胞。在 il-2 条件下,所有细胞均显示高 ki67 表达和低膜联蛋白 v 和/或 sytox blue表达(图 6a)。有趣的是,在 il-2 缺乏的情况下(图 6b),只有 bsab t 细胞和 bsab-car t 细胞(分泌bsab并通过 nkg2d 激活 t 细胞)表现出更好的增殖能力,大约80% ki67 表达,这与图 2d 中提供的数据以及减少的细胞凋亡和死亡(如膜联蛋白 v的低表达和/或 sytox blue 染色(图 6b)所示)一致。这些结果与其他三组(未修饰的 t 细胞、ev t 细胞和 bcma-car t 细胞)在图 6c 中进行了比较。因此,bsab-car t 增强了细胞增殖和增加了细胞存活率,很可能是通过 nkg2d 信号通路实现。
[0434]
为了比较未修饰的 t 细胞、ev t 细胞、bcma car t 细胞和 bsab-car t 细胞在体内的存活和增殖,申请人将这些人类细胞注射(静脉注射)到免疫缺陷的 nsg 小鼠中(图 7a,上图)。人类细胞的静脉注射前的背景染色也在第-1天进行了评估(图7a和图18)。在第 +1 天,接受每种人类 t 细胞注射的小鼠表现出相同的人类 cd3 表达,并且两个 car t 细胞群也通过它们的 f(ab)
2 表达进行鉴定。此外,在从 nsg小鼠分离的所有四种 t 细胞群中的97%上检测到激活标志物cd69(图 7a 和图 18)。有趣的是,在t 细胞注入14 天后,只有bsab-car t 细胞组保留了 cd3 和 cd69 的高共表达,而其他三组中 cd69 表达显著降低(图 7a 和图 18)。统计分析表明,在+14天时bsab-car t 细胞组中的cd3 和 cd3
+
cd69
+ t 细胞两者的百分比显著高于其他 3 组(图 7b 和 7c)。在各种转导 t 细胞注射 35 天后,直方图显示只有注射bsab-car t 细胞的小鼠仍然拥有高百分比的 hcd3 t 细胞(图 7b)。体内增殖数据显示ki67
+
cd69
+
百分比约为 61.1%,显著高于接受非转导或转导 t 细胞的其他三个组(图 7a 紫色计数图,图7c)。此外,申请人还确定了 bsab-car t 细胞在
体内的存活率,并观察到活的(膜联蛋白
—
vsytoxblue
—
)bsab-car t 细胞的百分比约为 87%,而死的(膜联蛋白v
+
sytoxblue
+
)细胞的百分比约为5%。统计分析表明,与其他三组相比,bsab-car t 细胞具有更高比例的活细胞和更低比例的死细胞(图 7d)。总之,与其他注射细胞组(包括 bcma car t 细胞)相比,bsab-car t 细胞不仅在体外表现出通过 nkg2d 信号通路的增强的细胞增殖,而且在体内表现出增强的增殖和存活。
[0435]
bsab-car t 细胞在离体时提高了对原发性骨髓瘤细胞的识别和杀伤:为了评估 bsab-car t 细胞的临床相关性,申请人研究了它们是否可以在离体时有效地识别和杀死从患者体内分离的 mm 细胞并增强ifn-g 的产生。使用阳性磁选分离从 8 名患者骨髓中获得的原代 cd138
+ mm细胞,并使用流式细胞术评估其 bcma 和 cs1 的表面表达(图 8a)。在不存在自体 pbmc 的情况下进行
51
cr 释放测定,申请人观察到,在所有 8 名患者中,来自患者的mm 细胞对 ev 转导的 t 细胞介导的裂解具有高度抗性。与 bcma car t 细胞或 bsab t 细胞相比,bsab-car t 细胞在所有接受测试的8 名患者中均显示出显著更高的细胞毒性,其中包括患者1,其肿瘤细胞的 cs1 表面密度表达非常低。bsab-car t 细胞和 bsab-bcma seq. trans. t 细胞之间的细胞溶解活性没有显著差异(图 8b)。申请人还在类似的共培养测定中测量到了在24 小时后的 ifn-g;与 ev 转导的 t 细胞、bsab t 细胞或 bcma-car t 细胞相比,bsab-car t 细胞也分泌显著更高水平的 ifn-g(图 8c)。这些发现表明,bsab-car t 细胞具有出色的离体清除患者 mm 细胞的能力。
[0436]
bsab-car t 细胞在原位异种移植 mm 模型中抑制 mm 肿瘤生长并延长荷瘤小鼠的生存期:为了进一步阐释bsab-car t细胞的潜在治疗应用,申请人在 mm.1s mm 移植的 nsg 小鼠模型中检查了它们的抗肿瘤活性。mm.1s mm 细胞的静脉注射已被广泛用于建立 mm 的小鼠异种移植模型,因为这可以导致骨髓移植以及持续建立多灶性溶骨性病变,这与人类 mm 非常相似
43,44
。为了便于监测肿瘤生长,申请人工程化改造了mm.1s mm 细胞以通过逆转录病毒感染表达 gfp 和萤火虫荧光素酶,并使用如先前报道
30
的在第 0 天静脉注射 8 x 10
6 的这些 mm 细胞以移植入 nsg 小鼠。然后将这些小鼠用盐水或1 x 10
7 ev t 细胞、1 x 10
7 bsab t 细胞、1 x 10
7 个bcma car t 细胞、1 x 10
7 个bsab-bcma seq. trans. t 细胞或 1 x 10
7 bsab-car t 细胞静脉注射 3 次(第 10 天、第 17 天和第 24 天)。对于存活至第80天的小鼠,申请人收集外周血淋巴细胞并用1 x 10
4 个mm.1s mm 细胞再次激发小鼠。生物发光成像用于监测 mm.1s mm 生长,并在所有六个治疗组均显示直至第 31 天的早期疾病进展(图 9a)。使用抗 f(ab)
2 抗体来鉴定 bcma car t 细胞,申请人在第 80 天注意到在mm.1s mm 小鼠血液中的bsab-bcma seq. trans. t细胞和 bsab-car t 细胞的百分比显著高于 bcma car t(图 9b),而每只小鼠的总淋巴细胞计数相似(数据未显示)。免疫印迹显示来自用bsab-bcma seq. trans. t细胞或 bsab-car t 细胞处理的第 80 天时的 mm.1s mm 小鼠的血清中仍含有分泌的 bsab(未显示)。到第 80 天时,用 bsab-bcma seq. trans. t细胞或 bsab t 细胞处理的 mm.1s mm 小鼠相对于用盐水对照、ev t 细胞、bsab t细胞处理的类似小鼠的存活时间显著延长。用 bcma car t 细胞处理的 mm.1s mm 小鼠的表现略差于用 bsab-bcma seq. trans. t细胞或 bsab-car t 细胞处理的 mm.1s mm 小鼠(图 9d)。在第 140 天(第一次肿瘤再次激发后 60 天),用bsab-car t 组处理的所有5只 mm.1s mm 小鼠都存活(图 9d)。在肿瘤再次激发后的这些存活数据可能说明上述图 7 中提到的 bsab-car t细胞的体内存活增强和体内增殖增强。总体而
言,这些结果表明,在原位异种移植mm 模型中,bsab-car t 细胞在抑制 mm 肿瘤生长和延长荷瘤小鼠存活的能力方面优于其他非转导或转导t细胞群。
[0437]
为了确定人非转导 nkg2d
+ 淋巴细胞在原位异种移植 mm 模型中的相关性(即,图 3e 中所示的体外实验的体内对应物),申请人接下来检查了盐水对照、ev t 细胞、bcma car t 细胞或 bsab-car t 细胞在携带 mm.1s mm 的 nsg 小鼠中的抗肿瘤功效,同时共同注射从同一供体分离的骨髓细胞耗尽的 pbmc。通过分选去除骨髓细胞是为了避免 gvhd(图 10a、10b)。图10a显示了注射 mm.1s mm 细胞、正常人淋巴细胞和各种转导 t 细胞的示意图,以及记录 mm 进展到第 37 天的成像。图 10b 和 10c 显示了在这些小鼠血液中检测到的人淋巴细胞百分比。在这些条件下的其他时间,申请人发现用 bcma car t 细胞治疗的小鼠(不分泌 bsab;到第 100 天0%存活)和用 bsab-car t 细胞治疗的小鼠(确实分泌 bsab;第 140 天 100%存活;图 10d)之间存在显著差异。这些数据表明,参与的 nkg2d+ 免疫细胞越多,bsab-car t 细胞对肿瘤根除的功效就越好。
[0438]
实施例2
ꢀ–ꢀ
bsab car t 细胞:产生及功效本公开的bsab car包含识别并结合第一抗原的car,而所述bsab识别并结合第二抗原。两种抗原均选自以下清单并且彼此不同:flt3、cd19、间皮素、人表皮生长因子受体 2(her2)、前列腺干细胞抗原(psca)、癌胚抗原(cea)、gtp 酶激活蛋白(gap)、神经节苷脂 g2(gd2)、cd5、前列腺特异性膜抗原 (psma)、受体酪氨酸激酶样孤儿受体 1 (ror1)、cd123、cd70、cd38、b细胞成熟抗原(bcma)、粘蛋白 1、(muc1)、肝配蛋白 a 型受体 2 前体(epha2)、野生型表皮生长因子受体(egfrwt)、表皮生长因子受体变体 iii (egfrviii)、白细胞介素 13 受体 α2(il13ra2)、cd133、磷脂酰肌醇蛋白聚糖3(gpc3)、上皮细胞粘附分子前体(epcam)、成纤维细胞活化蛋白 α(fap)、血管内皮生长因子受体 2(vegfr2)、癌症/睾丸(ct)、鸟苷酸环化酶 c(gucy2c)、肿瘤相关糖蛋白 72(tag-72)、胸苷激酶 1(tk1)和次黄嘌呤鸟嘌呤磷酸核糖基转移酶(hprt1)。对于 car,重链(vh)和轻链(vl)的抗第一taa可变区的编码序列可以重组产生或源自杂交瘤并使用接头进行重组。vh-接头-vl 片段与cd28-cd3ζ部分结合在框架中。将抗第一taa-scfv-cd28-cd3ζ片段亚克隆到慢病毒载体(例如 pcdh )中,以创建第二代 pcdh-第一taa car 构建体。为了制备抗nkg2d-抗第二taa bsab慢病毒构建体,将来自抗第二taa单克隆抗体
29
和抗nkg2d抗体的两个scfv或一个或两个经密码子优化的单链可变区片段(scfv)通过一种源自人肌肉醛糖
35
的非免疫原性蛋白接头连接在一起并且被克隆到 pcdh 慢病毒载体中。对于“一体式”bsab-抗第一car,抗第一taa-scfv-cd28-cd3
ꢀ‑
t2a 盒被并入 pcdh抗第二taa-nkg2d bsab-ef1a(可选)-gfp(可选)来构建完整的 pcdh-抗第一taa-car-t2a-抗第二taa-bsab-ef1a(可选)-gfp(可选)慢病毒构建体。正如对于技术人员显而易见的,临床构建体将不包含gfp及其启动子。这些方法用于产生如本文所述的 bsab-car。
[0439]
慢病毒转染和感染以先前报道的方案
36,37
所述的来进行。
[0440]
为了生产慢病毒,使用 lipofectamine
® 2000(invitrogen)将293t 细胞与 pcdh-抗第一taa-car-t2a-抗第二taa-bsab-ef1a-gfp 质粒或 pcdh 空载体质粒加上包装质粒 pcmv
‑ꢀ
vsvg 和 pcmv-δr9共转染。然后收集慢病毒上清液,并使用先前公布的方案
36,38
感染 k562 细胞。分离转染的细胞或然后使用 facs aria ii 细胞分选仪(bd biosciences,san jose,ca,usa)分选 gfp 阳性细胞。
[0441]
第一taa-k562 k562 细胞用携带编码全长第一 taa的cdna的载体转导。使用上述方法进行慢病毒生产、感染和分选。第二taa
+
第一taa
+
k562细胞是通过将pcdh-cmv-第二taa-ef1α-gfp慢病毒构建体转导至上述第一taa-k562细胞而产生的。双转导细胞用 apc-抗第一taa mab 染色,然后分选 gfp
+
第二taa
+
细胞群。在用于实验之前,这些 gfp
+
第二taa
+ 双阳性细胞在培养物中传代数次,以确保抗第一taa mab结合细胞的丧失。
[0442]
流式细胞术分析、免疫印迹、细胞毒性测定、elisa、携带mm的小鼠的体内处理和生物发光成像、通过免疫荧光显微镜检测的免疫突触、细胞培养和小鼠实验如上所述进行。
[0443]
产生了表达抗第一 taa 特异性 car 和/或抗 nkg2d-抗第二 taa 双特异性抗体的原代 t 细胞。例如,产生了具有慢病毒载体骨架的特异性抗第一taa-car构建体,其依次由信号肽(sp)、抗第一taa重链可变区(vh)、甘氨酸-丝氨酸(gs) 接头、抗第一 taa 轻链可变区(vl)、可选的 myc 标签、铰链、cd28 跨膜结构域和共刺激结构域以及 cd3ζ细胞内信号传导结构域组成。接下来,设计了具有慢病毒载体骨架的抗nkg2d-抗第二taa双特异性抗体(称为“bsab”)构建体。它由来自抗nkg2d 抗体和抗第二taa 单克隆抗体的单链可变区片段 (scfv)组成,通过源自人肌肉醛糖(hma)的非免疫原性蛋白接头连接在一起。每个 scfv 包含通过甘氨酸-丝氨酸(gs)接头连接的相应重链(vh)和轻链(vl)。从健康供体分离并由抗人 cd3/cd28 抗体珠激活的相同供体 t 细胞用空载体(ev)、bsab构建体、抗第一taa-car 构建体转导,或首先用 bsab 转导构建体,然后用抗第一taa-car构建体转导。为了确定 bsab 构建体和抗第一taa-car 构建体是否被成功转导,通过用抗fab 染色转导的 t 细胞来证明抗第一taa car 在细胞表面上的表达。此外,收获培养了4 天的培养物的无细胞上清液,并裂解4 天培养物的细胞沉淀。然后使用6x-his tagged ab(“6x-his”,seq id no:111)对上清液和细胞裂解物进行免疫印迹。细胞bsab和分泌的bsab 的产生表明bsab构建体的成功转导。
[0444]
然后在体外测试转导的 t 细胞与单独使用每种载体转导的 t 细胞相比杀死癌细胞(例如 mm 细胞)的有效性。例如,通过流式细胞术分析测试癌细胞和/或细胞系中第一和第二taa的表面表达。可以使用不表达第一 taa 或第二 taa 的细胞系作为阴性靶对照,进行标准的 4 小时 51
cr 释放测定。比较了五组 t 细胞:(1)未修饰的 t 细胞,(2)空载体(ev)转导的 t 细胞(ev t),(3)抗nkg2d-抗第二 taa-bsab转导的 t 细胞(以下简称 bsab t) , (4)抗第一taa-car-转导的t 细胞(以下称为 抗第一taa-car t)和(5)抗nkg2d-抗第二taa bsab 和 抗第一taa
ꢀ‑
car顺序转导的t细胞(称为bsab-抗第一taa-car seq.trans.t)。
[0445]
为了进一步确定上述转导 t 细胞在识别内源性表达第一 taa 和第二 taa 的癌细胞后的激活,通过 elisa 在来自未修饰 t 细胞、ev t 细胞、抗-第一-taa-car t 细胞、bsab t 细胞和 bsab-抗第一taa-car seq. trans. t细胞的上清液中测量 ifn-γ、il-2 和 tnf-α分泌。结果表明,细胞毒性 cd8(+) t 细胞上表达的 nkg2d 受体被分泌的 bsab的存在而激活。
[0446]
生成单个构建体工程化的bsab-car t细胞以靶向癌细胞中(例如在 mm 中)的第一taa和第二 taa:表达bsab和car的单个构建体(以下称为 bsab-car)在以下方面更实用:(1)在单个 t 细胞中产生两种构建体的有效表达;(2)降低制造成本;(3)节省时间。因此,申请人生成了一个单一的 bsab-car 构建体,该构建体将由 t2a 连接的两个部分包含慢
病毒载体骨架中。为了产生表达 bsab-car 的原代 t 细胞,使用与上述相同的方法,然后确定 bsab-car 转导的 t 细胞是否成功转导。car的表面表达可以通过流式细胞仪分析来确认。在第 4 天,在细胞裂解物和无血清培养基中都使用带 6x-his标记的 ab(“6x-his”, seq id no: 111)成功地检测到 bsab 融合蛋白。此外,为了动态测量 bsab 分泌,在第 5 天将 bsab-car t 细胞重新接种到无血清培养基中,然后在 12h、24h、48h、72h 和 96h 收集无细胞上清液。然后测试未分级的 bsab-car t 细胞的细胞毒性,并与 ev t 细胞和未修饰的 t 细胞对靶细胞的杀伤进行比较。car t 细胞分泌的 bsab 需要两种抗原才能发挥作用:第二taa 在肿瘤细胞上表达,nkg2d 在免疫细胞上表达。为了确定抗nkg2d-抗第二taa bsab 是否引发 nkg2d
+ 免疫细胞,按 10 个效应细胞(转导的或未修饰的 t 细胞)与 1 个靶细胞的比例,如上所述进行 4 小时铬
‑ꢀ
51 释放测定,但添加了不同数量的人 pbmc,即 1 倍、10 倍、100 倍或 200 倍于肿瘤细胞。不希望受限于理论并且基于在实施例1中获得的结果,申请人推测,如果从bsab t细胞和/或bsab-car t细胞分泌的bsab正在将非转导的nkg2d
+
溶细胞性效应细胞募集到第二 taa + 癌细胞系靶标,则由于添加未转导的 pbmc,靶标的杀伤会随着稀释度的增加而上升。pbmc 的每个子集,即 nk 细胞、nkt 细胞、cd8+ t 细胞和γ9vδ2 t 细胞,被富集至近 98% 的纯度,分别用 il-2、calcer 加 il-2、cd3/cd28 dynabeads 加 il
ꢀ‑
2 和 hmbpp 加 il-2启动,并且每个用对照或实验载体中的一种转导,然后对于每个都以 5:1 的 e:t 对癌细胞系进行 4h或 16h 51
cr 释放细胞毒性测定。为了确定 bsab-car t 细胞分泌的 bsab 是否可以诱导 bsab-car t 细胞和癌细胞之间的突触形成,共培养一小时后进行共聚焦显微镜分析。然后观察共定位。
[0447]
为了证明 bsab-car t 细胞增强的细胞毒作用依赖于靶向肿瘤抗原,在 bsab-car t 细胞抗性 k562 细胞系中强制过表达第一 taa 和第二taa 并测试它是否可以降低其针对该效应细胞群的裂解阈值。为此目的,用编码第一 taa 和第二 taa(或空载体 pcdh 作为对照)的慢病毒转导 k562 细胞,以产生异位表达第一taa 和第二 taa 的 k562 细胞系。在确认成功生成靶细胞系后,进行 51
cr 释放测定。进一步进行 elisa 测定以显示与具有 k562-第一taa-第二taa 的ev t细胞的共培养物相比,bsab-car t 细胞和 k562-第一taa-第二taa 细胞的共培养物中 ifn-γ和 il-2 分泌是否增加。
[0448]
此外,测试分泌的抗-nkg2d-抗第二 taa bsab 是否通过 nkg2d 信号传导增强体外car t 细胞增殖以及体内存活和增殖。与在相似时间点,与没有 bsab 的其他条件相比,在 bsab 转导的 t 细胞培养基中培养的 bsab-car t 细胞中测量了细胞数量、细胞增殖、细胞活力和代谢。
[0449]
为了研究转导的 t 细胞在体外存活的能力,在存在或不存在 il-2 的情况下培养各种转导的 t 细胞。评估 ki67、膜联蛋白v 和/或 sytox blue表达。为了比较未修饰的 t 细胞、ev t 细胞、抗第一taa car t 细胞和 bsab-car t 细胞在体内的存活和增殖,将这些人类细胞静脉注射到免疫缺陷的 nsg 小鼠中。人类细胞静脉注射前的背景染色也在第-1天进行评估。cd3、f(ab)2、活化标志物cd69在不同的日子(例如注射后第14天和注射后第35天)进行评估。
[0450]
bsab-cart细胞对原发性癌细胞的识别和杀伤能力在离体进行了测试:为了评
估bsab-cart细胞的临床相关性,研究它们是否可以在离体后有效识别和杀死从患者体内分离的癌细胞并增强ifn-γ的产生。从患者身上获得原发性癌细胞,并使用正磁选择进行分离。流式细胞术用于评估它们的第一taa和第二taa的表面表达。在没有自体pbmc的情况下进行
51
cr释放试验。24小时后在类似的共培养测定中测量ifn-γ。
[0451]
还在癌症动物模型(例如本文所述的原位异种移植mm模型)中测试了bsab-cart细胞是否抑制癌症肿瘤生长并延长荷瘤小鼠的存活率。为了确定人类非转导nkg2d+淋巴细胞在癌症动物模型中的相关性,检测了盐水对照、evt细胞、第一抗taacart细胞或bsab-cart细胞的抗肿瘤功效。携带癌细胞的nsg小鼠同时共同注射从同一供体分离的骨髓细胞耗尽的pbmc。通过分选去除骨髓细胞是为了避免gvhd。癌症进展通过第37天或更长时间(例如第100天、第140天或更长时间)成像。在这些小鼠的血液中检测到人类淋巴细胞的百分比。
[0452]
等效物除非另有定义,否则本文使用的所有技术和科学术语与本技术所属领域的普通技术人员通常理解的含义相同。
[0453]
本文中示例性描述的本技术可在本文未特别地公开的、缺乏任何元素或多个元素、缺乏限制或多种限制的情况下适当地实践。因此,例如,术语“包含”、“包括”、“含有”等应被广泛地理解而不理解为限制。此外,此处使用的术语和表达已被用作描述性术语而不是限制性术语,并且在使用这些术语和表达时无意排除所示和描述的特征或其部分的任何等同物,但应认识到,在要求保护的本技术范围内可以进行各种修改。
[0454]
因此,应当理解,这里提供的材料、方法和示例是优选方面的代表,是示例性的,并且不旨在限制本技术的范围。本技术已在本文中进行了广泛和一般性的描述。落入一般公开内容的每个较窄的种类和亚属分组也构成本技术的一部分。无论本文是否具体引用了删减的材料,本文都包括本技术的带有条件地或移除来自所述任何主题的负面限制的一般描述。此外,在本技术的特征或方面根据马库什组描述的情况下,本领域技术人员将认识到本技术因此也根据马库什组的任何单个成员或成员子组来描述。
[0455]
本文提及的所有出版物、专利申请、专利和其他参考文献均以引用的方式整体并入,其程度与每个单独以引用的方式并入的程度相同。在冲突的情况下,以本说明书(包括定义)为准。
[0456]
其他方面在以下权利要求书中阐述。
[0457]
参考文献1.grupp,s.a.,etal.chimericantigenreceptor-modifiedtcellsforacutelymphoidleukemia.thenewenglandjournalofmedicine368,1509-1518(2013).2.maude,s.l.,etal.chimericantigenreceptortcellsforsustainedremissionsinleukemia.nengljmed371,1507-1517(2014).3.porter,d.l.,levine,b.l.,kalos,m.,bagg,a.&june,c.h.chimericantigenreceptor-modifiedtcellsinchroniclymphoidleukemia.thenew england journal of medicine 365, 725-733 (2011).
4. brown, c.e., et al. regression of glioblastoma after chimeric antigen receptor t-cell therapy. n engl j med 375, 2561-2569 (2016).5. velasquez, m.p., bonifant, c.l. & gottschalk, s. redirecting t cells to hematological malignancies with bispecific antibodies. blood 131, 30-38 (2018).6. maude, s. & barrett, d.m. current status of chimeric antigen receptor therapy for haematological malignancies. br j haematol 172, 11-22 (2016).7. brentjens, r.j., et al. cd19-targeted t cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia. sci transl med 5, 177ra138 (2013).8. porter, d.l., et al. chimeric antigen receptor t cells persist and induce sustained remissions in relapsed refractory chronic lymphocytic leukemia. sci transl med 7, 303ra139 (2015).9. oak, e. & bartlett, n.l. blinatumomab for the treatment of b-cell lymphoma. expert opin investig drugs 24, 715-724 (2015).10. von stackelberg, a., et al. phase i/phase ii study of blinatumomab in pediatric patients with relapsed/refractory acute lymphoblastic leukemia. j clin oncol 34, 4381-4389 (2016).11. raulet, d.h. roles of the nkg2d immunoreceptor and its ligands. nat rev immunol 3, 781-790 (2003).12. groh, v., et al. costimulation of cd8alphabeta t cells by nkg2d via engagement by mic induced on virus-infected cells. nat immunol 2, 255-260 (2001).13. palumbo, a. & anderson, k. multiple myeloma. n engl j med 364, 1046-1060 (2011).14. dimopoulos, m.a., et al. daratumumab, lenalidomide, and dexamethasone for multiple myeloma. n engl j med 375, 1319-1331 (2016).15. van de donk, n.w., kamps, s., mutis, t. & lokhorst, h.m. monoclonal antibody-based therapy as a new treatment strategy in multiple myeloma. leukemia 26, 199-213 (2012).16. caligiuri, m.a. human natural killer cells. blood 112, 461-469 (2008).17. benson, d.m., et al. the pd-1/pd-l1 axis modulates the natural killer cell versus multiple myeloma effect: a therapeutic target for ct-011, a novel monoclonal anti-pd-1 antibody. blood 116, 2286-2294 (2010).18. godfrey, j. & benson, d.m. the role of natural killer cells in immunity against multiple myeloma. leuk lymphoma 53, 1666-1676 (2012).19.szmania,s.,etal.exvivo-expandednaturalkillercells
demonstraterobustproliferationinvivoinhigh-riskrelapsedmultiplemyelomapatients.jimmunother38,24-36(2015).20.ruggeri,l.,mancusi,a.,capanni,m.,martelli,m.f.&velardi,a.exploitationofalloreactivenkcellsinadoptiveimmunotherapyofcancer.currentopinioninimmunology17,211-217(2005).21.felgar,r.e.&hiserodt,j.c.invivomigrationandtissuelocalizationofhighlypurifiedlymphokine-activatedkillercells(a-lakcells)intumor-bearingrats.cellimmunol129,288-298(1990).22.brand,j.m.,etal.kineticsandorgandistributionofallogeneicnaturalkillerlymphocytestransfusedintopatientssufferingfromrenalcellcarcinoma.stemcellsdev13,307-314(2004).23.champsaur,m.&lanier,l.l.effectofnkg2dligandexpressiononhostimmuneresponses.immunologicalreviews235,267-285(2010).24.avery,d.t.,etal.baffselectivelyenhancesthesurvivalofplasmablastsgeneratedfromhumanmemorybcells.jclininvest112,286-297(2003).25.chiu,a.,etal.hodgkinlymphomacellsexpresstaciandbcmareceptorsandgeneratesurvivalandproliferationsignalsinresponsetobaffandapril.blood109,729-739(2007).26.sidaway,p.haematologicalcancer:anti-bcmacartcellsshowpromiseinmm.natrevclinoncol13,530(2016).27.carpenter,r.o.,etal.b-cellmaturationantigenisapromisingtargetforadoptivet-celltherapyofmultiplemyeloma.clinicalcancerresearch:anofficialjournaloftheamericanassociationforcancerresearch19,2048-2060(2013).28.bellucci,r.,etal.graft-versus-tumorresponseinpatientswithmultiplemyelomaisassociatedwithantibodyresponsetobcma,aplasma-cellmembranereceptor.blood105,3945-3950(2005).29.chu,j.,etal.cs1-specificchimericantigenreceptor(car)-engineerednaturalkillercellsenhanceinvitroandinvivoantitumoractivityagainsthumanmultiplemyeloma.leukemia28,917-927(2014).30.chu,j.,etal.geneticmodificationoftcellsredirectedtowardcs1enhanceseradicationofmyelomacells.clinicalcancerresearch:anofficialjournaloftheamericanassociationforcancerresearch20,3989-4000(2014).31.hsi,e.d.,etal.cs1,apotentialnewtherapeuticantibodytargetforthetreatmentofmultiplemyeloma.clinicalcancerresearch:anofficialjournaloftheamericanassociationforcancerresearch14,2775-2784 (2008).
32. raedler, l.a. darzalex (daratumumab): first anti-cd38 monoclonal antibody approved for patients with relapsed multiple myeloma. american health & drug benefits 9, 70-73 (2016).33. jamieson, a.m., et al. the role of the nkg2d immunoreceptor in immune cell activation and natural killing. immunity 17, 19-29 (2002).34. vivier, e., tomasello, e. & paul, p. lymphocyte activation via nkg2d: towards a new paradigm in immune recognition current opinion in immunology 14, 306-311 (2002).35. vallera, d.a., et al. a bispecific recombinant immunotoxin, dt2219, targeting human cd19 and cd22 receptors in a mouse xenograft model of b-cell leukemia/lymphoma. clin cancer res 11, 3879-3888 (2005).36. yu, j., et al. pro
‑ꢀ
and antiinflammatory cytokine signaling: reciprocal antagonism regulates interferon-gamma production by human natural killer cells. immunity 24, 575-590 (2006).37. chen, l., et al. targeting flt3 by chimeric antigen receptor t cells for the treatment of acute myeloid leukemia. leukemia 31, 1830-1834 (2017).38. becknell, b., et al. efficient infection of human natural killer cells with an ebv/retroviral hybrid vector. journal of immunological methods 296, 115-123 (2005).39. metelitsa, l.s., weinberg, k.i., emanuel, p.d. & seeger, r.c. expression of cd1d by myelomonocytic leukemias provides a target for cytotoxic nkt cells. leukemia 17, 1068-1077 (2003).40. hintz, m., et al. identification of (e)-4-hydroxy-3-methyl-but-2-enyl pyrophosphate as a major activator for human gammadelta t cells in escherichia coli. febs letters 509, 317-322 (2001).41. cardone, j., et al. complement regulator cd46 temporally regulates cytokine production by conventional and unconventional t cells. nature immunology 11, 862-871 (2010).42. d'errico, g., machado, h.l. & sainz, b., jr. a current perspective on cancer immune therapy: step-by-step approach to constructing the magic bullet. clin transl med 6, 3 (2017).43. morales-kastresana, a., labiano, s., quetglas, j.i. & melero, i. better performance of cars deprived of the pd-1 brake. clinical cancer research: an official journal of the american association for cancer research 19, 5546-5548 (2013).44. zitvogel, l., apetoh, l., ghiringhelli, f. & kroemer, g. immunological aspects of cancer chemotherapy. nature reviews. immunology 8, 59-73 (2008)。
[0458]
部分序列表igg1铰链结构域:lepkscdkthtcppcpdpkgt (seq id no: 1)cd28跨膜和细胞质结构域:fwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrs (seq id no: 2)cd3ζ信号结构域:rvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (seq id no: 3)il 2信号肽:myrmqllscialslalvtns (seq id no: 4),igg1信号肽:mgwssiilflvatatgvh (seq id no: 5)抗-nkg2d抗原结合结构域的cdr:cdrl1:sgsssnignnavn (seq id no: 6)cdrl2:yddllps (seq id no: 7)cdrl3:aawddslngpv (seq id no: 8)cdrh1:gftfssy (seq id no: 9)cdrh2:rydgsn (seq id no: 10)cdrh3:drglgdgtyfdy (seq id no: 11)抗-nkg2d轻链可变区:qsaltqpasvsgspgqsitiscsgsssnignnavnwyqqlpgkapklliyyddllpsgvsdrfsgsksgtsaflaisglqsedeadyycaawddslngpvfgggtkltvl (seq id no: 12)抗-nkg2d重链可变区:qvqlvesggglvkpggslrlscaasgftfssygmhwvrqapgkglewvafirydgsnkyyadsvkgrftisrdnskntlylqmnslraedtavyycakdrglgdgtyfdywgqgttvtvss (seq id no: 13)肽接头:ggggsggggsggggs (seq id no: 14)抗-flt3抗原结合结构域的cdr:cdrl1:rasqsisnnlh (seq id no: 15)cdrl2:yasqsis (seq id no: 17)cdrl3:qqsntwpyt (seq id no: 19)cdrh1:sywmh (seq id no: 21)cdrh2:eidpsdsykdynqkfkd (seq id no: 23)cdrh3:aitttpfdf (seq id no: 25)抗-flt3抗原结合结构域的cdr:cdrl1:kssqsllnsgnqknym (seq id no: 16);cdrl2:gastres (seq id no: 18)cdrl3:qndhsyplt (seq id no: 20)cdrh1:nyglh (seq id no: 22)cdrh2:viwsggstdynaafis (seq id no: 24)cdrh3:ggiyyanhyyamdy (seq id no: 26)抗-flt3轻链可变区1:
divltqspatlsvtpgdsvslscrasqsisnnlhwyqqkshesprllikyasqsisgipsrfsgsgsgtdftlsinsvetedfgvyfcqqsntwpytfgggtkleikr (seq id no: 27)抗-flt3重链可变区1:qvqlqqpgaelvkpgaslklsckssgytftsywmhwvrqrpghglewigeidpsdsykdynqkfkdkatltvdrssntaymhlssltsddsavyycaraitttpfdfwgqgttltvss (seq id no: 29)抗-flt3轻链可变区2:divmtqspsslsvsagekvtmsckssqsllnsgnqknymawyqqkpgqppklliygastresgvpdrftgsgsgtdftltissvqaedlavyycqndhsypltfgagtklelkr (seq id no: 28)抗-flt3重链可变区2:qvqlkqsgpglvqpsqslsitctvsgfsltnyglhwvrqspgkglewlgviwsggstdynaafisrlsiskdnsksqvffkmnslqaddtaiyycarkggiyyanhyyamdywgqgtsvtvss (seq id no: 30)抗-egfr抗原结合结构域的cdr:cdrl1:rssqnivhnngityle (seq id no: 31)cdrl2:kvsdrfs (seq id no: 33)cdrl3:fqgshippt (seq id no: 35)cdrh1:gdtftsy (seq id no: 37)cdrh2:ypgsgg (seq id no: 39)cdrh3:sggpyffdy (seq id no: 41)抗-egfr抗原结合结构域的cdr:cdrl1:rasqgirnnla (seq id no: 32)cdrl2:aasnlqs (seq id no: 34)cdrl3:lqhhsyplt (seq id no: 36)cdrh1:gftfssy (seq id no: 38)cdrh2:sgsggs (seq id no: 40)cdrh3:ssgwsey (seq id no: 42)抗-egfr轻链可变区1:dilmtqsplslpvslgdqasiscrssqnivhnngitylewylqrpgqspklliykvsdrfsgvpdrfsgsgsgtdftlkisrveaedlgiyycfqgshipptfgggtkleikraa (seq id no: 43)抗-egfr重链可变区1:qvqlqqsgsemarpgasvklpckasgdtftsywmhwvkqrhghgpewigniypgsggtnyaekfknkvtltvdrssrtvymhlsrltsedsavyyctrsggpyffdywgqgttltvss (seq id no: 45)抗-egfr轻链可变区2:diqmtqspsslsasvgdrvtitcrasqgirnnlawyqqkpgkapkrliyaasnlqsgvpsrftgsgsgteftlivsslqpedfatyyclqhhsypltsgggtkveikyahns (seq id no: 44)抗-egfr重链可变区2:evqvlesggglvqpggslrlscaasgftfssyamswvrqapgkglewvsaisgsggstnyadsvkgrftisrdnskntlylqmnslraedtavyycagssgwseywgqgtlvtvss (seq id no: 46)抗-bcma抗原结合结构域的cdr:cdrl1:rasesvtilgshlih (seq id no: 47)
cdrl2:lasnvqt (seq id no: 50)cdrl3:lqsrtiprt (seq id no: 53)cdrh1:gytftdy (seq id no: 56)cdrh2:intetre (seq id no: 59)cdrh3:dysyamdy (seq id no: 62)抗-bcma抗原结合结构域的cdr:cdrl1:sasqdisnyln (seq id no: 48)cdrl2:ytsnlhs (seq id no: 51)cdrl3:qqyrklpwt (seq id no: 54)cdrh1:ggtfsny (seq id no: 57)cdrh2:yrghsd (seq id no: 60)cdrh3:gaiyngydvldn (seq id no: 63)抗-bcma抗原结合结构域的cdr:cdrl1:rasesvtilgshliy (seq id no: 49)cdrl2:lasnvqt (seq id no: 52)cdrl3:lqsrtiprt (seq id no: 55)cdrh1:gytfrhy (seq id no: 58)cdrh2:ntesgv (seq id no: 61)cdrh3: dylysldf (seq id no: 64)抗-bcma轻链可变区1:divltqsppslamslgkratiscrasesvtilgshlihwyqqkpgqpptlliqlasnvqtgvparfsgsgsrtdftltidpveeddvavyyclqsrtiprtfgggtkleik (seq id no: 65)抗-bcma重链可变区1:qiqlvqsgpelkkpgetvkisckasgytftdysinwvkrapgkglkwmgwintetrepayaydfrgrfafsletsastaylqinnlkyedtatyfcaldysyamdywgqgtsvtvss (seq id no: 68)抗-bcma轻链可变区2:diqmtqspsslsasvgdrvtitcsasqdisnylnwyqqkpgkapklliyytsnlhsgvpsrfsgsgsgtdftltisslqpedfatyycqqyrklpwtfgqgtkleikr (seq id no: 66)抗-bcma重链可变区2:qvqlvqsgaevkkpgssvkvsckasggtfsnywmhwvrqapgqglewmgatyrghsdtyynqkfkgrvtitadkststaymelsslrsedtavyycargaiyngydvldnwgqgtlvtvss (seq id no: 69)抗-bcma轻链可变区3:divltqsppslamslgkratiscrasesvtilgshliywyqqkpgqpptlliqlasnvqtgvparfsgsgsrtdftltidpveeddvavyyclqsrtiprtfgggtkleik (seq id no: 67)抗-bcma重链可变区3:qiqlvqsgpelkkpgetvkisckasgytfrhysmnwvkqapgkglkwmgrintesgvpiyaddfkgrfafsvetsastaylvinnlkdedtasyfcsndylysldfwgqgtaltvss (seq id no: 70)抗-cs1抗原结合结构域的cdr:cdrl1:kasqdvitgva(seqidno:71)
cdrl2:sasyryt(seqidno:72)cdrl3:qqhystplt(seqidno:73)cdrh1:gysftty(seqidno:74)cdrh2:hpsdse(seqidno:75)cdrh3:stmiatramdy(seqidno:76)抗-cs1轻链可变区:sdivmtqsqksmstsvgdrvsitckasqdvitgvawyqqkpgqspklliysasyrytgvpdrftgsgsgtdftftisnvqaedlavyycqqhystpltfgagtklelk(seqidno:77)或klelktgagftlptsyhqqcyyvaldeaqvnsitftfdtgsgsgtfrdpvgtyrysasyillkpsqgpkqqywavgtivdqsakctisvrdgvstsmskqsqtmvids(seqidno:154)或divmtqsqksmstsvgdrvsitckasqdvitgvawyqqkpgqspklliysasyrytgvpdrftgsgsgtdftftisnvqaedlavyycqqhystpltfgagtklelk(seqidno:78)。
[0459]
抗-cs1重链可变区:svtvstgqgwydmartaimtsracyyvasdestpsslqmyatssskdvtltakdkfkqnlrtesdsphimgiwelgqgprqkvwnmwyttfsygsakcslkvsagprvleagpqqlqvqs(seqidno:79)或ssvtvstgqgwydmartaimtsracyyvasdestpsslqmyatssskdvtltakdkfkqnlrtesdsphimgiwelgqgprqkvwnmwyttfsygsakcslkvsagprvleagpqqlqvq(seqidno:149),或sqvqlqqpgaelvrpgasvklsckasgysfttywmnwvkqrpgqglewigmihpsdsetrlnqkfkdkatltvdkssstaymqlssptsedsavyycarstmiatramdywgqgtsvtvs(seqidno:80)或qvqlqqpgaelvrpgasvklsckasgysfttywmnwvkqrpgqglewigmihpsdsetrlnqkfkdkatltvdkssstaymqlssptsedsavyycarstmiatramdywgqgtsvtvss(seqidno:150)人igg4fc区:eskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:81)具有f234a、l235a和n297q突变(即,分别在seqidno:81的aa16、aa17和aa79的突变)的人igg4fc区等效物eskygppcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:82)人肌肉醛缩酶(hma)肽接头:psgqagaaaseslfvsnhay(seqidno:83)可检测标志物:ypydvpdya(seqidno:84)t2a肽:hvgsgegrgslltcgdveenpgp(seqidno:85)编码信号肽的核苷酸序列:atggggtggtcaagcattattctgtttctggtcgctaccgctacaggcgtccat(seqidno:86)编码信号肽的核苷酸序列:
atgtacaggatgcaactcctgtcttgcattgcactaagtcttgcacttgtcacaaacagt (seq id no: 87)编码接头肽的核苷酸序列:ggtgggggcggctctggtggcggtggcagcggcggaggtggcagt (seq id no: 88)编码跨膜和细胞质结构域的核苷酸序列:ttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcc (seq id no: 89)编码信号域的核苷酸序列:agagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgc (seq id no: 90) 或其等效物;编码可切割肽的核苷酸序列:cacgtgggttctggagaaggacgcggttccttgttgacgtgtggcgatgtagaggaaaatccgggtcca (seq id no: 91)编码接头的核苷酸序列:ccgagcggccaggcgggcgcggcggcatcggagtccctgtttgtgtcaaatcacgcctac (seq id no: 92)编码抗bcma轻链可变区的核苷酸序列:gatattgttcttactcaatcacccccaagccttgcgatgtctcttggtaaacgagcgacaattagttgtagagcttctgaaagcgtaactattcttgggtcacatcttattcattggtatcaacaaaagccgggacaaccgcctacactcttgattcaactcgcgagcaatgttcaaacgggtgtccctgcacgcttttctgggagcggttcacgaacagattttactctcacgattgatccagtcgaagaagatgatgtcgctgtatattattgtctccaaagtaggacaataccaagaacttttggtggtggtacaaaattggaaattaaa (seq id no: 93)编码抗-bcma轻链可变区的核苷酸序列:gacatccagatgacccagagccctagctcactgagcgccagcgtgggcgacagggtgaccattacctgctccgccagccaggacatcagcaactacctgaactggtaccagcagaagcccggcaaggcccccaagctgctgatctactacacctccaacctgcactccggcgtgcccagcaggttcagcggaagcggcagcggcaccgatttcaccctgaccatctccagcctgcagcccgaggacttcgccacctactactgccagcagtacaggaagctcccctggactttcggccagggcaccaaactggagatcaagcgt (seq id no: 94) 编码抗bcma轻链可变区(即抗bcma序列1 scfv轻链)的核苷酸序列:gacatcgtgctgacccagagcccccccagcctggccatgtctctgggcaagagagccaccatcagctgccgggccagcgagagcgtgaccatcctgggcagccacctgatctactggtatcagcagaagcctggccagccccccaccctgctgatccagctggctagcaatgtgcagaccggcgtgcccgccagattcagcggcagcggcagcagaaccgacttcaccctgaccatcgaccccgtggaagaggacgacgtggccgtgtactactgcctgcagagccggaccatcccccggacctttggcggaggaacaaagctggaaatcaag (seq id no: 95)编码抗-bcma轻链可变区的核苷酸序列:
gacatcgtgctgacccagagcccccccagcctggccatgtctctgggcaagagagccaccatcagctgccgggccagcgagagcgtgaccatcctgggcagccacctgatccactggtatcagcagaagcccggccagccccccaccctgctgatccagctcgccagcaatgtgcagaccggcgtgcccgccagattcagcggcagcggcagcagaaccgacttcaccctgaccatcgaccccgtggaagaggacgacgtggccgtgtactactgcctgcagagccggaccatcccccggacctttggcggaggcaccaaactggaaatcaag (seq id no: 96)编码抗-bcma重链可变区的核苷酸序列:cagatccagctggtgcagtccggccccgagctgaagaagcccggcgagaccgtgaagatctcctgcaaggcctccggctacaccttcaccgactactccatcaactgggtgaagcgggcccccggcaagggcctgaagtggatgggctggatcaacaccgagacccgggagcccgcctacgcctacgacttccggggccggttcgccttctccctggagacctccgcctccaccgcctacctgcagatcaacaacctgaagtacgaggacaccgccacctacttctgcgccctggactactcctacgccatggactactggggccagggcacctccgtgaccgtgtcctcc (seq id no: 97)编码抗-bcma重链可变区的核苷酸序列:caggtgcagctggtccagagcggcgccgaagtgaagaagcccggcagctccgtgaaagtgagctgcaaggccagcggcggcaccttcagcaactactggatgcactgggtgaggcaggcccccggacagggcctggagtggatgggcgccacctacaggggccacagcgacacctactacaaccagaagttcaagggccgggtgaccatcaccgccgacaagagcaccagcaccgcctacatggaactgagcagcctcaggagcgaggacaccgctgtgtattactgcgccaggggcgccatctacaacggctacgacgtgctggacaactggggccagggcacactagtgaccgtgtccagc (seq id no: 98)编码抗-bcma重链可变区(即抗-bcma序列1 scfv重链)的核苷酸序列:atgggatggagctctatcatcctcttcttggtagcaacagctacaggtgtccaccagattcagctggtgcagagcggccctgagctgaagaaacccggcgagacagtgaagatcagctgcaaggcctccggctacaccttccggcactacagcatgaactgggtgaaacaggcccctggcaagggcctgaagtggatgggccggatcaacaccgagagcggcgtgcccatctacgccgacgacttcaagggcagattcgccttcagcgtggaaaccagcgccagcaccgcctacctggtgatcaacaacctgaaggacgaggataccgccagctacttctgcagcaacgactacctgtacagcctggacttctggggccagggcaccgccctgaccgtgtccagc (seq id no: 99)编码抗-bcma重链可变区的核苷酸序列:cagattcagctggtgcagagcggccctgagctgaagaaacccggcgagacagtgaagatcagctgcaaggcctccggctacaccttcaccgactacagcatcaactgggtgaaaagagcccctggcaagggcctgaagtggatgggctggatcaacaccgagacaagagagcccgcctacgcctacgacttccggggcagattcgccttcagcctggaaaccagcgccagcaccgcctacctgcagatcaacaacctgaagtacgaggacaccgccacctacttttgcgccctggactacagctacgccatggactactggggccagggcaccagcgtgaccgtgtccagc (seq id no: 100)编码抗-nkg2d轻链可变区的核苷酸序列:cagtcagcgcttacgcagccggcgtcggtgtcgggttccccgggtcagtcgatcacgatcagctgtagtgggagcagctccaacatcggtaacaacgcagtgaactggtatcagcaactgccgggaaaagcgccgaaactgctgatttactatgatgatttgctgccaagtggagttagtgaccgcttttccggcagtaaatcgggtacctcggcttttctggctatttcgggtctccagagcgaggatgaagctgattattattgcgccgcatgggatgatagcttaaatggcccagtttttggcggcggtactaaactgaccgtgctg (seq id no: 101)编码抗-nkg2d重链可变区的核苷酸序列:caagtgcagctggttgaatccggtggcggtctggtcaagccgggcggctctttgcgtctgagctgtgc
cgcgtcgggttttaccttcagctcttatggtatgcattgggtgcgtcaggcgcctggcaaaggtctggagtgggttgcgttcatccgctacgatgggtctaacaaatattatgccgactcagtaaaaggacgcttcactattagccgcgacaatagcaaaaataccctgtacctgcaaatgaatagcctgcgcgccgaagataccgccgtttactattgcgctaaagatcgtggcctgggtgatggtacgtacttcgattactggggtcagggcaccaccgttaccgttagttca(seqidno:102)编码抗-flt3轻链可变区的核苷酸序列:gatattgtgctaactcagtctccagccaccctgtctgtgactccaggagatagcgtcagtctttcctgcagggccagccagagtattagcaacaacctacactggtatcaacaaaaatcacatgagtctccaaggcttctcatcaagtatgcttcccagtccatctctgggatcccctccaggttcagtggcagtggatcagggacagatttcactctcagtatcaacagtgtggagactgaagattttggagtgtatttctgtcaacagagtaacacctggccgtacacgttcggaggggggaccaagctggaaataaaacgg(seqidno:103)编码抗-flt3轻链可变区的核苷酸序列:gacattgtgatgacacagtctccatcctccctgagtgtgtcagcaggagagaaggtcactatgagctgcaagtccagtcagagtctgttaaacagtggaaatcaaaagaactatatggcctggtatcagcagaaaccagggcagcctcctaaactgttgatctacggggcatccactagggaatctggggtccctgatcgcttcacaggcagtggatctggaaccgatttcactcttaccatcagcagtgtgcaggctgaagacctggcagtttattactgtcagaatgatcatagttatccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seqidno:104)编码抗-flt3重链可变区的核苷酸序列:caggtccaactgcagcagcctggggctgagcttgtgaagcctggggcttcattgaagctgtcctgcaagtcttccgggtacaccttcaccagctactggatgcactgggtgaggcagaggcctggacatggccttgagtggatcggagagattgatccttctgacagttataaagactacaatcagaagttcaaggacaaggccacattgactgtggacagatcctccaacacagcctacatgcacctcagcagcctgacatctgatgactctgcggtctattattgtgcaagagcgattacgacgaccccctttgacttctggggccaaggcaccactctcacagtctcctca(seqidno:105)编码抗flt3重链可变区的核苷酸序列:caggtgcagctgaagcagtcaggacctggcctagtgcagccctcacagagcctgtccatcacctgcacagtctctggtttctcattaactaactatggtttacactgggttcgccagtctccaggaaagggcctggagtggctgggagtgatatggagtggtggaagcacagactataatgcagctttcatatccagactgagcatcagcaaggacaactccaagagccaagttttctttaaaatgaacagtctgcaggctgatgacacagccatatactactgtgccagaaaaggagggatctactatgctaaccattactatgctatggactactggggtcaaggaacctcagtcaccgtctcctca(seqidno:106)编码抗-cs1轻链可变区的核苷酸序列:aaacttgagttgaagaccggtgccggcttcaccttaccgaccagttatcatcaacaatgctattacgtggccctggacgaagcacaggtgaattcaattacgtttacgtttgataccggctctggcagcggtacatttcgtgatcccgtgggcacttaccgctattcggcgagttatatcttgctgaaaccttcccaaggtccgaaacagcagtactgggcggttggcaccattgtagaccaatcagccaaatgtacaatctcggttcgcgatggtgtcagtacgtcgatgtctaagcagtcacagacaatggttatcgat(seqidno:107)编码抗cs1重链可变区的核苷酸序列: agcgttaccgtgagtacaggccagggctggtatgacatggcacgtacagccatcatgacctcgcgcgcatgttactacgtcgcgtcagatgaatcgacgccttcctcgctgcaaatgtatgcaacctcca
fckievmypppyldneksng tiihvkgkhl cpsplfpgps kpfwvlvvvg gvlacysllvtvafiifwvr skrsrllhsd ymnmtprrpg ptrkhyqpya pprdfaayrs (seq id no: 124)编码以下序列的icos共刺激信号区:编码以下序列的ox40共刺激信号区:agggaccag aggctgcccc ccgatgccca caagccccct gggggaggca gtttccggac ccccatccaa gaggagcagg ccgacgccca ctccaccctg gccaagatc (seq id no: 126)人flt3异构体1,mpalardggqlpllvvfsamifgtitnqdlpvikcvlinhknndssvgksssypmvsespedlgcalrpqssgtvyeaaavevdvsasitlqvlvdapgnisclwvfkhsslncqphfdlqnrgvvsmvilkmtetqageyllfiqseatnytilftvsirntllytlrrpyfrkmenqdalvcisesvpepivewvlcdsqgesckeespavvkkeekvlhelfgtdirccarnelgrectrlftidlnqtpqttlpqlflkvgeplwirckavhvnhgfgltwelenkaleegnyfemstystnrtmirilfafvssvarndtgyytcssskhpsqsalvtivekgfinatnssedyeidqyeefcfsvrfkaypqirctwtfsrksfpceqkgldngysiskfcnhkhqpgeyifhaenddaqftkmftlnirrkpqvlaeasasqascfsdgyplpswtwkkcsdkspncteeitegvwnrkanrkvfgqwvssstlnmseaikgflvkccaynslgtscetillnspgpfpfiqdnisfyatigvcllfivvltllichkykkqfryesqlqmvqvtgssdneyfyvdfreyeydlkwefprenlefgkvlgsgafgkvmnataygisktgvsiqvavkmlkekadsserealmselkmmtqlgshenivnllgactlsgpiylifeyccygdllnylrskrekfhrtwteifkehnfsfyptfqshpnssmpgsrevqihpdsdqisglhgnsfhsedeieyenqkrleeeedlnvltfedllcfayqvakgmeflefkscvhrdlaarnvlvthgkvvkicdfglardimsdsnyvvrgnarlpvkwmapeslfegiytiksdvwsygillweifslgvnpypgipvdanfykliqngfkmdqpfyateeiyiimqscwafdsrkrpsfpnltsflgcqladaeeamyqnvdgrvsecphtyqnrrpfsremdlgllspqaqveds (seq id no: 127)人flt3异构体2:mpalardggqlpllvvfsamifgtitnqdlpvikcvlinhknndssvgksssypmvsespedlgcalrpqssgtvyeaaavevdvsasitlqvlvdapgnisclwvfkhsslncqphfdlqnrgvvsmvilkmtetqageyllfiqseatnytilftvsirntllytlrrpyfrkmenqdalvcisesvpepivewvlcdsqgesckeespavvkkeekvlhelfgtdirccarnelgrectrlftidlnqtpqttlpqlflkvgeplwirckavhvnhgfgltwelenkaleegnyfemstystnrtmirilfafvssvarndtgyytcssskhpsqsalvtivekgfinatnssedyeidqyeefcfsvrfkaypqirctwtfsrksfpceqkgldngysiskfcnhkhqpgeyifhaenddaqftkmftlnirrkpqvlaeasasqascfsdgyplpswtwkkcsdkspncteeitegvwnrkanrkvfgqwvssstlnmseaikgflvkccaynslgtscetillnspgpfpfiqdnisfyatigvcllfivvltllichkykkqfryesqlqmvqvtgssdneyfyvdfreyeydlkwefprenlefgkvlgsgafgkvmnataygisktgvsiqvavkmlkekadsserealmselkmmtqlgshenivnllgactlsgpiylifeyccygdllnylrskrekfhrtwteifkehnfsfyptfqshpnssmpgsrevqihpdsdqisglhgnsfhsedeieyenqkrleeeedlnvltfedllcfayqvakgmeflefksarlpvkwmapeslfegiytiksdvwsygillweifslgvnpypgipvdanfykliqngfkmdqpfyateeiyiimqscwafdsrkrpsfpnltsflgcqladaeeamyqnvdgrvsecphtyqnrrpfsremdlgllspqaqveds (seq id no: 128)
adaghvchlc hpnctygctg pglegcptng pkipsiatgm vgalllllvv algiglfmrr rhivrkrtlr rllqerelve pltpsgeapn qallrilket efkkikvlgs gafgtvykgl wipegekvki pvaikelreatspkankeil deayvmasvd nphvcrllgi cltstvqlit qlmpfgclldyvrehkdnig sqyllnwcvq iakgmnyled rrlvhrdlaa rnvlvktpqhvkitdfglak llgaeekeyh aeggkvpikw malesilhri ythqsdvwsygvtvwelmtf gskpydgipa seissilekg erlpqppict idvymimvkc wmidadsrpk freliiefsk mardpqrylv iqgdermhlplmdeedmddv vdadeylipq qgffsspsts rtpllsslsa tsnnstvacidrnglqscpi kedsflqrys sdptgalted siddtflpvp eyinqsvpkrpagsvqnpvy hnqplnpaps rdphyqdphs tavgnpeyln tvqptcvnstfdspahwaqk gshqisldnp dyqqdffpke akpngifkgs taenaeylrvapqssefiga (seq id no: 131)编码抗egfr重链可变区1的多核苷酸:编码抗egfr轻链可变区1的多核苷酸:接头:ggggs (seq id no: 134)。
[0464]
接头:(ggggs)n,其中n可以是1的整数 (seq id no: 134)、或2 (seq id no: 135)、或3 (seq id no: 14)、或4 (seq id no: 136)、或5(seq id no: 137)、或6(seq id no: 138)、或7(seq id no: 139)、或8(seq id no: 140)、或9(seq id no: 141)、或10 (seq id no: 142)、或11(seq id no: 143)、或12(seq id no: 144)、或13 (seq id no: 145)、或14 (seq id no: 146) 、或15(seq id no: 147) 或更多。
[0465]
ef1α启动子序列:aaggatctgcgatcgctccggtgcccgtcagtgggcagagcgcacatcgcccacagtccccgagaagttggggggaggggtcggcaattgaacgggtgcctagagaaggtggcgcggggtaaactgggaaagtgatgtcgtgtactggctccgcctttttcccgagggtgggggagaaccgtatataagtgcagtagtcgccgtgaacgttctttttcgcaacgggtttgccgccagaacacagctgaagcttcgaggggctcgcatctctccttcacgcgcccgccgccctacctgaggccgccatccacgccggttgagtcgcgttctgccgcctcccgcctgtggtgcctcctgaactgcgtccgccgt
cttcactatt agccgcgaca atagcaaaaa taccctgtac ctgcaaatga atagcctgcg cgccgaagat accgccgttt actattgcgc taaagatcgt ggcctgggtg atggtacgta cttcgattac tggggtcagg gcaccaccgt taccgttagt tca (seq id no: 159)抗-nkg2d轻链dna序列cagtcagcgc ttacgcagcc ggcgtcggtg tcgggttccc cgggtcagtc gatcacgatc agctgtagtg ggagcagctc caacatcggt aacaacgcag tgaactggta tcagcaactg ccgggaaaag cgccgaaact gctgatttac tatgatgatt tgctgccaag tggagttagt gaccgctttt ccggcagtaa atcgggtacc tcggcttttc tggctatttc gggtctccag agcgaggatg aagctgatta ttattgcgcc gcatgggatg atagcttaaa tggcccagtt tttggcggcg gtactaaact gaccgtgctg (seq id no: 160)接头ggcggtggcggttctggtggcggtggctccggcggtggcggttct (seq id no: 161)抗-nkg2d重链caagtgcagctggttgaatccggtggcggtctggtcaagccgggcggctctttgcgtctgagctgtgccgcgtcgggttttaccttcagctcttatggtatgcattgggtgcgtcaggcgcctggcaaaggtctggagtgggttgcgttcatccgctacgatgggtctaacaaatattatgccgactcagtaaaaggacgcttcactattagccgcgacaatagcaaaaataccctgtacctgcaaatgaatagcctgcgcgccgaagataccgccgtttactattgcgctaaagatcgtggcctgggtgatggtacgtacttcgattactggggtcagggcaccaccgttaccgttagttcaggtgggggcggctct (seq id no: 162)抗-nkg2d轻链cagcgcttacgcagccggcgtcggtgtcgggttccccgggtcagtcgatcacgatcagctgtagtgggagcagctccaacatcggtaacaacgcagtgaactggtatcagcaactgccgggaaaagcgccgaaactgctgatttactatgatgatttgctgccaagtggagttagtgaccgcttttccggcagtaaatcgggtacctcggcttttctggctatttcgggtctccagagcgaggatgaagctgattattattgcgccgcatgggatgatagcttaaatggcccagtttttggcggcggtactaaactgaccgtgctg (seq id no: 163)抗-cs1重链ctccgtgacggtgtcgacgggccaaggatggtacgatatggcacggaccgcgattatgacatcgcgggcgtgctattacgtggccagcgatgagtcgaccccttcctctctgcaaatgtatgccacctcctcttcaaaagacgtgactctgactgcgaaagacaaatttaaacagaatctgcgcaccgaaagcgatagcccacatatcatgggcatctgggaactgggccagggcccccgccagaaagtgtggaacatgtggtacaccaccttcagctatggttcggccaaatgttccctgaaggtatcagccggcccgcgcgttcttgaggcgggtccgcagcagctgcaggtacagagc (seq id no: 164)抗-cs1轻链aaactggaactcaagacgggtgcgggatttaccctccctacgagctatcaccagcagtgctattacgtggcgcttgacgaagcgcaggtgaactctattacctttacctttgatacaggatcaggcagcggtacgttccgtgatccggtaggtacgtaccggtatagtgcaagctatatccttctgaaaccttctcagggtccgaaacagcagtactgggcggtgggaacgatcgtggaccagtctgccaaatgtacaatttcagttcgcgacggagttagcacctccatgagcaagcagtcccaaaccatggtgattgactct (seq id no: 165)抗-bcma重链序列2
cagattcagctggtgcagagcggccctgagctgaagaaacccggcgagacagtgaagatcagctgcaaggcctccggctacaccttcaccgactacagcatcaactgggtgaaaagagcccctggcaagggcctgaagtggatgggctggatcaacaccgagacaagagagcccgcctacgcctacgacttccggggcagattcgccttcagcctggaaaccagcgccagcaccgcctacctgcagatcaacaacctgaagtacgaggacaccgccacctacttttgcgccctggactacagctacgccatggactactggggccagggcaccagcgtgaccgtgtccagc (seq id no: 166)抗-bcma轻链序列2gacatcgtgctgacccagagcccccccagcctggccatgtctctgggcaagagagccaccatcagctgccgggccagcgagagcgtgaccatcctgggcagccacctgatccactggtatcagcagaagcccggccagccccccaccctgctgatccagctcgccagcaatgtgcagaccggcgtgcccgccagattcagcggcagcggcagcagaaccgacttcaccctgaccatcgaccccgtggaagaggacgacgtggccgtgtactactgcctgcagagccggaccatcccccggacctttggcggaggcaccaaactggaaatcaag (seq id no: 167)igg1重链信号肽dnaatggaatttgggctgcgctgggttttccttgttgctattttaaaagatgtccagtgt (seq id no: 168)蛋白质mefglrwvflvailkdvqc (seq id no: 169)igg1 fcdnagagcccaaatcttgtgacaaaactcacacatgcccaccgtgcccagcacctgaactcctggggggaccgtcagtcttcctcttccccccaaaacccaaggacaccctcatgatctcccggacccctgaggtcacatgcgtggtggtggacgtgagccacgaagaccctgaggtcaagttcaactggtacgtggacggcgtggaggtgcataatgccaagacaaagccgcgggaggagcagtacaacagcacgtaccgtgtggtcagcgtcctcaccgtcctgcaccaggactggctgaatggcaaggagtacaagtgcaaggtctccaacaaagccctcccagcccccatcgagaaaaccatctccaaagccaaagggcagccccgagaaccacaggtgtacaccctgcccccatcccgggatgagctgaccaagaaccaggtcagcctgacctgcctggtcaaaggcttctatcccagcgacatcgccgtggagtgggagagcaatgggcagccggagaacaactacaagaccacgcctcccgtgctggactccgacggctccttcttcctctacagcaagctcaccgtggacaagagcaggtggcagcaggggaacgtcttctcatgctccgtgatgcatgaggctctgcacaaccactacacacagaagagcctctccctgtctccggagctgcaactggaggagagctgtgcggaggcgcaggacggggagctggacgggctgtggacgaccatcaccatcttcatcacactcttcctgttaagcgtgtgctacagtgccaccgtcaccttcttcaaggtgaagtggatcttctcctcggtggtggacctgaagcagaccatcatccccgactacaggaacatgatcggacagggggcc (seq id no: 170)由igg1 fcdna编码的蛋白质epkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspelqleescaeaqdgeldglwttitifitlfllsvcysatvtffkvkwifssvvdlkqtiipdyrnmigqga (seq id no: 171)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1