耳蜗外毛细胞启动子及其用途的制作方法
耳蜗外毛细胞启动子及其用途
1.序列表
2.本技术含有已以ascii格式以电子方式提交且特此以引用的方式整体并入的序列表。2020年11月3日创建的ascii拷贝名为51471-007wo2_sequence_listing_11.02.20_st25且大小为6,362字节。
背景技术:
3.听力损失是重大的公共卫生问题,估计将影响近15%的学龄儿童和三分之一65岁的人。听力损失最常见的类型是感觉神经性听力损失,这是一类由内耳细胞(诸如耳蜗毛细胞)或从内耳伸出到脑部的神经通路的缺陷引起的听力损失。感觉神经性听力损失通常是获得性的,其原因多种多样,包括声创伤、疾病或感染、头部创伤、耳毒性药物和衰老。感觉神经性听力损失也有遗传原因,诸如参与内耳发育和功能的基因的突变。已经鉴定出超过90种此类基因的突变,包括以常染色体隐性、常染色体显性和x连锁模式遗传的突变。
4.近年来,治疗听力损失的努力越来越多地集中在作为可能解决方案的基因疗法上;然而,仍存在很少特异性地靶向毛细胞的方法,而毛细胞通常与听力损失有关。需要靶向毛细胞以治疗感觉神经性听力损失的新疗法。
5.癌调蛋白(ocm)是由柯蒂氏器官中的外毛细胞表达的小白蛋白家族的钙结合蛋白。ocm优先定位于基底外侧外毛细胞膜和毛束的基底。ocm也在前庭的纹状毛细胞中表达。在ocm中携带靶向缺失的小鼠表现出进行性听力损失和ohc退化。这种定位模式表明,在耳蜗中,ocm可在ohc中特异性表达。然而,ocm启动子以前尚未进行分离和表征。
技术实现要素:
6.本发明提供了用于促进目标基因,诸如促进或改善毛细胞功能、再生或存活的基因在特定细胞类型中的表达的组合物和方法。本文所述的组合物和方法涉及刺激转基因在内耳的耳蜗毛细胞(例如,外耳细胞(ohc))中的转录的多核苷酸。本文所述的多核苷酸可以可操作地连接至转基因,并且可施用于患者以治疗或预防听力损失(例如,感觉神经性听力损失)。
7.在一些实施方案中,本发明提供了一种核酸载体,所述核酸载体包含与seq id no:1-3中的任一个具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸。在一些实施方案中,所述多核苷酸与seq id no:1具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。在一些实施方案中,所述多核苷酸与seq id no:2具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。在一些实施方案中,所述多核苷酸与seq id no:3具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。
8.在一些实施方案中,所述多核苷酸可操作地连接至转基因。在一些实施方案中,所述转基因是异源序列。在一些实施方案中,所述转基因含有编码蛋白质(例如,治疗性蛋白质、报告蛋白或其他目标蛋白质)、短干扰rna(sirna)、反义寡核苷酸(aso)、核酸酶(例如,crispr相关蛋白9(cas9)、转录激活因子样效应物核酸酶(talen)、锌指核酸酶(zfn)或引导rna(grna)的多核苷酸序列,或者是微小rna。在一些实施方案中,所述蛋白质是治疗性蛋白质。在一些实施方案中,所述多核苷酸能够指导哺乳动物ohc中来自所述多核苷酸序列的蛋白质、sirna、aso、核酸酶(例如,cas9、talen、zfn或grna)或微小rna的ohc特异性表达。在一些实施方案中,所述哺乳动物ohc是人ohc。
9.在一些实施方案中,所述治疗性蛋白质是肌动蛋白γ1(actg1)、成束蛋白肌动蛋白集束蛋白2、视黄醛(fscn2)、根蛋白(rdx)、pou 4类同源框3(pou4f3)、trio和f-肌动蛋白结合蛋白(triobp)、taperin(tprn)、含xin肌动蛋白结合重复序列的2(xirp2)、atonal bhlh转录因子1(atoh1)、非生长因子依赖性1转录阻遏蛋白(gfi1)、胆碱能受体烟酸α9亚基(chrna9)、胆碱能受体烟酸α10亚基(chrna10)、钙和整联蛋白结合家族成员3(cib3)、钙粘素23(cdh23)、原钙粘附蛋白15(pcdh15)、kinocilin(kncn)、pejvakin(dfnb59)、耳畸蛋白(otoferlin)(otof)、mkrn2相反链(mkrn2os)、lim同源框蛋白3(lhx3)、跨膜通道样1(tmc1)、肌球蛋白15(myo15)、肌球蛋白7a(myo7a)、肌球蛋白6(myo6)、肌球蛋白iiia(myo3a)、肌球蛋白iiib(myo3b)、含谷氧还蛋白结构域的富半胱氨酸蛋白1(grxcr1)、蛋白酪氨酸磷酸酶受体型q(ptprq)、晚期角质化包膜蛋白6a(lce6a)、含脂氧合酶同源结构域的蛋白1(loxhd1)、adp-核糖转移酶1(art1)、atp酶质膜ca2+转运2(atp2b2)、钙和整联蛋白结合家族成员2(cib2)、钙电压门控通道辅助亚基α2δ4(cacna2d4)、钙结合蛋白2(cabp2)、表皮生长因子受体途径底物8(eps8)、eps8样2(eps8l2)、espin(espn)、espin样(espnl)、外周蛋白2(prph2)、硬纤毛蛋白(strc)、溶质载体家族8成员a2(slc8a2)、含cchc型锌指的蛋白12(zcchc12)、含富亮氨酸跨膜和o-甲基转移酶结构域的蛋白质(lrtomt2、lrtomt1)、ush1蛋白网络组分和谐素(ush1c)、溶质载体家族26成员5(slc26a5)、压电型机械敏感离子通道组分2(piezo2)、含细胞外富亮氨酸重复序列和纤连蛋白iii型结构域的1(elfn1)、三十四肽重复蛋白24(ttc24)、肌营养不良蛋白(dytn)、kielin/腱蛋白样蛋白(kcp)、卷曲螺旋富谷氨酸蛋白2(coiled-coil glutamate rich protein 2,ccer2)、含富亮氨酸重复序列和跨膜结构域的蛋白质2(leucine-rich repeat and transmembrane domain-containing protein 2,lrtm2)、钾电压门控通道亚家族a成员10(kcna10)、clarin 1(clrn1)、clarin 2(clrn2)、ski家族转录辅阻遏蛋白1(skor1)、含tctex1结构域的蛋白1(tctex1d1)、fc受体样b(fcrlb)、溶质载体家族17成员8(slc17a8)、含谷氧还蛋白结构域的富半胱氨酸蛋白2(grxcr2)、脑源性神经营养因子(bdnf)、丝氨酸蛋白酶抑制剂(serpin)家族e成员3(serpine3)、无义螺旋环螺旋1(nescient helix-loop helix 1,nhlh1)、热激蛋白70(hsp70)、热激蛋白90(hsp90)、转录激活因子6(atf6)、真核翻译起始因子2α激酶3(perk)、丝氨酸/苏氨酸-蛋白激酶/内切核糖核酸酶ire1(ire1)、whirlin(whrn)、癌调蛋白(ocm)、lim同源框1(isl1)、神经营养蛋白3(ntf3)、含跨膜和三十四肽重复序列的4(tmtc4)或结合免疫球蛋白蛋白质(bip)。
10.在一些实施方案中,所述核酸载体是病毒载体、质粒、粘粒或人工染色体。在一些实施方案中,所述核酸载体是选自包括以下的组的病毒载体:腺相关病毒(aav)、腺病毒和
慢病毒。在一些实施方案中,所述病毒载体是aav载体。在一些实施方案中,所述aav载体具有aav1、aav2、aav2quad(yf)、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、rh10、rh39、rh43、rh74、anc80、anc80l65、dj/8、dj/9、7m8、php.b、php.eb或php.s衣壳。在一些实施方案中,所述aav载体具有aav1衣壳。在一些实施方案中,所述aav载体具有aav9衣壳。在一些实施方案中,所述aav载体具有aav6衣壳。在一些实施方案中,所述aav载体具有aav8衣壳。在一些实施方案中,所述aav载体具有anc80衣壳。在一些实施方案中,所述aav载体具有anc80l65衣壳。在一些实施方案中,所述aav载体具有dj/9衣壳。在一些实施方案中,所述aav载体具有7m8衣壳。在一些实施方案中,所述aav载体具有aav2衣壳。在一些实施方案中,所述aav载体具有php.b衣壳。在一些实施方案中,所述aav载体具有aav2quad(y-f)衣壳。
11.在另一方面,本发明提供一种含有本发明的核酸载体的组合物。在一些实施方案中,所述组合物还包含药学上可接受的赋形剂。
12.在另一个方面,本发明提供了一种可操作地连接至转基因的多核苷酸,所述多核苷酸与seq id no:1-3中的任一个具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。在一些实施方案中,所述多核苷酸与seq id no:1具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。在一些实施方案中,所述多核苷酸与seq id no:2具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。在一些实施方案中,所述多核苷酸与seq id no:3具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)。
13.在一些实施方案中,所述转基因是异源序列。在一些实施方案中,所述转基因编码蛋白质(例如,治疗性蛋白质、报告蛋白或其他目标蛋白质)、sirna、aso、核酸酶(例如,cas9、talen、zfn或grna),或者是微小rna。在一些实施方案中,所述蛋白质是治疗性蛋白质。
14.在一些实施方案中,所述治疗性蛋白质是actg1、fscn2、rdx、pou4f3、triobp、tprn、xirp2、atoh1、gfi1、chrna9、chrna10、cib3、cdh23、pcdh15、kncn、dfnb59、otof、mkrn2os、lhx3、tmc1、myo15、myo7a、myo6、myo3a、myo3b、grxcr1、ptprq、lce6a、loxhd1、art1、atp2b2、cib2、cacna2d4、cabp2、eps8、eps8l2、espn、espnl、prph2、strc、slc8a2、zcchc12、lrtomt2、lrtomt1、ush1c、slc26a5、piezo2、elfn1、ttc24、dytn、kcp、ccer2、lrtm2、kcna10、clrn1、clrn2、skor1、tctex1d1、fcrlb、slc17a8、grxcr2、bdnf、serpine3、nhlh1、hsp70、hsp90、atf6、perk、ire1、whrn、ocm、isl1、ntf3、tmtc4或bip。
15.在另一个方面,本发明提供了一种细胞(例如哺乳动物细胞,例如人细胞,如ohc),所述细胞包含前述方面和实施方案中任一项的多核苷酸或核酸载体。在一些实施方案中,所述细胞是哺乳动物ohc。在一些实施方案中,所述哺乳动物ohc是人ohc。
16.在另一个方面,本发明提供了一种在哺乳动物ohc中表达转基因的方法,所述方法通过使所述哺乳动物ohc与本发明的核酸载体或本发明的组合物接触来进行。在一些实施方案中,所述转基因在ohc中特异性地表达。在一些实施方案中,所述哺乳动物ohc是人ohc。在一些实施方案中,所述转基因基本上不在不是ohc的内耳细胞中表达。
17.在另一个方面,本发明提供了一种治疗患有听力损失(例如,感觉神经性听力损失、耳聋或听神经病)或有此风险的受试者的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。在一些实施方案中,所述听力损失是遗传性听力损失。在一些实施方案中,所述遗传性听力损失是常染色体显性听力损失、常染色体隐性听力损失或x连锁性听力损失。在一些实施方案中,所述听力损失是获得性听力损失。在一些实施方案中,所述获得性听力损失是噪声引起的听力损失、年龄相关的听力损失、疾病或感染相关的听力损失、头部创伤相关的听力损失或耳毒性药物引起的听力损失。在一些实施方案中,所述获得性听力损失是年龄相关的听力损失。在一些实施方案中,所述听力损失是噪声引起的听力损失。在一些实施方案中,所述听力损失是耳毒性药物引起的听力损失。
18.在前述方面中任一项的一些实施方案中,所述受听力损失与ohc的损失相关。
19.在另一个方面,本发明提供了一种促进有需要的受试者的ohc再生的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。
20.在另一个方面,本发明提供了一种预防或减少有需要的受试者的耳毒性药物引起的ohc损伤或死亡的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。
21.在前述方面中任一项的一些实施方案中,所述耳毒性药物选自包括以下的组:氨基糖苷(例如,庆大霉素、新霉素、链霉素、妥布霉素、卡那霉素、万古霉素和阿米卡星)、抗肿瘤药(例如,含铂化疗剂,诸如顺铂、卡铂和奥沙利铂)、依他尼酸、呋塞米(furosemide)、水杨酸盐(例如,阿司匹林,特别是在高剂量下)和奎宁。
22.在另一个方面,本发明提供了一种治疗患有耳鸣或有此风险的受试者的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。
23.在另一个方面,本发明提供了一种预防或减少有需要的受试者的ohc损伤或死亡的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。
24.在另一个方面,本发明提供了一种增加有需要的受试者的ohc存活的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。
25.在另一个方面,本发明提供了一种诱导或增加有需要的受试者的ohc成熟的方法,所述方法通过向所述受试者施用有效量的本发明的核酸载体或本发明的组合物来进行。
26.在前述方面中任一项的一些实施方案中,所述ohc是哺乳动物ohc。在一些实施方案中,所述哺乳动物ohc是人ohc。
27.在前述方面中任一项的一些实施方案中,所述方法还包括在施用所述核酸载体或组合物之前评估所述受试者的听力(例如,使用标准测试评估听力,所述标准测试诸如听力测验法(audiometry)、听性脑干反应(auditory brainstem response,abr)、耳蜗电图描记法(electrocochleography,ecog)或耳声发射)。
28.在前述方面中任一项的一些实施方案中,所述方法还包括在施用所述核酸载体或组合物之后评估受试者的听力(例如,使用标准测试评估听力,所述标准测试诸如听力测验法、abr、ecog或耳声发射)。
29.在前述方面中任一项的一些实施方案中,所述核酸载体或组合物局部施用。在一
些实施方案中,所述核酸载体或组合物施用于所述受试者的耳朵(例如,如通过卵圆窗、圆窗或水平管或通过经鼓室或鼓室内注射施用于内耳,例如施用至外淋巴或内淋巴中)。
30.在前述方面中任一项的一些实施方案中,所述核酸载体或组合物以足以预防或减少听力损失、预防或减少耳鸣、延迟听力损失的发展、减缓听力损失的进展、改善听力、改善毛细胞功能(例如,ohc功能)、预防或减少毛细胞损伤(例如,ohc损伤)、预防或减少毛细胞死亡(例如,ohc死亡)、促进或增加毛细胞存活(例如,ohc存活)、增加毛细胞成熟(例如,ohc成熟)或增加毛细胞数量(例如,ohc数量)的量施用。
31.在前述方面中任一项的一些实施方案中,所述受试者是人。
32.在另一个方面,本发明提供了一种药盒,所述药盒含有本发明的核酸载体或本发明的组合物。
33.定义
34.如本文所用,术语“约”是指在所述值的上下10%以内的值。
35.如本文所用,“施用”是指通过任何有效途径向受试者提供或给予治疗剂(例如,含有可操作地连接至转基因的外毛细胞(ohc)特异性启动子的核酸载体)。示例性的施用途径在下文描述。
36.如本文所用,术语“细胞类型”是指共享基于基因表达数据在统计学上可分离的表型的一组细胞。例如,常见细胞类型的细胞可共享相似的结构和/或功能特征,诸如相似的基因激活模式和抗原呈递特征谱。常见细胞类型的细胞可包括从常见组织(例如,上皮组织、神经组织、结缔组织或肌肉组织)分离的那些和/或从常见器官、组织系统、血管或生物体的其他结构和/或区域分离的那些。
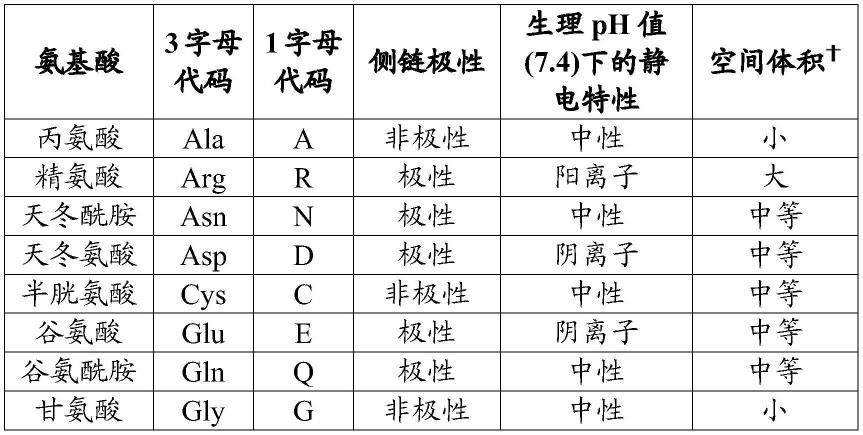
37.如本文所用,术语“保守突变”、“保守取代”和“保守氨基酸取代”是指一个或多个氨基酸取代成表现出相似物理化学特性(诸如极性、静电荷和空间体积)的一个或多个不同的氨基酸。下表1中汇总了20种天然存在的氨基酸中的每一种的这些特性。
38.表1.天然存在的氨基酸的代表性物理化学性质
39.[0040][0041]
由此表应认识到,保守氨基酸家族包括(i)g、a、v、l和i;(ii)d和e;(iii)c、s和t;(iv)h、k和r;(v)n和q;以及(vi)f、y和w。因此,保守突变或取代是一个氨基酸取代成同一氨基酸家族的成员的一种突变或取代(例如,ser取代成thr或lys取代成arg)。
[0042]
如本文所用,术语本文所述的组合物、载体构建体或病毒载体的“有效量”、“治疗有效量”和“足够量”是指当施用于包括哺乳动物(例如人)的受试者时足以实现有益或期望结果(包括临床结果)的量,并且因此,“有效量”或其同义词取决于其所应用的背景。例如,在治疗感觉神经性听力损失的背景中,它是与不施用组合物、载体构建体或病毒载体的情况下获得的响应相比,足以实现治疗响应的组合物、载体构建体或病毒载体的量。将与这样的量相对应的本文所述的给定组合物的量将根据各种因素而变化,诸如给定的剂、药物制剂、施用途径、疾病或病症的类型、所治疗的受试者(例如年龄、性别、体重)或宿主的身份等,但是仍然可由本领域技术人员常规确定。同样,如本文所用,本公开的组合物、载体构建体或病毒载体的“治疗有效量”是与对照相比,在受试者中产生有益或期望结果的量。如本文所定义,本公开的组合物、载体构建体或病毒载体的治疗有效量可由普通技术人员通过本领域已知的常规方法容易地确定。可调整剂量方案以提供最佳治疗响应。
[0043]
如本文所用,术语“内源性”是指天然存在于特定生物体(例如,人)中或生物体内的特定位置(例如,器官、组织或细胞,诸如人细胞,例如ohc)中的分子(例如,多肽、核酸或辅因子)。
[0044]
如本文所用,术语“表达”是指以下事件中的一个或多个:(1)从dna序列产生rna模
板(例如,通过转录);(2)rna转录物的加工(例如,通过剪接、编辑、5'帽形成和/或3'端加工);(3)将rna翻译成多肽或蛋白质;以及(4)多肽或蛋白质的翻译后修饰。
[0045]
如本文所用,术语“外源性”描述不天然存在于特定生物体(例如,人)中或生物体内的特定位置(例如,器官、组织或细胞,诸如人细胞,例如人ohc)中的分子(例如,多肽、核酸或辅因子)。外源性材料包括由外部来源提供至生物体或提供至从其中提取的培养物质的那些材料。
[0046]
如本文所用,术语“外显子”是指基因的编码区内其核苷酸序列决定相应蛋白质的氨基酸序列的区域。术语外显子还指从基因转录的rna的相应区域。外显子被转录成前体mrna,并且可包含在成熟mrna中,这取决于基因的选择性剪接。在加工后包含于成熟mrna中的外显子被翻译成蛋白质,其中外显子的序列决定蛋白质的氨基酸组成。
[0047]
如本文所用,术语“异源的”是指非天然存在的元件的组合。例如,异源转基因是指由与其可操作连接的启动子不天然表达的转基因。
[0048]
如本文所用,术语“外毛细胞特异性表达”或“ohc特异性表达”是指与耳蜗的其他细胞类型(例如,螺旋神经节神经元、神经胶质或其他耳蜗细胞类型)相比,rna转录物或多肽主要耳蜗ohc内产生。转基因的ohc特异性表达可通过使用任何标准技术(例如,定量rt pcr、免疫组织化学、蛋白质印迹分析,或可操作地连接至启动子的报告基因(例如,gfp)的荧光的测量)在耳蜗的各种细胞类型(例如,ohc相对于非ohc)之间比较转基因表达(例如,rna或蛋白质表达)来确认。ohc特异性启动子所诱导的与其可操作地连接的转基因的表达(例如,rna或蛋白质表达)在ohc中比在至少2种(例如,2、3、4、5、6、7、8、9、10种或更多种)以下内耳细胞类型中大至少50%(例如,大50%、75%、100%、125%、150%、175%、200%或更多):内毛细胞、边界细胞、内指细胞、内柱细胞、外柱细胞、第一排deiter细胞、第二排deiter细胞、第三排deiter细胞、汉森细胞、克劳迪厄斯氏(claudius)细胞、内沟细胞、外沟细胞、螺旋突细胞、根细胞、齿间细胞、血管纹的基底细胞、血管纹的中间细胞、血管纹的边缘细胞、螺旋神经节神经元、施旺(schwann)细胞。ohc特异性启动子所诱导的与其可操作连接的转基因的表达(例如,rna或蛋白质表达)在耳蜗的ohc中比在耳蜗的其他细胞中大至少50%(例如,大50%、75%、100%、125%、150%、175%、200%或更多)。
[0049]
如本文所用,术语“增加”和“减少”是指相对于参考分别产生更大或更少量的功能、表达或活性的调节。例如,在以本文所述的方法施用组合物之后,如本文所述的度量(例如,转基因表达)的标志物的量可相对于施用之前的标志物的量在受试者中增加或减少至少5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或98%或更多。通常,在施用后,在施用已达到所述效果的时间,例如,在治疗方案开始之后至少一周、一个月、3个月或6个月测量所述度量。
[0050]
如本文所用,术语“内含子”是指基因的编码区内其核苷酸序列不翻译成相应蛋白质的氨基酸序列的区域。术语内含子还指从基因转录的rna的相应区域。内含子被转录成前体mrna,但在加工过程中去除,不包括在成熟mrna中。
[0051]
如本文所用,“局部”或“局部施用”是指在身体的特定部位上旨在局部作用而不是全身作用的施用。局部施用的实例是表皮、吸入、关节内、鞘内、阴道内、玻璃体内、子宫内、病灶内施用、淋巴结施用、肿瘤内施用、向内耳施用和向受试者的粘膜施用,其中施用旨在产生局部而非全身作用。
[0052]
如本文所用的术语“可操作连接”是指第一分子连结到第二分子,其中所述分子的排列使得第一分子影响第二分子的功能。两个分子可为或可不为单个邻接分子的一部分且可为或可不为相邻的。例如,如果启动子调节目标可转录多核苷酸分子在细胞中的转录,那么启动子可操作地连接至可转录多核苷酸分子。另外,如果转录调控元件的两个部分相互连接,使得一部分的转录激活功能不受另一部分的存在的不利影响,那么所述两个部分彼此可操作地连接。两个转录调控元件可借助接头多核苷酸(例如,居间的非编码多核苷酸)彼此可操作地连接或可在不存在居间核苷酸的情况下彼此可操作地连接。
[0053]
如本文所用,术语“质粒”是指另外的dna区段可连接到其中的染色体外环状双链dna分子。质粒是一种载体,是能够转运已与其连接的另一核酸的核酸分子。某些质粒能够在其被引入的宿主细胞中自主复制(例如,具有细菌复制起点的细菌质粒和附加型哺乳动物质粒)。其它载体(例如非附加型哺乳动物载体)可在导入宿主细胞后整合到宿主细胞的基因组中,由此随宿主基因组一起复制。某些质粒能够指导它们可操作地连接的基因的表达。
[0054]
如本文所用,术语“多核苷酸”是指核苷酸的聚合物。通常,多核苷酸由通过磷酸二酯键连接的天然存在于dna或rna中的核苷(例如,腺苷、胸苷、鸟苷、胞苷、尿苷、脱氧腺苷、脱氧胸苷、脱氧鸟苷和脱氧胞苷)构成。该术语涵盖包含含有化学或生物学修饰的碱基、修饰的骨架等的核苷或核苷类似物的分子,无论是否存在于天然存在的核酸中,并且此类分子对于某些应用可以是优选的。当本技术涉及多核苷酸时,应理解,提供了dna、rna,并且在每种情况下都提供了单链和双链形式(以及每个单链分子的互补物)。如本文所用,“多核苷酸序列”可以指多核苷酸材料本身和/或生物化学表征特定核酸的序列信息(即,用作碱基缩写的一连串字母)。除非另外指明,否则本文给出的多核苷酸序列以5'至3'方向给出。
[0055]
如本文所用,术语“启动子”是指dna上由rna聚合酶结合的识别位点。聚合酶驱动转基因的转录。
[0056]
相对于参考多核苷酸或多肽序列而言的“序列同一性百分比(%)”定义为在将序列比对并且在需要时引入空位以实现最大序列同一性百分比之后,在候选序列中与参考多核苷酸或多肽序列中的核酸或氨基酸相同的核酸或氨基酸的百分比。用于确定核酸或氨基酸序列同一性百分比的比对可以以在本领域技术人员能力范围内的各种方式实现,例如,使用可公开获得的计算机软件,诸如blast、blast-2或megalign软件。本领域技术人员可以确定用于比对序列的适当参数,包括实现在所比较序列的全长上实现最大比对所需的任何算法。例如,可使用序列比较计算机程序blast生成序列同一性百分比值。例如,给定核酸或氨基酸序列a与给定核酸或氨基酸序列b的序列同一性百分比(也可以表述为给定核酸或氨基酸序列a与给定核酸或氨基酸序列b具有一定的序列同一性百分比)计算公式如下:
[0057]
100
×
(分数x/y)
[0058]
其中x是通过序列比对程序(例如,blast)在所述程序的a和b的比对中评分为相同匹配的核苷酸或氨基酸的数目,并且其中y是b中核酸的总数。应当理解,在核酸或氨基酸序列a的长度不等于核酸或氨基酸序列b的长度的情况下,a对于b的序列同一性百分比将不等于b对于a的序列同一性百分比。
[0059]
如本文所用,术语“药物组合物”是指含有任选地与一种或多种药学上可接受的赋形剂、稀释剂和/或载剂组合的治疗剂,待施用给受试者(诸如哺乳动物,例如人)以便预防、
治疗或控制影响或可能影响受试者的特定疾病或疾患的混合物。
[0060]
如本文所用的术语“药学上可接受的”是指适于与受试者(例如哺乳动物,例如人)的组织接触而无过度毒性、刺激、过敏反应和其它问题并发症并与合理效益/风险比相称的那些化合物、材料、组合物和/或剂型。
[0061]
如本文所用,术语“样品”是指从受试者中分离的样本(例如,血液、血液组分(例如,血清或血浆)、尿液、唾液、羊水、脑脊液、组织(例如,胎盘或真皮组织)、胰液、绒毛膜和细胞)。
[0062]
如本文所用,术语“转录调控元件”是指至少部分地控制目标基因的转录的多核苷酸。转录调控元件可包括启动子、增强子以及控制或帮助控制基因转录的其他多核苷酸(例如,聚腺苷酸化信号)。转录调控元件的实例描述于,例如,lorence,recombinant gene expression:reviews and protocols(humana press,new york,ny,2012)。
[0063]
如本文所用,术语“转染”是指常用于将外源dna引入原核或真核宿主细胞中的广泛多种技术中的任一种,例如电穿孔、脂质转染、磷酸钙沉淀、deae-葡聚糖转染、核转染、挤压-穿孔(squeeze-poration)、声致穿孔、光学转染(optical transfection)、磁转染、穿刺转染(impalefection)等。
[0064]
如本文所用,术语“受试者”和“患者”是指动物(例如,哺乳动物,诸如人)。待根据本文所述的方法治疗的受试者可以是已被诊断为患有听力损失(例如,感觉神经性听力损失)的受试者或有发展这种疾患的风险的受试者。可通过本领域已知的任何方法或技术进行诊断。本领域技术人员将理解,待根据本公开治疗的受试者可能已经接受了标准测试,或可能由于存在一种或多种与疾病或疾患相关的风险因素而未经检查就被鉴定为有风险的受试者。
[0065]
如本文所用,术语“转导(transduction和transduce)”是指将载体构建体或其部分引入细胞中的方法。其中载体构建体包含在病毒载体例如aav载体中,转导是指细胞的病毒感染以及随后载体构建体或其部分转移和整合到细胞基因组中。
[0066]
如本文所用,关于疾病或疾患的“治疗(treatment)”和“治疗(treating)”是指用于获得有益或所需结果(例如临床结果)的方法。有益的或期望的结果可包括但不限于减轻或改善一种或多种症状或疾患;减少疾病或疾患的程度;稳定(即,不恶化)疾病、病症或疾患的状态;防止疾病或疾患的传播;延迟或减缓疾病或疾患的进展;改善或缓解疾病或疾患;以及可检测的或不可检测的缓解(部分或全部)。“改善”或“减轻”疾病或疾患是指与在不治疗的情况下的程度或时间过程相比,疾病、病症或疾患的程度和/或不期望的临床表现减轻和/或进展的时间过程减慢或延长。“治疗”还可意指相比于不接受治疗时的预期生存,延长生存。需要治疗的那些包括已经患有疾患或病症的那些,以及易患疾患或病症的那些或将预防疾患或病症的那些。
[0067]
如本文所用,术语“载体”是指核酸载体,例如,dna载体,诸如质粒、粘粒或人工染色体、rna载体、病毒或任何其他合适的复制子(例如,病毒载体)。已开发出多种载体,以用于将编码外源蛋白质的多核苷酸递送到原核或真核细胞中。此类表达载体的实例描述于,例如,gellissen,production of recombinant proteins:novel microbial and eukaryotic expression systems(john wiley&sons,marblehead,ma,2006)。适于与本文所述的组合物和方法一起使用的表达载体包含多核苷酸序列,以及例如,用于表达蛋白质
和/或将这些多核苷酸序列整合到哺乳动物细胞的基因组中的另外的序列元件。可以用于表达如本文所述的转基因的某些载体包括包含指导基因转录的调控序列(诸如启动子和增强子区域)的载体。用于表达转基因的其他可用载体包含提高转基因的翻译速率或改善由基因转录产生的mrna的稳定性或核输出的多核苷酸序列。这些序列元件包括,例如,5’和3’非翻译区和聚腺苷酸化信号位点,以便指导表达载体上携带的基因的有效转录。适于与本文所述的组合物和方法一起使用的表达载体还可包含编码用于选择包含所述载体的细胞的标志物的多核苷酸。适宜标记物的实例包括编码抗生素(例如氨苄青霉素(ampicillin)、氯霉素(chloramphenicol)、卡那霉素(kanamycin)或诺尔斯菌素(nourseothricin))抗性的基因。
[0068]
如本文所用,术语“野生型”是指在给定生物体中对于特定基因具有最高频率的基因型。
附图说明
[0069]
图1a-1b是用在遍在巨细胞病毒(cmv)启动子的控制下表达绿色荧光蛋白(gfp)的腺相关病毒(aav)载体(图1a)或在癌调蛋白(ocm)启动子(seq id no:1;图1b)的控制下表达gfp的aav载体转导的小鼠耳蜗的一系列荧光图像。示出天然gfp荧光。使用遍在启动子,aav-cmv-gfp在耳蜗内的许多细胞类型中诱导gfp表达,所述细胞类型包括内毛细胞(ihc)、外毛细胞(ohc)、螺旋神经节神经元、间充质细胞和神经胶质细胞(图1a)。使用ohc特异性启动子,aav-ocm(seq id no:1)-gfp仅在ohc中诱导gfp表达(图1b)。
具体实施方式
[0070]
本文描述了用于在耳蜗外毛细胞(ohc)中特异性地诱导转基因表达的组合物和方法。本发明的特征在于能够在内耳的ohc中特异性地表达转基因的ohc特异性启动子。本发明的特征还在于含有可操作地连接至编码多肽的多核苷酸的所述启动子的核酸载体。本文所述的组合物和方法可用于在ohc中特异性地表达编码蛋白质(例如,治疗性蛋白质、报告蛋白或其他目标蛋白质)的多核苷酸,并且因此,可将本文所述的组合物施用于受试者(诸如哺乳动物受试者,例如人)以治疗由ohc的功能障碍引起的病症,诸如听力损失。
[0071]
毛细胞
[0072]
毛细胞是驻留在内耳中的听觉和前庭系统的感觉细胞。耳蜗毛细胞是听觉系统的感觉细胞,并且由两种主要细胞类型组成:负责感测声音的内耳毛细胞和被认为放大低音量声音的ohc。毛细胞以从细胞顶表面突出形成毛细胞束的静纤毛命名。静纤毛的偏转(例如,通过耳蜗毛细胞中的声波)导致机械门控的离子通道打开,从而允许毛细胞释放神经递质以激活神经,从而将机械声音信号转换成可传输到脑部的电信号。耳蜗毛细胞对于正常听力必不可少,并且耳蜗毛细胞的损伤和破坏耳蜗毛细胞功能的基因突变与听力损失和耳聋有关。基因疗法最近已成为治疗听力损失的一种颇具吸引力的治疗方法;然而,本领域缺乏用于使基因疗法中使用的核酸载体特异性地靶向毛细胞的方法。
[0073]
本发明部分地基于与其他耳蜗细胞类型相比在耳蜗ohc中特异性地表达的基因的发现。因此,这些基因的启动子可在内耳的ohc中特异性地诱导基因表达。因此,本文所述的组合物和方法可用于在ohc中表达目标基因(例如,与ohc发育、ohc功能、ohc命运决定、ohc
再生、ohc存活或ohc维持有关的基因,或已知在患有听力损失的受试者中被破坏(例如突变)的基因),以治疗患有听力损失(例如,感觉神经性听力损失)或有此风险的受试者。
[0074]
癌调蛋白
[0075]
本发明部分基于位于ocm翻译起始位点上游的1,140个碱基对(bp)区域的发现,所述区域足以驱动外毛细胞中的基因表达。因此,本文所述的组合物和方法可用于在ohc中表达目标基因(例如,与ohc细胞发育、功能、细胞命运决定、再生、存活或维持有关的基因,或已知在患有听力损失的受试者中被破坏(例如突变)的基因),以治疗患有听力损失(例如,感觉神经性听力损失)或有此风险的受试者。
[0076]
本文所述的组合物和方法包括表2中列出的能够在ohc中特异性地表达转基因的ocm启动子(例如,seq id no:1-3中的任一个),如与seq id no:1-3中的任一个具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸序列。本文所述的多核苷酸可包括位于ocm基因的tss上游和下游的区域,或者可仅包括ocm基因的tss上游的区域。
[0077]
ocm的示例性启动子序列在表2中列出。
[0078]
表2:ocm启动子序列
[0079]
[0080]
[0081]
[0082][0083]
前述多核苷酸可包括在核酸载体中并且可操作地连接至转基因以在ohc中特异性地表达转基因。在一些实施方案中,转基因编码与ohc功能、ohc发育、ohc命运决定、ohc再生、ohc存活或ohc维持有关的蛋白质,或转基因是已发现在患有听力损失、耳聋、听神经病或耳鸣的受试者中发生突变的基因的野生型形式。根据本文所述的方法,可向受试者施用含有一种或多种前述多核苷酸(例如,ohc特异性启动子,例如表2中列出的多核苷酸中的任一者(例如,seq id no:1-3))的组合物,所述多核苷酸可操作地连接至编码用于治疗听力损失、耳聋、听神经病或耳鸣的治疗性蛋白质的转基因。在一些实施方案中,所述转基因编码选自包括以下的组的蛋白质:成束蛋白肌动蛋白集束蛋白2、视黄醛(fscn2)、根蛋白(rdx)、pou 4类同源框3(pou4f3)、trio和f-肌动蛋白结合蛋白(triobp)、taperin(tprn)、含xin肌动蛋白结合重复序列的2(xirp2)、atonal bhlh转录因子1(atoh1)、非生长因子依赖性1转录阻遏蛋白(gfi1)、胆碱能受体烟酸α9亚基(chrna9)、胆碱能受体烟酸α10亚基(chrna10)、钙和整联蛋白结合家族成员3(cib3)、钙粘素23(cdh23)、原钙粘附蛋白15
(pcdh15)、kinocilin(kncn)、pejvakin(dfnb59)、耳畸蛋白(otoferlin)(otof)、mkrn2相反链(mkrn2os)、lim同源框蛋白3(lhx3)、跨膜通道样1(tmc1)、肌球蛋白15(myo15)、肌球蛋白7a(myo7a)、肌球蛋白6(myo6)、肌球蛋白iiia(myo3a)、肌球蛋白iiib(myo3b)、含谷氧还蛋白结构域的富半胱氨酸蛋白1(grxcr1)、蛋白酪氨酸磷酸酶受体型q(ptprq)、晚期角质化包膜蛋白6a(lce6a)、含脂氧合酶同源结构域的蛋白1(loxhd1)、adp-核糖转移酶1(art1)、atp酶质膜ca2+转运2(atp2b2)、钙和整联蛋白结合家族成员2(cib2)、钙电压门控通道辅助亚基α2δ4(cacna2d4)、钙结合蛋白2(cabp2)、表皮生长因子受体途径底物8(eps8)、eps8样2(eps8l2)、espin(espn)、espin样(espnl)、外周蛋白2(prph2)、硬纤毛蛋白(strc)、溶质载体家族8成员a2(slc8a2)、含cchc型锌指的蛋白12(zcchc12)、含富亮氨酸跨膜和o-甲基转移酶结构域的蛋白质(lrtomt2、lrtomt1)、ush1蛋白网络组分和谐素(ush1c)、溶质载体家族26成员5(slc26a5)、压电型机械敏感离子通道组分2(piezo2)、含细胞外富亮氨酸重复序列和纤连蛋白iii型结构域的1(elfn1)、三十四肽重复蛋白24(ttc24)、肌营养不良蛋白(dytn)、kielin/腱蛋白样蛋白(kcp)、卷曲螺旋富谷氨酸蛋白2(coiled-coil glutamate rich protein 2,ccer2)、含富亮氨酸重复序列和跨膜结构域的蛋白质2(leucine-rich repeat and transmembrane domain-containing protein 2,lrtm2)、钾电压门控通道亚家族a成员10(kcna10)、clarin 1(clrn1)、clarin 2(clrn2)、ski家族转录辅阻遏蛋白1(skor1)、含tctex1结构域的蛋白1(tctex1d1)、fc受体样b(fcrlb)、溶质载体家族17成员8(slc17a8)、含谷氧还蛋白结构域的富半胱氨酸蛋白2(grxcr2)、脑源性神经营养因子(bdnf)、丝氨酸蛋白酶抑制剂(serpin)家族e成员3(serpine3)、无义螺旋环螺旋1(nescient helix-loop helix 1,nhlh1)、热激蛋白70(hsp70)、热激蛋白90(hsp90)、转录激活因子6(atf6)、真核翻译起始因子2α激酶3(perk)、丝氨酸/苏氨酸-蛋白激酶/内切核糖核酸酶ire1(ire1)、whirlin(whrn)、癌调蛋白(ocm)、lim同源框1(isl1)、神经营养蛋白3(ntf3)、含跨膜和三十四肽重复序列的4(tmtc4)和结合免疫球蛋白蛋白质(bip)。
[0084]
外源多核苷酸在哺乳动物细胞中的表达
[0085]
诸如myo7a、pou4f3、slc17a8和tmc1的多种基因的突变与感觉神经性听力损失有关。本文所述的组合物和方法可用于诱导或增加由目标基因(例如,与听力损失有关的基因的野生型形式,或参与ohc发育、ohc功能、ohc命运决定、ohc再生、ohc存活或ohc维持的基因)编码的蛋白质在例如ohc中的特异性表达,这通过施用核酸载体来实现,所述核酸载体含有可操作地连接至编码目标蛋白质的多核苷酸序列的ohc特异性启动子序列(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)。已经建立了广泛的方法将蛋白质递送至哺乳动物细胞并用于在哺乳动物细胞中稳定表达编码蛋白质的基因。
[0086]
可结合本文所述的组合物表达的蛋白质(例如,当编码所述蛋白质的转基因可操作地连接至ohc特异性启动子(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸时)是在健康ohc中表达的蛋白质(例如,在ohc发育、ohc功能、ohc再生、ohc命运决定、ohc存活或ohc维持中发挥作用的蛋白质,或在患有感觉神经性听力损失的受试者中缺乏的蛋白质)或
其他目标蛋白质。使用本文所述的组合物和方法可在毛细胞中表达的蛋白质包括actg1、fscn2、rdx、pou4f3、triobp、tprn、xirp2、atoh1、gfi1、chrna9、chrna10、cib3、cdh23、pcdh15、kncn、dfnb59、otof、mkrn2os、lhx3、tmc1、myo15、myo7a、myo6、myo3a、myo3b、grxcr1、ptprq、lce6a、loxhd1、art1、atp2b2、cib2、cacna2d4、cabp2、eps8、eps8l2、espn、espnl、prph2、strc、slc8a2、zcchc12、lrtomt2、lrtomt1、ush1c、slc26a5、piezo2、elfn1、ttc24、dytn、kcp、ccer2、lrtm2、kcna10、clrn1、clrn2、skor1、tctex1d1、fcrlb、slc17a8、grxcr2、bdnf、serpine3、nhlh1、hsp70、hsp90、atf6、perk、ire1、whrn、ocm、isl1、ntf3、tmtc4和bip。本文所述的多核苷酸(例如,ohc特异性启动子)也可用于表达短干扰rna(sirna)、反义寡核苷酸(aso)、核酸酶(例如,crispr相关蛋白9(cas9)、转录激活因子样效应物核酸酶(talen)、锌指核酸酶(zfn)或引导rna(grna)),或ohc中的微小rna。
[0087]
编码目标蛋白质的多核苷酸
[0088]
可用于在哺乳动物细胞中实现治疗有效的细胞内目标蛋白质浓度的一种平台是通过编码目标蛋白质的基因的稳定表达(例如,通过整合到哺乳动物细胞的核或线粒体基因组中,或通过在哺乳动物细胞的核中形成附加型串联体(concatemer))。该基因是编码相应蛋白质的一级氨基酸序列的多核苷酸。为了将外源性基因引入哺乳动物细胞中,可将基因并入载体中。可通过多种方法将载体引入细胞中,所述方法包括转化、转染、转导、直接摄取、射弹轰击以及通过将载体囊封在脂质体中。转染或转化细胞的合适方法的实例包括磷酸钙沉淀、电穿孔、显微注射、感染、脂质转染和直接摄取。此类方法更详细地描述于例如green等,molecular cloning:a laboratory manual,第四版(cold spring harbor university press,new york 2014);以及ausubel等,current protocols in molecular biology(john wiley&sons,new york 2015)中,其中每一个的公开内容通过引用并入本文。
[0089]
还可通过将含有编码目标蛋白质的基因的载体靶向细胞膜磷脂来将目标蛋白质引入哺乳动物细胞中。例如,通过将载体分子连接至vsv-g蛋白(对所有细胞膜磷脂具有亲和力的病毒蛋白),可将载体靶向细胞膜的细胞外表面上的磷脂。可使用本领域技术人员众所周知的方法产生这样的构建体。
[0090]
哺乳动物rna聚合酶对编码目标蛋白质的多核苷酸的识别和结合对于基因表达很重要。因此,可在多核苷酸内包括对募集rna聚合酶并促进转录复合物在转录起始位点的组装的转录因子表现出高亲和力的序列元件。此类序列元件包括,例如,哺乳动物启动子,其序列可被特异性转录起始因子和最终的rna聚合酶识别并结合。哺乳动物启动子的实例已经描述于在线公布的smith等,mol.sys.biol.,3:73中,其公开内容以引用的方式并入本文。本文所述的方法和组合物中使用的启动子是ohc特异性启动子(例如,具有至少85%序列同一性的多核苷酸(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)。
[0091]
一旦将编码目标蛋白质的多核苷酸并入哺乳动物细胞的核dna中,就可通过本领域已知的方法诱导这种多核苷酸的转录。例如,可通过使哺乳动物细胞暴露于外部化学试剂(如调节转录因子和/或rna聚合酶与哺乳动物启动子的结合且由此调控基因表达的剂)来诱导表达。化学试剂可以用于促进rna聚合酶和/或转录因子与哺乳动物启动子的结合,
dermatology 14:315(2005)以及us 2010/0317114中详细描述,其各自的公开内容以引用的方式并入本文。
[0097]
可用于转染靶细胞的其它技术包括挤压穿孔方法。此技术诱导细胞的快速机械变形,以刺激通过响应于所施加的应力而形成的膜孔摄取外源dna。此技术的优点在于,载体不是将多核苷酸递送到细胞(诸如人靶细胞)中所必需的。挤压-穿孔详细描述于,例如,sharei等,journal of visualized experiments 81:e50980(2013)中,其公开内容通过引用并入本文。
[0098]
脂质转染代表可用于转染靶细胞的另一技术。此方法涉及将多核苷酸负载到脂质体中,所述脂质体通常具有朝向脂质体外部的阳离子型官能团(例如季胺或质子化胺)。这由于细胞膜的阴离子性质而促进脂质体与细胞之间的静电相互作用,最终引起外源多核苷酸的摄取,例如通过脂质体与细胞膜的直接融合或通过复合物的内吞作用。脂质转染详细描述于,例如,美国专利7,442,386中,其公开内容通过引用并入本文。利用与细胞膜的离子相互作用来引起外来多核苷酸的摄取的类似技术包括使细胞与阳离子聚合物-多核苷酸复合物接触。与多核苷酸缔合以赋予有利于与细胞膜相互作用的正电荷的示例性阳离子型分子包括活化的树枝状化合物(dendrimer)(描述于,例如,dennig,topics in current chemistry 228:227(2003)中,其公开内容通过引用并入本文)、聚乙烯亚胺和二乙基氨基乙基(deae)-葡聚糖,其作为转染剂的使用详细描述于,例如,gulick等,current protocols in molecular biology 40:i:9.2:9.2.1(1997)中,其公开内容通过引用并入本文。磁珠是可用于以温和且有效的方式转染靶细胞的另一工具,因为此方法利用施加的磁场来指导多核苷酸的摄取。此技术详细描述于例如us 2010/0227406中,其公开内容通过引用并入本文。
[0099]
用于诱导靶细胞对外源多核苷酸的摄取的另一可用工具是激光转染(laserfection),也称为光学转染,一种包括将细胞暴露于特定波长的电磁辐射以温和地对细胞透化并允许多核苷酸穿透细胞膜的技术。此技术的生物活性类似于且在一些情况下被发现优于电穿孔。
[0100]
刺穿转染(impalefection)是可用于将遗传物质输送至靶细胞的另一种技术。它依赖于纳米材料的使用,诸如碳纳米纤维、碳纳米管和纳米线。垂直于基底表面合成针状纳米结构。包含旨在进行细胞内递送的基因的dna连接至纳米结构表面。然后将具有这些针的阵列的芯片压贴在细胞或组织上。被纳米结构刺穿的细胞可以表达一种或多种递送的基因。此技术的实例描述于shalek等,pnas 107:1870(2010)中,其公开内容通过引用并入本文。
[0101]
磁转染也可用于将多核苷酸递送至靶细胞。磁转染原理是使多核苷酸与阳离子型磁性纳米颗粒缔合。磁性纳米颗粒由完全可生物降解的氧化铁制成,并涂有根据应用而变化的特定阳离子型专有分子。它们与基因载体(dna、sirna、病毒载体等)的缔合是通过盐诱导的胶体聚集和静电相互作用实现的。然后,磁性颗粒受到磁体产生的外部磁场的影响而集中在靶细胞上。此技术详细描述于scherer等,gene therapy 9:102(2002)中,其公开内容通过引用并入本文。
[0102]
用于诱导靶细胞对外源多核苷酸的摄取的另一可用工具是声致穿孔,一种包括使用声音(通常是超声频率)改变细胞质膜的通透性,以使细胞透化并允许多核苷酸穿透细胞
膜的技术。此技术详细描述于,例如,rhodes等,methods in cell biology 82:309(2007)中,其公开内容通过引用并入本文。
[0103]
微囊泡代表可用于根据本文所述的方法修饰靶细胞基因组的另一潜在媒介物。例如,可以使用通过糖蛋白vsv-g与例如基因组修饰蛋白(诸如核酸酶)的共过表达引起的微囊泡将蛋白质有效地递送到细胞中,其随后催化内源多核苷酸序列的位点特异性裂解,以制备用于共价掺入目标多核苷酸(诸如基因或调控序列)的细胞的基因组。此类囊泡(也称为纳米囊泡(gesicle))在真核细胞的遗传修饰中的使用详细描述于,例如,quinn等,genetic modification of target cells by direct delivery of active protein[摘要].在:methylation changes in early embryonic genes in cancer[摘要]中,在:美国基因与细胞治疗学会第18届年会记录(proceedings of the 18th annual meeting of the american society of gene and cell therapy);2015年3月13日,摘要编号122中。
[0104]
用于将外源多核苷酸递送至靶细胞的载体
[0105]
除了实现高转录和翻译速率,外源基因在哺乳动物细胞中的稳定表达还可通过将含有所述基因的多核苷酸整合到哺乳动物细胞的核基因组中来实现。已开发出用于将编码外源蛋白质的多核苷酸递送并整合到哺乳动物细胞的核dna中的多种载体。表达载体的实例描述于,例如,gellissen,production ofrecombinant proteins:novel microbial and eukaryotic expression systems(john wiley&sons,marblehead,ma,2006)中。用于在本文所述的组合物和方法中使用的表达载体含有可操作地连接至编码目标蛋白质的多核苷酸序列的ohc特异性启动子(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸),以及,例如,用于表达这些剂和/或将这些多核苷酸序列整合到哺乳动物细胞的基因组中的另外的序列元件。可含有可操作地连接至编码目标蛋白质的转基因的毛细胞特异性启动子的载体包括质粒(例如,可在细胞内部自主复制的环状dna分子)、粘粒(例如,pwe或scos载体)、人工染色体(例如,人的人工染色体(hac)、酵母人工染色体(yac)、细菌人工染色体(bac),或p1衍生的人工染色体(pac))以及病毒载体。可以用于表达目标蛋白质的某些载体包括包含指导基因转录的调控序列(诸如增强子区域)的质粒。用于表达目标蛋白质的其他可用载体包含提高这些基因的翻译速率或改善由基因转录产生的mrna的稳定性或核输出的多核苷酸序列。这些序列元件包括,例如,5’和3’非翻译区、内部核糖体进入位点(ires)和聚腺苷酸化信号位点,以便指导表达载体上携带的基因的有效转录。适于与本文所述的组合物和方法一起使用的表达载体还可包含编码用于选择包含所述载体的细胞的标志物的多核苷酸。适宜标记物的实例包括编码抗生素(例如氨苄青霉素(ampicillin)、氯霉素(chloramphenicol)、卡那霉素(kanamycin)或诺尔斯菌素(nourseothricin))抗性的基因。
[0106]
用于多核苷酸递送的病毒载体
[0107]
病毒基因组提供可用于将相关基因有效递送到靶细胞(例如哺乳动物细胞,例如人细胞)基因组中的丰富载体源。病毒基因组是尤其可用于基因递送的载体,因为此类基因组内包含的多核苷酸通常通过一般化或特殊化转导掺入哺乳动物细胞的核基因组中。这些过程作为天然病毒复制周期的一部分发生,并且不需要添加蛋白质或试剂来诱导基因整
合。病毒载体的实例包括逆转录病毒(例如,逆转录病毒科病毒载体)、腺病毒(例如,ad5、ad26、ad34、ad35和ad48)、细小病毒(例如,腺相关病毒)、冠状病毒、负链rna病毒诸如正粘病毒(例如,流感病毒)、棒状病毒(例如,狂犬病毒和水疱性口炎病毒)、副粘病毒(例如麻疹病毒和仙台病毒)、正链rna病毒(诸如细小核糖核酸病毒和甲病毒)以及双链dna病毒,包括腺病毒、疱疹病毒(例如,1型和2型单纯疱疹病毒、eb病毒、巨细胞病毒)和痘病毒(例如,牛痘、改良安卡拉痘苗(modified vaccinia ankara,mva)、鸡痘和金丝雀痘)。其他病毒包括例如诺沃克(norwalk)病毒、囊膜病毒、黄病毒、呼肠孤病毒、乳多空病毒、嗜肝dna病毒、人乳头瘤病毒、人泡沫病毒和肝炎病毒。逆转录病毒的实例包括:禽白血病-肉瘤病毒、禽c型病毒、哺乳动物c型病毒、b型病毒、d型病毒、致癌逆转录病毒、htlv-blv组、慢病毒、α逆转录病毒、γ逆转录病毒、泡沫病毒(spumavirus)(coffin,j.m.,retroviridae:the viruses and their replication,virology,第三版(lippincott-raven,philadelphia,1996))。其他实例包括鼠白血病病毒、鼠肉瘤病毒、小鼠乳腺肿瘤病毒、牛白血病病毒、猫白血病病毒、猫肉瘤病毒、禽白血病病毒、人t细胞白血病病毒、狒狒内源病毒、长臂猿白血病病毒、梅森-辉瑞(mason pfizer)猴病毒、猿猴免疫缺陷病毒、猿猴肉瘤病毒、劳斯肉瘤病毒和慢病毒。载体的其他实例描述于例如美国专利5,801,030中,其涉及用于在基因疗法中使用的病毒载体的公开内容以引用方式并入本文。
[0108]
用于多核苷酸递送的aav载体
[0109]
在一些实施方案中,将本文所述的组合物和方法的多核苷酸并入raav载体和/或病毒体中,以便有助于将它们引入细胞中。可用于本文所述的组合物和方法中的raav载体是重组多核苷酸构建体,所述重组多核苷酸构建体包含:(1)本文所述的ohc特异性启动子(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸),(2)待表达的异源序列,以及(3)促进异源基因的整合和表达的病毒序列。病毒序列可包括aav的将dna顺式复制和包装(例如,功能性itr)到病毒体中所需的那些序列。在典型的应用中,转基因编码可促进毛细胞发育、毛细胞功能、毛细胞再生、毛细胞命运决定、毛细胞存活或毛细胞维持的蛋白质,或在具有遗传性听力损失形式的受试者中发生突变的毛细胞蛋白的野生型形式,其可用于改善携带与听力损失或耳聋相关的突变的受试者的听力。此类raav载体还可包含标志物或报告基因。可用的raav载体具有一个或多个整体或部分缺失但仍保留功能性侧接itr序列的aav wt基因。aav itr可具有适于特定应用的任一血清型。为了用于本文所述的方法和组合物,itr可以是aav2 itr。使用raav载体的方法描述于,例如,tal等,j.biomed.sci.7:279(2000)以及monahan和samulski,gene delivery 7:24(2000)中,其中每一个涉及用于基因递送的aav载体的公开内容以引用方式并入本文。
[0110]
可将本文所述的多核苷酸和载体(例如,可操作地连接至编码目标蛋白质的转基因的ohc特异性启动子)掺入raav病毒体中,以便有助于将多核苷酸或载体引入细胞中。aav的衣壳蛋白构成病毒体的外部非核酸部分并且由aav cap基因编码。cap基因编码病毒体组装所需的三种病毒外壳蛋白vp1、vp2和vp3。raav病毒体的构建已描述于,例如,us 5,173,414;us 5,139,941;us 5,863,541;us 5,869,305;us 6,057,152;和us 6,376,237;以及rabinowitz等,j.virol.76:791(2002)和bowles等,j.virol.77:423(2003)中,其中每一个
涉及用于基因递送的aav载体的公开内容以引用方式并入本文。
[0111]
可与本文所述的组合物和方法结合使用的raav病毒体包括源自多种aav血清型的那些,包括aav 1、2、3、4、5、6、7、8、9、10、rh10、rh39、rh43、rh74、anc80、anc80l65、dj/8、dj/9、7m8、php.b、php.eb和php.s。对于靶向毛细胞,aav1、aav2、aav2quad(y-f)、aav6、aav9、anc80、anc80l65、dj/9、7m8和php.b可特别有用。为转导视网膜而进化形成的血清型也可用于本文所述的方法和组合物中。不同血清型的aav载体和aav蛋白的构建和使用描述于,例如,chao等,mol.ther.2:619(2000);davidson等,proc.natl.acad.sci.usa 97:3428(2000);xiao等,j.virol.72:2224(1998);halbert等,j.virol.74:1524(2000);halbert等,j.virol.75:6615(2001);以及auricchio等,hum.molec.genet.10:3075(2001)中,其中每一个涉及用于基因递送的aav载体的公开内容以引用方式并入本文。
[0112]
还可与本文所述的组合物和方法结合使用的是假型化raav载体。假型化载体包括给定血清型(例如,aav9)的aav载体,其被衍生自除给定血清型之外的血清型(例如,aav1、aav2、aav2quad(y-f)、aav3、aav4、aav5、aav6、aav7、aav8等)的衣壳基因假型化。涉及假型化raav病毒粒子的构建和使用的技术是本领域已知的,并且描述于例如在duan等,j.virol.75:7662(2001);halbert等,j.virol.74:1524(2000);zolotukhin等,methods,28:158(2002);以及auricchio等,hum.molec.genet.10:3075(2001)中。
[0113]
可使用在病毒体衣壳内具有突变的aav病毒体,以比非突变衣壳病毒体更有效地感染特定细胞类型。例如,合适的aav突变体可具有用于促进aav对特定细胞类型的靶向的配体插入突变。aav衣壳突变体(包括插入突变体、丙氨酸筛选突变体和表位标签突变体)的构建和表征描述于wu等,j.virol.74:8635(2000)中。可在本文所述的方法中使用的其他raav病毒粒子包括通过病毒的分子育种以及通过外显子改组而产生的那些衣壳杂合体。参见,例如,soong等,nat.genet.,25:436(2000)以及kolman和stemmer,nat.biotechnol.19:423(2001)。
[0114]
药物组合物
[0115]
本文所述的多核苷酸(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)可以可操作地连接至转基因(例如,编码目标蛋白质的转基因)且并入媒介物中,以用于施用至患者,如患有感觉神经性听力损失的人患者。包含含有可操作地连接至治疗性转基因的本文所述的多核苷酸的载体(诸如病毒载体)的药物组合物可以使用本领域已知的方法制备。例如,此类组合物可以使用,例如,生理上可接受的载剂、赋形剂或稳定剂(remington:the science and practice of pharmacology第22版,allen,l.编(2013);以引用方式并入本文)并且以期望形式,例如以冻干制剂或水溶液的形式来制备。
[0116]
含有可操作地连接至转基因的本文所述的多核苷酸(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)的核酸载体(例如,病毒载体)的混合物可在与一种或多种赋形剂、载体或稀释剂适当混合的水中制备。分散液也可在甘油、液体聚乙二醇和它们的混合物以及在油中制备。在正常储存和使用条件下,这些制剂可含有防腐剂以防止微生物生长。适于
注射使用的药物形式包括无菌水溶液或分散液以及用于临时制备无菌可注射溶液或分散液的无菌粉末(描述于us 5,466,468中,其公开内容以引用方式并入本文)。在任一情况下,制剂可为无菌的且可为流体,达到存在容易可注射性的程度。制剂在制造和储存条件下可以是稳定的并且可在防止微生物(诸如细菌和真菌)的污染作用的条件下保存。载体可以是含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)、其合适的混合物,以及植物油的溶剂或分散介质。可例如通过使用包衣诸如卵磷脂、通过在分散液的情况下维持所需要的粒度以及通过使用表面活性剂来维持适当的流动性。可通过多种抗细菌剂和抗真菌剂(例如对羟苯甲酸酯、氯丁醇、酚、山梨酸、硫柳汞等)来预防微生物的作用。在许多情况下,将优选包括等渗剂,例如糖或氯化钠。延长可注射组合物的吸收可通过在组合物中使用延迟吸收的试剂,例如单硬脂酸铝和明胶来达成。
[0117]
例如,如果需要,可将包含本文所述的药物组合物的溶液适当地缓冲,并且首先用足够的盐水或葡萄糖使液体稀释剂等渗。这些特定的水溶液尤其适用于静脉内、肌内、皮下和腹膜内施用。就这一点而言,可使用的无菌水性介质将为本领域技术人员根据本公开内容所已知的。例如,可将一个剂量溶解于1ml等渗nacl溶液中并且添加到1000ml皮下输液流体中或在建议的输注部位注射。根据所治疗受试者的疾患,将必要地出现一定的剂量变化。为了向内耳局部施用,可将组合物配制成包含合成外淋巴液。示例性合成外淋巴液包括20-200mm nacl、1-5mm kcl、0.1-10mm cacl2、1-10mm葡萄糖和2-50mm hepe,具有介于约6与9之间的ph以及约300mosm/kg的渗透度。在任何事件中,负责施用的人员将确定用于个体受试者的适当剂量。此外,对于人施用,制剂应满足fda生物学标准办公室(fda office of biological standards)所要求的无菌性、热原性、一般安全性和纯度标准。
[0118]
治疗方法
[0119]
本文所述的组合物可通过多种途径施用于患有感觉神经性听力损失或有此风险的受试者,诸如对内耳局部施用(例如,诸如通过卵圆窗、圆窗或半规管(例如,水平半规管)施用到外淋巴或内淋巴中,或通过经鼓室或鼓室内注射,例如施用至ohc)、静脉内、肠胃外、皮内、透皮、肌内、鼻内、皮下、经皮、气管内、腹膜内、动脉内、血管内、吸入、灌注、灌洗和口服施用。在任何给定情况下,最合适的施用途径将取决于所施用的特定组合物、患者、药物配制方法、施用方法(例如,施用时间和施用途径)、患者的年龄、体重、性别、所治疗的疾病的严重程度、患者的饮食和患者的排泄率。组合物可施用一次或多于一次(例如,一年一次、一年两次、一年三次、两月一次或一月一次)。
[0120]
可如本文所述治疗的受试者是患有感觉神经性听力损失或有此风险的受试者。本文所述的组合物和方法可用于治疗具有ohc损伤(例如,与声创伤、疾病或感染、头部创伤、耳毒性药物或衰老相关的损伤)或有此风险的受试者、患有感觉神经性听力损失、耳聋或听神经病或有此风险的受试者、患有耳鸣(例如,仅耳鸣,或与感觉神经性听力损失相关的耳鸣)或有此风险的受试者、具有与听力损失相关的基因突变的受试者、或具有遗传性听力损失、耳聋、听神经病或耳鸣家族史的受试者。在一些实施方案中,与毛细胞(例如,ohc)的损伤或损失相关的疾病是自身免疫性疾病或疾患,其中自身免疫反应导致毛细胞损伤或死亡。与感觉神经性听力损失相关的自身免疫性疾病包括自身免疫性内耳病(aied)、结节性多动脉炎(pan)、科根综合征、复发性多软骨炎、系统性红斑狼疮(sle)、韦格纳氏肉芽肿病、斯耶格伦综合征和白塞氏病。一些感染性疾病(如莱姆病和梅毒)也可引起感觉神经性听力
损失(例如,通过触发自身抗体产生)。病毒感染(如风疹、巨细胞病毒(cmv)、淋巴细胞性脉络丛脑膜炎病毒(lcmv)、hsv 1和2型、西尼罗河病毒(wnv)、人免疫缺陷病毒(hiv)、水痘带状疱疹病毒(vzv)、麻疹和腮腺炎)也可引起感觉神经性听力损失。在一些实施方案中,受试者患有与ohc损失相关或由ohc损失引起的听力损失。本文所述的方法可包括在用本文所述的组合物治疗或施用之前,针对已知与听力损失相关的基因中的一种或多种突变筛选受试者的步骤。可使用本领域技术人员已知的标准方法(例如,基因测试)针对基因突变筛选受试者。本文所述的方法还可包括在用本文所述的组合物治疗或施用之前评估受试者的听力功能的步骤。可使用标准测试评估听力,诸如听力测验法、听性脑干反应(abr)、耳蜗电图描记法(ecog)和耳声发射。这些测试还可用于在用本文所述的组合物治疗或施用之后评估受试者的听力功能。本文所述的组合物和方法还可作为预防性治疗施用于有发展听力损失风险的患者,例如,具有听力损失家族史(例如,遗传性听力损失)的患者、携带与听力损失相关的基因突变但尚未表现出听力障碍的患者,或暴露于获得性听力损失(例如,声创伤、疾病或感染、头部创伤、耳毒性药物或衰老)的风险因素的患者。
[0121]
本文所述的组合物和方法可用于促进或诱导受试者的毛细胞再生(例如,ohc再生)。可受益于促进或诱导ohc再生的组合物的受试者包括因ohc损失(例如,与创伤(例如,声创伤或头部创伤)、疾病或感染、耳毒性药物或衰老相关的ohc损失)而导致患有听力损失的受试者,以及异常ohc(例如,与正常ohc相比不正常发挥作用的ohc)、ohc损伤(例如,与创伤(例如,声创伤或头部创伤)、疾病或感染、耳毒性药物或衰老相关的ohc损伤)或由基因突变或先天性异常导致的ohc数量减少的受试者。本文所述的组合物和方法还可用于促进或增加ohc存活(例如,增加损伤ohc的存活,促进损伤ohc的修复,或在有ohc损失(例如,由于年龄、暴露于嘈杂的噪音、疾病或感染、头部创伤或耳毒性药物引起的ohc损失)风险的受试者中保存ohc)。本文所述的组合物和方法还可用于促进或增加ohc成熟,这可导致改善的听觉功能。
[0122]
本文所述的组合物和方法还可用于在接受过耳毒性药物治疗或正在接受或即将开始接受耳毒性药物治疗的受试者中预防或减少耳毒性药物引起的毛细胞损伤或死亡(例如,ohc损伤或死亡)。耳毒性药物对内耳的细胞有毒,并且可引起感觉神经性听力损失、耳鸣或这些症状的组合。已发现具有耳毒性的药物包括氨基糖苷抗生素(例如,庆大霉素、新霉素、链霉素、妥布霉素、卡那霉素、万古霉素和阿米卡星)、紫霉素、抗肿瘤药(例如,含铂化疗剂,诸如顺铂、卡铂和奥沙利铂)、髓袢利尿剂(例如,依他尼酸和呋塞米)、水杨酸盐(例如,阿司匹林,特别是在高剂量下)和奎宁。在一些实施方案中,本文所述的方法预防或减少与声创伤、疾病或感染、头部创伤或衰老相关的毛细胞损伤或死亡(例如,ohc损伤或死亡)。
[0123]
用于治疗如本文所述的受试者的可操作地连接至ohc特异性启动子(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)的转基因可以是编码在健康ohc中表达的蛋白质(例如在ohc发育、ohc功能、ohc命运决定、ohc再生、ohc存活或ohc维持中起作用的蛋白质,或在患有感觉神经性听力损失的受试者中缺乏的蛋白质,另一种目标蛋白质(例如,治疗性蛋白质或报告蛋白,如荧光蛋白、lacz或荧光素酶)、sirna、aso、核酸酶或微小rna)的转基因。可基于受试者的听力损失的原因(例如,如果受试者的听力损失与特定基因突变相
关,那么转基因可以是在受试者中发生突变的所述基因的野生型形式,或如果受试者患有与毛细胞损失相关的听力损失,那么转基因可编码促进毛细胞再生的蛋白质)、受试者听力损失的严重程度、受试者的毛细胞的健康状况、受试者的年龄、受试者的听力损失家族史或其他因素选择转基因。可由可操作地连接至毛细胞特异性启动子的转基因表达以治疗如本文所述的受试者的蛋白质包括actg1、fscn2、rdx、pou4f3、triobp、tprn、xirp2、atoh1、gfi1、chrna9、chrna10、cib3、cdh23、pcdh15、kncn、dfnb59、otof、mkrn2os、lhx3、tmc1、myo15、myo7a、myo6、myo3a、myo3b、grxcr1、ptprq、lce6a、loxhd1、art1、atp2b2、cib2、cacna2d4、cabp2、eps8、eps8l2、espn、espnl、prph2、strc、slc8a2、zcchc12、lrtomt2、lrtomt1、ush1c、slc26a5、piezo2、elfn1、ttc24、dytn、kcp、ccer2、lrtm2、kcna10、clrn1、clrn2、skor1、tctex1d1、fcrlb、slc17a8、grxcr2、bdnf、serpine3、nhlh1、hsp70、hsp90、atf6、perk、ire1、whrn、ocm、isl1、ntf3、tmtc4和bip。
[0124]
治疗可包括以各种单位剂量施用包含含有本文所述的ohc特异性启动子的核酸载体(例如,aav病毒载体)的组合物。每个单位剂量通常将包含预定量的治疗性组合物。待施用的量以及具体施用途径和制剂在临床领域技术人员的技能范围内。单位剂量无需作为单个注射施用,但可包含设定时间段内的连续输注。可使用注射泵进行给药以控制输注速率,以便使对内耳(例如,耳蜗)的损伤最小化。在核酸载体是aav载体(例如,aav1、aav2、aav2quad(y-f)、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、rh10、rh39、rh43、rh74、anc80、anc80l65、dj/8、dj/9、7m8、php.b、php.eb或php.s载体)的情况下,病毒载体可以例如约1x109个载体基因组(vg)/ml至约1x10
16
vg/ml(例如,1x109vg/ml、2x109vg/ml、3x109vg/ml、4x109vg/ml、5x109vg/ml、6x109vg/ml、7x109vg/ml、8x109vg/ml、9x109vg/ml、1x10
10
vg/ml、2x10
10
vg/ml、3x10
10
vg/ml、4x10
10
vg/ml、5x10
10
vg/ml、6x10
10
vg/ml、7x10
10
vg/ml、8x10
10
vg/ml、9x10
10
vg/ml、1x10
11
vg/ml、2x10
11
vg/ml、3x10
11
vg/ml、4x10
11
vg/ml、5x10
11
vg/ml、6x10
11
vg/ml、7x10
11
vg/ml、8x10
11
vg/ml、9x10
11
vg/ml、1x10
12
vg/ml、2x10
12
vg/ml、3x10
12
vg/ml、4x10
12
vg/ml、5x10
12
vg/ml、6x10
12
vg/ml、7x10
12
vg/ml、8x10
12
vg/ml、9x10
12
vg/ml、1x10
13
vg/ml、2x10
13
vg/ml、3x10
13
vg/ml、4x10
13
vg/ml、5x10
13
vg/ml、6x10
13
vg/ml、7x10
13
vg/ml、8x10
13
vg/ml、9x10
13
vg/ml、1x10
14
vg/ml、2x10
14
vg/ml、3x10
14
vg/ml、4x10
14
vg/ml、5x10
14
vg/ml、6x10
14
vg/ml、7x10
14
vg/ml、8x10
14
vg/ml、9x10
14
vg/ml、1x10
15
vg/ml、2x10
15
vg/ml、3x10
15
vg/ml、4x10
15
vg/ml、5x10
15
vg/ml、6x10
15
vg/ml、7x10
15
vg/ml、8x10
15
vg/ml、9x10
15
vg/ml、or 1x10
16
vg/ml)的剂量以1μl至200μl(例如,1、2、3、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、110、120、130、140、150、160、170、180、190或200μl)的体积施用于患者。aav载体可以约约1x107vg/耳朵至约2x10
15
vg/耳朵(例如,1x107vg/耳朵、2x107vg/耳朵、3x107vg/耳朵、4x107vg/耳朵、5x107vg/耳朵、6x107vg/耳朵、7x107vg/耳朵、8x107vg/耳朵、9x107vg/耳朵、1x108vg/耳朵、2x108vg/耳朵、3x108vg/耳朵、4x108vg/耳朵、5x108vg/耳朵、6x108vg/耳朵、7x108vg/耳朵、8x108vg/耳朵、9x108vg/耳朵、1x109vg/耳朵、2x109vg/耳朵、3x109vg/耳朵、4x109vg/耳朵、5x109vg/耳朵、6x109vg/耳朵、7x109vg/耳朵、8x109vg/耳朵、9x109vg/耳朵、1x10
10
vg/耳朵、2x10
10
vg/耳朵、3x10
10
vg/耳朵、4x10
10
vg/耳朵、5x10
10
vg/耳朵、6x10
10
vg/耳朵、7x10
10
vg/耳朵、8x10
10
vg/耳朵、9x10
10
vg/耳朵、1x10
11
vg/耳朵、2x10
11
vg/耳朵、3x10
11
vg/耳朵、4x10
11
vg/耳朵、5x10
11
vg/耳朵、6x10
11
vg/耳朵、7x10
11
vg/耳朵、8x10
11
vg/耳朵、9x10
11
vg/耳朵、1x10
12
vg/耳
朵、2x10
12
vg/耳朵、3x10
12
vg/耳朵、4x10
12
vg/耳朵、5x10
12
vg/耳朵、6x10
12
vg/耳朵、7x10
12
vg/耳朵、8x10
12
vg/耳朵、9x10
12
vg/耳朵、1x10
13
vg/耳朵、2x10
13
vg/耳朵、3x10
13
vg/耳朵、4x10
13
vg/耳朵、5x10
13
vg/耳朵、6x10
13
vg/耳朵、7x10
13
vg/耳朵、8x10
13
vg/耳朵、9x10
13
vg/耳朵、1x10
14
vg/耳朵、2x10
14
vg/耳朵、3x10
14
vg/耳朵、4x10
14
vg/耳朵、5x10
14
vg/耳朵、6x10
14
vg/耳朵、7x10
14
vg/耳朵、8x10
14
vg/耳朵、9x10
14
vg/耳朵、1x10
15
vg/耳朵或2x10
15
vg/耳朵)的剂量施用于受试者。
[0125]
本文所述的组合物以足以改善听力、减少耳鸣、增加由可操作地连接至ohc特异性启动子的转基因编码的蛋白质的表达、增加由可操作地连接至ohc-特异性启动子的转基因编码的蛋白质的功能、预防或减少ohc损伤(例如,与声创伤、头部创伤、耳毒性药物、疾病或感染或衰老有关的ohc损伤)、预防或减少ohc死亡(例如,耳毒性药物引起的ohc死亡、噪音相关的ohc死亡、年龄相关的ohc死亡、疾病或感染相关的ohc死亡或头部创伤相关的ohc死亡)、促进或增加ohc发育、增加ohc数量(例如,促进或诱导ohc再生)、促进或增加ohc存活、促进或增加ohc成熟或改善ohc功能的量施用。听力可使用标准听力测试(例如,听力测验法、abr、耳蜗电图描记法(ecog)和耳声发射)进行评估,并且与治疗前获得的听力测量结果相比可改善5%或更多(例如,5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%、125%、150%、200%或更多)。在一些实施方案中,以足以改善受试者理解对话的能力的量施用组合物。本文所述的组合物也可以足以减缓或预防感觉神经性听力损失的发展或进展的量施用(例如,在携带与听力损失相关的基因突变,具有听力损失的家族史(例如,遗传性听力损失),或已暴露于与听力损失相关的风险因素(例如,耳毒性药物、头部创伤、疾病或感染或声创伤),但不表现出听力障碍的受试者中,或在表现出轻度至中度听力损失的受试者中)。施用于受试者的核酸载体中由可操作地连接至ohc特异性启动子的转基因编码的蛋白质的表达可使用免疫组织化学、蛋白质印迹分析、定量实时pcr或本领域已知的用于检测蛋白质或mrna的其他方法进行评估,并且与施用本文所述的组合物之前的表达相比,可增加5%或更多(例如,5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%、125%、150%、200%或更多)。ohc数量、ohc功能或由施用于受试者的核酸载体编码的蛋白质的功能可基于听力测试间接评估,并且与施用本文所述的组合物之前的ohc数量、ohc功能或蛋白质的功能相比,可增加5%或更多(例如,5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%、125%、150%、200%或更多)。与在未治疗的受试者中通常观察到的ohc损伤和死亡相比,ohc损伤或死亡可减少5%或更多(例如,5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%、125%、150%、200%或更多)。这些效果可发生在,例如,施用本文所述的组合物之后的1周、2周、3周、4周、5周、6周、7周、8周、9周、10周、15周、20周、25周或更长时间内。取决于用于治疗的施用剂量和途径,可在施用组合物之后1个月、2个月、3个月、4个月、5个月、6个月或更长时间对患者进行评估。根据评估结果,患者可能接受另外的治疗。
[0126]
药盒
[0127]
本文所述的组合物可提供于用于治疗感觉神经性听力损失的药盒中。组合物可包含本文所述的多核苷酸(例如,与表2中列出的启动子序列中的任一个(例如,seq id no:1-3中的任一个)具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)、含有此类
多核苷酸的核酸载体、以及含有可操作地连接至编码目标蛋白质(例如,可在毛细胞中表达以治疗听力损失的蛋白质)的转基因的本文所述的多核苷酸的核酸载体。可将核酸载体包装在aav病毒衣壳(例如,aav1、aav2、aav2quad(y-f)、aav6、aav8、aav9、anc80、anc80l65、dj/9、7m8或php.b)中。药盒还可包括包装说明书,其指示药盒的使用者(诸如医师)执行本文所述的方法。药盒可任选地包括注射器或用于施用组合物的其他装置。
[0128]
实施例
[0129]
提出以下实施例以便为本领域普通技术人员提供本文所述的组合物和方法可如何使用、制备和评价的描述,并且旨在纯粹是对本发明的举例说明且不旨在限制发明人所认定的发明范围。
[0130]
实施例1:ocm启动子序列在体内诱导鼠耳蜗中的ohc中的转基因表达
[0131]
为了确定构建的ocm启动子(seq id no:1)在体内诱导ohc中的转基因表达中的功效,用在巨细胞病毒(cmv)启动子的控制下表达gfp的aav载体或在ocm启动子的控制下表达gfp的aav载体转导小鼠耳蜗。具体地,通过后半规管将aav-ocm-gfp病毒以每耳朵7.7e+9个载体基因组的剂量输注至两天龄的cba/caj小鼠。使小鼠从手术中恢复并将其安乐死,并在19天后用10%的正常缓冲福尔马林灌注。收获内耳颞骨并在8%edta中脱钙三天。从脱钙的颞骨解剖耳蜗,用肌球蛋白7a(myo7a)抗体进行免疫染色以标记所有毛细胞,并安装在载玻片上进行共聚焦成像。示出天然gfp荧光。使用遍在启动子,aav-cmv-gfp在耳蜗内的许多细胞类型中诱导gfp表达,所述细胞类型包括内毛细胞、外毛细胞、螺旋神经节神经元、间充质细胞和神经胶质细胞(图1a)。使用外毛细胞特异性启动子,aav-ocm(seq id no:1)-gfp仅在外毛细胞中诱导gfp表达(图1b)。
[0132]
实施例2:将包含含有毛细胞特异性启动子的核酸载体的组合物施用于患有感觉神经性听力损失的受试者
[0133]
根据本文公开的方法,本领域的熟练医师可以治疗具有感觉神经性听力损失的患者,诸如人患者,以改善或恢复听力。为此,本领域的熟练医师可向人患者施用含有aav载体(例如,aav1、aav2、aav2quad(yf)、aav6、aav9、anc80、anc80l65、dj/9、7m8或php.b)的组合物,所述aav载体含有可操作地连接至编码治疗性蛋白质的转基因的外毛细胞特异性启动子(例如,与seq id no:1-3中的任一个的序列具有至少85%序列同一性(例如,85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性)的多核苷酸)。包含aav载体的组合物可以,例如,通过局部施用于内耳(例如,注射到外淋巴中或通过圆窗膜)而施用给患者,以治疗感觉神经性听力损失。
[0134]
在将组合物施用给患者后,本领域的熟练从业人员可以通过多种方法监测由转基因编码的治疗性蛋白质的表达,以及响应于疗法的患者的改善。例如,医师可在施用组合物之后通过执行标准测试(诸如听力测验法、abr、耳蜗电图描记法(ecog)和耳声发射)来监测患者的听力。与施用组合物之前的听力测试结果相比,发现在施用组合物之后患者在一种或多种测试中表现出听力的改善,这表明患者对治疗有良好的响应。可以按需确定和施用后续剂量。
[0135]
其他实施方案
[0136]
在不偏离本发明的范围和精神的情况下,所述发明的各种修改和变化对本领域技术人员将是显而易见的。尽管已结合具体实施方案对本发明进行了描述,但是应当理解所
要求保护的本发明不应当不适当地限定于此类具体实施方案。实际上,所描述的用于执行本发明的方式的各种修改对于本领域的技术人员是显而易见的,且旨在包含在本发明的范围内。其他实施方案在权利要求中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1