DC661在治疗肝细胞癌中的用途
本发明涉及肝细胞癌的预防和/或治疗领域,特别涉及dc661在治疗肝细胞癌中的用途。
背景技术:
dc661是最近新合成的氯喹二聚体衍生物,一种强效的、高选择性的棕榈酰蛋白硫酯酶1(ppt1)抑制剂,并且已被证明具有抗肿瘤活性。通过生物信息学分析发现,ppt1在肝细胞癌中高表达,并且高表达ppt1的hcc患者的总生存期更差。通过cox比例风险回归分析表明,ppt1表达是hcc患者总生存期的独立危险因素。因此,ppt1可能是靶向治疗肝细胞癌的潜在的分子靶标。
研究证明,dc661可以在体外和体内异种移植肿瘤模型中抑制溶酶体从而抑制自噬,并产生抗肿瘤活性,而不会产生明显的不良影响。并且,在相同的药物浓度下,与其他的氯喹衍生物(lys05或hcq)相比,dc661具有最高效率的抑制溶酶体从而抑制自噬,和最强的抗肿瘤活性。研究证明,dc661可以抑制肝癌细胞中的热休克蛋白70.1(hsp70.1)的表达,从而破坏溶酶体的膜稳定性。抑制溶酶体被认为是dc661的关键治疗作用,因为溶酶体内的组织蛋白酶释放至细胞质中会导致细胞凋亡。目前,dc661已经被证明在黑色素瘤中有抗肿瘤作用。但是,dc661抑制溶酶体的潜在的分子机制仍不清楚。而且,对于氯喹衍生物dc661治疗肝细胞癌的研究,目前尚未见报道。
自噬是一个吞噬自身细胞质蛋白或细胞器并使其包被进入囊泡,并与溶酶体融合形成自噬溶酶体,降解其所包裹的内容物的过程,借此实现细胞本身的代谢需要和某些细胞器的更新。实质上,自噬是机体在各种应激信号诱导下的一种自我保护机制,并且能够促进肿瘤细胞的存活。并且,肿瘤组织中的基础自噬水平要比正常器官组织的自噬水平要高的多。由于经典的和非经典的的自噬途径都依赖于溶酶体降解,溶酶体提供了抑制自噬的最佳靶点。多个临床研究证明,靶向溶酶体治疗能够显著地提高抗肿瘤疗效。
肝细胞癌,是原发性肝癌的一种。肝细胞癌在世界范围内是一种常见且多发的疾病,是世界上第7位常见癌症和排名第3位肿瘤致死病因。原发性肝癌是目前我国第4位常见恶性肿瘤及第2位肿瘤致死病因,严重威胁我国人民的生命和健康。
目前,人们认为,肝细胞癌被称之为“癌肿之王”,其最主要的治疗手段是以手术为主的综合治疗,例如,手术切除、肝移植、经动脉化疗栓塞、全身化疗、分子靶向治疗和免疫治疗等。然而,手术将不可避免地对患者带来较高的风险,如围术期死亡率高、远期效果欠佳,同时还会加重患者家庭的经济负担。并且,由于缺乏平时的定期体检,很大一部分hcc患者在确诊时就处于晚期阶段,失去了手术机会。
申请号cn201410648801.9的专利提供用于治疗肝细胞癌的治疗性生物制品,包含与抗体偶联的凝结剂的偶联物,其中所述抗体特异性地结合哺乳动物plvap蛋白的细胞外结构域表位。这些试剂特异性地靶向hcc肿瘤并治疗hcc。本发明还提供使用这些偶联物的方法,如通过施用本发明提供的偶联物或本发明提供的组合物如药物组合物治疗hcc的方法。然而,目前的分子靶向药由于适应性耐药的发生和严重的副作用影响了它们的治疗效果。
因此,亟待采用新的非手术方法来有效治疗肝细胞癌。
技术实现要素:
(一)解决的技术问题
本发明的目的在于提供dc661在治疗肝细胞癌中的用途,以解决现有技术采用手术治疗肝细胞癌将不可避免地对患者带来较高的风险,采用分子靶向药治疗由于适应性耐药的发生和严重的副作用影响治疗效果的问题。
(二)技术方案
为实现上述dc661在治疗肝细胞癌中的用途解决现有技术采用手术治疗肝细胞癌将不可避免地对患者带来较高的风险,采用分子靶向药治疗由于适应性耐药的发生和严重的副作用影响治疗效果的问题,本发明提供如下技术方案:
根据上述需求,本发明提供了dc661在制备用于预防和/或治疗个体的肝细胞癌中的用途。
在本发明中,dc661是指cas号为1872387-43-3;分子式为c31h39cl2n5的物质;其是二聚体的氯喹衍生物,其化学结构如图1a所示。
在本发明中,“预防和/或治疗”是指预防和/或延缓疾病或病症的发生或使之正常化。
在一个实施方案中,所述dc661的浓度为0.125μm-4μm。
进一步的,在优选的实施方案中,所述dc661的浓度为0.5μm-3μm。
更优选的实施方案中,所述dc661的浓度为0.5μm或3μm。
更优选的实施方案中,所述dc661的浓度为3μm。
在一个实施方案中,所述个体为哺乳动物,所述哺乳动物包括但不限于大鼠、小鼠、非人灵长类、人、犬、猫、马、牛、绵羊、猪、山羊。
优选地,所述个体为人。
(三)有益效果
与现有技术相比,本发明提供了dc661在治疗肝细胞癌中的用途,具备以下有益效果:采用本发明,dc661可以有效下调维持溶酶体膜稳定性的hsp70.1/bmp/asm通路当中的关键分子hsp70.1的表达,抑制溶酶体,从而抑制自噬并通过线粒体途径诱导肿瘤细胞凋亡,发挥抗肿瘤效果。
附图说明
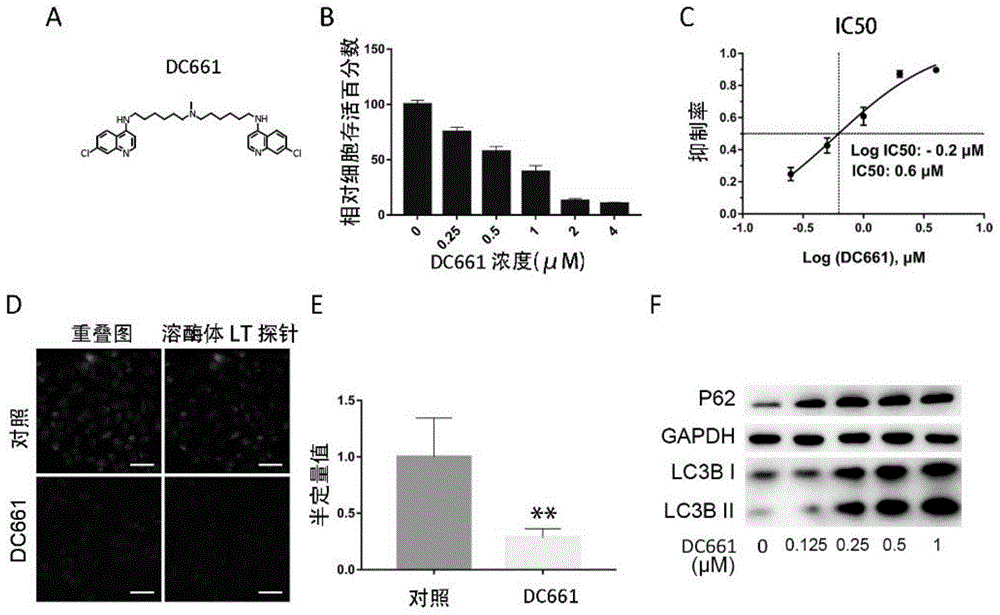
图1示出了:(a)dc661的化学结构;(b)cck8细胞生存活力检测,dc661具有剂量依赖的抗肿瘤效应;(c)ic50(半数抑制浓度,24h);(d)通过dc661(3μm,6h)处理,溶酶体lt绿色荧光探针染色减弱,与对照细胞相比显示出显着差异(**p<0.01);(e)溶酶体lt探针绿色荧光强度的相对定量;(f)用6小时的不同处理对p62和lc3b(自噬标签蛋白)进行western印迹。
图2示出了:(a)用6小时的不同处理对hsp70.1进行western印迹;(b)通过western印迹和半定量分析确定上述基因的蛋白表达水平,与对照组相比显示出显着差异(**p<0.01);(c)用6小时的不同处理对hsp70.1的免疫荧光染色;(d)通过hsp70.1的荧光强度测量半定量,与对照细胞相比显示出显着差异(*p<0.05);(e)用3μm的dc661对肝癌细胞系hep3b处理6小时,通过qrt-pcr检测hsp70.1的mrna表达水平,与对照细胞相比显示出显着差异(*p<0.05);(f)用6小时的不同处理对p-hsf1进行western印迹;(g)通过western印迹和半定量分析确定p-hsf1蛋白表达水平,与对照组相比显示出显着差异(**p<0.01)。
图3示出了:(a)用6小时的不同处理对组织蛋白酶b的免疫荧光染色,dc661处理能够诱导溶酶体内的组织蛋白酶b释放至胞质当中;(b)用6小时的不同处理对线粒体膜电位的jc-1染色,dc661处理能够诱导线粒体膜电位去极化;(c)用6小时的不同处理对细胞色素c的免疫荧光染色,dc661处理能够诱导线粒体内的细胞色素c释放至胞质当中,tom20为线粒体的标签蛋白;(d)用3μm的dc661对肝癌细胞系hep3b处理6小时,greennuctm活细胞caspase-3活性检测试剂盒对细胞进行染色,然后进行流式分析;(e)caspase-3活化的阳性肝癌细胞的流式定量分析;(f)用3μm的dc661对肝癌细胞系hep3b处理6小时,annexinv-fitc/pi细胞凋亡检测试剂盒对细胞进行染色,然后进行流式分析;(g)凋亡的肝癌细胞的流式定量分析。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1、dc661抑制人源肝细胞癌细胞系hep3b细胞的活性
采用如上述实施例1人源肝细胞癌细胞系hep3b细胞作为体外实验模型,并将人源肝细胞癌细胞系hep3b细胞分为2组,分别为对照组(pbs处理)和dc661组。使用不同浓度的dc661(dc661购自targetmol,产品目录编号:t5538)处理人源肝细胞癌细胞系hep3b,进行ic50测试、cck8测定、western印迹和溶酶体lt绿色荧光探针染色分析。
cck8细胞生存活力检测,dc661具有剂量依赖的抗肿瘤效应(图1b),表明dc661抑制人源肝细胞癌细胞的活性。ic50结果如图1c所示。通过dc661(3μm,6h)处理,溶酶体lt绿色荧光探针染色减弱,通过荧光半定量分析显示,与对照细胞相比显示出显著差异(**p<0.01)(图1d和1e),表明dc661能够抑制溶酶体。通过蛋白质印迹法检测了在有或没有dc661处理的肝细胞癌细胞的p62和lc3b的蛋白水平。结果表明,dc661能够抑制自噬(图1f)。
实施例2、dc661抑制人源肝细胞癌细胞维持溶酶体膜稳定性的基因蛋白表现情况
采用如上述实施例1人源肝细胞癌细胞系hep3b细胞作为体外实验模型,并将人源肝细胞癌细胞系hep3b细胞分为2组,分别为对照组(pbs处理)和dc661组。使用3μm的dc661来处理人源肝细胞癌细胞系hep3b细胞,于6h检测维持溶酶体膜稳定性的关键基因hsp70.1及其转录因子hsf1。
蛋白质印迹法检测结果显示,与对照组相比,dc661显著下调hsp70.1蛋白的表达(*p<0.05)(图2a和2b)。通过上述条件处理hep3b细胞上的hsp70.1进行免疫荧光染色,以另一种方式验证蛋白质表达。结果与蛋白质印迹结果一致(图2c和2d)。定量qrt-pcr结果显示,与对照组相比,dc661显著下调hsp70.1mrna的表达(*p<0.05)(图2e)。此外,蛋白质印迹法检测结果显示,与对照组相比,dc661显著下调p-hsf1(ser326)蛋白的表达(**p<0.01)(图2f和2g)。结果表明,dc661处理通过下调p-hsf1(ser326)蛋白的表达,进一步抑制hsp70.1的蛋白合成。
实施例3、dc661诱导人源肝细胞癌细胞凋亡
使用3μm的dc661来处理人源肝细胞癌细胞系hep3b细胞,于6h进行免疫荧光染色,检测组织蛋白酶b的细胞内分布。免疫荧光结果显示,与对照组相比,dc661处理细胞诱导溶酶体内的组织蛋白酶b释放至胞浆当中(图3a)。通过上述条件处理hep3b细胞,进行jc-1荧光探针染色检测线粒体膜电位。jc-1荧光探针染色结果显示,与对照组相比,dc661处理细胞呈现出红色荧光减弱,绿色荧光增强的趋势,表明线粒体膜电位发生了去极化(图3b)。通过上述条件处理hep3b细胞内的细胞色素c进行免疫荧光染色,结果显示,与对照组相比,dc661处理细胞诱导线粒体内的细胞色素c释放至胞浆当中(图3c)。通过dc661(3μm,6h)处理,使用细胞caspase-3活性检测试剂盒(碧云天,产品编号c1077s)对细胞进行染色,然后进行流式细胞检测。通过流式荧光定量分析显示,与对照细胞相比,dc661处理促进caspase3活化,显示出显著差异(***p<0.001)(图3d和3e)。通过上述条件处理hep3b细胞,annexinv-fitc/pi凋亡试剂盒(博士德生物,产品编号mk1028)对细胞进行染色,然后进行流式细胞检测。通过流式荧光定量分析显示,与对照细胞相比,dc661处理促进肿瘤细胞凋亡,显示出显著差异(**p<0.01)(图3f和3g)。结果表明,dc661处理通过诱导线粒体途径凋亡发挥抗肿瘤作用。
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个……”限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!