长链非编码RNA-NEAT1的应用及过表达RNA-NEAT1的腺相关病毒及应用
长链非编码rna
‑
neat1的应用及过表达rna
‑
neat1的腺相关病毒及应用
技术领域
1.本发明属于医药技术领域,具体涉及长链非编码rna
‑
neat1的应用及过表达rna
‑
neat1的sgrna和腺相关病毒及应用。
背景技术:
2.fuchs’角膜内皮营养不良(fecd),又叫滴状角膜,是一种常见的遗传性角膜内皮变性疾病,主要表现为发生角膜基质和上皮水肿,引起视力显著减退。目前,治疗fuchs’角膜内皮营养不良的临床治疗方案是进行角膜移植手术。尽管角膜移植手术在很大程度上成功治疗了fuchs’角膜内皮营养不良,但仍存在具有侵入性,角膜供体数量不足,价格昂贵等缺点,促使进行其他治疗手段的研发。
技术实现要素:
3.为了解决上述问题,本发明提供了长链非编码rna
‑
neat1的应用及过表达rna
‑
neat1的sgrna和腺相关病毒及应用。本发明在房前进行长链非编码rna
‑
neat1的过表达,对fuchs’角膜内皮营养不良进行治疗,可有效降低解角膜内皮损伤,缓解角膜水肿症状。
4.为了实现上述目的,本发明提供如下技术方案:
5.本发明提供了长链非编码rna
‑
neat1在制备治疗fuchs’角膜内皮营养不良药品中的应用。
6.本发明提供了一种用于过表达长链非编码rna
‑
neat1的sgrna,所述sgrna的核苷酸序列如seq id no:1所示。
7.本发明提供了一种用于过表达长链非编码rna
‑
neat1的腺相关病毒aav9
‑
neat1
‑
sgrna,所述腺相关病毒aav9
‑
neat1
‑
sgrna包括上述技术方案所述的sgrna。
8.优选的,所述腺相关病毒aav9
‑
neat1
‑
sgrna的骨架载体包括gv639。
9.优选的,所述腺相关病毒aav9
‑
neat1
‑
sgrna的包装的滴度为2
×
10
12
~3
×
10
12
v.g./ml。
10.本发明提供了一种治疗fuchs’角膜内皮营养不良的方法,使用上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna进行治疗。
11.优选的,所述腺相关病毒aav9
‑
neat1
‑
sgrna以注射手段注射到前房进行治疗;所述腺相关病毒aav9
‑
neat1
‑
sgrna的注射剂量优选为0.5~2μl。
12.本发明提供了上述技术方案中所述的sgrna或上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna在制备治疗fuchs’角膜内皮营养不良药品中的应用。
13.本发明提供了长链非编码rna
‑
neat1或上述技术方案中所述的sgrna或上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna在制备缓解角膜水肿症状的药品中的应用。
14.本发明提供了长链非编码rna
‑
neat1或上述技术方案中所述的sgrna或上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna在制备缓解角膜内皮细胞氧化损伤的药品中
的应用。
15.有益效果:
16.本发明提供了长链非编码rna
‑
neat1在制备治疗fuchs’角膜内皮营养不良药品中的应用。长链非编码rna
‑
neat1的过表达可有效降低解角膜内皮损伤,缓解角膜水肿症状,可以用于fuchs’角膜内皮营养不良的治疗;而且大大简化了治疗的操作步骤和风险,无需进行角膜移植手术,来源充足,治疗费用低。
附图说明
17.图1为腺相关病毒aav9
‑
neat1
‑
sgrna结构图;
18.图2为不同处理组对小鼠角膜内皮细胞进行zo
‑
1和dapi荧光染色结果图;
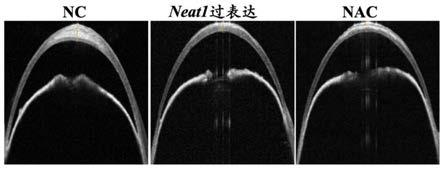
19.图3为不同处理组对小鼠中央角膜厚度的影响;
20.图4为不同处理组小鼠中央角膜厚度随时间的变化图。
具体实施方式
21.本发明提供了长链非编码rna
‑
neat1在制备治疗fuchs’角膜内皮营养不良药品中的应用。本发明通过长链非编码rna
‑
neat1的过表达可有效降低解角膜内皮损伤,缓解角膜水肿症状,可以用于fuchs’角膜内皮营养不良的治疗;而且大大简化了治疗的操作步骤和风险,无需进行角膜移植手术,来源充足,治疗费用低。
22.本发明提供了一种用于过表达长链非编码rna
‑
neat1的sgrna,所述sgrna的核苷酸序列如seq id no:1所示,具体核苷酸序列为aaggatcattgagcaatctga。在本发明中,所述长链非编码rna
‑
neat1是根据neat1设计得到。本发明提供的用于过表达长链非编码rna
‑
neat1的sgrna可以构建具有过表达长链非编码rna
‑
neat1的腺相关病毒载体,行前房注射手段将病毒注入眼部的前房,在前房中进行长链非编码rna
‑
neat1的过表达,对fuchs’角膜内皮营养不良进行治疗。
23.本发明提供了一种过表达长链非编码rna
‑
neat1的腺相关病毒aav9
‑
neat1
‑
sgrna,所述腺相关病毒aav9
‑
neat1
‑
sgrna包括上述技术方案所述的sgrna。本发明以腺病毒为骨架载体,在所述骨架载体插入了上述技术方案中所述的sgrna。在本发明中,所述腺相关病毒aav9
‑
neat1
‑
sgrna的骨架载体优选包括gv639。本发明对插入sgrna的方法没有特殊要求,采用本领域常规技术手段插入即可。本发明优选利用dsacas9系统合成腺相关病毒aav9
‑
neat1
‑
sgrna,合成的腺相关病毒aav9
‑
neat1
‑
sgrna的结构如图1所示。在本发明中,所述腺相关病毒aav9
‑
neat1
‑
sgrna最终包装的滴度优选为2
×
10
12
~3
×
10
12
v.g./ml,进一步优选为3
×
10
12
v.g./ml。本发明通过将上述技术方案中所述的sgrna插入腺病毒载体得到一种用于过表达长链非编码rna
‑
neat1的腺相关病毒aav9
‑
neat1
‑
sgrna,采用前房注射手段将本发明提供的腺相关病毒aav9
‑
neat1
‑
sgrna注入眼部的前房在前房中进行长链非编码rna
‑
neat1的过表达,以达到治疗fuchs’角膜内皮营养不良的目的。本发明对前房注射手段的具体实施方式没有特殊要求,采用本领域技术人员所熟知的即可。本发明提供的腺相关病毒aav9
‑
neat1
‑
sgrna可有效降低解角膜内皮损伤,缓解角膜水肿症状,可以用于fuchs’角膜内皮营养不良的治疗;且操作简单,来源充足,治疗费用低,为fuchs’角膜内皮营养不良的治疗开辟了新途径。
24.本发明提供了上述技术方案中所述的sgrna或上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna在制备治疗fuchs’角膜内皮营养不良药品中的应用。
25.本发明提供了长链非编码rna
‑
neat1或上述技术方案中所述的sgrna或上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna在制备缓解角膜水肿症状的药品中的应用。
26.本发明提供了长链非编码rna
‑
neat1或上述技术方案中所述的sgrna或上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna在制备缓解角膜内皮细胞氧化损伤的药品中的应用。
27.本发明提供了一种治疗fuchs’角膜内皮营养不良的方法,使用上述技术方案中所述的腺相关病毒aav9
‑
neat1
‑
sgrna进行治疗。本发明优选将所述腺相关病毒aav9
‑
neat1
‑
sgrna以注射手段注射到前房进行治疗,所述腺相关病毒aav9
‑
neat1
‑
sgrna的注射剂量优选为0.5~2μl,进一步优选为1μl。本发明提供的治疗fuchs’角膜内皮营养不良的方法只需注射一次即可,大大简化了治疗的操作步骤和风险,且无需进行角膜移植手术,来源充足,治疗费用低,治疗fuchs’角膜内皮营养不良的效果好,可有效降低解角膜内皮损伤,缓解角膜水肿症状。
28.为了进一步说明本发明,下面结合实施例对本发明提供长链非编码rna
‑
neat1的应用及过表达rna
‑
neat1的sgrna和腺相关病毒及应用进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
29.实施例1
30.腺相关病毒aav9
‑
neat1
‑
sgrna构建
31.本发明以长链非编码rna
‑
neat1,设计sgrna,其中长链非编码rna
‑
neat1的id为66961,sgrna的核苷酸序列如seq id no:1所示。将sgrna连入gv639腺病毒载体,将连接好的产物使用top10感受态转化,菌落pcr得到阳性克隆后测序,得到序列正确的表达sgrna的腺相关病毒aav9
‑
neat1
‑
sgrna。其中sgrna由吉凯基因化学技术有限公司合成;gv639腺病毒载体和top10感受态购自吉凯基因化学技术有限公司;菌落pcr引物购自上海捷瑞生物工程有限公司。最终包装得到的腺相关病毒aav9
‑
neat1
‑
sgrna的滴度为2.18
×
10
12
v.g./ml。
32.实施例2
33.对fuchs’角膜内皮营养不良治疗的考察
34.选取8~12周龄的c57bl/6j雌性小鼠(重量20g左右)构建fuchs’角膜内皮营养不良模型,考察对fuchs’角膜内皮营养不良治疗的治疗效果。模型构建的方法参考如下文献:
35.liu et al.,ultraviolet a light induces dna damage and estrogen
‑
dna adducts in fuchs endothelial corneal dystrophy causing females to be more affected.pnas latest articles.,january 7,2020117(1)573
‑
583.
36.本试验将c57bl/6j雌性小鼠随机分成三组,分别为neat1过表达组、nac(n
‑
乙酰
‑
l
‑
半胱氨酸)组和对照组。
37.neat1过表达组:造模前4周,给小鼠前房注射实施例1的腺相关病毒aav9
‑
neat1
‑
sgrna,单只眼的注射量为1μl,注射一次即可,使在前房中进行长链非编码rna
‑
neat1过表达;造模时,将c57bl/6j雌性小鼠安置在一个气候控制动物设施里,在uva循环光照射下保持12h。
38.nac组:c57bl/6j雌性小鼠在进行uva照射前2d开始喂食含有nac的水,每天nac的
摄入量为1g/kg,持续喂水摄入nac 3个月。
39.对照组(nc):造模前4周,给小鼠前房注射对照病毒,对照病毒的制备方法同实施例1的腺相关病毒aav9
‑
neat1
‑
sgrna,不同之处在于,将实施例1的sgrna的核苷酸序列替换为seq id no:3,具体核苷酸序列为caccggagaccacggcaggtctca。注射剂量、注射方法和造模方式与neat1过表达组相同。
40.采用oct对小鼠中央角膜厚度进行追踪,处理结束后,在小鼠腹腔注射氯胺酮(100mg/kg)和甲苯噻嗪(20mg/kg),麻醉小鼠,进行zo
‑
1和dapi染色,zo
‑
1试剂购自invitrogen公司,dapi试剂购自索莱宝公司。检测结果见图2~4。
41.图2为不同处理组对小鼠角膜内皮细胞进行zo
‑
1和dapi荧光染色结果图。由图2的结果可知,neat1过表达组的fecd小鼠角膜内皮比对照组维持了更好的形态。
42.nac(n
‑
乙酰
‑
l
‑
半胱氨酸)作为一种常用的抗氧化剂,在以往研究中可用于通过对小鼠持续喂水摄入nac的方式缓解uva诱导的fecd症状。为了评估neat1过表达组对小鼠角膜内皮fecd症状的改善效果,本发明加入nac组小鼠作为阳性对照。图3为不同处理组对小鼠中央角膜厚度的影响;由图3的结果可知,neat1过表达组的小鼠中央角膜厚度显著低于nc组,且和nac组小鼠的角膜厚度十分接近。
43.图4为不同处理组小鼠中央角膜厚度随时间的变化图。由图4的结果可知,在所有时间点neat1过表达组的小鼠角膜内皮厚度均显著低于nc组,且和nac组十分接近,有效缓解了fecd小鼠角膜水肿症状。
44.以上结果提示过表达neat1组可有效缓解fecd小鼠角膜内皮损伤症状;结合上述提到的小鼠角膜内皮细胞系氧化损伤试验和抗氧化剂nac组小鼠的对比结果,进一步提示neat1很可能通过调控氧化应激反应的途径实现对角膜内皮氧化还原稳态和fecd发病过程的调节,揭示了neat1在角膜内皮中的重要生物学功能及临床应用潜能。
45.尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其它实施例,这些实施例都属于本发明保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1