基于白蛋白和ECOG-PS的原发性中枢神经系统淋巴瘤预后模型建立方法及应用
基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型建立方法及应用
技术领域
1.本发明属于生物医学检测技术领域,具体涉及一种基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型建立方法及应用。
背景技术:
2.原发性中枢神经系统淋巴瘤(primary central nervous system lymphoma,pcnsl)是一种少见的发生在脑、脊髓、脑膜和眼的非霍奇金淋巴瘤,具有较强的侵袭性,并且不伴有其他脏器的受累。然而,营养不良是肿瘤患者的常见合并症,据统计,肿瘤患者营养不良的发生率在40%~80%之间。最近的回顾性研究表明,营养状况可影响接受r
‑
chop方案治疗的dlbcl患者生存。
3.现有技术中,较常用的营养状况测量工具有主观整体营养状况评定量表(subjective global assessment,sga)和专门为患者开发的主观整体营养状况评定量表(patient
‑
generated
‑
subjective global assessment,pg
‑
sga),包括血清白蛋白、前白蛋白和转铁蛋白等实验室检查,肱三头肌皮褶、臂中肌围、体重指数等人体测量指标,以及是否存在水肿和腹水等指标。此外,血清白蛋白作为预后因素之一,参与了与dlbcl相关的临床预后模型构建。格拉斯哥预后评分是结合c
‑
反应蛋白和白蛋白作为预后因素的评分。预后营养指数(是根据血清白蛋白浓度和淋巴细胞绝对数计算:白蛋白(g/l)+5
×
淋巴细胞总数
×
109/l;控制营养状态评分也可作为dlbcl患者独立的预后因素,是根据血清白蛋白、总胆固醇和淋巴细胞计数计算的营养评分系统。
4.申请人研究发现,尽管sga和pg
‑
sga简单实用、价格低廉且无创,但它们是主观评估量表,可能会受观察者和患者的影响。此外,虽然绝大部分pcnsl患者病理分型为dlbcl,但目前并没有针对pcnsl患者的营养相关指标的预后评分,基于营养状态研发专门针对pcnsl患者的预后模型具有重要的临床意义。
技术实现要素:
5.本发明的目的是要解决上述现有模型不一定适用于现在对pcnsl新的临床治疗模式于的技术问题,提供一种基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型建立方法及应用。
6.为了解决上述问题,本发明按以下技术方案予以实现的:
7.第一方面,本发明建立了一种基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型,该模型包括相关的预后因素、根据预后因素不同状态的评估分值对应的风险组以及各风险组对应的预后状态;
8.其中,所述预后因素由血清白蛋白含量和ecog
‑
ps组成。
9.结合第一方面,本发明还提供了第1种优选实施方式,所述预后因素ecog
‑
ps>1或血清白蛋白含量≤4.1g/dl时,每个预后因素赋值1分;
10.当预后因素的ecog
‑
ps≤1且血清白蛋白含量>4.1g/dl,评估分值为0分;
11.当预后因素的ecog
‑
ps≤1且血清白蛋白含量≤4.1g/dl,或者,ecog
‑
ps>1且血清白蛋白含量>4.1/dl,评估分值为1分;
12.当预后因素的ecog
‑
ps>1且血清白蛋白含量≤4.1g/dl,评估分值为2分。
13.结合第一方面,本发明还提供了第2种优选实施方式,所述模型包括低风险组、中风险组和高风险组;
14.所述低风险组对应的评估分值为0分;
15.所述中风险组对应的评估分值为1分;
16.所述高风险组对应的评估分值为2分。
17.结合第一方面,本发明还提供了第3种优选实施方式,所述低风险组的预后状态较好;所述中风险组的预后状态一般;所述高风险组的预后状态较差。
18.第二方面,本发明还提供了一种基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型,该模型如下表所示:
[0019][0020][0021]
第三方面,本发明还提供了一种如第一方面或第二方面所述的基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型的应用,所述基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型用于评价原发性中枢神经系统淋巴瘤患者预后。
[0022]
第四方面,本发明还提供了一种基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型的建立方法,包括以下步骤:
[0023]
收集原发性中枢神经系统淋巴瘤患者的临床数据;
[0024]
以患者总生存期(os)为结局,对所述临床数据进行k
‑
m生存分析,筛选显著影响患者从初诊至死亡或末次随访时间的危险因素;
[0025]
以患者总生存期(os)为结局,将危险因素统一纳入cox风险比例模型进行多因素生存分析,根据多因素分析的结果构建模型;
[0026]
其中,所述模型包括相关的预后因素、根据预后因素不同状态的评估分值对应的风险组以及各风险组对应的预后状态;所述预后因素由血清白蛋白含量和ecog
‑
ps组成。
[0027]
结合第四方面,本发明还提供了第四方面的第1种实施方式,所述预后因素ecog
‑
ps>1或血清白蛋白含量≤4.1g/dl时,每个预后因素赋值1分;
[0028]
当预后因素的ecog
‑
ps≤1且血清白蛋白含量>4.1g/dl,评估分值为0分;
[0029]
当预后因素的ecog
‑
ps≤1且血清白蛋白含量≤4.1g/dl,或者,ecog
‑
ps>1且血清白蛋白含量>4.1/dl,评估分值为1分;
[0030]
当预后因素的ecog
‑
ps>1且血清白蛋白含量≤4.1g/dl,评估分值为2分。
[0031]
结合第四方面,本发明还提供了第四方面的第2种实施方式,所述模型包括低风险组、中风险组和高风险组;
[0032]
所述低风险组对应的评估分值为0分;
[0033]
所述中风险组对应的评估分值为1分;
[0034]
所述高风险组对应的评估分值为2分。
[0035]
结合第四方面,本发明还提供了第四方面的第3种实施方式,选择k
‑
m生存分析结果p<0.05的危险因素纳入多因素生存分析中。
[0036]
与现有技术相比,本发明的有益效果是:
[0037]
本发明首次将血清白蛋白含量和ecog
‑
ps综合作为原发性中枢神经系统淋巴瘤的预后评估指标,建立了一种针对原发性中枢神经系统淋巴瘤患者的新型预后评估模型。通过临床验证,该模型能够有效对原发性中枢神经系统淋巴瘤患者预后进行预测,相比现有评分标准,本发明根据血清白蛋白含量和ecog
‑
ps的综合评分确定患者的风险组,具有较好的临床实用性,便捷、准确、高效评估pcnsl患者临床结局,以此协助临床医生判断患者的临床发展及疾病转归,更有利于医生制定合理的治疗方案以及及时有效的医患沟通。
附图说明
[0038]
下面结合附图对本发明的具体实施方式作进一步详细的说明,其中:
[0039]
图1是血清白蛋白含量的受试者工作特征曲线(roc)及曲线下面积为0.651;
[0040]
图2是mskcc评分3个风险组的os示意图;
[0041]
图3是低白蛋白组和高白蛋白组的os示意图;
[0042]
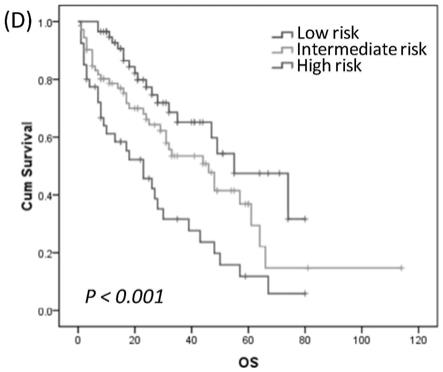
图4是方面模型3个风险组的os示意图。
具体实施方式
[0043]
以下结合附图对本发明的优选实施例进行说明,应当理解,此处所描述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
[0044]
本发明涉及的名词解释:
[0045]
pcnsl(primary central nervous system lymphoma):原发性中枢神经系统淋巴瘤;
[0046]
os(overall survival):总生存期;
[0047]
ecog
‑
ps:体力状况ecog评分标准zubrod
‑
ecog
‑
who(zps,5分法)。
[0048]
本发明所涉及的模型的预测患者os,os定义为从疾病确诊时间到任何原因引起死亡或末次随访时间,os以月为单位计算。
[0049]
本发明实施例提供一种基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型的建立方法,包括以下步骤:
[0050]
(1)收集原发性中枢神经系统淋巴瘤患者的临床数据。
[0051]
在本发明中,pcnsl患者临床数据包括临床资料和实验结果。其中,临床资料包括:性别、年龄、起源细胞类别(根据hans算法的gcb和abc亚型)、b症状、ecog
‑
ps、ldh及治疗方式。所述实验室结果包括:初诊时血常规检查中的血红蛋白,生化检查中的白蛋白、球蛋白和总蛋白水平,agr为白蛋白除以球蛋白比值。
[0052]
在一种优选实施中,对实验室数据中的连续型数据(如白蛋白)采取roc曲线最佳约登值的方法寻找最佳临界点,进行二分类分组;对临床数据中的分类数据均作为分组数据进行处理。需要说明的是,本发明所述的约登值为约登指数,约登指数=灵敏度+特异度
‑
1,约登指数最大时对应的界值距离机会线(y=x)较远,灵敏度和特异度均较高,在本发明中作为筛选血清白蛋白水平的最优界值的根据。
[0053]
(2)以患者总生存期(os)为结局,对所述临床数据进行k
‑
m生存分析,筛选显著影响患者从初诊至死亡或末次随访时间的危险因素。
[0054]
具体的,本发明以患者总生存期(os)为结局,采用kaplan
‑
meier法绘制生存曲线,组间差异采用log
‑
rank进行检验,以p<0.05为差异有统计学意义,对临床资料及炎症相关指标进行危险因素的筛选,筛选得到显著影响患者从初诊至死亡或末次随访时间的危险因素。
[0055]
(3)以患者总生存期(os)为结局,将危险因素统一纳入cox风险比例模型进行多因素生存分析,根据多因素分析的结果构建模型。
[0056]
具体的,本发明将以上有统计学差异的危险因素,以总生存期(os)为结局,统一纳入cox风险比例模型进行多因素生存分析,根据多因素分析的结果,构建模型。
[0057]
本发明所述的模型包括相关的预后因素、根据预后因素不同状态的评估分值对应的风险组以及各风险组对应的预后状态;其中,所述预后因素由血清白蛋白含量和ecog
‑
ps组成。
[0058]
需要说明的是,本发明首次将血清白蛋白含量和ecog
‑
ps综合作为原发性中枢神经系统淋巴瘤的预后评估指标,建立了一种针对原发性中枢神经系统淋巴瘤患者的新型预后评估模型。且本发明获得pcnsl新的独立预后因素—白蛋白,它是临床常规检测指标,成本低、重复性好;而肿瘤患者在接受治疗前均需评估ecog
‑
ps评分,因此,双因素模型具有较好的临床实用性,便捷、准确、高效评估pcnsl患者临床结局。
[0059]
在本发明的研究试验过程中,申请人收集了患者的临床资料包括性别、年龄、起源细胞类别(根据hans算法的gcb和abc亚型)、b症状(其中包括不明原因发热38℃以上、盗汗及6个月内体重下降大于10%)、ecog
‑
ps和ldh;实验室结果包括初诊时血常规检查中的血红蛋白,生化检查中的白蛋白、球蛋白、总蛋白及白蛋白比球蛋白比值。
[0060]
经过对上述临床资料进行单因素分析,结果显示:年龄>60岁、ecog
‑
ps>1、mskcc评分高风险组、单纯放疗是潜在的不良预后因素;治疗前总蛋白水平>7.0g/dl,治疗前白蛋白水平>4.1g/dl、治疗前血红蛋白水平>14.25g/dl和agr>1.5与较好的os显著相关。
[0061]
为此,申请人将以上因素指标统一纳入cox风险比例模型中与os进行多因素生存分析。统计结果显示:白蛋白与其他指标相比,是预测os的最有效的指标(p<0.001)。另一方面,申请人还研究发现,多因素分析的结果提示ecog
‑
ps>1几乎与不良预后显著相关(p=0.051)。经统计学分析提示白蛋白是独立预后指标,而用ecog作为预后模型参数之一的
原因有:
①
cox风险比例模型默认设置纳入标准为0.05,剔除标准为0.1,因为属于探索性研究,p<0.1是为了尽可能不漏掉调节性的协变量;
②
pcnsl的两个常用预后模型ielsg和mskcc都包含体力状况评分,基于这点我们也考虑用ecog和alb一起建立双因素三分类危险组的模型。
[0062]
具体的,所述模型包括所述模型包括低风险组、中风险组和高风险组;所述低风险组对应的评估分值为0分;所述中风险组对应的评估分值为1分;所述高风险组对应的评估分值为2分。所述低风险组的预后状态较好;所述中风险组的预后状态一般;所述高风险组的预后状态较差。
[0063]
具体的,所述预后因素ecog
‑
ps>1或血清白蛋白含量≤4.1g/dl时,每个预后因素赋值1分;
[0064]
当预后因素的ecog
‑
ps≤1且血清白蛋白含量>4.1g/dl,评估分值为0分;
[0065]
当预后因素的ecog
‑
ps≤1且血清白蛋白含量≤4.1g/dl,或者,ecog
‑
ps>1且血清白蛋白含量>4.1/dl,评估分值为1分;
[0066]
当预后因素的ecog
‑
ps>1且血清白蛋白含量≤4.1g/dl,评估分值为2分。
[0067]
本发明的基于白蛋白和ecog
‑
ps的原发性中枢神经系统淋巴瘤预后模型,该模型如下表所示:
[0068][0069]
在本发明的又一具体实施方式中,使用受试者工作特征曲线(roc)判断模型的区分度;我们的模型曲线下面积为0.669,表示预测模型的存在良好的区分度。
[0070]
在一种实施中,所述血清白蛋白含量的临界值通过以下方法得到:
[0071]
在本发明的研究过程中,使用os作为研究终点,并通过roc曲线来计算白蛋白的最佳临界值。白蛋白的roc曲线下面积为0.651,最大联合灵敏度和特异度相对应的最佳临界值为4.1g/dl。
[0072]
进一步的,对模型进行生存分析,根据生存分析表里的当前累及生存分析比例,得到5年生存率;根据生存分析时间的中位数表格里,得到这部分患者的中位生存期,如下表所示:
[0073]
风险组患者,n中位生存期5年生存率
低风险组58(34%)55个月47.5%中风险组72(42%)46个月36.9%高风险组40(24%)23个月11.9%
[0074]
模型校验
[0075]
病例背景:pcnsl是经病理证实的中枢神经系统原发性淋巴瘤,发生于脑、软脑膜、脊髓和眼睛,无全身受累,是一种高度侵袭性、罕见的结外非霍奇金淋巴瘤,占中枢神经系统肿瘤的4%,预后较差,中位生存期为36.9到46个月,5年生存率为22.3%~32%。
[0076]
收集初诊pcnsl患者治疗前血清白蛋白水平,评估患者ecog评分等资料。根据本发明模型的预后因素:血清白蛋白含量和ecog
‑
ps确定患者的风险组。
[0077]
患者治疗期间通过电话进行随访,随访截止日期为2020年3月3日。至随访截止日期未出现死亡的,以末次随访日期为截尾数值进行分析。死亡日期是从临床病历记载、死亡登记或通过打电话给患者亲属随访获得。os以月为单位计算,定义为从疾病确诊时间到任何原因引起死亡或末次随访时间。
[0078]
①
男性患者,66岁,ecog
‑
ps=3,血清白蛋白含量=3.96g/dl。根据本发明的模型确定患者为高风险组。结果显示:截止末次随访日期2020年3月3日,患者已经死亡,总生存期为8个月,远低于pcnsl患者的中位生存期,预后较差。
[0079]
②
男性患者,48岁,ecog
‑
ps=1,血清白蛋白含量=4.70g/dl。根据本发明的模型确定患者为低风险组。结果显示:截止末次随访日期2020年3月3日,患者存活,总生存期为74个月,高于pcnsl患者的中位生存期,预后较好。
[0080]
③
女性患者,74岁,ecog
‑
ps=1,血清白蛋白含量=4.20g/dl。根据本发明的模型确定患者为低风险组。结果显示:截止末次随访日期2020年3月3日,患者存活,总生存期为64个月,高于pcnsl患者的中位生存期,预后较好。
[0081]
④
男性患者,57岁,ecog
‑
ps=2,血清白蛋白含量=4.50g/dl。根据本发明的模型确定患者为中风险组。结果显示:截止末次随访日期2020年3月3日,患者存活,总生存期为41个月。
[0082]
通过临床验证,该模型能够有效对原发性中枢神经系统淋巴瘤患者预后进行预测,相比现有评分标准,本发明根据ecog
‑
ps和血清白蛋白水平确定患者的风险组,以此协助临床医生判断患者的临床发展及疾病转归,实现精准分层治疗,更有利于医生制定合理的治疗方案以及及时有效的医患沟通。
[0083]
以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,故凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何修改、等同变化与修饰,均仍属于本发明技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1