抗体和蛋白质制剂的制作方法
抗体和蛋白质制剂
1.本技术是申请日2013年8月28日,申请号201380051319.0,发明名称“抗体和蛋白质制剂”的中国发明专利申请的分案申请。本技术于2013年8月28日作为pct国际专利申请提交,并且要求于2012年8月31日提交的美国专利申请号13/601,598和于2013年3月15日提交的美国专利申请号13/843,780的优先权,所述美国专利申请的公开内容在此通过引用全文并入本文。
背景技术:
本公开内容一般涉及等渗且具有低粘度的抗体及其他蛋白质制剂,包括用于注射和一般施用的制剂。
3.血友病患者患有出血障碍,这导致在损伤或手术后延迟的血液凝固。延长出血由一种或多种血液凝固因子中的遗传缺陷引起。两类常见的血友病是已知的
‑‑
血友病a和血友病b。血友病a由因子viii中的缺陷引起,而血友病b由因子ix中的缺陷引起。总血友病患者中的约75-80%患有血友病a。
4.组织因子途径抑制剂(tfpi)是血液凝固的外源性途径的人抑制剂并在抗凝中起效。针对tfpi的抗体包括抗tfpi单克隆抗体(atfpi mab)在阻断tfpi功能的努力中得到开发。一种此类atfpi mab是人igg2抗tfpi mab,其开发用于治疗血友病a和b患者。
5.抗体及其他蛋白质可以经由静脉内、肌内和/或皮下注射施用于患者。为了确保患者依从性,希望皮下注射剂型是等渗的且包括小注射体积(《2.0ml/注射部位)。为了降低注射体积,蛋白质通常在1mg/ml-150mg/ml的范围内施用。
6.虽然液体和冻干剂型两者均用于目前销售的基于抗体及其他蛋白质的药物产品,但冻干形式更频繁用于具有高蛋白质浓度的蛋白质和抗体药物产品。
7.蛋白质和抗体剂型可以呈现制剂开发中的许多挑战,尤其是对于液体制剂。对于其中蛋白质浓度接近其表观溶解度限制的制剂,相分离可以通过沉淀、胶凝和/或结晶而发生。在高蛋白质浓度时,由于可溶性和不溶性蛋白质-蛋白质聚集体的形成,抗体或其他蛋白质的稳定性可以变得成问题。高度浓缩的蛋白质制剂通常是高度粘稠的,这呈现加工例如超滤和无菌过滤以及剂量溶液注射的困难。并且在对于预期用于肌内或皮下施用的制剂希望的蛋白质浓度时,需要高浓度的稳定剂例如蔗糖和氯化钠,以实现长期蛋白质稳定性。所得到的高渗溶液通常由于组织损害而引起注射疼痛。因此,对于高蛋白质浓度制剂的稳定性和渗透压摩尔浓度平衡稳定剂的量是关键的。
8.出于这些原因,本领域存在对以液体形式的基于抗体及其他蛋白质的治疗制剂的需要,所述治疗制剂显示出高蛋白质浓度,而无显著增加的蛋白质聚集、渗透压摩尔浓度或粘度和/或蛋白质稳定性减少的问题。因此,希望基于抗体及其他蛋白质的制剂含有有限量的赋形剂和小体积以便于治疗施用或递送。进一步希望基于抗体及其他蛋白质的治疗制剂可顺应于冻干,以增强在延长贮存条件下的蛋白质稳定性。
技术实现要素:
本公开内容提供了液体和冻干的基于抗体和蛋白质的制剂,其基本上是等渗和低粘度的,并且基本上不含无机盐。本文呈现的抗体及其他蛋白质制剂在约ph 4.0-约ph 6.0的ph下含有约0mm-约30mm组氨酸;约50ppm-约200ppm非离子型表面活性剂例如聚山梨酯80或聚山梨酯20;约88mm-约292mm糖或糖醇例如甘露糖醇、右旋糖、葡萄糖、海藻糖和/或蔗糖;约0mm-约50mm精氨酸;约0mm-约50mm赖氨酸;约0mm-约133mm甘氨酸或丙氨酸;约0mm-约10mm甲硫氨酸;和约1mg/ml-约150mg/ml的蛋白质。本文公开的制剂显示出范围为在22℃下约1mpa-s-约20mpa-s,或在22℃下约1mpa-s-约15mpa-s,或在22℃下约1mpa-s-约10mpa-s,或在22℃下约1mpa-s-约8mpa-s或在22℃下约1mpa-s-约6mpa-s的粘度和范围为约240-约380mmol/kg的渗透压摩尔浓度。
10.在进一步方面内,本公开内容提供了用于治疗患者中的病症的方法,其包括给患者施用治疗有效量的本文描述的一种或多种制剂。例如,提供的是用于治疗患者中的病症的方法,其包括给患者施用治疗有效量的如本文更详细地描述的抗体或其他蛋白质制剂。
11.本文教导的这些及其他特点在本文中阐述。
附图说明
技术人员应当理解下文描述的附图仅用于举例说明目的。附图不预期以任何方式限制本文教导的范围。
13.图1是显示氯化钠(nacl)浓度对20mg/ml以ph 5.5的抗tfpi mab制剂的浊度的作用的图示。
14.图2是显示ph对抗tfpi mab药品的浊度的作用的图示。
具体实施方式
如上所述,本公开内容提供了抗体及其他蛋白质制剂,其在预期贮存条件下以液体形式或冻干形式稳定抗体或其他蛋白质。本文描述的制剂包括一种或多种药学上可接受的赋形剂或稳定剂,并且包含在以合适ph的缓冲介质中,并且与生理溶液基本上等渗。对于全身施用,注射是一种施用途径,包括肌内、静脉内、腹膜内和皮下注射。
16.由于其低粘度,本文公开的蛋白质制剂可以方便地经由例如超滤和无菌过滤进行加工,并且可以经由注射包括皮下注射施用于患者。此外,因为它们基本上是等渗的,所以本文公开的抗体和蛋白质制剂降低组织损害或其他不利生理效应,并且从而实现有利的患者耐受和增加的患者依从性。
17.本文描述的制剂的特征在于基本上不存在添加的盐,其提供增加其他稳定剂例如蔗糖的浓度的灵活性,同时维持制剂的渗透压摩尔浓度用于改善的体内耐受性和因而增加的患者依从性。此外,本文描述的制剂的低粘度允许方便加工,包括但不限于超滤和无菌过滤,和通过针注射药物产品溶液。
18.如本文使用的,术语“粘度”指例如当在施用于患者期间通过注射针注射时,液体制剂对流动的抗性。粘度测量可以通过锥板技术用在限定温度例如如本文描述的22℃下设定的珀尔帖元件(peltier element)完成。通常,将明确限定的剪切应力梯度应用于液体制剂,并测量所得到的剪切速率。粘度是剪切应力与剪切速率的比。如本文使用的,粘度以在
22℃下的mpa-s单位表示,其中1mpa-s=1cp。本文公开的低粘度、基本上等渗的制剂通常特征在于具有范围为在22℃下约1mpa-s-约20mpa-s,或在22℃下约1mpa-s-约15mpa-s,或在22℃下约1mpa-s-约10mpa-s,或在22℃下约1mpa-s-约8mpa-s或在22℃下约1mpa-s-约6mpa-s的粘度。
19.如本文使用的,术语“渗透压摩尔浓度”指定义为每kg溶液的溶质mmole数的溶质浓度量度。所需渗透压摩尔浓度水平可以通过添加一种或多种稳定剂来实现,所述稳定剂例如糖或糖醇,包括但不限于甘露糖醇、右旋糖、葡萄糖、海藻糖和/或蔗糖。适合于提供渗透压摩尔浓度的另外稳定剂在参考文献例如pharmaceutical excipients(第四版,royal pharmaceutical society of great britain,science&practice publishers)或remingtons:the science and practice of pharmacy(第十九版,mack publishing company)的手册中描述。
20.如本文使用的,术语“约”指提供的单位值的+/-10%。如本文使用的,术语“基本上”指显示出总计或近似程度的目的特征或特性的定性状况。生物学领域的普通技术人员应当理解生物学和化学现象很少(如果有的话)实现或避免绝对结果。术语基本上因此在本文中用于捕获许多生物学和化学现象中固有的完全性的潜在缺乏。如本文使用的,术语“等渗的”和“等张的”可与术语“基本上等渗的”和“基本上等张的”互换使用,并且指特征在于具有的渗透压与另一种溶液的渗透压相同或至少基本上相等的制剂,这通过其中制剂中的溶质包括可渗透和不可渗透的溶质两者的总浓度与另一种溶液中的溶质总数目相同或至少基本上相等的制剂来实现。因此,虽然本领域技术人员应当理解用于体内施用的“等渗”和“等张”制剂一般具有范围为约270mmol/kg-约310mmol/kg的渗透压摩尔浓度,但在本公开内容的低粘度制剂的背景下,术语“等渗的”、“等张的”、“基本上等渗的”和“基本上等张的”可互换使用,以指具有范围为约240mmol/kg-约380mmol/kg、或约270mmol/kg-约370mmol/kg、或约300mmol/kg-约330mmol/kg的渗透压摩尔浓度的制剂。
21.本文公开的低粘度、基本上等渗的抗体及其他蛋白质制剂在约ph 4-约ph 6的ph下含有约0mm-约30mm组氨酸;约50ppm-约200ppm非离子型表面活性剂例如聚山梨酯80或聚山梨酯20;约88mm-约292mm糖或糖醇例如甘露糖醇、右旋糖、葡萄糖、海藻糖和/或蔗糖;约0mm-约50mm精氨酸;约0mm-约50mm赖氨酸;约0mm-约133mm甘氨酸或丙氨酸;约0mm-约10mm甲硫氨酸;和约1mg/ml-约150mg/ml的蛋白质。本文公开的制剂显示出范围为在22℃下约1mpa-s-约20mpa-s,或在22℃下约1mpa-s-约15mpa-s,或在22℃下约1mpa-s-约10mpa-s,或在22℃下约1mpa-s-约8mpa-s或在22℃下约1mpa-s-约6mpa-s的粘度和范围为约240-约380mmol/kg的渗透压摩尔浓度。
22.在这些制剂中,组氨酸是缓冲剂,其可以用于将制剂ph维持在约ph 4-约ph 6.0、或约ph 5-约ph 6,例如约ph 5、约ph 5.5或约ph 6。糖或糖醇例如甘露糖醇、右旋糖、葡萄糖、海藻糖和/或蔗糖分开或组合使用,作为液体制剂中抗体的以及在冻干期间和之后的冷冻保护剂和稳定剂。非离子型表面活性剂例如聚山梨酯,包括聚山梨酯20和聚山梨酯80;泊洛沙姆(polyoxamer),包括泊洛沙姆184和188;多元醇;及其他乙烯/聚丙烯嵌段聚合物,通过降低界面相互作用且阻止蛋白质吸附而在加工和贮存期间稳定抗体。精氨酸是蛋白质增溶剂以及稳定剂,其降低抗体及其他蛋白质聚集,例如atfpi mab聚集,和糖化。甲硫氨酸是阻止在加工和贮存期间的抗体氧化的抗氧化剂。
23.糖和无机盐通常用作蛋白质稳定剂;然而,糖和无机盐两者也是有效的张度剂。如果制剂需要高浓度的一种或多种糖来稳定蛋白质,则无机盐浓度应为零或保持极低,以便维持制剂的渗透压摩尔浓度,使得注射疼痛在施用时降低。非常令人惊讶的是,发现氯化钠增加抗体制剂的浊度。因而,无机盐基本上排除加入本文描述的制剂。这些无盐制剂维持抗体及其他蛋白质制剂的渗透压摩尔浓度伴随增加的稳定性,以及降低的相变化例如沉淀或聚集。
24.如本文使用的,术语“盐”指无机盐,其包括但不限于氯化钠(nacl)、硫酸钠(na2so4)、硫氰酸钠(nascn)、氯化镁(mgcl)、硫酸镁(mgso4)、硫氰酸铵(nh4scn)、硫酸铵((nh4)2so4)、氯化铵(nh4cl)、氯化钙(cacl2)、硫酸钙(caso4)、氯化锌(zncl2)等等或其组合。本文公开的抗体及其他蛋白质制剂的特征在于基本上不存在添加的盐,并且因此在本文中被称为无盐抗体和/或蛋白质制剂。本领域技术人员应当理解通过ph调整引入的无机盐在本文公开的制剂中的存在不视为添加的盐,并且如果存在于根据本公开内容的制剂中,则此类无机盐不应超过约2mm的浓度。
25.如本文使用的,术语“表面活性剂”包括非离子型表面活性剂,包括但不限于聚山梨酯例如聚山梨酯20或80、和泊洛沙姆例如泊洛沙姆184或188、多元醇及其他乙烯/聚丙烯嵌段聚合物。有效提供稳定的抗体及其他蛋白质制剂的表面活性剂的量通常在50ppm-200ppm的范围内。非离子型表面活性剂的使用允许制剂暴露于剪切和表面应力,而不引起抗体或其他蛋白质的变性,并且还降低在加工和贮存期间在表面上的吸附。本文公开的制剂包括但不限于具有一种或多种非离子型表面活性剂的制剂,所述非离子型表面活性剂包括例如一种或多种聚山梨酯,例如聚山梨酯20或80;一种或多种泊洛沙姆,例如泊洛沙姆184或188;一种或多种多元醇;和/或一种或多种乙烯/聚丙烯嵌段聚合物。本文例示的是具有聚山梨酯,例如聚山梨酯20(20)或聚山梨酯80(80)的制剂。
26.如本文使用的,术语“蛋白质”指含有通过肽键共价连接的至少5个组成氨基酸的氨基酸聚合物。组成氨基酸可以来自由遗传编码所编码的氨基酸的组,其包括:丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸、色氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、甘氨酸、脯氨酸、精氨酸、组氨酸、赖氨酸、天冬氨酸和谷氨酸。如本文使用的,术语“蛋白质”与相关术语“肽”和“多肽”同义。
27.如本文使用的,术语“抗体”指一般称为免疫球蛋白的一类蛋白质。抗体包括全长单克隆抗体(mab),例如igg2单克隆抗体,其包括免疫球蛋白fc区。术语抗体还包括双特异性抗体,双体(diabodies),单链分子和抗体片段例如fab、f(ab')2和fv。
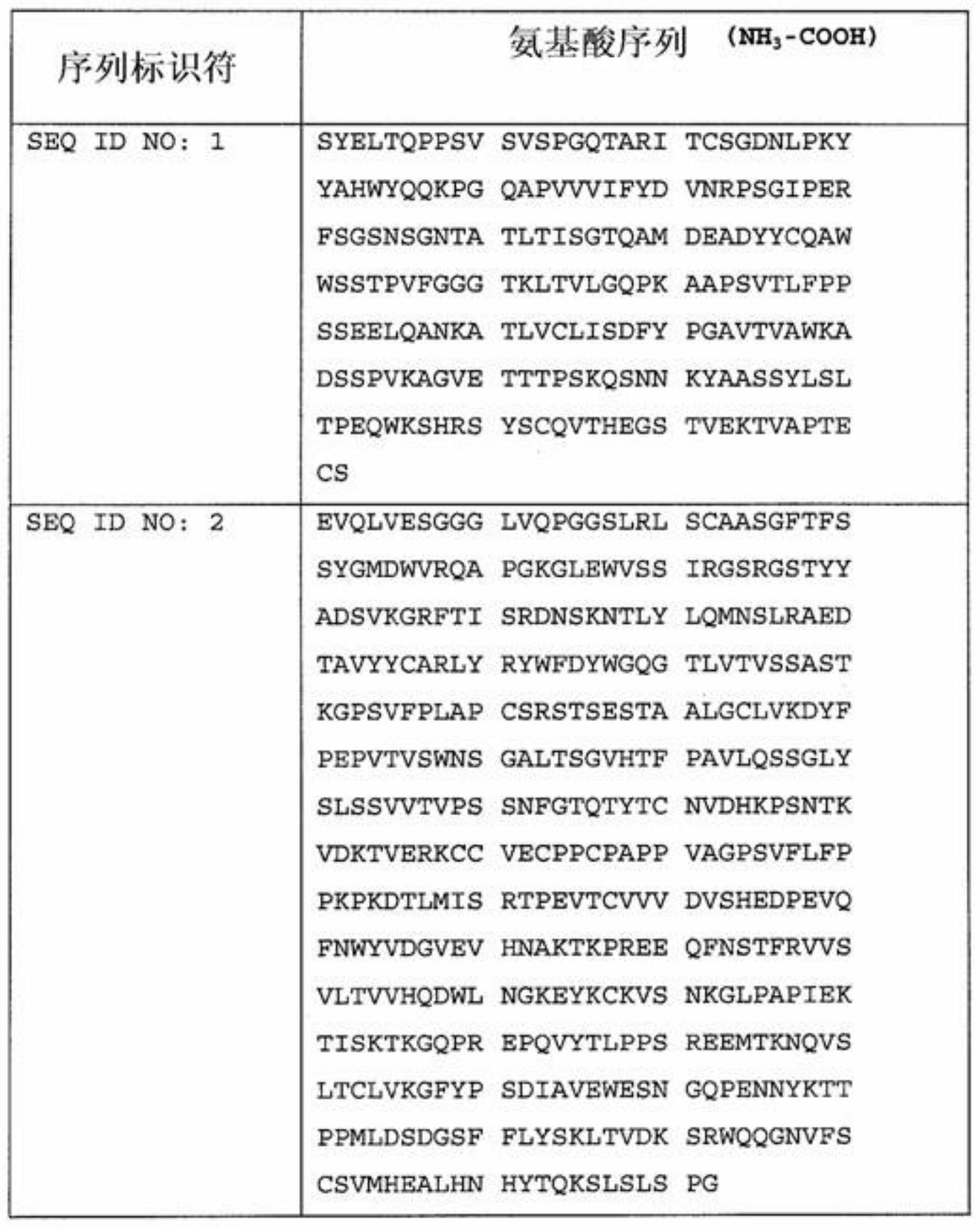
28.如本文使用的,术语“抗tfpi抗体”指具有针对人tfpi蛋白质以及人tfpi蛋白质的片段和变体的结合特异性的抗体。本文呈现的抗tfpi抗体可以是igg2抗体,并且包括抗tfpi igg2单克隆抗体,例如嵌合、人源化和全人抗tfpi igg2单克隆抗体。抗tfpi抗体在本公开内容中通过人抗tfpi igg2单克隆抗体例示,所述人抗tfpi igg2单克隆抗体具有包含本文呈现为seq id no:1的序列的轻链和/或本文呈现为seq id no:2的重链。其他抗tfpi单克隆抗体包括全长抗体及其抗原结合片段和变体(其也适用于本文公开的制剂)呈现于pct专利公开号wo 2011/109452和wo 2010/017196中,所述两个pct专利公开均通过引用全文并入本文。
[0029]“单克隆抗体”的特征在于具有对于单个抗原决定簇的特异性。单克隆抗体可以例如通过由kohler和milstein,nature256:495(1975)描述的杂交瘤方法或通过重组dna方法例如美国专利号4,816,567中所述的那些进行制备。使用诸如clackson等人,nature352:624-628(1991)和marks等人,j.mol.biol.222:581-597(1991)中所述那些的技术,还可以从噬菌体展示文库中分离单克隆抗体。
[0030]
单克隆抗体包括“嵌合单克隆抗体”,其中重和/或轻链的一部分包括来自来源于一个物种的抗体的序列,而抗体的剩余部分(包括fc区)包括来自来源于第二个物种的抗体的序列,通常第二个物种为人。参见例如美国专利号4,816,567和morrison等人,proc.natl.acad.sci.usa81:6851-6855(1984)。
[0031]
单克隆抗体还包括“人源化单克隆抗体”,其中来自来源于一个物种的抗体的重和/或轻链序列的一个或多个互补决定区(cdr)替换来自来源于第二个物种的抗体的重和/或轻链序列的一个或多个cdr,通常第二个物种为人。“人源化”过程通常应用于开发用于施用于人的单克隆抗体。参见例如riechmann等人,nature332(6162):323-27(1988)和queen等人,proc.natl.acad.sci.usa 86(24):10029-33(1989)。
[0032]
单克隆抗体还包括“全人单克隆抗体”,其中整个重和轻链序列来源于人抗体序列。全人单克隆抗体可以通过噬菌体展示技术生成,并且可以从小鼠中分离,所述小鼠已遗传改造为表达人抗体谱(antibody repertoire)。参见例如mccafferty等人,nature348(6301):552-554(1990),marks等人,j.mol.biol.222(3):581-597(1991),以及carmen和jermutus,brief funct.genomic proteomic1(2):189-203(2002)。
[0033]
如本文使用的,术语抗体或其他蛋白质制剂的“药学有效量”指在施用方案中提供疗效的制剂量。本文公开的抗体和蛋白质制剂通常包括浓度范围为下述的抗体或其他蛋白质:约1mg/ml-约150mg/ml、或约1mg/ml-约100mg/ml、或约1mg/ml-约50mg/ml、或约1mg/ml-约20mg/ml、或约1mg/ml-约10mg/ml、或约10mg/ml-约20mg/ml、或约20mg/ml-约150mg/ml、或约50mg/ml-约150mg/ml、或约60mg/ml-约150mg/ml、或约70mg/ml-约150mg/ml、或约80mg/ml-约150mg/ml、或约90mg/ml-约150mg/ml、或约100mg/ml-约150mg/ml、或约120mg/ml-约150mg/ml、或约140mg/ml-约150mg/ml。在一些方面内,在这些制剂内的蛋白质或抗体浓度为约150mg/ml。当皮下施用时,此类制剂通常以小于约2.0ml、或约1.5ml、或约1ml、或约0.5ml/注射部位的体积施用。
[0034]
在某些方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约30mm组氨酸、约100ppm tween 80、约292mm蔗糖、约20mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约30mm-约50mm精氨酸。
[0035]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 80、约234mm蔗糖、约50mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约30mm-约50mm精氨酸。
[0036]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 80、约234mm蔗糖、约100mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约30mm-约50mm精氨酸。
[0037]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 80、约88mm蔗糖、约133mm甘氨酸、约100mg/ml的抗体或其他
蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约30mm-约50mm精氨酸。
[0038]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 20、约88mm蔗糖、约133mm甘氨酸、约100mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约30mm-约50mm精氨酸。
[0039]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约200ppm tween 20、约88mm蔗糖、约133mm甘氨酸、约100mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约30mm-约50mm精氨酸。
[0040]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 80、约88mm蔗糖、约100mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约10mm-约50mm精氨酸。
[0041]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 80、约88mm蔗糖、约133mm甘氨酸、约10mm精氨酸、约100mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约0mm-约10mm甲硫氨酸。
[0042]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm tween 80、约88mm蔗糖、约133mm甘氨酸、约30mm赖氨酸、约100mg/ml的抗体或其他蛋白质。
[0043]
在其他方面内,抗体或其他蛋白质制剂在范围为约ph 5.0-约ph 6.0的ph下含有约10mm组氨酸、约75ppm约tween 80、约234mm蔗糖、约30mm精氨酸、约100mg/ml的抗体或其他蛋白质。在相关方面内,抗体及其他蛋白质制剂还含有约0mm-10mm甲硫氨酸。
[0044]
本文例示的是抗体制剂,其中所述抗体包括igg2抗体,例如抗组织因子途径抑制剂抗体(atfpi ab),包括具有包含seq id no:1的序列的轻链和包含seq id no:2的序列的重链的人igg2单克隆抗体。
[0045]
因此,本公开内容提供了抗tfpi mab制剂,包括抗tfpi igg
2 mab制剂,其中抗tfpi mab在高蛋白质浓度下是可溶的。通常,本文公开的制剂中的抗tfpi mab在约1mg/ml-约150mg/ml的浓度下保持可溶,并且在等渗贮存条件下保持稳定,并且与目前可用的抗体制剂相比较,显示出降低的粘度。
[0046]
具有包含seq id no:1的序列的轻链和包含seq id no:2的序列的重链的抗tfpi抗体是阻断组织因子途径抑制剂(tfpi)的igg2抗体。因为tfpi下调外源性凝血,所以抗tfpi抗体可以通过阻断tfpi来促进外源性途径驱动的凝血,从而绕过内源性途径中的fviii或fix缺陷用于血友病治疗。本文呈现的无盐抗tfpi抗体制剂可以经由皮下注射或其他注射途径施用于患者。
[0047]
作为本公开内容的一部分,发现抗tfpi抗体的可溶性和稳定性受赋形剂影响。抗tfpi抗体的可溶性随着nacl浓度减少而增加。在不存在nacl的情况下,抗tfpi抗体的可溶性高于包括nacl的制剂。另外,发现带正电的氨基酸例如精氨酸和赖氨酸可以改善抗tfpi抗体的稳定性,并且ph极大影响抗tfpi抗体可溶性。抗体溶液的浊度随着ph中的增加而增加;然而,当ph降低时,沉淀是可逆的。用于稳定本文呈现的抗tfpi抗体的最佳ph范围为约ph 4-约ph 6或约ph 5-约ph 6,例如约ph 5、约ph 5.5或约ph 6。
[0048]
本文例示的是如上所述的制剂,其中所述抗体是抗tfpi抗体(atfpi ab)。在至少
一个方面,抗tfpi抗体是人igg2单克隆抗体。例如,人抗tfp1 igg2单克隆抗体包括含有具有seq id no:1中呈现的氨基酸序列的轻链和具有seq id no:2中呈现的氨基酸序列的重链的抗体。示例性人抗tfpi igg2单克隆抗体的重和轻链序列
[0049]
本公开内容还提供了用于治疗患者中的病症的方法,其包括给患者施用治疗有效量的本文描述的一种或多种制剂。例如,提供的是用于治疗患者中的病症的方法,其包括给患者施用治疗有效量的抗体或其他蛋白质制剂,其在范围为约ph 4.0-约ph 6.0的ph下含有约0mm-约30mm组氨酸,和约50ppm-约200ppm聚山梨酯80或聚山梨酯20,约88mm-约292mm蔗糖,约0mm-约50mm精氨酸,约0mm-约50mm赖氨酸,约0mm-约133mm甘氨酸或丙氨酸,约0mm-约10mm甲硫氨酸,和约1mg/ml-约150mg/ml的蛋白质。在这些方法的至少一个方面内,抗体或其他蛋白质制剂可以静脉内施用。在这些方法的其他方
面内,抗体或其他蛋白质制剂可以皮下施用。在这些方法的其他方面内,抗体或其他蛋白质制剂可以肌内施用。
[0050]
在相关方面内,本公开内容提供了用于治疗患者中的血友病a或血友病b的方法,其包括给患者施用治疗有效量的抗tfpi抗体制剂,其在范围为约ph 4.0-约ph 6.0的ph下含有约0mm-约30mm组氨酸,和约50ppm-约200ppm聚山梨酯80或聚山梨酯20,约88mm-约292mm蔗糖,约0mm-约50mm精氨酸,约0mm-约50mm赖氨酸,约0%(0mm)-约1%(133mm)甘氨酸,约0mm-约10mm甲硫氨酸,和约1mg/ml-约150mg/ml的蛋白质。在这些方法的至少一个方面内,抗tfpi抗体制剂可以静脉内施用。在这些方法的其他方面内,抗tfpi抗体制剂可以皮下施用。在这些方法的其他方面内,抗体或其他蛋白质制剂可以肌内施用。
[0051]
根据用于治疗患者中的血友病a或血友病b的这些方法的某些方面,抗tfpi抗体是人抗tfpi igg2单克隆抗体,例如,含有具有seq id no:1中呈现的氨基酸序列的轻链和具有seq id no:2中呈现的氨基酸序列的重链的人抗tfpi igg2单克隆抗体。
[0052]
为了解释本说明书的目的,应用下述定义,并且适当时,以单数使用的术语还包括复数,并且反之亦然。在下文阐述的任何定义与该词语在任何其他文件(包括通过引用并入本文的任何文件)中的使用冲突的情况下,为了解释本说明书及其相关权利要求的目的,应始终以下文阐述的定义为准,除非明确指出相反的含义(例如在其中术语最初使用的文件中)。术语“或”意指“和/或”,除非另有说明。术语“一个/种”在本文中意指“一个或多个/一种或多种”,除非另有说明,或其中“一个或多个/一种或多种”的使用显然不合适。“包含(comprise)”、“包含(comprises)”、“包含(comprising)”、“包括(include)”、“包括(includes)”和“包括(including)”的使用是可互换使用的,并且不旨在是限制性的。此外,当一个或多个实施方案的描述使用术语“包含”时,本领域技术人员应当理解在一些具体情况下,一个或多个实施方案可以可替代地使用语言“基本上由
……
组成”和/或“由
……
组成”描述。
[0053]
本公开内容的方面可以进一步根据下述实施例加以理解,所述实施例不应解释为以任何方式限制本文教导的范围。实施例
[0054]
实施例1nacl浓度和ph对抗体溶液的浊度的作用该实施例公开了盐(nacl)浓度和ph对含有抗tfpi人单克隆抗体的溶液的浊度的作用,所述抗tfpi人单克隆抗体具有含有seq id no:1中呈现的氨基酸序列的轻链和含有seq id no:2中呈现的氨基酸序列的重链。
[0055]
溶液的浊度通过散射比浊法(nephelometry)进行测量,以快速评估盐浓度和ph对atfpi ab溶液的作用。在该实施例中使用的抗tfpi抗体的制剂含有10mm乙酸盐缓冲液、88mm蔗糖和200ppm tween 80。nacl浓度从0mm到30mm变化。关于以ph 5.5的抗tfpi制剂的nacl依赖性浊度测量的结果呈现于图1中。这些数据证实抗tfpi mab制剂的浊度随着nacl浓度增加而显著增加。使盐浓度从0增加到300mm导致通过散射比浊法在浊度值中的72fnu的增加,这可以归因于atfpi ab在溶液中的沉淀、聚集或不溶解。由于该发现,不含氯化钠的溶液推荐用于本文公开的抗tfpi抗体制剂。
[0056]
不受理论束缚,认为随着nacl浓度增加而增加的抗tfpi mab制剂浊度产生于抗tfpi mab精氨酸侧链上的正电荷的中和。伴随单价盐(nacl)的影响,在不同ph下的atfpi mab的相行为解释了为何可以实现稳定、可溶、无盐和基本同渗透压摩尔浓度(isosmolality)的atfpi mab制剂。
[0057]
本文公开的atfpi mab分子具有116个氨基酸(42个精氨酸和74个赖氨酸),所述氨基酸具有在低于pi的ph下携带正电荷的侧链。该抗tfpi抗体具有以~7.9的pi。在低于pi的ph下,例如ph 4-6,该抗tfpi抗体具有净正电荷。该抗tfpi抗体表面上的正电荷的排斥可能阻止各个分子之间的蛋白质-蛋白质结合,并且从而显著增加可溶性。假设盐的阴离子(cl-)与抗tfpi抗体表面上的精氨酸侧链上的胍基结合,以中和正电荷,这增强蛋白质-蛋白质相互作用,并且因此促使更低的可溶性和溶液浊度。通过将ph转变为4-6,开发了本文描述的无盐制剂,以实现增加的抗体可溶性和稳定性(参见图1)。在不存在盐的情况下,其他稳定剂例如蔗糖的浓度可以增加到》150mm且《300mm,而不妥协(compromising)渗透压摩尔浓度。
[0058]
还研究了ph对抗tfpi抗体的浊度的作用。如图2中所示,ph也可以极大地影响atfpi ab溶液的浊度。当ph从4增加到6.5时,atfpi ab溶液的浊度增加81fnu。进一步将ph增加至7,溶液的浊度超出准确测量的范围。然而,当ph降低时,在溶液中形成的沉淀物是可逆的。当ph增加至接近于atfpi ab的pi的值时,该结果可以归因于表面电荷中和,因为atfpi ab的pi值为大约7.9。根据该研究,更低的ph对于atfpi ab制剂是优选的。然而,低ph可以引起在注射期间的组织刺激。因此,从患者依从性观点来看,中性ph是优选的。平衡这两种因素,atfpi ab制剂的最佳ph为ph 5-ph 6。
[0059]
实施例2抗tfpi抗体制剂基于实施例1中呈现的出乎意料的发现,制备不含nacl的基本上等渗的抗tfpi ab制剂。这些制剂通常采用高蔗糖浓度,以帮助稳定抗tfpi ab。
[0060]
将冷冻的抗tfpi抗体解冻,且根据表1中呈现的制剂通过透析再配制。制备制剂且用0.22μm滤器过滤,并且填充到玻璃管材小瓶中且用橡胶塞子塞住。
[0061]
还发现在不存在nacl的情况下,以及在蔗糖88mm-292mm和聚山梨酯80或聚山梨酯20(50-200ppm)的存在下,带正电的氨基酸例如精氨酸(10-50mm)可以有效抑制atfpi ab糖化。表1抗tfpi抗体制剂
[0062]
通过hplc-sec对蛋白质聚集和降解,lc-ms对atfpi结构变化(糖化和氧化),以及散射比浊法对浊度评价,粘度计对粘度测量,以及渗透压摩尔浓度仪器对渗透压摩尔浓度测量,来分析这些抗tfpi mab制剂中的每一种。这些分析的结果呈现于表2中。表2抗tfpi抗体制剂的渗透压摩尔浓度和浊度
*基于计算估计的渗透压摩尔浓度
[0063]
实施例3精氨酸对抗tfpi ab糖化的作用实施例证实与无添加的精氨酸的抗tfpi ab制剂相比较,含有精氨酸的抗tfpi ab制剂显示出降低的抗体糖化。
[0064]
以ph 6、含和不含精氨酸的抗tfpi ab制剂贮存于40℃下14天,并且通过lc-ms进行测试。表3中呈现的结果证实可能是由于atfpi ab的独特结构,带正电的氨基酸精氨酸使抗tfpi ab的糖化降低至在参考标准品中发现的水平。表3精氨酸降低抗tfpi mab糖化
[0065]
基于该研究的结果可以得出结论:atfpi ab的稳定性高度受制剂ph影响,并且当考虑iv、im和皮下注射时,对于制剂稳定性的最佳ph为ph 5-ph 6。精氨酸看起来能够阻止atfpi ab糖化。实施例4和实施例5中呈现的制剂开发和稳定性研究基于这些发现进行设
计。
[0066]
实施例4抗tfpi ab制剂的稳定性抗tfpi ab制剂的hplc-sec结果和lc-ms结果概括于表4-7中。表4在5℃下3个月后抗tfpi ab冻干制剂的稳定性1计算基于2个月值。2如果速率是负的,则记入零。y:与参考标准品是可比较的y*:与参考标准品是可比较的,伴随较少修饰表5在40℃下3个月后抗tfpi ab冻干制剂的稳定性1计算基于2个月值。2如果速率是负的,则记入零。y:与参考标准品是可比较的y*:与参考标准品是可比较的,伴随较少修饰表6在5℃下3个月的液体制剂1计算基于2个月值。2如果速率是负的,则记入零。
y:与参考标准品是可比较的y*:与参考标准品是可比较的,伴随较少修饰表7在40℃下3个月的液体制剂1计算基于2个月值。y:与参考标准品是可比较的
y*:与参考标准品是可比较的,伴随较少修饰。本发明提供了1.一种无盐蛋白质或抗体制剂,其包含:a.10mm-30mm组氨酸;b.50ppm-200ppm非离子型表面活性剂;c.88mm-292mm选自甘露糖醇、右旋糖、葡萄糖、海藻糖和蔗糖的糖或糖醇;d.0mm-50mm精氨酸;e.0mm-50mm赖氨酸;f.0mm-133mm甘氨酸或丙氨酸;g.0mm-10mm甲硫氨酸;和h.1mg/ml-150mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 4.0-ph 6.0的ph,并且其中所述蛋白质制剂基本上不含无机盐。2.项1的无盐蛋白质或抗体制剂,其中所述制剂具有在22℃下范围为1-8mpa-s的粘度。3.项1的无盐蛋白质或抗体制剂,其中所述制剂具有范围为240-380mmol/kg的渗透压摩尔浓度。4.项1中任一项的无盐蛋白质或抗体制剂,其中所述非离子型表面活性剂是选自聚山梨酯20和聚山梨酯80的聚山梨酯。5.项1的无盐蛋白质或抗体制剂,其中所述糖是蔗糖。6.项1的无盐蛋白质或抗体制剂,其包含10mm-50mm精氨酸。7.项1的无盐蛋白质或抗体制剂,其包含:a.30mm组氨酸,b.100ppm聚山梨酯80,c.292mm蔗糖,和d.20mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。8.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯80,c.234mm蔗糖,d.50mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。9.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯80,c.234mm蔗糖,和d.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。
10.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯80,c.88mm蔗糖,d.133mm甘氨酸,和e.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。11.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯20,c.88mm蔗糖,d.133mm甘氨酸,和e.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。12.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.200ppm聚山梨酯20,c.88mm蔗糖,d.133mm甘氨酸,和e.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。13.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯80,c.88mm蔗糖,和d.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。14.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯80,c.88mm蔗糖,d.10mm精氨酸,和e.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。15.项1的无盐蛋白质或抗体制剂,其包含5mm-10mm甲硫氨酸。16.项1的无盐蛋白质或抗体制剂,其包含:a.10mm组氨酸,b.75ppm聚山梨酯80,c.88mm蔗糖,
d.30mm赖氨酸,和e.100mg/ml蛋白质或抗体;其中所述蛋白质或抗体制剂具有范围为ph 5.0-ph 6.0的ph。17.一种无盐抗tfpi抗体制剂,其包含:a.10mm-30mm组氨酸,b.50ppm-200ppm非离子型表面活性剂,c.88mm-292mm选自甘露糖醇、右旋糖、葡萄糖、海藻糖和蔗糖的糖或糖醇,d.0mm-50mm精氨酸,e.0mm-50mm赖氨酸,f.0mm-133mm甘氨酸或丙氨酸g.0mm-10mm甲硫氨酸,和h.1mg/ml-150mg/ml抗tfpi抗体;其中所述抗tfpi抗体制剂具有ph 4.0-ph 6.0的ph,并且其中所述抗tfpi抗体制剂基本上不含无机盐。18.项17的无盐抗tfpi抗体制剂,其中所述制剂具有在22℃下范围为1-8mpa-s的粘度。19.项17的无盐抗tfpi抗体制剂,其中所述制剂具有范围为240-380mmol/kg的渗透压摩尔浓度。20.项17的无盐抗tfpi抗体制剂,其中所述非离子型表面活性剂是选自聚山梨酯20和聚山梨酯80的聚山梨酯。21.项17的无盐抗tfpi抗体制剂,其中所述糖是蔗糖。22.项17的无盐抗tfpi抗体制剂,其包含:a.10mm组氨酸,b.75ppm tween 80,c.234mm蔗糖,d.30mm精氨酸,和e.10mm甲硫氨酸,和f.100mg/ml抗tfpi抗体;其中所述抗tfpi抗体制剂具有ph 5.5。23.项17的无盐抗tfpi抗体制剂,其中所述抗tfpi抗体是人igg2单克隆抗体。24.项17的无盐抗tfpi抗体制剂,其中所述人igg2单克隆抗体包含含有seq id no:1的氨基酸序列的轻链和含有seq id no:2的氨基酸序列的重链。25.一种用于治疗患者中的病症的方法,所述方法包括给所述患者施用治疗有效量的蛋白质或抗体制剂,其在ph 4.0-ph 6.0的ph下包含10mm-30mm组氨酸、50ppm-200ppm聚山梨酯80或聚山梨酯20、88mm-292mm蔗糖、0mm-50mm精氨酸、0mm-50mm赖氨酸、0mm-133mm甘氨酸、0mm-10mm甲硫氨酸、和1mg/ml-150mg/ml的蛋白质或抗体,其中所述蛋白质或抗体制剂基本上不含无机盐。26.项25的方法,其中所述蛋白质或抗体制剂静脉内、皮下或肌内施用。27.一种用于治疗患者中的血友病a或血友病b的方法,所述方法包括给所述患者
施用治疗有效量的抗tfpi抗体制剂,其在ph 4.0-ph 6.0的ph下含有10mm-30mm组氨酸、50ppm-200ppm聚山梨酯80或聚山梨酯20、88mm-292mm蔗糖、0mm-50mm精氨酸、0mm-50mm赖氨酸、0mm-133mm甘氨酸、0mm-10mm甲硫氨酸、和1mg/ml-150mg/ml的蛋白质,并且其中所述抗tfpi制剂基本上不含无机盐。28.项27的方法,其中所述抗tfpi抗体是人igg2单克隆抗体。29.项28的方法,其中所述人igg2单克隆抗体包含含有seq id no:1的氨基酸序列的轻链和含有seq id no:2的氨基酸序列的重链。30.项27的方法,其中所述抗tfpi抗体制剂静脉内、肌内或皮下施用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1