STAT3磷酸化抑制剂、自身免疫性疾病和冠状病毒传染病的预防或治疗剂
stat3磷酸化抑制剂、自身免疫性疾病和冠状病毒传染病的预防或治疗剂
【技术领域】
1.[相关申请案的交叉引用]本技术提出对2020年6月30日提交的日本国专利申请第2020-112680号说明书的优先权要求,本说明书参照引用其全部内容。本发明涉及一种自身免疫性疾病和冠状病毒传染病的预防或治疗剂。
背景技术:
[0002]
在呼吸道领域,间质干细胞(mscs:mesenchymal stem cells)的肺损伤和肺纤维化抑制作用、消炎作用备受关注(非专利文献3)。再者,tnf-α、il-1β、ccl2、il-6等炎性细胞因子是细胞因子风暴中的重要因子。特别是经由il-6/jak/stat传导通路等诱导il-6的机制被称为il-6放大器(il-6amplifier,il-6amp),是细胞因子风暴的主要机制,而细胞因子风暴被视为以类风湿性关节炎等为代表的自身免疫性疾病、covid-19等重症化的原因(非专利文献4)。
[0003]
自身免疫性疾病是指免疫系统对自身的正常细胞和/或组织发生过度反应并攻击正常细胞和/或组织所引起的疾病,是因免疫耐受失衡而引起的疾病的总称。许多疾病被列为自身免疫性疾病,有的还被指定为难治性疾病,因此其治疗方法的开发备受期待。
[0004]
另一方面,冠状病毒作为引起所谓感冒症状的病毒而广为人知,其有时会因突变而生成传染性强、毒性大的毒株而造成问题。特别是现在,属于突变株的严重急性呼吸综合征冠状病毒2(sars-cov2)所引起的传染病,即新型冠状病毒肺炎(coronavirus disease 2019,covid-19),也就是所谓的新型冠状病毒传染病正在全世界蔓延,还出现了许多死者,因此其治疗方法的开发迫在眉睫。【现有技术文献】【专利文献】
[0005]
专利文献1:日本专利第5946191号公报【非专利文献】
[0006]
非专利文献1:hoffmann et al.cell 181,1-10(2020)非专利文献2:东京大学网站《有望阻止新型冠状病毒感染的国内现有药剂之鉴定》:https://www.ims.u-tokyo.ac.jp/imsut/content/000002328.pdf非专利文献3:clin med insights circ respir pulm med.2015;9:91-6非专利文献4:immunity.2020;52:731-33.非专利文献5:mol immunol 2007 2497非专利文献6:病毒(
ウイルス
)第69巻第1号,pp.61-72,2019
技术实现要素:
【发明要解决的技术问题】
[0007]
本发明要解决的技术问题,在于提供一种对stat3磷酸化和il6amp的新型抑制剂。再者,对于能够通过抑制stat3磷酸化来处理的疾病,提供一种新型预防或治疗剂,也是本发明要解决的技术问题。例如,本发明要解决的进一步的技术问题,在于提供一种新颖的自身免疫性疾病预防或治疗剂,其有效成分是对自身免疫性疾病疗效至今不为人知的物质。此外,还在于提供一种新颖的冠状病毒传染病预防或治疗剂,其有效成分是对冠状病毒传染病疗效至今不为人知的物质。【用于解决技术问题的技术方案】
[0008]
在这种情况下,发明人探讨了数千种化合物,结果发现斯钙素1(stc1)会抑制位于il-6/jak/stat传导通路下游的stat3磷酸化。更进一步,发明人通过采用stc1抑制stat3磷酸化,得出下述见解。具体而言,就是发明人也发现,stc1在表观遗传学上会诱导抗炎因子socs1的表达。并且,发明人还发现,stc1会通过抑制在细胞表面的冠状病毒s蛋白受体、以及病毒外膜与细胞膜融合所需的重要因子的表达,而抑制冠状病毒感染细胞。本发明以此类新见解为基础。
[0009]
因此,本发明提供以下项目:项1.一种stat3磷酸化抑制剂,其特征在于含有斯钙素1(stc1)作为有效成分。
[0010]
项2.一种jak表达或磷酸化抑制剂,其特征在于含有斯钙素1作为有效成分。
[0011]
项3.一种自身免疫性疾病的预防或治疗剂,其特征在于含有斯钙素1作为有效成分。
[0012]
项4.一种流行性感冒病毒传染病的预防或治疗剂,其特征在于含有斯钙素1作为有效成分。
[0013]
项5.一种冠状病毒传染病的预防或治疗剂,其特征在于含有斯钙素1作为有效成分。
[0014]
项6.如项5所述的冠状病毒传染病的预防或治疗剂,其特征在于前述冠状病毒具有能够与ace2结合的s蛋白。
[0015]
项7.如项5或6所述的冠状病毒传染病的预防或治疗剂,其特征在于前述冠状病毒为sa rs相关冠状病毒。
[0016]
项8.一种ace2和tmprss2的表达抑制剂,其特征在于含有斯钙素1作为有效成分。
[0017]
项9.一种il6amp抑制剂,其特征在于含有斯钙素1作为有效成分。
[0018]
项10.如项1所述的stat3磷酸化抑制剂、项2所述的jak表达或磷酸化抑制剂、项3所述的自身免疫性疾病的预防或治疗剂、项4所述的流行性感冒病毒传染病的预防或治疗剂、项5~7中任一项所述的冠状病毒传染病的预防或治疗剂、项8所述的ace2和tmprss2表达抑制剂或项9所述的il6amp抑制剂。【发明效果】
[0019]
根据本发明,可以提供一种stat3磷酸化和il6amp的新型抑制剂。再者,对于能够通过抑制stat3磷酸化来处理的疾病,本发明也提供一种新型预防或治疗剂。例如,本发明提供一种新颖的自身免疫性疾病预防或治疗剂,其有效成分是对自身免疫性疾病疗效至今不为人知的物质。更进一步,本发明通过采用对冠状病毒传染病疗效至今不为人知的物质stc1作为有效成分,可以提供一种新颖的冠状病毒传染病预防或治疗剂。具体而言,根据本发明,可以通过抑制ace2和tmprss2的表达来抑制冠状病毒感染,因此对预防和治疗冠状病
毒传染病有用。再者,发明人还发现stc1会有效抑制肺纤维化(专利文献1)。因此,根据本发明,不仅可以预防或治疗冠状病毒传染病,而且在冠状病毒传染病重症化时可望预防肺纤维化,并在肺纤维化已发生时也可望取得治疗、抑制恶化的效果,因此更加有用。另外,能够抑制肺纤维化的药剂未必会对预防或治疗冠状病毒传染病起效,因此本发明的这种效果是出乎预料的。
【附图说明】
[0020]
【图1】为实施例的博来霉素(blm)小鼠气管给药肺损伤模型的概要。【图2】为实施例1的蛋白免疫印迹检测和定量pcr的结果。【图3】为stc1对线粒体的tca循环及其周边代谢造成影响的概要。【图4】为实施例2的蛋白免疫印迹检测结果。【图5】为实施例2的半定量甲基化特异性pcr结果。【图6】为实施例2的smad7蛋白乙酰化程度的测定结果。【图7】为实施例3的苏木精-伊红染色结果。【图8】表示在序列号1中登录号为np_003146.1的人类stc1的氨基酸序列。【图9】为实施例4-1)的蛋白免疫印迹检测结果。【图10】为实施例4-2)的蛋白免疫印迹检测结果。【图11】为实施例4-3)的蛋白免疫印迹检测(a)、半定量pcr(b)、半定量甲基化特异性pcr的结果。【图12】为实施例4-4)的蛋白免疫印迹检测结果。【图13】为实施例4-5)的免疫沉淀结果。【图14】为实施例4-6)的蛋白免疫印迹检测结果。【图15】为实施例4-7)的蛋白免疫印迹检测结果。【图16】为实施例4-8)的动物实验结果。【图17】为实施例中所阐明的见解的示意图。
【具体实施方式】
[0021]
stat3磷酸化抑制剂本发明提供一种含有斯钙素1作为有效成分的stat3磷酸化抑制剂。stat3(信号转导和转录激活因子3,signal transducer and activator of transcription 3)是stat蛋白家族的一员,且已知在il-6/jak/stat传导通路等被磷酸化后激活。典型例子是氨基酸序列的ncbi登录号为np_001356441.1的stat3。本发明的有效成分stc1是专利文献1等中记载的公知成分,属于一种二聚体糖蛋白激素。在本发明中,stc1既可以是从动物细胞或组织等中获得的天然stc1分子,又可以是氨基酸序列与天然stc1相同的重组型stc1、以利用基因工程技术改变的stc1基因为基础而产生的重组型stc1、合成stc1。再者,在本发明中,stc1也可以是stc1活性片段等功能等价物。因此,在本发明中,只要未注明并非如此,术语“斯钙素1”(stc1)就以包含上述各种stc1的含义使用。
[0022]
再者,本发明中使用的stc1,宜为具有人源氨基酸序列的stc1,或是根据人源氨基
酸序列在不损害其功能下改变的stc1(例如1个或数个(例如2个、2~3个、2~4个、2~5个)氨基酸缺失、插入和/或被取代的stc1)。人类stc1的氨基酸序列和碱基序列是公知的,登录号为np#003146.1、nm#003155.2。例如,序列号1表示登录号为np_003146.1的人类stc1氨基酸序列。再者,许多非人源的动物源stc1,其氨基酸序列和碱基序列也是已知的。已知此类动物源stc1与人源stc1的一致性都很高(表1)。
[0023]
【表1】
[0024]
因此,在本发明的一实施例中,可以使用的stc1与人类stc1氨基酸序列的一致性在80%以上,90%以上较宜,94%以上更佳。更好的典型例子是使用氨基酸序列与人类stc1序列(例如来源于293细胞的人类stc1序列)完全一致的天然或重组stc1(rstc1)。在本发明中,此类stc1既可单独使用1种,又能组合2种以上使用。
[0025]
本发明的有效成分stc1及其盐,也会以水合物或溶剂合物的形式存在,因此这些水合物和溶剂合物也包含在本发明的化合物有效成分中。
[0026]
关于形成溶剂合物的溶剂,可以列举乙醇、丙醇等醇类,乙酸等有机酸、乙酸乙酯等酯类,四氢呋喃、二乙醚等醚类,丙酮等酮类,以及dmso等。此类溶剂既可单独使用1种,又能组合2种以上作为混合溶剂使用。
[0027]
在本发明中,既可将本发明的有效成分stc1本身用作stat3磷酸化抑制剂,又能作为与药学上允许的各种载体(例如张度剂、螯合剂、稳定剂、ph调节剂、防腐剂、抗氧化剂、增溶剂、增稠剂等)组合而成的药物组合物使用。
[0028]
关于张度剂,可以列举葡萄糖、海藻糖、乳糖、果糖、甘露醇、木糖醇、山梨糖醇等糖类,甘油、聚乙二醇、丙二醇等多元醇类,氯化钠、氯化钾、氯化钙等无机盐类等。此类张度剂既可单独使用1种,又能组合2种以上使用。
[0029]
关于螯合剂,可以列举依地酸二钠、依地酸钙钠、依地酸三钠、依地酸四钠、依地酸钙等依地酸盐类,以及乙二胺四乙酸盐、氨三乙酸或其盐、六偏磷酸钠、柠檬酸等。此类螯合剂既可单独使用1种,又能组合2种以上使用。
[0030]
关于稳定剂,可以列举亚硫酸氢钠等。
[0031]
关于ph调节剂,可以列举盐酸、碳酸、乙酸、柠檬酸等酸类,氢氧化钠、氢氧化钾等碱金属氢氧化物,碳酸钠等碱金属碳酸盐或碳酸氢盐、乙酸钠等碱金属乙酸盐,柠檬酸钠等碱金属柠檬酸盐,三羟甲基氨基甲烷(trometamol)等碱基等。此类ph调节剂既可单独使用1种,又能组合2种以上使用。
[0032]
关于防腐剂,可以列举山梨酸、山梨酸钾、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、对羟基苯甲酸丁酯等对羟基苯甲酸酯、葡萄糖酸氯己定、氯化苯甲烃铵、氯化苄氧乙铵、氯化十六烷基吡啶等季铵盐,烷基二氨基乙基甘氨酸、三氯叔丁醇、polyquad、聚六亚甲基双胍、双氯苯双胍己烷等。此类防腐剂既可单独使用1种,又能组合2种以上使用。
[0033]
关于抗氧化剂,可以列举亚硫酸氢钠、干燥亚硫酸钠、焦亚硫酸钠、浓缩混合生育酚等。此类抗氧化剂既可单独使用1种,又能组合2种以上使用。
[0034]
关于增溶剂,可以列举苯甲酸钠、甘油、d-山梨糖醇、葡萄糖、丙二醇、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚乙二醇、d-甘露醇等。此类增溶剂既可单独使用1种,又能组合2种以上使用。
[0035]
关于增稠剂,可以列举聚乙二醇、甲基纤维素、乙基纤维素、羧甲基纤维素钠、黄原胶、硫酸软骨素钠、羟乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、聚乙烯吡咯烷酮、聚乙烯醇等。此类增稠剂既可单独使用1种,又能组合2种以上使用。
[0036]
药物组合物的实施方式,对于组成物中的stc1含量并无特别限制,例如可以根据90质量%以上、70质量%以上、50质量%以上、30质量%以上、10质量%以上、5质量%以上、1质量%以上等条件适当设定。
[0037]
对于制剂形态并无特别限制,可以列举片剂、丸剂、胶囊剂、散剂、颗粒剂、糖浆剂等经口给药剂;注射剂(静脉注射、肌肉注射、局部注射等)、含漱剂、点滴剂、外用剂(软膏、乳霜、贴敷药、吸入药)、栓剂等非经口给药剂等各种制剂形态。上述制剂形态中,以外用剂等为宜,其中又可列举吸入药(经气管注入药)。
[0038]
在本发明中,stc1给药剂量因给药途径以及患者的年龄、体重、症状等而异,无法笼统规定,但是成人的每日给药剂量通常约为5000mg以下,理想的每日给药剂量约为1000mg以下。stc1给药剂量的下限也并无特别限制,例如成人的每日stc1给药剂量通常可适当设定为0.1mg以上,且宜设定为0.5mg以上。每日给药一次时,每份制剂中含有该剂量即可;每日给药三次时,每份制剂中含有该剂量的三分之一即可。
[0039]
本发明的stat3磷酸化抑制剂,给药对象是哺乳动物等患者。关于哺乳动物,可以列举人、猴、小鼠、大鼠、兔、猫、狗、猪、牛、马、羊等。
[0040]
自身免疫性疾病的预防或治疗剂本发明提供一种含有斯钙素1作为有效成分的自身免疫性疾病的预防或治疗剂。il6等细胞因子与受体结合后,会诱导jak和stat的磷酸化,并诱导急性期蛋白等的转录(非专利文献5)。socs通过抑制jak的磷酸化,也间接抑制stat的磷酸化。il6/jak/stat传导通路被视为与类风湿性关节炎等自身免疫性疾病发作有关的重要信号通路,成为药物研发的标的。至此,如前所述,发明人此次发现stc1会抑制在il-6/jak/stat传导通路下游的stat3发生磷酸化。本发明以此新见解为基础。本发明的有效成分stc1,则也可使用其水合物和溶
剂合物等,关于此点如前所述。
[0041]
关于本发明的目标疾病,可以列举类风湿性关节炎、卡斯特曼病、克罗恩病、韦格纳肉芽肿、肉样瘤病、特应性皮炎、慢性脓皮病、牛皮癣、伴随肺炎的高ige综合征等自身免疫性疾病。
[0042]
在本发明中,可将本发明的有效成分stc1本身用作自身免疫性疾病的预防或治疗剂,也能作为与药学上允许的各种载体组合而成的药物组合物使用。关于载体,可按前述剂量同样使用前述stat3磷酸化抑制剂的载体。
[0043]
再者,上述药物组合物,除了stc1之外,还可进一步含有被认为具有预防或治疗自身免疫性疾病作用的化合物。关于已知具有预防或治疗自身免疫性疾病作用的化合物,可以列举皮质类固醇(泼尼松龙(prednisolone)等)、jak抑制剂(托法替尼(tofacitinib)等)、钙调磷酸酶抑制剂(环孢素(ciclosporin)、他克莫司(tacrolimus)等)、dna合成抑制剂(环磷酰胺(cyclophosphamide)等)、mtor抑制剂(西罗莫司(sirolimus)等)、imdh抑制剂(霉酚酸酯等)、抗体制剂(托珠单抗(tocilizumab)、利妥昔单抗(rituximab)等)等。此类化合物既可单独使用1种,又能组合2种以上使用。在药物组合物的实施方式中,组成物中stc1的含量、制剂形态、给药剂量、给药对象(患者)等,与前述stat3磷酸化抑制剂的相同。
[0044]
冠状病毒传染病的预防或治疗剂本发明提供一种含有stc1的冠状病毒传染病的预防或治疗剂。关于本发明的有效成分stc1也能使用其水合物和溶剂合物等,如前所述。
[0045]
关于本发明的目标疾病,冠状病毒是指属于冠状病毒科(coronaviridae)的病毒。关于冠状病毒,可以列举α属冠状病毒、β属冠状病毒等,且宜列举β属冠状病毒等。关于α属冠状病毒,可以列举duvinacovirus亚属(例如hcov-229e等)、setracovirus亚属(例如hcov-nl63等)等。关于β属冠状病毒,可以列举embecovirus亚属(例如hcov-oc43、hcov-hku1等)、sarbecovir us亚属、merbecovirus亚属(例如中东呼吸综合症冠状病毒(mers-cov)等)等,且宜列举sarbeco virus亚属等。关于sarbecovirus亚属等,可以列举严重急性呼吸综合征相关冠状病毒(sarsr-cov)等。关于sarsr-cov,可以列举严重急性呼吸综合症冠状病毒(sars-cov)、严重急性呼吸综合征冠状病毒2(sars-cov2)等。
[0046]
以sars-cov2等冠状病毒为例,其包膜上有刺突蛋白(s蛋白),该s蛋白与细胞膜受体(ace2)结合,然后在跨膜丝氨酸蛋白酶2(tmprss2)这种蛋白水解酶的作用下,s蛋白被激活,目前已知这是病毒外膜与细胞膜融合的关键,气管细胞中有ace2和tmprss2被视为sars-cov-2感染的必要条件(非专利文献1、非专利文献2)。发明人发现,当肺损伤导致ace2和tmprss2的表达增强时,通过使用本发明的预防或治疗剂的有效成分stc1,会抑制该肺损伤时ace2和tmprss2的表达增强。因此,冠状病毒传染病的预防或治疗剂,对于具有s蛋白的冠状病毒、尤其是具有能够与ace2结合的s蛋白的冠状病毒特别有效。
[0047]
在本发明中,可将本发明的有效成分stc1本身用作自身免疫性疾病的预防或治疗剂,也能作为与药学上允许的各种载体组合而成的药物组合物使用。关于载体,可同样使用前述stat3磷酸化抑制剂的载体。
[0048]
再者,上述药物组合物,除了stc1之外,还可进一步含有被认为具有预防或治疗自身免疫性疾病作用的化合物。关于已知具有预防或治疗自身免疫性疾病作用的化合物,可以列举法匹拉韦(favipiravir)、瑞德西韦(remdesivir)、伊维菌素(ivermectin)、环索奈
德(cicleson ide)、托珠单抗(tocilizumab)、卡莫司他(camostat)、萘莫司他(nafamostat)。此类化合物既可单独使用1种,又能组合2种以上使用。在药物组合物的实施方式中,组成物中的stc1的含量、制剂形态、给药剂量、给药对象(患者)等,与前述stat3磷酸化抑制剂的相同。
[0049]
本发明的冠状病毒传染病预防或治疗剂的有效成分stc1,至少会通过抑制ace2和tmprs s2的表达来预防、治疗和/或缓解冠状病毒传染病。因此,本发明也提供一种含有stc1的ace2和tmpr ss2的表达抑制剂。再者,发明人发现stc1会有效抑制肺纤维化,且含有stc1作为有效成分的肺纤维化的预防、治疗和/或抑制恶化用药物组合物已获得专利权(专利文献1)。可是,目前已知虽然冠状病毒传染病重症化时可能会发生肺纤维化,但是肺纤维化会因各种各样的原因而发生,冠状病毒传染病只是其中一种,显然能够治疗肺纤维化的化合物不一定会抑制冠状病毒感染本身。而且,关于ace2和tmprss2的表达与stc1的关系,迄今为止没有任何报告。因此,在本发明中stc1对ace2和tm prss2的表达抑制效果和对冠状病毒传染病的预防或治疗效果,依靠现有技术无望实现。有报告指出,tmprss2在流行性感冒(a型、b型)、其他呼吸道相关病毒等的感染中也起到重要作用(非专利文献6)。因此,本发明的ace2和tmprss2的表达抑制剂,也能用作呼吸道相关病毒(例如冠状病毒、流行性感冒病毒)等的预防或治疗剂。另外,ace2和tmprss2的表达抑制剂、呼吸道相关病毒的预防或治疗剂的有效成分、制剂形态、给药剂量等,与冠状病毒传染病的预防或治疗剂相同。il-6amp抑制剂sars-cov2与ace2结合后,会使本应与ace2结合后被水解的血管紧张素ⅱ,通过at1r受体诱导tn fα、il6等。结果stat3被激活,进一步增强il6的合成。这是il6在对il6自身放大,因此被称为il-6放大器(amp),且被认为与covid19的急剧重症化有关。再者,病毒被先天免疫系统识别后激活nf kb的通路,也被认为会促进il6amp。如前所述,本发明的有效成分stc1通过阻碍il-6/jak/stat传导通路来抑制il-6amp。因此,本发明也提供一种含有stc1的il-6amp抑制剂。另外,il-6amp抑制剂的有效成分、制剂形态、给药剂量等与前述的相同。
[0050]
下面列举实施例更加具体地说明本发明,但本发明的实施方式不限于此。【实施例】
[0051]
在本实施例中,重组人(r)stc1是由biovender公司制造的。具体而言,将附加了tag结构的人源stc1基因导入293细胞,并用tag序列分离出rstc1。在以下实施例中,有时会将上述重组人(r)stc1仅表示为stc1。
[0052]
实施例1在博来霉素肺损伤模型中stc1经气管给药抑制ace2和tmprss2的表达在本实施例中,使用小鼠的博来霉素(blm)经气管给药肺损伤模型(图1)。具体而言,在day0,向每组各6只c57bl6/j小鼠(雌性,8周龄)腹腔内注射麻醉药(将300μg盐酸氯胺酮和160ng甲苯噻嗪在100μl生理盐水中稀释而成)麻醉。然后切开颈部露出气管,将23g的静脉留置针(surflo)外套插入气管。进而从surflo外套将以下药剂分别注入到各组小鼠气管内。(i)生理盐水组(对照组):生理盐水50μl(ii)blm组:含博来霉素生理盐水50μl(博来霉素浓度0.4mg/ml)
bisulfite conversion kit ver.2),并使用甲基化特异性pcr用聚合酶(takara episcope msp kit)和abi 7500real time pcr system进行处理。如图5所示,stc1也诱导了smad7的去甲基化。图6为stc1对smad7蛋白的乙酰化造成的影响。关于stc1对小鼠肺部的smad7造成的影响,通过免疫荧光染色对摘除的小鼠肺部进行分析。具体而言,将实施例1中使用的肺部切片,让其固定在玻片上,并将molecular device公司的alexa-488抗体、alexa594抗体与smad7抗体(santacruz公司b8)、抗乙酰化赖氨酸抗体(cell signaling technology公司ac-k-103)、核染色(daco公司dapi)组合起来,使用相衬显微镜进行研究。图6为其结果。如图6所示,stc1也诱导了smad7赖氨酸基的乙酰化。smad7被乙酰化后,可以稳定表达。也就是说,显然stc1通过smad7的表观遗传调控来增强smad7的表达。
[0057]
实施例3再者,使用在实施例1中获得的各组小鼠的肺标本,进行苏木精-伊红染色。图7显示其结果。如图7所示,stc1抑制了博来霉素导致的肺部炎症、肺纤维化。
[0058]
实施例4评估stc1对stat3磷酸化、il-6amp等的影响<方法>
·
细胞实验人单核细胞thp1细胞在含有10%胎牛血清(nichirei)和1%青霉素链霉素(sigma)的rpmi培养基(sigma)中培养24小时后,通过添加10um佛波醇12-十四酸酯13-乙酸酯(pma)使其分化为巨噬细胞。添加pma经过24小时后,准备3组,即不添加重组人il6组、添加10ng/ml的il6组、添加50ng/ml的il6组,并且再给这些组准备不添加、添加50ng/ml的stc1组,即准备3
×
2=6组。在这些条件下培养24小时后,进行蛋白免疫印迹检测、免疫沉淀、pcr、甲基化特异性pcr、使用sirna抑制特异性基因转录。
·
动物实验在本实施例中,使用小鼠的博来霉素(blm)经气管给药肺损伤模型。具体而言,依照实施例1所述的方法,准备博来霉素(blm)经气管给药肺损伤模型小鼠,在day3和day14摘除每组各3只小鼠的肺部。
·
蛋白免疫印迹检测方法经过用ripa缓冲液制备的thp1细胞全提取液或小鼠摘除肺提取液处理和sds-page凝胶电泳后,将源于细胞或组织的蛋白转录到pvdf膜上,并用一抗和hrp偶联二抗培养后,用生色底物使其显色,并用化学发光检测仪测定蛋白的表达。用于蛋白免疫印迹检测的一抗如下所示:抗stat3抗体(cell signaling technology公司(cst),12640)、抗pstat3抗体(cst,9145)、抗socs1抗体(cst,3950)、抗il6抗体(cst,12153)、抗jak1抗体(cst,3344)、抗pjak1抗体(cst,74129)抗体、抗泛素抗体(cst,58395)、抗ace2抗体(santacruz公司(sc),390851)、抗tmprss2抗体(sc,515727)、抗β肌动蛋白抗体(r&d,mab8929)。二抗使用适合各个动物种的hrp偶联抗体。
·
免疫沉淀方法使protein a/g plus agarose(sc,2003)与抗jak1抗体(sc,1677)结合后,添加用
ripa缓冲液制备的thp1细胞全提取液或小鼠摘除肺提取液,借此回收这些提取液的jak1和与jak1结合的蛋白。通过与还原液一起煮沸,分离出jak1蛋白和与jak1结合的蛋白。
·
半定量pcr使用rneasy mini kit(qiagen)从thp1细胞和小鼠肺组织分离mrna后,使用high capacity cdna kit(applied biosystems)制作从mrna反转录的cdna。使用primer-blast(ncbi)设计引物,并使用sybr green pcr master mix和abi7500实时pcr系统(applied biosystems)进行半定量pcr。
·
甲基化特异性pcr使用methyl primer express软件(applied biosystems)设计socs1基因启动子区域的甲基化和去甲基化引物。使用dneasy blood&tissue kit(qiagen)从thp1细胞提取基因组dna后,进行重亚硫酸盐处理(fujifilm-wako,episight
tm bisulfite conversion kit ver.2),并使用甲基化特异性pcr用聚合酶(takara episcope msp kit)和abi 7500real time pcr system进行处理。
·
sirnasocs1特异性sirna和对照组sirna使用predesigned sirna(ambion)。转染试剂使用lipofectamine rnaimax(invitrogen)。
[0059]
<结果>(thp1细胞数据)1)stc1强有力地抑制thp1细胞中的il6诱导性stat3磷酸化按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)的细胞全提取液,通过蛋白免疫印迹检测来测定其中是否存在stat3和磷酸化stat3,图9为其结果。如图9所示,stc1抑制了il6诱导的stat3磷酸化。也就是说,stc1通过抑制il6诱导性stat3磷酸化,有助于治疗细胞因子综合征和各种自身免疫性疾病。
[0060]
2)stc1抑制thp1细胞中的il6诱导性il6生成增強(il-6放大器)按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)的细胞全提取液,采用蛋白免疫印迹法测定其中是否存在il-6,图10为其结果。如图10所示,stc1抑制了il6诱导的il6生成增強(il6放大器)。也就是说,stc1通过抑制il6诱导性il6放大(il6放大器),有助于治疗细胞因子综合征和各种自身免疫性疾病。
[0061]
3)stc1在thp1细胞中诱导socs1按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)的细胞全提取液,采用蛋白免疫印迹法测定其中的socs1(结果见图11中的a),使用细胞全提取液mrna并采用半定量pcr法测定socs1mrna(结果见图11中的b),使用细胞全提取液dna并采用甲基化特异性pcr法测定socs1基因启动子区域的甲基化程度(结果见图11中的c)。如图11中的a所示,stc1增强了socs1蛋白的生成。再者,图11中的b所示,stc1增强
了socs1的mrna生成。如图11中的c所示,stc1抑制了socs1基因启动子区域的甲基化。图11中的a-c的结果均意味着stc1会增强socs1蛋白的生成。也就是说,stc1通过诱导具有抑制jak作用的socs1,有助于治疗细胞因子综合征和各种自身免疫性疾病。
[0062]
4)stc1抑制jak1在thp1细胞中的表达和磷酸化按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)的细胞全提取液,采用蛋白免疫印迹法测定其中是否存在jak1和jak1磷酸化,图12为其结果。如图12所示,stc1抑制了jak1的表达和磷酸化。
[0063]
5)存在il6时,stc1会促进thp1细胞中socs1与jak1的结合,并促进jak1的泛素化(免疫沉淀法)按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)的细胞全提取液进行免疫沉淀,图13显示其结果。免疫沉淀使用thp1全细胞溶解物,并使用jak抗体和a/g琼脂糖凝胶,回收jak1和jak1结合蛋白质,添加还原剂煮沸后进行蛋白免疫印迹检测。如图13所示,存在il-6时,与jak1结合的socs1会减少,但当stc1存在时,与jak1结合的socs1会增加。因此,显然stc1也会促进jak1的泛素化。也就是说,stc1促进jak1与socs1的结合,并增强jak1的泛素化(jak1的分解)。
[0064]
6)stc1在thp1细胞中抑制il6诱导的ace2、tmprss2的表达。按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)的细胞全提取液进行蛋白免疫印迹检测,图14为其结果。如图14所示,stc1抑制了ace2和tmprss2的表达。因此,stc1通过抑制ace2和tmprss2的表达,有可能减少细胞感染sars-cov2的机会。
[0065]
7)stc1呈socs1依存性地抑制ace2、tmprss2的表达。按照上述方法,对于添加il6(10ng/ml)、il6(50ng/ml)和/或stc1(50ng/ml)的thp1细胞以及未添加这些物质的thp1细胞(对照组)进行蛋白免疫印迹检测,确认使用sirna抑制socs1的情况,图15为其结果。sictr为对照组,显示socs1在正常情况下的变化。如图15所示,使用sirna敲低socs1时,stc1在thp1细胞中诱导的ace2、tmprss2诱导抑制效果会消失。由此可见,stc1对ace2和tmprss2的抑制作用呈socs1依存性。(动物模型:小鼠,博来霉素经气管给药模型,肺部发炎的状态)
[0066]
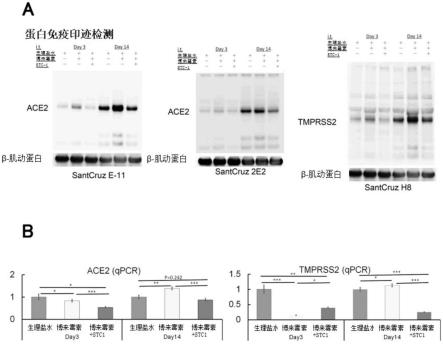
8)stc1抑制通过博来霉素经气管给药在小鼠肺部诱导的jak1表达诱导、jak1磷酸化、ace2和tmprss2的表达上升。按照上述方法,给动物(c57bl6小鼠)经气管注入生理盐水或溶解博来霉素的生理盐水,对于经气管注入溶解博来霉素的生理盐水的实验组,在次日经气管注入生理盐水或溶解stc1的生理盐水,在3日后和14日后回收肺组织进行蛋白免疫印迹检测,图16为其结果。如图16所示,stc1抑制了博来霉素引发的炎症所导致的jak1磷酸化、stat3磷酸化、ace2表达上升、tmprss2表达上升。因此,经气管注入stc1在抑制jak/stat3通路的同时,还抑制ace2和tmprss2的表达。也就是说,针对covid19,stc1通过抑制细胞因子释放综合征,并抑制ace2和tmprss2的表达,有可能抑制covid19的感染和重症化。
图17汇总这次阐明的stc1作用机制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1