细菌蛋白载体和缀合方法与流程
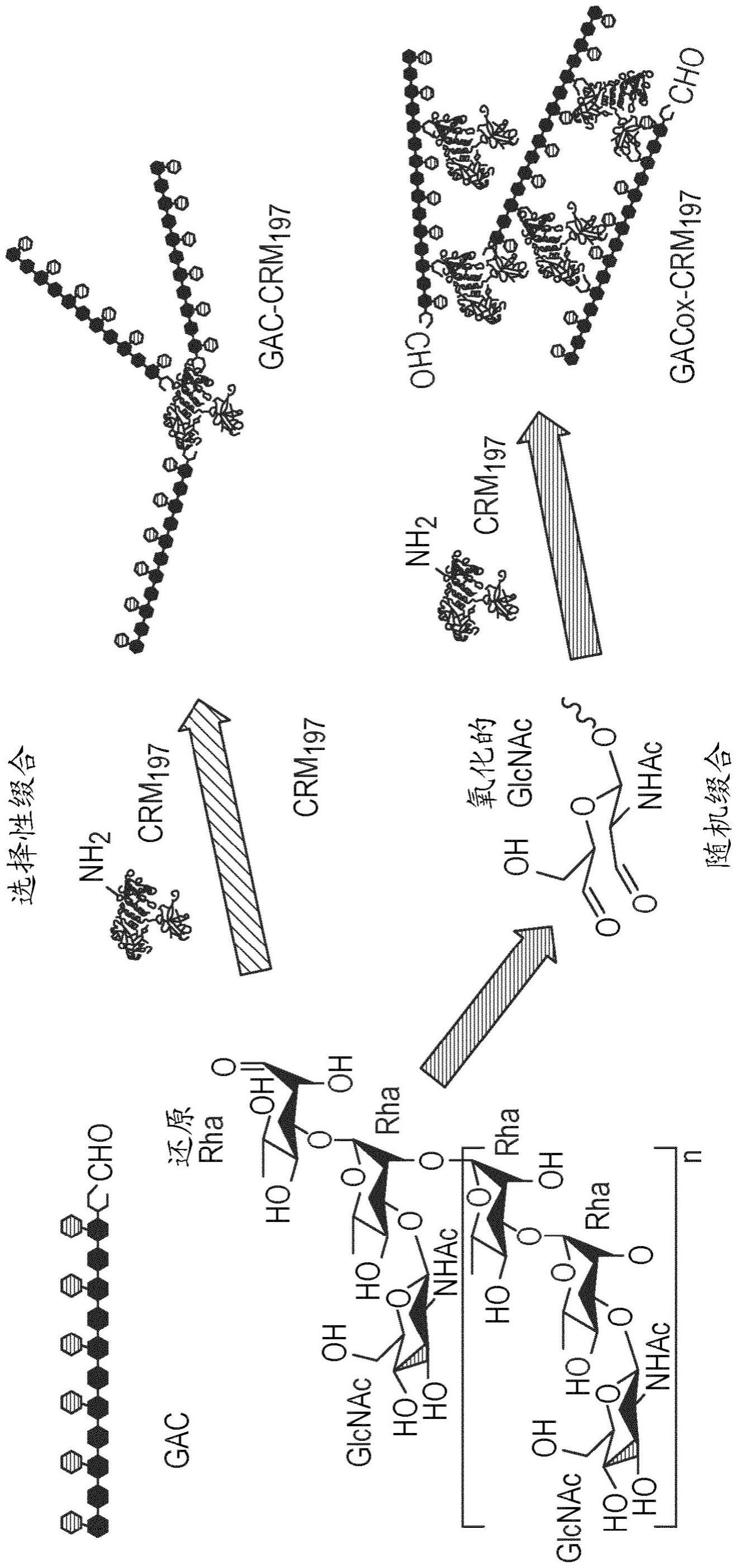
发明领域本发明涉及来自化脓性链球菌(streptococcus pyogenes)(a群链球菌)的抗原用作载体蛋白的用途,连同改进的缀合方法以及所述缀合物用于预防和/或治疗疾病的用途。发明背景a群链球菌(gas)引起多种疾病,从浅表感染(咽炎、皮肤感染、蜂窝组织炎)到严重的侵袭性疾病(产后败血症、坏死性筋膜炎、链球菌中毒性休克综合征),其中在低收入和中等收入国家(lmic)中具有高频的严重后遗症(急性风湿热、arf;风湿性心脏病、rhd和肾小球肾炎)[1]。咽炎是全世界儿童中最常见的症状性gas感染,估计每年有超过4亿例[2]并且是抗生素使用的重要驱动因素[3],其最终可能导致抗生素抗性增加,这是一场日益严重的公共卫生危机[4]。咽炎可能导致rhd,一种慢性炎性心脏瓣膜病况,其代表gas的主要全球负担。在2015年,估计31.9万人死于rhd,其中rhd病例超过3300万且损失1000万伤残调整生命年(daly)[5]。接种疫苗是长期减少全球gas相关疾病负担的最实用策略。然而,目前还没有针对这种病原体的商业疫苗[6]。a群碳水化合物(gac)是一种表面多糖,其由聚鼠李糖骨架与侧链上交替的n-乙酰葡糖胺(glcnac)构成。它代表了一种有吸引力的疫苗候选物,因为它高度保守并在gas菌株中表达。实际上,疫苗策略开发的主要障碍之一由与其他非碳水化合物抗原相关的gas血清型多样性代表[7]。多糖(ps)与适当的载体蛋白的缀合是提高其免疫原性的常用程序[8]。ps是典型的t-细胞非依赖性抗原,其天然仅含有b-细胞表位且缺乏t-细胞表位。与作为t-细胞表位的来源的蛋白的共价缀合将ps转化为t-依赖性抗原,其在婴儿中具有增强的记忆应答、类别转换和抗体产生[9,10]。已经报道,人抗gac血清成功促进了几种gas菌株的吞噬作用[11],而用与破伤风类毒素(tt)或crm197载体蛋白缀合的gac免疫的小鼠被保护免于gas攻击[12,13]。此外,高抗gac抗体滴度和墨西哥儿童喉咙中gas的存在之间的反比关系得到证明[13]。保守蛋白抗原也在针对gas的疫苗开发中。具体而言,通过反向疫苗学方法,链球菌溶血素o(slo)、spyad和spycep被鉴定为有前途的疫苗候选物[14]。slo通过防止细菌内化至溶酶体中已被显示为gas的关键毒力因子,在溶酶体中细菌可以被破坏[15]。此外,slo促进gas对中性粒细胞的吞噬清除的抵抗力,促进gas从先天免疫杀伤中逃逸,并且灭活的slo表明在小鼠模型中针对gas攻击是保护性的[16]。spyad是一种表面-暴露的粘附素,其介导gas与宿主细胞的相互作用。此外,gas菌株中spyad基因的缺失导致敲除突变体正确分裂的能力受损,表明在细菌分裂中也具有重要作用[17]。最后,spycep是一种多结构域蛋白酶,具有负责白介素(il)-8和其他趋化因子切割的催化结构域。il-8的切割代表了一种免疫逃避机制,防止il-8c-末端介导的内皮易位和随后的中性粒细胞的募集[18,19]。这三种蛋白抗原在临床收集物中高度保守和普遍,并且与gac一起几乎可以覆盖所有gas临床分离株[20]。因此,已经提出由重组slo、spyad和spycep与gac-crm197缀合物构成的多组分疫苗的制剂[6]。由于gas的严重后遗症主要影响lmic,因此需要尽可能降低生产成本,以使疫苗在经济上可行。发明详述在这里,测试了使用具有用于gac的抗原和载体的双重作用的gas蛋白之一的可能性,旨在降低最终疫苗制剂的复杂性。crm197是目前用于许可的针对细菌感染的糖缀合物疫苗中的少数载体蛋白之一。出于该原因,人们越来越担心预暴露或共同暴露于该载体可能导致免疫干扰和抗碳水化合物免疫应答的减少[9],因此驱动鉴定替代载体蛋白的需要[21,22]。本发明人令人惊讶地发现slo、spyad和spycep各自都可用作ps的载体蛋白。ps与载体蛋白的化学缀合是一个复杂的过程,如果不在稳健的条件下进行,其可能导致缺乏重现性和一致性。尽管crm197是众所周知的具有完全确立缀合条件的载体蛋白,但本发明人令人惊讶地发现,使用实验设计(doe)方法,可以改进ps(诸如gac)与crm197和gas抗原的连接的稳健性和产率。因此,本发明的第一个方面提供了多糖缀合物,其包含以下或由以下组成:与载体多肽缀合的一种或多种多糖,其中所述载体多肽为:(a)化脓性链球菌spyad(spy0269,gas40)、化脓性链球菌spycep(spy0416,gas57)或化脓性链球菌slo(spy0167,gas25);(b)crm197;或(c)(a)或(b)的片段、变体和/或融合体。通过使用gas抗原作为载体蛋白,提供了crm197的替代物,消除了预先暴露或共同暴露于该载体可能导致免疫干扰和抗碳水化合物免疫应答降低的担忧。此外,使用gas抗原作为载体多肽可能允许从提出的重组slo、spyad和spycep与gac-crm197缀合物的多组分疫苗制剂中除去crm197。这种简化将降低生产成本,使疫苗在经济上更可行,尤其是在利润空间较低的lmic中。如果crm197保留在疫苗制剂中,则目前公开的缀合方法提供的增加的产率和稳健性将有助于降低生产成本,并因此提高lmic中的商业可行性。因此,在一个实施方案中,多糖缀合物是根据本发明的第十个方面的方法产生的(如下所述)。可替代地或另外地,所述载体多肽为:(a)选自化脓性链球菌spyad(spy0269,gas40)、化脓性链球菌spycep(spy0416,gas57)和化脓性链球菌slo(spy0167,gas25),或(b)(a)的变体、片段和/或融合体。“与载体多肽缀合的一种或多种多糖”意指或包括(a)一种或多种多糖分子可以与载体多肽缀合;和/或(b)一种或多种分子种类的多糖可以与载体多肽(例如,相同属、种或菌株的不同多糖,或来自不同属、种或菌株的多糖)缀合。“spyad(spy0269,gas40)”意指或包括包含根据seq id no:1、seq id no:2或ncbi参考序列wp_010921884.1的氨基酸序列或由其组成的多肽。[seq id no:1]-减去n-末端排除结构域的来自gas亲本菌株sf370的天然序列[seq id no:2]-具有n-末端排除结构域的来自gas亲本菌株sf370的天然序列(排除结构域通过下划线指示)“spycep(spy0416,gas57)”意指或包括包含根据seq id no:3、seq id no:4或ncbi参考序列wp_010921938.1的氨基酸序列或由其组成的多肽。[seq id no:3]-spycep脱毒的双突变体[seq id no:4]-来自gas菌株sf370的全长、天然spycep“slo(spy0167,gas25)”意指或包括包含根据seq id no:5、seq id no:6或ncbi参考序列wp_010921831.1的氨基酸序列或由其组成的多肽。[seq id no:5]-slo脱毒的双突变体[seq id no:6]-来自gas菌株sf370的全长、天然slo可替代地或另外地,所述载体多肽为:(a)crm197,或(b)(a)的变体、片段和/或融合体。“crm197”意指或包括包含根据seq id no:7的氨基酸序列或由其组成的多肽。[seq id no:7]-crm197如本文所用的术语“氨基酸”包括标准的二十种基因编码的氨基酸及其相应的“d”型立体异构体(与天然“l”型相比)、ω-氨基酸和其他天然存在的氨基酸、非常规氨基酸(例如α,α-双取代氨基酸、n-烷基氨基酸等)和化学衍生氨基酸(参见下文)。因此,当具体列举氨基酸、诸如“丙氨酸”或“ala”或“a”时,该术语是指l-丙氨酸和d-丙氨酸,除非另有明确说明。其他非常规氨基酸也可以是本发明多肽的合适组分,只要该多肽保留期望的功能特性即可。对于所示的肽,每个编码的氨基酸残基在适当的情况下由单个字母名称代表,对应于常规氨基酸的普通名称。“分离的”意指本发明的特征(例如,多肽)是在不同于其天然存在的环境中提供的。本领域技术人员会理解,“分离的”意指“通过人手”从其自然状态改变,即,如果其存在于自然界中,则其已从其原始环境改变或除去,或两者。例如,当该术语用于本公开中时,天然存在于活生物体中的多核苷酸或多肽当在这种活生物体中时不是“分离的”,但从其自然状态的共存材料中分离的相同多核苷酸或多肽是“分离的”。此外,通过转化、遗传操作或任何其他重组方法引入生物体的多核苷酸或多肽将被理解为“分离的”,即使它仍然存在于所述生物体中,该生物体可以是活的或非活的,除非此类转化、基因操作或其他重组方法产生的生物体以其他方式无法与天然存在的生物体区分开。“多肽”意指或包括多肽和蛋白。多肽的“变体”包括插入、缺失和/或取代,保守的或非保守的。具体而言,变体多肽可以是非天然存在的变体(即,在自然界中不存在或不知道在自然界中存在)。“序列同一性”或“同一性”可以通过如mpsrch程序(oxford molecular)中执行的smith-waterman同源性检索算法使用仿射缺口检索(参数为缺口开放罚分=12和缺口延伸罚分=1)测定,或者通过needleman-wunsch全局比对算法(参见例如,rubin(2000)pediatric.clin.north am.47:269-285)使用默认参数(例如,缺口开放罚分=10.0和缺口延伸罚分=0.5,使用eblosum62评分矩阵)测定。在emboss软件包中的needle工具方便地进行该算法。除非另有指明,否则在申请涉及与具体参考序列的序列同一性的情况下,该同一性意欲在该参考序列的整个长度上计算。或者,同一性百分比可以通过本领域众所周知的方法来确定,例如在expasy设施网站(www.ch.embnet.org/software/lalign_form.html)使用lalign程序(huang和miller,adv.appl.math.(1991)12:337-357,其公开内容通过引用并入本文)使用全局比对选项、评分矩阵blosum62、开放空位罚分-14、延长空位罚分-4作为参数。或者,可以使用合适的计算机程序,例如alignx、vector nti advance 10(来自invitrogen corporation)或gap程序(来自the university of wisconsin geneticcomputing group)来确定两个多肽之间的百分比序列同一性。应理解,同一性百分比是相对于其序列已比对的聚合物(例如,多肽或多核苷酸)计算的。片段和变体可以使用本领域众所周知的蛋白工程改造和定点诱变的方法制备(例如,参见molecular cloning:a laboratory manual,3rd edition,sambrook&russell,2001,cold spring harbor laboratory press,其公开内容通过引用并入本文)。可替代地或另外地,所述载体多肽为:(a)化脓性链球菌spyad(spy0269);或(b)化脓性链球菌spyad(spy0269)的变体、片段和/或融合体。可替代地或另外地,所述化脓性链球菌spyad(spy0269)包含以下或由以下组成:(i)seq id no:1或seq id no:2的氨基酸序列;(ii)与seq id no:1或seq id no:2相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:1或seq id no:2具有至少70%序列同一性、例如与seq idno:1或seq id no:2具有至少80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%同一性的氨基酸序列;和/或(iv)来自seq id no:1或seq id no:2的至少10个连续氨基酸、例如来自seq idno:1或seq id no:2的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340或350个连续氨基酸的片段。可替代地或另外地,所述载体多肽为:(a)化脓性链球菌spycep(spy0416);(b)化脓性链球菌spycep(spy0416)的变体、片段和/或融合体。可替代地或另外地,所述化脓性链球菌spycep(spy0416)包含以下或由以下组成:(i)seq id no:3或seq id no:4的氨基酸序列;(ii)与seq id no:3或seq id no:4相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:3或seq id no:4具有至少70%序列同一性、例如与seq idno:3或seq id no:4具有至少80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%同一性的氨基酸序列;和/或(iv)来自seq id no:3或seq id no:4的至少10个连续氨基酸、例如来自seq idno:3或seq id no:4的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、500、750、1000、1250、1500、1550、1600、1610、1620、1630、1640、1650或1660个连续氨基酸的片段。可替代地或另外地,所述载体多肽为:(a)化脓性链球菌slo(spy0167);或(b)化脓性链球菌slo(spy0167)的变体、片段和/或融合体。可替代地或另外地,所述化脓性链球菌slo(spy0167)包含以下或由以下组成:(i)seq id no:5或seq id no:6的氨基酸序列;(ii)与seq id no:5或seq id no:6相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:5或seq id no:6具有至少70%序列同一性、例如与seq idno:5或seq id no:6具有至少80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%同一性的氨基酸序列;和/或(iv)来自seq id no:5或seq id no:6的至少10个连续氨基酸、例如来自seq idno:5或seq id no:6的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、400、450、500、510、520、530、540、550、560或570个连续氨基酸的片段。可替代地或另外地,所述载体多肽为:(a)crm197;或(b)crm197的变体、片段和/或融合体。可替代地或另外地,所述crm197包含以下或由以下组成:(i)seq id no:7的氨基酸序列;(ii)与seq id no:7相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:7具有至少70%序列同一性、例如与seq id no:7具有至少80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%同一性的氨基酸序列;和/或(iv)来自seq id no:7的至少10个连续氨基酸、例如来自seq id no:7的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、400、450、500、510、520、530或535个连续氨基酸的片段。可替代地或另外地,所述一种或多种多糖是微生物多糖,诸如细菌多糖、古细菌多糖、真菌多糖或原生生物多糖。可替代地或另外地,所述微生物是病原体,例如人类病原体。可替代地或另外地,所述多糖来自哺乳动物细胞,例如癌细胞。在多糖来自哺乳动物癌细胞的情况下,优选多糖仅或主要由癌细胞表达。优选地,所述哺乳动物细胞是人类细胞。“主要表达”意指或包括(a)宿主非癌细胞上的多糖的表达(特别是当细胞完整时[例如,当细胞未凋亡时]以宿主抗体可接近的方式表达)比宿主肿瘤细胞上少至少50%w/w,例如,比宿主肿瘤细胞上少至少60%、70%、80%、90%、95%、98%、99%或至少99.9%(b)和/或多糖在至少50%或更少的宿主非癌细胞,例如至少60%、70%、80%、90%、95%、98%、99%或至少99.9%更少的宿主非癌细胞中表达。可替代地或另外地,所述一种或多种多糖是表面表达的。“一种或多种多糖是表面表达的”意指或包括多糖在其起源细胞的细胞表面上表达(例如,如果多糖是细菌来源的,则它由细菌在其细胞表面上表达),例如,以宿主抗体可接近的方式。可替代地或另外地,所述一种或多种多糖是细菌多糖,例如,选自以下的细菌的多糖(诸如荚膜多糖或脂多糖):放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。可替代地或另外地,所述一种或多种多糖包含以下或由以下组成:脱氧糖单体,例如,选自鼠李糖(6-脱氧-l-甘露糖)、墨角藻糖(fuculose)(6-脱氧-l-塔格糖)或岩藻糖(6-脱氧-l-半乳糖)的脱氧糖。可替代地或另外地,所述一种或多种多糖包含侧链,例如,包含n-乙酰葡糖胺(glcnac)或由其组成的侧链,然而,一种或多种多糖可替代地由无侧链的多糖(所谓的主链多糖)组成。“多糖”意指或包括由单糖残基组成的任何直链或支链聚合物,通常通过糖苷键连接,且因此包括寡糖。所述多糖可含有2至50个单糖单元,更优选6至30个单糖单元。多糖的片段意指与野生型多糖相比被截短的多糖(例如,与野生型多糖相比具有平均[均值]数量的单糖单元)。多糖截短可通过本领域中已知的任何合适的方法实现,诸如化学消化、具有比野生型更少的单糖单元的多糖的体外多糖合成或多糖产生菌株的遗传修饰。多糖的变体意指或包括多糖主链和/或侧链的一个或多个化学基团与野生型多糖相比被修饰。多糖修饰可以通过本领域中已知的任何合适的方式(诸如多糖产生菌株的化学反应或遗传修饰)实现。多糖的融合体意指或包括多糖、其片段或变体与一种或多种其他组分共价或离子键合或以其他方式融合。一种或多种其他组分可以是不同分子种类(例如,来自不同属、种或菌株)的多糖或其片段或变体。应理解,所述或每种载体蛋白可以具有与其缀合的单个或多个多糖。因此,可替代地或另外地,平均1、1.5、2、2.5、3、3.5、4、4.5、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20个多糖分子与所述载体多肽缀合。“平均x个多糖分子与载体多肽缀合”(其中x是1和15之间的数字)意指或包括平均(均值)x个多糖与所述或每个载体多肽缀合。在多个多糖与所述或每个载体蛋白缀合的情况下,应理解每个多糖可以是相同的种类,例如,以增加诱导的免疫应答的效力。另一方面,多糖种类的混合物可以与所述或每个载体蛋白缀合,例如,以增加诱导的免疫应答的效价(即,扩大物种/菌株覆盖范围或靶向单一物种/菌株上的多种抗原)。因此,可替代地或另外地,所述一种或多种多糖包含以下或由以下组成:i.单一分子种类;或ii.分子种类的混合物,例如,2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20种分子种类的混合物。“分子种类”意指或包括多糖,其包含以下或由以下组成:(a)化学相同的糖主链,(b)化学相同的糖主链和侧链,或(c)化学相同的糖主链、化学相同的侧链和相同的糖主链长度和侧链长度,(d)完全相同的多糖分子。“分子种类的混合物”意指或包括与载体多肽缀合的多糖包含至少两种不同的“分子种类”或由其组成。例如,不同的分子种类可能(a)具有化学不同的糖主链,(b)具有化学不同的糖主链和侧链,或(c)具有化学不同的糖主链、化学不同的侧链和不同的糖主链长度和侧链长度,(d)是完全不同的多糖分子。至少两种不同的分子种类可以以相等的比率与载体多肽缀合(例如,其中两种种类以1∶1的比率缀合,其中三种种类以1∶1∶1的比率缀合)。或者,一种或多种分子种类可以不等比率与载体多肽缀合,例如,在存在两种分子种类的情况下,比率为1.5∶1、2∶1、3∶1、4∶1、5∶1、6∶1、7∶1、8∶1、9∶1或10∶1,或在存在三种分子种类的情况下,比率为1.5∶1∶1、2∶1∶1、3∶1∶1、4∶1∶1、5∶1∶1、6∶1∶1、7∶1∶1、8∶1∶1、9∶1∶1或10∶1∶1。所述比率可能具有+/-5%、例如+/-4%、+/-3%、+/-2%、+/-1%、+/-0.5%、+/-0.25%或+/-0.1%的公差。在一个实施方案中,gac是第一分子种类。在一个替代实施方案中,gac是第二种或(如果存在)第三种分子种类。所述一种或多种多糖可以与所述载体蛋白直接缀合。可替代地或另外地,所述一种或多种多糖经由接头与所述载体蛋白缀合。可以使用任何合适的缀合反应,在必要时用任何合适的接头。多糖与载体多肽的连接优选经由-nh2基团,例如,通过载体多肽中的赖氨酸残基或精氨酸残基的侧链。在多糖具有游离醛基的情况下,该基团可以通过还原胺化与载体多肽中的胺反应以形成缀合物。也可以经由-sh基团连接至载体,例如通过载体多肽中半胱氨酸残基的侧链。或者,多糖可以经由接头分子连接至载体蛋白。多糖通常将在缀合前活化或官能化。活化可涉及例如氰化试剂诸如cdap(1-氰基-4-二甲基氨基四氟硼酸吡啶)。其他合适的技术使用碳二亚胺、酰肼、活性酯、降冰片烷、对硝基苯甲酸、n-羟基琥珀酰亚胺、s-nhs、edc、tstu(参见,例如,对wo98/42721的介绍)。与载体多肽的直接连接可以包含多糖的氧化和随后与载体多肽还原胺化,如描述于,例如,美国专利号4,761,283和美国专利号4,356,170。可以使用任何已知程序,例如美国专利号4,882,317和美国专利号4,695,624中所述的程序经由接头基团进行连接。通常,接头经由多糖的异头碳连接。连接的优选类型是己二酸接头,其可以通过以下形成:偶联游离-nh2基团(例如,通过胺化引入多糖)与己二酸(使用,例如,二酰亚胺活化),且然后将蛋白偶联至所得糖-己二酸中间体(参见,例如,ep-b-0477508、mol.immunol,(1985)22,907-919和ep-a-0208375)。连接的类似优选类型是戊二酸接头,其可以通过以相同的方式偶联游离-nh基团与戊二酸来形成。己二酸和戊二酸接头也可以通过直接偶联至多糖,即无需先前引入自由基(例如,游离的-nh基团)至多糖,随后将蛋白偶联至所得糖-己二酸/戊二酸中间体来形成。连接的另一种优选类型是羰基接头,其可以通过以下形成:使修饰多糖的游离羟基与cdi反应(bethell g.s.等人(1979)j biol chem 254,2572-4和hearn m.t.w.(1981)j.chromatogr 218,509-18);随后与蛋白反应以形成氨基甲酸酯连接。其他接头包括β-丙酰胺基(wo00/10599)、硝基苯基-乙胺(gever等人(1979)med microbiol immunol165,171-288)、卤代酰基卤化物(美国专利号4,057,685)、糖苷键(美国专利号4,673,574;4,761,283;和4,808,700)、6-氨基己酸(美国专利号4,459,286)、n-琥珀酰亚胺基-3-(2-吡啶基二硫代)-丙酸酯(spdp)(美国专利号5,204,098)、己二酸二酰肼(adh)(美国专利号4,965,338)、c4至c12部分(美国专利号4,663,160)等。还可以使用碳二亚胺缩合(wo2007/000343)。双官能接头可用于提供用于偶联至多糖中的胺基团的第一基团(例如,通过胺化引入至多糖)和用于偶联至载体(通常用于偶联至载体中的胺)的第二基团。或者,第一基团能够直接偶联至多糖,即,无需事先引入基团(例如胺基)至多糖。在一些实施方案中,双官能接头中的第一基团因此能够与多糖上的胺基(-nh2)反应。该反应通常涉及胺的氢的亲电取代。在其他实施方案中,双官能接头中的第一基团能够直接与多糖反应。在两组实施方案中,双官能接头中的第二基团通常能够与载体多肽上的胺基反应。该反应将再次通常涉及胺的亲电取代。在与多糖和载体蛋白两者的反应涉及胺的情况下,则优选使用双官能接头。例如,可以使用式x-l-x的同双官能接头,其中:两个x基团是彼此相同的,并且可以与胺反应;并且其中l是接头中的连接部分。类似地,可以使用式x-l-x的异双官能接头,其中:两个x基团是不同的,并且可以与胺反应;并且其中l是接头中的连接部分。优选的x基团是n-氧基琥珀酰亚胺。l优选具有式l′-l2-l′,其中l′是羰基。优选的l2基团是具有1-1 10个碳原子(例如c1、c2、c3、c4、c5、c6、c7、c8、c9、c10)的直链烷基,例如-(ch2)4-或-(ch2)3-。用于前述段落中所述的双官能接头中的其他x基团是当与ho-l-oh组合时形成酯的那些,诸如降冰片烷、对-硝基苯甲酸和磺基-n-羟基琥珀酰亚胺。用于本发明的进一步双官能接头包括丙烯酰卤化物(例如丙烯酰氯)和卤代酰基卤化物。特别有用的其他双官能接头选自:丙烯酰卤,优选丙烯酰氯、二琥珀酰亚胺基戊二酸酯、二琥珀酰亚胺基辛二酸酯和乙二醇双[琥珀酰亚胺基琥珀酸酯]。其他有用的接头选自:β-丙酰胺基、硝基苯基-乙基胺、卤代酰卤、糖苷衍生物键、6-氨基己酸。所述接头可以选自:n-羟基琥珀酰亚胺、n-氧基琥珀酰亚胺和n-羟基琥珀酰亚胺二酯(sidea)。当与载体蛋白和多糖的反应涉及不同的官能团时,应理解将使用能够与两种不同官能团选择性反应的异双官能接头。在这种情况下,优选的异双官能接头选自以下中的至少一种:琥珀酰亚胺基3-(2-吡啶基二硫基)丙酸酯(spdp)、琥珀酰亚胺基6-(3-[2-吡啶基二硫基]丙酰胺基)己酸酯(lc-spdp)、磺基琥珀酰亚胺基6-(3′-(2-吡啶基二硫基)丙酰胺基)己酸酯(磺基-lc-spdp)、4-琥珀酰亚胺基氧基羰基-α-甲基-α-(2-吡啶基二硫基)甲苯(smpt)、磺基琥珀酰亚胺基-6-[α-甲基-α-(2-吡啶基二硫基)甲苯酰胺基(tolueamideo)]己酸酯(磺基-lc-smpt)、琥珀酰亚胺基4-(n-马来酰亚胺甲基)环己烷-1-羧酸酯(smcc)、磺基琥珀酰亚胺基4-(n-马来酰亚胺甲基)环己烷-1-羧酸酯(磺基-smcc)、间-马来酰亚胺基苯甲酰基-n-羟基琥珀酰亚胺酯(mbs)、间-马来酰亚胺基苯甲酰基-n-羟基磺基琥珀酰亚胺酯(磺基-mbs)、n-琥珀酰亚胺基(4-碘乙酰基)氨基苯甲酸酯(siab)、磺基琥珀酰亚胺基(4-碘乙酰基)氨基苯甲酸酯(磺基-siab)、琥珀酰亚胺基4-(n-马来酰亚胺基苯基)丁酸酯(smpb)、磺基琥珀酰亚胺基4-(n-马来酰亚胺基苯基)丁酸酯(磺基-smpb)、n-γ-马来酰亚胺基丁酰基-氧基琥珀酰亚胺酯(gmbs)、n-γ-马来酰亚胺丁酰基-氧基磺基琥珀酰亚胺酯(磺基-gmbs)、琥珀酰亚胺基-6-((((4-(碘乙酰基)氨基)甲基)环己烷-1-羰基)氨基)己酸酯(siacx)、琥珀酰亚胺基6[6-(((碘乙酰基))氨基)己酰基)氨基]己酸酯(siaxx)、琥珀酰亚胺基-4-(((碘乙酰基)氨基)甲基)环己烷-1-羧酸酯(siac)和琥珀酰亚胺基6-[(碘乙酰基)氨基]己酸酯(siax)和对硝基苯基碘乙酸酯(npia)。在偶联至多糖的过程中,接头通常以摩尔过量添加至多糖。缀合物可以具有过量的载体(w/w)或过量的多糖(w/w),例如,比率范围为1∶5至5∶1。具有过量载体蛋白的缀合物是典型的,例如,在0.2∶1至0.9∶1的范围内,或相等的重量。所述缀合物可包括少量游离(即未缀合的)载体。当给定的载体蛋白以游离和缀合形式存在于本发明的组合物中时,非缀合形式优选不超过整个组合物中载体蛋白总量的5%,且更优选以小于2%(按重量计)存在。所述组合物还可以包含作为免疫原的游离载体蛋白(wo96/40242)。在缀合后,可分离游离和缀合的多糖。存在许多合适的方法,例如疏水层析、切向超滤、渗滤等。(还参见lei等人(2000)dev biol(basel)103:259-264and wo00/3871 1)。切向流超滤是优选的。蛋白-多糖缀合物优选溶解在水和/或生理缓冲液中。对于一些多糖,如果多糖和载体蛋白之间存在间隔基,则免疫原性可以得到改善。在这种背景下,“间隔基”是比单一共价键更长的部分。该间隔基可以是如上所述的接头。或者,它可以是多糖和接头之间共价键合的部分。通常,该部分在偶联至接头或载体之前将被共价键合至多糖。例如,间隔基可以是部分y,其中y包含具有1至10个碳原子(例如,c1、c2、c3、c4、c5、c6、c7、c8、c9、c10)、通常1至6个碳原子(例如,c1、c2、c3、c4、c5、c6)的直链烷基。本发明人已经发现,具有6个碳原子的直链烷基(即,-(ch2)6)是特别合适的,并且可以提供比更短链(例如,-(ch2)2)更大的免疫原性。通常,y连接至多糖的异头碳,通常经由-o-键。然而,y可以连接至多糖的其他部分和/或经由其他键。y的另一端通过任何合适的连接键合至接头。通常,y用胺基终止,以便于连接至如上所述的双官能接头。在这些实施方案中,y因此通过-nh-键键合至接头。应理解,一种或多种多糖可具有多种分子量,然而,可替代地或另外地,一种或多种多糖具有小于100kda(例如小于80、70、60、50、40、30、25、20、15、14、13、12、11、10、9、8、7、6、5、4、3、2或1kda)的分子量或平均分子量。在一个实施方案中,一种或多种多糖中的至少一种具有7kda的分子量或平均分子量。“平均分子量”意指或包括与载体多肽缀合的给定分子种类的所有多糖的平均(均值)分子量对应于给定值。同样,一种或多种多糖可以具有多种分子量,例如,可替代地或另外地,一种或多种多糖具有1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30个或更少的单糖单元。“x个或更少的单糖单元”(其中x代表1和30之间的数字)意指或包括与所述或每个载体多肽缀合的一种或多种指定多糖的单糖单元的平均(均值)数是x。如所提及,一种或多种多糖可以是细菌多糖,诸如脂多糖(lps)或荚膜多糖(cps)。可替代地或另外地,在一种或多种多糖包含细菌的荚膜多糖或由其组成的情况下,其选自:流感嗜血杆菌b型或a型;脑膜炎奈瑟氏菌血清群a、c、w135、x和y;肺炎链球菌血清型1、2、3、4、5、6a、6b、7f、8、9n、9v、10a、11a、12f、14、15b、17f、18c、19a、19f、20、22f、23f和33f;沙门氏菌,包括肠沙门氏菌伤寒血清型(salmonella enterica serovar typhi)vi,全长或片段化的(表示为fvi);志贺氏菌属,a群和b群链球菌(分别为gas和gbs)。优选地,所述一种或多种多糖是a群碳水化合物(gac)。可替代地或另外地,可通过本领域中已知的任何合适的方法将多糖与载体蛋白缀合。可替代地或另外地,所述一种或多种多糖通过如下与所述载体蛋白缀合:(a)由所述多糖链的多糖链的末端残基的醛或酮基的还原端残基和所述载体蛋白的赖氨酸形成的胺;和/或(b)由所述多糖的氧化主链和/或侧链(例如,对于gac,glcnac侧链的邻位二醇(1,2-二醇))和所述载体蛋白的赖氨酸形成的一个或多个醛基。“还原残基”意指或包括醛基或酮基,特别是多糖链的末端糖的醛基或酮基(例如,o-抗原链的末端3-脱氧-d-甘露糖-辛-2-酮糖酸[kdo])。可替代地或另外地,所述多糖缀合物进一步包含佐剂,例如,氢氧化铝、alhydrogel(氢氧化铝2%湿凝胶悬浮液,croda international plc)和alum-tlr7。本发明的组合物中可以使用的佐剂包括但不限于不溶性金属盐,水包油乳剂(例如mf59或as03,两者均含有角鲨烯),皂苷,lps的无毒衍生物(诸如单磷酰脂质a或3-o-脱酰化mpl),免疫刺激性寡核苷酸,脱毒的细菌adp-核糖基化毒素,微粒,脂质体,咪唑并喹诺酮类(imidazoquinolones),或其混合物。充当免疫刺激剂的其他物质公开于例如watson,pediatr.infect.dis.j.(2000)19:331-332。使用氢氧化铝和/或磷酸铝佐剂是特别优选的。这些盐包括羟基氧化物和羟基磷酸盐。所述盐可采取任何合适的形式(例如,凝胶、晶体、无定形等)。可替代地或另外地,所述多糖缀合物包含以下或由以下组成:i.所述载体多肽包含根据seq id no:1的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。可替代地或另外地,所述多糖缀合物包含以下或由以下组成:i.所述载体多肽包含根据seq id no:3的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。可替代地或另外地,所述多糖缀合物包含以下或由以下组成:i.所述载体多肽包含根据seq id no:5的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。可替代地或另外地,所述多糖缀合物包含以下或由以下组成:i.所述载体多肽包含根据seq id no:7(crm197)的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。可替代地或另外地,gac∶crm197比率可以是0.1∶1、0.2∶1、0.5∶1、0.7∶10.9∶1、1∶11∶0.9、1∶0.7、1∶0.5、1∶0.2或1∶0.1。本发明的多糖缀合物可用作免疫原性组合物中的活性成分(免疫原),并且此类组合物可用作疫苗。根据本发明的疫苗可以是预防性的(即预防感染)和/或治疗性的(即治疗感染)。可替代地或另外地,本发明的多糖缀合物的载体多肽不是crm197或其变体、片段或融合体。可替代地或另外地,所述多糖缀合物诱导和/或能够诱导的抗多糖免疫应答与具有crm197作为载体多肽的其他方面等同的多糖缀合物的量级至少相同。抗多糖免疫应答的量级可以通过本领域已知的任何合适的方法测量,但在一个实施方案中,使用elisa(例如,如以下实施例部分中所述,和具体而言,其中的材料和方法中所述)测量。可替代地或另外地,所述多糖缀合物诱导和/或能够诱导抗多糖免疫应答的量级是具有crm197作为载体多肽的其他方面等同的多糖缀合物的量级的至少50%,例如至少60%、70%、80%、90%、95%、96%、97%、98%、99%或至少100%。可替代地或另外地,所述多糖缀合物诱导和/或能够诱导保护性免疫的量级与具有crm197作为载体多肽的其他方面等同的多糖缀合物的量级至少相同,例如至少100%、90%、80%、70%、60%、50%、40%、30%或至少20%。可以使用本领域中任何合适的方法确定保护性免疫,例如小鼠模型(例如,如以下实施例部分中所述,和具体而言其中的材料和方法,例如部分4.6和4.7)。可替代地或另外地,所述多糖缀合物诱导和/或能够诱导的抗载体多肽免疫应答的量级是未与多糖缀合的其他方面等同的多肽的量级的至少50%,例如至少60%、70%、80%、90%、95%、96%、97%、98%、99%或至少100%。抗载体多肽免疫应答的量级可以通过本领域中已知的任何合适的方法测量,但在一个实施方案中,使用elisa测量(例如,如以下实施例部分中所述,和具体而言其中的材料和方法)。可替代地或另外地,所述多糖缀合物诱导和/或能够诱导的保护性免疫的量级比未与多糖缀合的其他多肽更大或相同,例如,至少200%、175%、150%、140%、130%、120%、110%、100%、90%、80%、70%、60%、50%、40%、30%或至少20%。保护性免疫可以使用本领域中任何合适的方法确定,例如小鼠模型(例如,如以下实施例部分中所述,和具体而言其中的材料和方法、例如部分4.6和4.7)。因此,本发明的第二个方面提供了包含第一个方面的多糖缀合物的疫苗。免疫原性组合物将是药学上可接受的。它们将通常包括除了所述抗原以外的组分,例如它们通常包括一种或多种药物载体、赋形剂和/或佐剂。对载体和赋形剂的充分讨论可见于current protocols in molecular biology(f.m.ausubel等人,编,1987)supplement 30,其通过引用并入本文。对疫苗佐剂的充分讨论可见于vaccine design:thesubunit and adjuvant approach(powell&newman编)plenum press 1995(isbn 0-306-44867-x);和vaccine adjuvants:preparation methods and research protocols(volume 42 of methods in molecular medicine series),isbn:1-59259-083-7.ed.o′hagan,其通过引用并入本文。组合物将通常以水性形式施用于哺乳动物。然而,在施用前,该组合物可能已经呈非水形式。例如,尽管一些疫苗以水性形式制备,然后也以水性形式填装和分布和施用,但其他疫苗在制备过程中冻干,并在使用时重构成水性形式。因此,本发明的组合物可以干燥,诸如冻干制剂。该组合物可包括防腐剂,诸如硫柳汞或2-苯氧乙醇。然而,优选的是,疫苗应当基本不含(即少于5μg/ml)含汞物质,例如不含硫柳汞。更优选不合汞的疫苗。特别优选不含防腐剂的疫苗。为了改善热稳定性,组合物可包括温度保护剂。为了控制涨度,优选包括生理盐,诸如钠盐。优选氯化钠(nacl),其可以以1至20mg/ml,例如约10±2mg/ml nacl存在。可存在的其他盐包括氯化钾、磷酸二氢钾、无水磷酸氢二钠、氯化镁、氯化钙等。组合物将通常具有200mosm/kg至400mosm/kg,优选240-360mosm/kg的摩尔渗透压浓度(osmolality),且将更优选落在290-310mosm/kg的范围内。组合物可包括一种或多种缓冲剂。典型的缓冲剂包括:磷酸盐缓冲剂;tris缓冲剂;硼酸盐缓冲剂;琥珀酸盐缓冲剂;组氨酸缓冲剂(特别是具有氢氧化铝佐剂);或柠檬酸盐缓冲剂。缓冲剂通常将包括在5-20mm范围内。组合物的ph将通常为5.0至8.1,且更通常6.0至8.0,例如6.5至7.5,或7.0至7.8。该组合物优选是无菌的。该组合物优选无热原,例如每剂含有<1eu(内毒素单位,标准量度),且优选每剂<0.1eu。该组合物优选不含谷蛋白。所述组合物可包括用于单次免疫的材料,或者可包括用于多次免疫的材料(即“多剂量”药剂盒)。多剂量配置优选包括防腐剂。作为多剂量组合物中包括防腐剂的替代方案(或除此以外),所述组合物可包含在具有用于移取材料的无菌接头的容器中。人疫苗通常以约0.5ml的剂量体积施用,尽管可将一半剂量(即约0.25ml)施用于儿重。本发明的免疫原性组合物还可以包含一种或多种免疫调节剂。优选地,一种或多种免疫调节剂包括一种或多种佐剂。可替代地或另外地,所述疫苗包含佐剂(例如,关于第一个方面所述的佐剂)。或者,所述疫苗包含一种或多种额外的多肽和/或多糖抗原,例如,选自以下的抗原的细菌抗原:放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。可替代地或另外地,所述疫苗包含未缀合的载体蛋白。所述未缀合的载体蛋白可以小于或等于缀合的载体蛋白的50%w/w、例如小于或等于40%、30%、20%、10%、5%、1%、0.1%、0.01%或小于或等于0.01%存在。可替代地或另外地,所述疫苗包含免疫有效量的未缀合的载体蛋白。因此,本发明的第三个方面提供了第一个方面的多糖缀合物或第二个方面的疫苗,其用于药物中。本发明的第四个方面提供了第一个方面的多糖缀合物或第二个方面的疫苗,其用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。本发明的第五个方面提供了第一个方面的多糖缀合物或第二个方面的疫苗,其用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。本发明的第六个方面提供了第一个方面的多糖缀合物或第二个方面的疫苗,其用于制备药物,所述药物用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。本发明的第七个方面提供了在哺乳动物中产生免疫应答的方法,所述方法包括以下或由以下组成:向所述哺乳动物施用有效量的第一个方面的多糖缀合物或第二个方面的疫苗。可替代地或另外地,在本发明的第三个至第七个方面中治疗或预防的疾病是选自以下的一种或多种细菌的感染和/或其症状:放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。具体而言,本发明的第三个至第七个方面中治疗或预防的疾病是化脓性链球菌(即,a群链球菌)的感染和/或其症状。本发明的第八个方面提供了氧化多糖的方法,其包括以下步骤:i.通过如下氧化多糖:i.使多糖,例如,浓度为0.1-100mg/ml,例如,0.5-50、0.5-25、1-10、2.5-7.5、4-6或5mg/ml的多糖,与ii浓度为0.5-10m的氧化剂(例如,naio4[高碘酸钠+、kmno4[高锰酸钾]、高碘酸[hio4]或四乙酸铅[pb(oac)4]),iii.在合适的缓冲液(例如,磷酸盐缓冲液或硼酸盐缓冲液)ph 3-9,例如,ph 5-8(例如,ph 5或ph 8)中,iv.在合适的温度(例如,20-30℃,诸如25℃)下,v.反应合适的时间(例如,15min-5hr,诸如,30min-3hr、30min-1hr或30min);ii.(任选地)通过如下淬灭残余的naio4:vi.添加合适量的还原剂,例如,na2so3(亚硫酸钠),例如相对于步骤i(ii)中naio4的浓度摩尔过量,例如步骤i(ii)中的naio4浓度的5-10倍,或16mm,vii.在合适的温度(例如,20-30℃、室温或25℃)下,viii.持续合适的时间(例如,10-30min或15min);iii.(任选地)纯化和/或浓缩氧化多糖,例如,使用选自冻干、离心蒸发、旋转蒸发和切向流过滤的方法。本发明的第九个方面提供了缀合氧化的多糖的方法,其包括以下步骤:a.a.使浓度为5-75mg/ml(例如,10-60mg/ml、20-50mg/ml或40mg/ml)的氧化的多糖(例如,第八个方面的氧化的多糖)与;b.浓度为5-75mg/ml(例如40mg/ml)的蛋白;和c.浓度为0.5-10.0mg/ml的nabh3cn(氰基硼氢化钠);d.在ph 7-9、例如ph 7.5-8.5、ph8的硼酸盐缓冲液或磷酸盐缓冲液中;e.在合适的温度(例如,17.5-42.5℃、室温、25℃、30℃或37℃)下,f.反应合适的时间(例如,1小时、2小时、4小时、6小时、0.5至3天、1天或2天;b.(任选地)通过如下淬灭氧化的多糖的残余醛:a.添加合适量的nabh4(例如,nabh4∶多糖比[w/w]为0.5∶1,或例如相对于生成的醛基或氧化的多糖的摩尔数摩尔过量,例如,5-10倍、50倍、100倍或1000倍),b.在合适的温度(例如,20-30℃、25℃或室温)下,c.持续合适的时间(例如,1至12小时、2-4小时、3小时或2小时)。c.(任选地)通过切向流过滤(tff)和/或无菌过滤(例如,tff,随后无菌过滤)纯化由步骤(b)产生的多糖缀合物。可替代地或另外地,缀合产率比传统的末端还原胺化方法(即,kabanova等人[12]的方法和本材料和方法部分的部分4.2中描述的方法)高至少5%,例如,比传统的末端还原胺化方法高至少10%、15%、20%、25%、30%、35%、40%、45%、50%、60%、70%、80%、90%、100%、150%或200%。产率可通过本领域已知的任何合适的方法计算,但优选使用本文实施例部分中描述的方法计算。可替代地或另外地,上述方法中的任一种被配置为实现所述多糖的至少5%、至少10%、至少15%、10%和30%之间、10%和25%之间或约15%的氧化。可替代地或另外地,上述方法中任一种中使用的多糖浓度、氧化剂、氧化剂浓度、合适的缓冲液、合适的温度和合适的时间中的至少一种可以确保所述方法实现所述多糖的至少5%、至少10%、至少15%、10%和30%之间、10%和25%之间或约15%的氧化。实施例中描述了确定是否已实现氧化水平的方法,以及实现不同氧化水平的合适条件。可替代地或另外地,当多糖是gac时,上述方法中的任一种可以被配置为实现期望量的gac回收率。在氧化的情况下,gac回收率是指在gac经历氧化过程后回收的氧化gac的量。因此,作为百分比的gac回收率可以显示为(氧化的)gac的最终量除以gac的起始量,乘以100。上述氧化方法中的任一种可以被配置为实现至少60%、至少65%、至少70%、至少75%、60%和100%之间、65%和100%之间、70%和90%之间或75%和90%之间的gac回收率。所述方法中使用的多糖浓度、氧化剂、氧化剂浓度、合适的缓冲液、合适的温度和合适的时间中的至少一种可以确保所述方法实现至少60%、至少65%、至少70%、至少75%、60%和100%之间、65%和100%之间、70%和90%之间或75%和90%之间的gac回收率。在缀合的情况下,gac回收率是指在gac经历缀合过程后回收的缀合gac的量。因此,作为百分比的gac回收率可以显示为缀合gac的最终量除以(氧化的)gac的起始量,乘以100。上述缀合方法中的任一种可以被配置为实现至少25%、至少30%、至少35%、25%和80%之间、30%和70%之间或35%和60%之间的gac回收率。所述方法中使用的氧化多糖浓度、载体多肽/蛋白浓度、氰基硼氢化钠浓度、硼酸盐缓冲液的ph和合适的温度中的至少一种可以确保所述方法实现至少25%、至少30%、至少35%、25%和80%之间、30%和70%之间或35%和60%之间的gac回收率。实施例中描述了确定是否已实现特定gac回收百分比的方法,以及实现特定gac回收百分比的合适方式。本发明的第十个方面提供了将多糖与多肽缀合的方法,其包括本发明的第八个和第九个方面的方法。可替代地或另外地,所述多糖是本发明的第一个方面中描述的多糖,例如gac。可替代地或另外地,所述蛋白是第一个方面中所述的蛋白,例如,spyad(例如,seqid no:1或seq id no:2)、spycep(例如,seq id no:3或seq id no:4)、slo(例如,seq idno:5或seq id no:6)或crm197(例如,seq id no:7)。可替代地或另外地,方法产物是本发明的第一个方面中所述的多糖缀合物,例如:i.与gac缀合的spyad(例如,seq id no:1或seq id no:2);ii.与gac缀合的spycep(例如,seq id no:3或seq id no:4);iii.与gac缀合的slo(例如,seq id no:5或seq id no:6);或iv.与gac缀合的crm197(例如,seq id no:7)。可替代地或另外地,反应在所述多肽的tm以下、例如比所述多肽的tm低至少0.5、1.0、1.5、2.0、2.5、3.0、4.0、5.0、6.0、7.0或7.5℃进行。本发明的第十一个方面提供了根据本发明的第十个方面的方法产生的多糖缀合物。现在将参考以下附图描述体现本发明的某些方面的优选的非限制性实例。图1.用于产生gac缀合物的缀合策略:gac的还原残基上的醛基和载体蛋白的赖氨酸之间的选择性直接还原胺化(“选择性缀合”方法)[12]以及通过gac的氧化随机产生的醛基和载体蛋白的赖氨酸之间的还原胺化(“随机缀合”方法)。图2.(a)通过缀合混合物的sds-page分析(7%tris-乙酸凝胶)的表征(与未缀合的crm197比较)。每孔加载10μg缀合蛋白和2μg未缀合crm197。泳道1:标记,泳道2:crm197,泳道3:选择性gac-crm197,泳道4:随机gacox-crm197。(b)选择性gac-crm197缀合混合物、随机gacox-crm197缀合混合物和未缀合的crm197的hplc-sec概况(荧光发射检测),将80μl样品注入tsk凝胶g3000pwxl柱上;0.1m nacl 0.1m nah2po45%ch3cn ph7.2,0.5ml/min。vtot 23.326分钟,v0 10.663分钟。图3.当通过不同的化学法与crm197缀合时gac的免疫原性。在第0天和第28天,用以2mg/ml alhydrogel配制的4μg/gac剂量,对cd1小鼠进行i.p.免疫。报告了抗gac特异性igg几何平均单位(条)和个体抗体水平(点)的总结图(gac-hsa用作包被抗原)。进行mann-whitney双尾检验以比较两个免疫组诱导的应答(p>0.05),而进行wilcoxon检验以比较每组在第27天和第42天的应答(*p<0.05)。图4.与未缀合的gac相比,gacox-crm197、gacox-slo、gacox-spyad、gacox-spycep缀合物的hplc-sec概况(折光率检测)。将80μl样品注入tsk凝胶g3000 pwxl柱上;0.1mnacl 0.1m nah2po45%ch3cn ph 7.2,0.5ml/min。vtot 23.326分钟,v0 10.663分钟。图5.gac当与crm197或gas蛋白slo、spyad和spycep缀合时的免疫原性。在第0天和第28天,用1.5μg/gac剂量或用相应剂量的单独的载体蛋白(全部用2mg/ml alhydrogel配制),对cd1小鼠进行i.p.免疫。使用gac-has(a)或slo、spyad和spycep(b)作为包被抗原通过elisa分析血清。报告了抗抗原特异性igg几何平均单位(条)和个体抗体水平(点)的总结图。在图(a)中的4组间进行kruskal-wallis检验,在图(a)中在第27天和第42天的应答之间进行wilcoxon检验(p>0.05)并且在图(b)中用单独的蛋白或gacox-蛋白缀合物免疫的每个组之间进行mann-whitney双尾检验(*p<0.05,**p<0.01,***p<0.001)。在溶血抑制测定(c)和il-8切割抑制测定(d)中测试血清,以分别评估它们阻断天然slo和spycep活性的能力。对于每个免疫组的免疫前血清、标准血清和一个选定的第42天血清,报告了在每个测试的血清稀释度下观察到的兔红血细胞释放的血红蛋白(c)和未切割的il-8(d)的量。在facs(e)中测试第42天的合并血清,以评估它们结合gas细菌细胞的能力。细菌与不同血清孵育后,使用apc-缀合的抗小鼠igg二抗用于检测。与免疫前血清相比,报告了每种血清测量的平均荧光强度(mfi)。图6.(a)未缀合的slo vs gacox-slo和(b)未缀合的spyad vs gacox-spyad的dsc热分析图。gas蛋白和相应的缀合物在ph 7.2的磷酸盐缓冲液中进行分析,对于slo为3μm的相同摩尔浓度,且对于spyad为2μm的相同摩尔浓度。每个热分析图的δh值(来自积分的曲线下面积)为:slo:1.3e5kcal/mol;gacox-slo:nd;spyad:3.7e5kcal/mol;gacox-spyad:2.4e5kcal/mol。图7.gac氧化的最佳条件的鉴定:%glcnac氧化反应的3d表面模型图。2.4(a)、5.3(b)、8.0(c)的nao4浓度下ph和gac浓度之间的相关性。图8.gacox与crm197缀合的最佳条件的鉴定:gac/crm197w/w比率(a-c)和gac产率(d-f)响应的3d表面模型图。10(a,d)、25(b,e)和40(c,f)的nabh3cn浓度下crm197和gac浓度之间的相关性。图9.方案1.gac至crm197优化缀合工艺的流程图。图10(图s1).通过不同的化学法与crm197缀合时gac的免疫原性。在第0天和第28天,用以2mg/ml alhydrogel配制的4μg gac/剂量,对cd1小鼠进行i.p.免疫。报告了抗crm197特异性igg几何平均单位(条)和个体抗体水平(点)的总结图(crm197用作包被抗原)。进行mann-whitney双尾检验以比较两个免疫组诱导的应答(p>0.05)。图11(图s2).通过缀合混合物(与相应的未缀合蛋白相比)的sds-page分析(对于gas蛋白缀合物,3-8%tris-乙酸凝胶,对于crm197缀合物,7%tris-乙酸凝胶)的表征。每孔加载10μg缀合物和2μg未缀合的蛋白。泳道1:标记,泳道2:slo;泳道3:slo缀合物;泳道4:spyad;泳道5:spyad缀合物;泳道6:spycep;泳道7:spycep缀合物;泳道8:crm197,泳道9:crm197缀合物。实施例引言目前还没有针对a群链球菌(gas)(咽炎和脓疱病的主要原因,在低收入和中等收入国家中具有高频率的严重后遗症)的商业疫苗。与适当的载体蛋白缀合的a群碳水化合物(gac)已被提议作为有吸引力的疫苗候选物。在这里,我们探讨了使用具有抗原和载体的双重作用的gas链球菌溶血素o(slo)、spycep和spyad蛋白抗原来增强最终疫苗的效力并降低其复杂性的可能性。所有蛋白抗原都产生用于gac的良好载体,在小鼠中诱导了针对更传统的crm197缀合物的类似抗gac igg应答。然而,与多糖的缀合对抗蛋白应答具有负面影响,特别是在通过spycep的il-8切割测定和slo的溶血测定所评估的功能方面。在选择crm197作为载体后,通过实验设计方法鉴定了其与gac缀合的最佳条件,提高了工艺稳健性和产率。该工作支持开发针对gas的疫苗,并显示新型的统计工具和缀合领域的最新进展可以导致糖缀合物疫苗的设计。2.结果2.1.测试gac与crm197的连接的随机和选择性缀合化学法比较gac与crm197缀合的两种不同方法,所述crm197是糖缀合物疫苗中使用的最广泛和成功的载体蛋白之一[21]。gac的还原残基处的醛基和载体蛋白的赖氨酸之间的选择性直接还原胺化[12]产生缀合物,其特征在于gac与crm197w/w比率为0.18,对应于每个载体分子平均有1.5条gac链。当我们产生通过使用相同的缀合条件进行额外的缀合批次,批次间存在很大的不一致性,其中gac与crm197的比率范围在0.01和0.18之间。此外,在一些情况下,验证没有缀合物形成。测试一种替代随机方法,其仍然依赖于还原胺化化学法。具体而言,引入用高碘酸钠随机gac氧化的步骤,其沿着多糖链产生额外的醛基。氧化发生在gac的glcnac侧链的邻位二醇处。用与用于连接gac的相同条件经由其还原端(gac浓度为10mg/ml,gac与crm197与nabh3cn w/w/w比率为4∶1∶2,200mm磷酸盐缓冲液,ph 8,在37℃2天)进行氧化gac的还原胺化,产生gac与crm197w/w比率为0.2的缀合物,类似于选择性缀合物的比率。两种缀合方案报告于图1中。如所预期,随机和选择性缀合物通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sds-page)分析显示不同的蛋白模式:对于选择性方法,在递增分子量(mw)处存在单一条带,对应于递增数量的与crm197连接的gac链,相比之下,对于随机缀合物,在非常高mw处存在多分散弥散条带(图2(a))。高效液相色谱-大小排阻色谱(hplc-sec)也证实了缀合物形成(图2(b))。两种缀合物的概况与sds-page模式差异显著。事实上,与预期不同,与选择性缀合物相比,随机缀合物在略微更高的保留时间处显示主峰。实际上,hplc-sec估计的表观分子量可以反映两种构建体的不同结构。hplc-sec分析也证实两种缀合混合物中不存在游离crm197。在sephacryl s-100hr柱上通过大小排阻色谱除去残余的未缀合的gac。两种缀合物在纯化后的总gac回收率为近似5%。在小鼠中比较经由随机和选择性方法产生的两种缀合物,以检查gac与蛋白的随机连接是否对诱导的免疫应答产生负面影响。两种缀合物在第一次免疫后4周没有诱导显著不同的抗gac igg应答,在第二次剂量后2周用类似的加强剂(p<0.05)(图3)。还诱导了类似的抗crm197 igg应答(图s1)。2.2.应用随机化学法将gac与gas蛋白连接为了增加gac回收率,略微修改还原胺化步骤条件(gac浓度从10mg/ml增加至40mg/ml,gac与crm197与nabh3cn w/w/w比率为4∶1∶2,ph 8的硼酸盐缓冲液代替磷酸盐[23],在37℃2天),产生缀合物,gac/crm197w/w比率从0.2增加至0.86,且gac产率从5%增加至21.5%。应用相同的条件将gac与gas slo、spyad和spycep蛋白抗原连接。然而,因为这些蛋白的差示扫描量热法(dsc)的熔解温度(tm)接近37℃(slo的tm为39.35℃,spyad的tm为44.37℃,spycep的tm为40.03℃),因此反应在25℃而不是37℃进行,试图保持gas蛋白折叠,并可能保留最终缀合物中的功能。通过sds-page证实所有缀合物的缀合物形成,还揭示不存在游离蛋白(图s2)。通过amicon 30kda截止值的纯化成功地将所有缀合物的游离gac水平降低至<10%(图4(b)),如通过hplc-sec(折光率检测)所验证(图4),也证实了缀合物形成。缀合物的特征在于相似的gac/蛋白摩尔比,高于slo(表1)。表1.纯化的gac与crm197和gas蛋白的缀合物的主要特征。当在小鼠中进行比较时,与gac-crm197相比,具有gas蛋白抗原的缀合物在第一次注射后4周和第二次注射后2周均诱导相同的抗gac igg应答,显示测试的所有gas蛋白都是gac的良好载体。所有缀合物在再次注射后都能够引发加强应答(图5(a))。重要的是,gac与测试的载体蛋白之一的物理混合物没有产生显著的抗gac igg应答,证实所述载体蛋白在诱导t-细胞活化和同种型转换中的作用。用在第二次注射后2周从每个免疫组收集的合并血清进行针对gas细菌细胞的流式细胞术分析(facs)(图5(e))。所有缀合物诱导的抗体都能够类似地结合细菌细胞。与相应的缀合物相比,未缀合的gas蛋白诱导的血清结合gas细菌的程度较低。然而,当gas蛋白用作载体时,如果与用相同剂量的未缀合蛋白进行免疫相比,抗蛋白特异性总igg减少(图5(b))。当分析血清功能时,gac与gas蛋白缀合的影响是显而易见的。gac的缀合完全消除了slo和spycep引发抗体的能力,所述抗体能够分别阻断天然slo溶血活性(图5(c))和天然spycep蛋白酶活性(图5(d))。通过dsc分析,验证缀合对slo和spyad折叠的强烈影响,可能与所证明的功能丧失相关。对于slo,折叠在缀合后根本没有保留,而对于spyad,观察到焓变(δh)减少(图6)。因此,基于获得的结果,crm197被选为gac的最佳载体,并通过doe方法进一步优化缀合工艺,主要目的是使gac产量最大化并确保工艺的稳健性。2.3.通过doe方法优化随机化学法2.3.1.鉴定gac氧化的最佳条件在进行一些初步实验后,进行第一doe以理解哪些参数可能影响gac氧化步骤,目的在于鉴定它们的最佳组合以获得有效缀合的最佳氧化程度,防止对gac结构完整性的重大影响。使用全因子、响应面设计,其中α为1.68179(可旋转),具有1个轴和因子点重复以及6个中心点重复。1-10mg/ml范围内的gac浓度、5-8范围内的ph和0.5-10mm范围内的naio4浓度是评估的因素。反应时间和温度分别设定为30分钟和25℃。用于氧化的条件和结果概述于表s1中。在所有反应条件下都获得类似的gac回收率。我们还验证了对多糖链长度没有影响,如对于glcnac所预期的一样,所述glcnac是受氧化影响的糖,位于侧链而不是gac的骨架中。在测试的设计空间中,%glcnac氧化在8.5-19.4%的范围内,意味着每条ps链平均最多3个重复单元被氧化(考虑到每条gac链平均有14个重复单元)。为了详细说明数据,选择具有二次模型的响应面,并用反向消除过程,从模型中去除非显著项(p-值>0.05)(表s3中的统计分析)。残差(外部学生化)是正态分布的(anderson-darling正态性检验,p=0.837),并且模型的调整后r2为0.71。glcnac氧化反应受所有研究因素的影响,并且主要受naio4浓度的影响(p=0.0003)(图7)。从模型中,我们实现了15%的氧化目标。在ph8下工作,允许用na2so3淬灭过量的naio4,随后无需gacox中间体纯化即可缀合。通过将ph固定在8,可以通过用8mm naio4达到目标氧化水平,完全独立于所研究范围内的gac浓度。2.3.2.鉴定gac与crm197缀合的最佳条件在已经鉴定gac氧化的最佳条件后,使用doe方法来理解哪些参数对缀合步骤至关重要,并鉴定它们的最佳组合以使gac产量最大化,确保工艺的稳健性。使用全因子、响应面设计,其中α为1.0(以面为中心),具有1个轴和因子点重复以及6个中心点重复。gacox、crm197和nabh3cn浓度是评估的因素,所有都在10-40mg/ml的范围内进行测试。在硼酸盐缓冲液中,反应时间、温度和ph分别设置为2天、25℃和ph 8。用于缀合测试的条件和获得的结果概述于表s2中。未缀合的crm197仅在进行的20项测试中的3项中>10%,并且在其中15项中不存在,如根据hplc-sec分析所计算。在测试的设计空间中,gac/crm197 w/w比率在0.12-0.65的范围内,而gac回收率范围为9.2至41.9%,如通过阴离子交换色谱法结合脉冲安培检测(hpaec-pad)所计算。为了详细说明数据,对于gac/crm197 w/w比率和gac产量,选择具有线性模型的响应面。使用向后消除过程从模型中去除非显著项(p-值>0.05)(表s4中的统计分析)。两个模型的残差(外部学生化)是正态分布的。正态性是通过anderson-darling检验计算(对于gac/crm197 w/w比率,p=0.166,且对于gac产量,p=0.676),并且模型导致gac与蛋白比率和gac回收率的调整-r2分别为0.87和0.83.对于评估的两种响应,doe中研究的所有因素都影响响应(图8)。有趣的是,gac/crm197 w/w比率和gac回收率通过降低nabh3cn浓度而增加。基于结果,进行优化,所有因素都在范围内,使gac回收的%最大化,其重要性高于gac/crm197 w/w比率最大化。鉴定的最佳条件、连同预测的响应和通过在鉴定的反应条件下进行缀合获得的实际结果报告于表2中。获得的结果与预期的那些一致,证实工艺的一致性,因为获得的所有响应均在平均值的95%置信区间(c1)内。表2.gacox-crm缀合的优化条件和模型的预测响应,通过进行额外的缀合测试所证实。已经将nabh3cn浓度鉴定为工艺的关键因素,进行额外的结合测试,进一步将nabh3cn浓度从10mg/ml降低至5mg/ml和1mg/ml,以检查进一步降低该试剂的浓度是否有利于缀合效率。此外,研究反应时间的作用,以4小时、过夜(on)或2天运行缀合。根据doe优化,其他参数保持相同。与10mg/ml nabh3cn浓度相比,用5mg/m和1mg/ml还原剂进行反应产生gac与crm197比率略高的缀合物(表3)。表3.研究nabh3cn浓度和反应时间对gacox与crml97缀合的作用。将nabh3cn浓度从1mg/ml进一步降低至0.25mg/ml对gac与crm197的比率和gac回收率%产生负面影响(数据未显示)。基于此类结果,选择5mg/ml nabh3cn并将反应时间缩短至on。优化的缀合工艺描述于图9(方案1)中。还将该工艺按比例放大至100mg gac,进一步证实了该工艺的稳健性,因为与以10mg规模生产的缀合物相比,所得缀合物的特征在于相似的gac与crm197 w/w比率和gac%产率(表4),并且再次获得的结果在表2中报告的doe优化的平均值的95%ci之内。表4.在优化条件下以不同规模生产的缀合物证实在gac与crm197的比率和工艺产率方面的预期结果。在小鼠中测试这种缀合物,证实其诱导与优化前产生的crm197缀合物引发的应答相当的抗gac igg应答的能力(图5)。3.讨论目前还没有获得许可的针对gas的疫苗,所述gas是世界上全球发病率和死亡率的主要原因,导致范围广泛的疾病,并且估计每年引起约50万人死亡,大部分在年轻人中[2]。疫苗开发的主要障碍之一与高gas菌株多样性有关,在血清学上基于表面m蛋白的血清型[15],gas的主要毒力和免疫学决定簇之一[24],迄今为止,只有基于m蛋白的候选疫苗已在临床试验中进行测试[6,25-27],但基于保守蛋白抗原和表面多糖的新型疫苗也在开发中[28]。与载体蛋白缀合的高度保守的slo、spyad、spycep和gac已被提议作为一种有吸引力的替代疫苗候选物[6]。在这里,这三种蛋白抗原已作为gac的载体进行测试,目的在于简化最终疫苗设计,将四种抗原中的两种组合在一个构建体中。迄今为止,只有很少的载体蛋白被用于许可的糖缀合物疫苗,并且越来越关注载体-诱导的表位抑制(c1es),这可能导致在患者同时或密切相继重复暴露于给定载体后抗碳水化合物免疫应答降低[21,29,30]。新载体的鉴定还受到探索病原体相关蛋白可以作为载体和抗原的双重作用的兴趣的驱动,因此产生一种疫苗,其通过同时施用碳水化合物和蛋白抗原,解决了病原体的两种不同毒力因子[21]。已经在临床前水平提出并研究了这种类型的组合[31-36]。其中,也很少探索gas蛋白作为可能的载体。在小鼠中的攻击研究中,与gas精氨酸脱亚氨酶(adi)蛋白抗原缀合的gac链的变体能够保护免于浅表皮肤感染,但不能保护免于侵袭性gas疾病[37]。与gas c5a肽酶(scpa)的非活性突变体scpa193缀合的gac寡糖在小鼠中诱导了稳健的抗碳水化合物免疫应答。抗体在体外诱导介导的gas调理吞噬作用,以及有效保护动物免于gas攻击和gas-诱导的肺损伤。然而,由单独该蛋白诱导的抗scpa193抗体对gas细胞只有中等结合活性,并且没有调理吞噬活性,尽管诱导了高滴度[38,39]。此处测试的slo、spyad和spycep蛋白已被证明是基准crm197的良好替代载体,用于促进抗gac igg应答以及通过facs与gas细菌结合(图5)。这些结果使这些蛋白作为新的载体蛋白有吸引力,也可能与其他ps抗原一起使用。由缀合物诱导的抗蛋白特异性抗体得到维持,尽管其水平低于由单独的蛋白诱导的水平。用与金黄色葡萄球菌α毒素(hla)连接的金黄色葡萄球菌5型荚膜ps(cp5)产生的生物缀合物疫苗已经显示针对菌血症和致死性肺炎是保护性的,提供针对葡萄球菌侵袭性疾病的广谱效力,具有针对聚糖和蛋白部分诱导特异性保护性抗体[44]。在这里,更传统的半合成方法用于gac的缀合。使用的缀合化学法(其实际上影响缀合的效率、糖与蛋白的比率以及糖缀合物的结构和大小)是可以主要影响糖缀合物疫苗的免疫原性的参数之一[45-47]。我们将gac与crm197的末端连接与随机方法进行比较。两种缀合物在小鼠中引发相似的免疫应答。原则上,在生产一致性的方面,使用选择性化学法(其产生更均匀和明确的结构而不影响糖链)应当是优选的。然而,在我们的情况下,使用选择性方法导致批次间不一致,在一些情况下没有形成缀合物。与糖的末端还原端上的醛基相比,沿着gac链引入少量更多的反应性醛基允许更可重现的缀合。从工艺角度来看,与选择性合成相比,随机缀合物的合成需要多一步。然而,通过用亚硫酸钠淬灭过量的氧化剂,可以在混合物中直接添加载体蛋白,避免gacox中间体纯化并将工艺简化为仅一步(图9-方案1)。由于随机方法导致形成交联的且相当不确定和异质的结构,因此对制造工艺进行仔细和严格的控制对于保证一致性以及适当的分析表征是必不可少的[46]。在这里,使用doe方法以鉴定最佳缀合条件,用于确保工艺稳健性和提高产率。产率增加意味着降低商品成本以具有更可持续和可负担的产品,这是满足lmic中的接种疫苗需求的重要事项。与传统的一次一个因素(ofat)方法相比,doe方法允许鉴定关键参数的最佳组合,考虑它们的相互作用,并在研究的设计空间中模拟工艺,预测最终产品的质量的关键参数的变化的影响[52,53]。在疫苗领域,doe已用于开发或优化分析和免疫学测定[54-56]或用于改进疫苗制剂或纯化工艺[57-60]。在我们的研究中,doe已被用于优化缀合过程。通过这种方法,缀合产率从5%增加至约40%,并且工艺稳健性得到保证和证实,还将工艺按比例放大至100mg规模的gac。总之,这项工作支持针对gas的通用疫苗的开发,并显示可以如何使用新型工具来设计改进的疫苗,最终目标是用稳健的制造工艺确保始终如一地交付安全且有效的产品。4.材料和方法4.1.材料从罗斯托克大学(the university of rostock)友情提供的野生型菌株hro-k-51产生的m蛋白-突变菌株(gas51δm1)提取gac。如先前所述[17,61]在gvgh生产和纯化gas重组蛋白spyad(spyadstop,89.5kda,总共62个赖氨酸)和spycep(spycep双突变体,174.0kda,总共133个赖氨酸),从gsk r&d获得gas重组蛋白slo(slo双突变体,60.6kda,总共56个赖氨酸)和crm197(58.4kda,总共39个赖氨酸)。通过亚硝酸盐/冰醋酸处理从细菌培养物化学提取gac[51]。如先前所述[12],使用切向流过滤和阴离子交换色谱的组合进行纯化。纯化的gac不含透明质酸、含有<4%蛋白和<1%dna杂质(相对于gac,w/w)。通过hplc-sec分析(tsk凝胶g3000 pwxl柱)使用葡聚糖(5、25、50、80、150kda)作为标准品(默克)估计平均分子大小为7.0kda,对应于每条链平均14个重复单元。本研究中使用以下化学品:磷酸二氢钠(nah2po4)、磷酸氢二钠(na2hpo4)、氰基硼氢化钠(nabh3cn)、高碘酸钠(naio4)、亚硫酸钠(na2so3)、硼氢化钠(nabh4)、脱氧胆酸盐(doc)、盐酸(hcl)、氯化钠(nacl)[merck]、硼酸溶液、磷酸盐缓冲盐水片(pbs)[fluka]、二硫苏糖醇(dtt)[invitrogen]。4.2.通过选择性直接还原胺化将gac与crm197缀合如kabanova等人[12]所报道进行缀合。简而言之,反应在ph8的200mm磷酸盐缓冲液(napi)中进行,其中gac浓度为10mg/ml,gac与crm197与nabh3cn的w/w/w比率为4∶1∶2。在37℃2天后,将缀合物在1.6x60cm sephacryl s-100hr柱(cytiva life sciences,以前为ge healthcare life sciences)上通过大小排阻色谱纯化,在10mm napi ph7.2中以0.5ml/分钟洗脱。最终纯化的缀合物命名为gac-crm197。4.3.通过随机氧化、随后还原胺化将gac与不同的载体蛋白缀合4.3.1.gac氧化通过doe优化该步骤后,在ph 8的硼酸盐中用8mm naio4氧化gac 1-10mg/ml。将溶液在黑暗中在25℃保持30分钟。之后,在ph8的硼酸盐中用16mm na2so3淬灭过量的naio4。将混合物在室温(rt)下轻轻搅拌15分钟。混合物直接用于缀合而无需中间纯化,或通过pd-10脱盐柱(cytiva life sciences,以前为ge healthcare life sciences)脱盐。在更高的规模下,通过切向流过滤(tff)进行纯化。用具有200cm2膜面积的sartorius hydrosart10kda截止膜进行tff。针对水进行15体积的渗滤(pin 1.0巴,pout0.0巴,tmp 0.5巴和渗透流速:8-10ml/min),保持滞留体积恒定在50ml。指定为gacox的纯化物质在-80℃下冷冻并冻干。4.3.2.缀合在nabh3cn存在的情况下,将gacox在ph 8的硼酸盐缓冲液中与不同的载体蛋白(crm197、slo、spyad、spycep)缀合,其中gac与蛋白与nabh3cn的比率为4∶1∶2w/w/w,并且gacox浓度为40mg/ml。将反应混合物在25℃(对于gas蛋白)或37℃(对于crm197)下孵育2天。通过amicon ultra(merck)30kda截止值针对10mm napi ph 7.2(3500xg;4℃;8次洗涤)纯化gas蛋白的缀合物。通过1ml sepharose q.ff柱(cytiva life sciences,以前为gehealthcare life sciences)上的阴离子交换色谱纯化crm197缀合物:在10mm napi ph 7.2中每ml树脂上样1mg蛋白,并且用1m nacl的梯度洗脱纯化的缀合物。将收集的级分针对10mm napi ph7.2缓冲液进行透析。最终纯化的缀合物被指定为gacox-蛋白。在doe优化后,条件改变如下:gacox40mg/ml,gacox与crm197 1∶1w/w比率,nabh3cn5mg/ml,硼酸盐ph 8,在25℃过夜。然后将反应混合物用pbs稀释10倍,并添加nabh4(nabh4∶gac w/w比率为0.5∶1)以淬灭gacox的残余的未反应醛基[62]。将混合物在室温下保持2小时。基于规模,如先前所述通过amicon ultra 30kda截止值或通过tff针对pbs进行纯化。用具有200cm2膜面积的sartorius pesu 50kda截止膜进行tff。进行针对pbs 1m nacl的10体积渗滤,随后进行针对单独的pbs的20体积渗滤(pin 0.5巴,pout 0.0巴,tmp 0.25巴,渗透液流速:25-27ml/分钟),保持滞留物体积恒定在50ml。4.4.实验设计(doe)用design-expert 10,stat-ease inc.进行实验计划和数据阐述。使用minitab18,minitab inc.进行anderson-darling正态性检验。对于氧化步骤,在200μl的总体积上进行每个反应测试,并且通过vivaspin 3kda截止值(sartorius)针对水进行纯化。对氧化的gac样品进行%gac回收率(基于通过hpaec-pad的rha定量)、%glcnac氧化以及通过hplc-sec分析的gac平均链长的评估。对于缀合反应,gac在10mg/ml下用ph 8硼酸盐中的8mm naio4在黑暗中在25℃下氧化30分钟。在淬灭过量naio4后,混合物通过pd 10针对水脱盐,并分装在不同的小瓶中用于缀合运行。所有缀合都在20和50μl之间的总体积上进行,并经由amicon ultra 30kda截止值针对ph7.2的10mm napi进行纯化。对缀合物进行%gac回收率、gac/crm197 w/w比率和混合物中%未缀合的crm197的评估。对于两种doe,遵循用于进行反应的相同随机化方案进行分析。4.5.分析方法氧化的gac通过hpaec-pad[63]表征,用于通过比较氧化前(开始)和氧化后(ox)后的glcnac与鼠李糖(rha)的摩尔比来评估氧化的glcnac的%。使用以下方程,所有浓度都表示为μmol/ml:%glcnac氧化=1-([glcnacox]/(([glcnac开始]/[rha开始])*[rhaox])))*100。hplc-sec用于检查氧化后gac链长没有变化。纯化的缀合物通过微bca(thermo scientific)和hpaec-pad[63]分别表征总蛋白和总gac含量,并测定最终产品中ps与蛋白的比率。来自hpaec-pad分析的gac浓度基于rha定量进行确定,因为glcnac在氧化步骤中受到影响。通过缀合物与doc共沉淀将游离gac与缀合物分离后,通过hpaec-pad定量游离gac[64]。通过sds-page分析反应混合物以及纯化的缀合物,以比较缀合物的蛋白模式与相应的未缀合蛋白,并通过hplc-sec分析以验证缀合物形成(与未缀合蛋白和糖相比,缀合物在更高mw处的偏移)。最后,dsc分析用于评估gas蛋白和相应的缀合物热稳定性。4.5.1.十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sds-page)tris-乙酸凝胶7%(nupage,来自invitrogen)用于运行sds-page分析。将样品(5-20μl,蛋白含量为2-10μg)与0.5m dtt(1/5,v/v)和nupage lds样品缓冲液(1/5,v/v)混合。将混合物在100℃加热5分钟。含有加载样品的凝胶在nupage tris-乙酸sds运行缓冲液(20x,invitrogen)中以45ma进行电泳,并用blue staining(thermofischer)染色。4.5.2.高效液相色谱-大小排阻色谱(hplc-sec)在具有tsk凝胶pwxl保护柱(4.0cm x 6.0mm;粒径12μm)的tsk凝胶g3000 pwxl(30cm x 7.8mm)柱(粒径7μm)(tosohbioscience)上洗脱缀合物、游离蛋白和游离gacox样品。流动相为0.1m nacl、0.1m nah2po4、5%ch3cn、ph 7.2,流速为0.5ml/分钟(等度法,持续35分钟)。注射样品体积为80μl。分别用λ-dna(λ-dna分子量标记iii0.12-21.2kbp,roche)和叠氮化钠(nan3,merck)进行空隙和床体积校准。通过折射率(ri)检测gacox峰。还使用色氨酸荧光(336nm处的发射光谱,与280nm处的激发波长)检测蛋白和缀合物峰。对于kd测定,使用以下方程:kd=[(te-t0)/(tt-t0)],其中:te=分析物的洗脱时间,t0=λ-dna的较大片段的洗脱时间,和tt=nan3的洗脱时间。4.5.3.差示扫描量热法(dsc)对于dsc分析,在ph 7.2的10mm napi中以~2-3μm的蛋白浓度制备样品。dsc温度扫描范围为10℃至110℃,其中热升温速率为每小时150℃,且过滤时段为5秒。通过减去仅含缓冲液的样品的参考数据来分析数据。所有实验一式三份进行,并确定解链温度(tm)的平均值。4.6.小鼠中的免疫原性研究在toscana life sciences动物设施(siena,italy),符合相关指南(意大利d.lgs.n.26/14和欧洲指令2010/63/ue)和gsk的机构政策,进行小鼠研究。动物方案得到toscana life sciences的动物福利机构和意大利卫生部的批准(aec项目编号201309和gas 734/2018-pr)。在研究第0天和第28天,雌性5周龄cd1小鼠(每组8只)用200μl配制的抗原腹膜内(i.p.)接种疫苗。在第-1天(合并血清)和第27天(单独血清)收集近似100μl血液(50μl血清),其中最后一次采血在第42天。用2mg/ml alhydrogel(al3+)配制缀合物。通过sds-page银染分析,验证>90%的缀合物吸附在alhydrogel上。4.7.小鼠中的抗gac和抗gas载体蛋白免疫应答的评价如先前所述[65](稍作修改),通过酶联免疫吸附测定(elisa)分析第一次免疫后4周和第二次免疫后两周收集的免疫前血清和个体小鼠血清的抗gac、抗spycep、抗slo和抗spyad总igg。简而言之,小鼠血清在含有0.05%tween20和0.1%bsa的pbs中1∶100、1∶4000和1∶160000稀释。elisa单位相对于小鼠抗抗原标准血清曲线表示,其中最佳5参数拟合由五参数逻辑方程确定。一个elisa单位被定义为在测定中吸光度值等于1的标准血清稀释度的倒数。每份小鼠血清一式三份运行。数据呈现为单个小鼠elisa单位的散点图和每组的几何平均值。gac-hsa(碳酸盐缓冲液ph 9.6中浓度为1μg/ml)、spycep、slo和spyad(碳酸盐缓冲液ph 9.6中浓度为2μg/ml)用作包被抗原。4.8.流式细胞术(facs)gas菌株gas51δm1在todd hewitt液体培养基+酵母提取物(thy)中在37℃在5%co2存在的情况下生长过夜。细菌以8,000x g沉淀5分钟并用pbs洗涤。然后用含有3%(w/v)bsa的pbs封闭细菌15分钟,并与在pbs+1%(w/v)bsa(1∶500、1∶5000和1∶10000)中稀释的小鼠血清孵育1小时。用pbs洗涤后,将样品与alexa fluor 647山羊抗小鼠igg(1∶500)(molecular probes)孵育30分钟。最后,将细菌用4%(w/v)甲醛固定20分钟,并使用facscanto ii流式细胞仪(bd biosciences)进行流式细胞术分析。4.9.功能测定4.9.1.il-8切割抑制测定在il-8切割elisa测定中测试免疫前和第二次免疫后的个体血清,以评估它们阻断spycep蛋白水解活性的能力。该测定如先前所述[14]进行,并进行一些修改。简而言之,将spycep(5ng/ml)与小鼠多克隆抗spycep血清以四种不同的稀释度(1∶100、1∶300、1∶900、1∶2700)在4℃在pbs 0.5mg bsa中预孵育5分钟。与仅缓冲液和与免疫前血清预孵育的spycep用作阴性对照。然后,添加人il-8(gibco,10ng/ml)并将反应物在37℃孵育(无酶反应用作对照)。2小时后,将每个反应混合物稀释20倍,并在用针对il-8的不同表位的单克隆抗体的共混物包被的96孔板(life technologies)中孵育。根据制造商的方案,使用il-8的标准曲线,测定每个样品和对照反应(不含酶)中il-8的量。每个血清稀释度测试两次,并在图中报告具有误差条的平均值。结果表示为每个测试血清浓度下未切割的il-8的量(ng/ml)。4.9.2.体外溶血测定在溶血测定中测试免疫前和第二次免疫后的个体血清,以评估它们阻断slo溶血活性的能力。该测定如先前所述[14]进行,并进行一些修改。简而言之,通过在pbs中洗涤兔红血细胞(emozoo)四次并重悬于pbs中制备红血细胞悬浮液(pbs中的20%兔红血细胞悬浮液)。在96孔圆底板中制备在含有0.5%bsa的pbs中稀释的抗slo血清或阴性对照免疫前血清的8个连续2倍稀释液,然后与900单位/ml的slo毒素(sigma,稀释于含有15mm二硫苏糖醇的pbs中,invitrogen)在室温下预孵育30分钟(在150μl的最终体积中)。添加兔血细胞悬浮液(50μl)后,在37℃下继续孵育30分钟。最后将板以1000xg离心5分钟,并将上清液小心转移至96孔平底板。在540nm处读取释放的血红蛋白的吸光度。每个血清稀释度测试两次,并在图中报告具有误差条的平均值。结果表示为兔红细胞在每个测试血清浓度下释放的血红蛋白量(od540)。4.10.统计学mann-whitney双尾检验用于比较两种不同抗原引发的免疫应答,kruskal-wallis检验与dunn氏事后分析用于多于两组间的比较。进行wilcoxon检验匹配对符号秩双尾检验以比较相同抗原在第27天和第42天诱导的应答。缩略语gas a群链球菌gac a群碳水化合物slo 链球菌溶血素olmics 低收入和中等收入国家rhd 风湿性健康疾病glcnac n-乙酰葡糖胺ps 多糖sds-page 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳mw 分子量hplc-sec 高效液相色谱-大小排阻色谱i.p. 腹膜内dsc 差示扫描量热法facs 流式细胞术doe 实验设计rt 室温rha 鼠李糖hpaec- 阴离子交换色谱联用脉冲安培检测padtff 切向流过滤elisa 酶联免疫吸附测定5.编号参考文献1.ralph,a.p.;carapetis,j.r.,group a streptococcal diseases and theirglobal burden.curr top microbiol immunol 2013,368,1-27.2.carapetis,j.r.;steer,a.c.;mulholland,e.k.;weber,m.,the globalburden of group a streptococcal diseases.lancet infect dis 2005,5,(11),685-94.3.dooling,k.l.;shapiro,d.j.;van beneden,c.;hersh,a.l.;hicks,l.a.,overprescribing and inappropriate antibiotic selection for children withpharyngitis in the united states,1997-2010.jama pediatr 2014,168,(11),1073-4.4.jansen,k.u.;knirsch,c.;anderson,a.s.,the role of vaccines inpreventing bacterial antimicrobial resistance.nature medicine 2018,24,(1),10-19.5.watkins,d.a.;johnson,c.o.;colquhoun,s.m.;karthikeyan,g.;beaton,a.;bukhman,g.;forouzanfar,m.h.;longenecker,c.t.;mayosi,b.m.;mensah,g.a.;nascimento,b.r.;ribeiro,a.l.p.;sable,c.a.;steer,a.c.;naghavi,m.;mokdad,a.h.;murray,c.j.l.;vos,t.;carapetis,j.r.;roth,g.a.,global,regional,and nationalburden of rheumatic heart disease,1990-2015.n engl j med 2017,377,(8),713-722.6.vekemans,j.;gouvea-reis,f.;kim,j.h.;excler,j.l.;smeesters,p.r.;o′brien,k.l.;van beneden,c.a.;steer,a.c.;carapetis,j.r.;kaslow,d.c.,the path togroup a streptococcus vaccines:world health organization research anddevelopment technology roadmap and preferred product characteristics.clininfect dis 2019,69,(5),877-883.7.walker,m.j.;barnett,t.c.;mcarthur,j.d.;cole,j.n.;gillen,c.m.;henningham,a.;sriprakash,k.s.;sanderson-smith,m.l.;nizet,v.,diseasemanifestations and pathogenic mechanisms of group a streptococcus.clinmicrobiol rev 2014,27,(2),264-301.8.schneerson,r.;barrera,o.;sutton,a.;robbins,j.b.,preparation,characterization,and immunogenicity of haemophilus influenzae type bpolysaccharide-protein conjugates.j exp med 1980,152,(2),361-76.9.berti,f.;micoli,f.,improving efficacy of glycoconjugate vaccines:from chemical conjugates to next generation constructs.curr opin immunol2020,65,42-49.10.rappuoli,r.,glycoconjugate vaccines:principles and mechanisms.scitransl med 2018,10,(456).11.salvadori,l.g.;blake,m.s.;mccarty,m.;tai,j.y.;zabriskie,j.b.,groupa streptococcus-liposome elisa antibody titers to group a polysaccharide andopsonophagocytic capabilities of the antibodies.j infect dis 1995,171,(3),593-600.12.kabanova,a.;margarit,i.;berti,f.;romano,m.r.;grandi,g.;bensi,g.;chiarot,e.;proietti,d.;swennen,e.;cappelletti,e.;fontani,p.;casini,d.;adamo,r.;pinto,v.;skibinski,d.;capo,s.;buffi,g.;gallotta,m.;christ,w.j.;campbell,a.s.;pena,j.;seeberger,p.h.;rappuoli,r.;costantino,p.,evaluation of a group astreptococcus synthetic oligosaccharide as vaccine candidate.vaccine 2010,29,(1),104-14.13.sabharwal,h.;michon,f.;nelson,d.;dong,w.;fuchs,k.;manjarrez,r.c.;sarkar,a.;uitz,c.;viteri-jackson,a.;suarez,r.s.;blake,m.;zabriskie,j.b.,groupa streptococcus(gas)carbohydrate as an immunogen for protection against gasinfection.j infect diss 2006,193,(1),129-35.14.bensi,g.;mora,m.;tuscano,g.;biagini,m.;chiarot,e.;bombaci,m.;capo,s.;falugi,f.;manetti,a.g.;donato,p.;swennen,e.;gallotta,m.;garibaldi,m.;pinto,v.;chiappini,n.;musser,j.m.;janulczyk,r.;mariani,m.;scarselli,m.;telford,j.l.;grifantini,r.;norais,n.;margarit,i.;grandi,g.,multi high-throughput approach for highly selective identification of vaccinecandidates:the group a streptococcus case.mol cell proteomics 2012,11,(6),m111015693.15.cunningham,m.w.,pathogenesis of group a streptococcalinfections.clin microbiol rev 2000,13,(3),470-511.16.uchiyama,s.;dohrmann,s.;timmer,a.m.;dixit,n.;ghochani,m.;bhandari,t.;timmer,j.c.;sprague,k.;bubeck-wardenburg,j.;simon,s.i.;nizet,v.,streptolysin o rapidly impairs neutrophil oxidative burst and antibacterialresponses to group a streptococcus.front immunol 2015,6,581.17.gallotta,m.;gancitano,g.;pietrocola,g.;mora,m.;pezzicoli,a.;tuscano,g.;chiarot,e.;nardi-dei,v.;taddei,a.r.;rindi,s.;speziale,p.;soriani,m.;grandi,g.;margarit,i.;bensi,g.,spyad,a moonlighting protein of group astreptococcus contributing to bacterial division and host celladhesion.infect immun 2014,82,(7),2890-901.18.edwards,r.j.;taylor,g.w.;ferguson,m.;murray,s.;rendell,n.;wrigley,a.;bai,z.;boyle,j.;finney,s.j.;jones,a.;russell,h.h.;turner,c.;cohen,j.;faulkner,l.;sriskandan,s.,specific c-terminal cleavage and inactivation ofinterleukin-8 by invasive disease isolates of streptococcus pyogenes.j infectdis 2005,192,(5),783-90.19.jobichen,c.;tan,y.c.;prabhakar,m.t.;nayak,d.;biswas,d.;pannu,n.s.;hanski,e.;sivaraman,j.,structure of scpc,a virulence protease fromstreptococcus pyogenes,reveals the functional domains and maturationmechanism.biochem j 2018,475,(17),2847-2860.20.davies,m.r.;mclntyre,l.;mutreja,a.;lacey,j.a.;lees,j.a.;towers,r.j.;duchene,s.;smeesters,p.r.;frost,h.r.;price,d.j.;holden,m.t.g.;david,s.;giffard,p.m.;worthing,k.a.;seale,a.c.;berkley,j.a.;harris,s.r.;rivera-hernandez,t.;berking,o.;cork,a.j.;torres,r.;lithgow,t.;strugnell,r.a.;bergmann,r.;nitsche-schmitz,p.;chhatwal,g.s.;bentley,s.d.;fraser,j.d.;moreland,n.j.;carapetis,j.r.;steer,a.c.;parkhill,j.;saul,a.;williamson,d.a.;currie,b.j.;tong,s.y.c.;dougan,g.;walker,m.j.,atlas of group a streptococcalvaccine candidates compiled using large-scale comparative genomics.nat genet2019,51,(6),1035-1043.21.micoli,f.;adamo,r.;costantino,p.,protein carriers forglycoconjugate vaccines:history,selection criteria,characterization and newtrends.molecules 2018,23,(6).22.tontini,m.;romano,m.r.;proietti,d.;balducci,e.;micoli,f.;balocchi,c.;santini,l.;masignani,v.;berti,f.;costantino,p.,preclinical studies on newproteins as carrier for glycoconjugate vaccines.vaccine 2016,34,(35),4235-4242.23.roy,r.;katzenellenbogen,e.;jennings,h.j.,lmproved procedures forthe conjugation of oligosaccharides to protein by reductive amination.can jbiochem cell biol 1984,62,(5),270-5.24.steer,a.c.;law,i.; matatolu,l.;beall,b.w.;carapetis,j.r.,globalemm type distribution of group a streptococci:systematic review andimplications for vaccine development.lancet infect dis 2009,9,(10),611-6.25.dale,j.b.;penfound,t.a.;chiang,e.y.;walton,w.j.,new 30-valent mprotein-based vaccine evokes cross-opsonic antibodies against non-vaccineserotypes of group a streptococci.vaccine 2011,29,(46),8175-8.26.postol,e.;alencar,r.;higa,f.t.;freschi de barros,s.;demarchi,l.m.;kalil,j.;guilherme,l.,streptlncor:a candidate vaccine epitope againsts.pyogenes infections induces protection in outbred mice.plos one 2013,8,(4),e60969.27.sekuloski,s.;batzloff,m.r.;griffin,p.;parsonage,w.;elliott,s.;hartas,j.;o′rourke,p.;marquart,l.;pandey,m.;rubin,f.a.;carapetis,j.;mccarthy,j.;good,m.f.,evaluation of safety and immunogenicity of a group astreptococcus vaccine candidate(mj8vax)in a randomized clinical trial.plosone 2018,13,(7),e0198658.28.steer,a.c.;carapetis,j.r.;dale,j.b.;fraser,j.d.;good,m.f.;guilherme,l.;moreland,n.j.;mulholland,e.k.;schodel,f.;smeesters,p.r.,statusof research and development of vaccines for streptococcus pyogenes.vaccine2016,34,(26),2953-2958.29.avci,f.;berti,f.;dull,p.;hennessey,j.;pavliak,v.;prasad,a.k.;vann,w.;wacker,m.;marcq,o.,glycoconjugates:what it would take to master thesewell-known yet little-understood immunogens for vaccine development.msphere2019,4,(5).30.dagan,r.;poolman,j.;siegrist,c.a.,glycoconjugate vaccines andimmune interference:a review.vaccine 2010,28,(34),5513-23.31.michon,f.;fusco,p.c.;minetti,c.a.;laude-sharp,m.;uitz,c.;huang,c.h.;d′ambra,a.j.;moore,s.;remeta,d.p.;heron,i.;blake,m.s.,multivalentpneumococcal capsular polysaccharide conjugate vaccines employing geneticallydetoxified pneumolysin as a carrier protein.vaccine 1998,16,(18),1732-41.32.nilo,a.;morelli,l.;passalacqua,i.;brogioni,b.;allan,m.;carboni,f.;pezzicoli,a.;zerbini,f.;maione,d.;fabbrini,m.;romano,m.r.;hu,q.y.;margarit,i.;berti,f.;adamo,r.,anti-group b streptococcus glycan-conjugate vaccinesusing pilus protein gbs80 as carrier and antigen:comparing lysine andtyrosine-directed conjugation.acs chem biol 2015,10,(7),1737-46.33.nilo,a.;passalacqua,i.;fabbrini,m.;allan,m.;usera,a.;carboni,f.;brogioni,b.;pezzicoli,a.;cobb,j.;romano,m.r.;margarit,i.;hu,q.y.;berti,f.;adamo,r.,exploring the effect of conjugation site and chemistry on theimmunogenicity of an anti-group b streptococcus glycoconjugate vaccine basedon gbs67 pilus protein and type v polysaccharide.bioconjug chem 2015,26,(8),1839-49.34.pinto,v.b.;burden,r.;wagner,a.;moran,e.e.;lee,c.h.,the developmentof an experimental multiple serogroups vaccine for neisseriameningitidis.plos one 2013,8,(11),e79304.35.pozzi,c.;wilk,k.;lee,j.c.;gening,m.;nifantiev,n.;pier,g.b.,opsonicand protective properties of antibodies raised to conjugate vaccinestargeting six staphylococcus aureus antigens.plos one 2012,7,(10),e46648.36.simon,r.;tennant,s.m.;wang,j.y.;schmidlein,p.j.;lees,a.;ernst,r.k.;pasetti,m.f.;galen,j.e.;levine,m.m.,salmonella enterica serovarenteritidis core o polysaccharide conjugated to h:g,m flagellin as acandidate vaccine for protection against invasive infection withs.enteritidis.infect immun 2011,79,(10),4240-9.37.rivera-hernandez,t.;pandey,m.;henningham,a.;cole,j.;choudhury,b.;cork,a.j.;gillen,c.m.;ghaffar,k.a.;west,n.p.;silvestri,g.;good,m.f.;moyle,p.m.;toth,i.;nizet,v.;batzloff,m.r.;walker,m.j.,differing efficacies of leadgroup a streptococcal vaccine candidates and full-length m protein incutaneous and invasive disease models.mbio 2016,7,(3).38.wang,s.;zhao,y.;wang,g.;feng,s.;guo,z.;gu,g.,group a streptococcuscell wall oligosaccharide-streptococcal c5a peptidase conjugates as effectiveantibacterial vaccines.acs irfectious diseases 2020,6,(2),281-290.39.zhao,y.;wang,s.;wang,g.;li,h.;guo,z.;gu,g.,synthesis andimmunological studies of group a streptococcus cell-wall oligosaccharide-streptococcal c5a peptidase conjugates as bivalent vaccines.organic chemistryfrontiers 2019,6,(20),3589-3596.40.chiarot,e.;faralla,c.;chiappini,n.;tuscano,g.;falugi,f.;gambellini,g.;taddei,a.;capo,s.;cartocci,e.;veggi,d.;corrado,a.;mangiavacchi,s.;tavarini,s.;scarselli,m.;janulczyk,r.;grandi,g.;margarit,i.;bensi,g.,targeted amino acid substitutions impair streptolysin o toxicity and group astreptococcus virulence.mbio 2013,4,(1),e00387-12.41.mckenna,s.;malito,e.;rouse,s.l.;abate,f.;bensi,g.;chiarot,e.;micoli,f.;mancini,f.;gomes moriel,d.;grandi,g.;mossakowska,d.;pearson,m.;xu,y.;pease,j.;sriskandan,s.;margarit,i.;bottomley,m.j.;matthews,s.,structure,dynamics and immunogenicity of a catalytically inactive cxc chemokine-degrading protease spycep from streptococcus pyogenes.computational andstructural biotechnology journal 2020,18,650-660.42.stefanetti,g.;hu,q.y.;usera,a.;robinson,z.;allan,m.;singh,a.;imase,h.;cobb,j.;zhai,h.;quinn,d.;lei,m.;saul,a.; adamo,r.;maclennan,c.a.;micoli,f.,sugar-protein connectivity impacts on the immunogenicity of site-selective salmonella o-antigen glycoconjugate vaccines.angew chem int ed engl2015,54,(45),13198-203.43.wacker,m.;linton,d.;hitchen,p.g.;nita-lazar,m.;haslam,s.m.;north,s.j.;panico,m.;morris,h.r;dell,a.;wren,b.w.;aebi,m.,n-linked glycosylation incampylobacter jejuni and its functional transfer into e.coli.science(newyork,n.y.)2002,298,(5599),1790-3.44.wacker,m.;wang,l.;kowarik,m.;dowd,m.;lipowsky,g.;faridmoayer,a.;shields,k.;park,s.;alaimo,c.;kelley,k.a.;braun,m.;quebatte,j.;gambillara,v.;carranza,p.;steffen,m.;lee,j.c.,prevention of staphylococcus aureusinfections by glycoprotein vaccines synthesized in escherichia coli.j infectdis 2014,209,(10),1551-61.45.carmenate,t.;canaan,l.;alvarez,a.;delgado,m.;gonzalez,s.;menendez,t.;rodes,l.;guillen,g.,effect of conjugation methodology on theimmunogenicity and protective efficacy of meningococcal group cpolysaccharide-p64k protein conjugates.fems immunol med microbiol 2004,40,(3),193-9.46.costantino,p.;rappuoli,r.;berti,f.,the design of semi-syntheticand synthetic glycoconjugate vaccines.expert opin drug discov 2011,6,(10),1045-66.47.fattom,a.;li,x.;cho,y.h.;burns,a.;hawwari,a.;shepherd,s.e.;coughlin,r.;winston,s.;naso,r.,effect of conjugation methodology,carrierprotein,and adjuvants on the immune response to staphylococcus aureuscapsular polysaccharides.vaccine 1995,13,(14),1288-93.48.rush,j.s.;edgar,r.j.;deng,p.;chen,j.;zhu,h.;van sorge,n.m.;morris,a.j.;korotkov,k.v.;korotkova,n.,the molecular mechanism of n-acetylglucosamine side-chain attachment to the lancefield group acarbohydrate in streptococcus pyogenes.j biol chem 2017,292,(47),19441-19457.49.duan,j.;kasper,d.l.,oxidative depolymerization of polysaccharidesby reactive oxygen/nitrogen species.glycobiology 2011,21,(4),401-9.50.kholy,a.e.;facklam,r.;sabri,g.;rotta,j.,serological identificationof group a streptococci from throat scrapings before culture.j clin microbiol1978,8,(6),725-8.51.pancholi,v.;fischetti,v.a.,lsolation and characterization of thecell-associated region of group a streptococcal m6 protein.j bacteriol 1988,170,(6),2618-24.52.beg,s.;swain,s.;rahman,m.;hasnain,m.s.;lmam,s.s.,chapter 3-application of design of experiments(doe)in pharmaceutical product andprocess optimization.in pharmaceutical quality by design,beg,s.;hasnain,m.s.,eds.academic press:2019;pp 43-64.53.montgomery,d.c.,response surface methods and other approaches toprocess optimization.design and analysis of experiments 1997.54.giannelli,c.;raso,m.m.;palmieri,e.;de felice,a.;pippi,f.;micoli,f.,development of a specific and sensitive hpaec-pad method forquantification of vi polysaccharide applicable to other polysaccharidescontaining amino uronic acids.anal chem 2020,92,(9),6304-6311.55.joelsson,d.;moravec,p.;troutman,m.;pigeon,j.;dephillips,p.,optimizing elisas for precision and robustness using laboratory automationand statistical design of experiments.j immunol methods 2008,337,(1),35-41.56.necchi,f.;carducci,m.;pisoni,i.;rossi,o.;saul,a.;rondini,s.,development of face(formulated alhydrogel competitive elisa)method for directquantification of oag present in shigella sonnei gmma-based vaccine and itsoptimization using design pf experiments approach.j immunol methods 2019,471,11-17.57.ahl,p.l.;mensch,c.;hu,b.;pixley,h.;zhang,l.;dieter,l.;russell,r.;smith,w.j.;przysiecki,c.;kosinski,m.;blue,j.t.,accelerating vaccineformulation development using design of experiment stability studies.journalof pharmaceutical sciences 2016,105,(10),3046-3056.58.ji,y.;tian,y.;ahnfelt,m.;sui,l.,design and optimization of achromatographic purification process for streptococcus pneumoniae serotype23f capsular polysaccharide by a design of experiments approach.journal ofchromatography.a 2014,1348,137-49.59.kanojia,g.;willems,g.j.;frijlink,h.w.;kersten,g.f.;soema,p.c.;amorij,j.p.,a design of experiment approach to predict product and processparameters for a spray dried influenza vaccine.international journal ofpharmaceutics 2016,511,(2),1098-111.60.patel,a.;erb,s.m.;strange,l.;shukla,r.s.;kumru,o.s.;smith,l.;nelson,p.;joshi,s.b.;livengood,j.a.;volkin,d.b.,combined semi-empiricalscreening and design of experiments(doe)approach to identify candidateformulations of a lyophilized live attenuated tetravalent viral vaccinecandidate.vaccine 2018,36,(22),3169-3179.61.abate,f.;malito,e.;falugi,f.;margarit,y.r.i.;bottomley,m.j.,cloning,expression,purification,crystallization and preliminary x-raydiffraction analysis of spycep,a candidate antigen for a vaccine againststreptococcus pyogenes.acta crystallogr sect f struct biol cryst commun 2013,69,(pt 10),1103-6.62.stefanetti,g.;rondini,s.;lanzilao,l.;saul,a.;maclennan,c.a.;micoli,f.,impact of conjugation chemistry on the immunogenicity ofs.typhimurium conjugate vaccines.vaccine 2014,32,(46),6122-9.63.pitirollo,o.;micoli,f.;necchi,f.;mancini,f.;carducci,m.;adamo,r.;evangelisti,c.;morelli,l.;polito,l.;lay,l.,gold nanoparticles morphology doesnot affect the multivalent presentation and antibody recognition of group astreptococcus synthetic oligorhamnans.bioorg chem 2020,99,103815.64.lei,q.p.;lamb,d.h.;heller,r.;pietrobon,p.,quantitation of lowlevel unconjugated polysaccharide in tetanus toxoid-conjugate vaccine byhpaec/pad following rapid separation by deoxycholate/hcl.j pharm biomed anal2000,21,(6),1087-91.65.lanzilao,l.;stefanetti,g.;saul,a.;maclennan,c.a.;micoli,f.;rondini,s.,strain selection for generation of o-antigen-based glycoconjugatevaccines against invasive nontyphoidal salmonella disease.plos one 2015,10,(10),e0139847.6.补充表表s1.应用于gac氧化的doe方法:测试条件和获得结果的概述。 因素1 因素2 因素3 响应1 响应2 响应3 std 运行 a:[ps] <![cdata[b:[nalo<sub>4</sub>]]]> c:ph 回收率 氧化glcnac 大小 mg/ml mm % % da 5 1 2.8 2.4 7.4 62 10.2 6970 1 2 2.8 2.4 5.6 69 13.5 6970 20 3 5.5 5.3 6.5 62 11.9 6782 15 4 5.5 5.3 6.5 76 12.7 6766 2 5 8.2 2.4 5.6 87 10.3 6886 6 6 8.2 2.4 7.4 78 8.5 6927 16 7 5.5 5.3 6.5 80 12.2 6807 12 8 5.5 10.0 6.5 88 16.7 6625 4 9 8.2 8.0 5.6 93 13.3 6825 17 10 5.5 5.3 6.5 78 12.8 6784 14 11 5.5 5.3 8.0 82 11.8 6808 7 12 2.8 8.0 7.4 77 14.4 6764 3 13 2.8 8.0 5.6 72 19.2 6766 9 14 1.0 5.3 6.5 70 19.4 6447 11 15 5.5 0.5 6.5 77 nd 7028 8 16 8.2 8.0 7.4 80 17.8 6726 13 17 5.5 5.3 5.0 84 17.8 6825 18 18 5.5 5.3 6.5 76 14.9 6774 10 19 10.0 5.3 6.5 88 15.1 6835 19 20 5.5 5.3 6.5 88 nd 6694 表s2.应用于gacox与crm197缀合的doe方法:测试条件和获得结果的概述。响应面减小二次模型的anova方差分析表[偏平方和-iii型]表s3.gac氧化的最佳条件的鉴定:doe的模型的统计分析。(a)响应 w/w比率gac/crm197响应面线性模型的an0va方差分析表[偏平方和-iii型](b)响应 回收的ps%响应面线性模型的an0va方差分析表[偏平方和-iii型]表s4.gacox与crm197缀合的优化条件的鉴定:gac/crm197w/w比率(a)和gac产率(b)的模型的统计分析。本发明的方面1.多糖缀合物,其包含以下或由以下组成:与载体多肽缀合的一种或多种多糖,其中所述载体多肽为:(a)选自化脓性链球菌spyad(spy0269,gas40)、化脓性链球菌spycep(spy0416,gas57)或化脓性链球菌slo(spy0167,gas25);(b)crm197;和(c)(a)或(b)的变体、片段和/或融合体。2.方面1的多糖缀合物,其中所述载体多肽为:(a)化脓性链球菌spyad(spy0269);或(b)化脓性链球菌spyad(spy0269)的变体、片段和/或融合体。3.方面1或2的多糖缀合物,其中所述化脓性链球菌spyad(spy0269)包含以下或由以下组成:(i)seq id no:1或seq id no:2的氨基酸序列;(ii)与seq id no:1或seq id no:2相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:1或seq id no:2具有至少70%序列同一性的氨基酸序列;和/或(iv)来自seq id no:1或seq id no:2的至少10个连续氨基酸、例如来自seq idno:1或seq id no:2的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340或350个连续氨基酸的片段。4.方面1的多糖缀合物,其中所述载体多肽为:(a)化脓性链球菌spycep(spy0416);(b)化脓性链球菌spycep(spy0416)的变体、片段和/或融合体。5.方面4的多糖缀合物,其中所述化脓性链球菌spycep(spy0416)包含以下或由以下组成:(i)seq id no:3或seq id no:4的氨基酸序列;(ii)与seq id no:3或seq id no:4相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:3或seq id no:4具有至少70%序列同一性的氨基酸序列;和/或(iv)来自seq id no:3或seq id no:4的至少10个连续氨基酸、例如来自seq idno:3或seq id no:4的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、500、750、1000、1250、1500、1550、1600、1610、1620、1630、1640、1650或1660个连续氨基酸的片段。6.方面1的多糖缀合物,其中所述载体多肽为:(a)化脓性链球菌slo(spy0167);或(b)化脓性链球菌slo(spy0167)的变体、片段和/或融合体。7.方面6的多糖缀合物,其中所述化脓性链球菌slo(spy0167)包含以下或由以下组成:(i)seq id no:5或seq id no:6的氨基酸序列;(ii)与seq id no:5或seq id no:6相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:5或seq id no:6具有至少70%序列同一性的氨基酸序列;和/或(iv)来自seq id no:5或seq id no:6的至少10个连续氨基酸、例如来自seq idno:5或seq id no:6的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、400、450、500、510、520、530、540、550、560或570个连续氨基酸的片段。8.方面1的多糖缀合物,其中所述载体多肽为:(a)crm197;或(b)crm197的变体、片段和/或融合体。9.方面8的多糖缀合物,其中所述crm197包含以下或由以下组成:(i)seq id no:7的氨基酸序列;(ii)与seq id no:7相比包含1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:7具有至少70%序列同一性的氨基酸序列;和/或(iv)来自seq id no:7的至少10个连续氨基酸、例如来自seq id no:6的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、400、450、500、510、520、530或535个连续氨基酸的片段。10.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖是微生物多糖,诸如细菌多糖、古细菌多糖、真菌多糖或原生生物多糖。11.方面10的多糖缀合物,其中所述微生物是病原体,例如人类病原体。12.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖是表面表达的。13.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖是细菌多糖,例如,选自以下的细菌的多糖:放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。14.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含以下或由以下组成:脱氧糖单体,例如,选自鼠李糖(6-脱氧-l-甘露糖)、墨角藻糖(fuculose)(6-脱氧-l-塔格糖)或岩藻糖(6-脱氧-l-半乳糖)的脱氧糖。15.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含侧链,例如,包含n-乙酰葡糖胺(glcnac)或由其组成的侧链。16.前述方面中任一项的多糖缀合物,其中平均1、1.5 2、2.5 3、3.5 4、4.5、5、6、7、8、9 10、11、12、13、14、15、16、17、18、19或20个多糖分子与所述载体多肽缀合。17.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含以下或由以下组成:i.单一分子种类;或ii.分子种类的混合物,例如,2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20种分子种类的混合物。18.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖与所述载体蛋白直接缀合。19.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖经由接头与所述载体蛋白缀合。20.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖具有小于100kda(例如小于80、70、60、50、40、30、25、20、15、14、13、12、11、10、9、8、7、6、5、4、3、2或1kda)的分子量。21.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖具有1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30个或更少的单糖单元。22.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含选自以下的细菌的荚膜多糖或由其组成:流感嗜血杆菌b型或a型;脑膜炎奈瑟氏菌血清群a、c、w135、x和y;肺炎链球菌血清型1、2、3、4、5、6a、6b、7f、8、9n、9v、10a、11a、12f、14、15b、17f、18c、19a、19f、20、22f、23f和33f;沙门氏菌,包括肠沙门氏菌伤寒血清型(salmonella entericaserovar typhi)vi,全长或片段化的(表示为fvi);志贺氏菌属,a群和b群链球菌(分别为gas和gbs)。23.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖通过如下与所述载体蛋白缀合:(a)由所述多糖链的多糖链的末端残基的醛或酮基的还原端残基和所述载体蛋白的赖氨酸形成的胺;和/或(b)由所述多糖的氧化主链和/或侧链(例如,对于gac,glcnac侧链的邻位二醇(1,2-二醇))和所述载体蛋白的赖氨酸形成的一个或多个醛基。24.前述方面中任一项的多糖缀合物,其进一步包含佐剂,例如,氢氧化铝、alhydrogel(氢氧化铝2%湿凝胶悬浮液,croda international plc)和alum-tlr7。25.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含根据seq id no:1的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。26.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含根据seq id no:3(突变型spycep)的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。27.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含根据seq id no:5(slo)的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。28.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含根据seq id no:7(crm197)的氨基酸序列或由其组成;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。29.疫苗,其包含方面1-28中任一项的多糖缀合物。30.方面29的疫苗,其进一步包含佐剂。31.方面29或方面30的疫苗,其进一步包含一种或多种额外的抗原,例如,选自以下的抗原的细菌抗原:放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。32.方面1-28中任一项的多糖缀合物或方面29-31中任一项的疫苗,其用于药物中。33.方面1-28中任一项的多糖缀合物或方面29-31中任一项的疫苗,其用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。34.方面1-28中任一项的多糖缀合物或方面29-31中任一项的疫苗用于在哺乳动物中产生免疫应答、例如用于治疗和/或预防一种或多种疾病的用途。35.方面2-28中任一项的多糖缀合物或方面29-31中任一项的疫苗用于制备药物的用途,所述药物用于在哺乳动物中产生免疫应答、例如用于治疗和/或预防一种或多种疾病。36.用于在哺乳动物中产生免疫应答的方法,所述方法包括以下或由以下组成:向所述哺乳动物施用有效量的方面2-18中任一项的多糖缀合物或方面29-31中任一项的疫苗。37.氧化多糖的方法,其包括以下步骤:i.通过如下氧化多糖:i.使多糖,例如,浓度为0.1-100mg/ml,例如,0.5-50、0.5-25、1-10、2.5-7.5、4-6或5mg/ml的多糖,与ii浓度为0.5-10m的氧化剂(例如,naio4[高碘酸钠+、kmno4[高锰酸钾]、高碘酸[hio4]或四乙酸铅[pb(oac)4]),iii.在合适的缓冲液(例如,200mm磷酸盐缓冲液或硼酸盐缓冲液)ph 3-9,例如,ph 5-8(例如,ph 5或ph 8)中,iv.在合适的温度(例如,20-30℃,诸如25℃)下,v.反应合适的时间(例如,15min-5hr,诸如,30min-3hr、30min-1hr或30min);ii.(任选地)通过如下淬灭残余的naio4:i.添加合适量的还原剂,例如,na2so3(亚硫酸钠),例如相对于步骤i(ii)中naio4的浓度摩尔过量,例如步骤i(ii)中的naio4浓度的5-10倍,或16mm,ii在合适的温度(例如,20-30℃、室温或25℃)下,iii.持续合适的时间(例如,10-30min或15min);iii.(任选地)纯化和/或浓缩氧化的多糖,例如,使用选自冻干、离心蒸发、旋转蒸发和切向流过滤的方法。38.缀合氧化的多糖的方法,其包括以下步骤:a.a.使浓度为5-75mg/ml(例如,40mg/ml)的氧化的多糖(例如,方面37的氧化的多糖)与;b.浓度为5-75mg/ml(例如40mg/ml)的蛋白;和c.浓度为0.5-10.0mg/ml的nabh3cn(氰基硼氢化钠);d.在ph 7-9、例如ph 7.5-8.5、ph8的硼酸盐缓冲液中;e.在合适的温度(例如,17.5-42.5℃、室温、25℃、30℃或37℃)下,f.反应合适的时间(例如,1小时、2小时、4小时、6小时、0.5至3天、1天或2天;b.(任选地)通过如下淬灭氧化的多糖的残余醛:a.添加合适量的nabh4(例如,nabh4∶多糖比[w/w]为0.5∶1,或例如相对于生成的醛基或氧化多糖的摩尔数摩尔过量,例如,5-10倍、50倍、100倍或1000倍),b.在合适的温度(例如,20-30℃、25℃或室温)下,c.持续合适的时间(例如,1至12小时、2-4小时)。c.(任选地)通过切向流过滤(tff)和/或无菌过滤(例如,tff,随后无菌过滤)纯化由步骤(b)产生的多糖缀合物。39.将多糖与多肽缀合的方法,其包括方面37的步骤(i)至(iv)和方面38的步骤(a)至(c)或由其组成。40.方面37-39中任一项的方法,其中所述多糖是方面1-28中任一项中所述的多糖,例如,gac。41.方面37-40中任一项的方法,其中所述蛋白是方面1-28中任一项中所述的蛋白,例如,spyad(例如,seq id no:1或seq id no:2)、spycep(例如,seq id no:3或seq idno:4)、slo(例如,seq id no:5或seq id no:6)或crm197(例如,seq id no:7)。42.方面37-41中任一项的方法,其中方法产物是方面1-28中任一项中所述的多糖缀合物,例如:i.与gac缀合的spyad(例如,seq id no:1或seq id no;2);ii.与gac缀合的spycep(例如,seq id no:3或seq id no:4);iii.与gac缀合的slo(例如,seq id no:5或seq id no:6);或iv.与gac缀合的crm197(例如,seq id no:7)。43.根据方面38-42中任一项所述的方法,其中反应在所述多肽的tm以下、例如比所述多肽的tm低至少0.5、1.0、1.5、2.0、2.5、3.0、4.0、5.0、6.0、7.0或7.5℃进行。44.根据方面37-42中任一项的方法产生的多糖缀合物。45.如本文的说明书和/或附图中任何处所述的多糖缀合物、用途或方法。本发明的进一步方面1.多糖缀合物,其包含以下或由以下组成:与载体多肽缀合的一种或多种多糖,其中所述载体多肽包含如下多肽:(a)选自化脓性链球菌spyad、化脓性链球菌spycep和化脓性链球菌slo;或(b)crm197;或(c)(a)或(b)的变体、片段和/或融合体。2.方面1的多糖缀合物,其中所述载体多肽为:(a)化脓性链球菌spyad(spy0269);或(b)化脓性链球菌spyad(spy0269)的变体、片段和/或融合体。3.方面1或2的多糖缀合物,其中所述载体多肽包含以下或由以下组成:(i)seq id no:1或seq id no:2的氨基酸序列;(ii)与seq id no:1或seq id no:2相差1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:1或seq id no:2具有至少70%、80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%序列同一性的氨基酸序列;和/或(iv)来自seq id no:1或seq id no:2的至少10个连续氨基酸、例如来自seq idno:1或seq id no:2的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340或350个连续氨基酸的片段。4.方面3的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seq id no:1或seq id no:2的至少300个氨基酸的片段具有至少95%同一性的氨基酸。5.方面3或方面4的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seqid no:1或seq id no:2具有至少95%同一性的氨基酸。6.前述方面中任一项的多糖缀合物,其中所述载体多肽为:(a)化脓性链球菌spycep(spy0416);或(b)化脓性链球菌spycep(spy0416)的变体、片段和/或融合体。7.方面6的多糖缀合物,其中所述载体多肽包含以下或由以下组成:(i)seq id no:3或seq id no:4的氨基酸序列;(ii)与seq id no:3或seq id no:4相差1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:3或seq id no:4具有至少70%、80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%序列同一性的氨基酸序列;和/或(iv)来自seq id no:3或seq id no:4的至少10个连续氨基酸、例如来自seq idno:3或seq id no:4的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、500、750、1000、1250、1500、1550、1600、1610、1620、1630、1640、1650或1660个连续氨基酸的片段。8.方面7的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seq id no:3或seq id no:4的至少1500个氨基酸的片段具有至少95%同一性的氨基酸。9.方面7或方面8的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seqid no:3或seq id no:4具有至少95%同一性的氨基酸。10.前述方面中任一项的多糖缀合物,其中所述载体多肽包含:(a)化脓性链球菌slo(spy0167);或(b)化脓性链球菌slo(spy0167)的变体、片段和/或融合体。11.方面10的多糖缀合物,其中所述载体多肽包含以下或由以下组成:(i)seq id no:5或seq id no:6的氨基酸序列;(ii)与seq id no:5或seq id no:6相差1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:5或seq id no:6具有至少70%、80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%序列同一性的氨基酸序列;和/或(iv)来自seq id no:5或seq id no:6的至少10个连续氨基酸、例如来自seq idno:5或seq id no:6的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、400、450、500、510、520、530、540、550、560或570个连续氨基酸的片段。12.方面11的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seq idno:5或seq id no:6的至少500个氨基酸的片段具有至少95%同一性的氨基酸。13.方面11或方面12的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seq id no:5或seq id no:6具有至少95%同一性的氨基酸。14.方面1的多糖缀合物,其中所述载体多肽为:(a)crm197;或(b)crm197的变体、片段和/或融合体。15.方面14的多糖缀合物,其中所述crm197包含以下或由以下组成:(i)具有seq id no:7的氨基酸序列的多肽;(ii)与seq id no:7相差1至10个单个氨基酸改变的氨基酸序列;(iii)与seq id no:7具有至少70%、80%、85%、90%、95%、96%、97%、98%、99%或至少99.5%序列同一性的氨基酸序列;和/或(iv)来自seq id no:7的至少10个连续氨基酸、例如来自seq id no:7的至少20、30、40、50、60、70、80、90、100、125、150、175、200、250、275、280、290、300、310、320、330、340、350、400、450、500、510、520、530或535个连续氨基酸的片段。16.方面15的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seq idno:7的至少500个氨基酸的片段具有至少95%同一性的氨基酸。17.方面15或方面16的多糖缀合物,其中所述载体多肽包含以下或由以下组成:与seq id no:7具有至少95%同一性的氨基酸。18.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖是微生物多糖,诸如细菌多糖、古细菌多糖、真菌多糖或原生生物多糖。19.方面18的多糖缀合物,其中所述微生物是病原体,例如人类病原体。20.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖是表面表达的。21.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖是细菌多糖,例如,选自以下的细菌的多糖:放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。22.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含以下或由以下组成:脱氧糖单体,例如,选自鼠李糖(6-脱氧-l-甘露糖)、墨角藻糖(fuculose)(6-脱氧-l-塔格糖)和岩藻糖(6-脱氧-l-半乳糖)的脱氧糖。23.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含侧链,例如,包含n-乙酰葡糖胺(glcnac)或由其组成的侧链。24.前述方面中任一项的多糖缀合物,其中平均至少1、1.5、2、2.5、3、3.5、4、4.5、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20个多糖分子与所述载体多肽缀合。25.前述方面中任一项的多糖缀合物,其中多糖与载体多肽的比率大于0.3、大于0.4、在0.3和1.0之间、或在0.4和0.6(w/w)之间。26.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含以下或由以下组成:i.单一分子种类;或ii.分子种类的混合物,例如,至少2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20种分子种类的混合物。27.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖与所述载体蛋白直接缀合。28.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖经由接头与所述载体蛋白缀合。29.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖具有小于100kda(例如小于80、70、60、50、40、30、25、20、15、14、13、12、11、10、9、8、7、6、5、4、3、2或1kda)的分子量。30.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖具有1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30个或更少的单糖单元。31.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含选自以下的细菌的荚膜多糖或由其组成:流感嗜血杆菌b型或a型;脑膜炎奈瑟氏菌血清群a、c、w135、x和y;肺炎链球菌血清型1、2、3、4、5、6a、6b、7f、8、9n、9v、10a、11a、12f、14、15b、17f、18c、19a、19f、20、22f、23f和33f;沙门氏菌,包括肠沙门氏菌伤寒血清型(salmonella entericaserovar typhi)vi,全长或片段化的(表示为fvi);志贺氏菌属,a群和b群链球菌(分别为gas和gbs)。32.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖包含a群碳水化合物(gac)。33.前述方面中任一项的多糖缀合物,其中所述一种或多种多糖通过如下与所述载体蛋白缀合:(a)由所述多糖链的多糖链的末端残基的醛或酮基的还原端残基和所述载体蛋白的赖氨酸形成的胺;和/或(b)由所述多糖的氧化主链和/或侧链(例如,对于gac,glcnac侧链的邻位二醇(1,2-二醇))和所述载体蛋白的赖氨酸形成的一个或多个醛基。34.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含以下或由以下组成:根据seq id no:1的氨基酸序列;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。35.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含以下或由以下组成:根据seq id no:3(突变型spycep)的氨基酸序列;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。36.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含以下或由以下组成:根据seq id no:5(slo)的氨基酸序列;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。37.前述方面中任一项的多糖缀合物,其中:i.所述载体多肽包含以下或由以下组成:根据seq id no:7(crm197)的氨基酸序列;且ii.与载体多肽缀合的一种或多种多糖包含gac(化脓性链球菌的a群碳水化合物)或由其组成。38.组合物,其包含方面1-37中任一项的多糖缀合物,所述组合物进一步包含佐剂,例如,氢氧化铝、alhydrogel(氢氧化铝2%湿凝胶悬浮液,croda international plc)或alum-tlr7。39.免疫原性组合物,其包含方面1-37中任一项的多糖缀合物。40.疫苗,其包含方面1-37中任一项的多糖缀合物。41.方面40的疫苗,其进一步包含佐剂,例如,氢氧化铝、alhydrogel(氢氧化铝2%湿凝胶悬浮液,croda international plc)或alum-tlr7。42.方面38的组合物、方面39的免疫原性组合物、或方面40或方面41的疫苗,其进一步包含一种或多种额外的抗原,例如,选自以下的抗原的细菌抗原:放线菌(例如,以色列放线菌),芽孢杆菌(例如,炭疽芽孢杆菌或蜡样芽胞杆菌),巴尔通体(例如,汉氏巴尔通体或五日热巴尔通体),博德特氏菌(例如,百日咳博德特氏菌),疏螺旋体(例如,伯氏疏螺旋体、伽氏疏螺旋体、阿氏疏螺旋体、回归热疏螺旋体),布鲁氏菌(例如,流产布鲁氏菌、犬布鲁氏菌、羊布鲁氏菌或猪布鲁氏菌),弯曲杆菌(例如,空肠弯曲杆菌),衣原体(例如,肺炎衣原体或沙眼衣原体),嗜衣原体(例如,鹦鹉热嗜衣原体),梭菌(例如,肉毒梭菌、艰难梭菌、产气荚膜梭菌、破伤风梭菌),棒状杆菌(例如,白喉棒状杆菌),肠球菌(例如,粪肠球菌或屎肠球菌),埃希氏杆菌(例如,大肠杆菌),弗朗西斯氏菌(例如,土拉弗朗西斯氏菌),嗜血杆菌(例如,流感嗜血杆菌),螺杆菌(例如,幽门螺杆菌),克雷伯氏菌(例如,肺炎克雷伯氏菌和产酸克雷伯氏菌),军团菌(例如,嗜肺军团菌),钩端螺旋体(例如,问号钩端螺旋体、圣地罗斯钩端螺旋体、韦氏钩端螺旋体、野口氏钩端螺旋体),李斯特菌(例如,单核细胞增多性李斯特菌),分枝杆菌(例如,麻风分枝杆菌、结核分枝杆菌或溃疡分枝杆菌),支原体(例如,肺炎支原体),奈瑟氏菌(例如,淋病奈瑟氏菌或脑膜炎奈瑟氏菌),假单胞菌(例如,铜绿假单胞菌),立克次氏体(例如,立氏立克次体),沙门氏菌(例如,伤寒沙门氏菌、肠炎沙门氏菌、副伤寒沙门氏菌、鼠伤寒沙门氏菌或猪霍乱沙门氏菌),志贺氏菌(例如,鲍氏志贺氏菌、弗氏沙门氏菌、宋内沙门氏菌或痢疾沙门氏菌),葡萄球菌(例如,金黄色葡萄球菌、表皮葡萄球菌或腐生葡萄球菌),链球菌(例如,无乳链球菌、肺炎链球菌或化脓性链球菌),密螺旋体(例如,苍白密螺旋体),脲原体(例如,解脲脲原体),弧菌(例如,霍乱弧菌)或耶尔森氏菌(例如,鼠疫耶尔森氏菌、小肠结肠炎耶尔森氏菌或假结核耶尔森氏菌)。43.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗,其用于药物中。44.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗,其用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。45.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗,其用于治疗和/或预防gas感染。46.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗用于在哺乳动物中产生免疫应答、例如用于治疗和/或预防一种或多种疾病的用途。47.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面29-31中任一项的疫苗用于治疗和/或预防gas感染的用途。48.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗用于制备药物的用途,所述药物用于在哺乳动物中产生免疫应答、例如用于治疗和/或预防一种或多种疾病。49.方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗用于制备药物的用途,所述药物用于治疗和/或预防gas感染。50.用于在哺乳动物中产生免疫应答的方法,所述方法包括以下或由以下组成:向所述哺乳动物施用有效量的方面1-37中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗。51.氧化多糖的方法,其包括以下步骤:i.通过如下氧化多糖:i.使多糖,例如,浓度为0.1-100mg/ml,例如,0.5-50、0.5-25、1-10、2.5-7.5、4-6或5mg/ml的多糖,与ii浓度为0.5-10m的氧化剂(例如,naio4[高碘酸钠+、kmno4[高锰酸钾]、高碘酸[hio4]或四乙酸铅[pb(oac)4]),iii.在合适的缓冲液(例如,200mm磷酸盐缓冲液或硼酸盐缓冲液)ph 3-9,例如,ph 5-8(例如,ph 5或ph 8)中,iv.在合适的温度(例如,20-30℃,诸如25℃)下,v.反应合适的时间(例如,15min-5hr,诸如,30min-3hr、30min-1hr或30min);ii.(任选地)通过如下淬灭残余的naio4:i.添加合适量的还原剂,例如,na2so3(亚硫酸钠),例如相对于步骤i(ii)中naio4的浓度摩尔过量,例如步骤i(ii)中的naio4浓度的5-10倍,或16mm,ii在合适的温度(例如,20-30℃、室温或25℃)下,iii.持续合适的时间(例如,10-30min或15min);iii.(任选地)纯化和/或浓缩氧化的多糖,例如,使用选自冻干、离心蒸发、旋转蒸发和切向流过滤的方法。52.缀合氧化的多糖的方法,其包括以下步骤:a.a.使浓度为5-75mg/ml(例如,40mg/ml)的氧化多糖(例如,方面37的氧化的多糖)与;b.浓度为5-75mg/ml(例如40mg/ml)的蛋白;和c.浓度为0.5-10.0mg/ml的nabh3cn(氰基硼氢化钠);d.在ph 7-9、例如ph 7.5-8.5、ph8的硼酸盐缓冲液中;e.在合适的温度(例如,17.5-42.5℃、室温、25℃、30℃或37℃)下,f.反应合适的时间(例如,1小时、2小时、4小时、6小时、0.5至3天、1天或2天;b.(任选地)通过如下淬灭氧化的多糖的残余醛:g.添加合适量的nabh4(例如,nabh4∶多糖比[w/w]为0.5∶1,或例如相对于生成的醛基或氧化的多糖的摩尔数摩尔过量,例如,5-10倍、50倍、100倍或1000倍),h.在合适的温度(例如,20-30℃、25℃或室温)下,i.持续合适的时间(例如,1至12小时、2-4小时)。c.(任选地)通过切向流过滤(tff)和/或无菌过滤(例如,tff,随后无菌过滤)纯化由步骤(b)产生的多糖缀合物。53.将多糖与多肽缀合的方法,其包括方面51的步骤(i)至(iii)和方面52的步骤(a)至(c)或由其组成。54.方面51-53中任一项的方法,其中所述多糖是方面1-37中任一项中所述的多糖,例如,gac。55.方面51-54中任一项的方法,其中所述蛋白是方面1-37中任一项中所述的蛋白,例如,spyad(例如,seq id no:1或seq id no:2)、spycep(例如,seq id no:3或seq idno:4)、slo(例如,seq id no:5或seq id no:6)或crm197(例如,seq id no:7)。56.方面51-55中任一项的方法,其中方法产物是方面1-37中任一项中所述的多糖缀合物,例如:i.与gac缀合的spyad(例如,seq id no:1或seq id no:2);ii.与gac缀合的spycep(例如,seq id no:3或seq id no:4);iii.与gac缀合的slo(例如,seq id no:5或seq id no:6);或iv.与gac缀合的crm197(例如,seq id no:7)。57.根据方面52-56中任一项所述的方法,其中反应在所述多肽的tm以下、例如比所述多肽的tm低至少0.5、1.0、1.5、2.0、2.5、3.0、4.0、5.0、6.0、7.0或7.5℃进行。58.根据方面51-56中任一项的方法产生的多糖缀合物。59.如本文的说明书和/或附图中任何处所述的多糖缀合物、用途或方法。60.将gac多糖与载体蛋白缀合的方法,其包括通过使所述多糖与氧化剂反应来氧化所述多糖的步骤。61.方面52-57或60的方法,其中通过使所述多糖与氧化剂反应来氧化所述多糖的步骤在合适的缓冲液中在合适的温度下进行合适的时间。62.氧化多糖的方法,所述方法包括氧化所述多糖的步骤,其包括以下步骤:i.通过如下氧化所述多糖:使所述多糖与(a)氧化剂,(b)在合适的缓冲液中,(c)在合适的温度下,(d)反应合适的时间。63.方面51、54至56、61或62的方法,其中所使用的多糖浓度、氧化剂、氧化剂浓度、合适的缓冲液、合适的温度和合适的时间中的至少一种确保所述方法实现所述多糖的至少5%、至少10%、至少15%、10%和30%之间、10%和25%之间或约15%的氧化。64.方面63的方法,其中所述方法中使用的多糖浓度、氧化剂、氧化剂浓度、合适的缓冲液、合适的温度和合适的时间确保所述方法实现所述多糖的至少5%、至少10%、至少15%、10%和30%之间、10%和25%之间或约15%的氧化。65.方面51、54至56或61至63中任一项的方法,其中所述方法被配置为实现所述多糖的至少5%、至少10%、至少15%、10%和30%之间、10%和25%之间或约15%的氧化。66.方面51、54至56或61至65中任一项的方法,其中所述多糖是gac且所述方法中使用的多糖浓度、氧化剂、氧化剂浓度、合适的缓冲液、合适的温度和合适的时间中的至少一种确保所述方法实现至少60%、至少65%、至少70%、至少75%、60%和100%之间、65%和100%之间、70%和90%之间或75%和90%之间的gac回收率。67.方面51、54至56或61至66中任一项的方法,其中所述多糖是gac且所述方法中使用的多糖浓度、氧化剂、氧化剂浓度、合适的缓冲液、合适的温度和合适的时间确保所述方法实现至少60%、至少65%、至少70%、至少75%、60%和100%之间、65%和100%之间、70%和90%之间或75%和90%之间的gac回收率。68.方面51、54至56或61至66中任一项的方法,其中所述多糖是gac且所述方法被配置为实现至少60%、至少65%、至少70%、至少75%、60%和100%之间、65%和100%之间、70%和90%之间或75%和90%之间的gac回收率。69.方面51、54至56或61至68中任一项的方法,其中所述多糖浓度为0.1-100mg/ml、0.5-50mg/ml、0.5-25mg/ml、1-10mg/ml、2.5-7.5mg/ml、4-6mg/ml或约5mg/ml。70.方面69的方法,其中所述多糖浓度为1-10mg/ml。71.方面51、54至56或61至70中任一项的方法,其中所述氧化剂选自高碘酸钠(naio4)、高锰酸钾(kmno4)、高碘酸(hio4)或四乙酸铅(pb(oac)4)。72.方面71的方法,其中所述氧化剂为naio4。73.方面51、54至56或61至72中任一项的方法,其中所述氧化剂浓度为0.1-25mm、0.5-10mm、1-10mm、2-10mm、5-10mm或约8mm。74.方面73的方法,其中所述氧化剂浓度为2-10mm或约8mm。75.方面51、54至56或61至74中任一项的方法,其中所述多糖的氧化步骤发生在包含多糖、氧化剂和合适的缓冲液的反应混合物中,且合适的缓冲液维持反应混合物的ph在ph 3-9、ph 5-9、ph 6-9或约ph 8。76.方面75的方法,其中合适的缓冲液维持反应混合物的ph在ph 5-9或约ph 8。77.方面51、54至56或61至76中任一项的方法,其中合适的缓冲液是磷酸盐缓冲液或硼酸盐缓冲液。78.方面51、54至56或61至77中任一项的方法,其中合适的温度为20℃-30℃、22℃-28℃、室温或约25℃。79.方面51、54至56、61至78中任一项的方法,其中合适的时间是15分钟至5小时、30分钟至3小时、30分钟至1小时或约30分钟。80.方面51、54至56、61至79中任一项的方法,其进一步包括通过添加合适的还原剂来淬灭残余氧化剂的步骤。81.方面80的方法,其中合适的还原剂是亚硫酸钠(na2so3)。82.方面80或81的方法,其中淬灭残余氧化剂的步骤在20℃至30℃或约25℃的温度下进行。83.方面51、54至56或60至82中任一项的方法,其中使所述多糖与氧化剂反应的步骤提供氧化的多糖且进一步包括纯化和/或浓缩氧化的多糖的步骤。84.方面83的方法,其中纯化和/或浓缩氧化的多糖的步骤使用包括冻干、离心蒸发、旋转蒸发和/或切向流过滤的方法实施。85.方面51、54至56或60至84中任一项的将gac多糖与载体蛋白缀合的方法,其中使所述多糖与氧化剂反应的步骤提供氧化的gac多糖且其中所述方法进一步包括使氧化的gac多糖与载体多肽反应的步骤。86.方面85的方法,其中使gac氧化的多糖与载体多肽反应的步骤包括使gac氧化的多糖与载体多肽和氰基硼氢化钠在硼酸盐缓冲液中在合适的温度下反应合适的时间。87.方面85或86的方法,其中所述方法在使所述多糖与氧化剂反应的步骤和使氧化的gac多糖与载体多肽反应的步骤之间不包括纯化步骤。88.缀合氧化的多糖的方法,其包括以下步骤:a.使氧化的多糖与;b.载体多肽/蛋白;和c.氰基硼氢化钠;d.在硼酸盐缓冲液中;e.在合适的温度下;f.反应合适的时间。89.方面52至57或86至88中任一项的方法,其中所述方法中使用的氧化的多糖浓度、载体多肽/蛋白浓度、氰基硼氢化钠浓度、硼酸盐缓冲液的ph和合适的温度中的至少一种确保所述方法实现至少0.25、至少0.3、至少0.35、至少0.4、0.25和1之间、0.3和0.8之间或0.4和0.8之间的多糖与载体多肽/蛋白比率。90.方面52至57或86至89中任一项的方法,其中所述方法中使用的氧化的多糖浓度、载体多肽/蛋白浓度、氰基硼氢化钠浓度、硼酸盐缓冲液的ph和合适的温度确保所述方法实现至少0.25、至少0.3、至少0.35、至少0.4、0.25和1之间、0.3和0.8之间或0.4和0.8之间的多糖与载体多肽/蛋白比率。91.方面52至57或86至90中任一项的方法,其中所述方法被配置为实现至少0.25、至少0.3、至少0.35、至少0.4、0.25和1之间、0.3和0.8之间或0.4和0.8之间的多糖与载体多肽/蛋白比率。92.方面52至57或86至91中任一项的方法,其中所述多糖是gac且所述方法中使用的氧化的多糖浓度、载体多肽/蛋白浓度、氰基硼氢化钠浓度、硼酸盐缓冲液的ph和合适的温度中的至少一种确保所述方法实现至少25%、至少30%、至少35%、25%和80%之间、30%和70%之间或35%和60%之间的gac回收率。93.方面52至57或86至92中任一项的方法,其中所述多糖是gac且所述方法中使用的氧化的多糖浓度、载体多肽/蛋白浓度、氰基硼氢化钠浓度、硼酸盐缓冲液的ph和合适的温度确保所述方法实现至少25%、至少30%、至少35%、25%和80%之间、30%和70%之间或35%和60%之间的gac回收率。94.方面52至57或86至93中任一项的方法,其中所述多糖是gac且所述方法被配置为实现至少25%、至少30%、至少35%、25%和80%之间、30%和70%之间或35%和60%之间的gac回收率。95.方面52至57或86至94中任一项的方法,其中多糖与载体多肽/蛋白与氰基硼氢化钠的比率为1-20∶1-20∶1mg/ml、5-15∶5-15∶1mg/ml或约8∶8∶1w/w/v。96.方面52至57或86至95中任一项的方法,其中所述氧化多糖的浓度为5-75mg/ml、10-50mg/ml、20-60mg/ml或约40mg/ml。97.方面52至57或86至96中任一项的方法,其中所述载体多肽/蛋白的浓度为5-75mg/ml、10-50mg/ml、20-60mg/ml或约40mg/ml。98.方面52至57或86至97中任一项的方法,其中所述氰基硼氢化钠的浓度为0.5-10mg/ml、2-8mg/ml或约5mg/ml。99.方面52至57或86至98中任一项的方法,其中所述硼酸盐缓冲液的ph为7-9、7.8-8.5或约8。100.方面52至57或86至99中任一项的方法,其中所述合适的温度是17.5-42.5℃、20-40℃、约25℃、约28℃、约30℃或约37℃的温度。101.方面52至57或86至100中任一项的方法,其中所述合适的时间是至少1小时、至少5小时、至少24小时、1小时和5天之间、5小时和3天之间或约2天。102.方面52至57或86至101中任一项的方法,其进一步包括通过添加合适量的硼氢化钠(nabh4)来淬灭氧化多糖上残余的醛的步骤。103.方面52至57或102中任一项的方法,其中如下实施淬灭所述氧化多糖上残余的醛的步骤:(i)添加nabh4,其量等于至少0.1∶1、至少0.2∶1、约0.5∶1的nabh4∶多糖比率(w/w),或者nabh4相对于生成的醛基数或氧化的多糖的摩尔数5-1000倍、10-500倍、50-250倍、约50倍、约100倍或约1000倍过量;和/或(ii)在20-30℃、22-28℃、约25℃或室温的温度下;和/或(iii)持续1-12小时或2-4小时的时间。104.方面52至57或85至105中任一项的方法,其中使氧化的多糖或氧化的gac多糖与载体多肽/蛋白反应的步骤提供多糖缀合物,且所述方法进一步包括纯化多糖缀合物的步骤。105.方面52至57或104中任一项的方法,其中纯化多糖缀合物的步骤包括切向流过滤(tff)和/或无菌过滤。106.将多糖与载体多肽/蛋白缀合的方法,其包括方面51或60至84中任一项的方法,随后为方面52至57或88至105中任一项的方法。107.方面106的方法,其中所述方法在方面88至105中任一项的方法和方面60至84中任一项的方法之间不包括纯化步骤。108.方面52或62至84中任一项的方法,其中所述多糖或gac多糖是如方面18至23或26至32中任一项中所定义的一种或多种多糖。109.方面108的方法,其中所述多糖是gac多糖。110.方面52、85至108中任一项的方法,其中所述氧化的多糖或氧化的gac多糖是如方面18至23或26至32中任一项中所定义的一种或多种多糖的氧化形式。111.方面110的方法,其中所述多糖是氧化的gac多糖。112.方面62至110中任一项的方法,其中所述载体多肽/蛋白是如方面2至17中任一项中所定义的载体多肽/蛋白。113.方面60至111中任一项的方法,其中所述载体多肽/蛋白包含:(i)seq id no:1-7中任一个的氨基酸序列;(ii)与seq id no:1-7中任一个具有至少90%、至少95%、至少98%、至少99%或100%同一性的氨基酸序列;或(iii)与seq id no:1-7中任一个的至少500个氨基酸的片段具有至少95%同一性的氨基酸序列。114.方面60至113中任一项的方法,其中所述方法提供批次间一致性。115.通过方面60至114中任一项的方法可获得的多糖缀合物。116.通过方面60至114中任一项的方法获得的多糖缀合物。117.方面115或116的多糖缀合物,其用于药物中。118.方面115或116的多糖缀合物,其用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。119.方面115或116的多糖缀合物,其用于治疗和/或预防gas感染。120.方面115或116的多糖缀合物用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病的用途。121.方面115或116的多糖缀合物用于治疗和/或预防gas感染的用途。122.方面115或116的多糖缀合物用于制备药物的用途,所述药物用于在哺乳动物中产生免疫应答,例如,用于治疗和/或预防一种或多种疾病。123.方面115或116的多糖缀合物用于制备药物的用途,所述药物用于治疗和/或预防gas感染。124.在哺乳动物中产生免疫应答、例如用于治疗和/或预防一种或多种疾病的方法,所述方法包括向哺乳动物施用有效量的方面1-37、115或116中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗。125.治疗和/或预防一种或多种疾病的方法,所述方法包括向哺乳动物施用有效量的方面1-37、115或116中任一项的多糖缀合物、方面38的组合物、方面39的免疫原性组合物或方面40-42中任一项的疫苗。126.方面124或125的方法,其中所述一种或多种疾病之一是gas感染。 序列表<110> glaxosmithkline biologicals sa<120> 新型载体和缀合方法<130> n421966wo<140> 20207547.9<141> 2020-11-13<160> 7<170> patentin version 3.5<210> 1<211> 824<212> prt<213> 化脓性链球菌<400> 1met ser val gly val ser his gln val lys ala asp asp arg ala ser1 5 10 15gly glu thr lys ala ser asn thr his asp asp ser leu pro lys pro 20 25 30glu thr ile gln glu ala lys ala thr ile asp ala val glu lys thr 35 40 45leu ser gln gln lys ala glu leu thr glu leu ala thr ala leu thr 50 55 60lys thr thr ala glu ile asn his leu lys glu gln gln asp asn glu65 70 75 80gln lys ala leu thr ser ala gln glu ile tyr thr asn thr leu ala 85 90 95ser ser glu glu thr leu leu ala gln gly ala glu his gln arg glu 100 105 110leu thr ala thr glu thr glu leu his asn ala gln ala asp gln his 115 120 125ser lys glu thr ala leu ser glu gln lys ala ser ile ser ala glu 130 135 140thr thr arg ala gln asp leu val glu gln val lys thr ser glu gln145 150 155 160asn ile ala lys leu asn ala met ile ser asn pro asp ala ile thr 165 170 175lys ala ala gln thr ala asn asp asn thr lys ala leu ser ser glu 180 185 190leu glu lys ala lys ala asp leu glu asn gln lys ala lys val lys 195 200 205lys gln leu thr glu glu leu ala ala gln lys ala ala leu ala glu 210 215 220lys glu ala glu leu ser arg leu lys ser ser ala pro ser thr gln225 230 235 240asp ser ile val gly asn asn thr met lys ala pro gln gly tyr pro 245 250 255leu glu glu leu lys lys leu glu ala ser gly tyr ile gly ser ala 260 265 270ser tyr asn asn tyr tyr lys glu his ala asp gln ile ile ala lys 275 280 285ala ser pro gly asn gln leu asn gln tyr gln asp ile pro ala asp 290 295 300arg asn arg phe val asp pro asp asn leu thr pro glu val gln asn305 310 315 320glu leu ala gln phe ala ala his met ile asn ser val arg arg gln 325 330 335leu gly leu pro pro val thr val thr ala gly ser gln glu phe ala 340 345 350arg leu leu ser thr ser tyr lys lys thr his gly asn thr arg pro 355 360 365ser phe val tyr gly gln pro gly val ser gly his tyr gly val gly 370 375 380pro his asp lys thr ile ile glu asp ser ala gly ala ser gly leu385 390 395 400ile arg asn asp asp asn met tyr glu asn ile gly ala phe asn asp 405 410 415val his thr val asn gly ile lys arg gly ile tyr asp ser ile lys 420 425 430tyr met leu phe thr asp his leu his gly asn thr tyr gly his ala 435 440 445ile asn phe leu arg val asp lys his asn pro asn ala pro val tyr 450 455 460leu gly phe ser thr ser asn val gly ser leu asn glu his phe val465 470 475 480met phe pro glu ser asn ile ala asn his gln arg phe asn lys thr 485 490 495pro ile lys ala val gly ser thr lys asp tyr ala gln arg val gly 500 505 510thr val ser asp thr ile ala ala ile lys gly lys val ser ser leu 515 520 525glu asn arg leu ser ala ile his gln glu ala asp ile met ala ala 530 535 540gln ala lys val ser gln leu gln gly lys leu ala ser thr leu lys545 550 555 560gln ser asp ser leu asn leu gln val arg gln leu asn asp thr lys 565 570 575gly ser leu arg thr glu leu leu ala ala lys ala lys gln ala gln 580 585 590leu glu ala thr arg asp gln ser leu ala lys leu ala ser leu lys 595 600 605ala ala leu his gln thr glu ala leu ala glu gln ala ala ala arg 610 615 620val thr ala leu val ala lys lys ala his leu gln tyr leu arg asp625 630 635 640phe lys leu asn pro asn arg leu gln val ile arg glu arg ile asp 645 650 655asn thr lys gln asp leu ala lys thr thr ser ser leu leu asn ala 660 665 670gln glu ala leu ala ala leu gln ala lys gln ser ser leu glu ala 675 680 685thr ile ala thr thr glu his gln leu thr leu leu lys thr leu ala 690 695 700asn glu lys glu tyr arg his leu asp glu asp ile ala thr val pro705 710 715 720asp leu gln val ala pro pro leu thr gly val lys pro leu ser tyr 725 730 735ser lys ile asp thr thr pro leu val gln glu met val lys glu thr 740 745 750lys gln leu leu glu ala ser ala arg leu ala ala glu asn thr ser 755 760 765leu val ala glu ala leu val gly gln thr ser glu met val ala ser 770 775 780asn ala ile val ser lys ile thr ser ser ile thr gln pro ser ser785 790 795 800lys thr ser tyr gly ser gly ser ser thr thr ser asn leu ile ser 805 810 815asp val asp glu ser thr gln arg 820<210> 2<211> 873<212> prt<213> 化脓性链球菌<400> 2met asp leu glu gln thr lys pro asn gln val lys gln lys ile ala1 5 10 15leu thr ser thr ile ala leu leu ser ala ser val gly val ser his 20 25 30gln val lys ala asp asp arg ala ser gly glu thr lys ala ser asn 35 40 45thr his asp asp ser leu pro lys pro glu thr ile gln glu ala lys 50 55 60ala thr ile asp ala val glu lys thr leu ser gln gln lys ala glu65 70 75 80leu thr glu leu ala thr ala leu thr lys thr thr ala glu ile asn 85 90 95his leu lys glu gln gln asp asn glu gln lys ala leu thr ser ala 100 105 110gln glu ile tyr thr asn thr leu ala ser ser glu glu thr leu leu 115 120 125ala gln gly ala glu his gln arg glu leu thr ala thr glu thr glu 130 135 140leu his asn ala gln ala asp gln his ser lys glu thr ala leu ser145 150 155 160glu gln lys ala ser ile ser ala glu thr thr arg ala gln asp leu 165 170 175val glu gln val lys thr ser glu gln asn ile ala lys leu asn ala 180 185 190met ile ser asn pro asp ala ile thr lys ala ala gln thr ala asn 195 200 205asp asn thr lys ala leu ser ser glu leu glu lys ala lys ala asp 210 215 220leu glu asn gln lys ala lys val lys lys gln leu thr glu glu leu225 230 235 240ala ala gln lys ala ala leu ala glu lys glu ala glu leu ser arg 245 250 255leu lys ser ser ala pro ser thr gln asp ser ile val gly asn asn 260 265 270thr met lys ala pro gln gly tyr pro leu glu glu leu lys lys leu 275 280 285glu ala ser gly tyr ile gly ser ala ser tyr asn asn tyr tyr lys 290 295 300glu his ala asp gln ile ile ala lys ala ser pro gly asn gln leu305 310 315 320asn gln tyr gln asp ile pro ala asp arg asn arg phe val asp pro 325 330 335asp asn leu thr pro glu val gln asn glu leu ala gln phe ala ala 340 345 350his met ile asn ser val arg arg gln leu gly leu pro pro val thr 355 360 365val thr ala gly ser gln glu phe ala arg leu leu ser thr ser tyr 370 375 380lys lys thr his gly asn thr arg pro ser phe val tyr gly gln pro385 390 395 400gly val ser gly his tyr gly val gly pro his asp lys thr ile ile 405 410 415glu asp ser ala gly ala ser gly leu ile arg asn asp asp asn met 420 425 430tyr glu asn ile gly ala phe asn asp val his thr val asn gly ile 435 440 445lys arg gly ile tyr asp ser ile lys tyr met leu phe thr asp his 450 455 460leu his gly asn thr tyr gly his ala ile asn phe leu arg val asp465 470 475 480lys his asn pro asn ala pro val tyr leu gly phe ser thr ser asn 485 490 495val gly ser leu asn glu his phe val met phe pro glu ser asn ile 500 505 510ala asn his gln arg phe asn lys thr pro ile lys ala val gly ser 515 520 525thr lys asp tyr ala gln arg val gly thr val ser asp thr ile ala 530 535 540ala ile lys gly lys val ser ser leu glu asn arg leu ser ala ile545 550 555 560his gln glu ala asp ile met ala ala gln ala lys val ser gln leu 565 570 575gln gly lys leu ala ser thr leu lys gln ser asp ser leu asn leu 580 585 590gln val arg gln leu asn asp thr lys gly ser leu arg thr glu leu 595 600 605leu ala ala lys ala lys gln ala gln leu glu ala thr arg asp gln 610 615 620ser leu ala lys leu ala ser leu lys ala ala leu his gln thr glu625 630 635 640ala leu ala glu gln ala ala ala arg val thr ala leu val ala lys 645 650 655lys ala his leu gln tyr leu arg asp phe lys leu asn pro asn arg 660 665 670leu gln val ile arg glu arg ile asp asn thr lys gln asp leu ala 675 680 685lys thr thr ser ser leu leu asn ala gln glu ala leu ala ala leu 690 695 700gln ala lys gln ser ser leu glu ala thr ile ala thr thr glu his705 710 715 720gln leu thr leu leu lys thr leu ala asn glu lys glu tyr arg his 725 730 735leu asp glu asp ile ala thr val pro asp leu gln val ala pro pro 740 745 750leu thr gly val lys pro leu ser tyr ser lys ile asp thr thr pro 755 760 765leu val gln glu met val lys glu thr lys gln leu leu glu ala ser 770 775 780ala arg leu ala ala glu asn thr ser leu val ala glu ala leu val785 790 795 800gly gln thr ser glu met val ala ser asn ala ile val ser lys ile 805 810 815thr ser ser ile thr gln pro ser ser lys thr ser tyr gly ser gly 820 825 830ser ser thr thr ser asn leu ile ser asp val asp glu ser thr gln 835 840 845arg ala leu lys ala gly val val met leu ala ala val gly leu thr 850 855 860gly phe arg phe arg lys glu ser lys865 870<210> 3<211> 1581<212> prt<213> 化脓性链球菌<400> 3met ala asp glu leu ser thr met ser glu pro thr ile thr asn his1 5 10 15ala gln gln gln ala gln his leu thr asn thr glu leu ser ser ala 20 25 30glu ser lys ser gln asp thr ser gln ile thr leu lys thr asn arg 35 40 45glu lys glu gln ser gln asp leu val ser glu pro thr thr thr glu 50 55 60leu ala asp thr asp ala ala ser met ala asn thr gly ser asp ala65 70 75 80thr gln lys ser ala ser leu pro pro val asn thr asp val his asp 85 90 95trp val lys thr lys gly ala trp asp lys gly tyr lys gly gln gly 100 105 110lys val val ala val ile ala thr gly ile asp pro ala his gln ser 115 120 125met arg ile ser asp val ser thr ala lys val lys ser lys glu asp 130 135 140met leu ala arg gln lys ala ala gly ile asn tyr gly ser trp ile145 150 155 160asn asp lys val val phe ala his asn tyr val glu asn ser asp asn 165 170 175ile lys glu asn gln phe glu asp phe asp glu asp trp glu asn phe 180 185 190glu phe asp ala glu ala glu pro lys ala ile lys lys his lys ile 195 200 205tyr arg pro gln ser thr gln ala pro lys glu thr val ile lys thr 210 215 220glu glu thr asp gly ser his asp ile asp trp thr gln thr asp asp225 230 235 240asp thr lys tyr glu ser his gly met his val thr gly ile val ala 245 250 255gly asn ser lys glu ala ala ala thr gly glu arg phe leu gly ile 260 265 270ala pro glu ala gln val met phe met arg val phe ala asn asp ile 275 280 285met gly ser ala glu ser leu phe ile lys ala ile glu asp ala val 290 295 300ala leu gly ala asp val ile asn leu ser leu gly thr ala asn gly305 310 315 320ala gln leu ser gly ser lys pro leu met glu ala ile glu lys ala 325 330 335lys lys ala gly val ser val val val ala ala gly asn glu arg val 340 345 350tyr gly ser asp his asp asp pro leu ala thr asn pro asp tyr gly 355 360 365leu val gly ser pro ser thr gly arg thr pro thr ser val ala ala 370 375 380ile asn ser lys trp val ile gln arg leu met thr val lys glu leu385 390 395 400glu asn arg ala asp leu asn his gly lys ala ile tyr ser glu ser 405 410 415val asp phe lys asp ile lys asp ser leu gly tyr asp lys ser his 420 425 430gln phe ala tyr val lys glu ser thr asp ala gly tyr asn ala gln 435 440 445asp val lys gly lys ile ala leu ile glu arg asp pro asn lys thr 450 455 460tyr asp glu met ile ala leu ala lys lys his gly ala leu gly val465 470 475 480leu ile phe asn asn lys pro gly gln ser asn arg ser met arg leu 485 490 495thr ala asn gly met gly ile pro ser ala phe ile ser his glu phe 500 505 510gly lys ala met ser gln leu asn gly asn gly thr gly ser leu glu 515 520 525phe asp ser val val ser lys ala pro ser gln lys gly asn glu met 530 535 540asn his phe ser asn trp gly leu thr ser asp gly tyr leu lys pro545 550 555 560asp ile thr ala pro gly gly asp ile tyr ser thr tyr asn asp asn 565 570 575his tyr gly ser gln thr gly thr ala met ala ser pro gln ile ala 580 585 590gly ala ser leu leu val lys gln tyr leu glu lys thr gln pro asn 595 600 605leu pro lys glu lys ile ala asp ile val lys asn leu leu met ser 610 615 620asn ala gln ile his val asn pro glu thr lys thr thr thr ser pro625 630 635 640arg gln gln gly ala gly leu leu asn ile asp gly ala val thr ser 645 650 655gly leu tyr val thr gly lys asp asn tyr gly ser ile ser leu gly 660 665 670asn ile thr asp thr met thr phe asp val thr val his asn leu ser 675 680 685asn lys asp lys thr leu arg tyr asp thr glu leu leu thr asp his 690 695 700val asp pro gln lys gly arg phe thr leu thr ser his ser leu lys705 710 715 720thr tyr gln gly gly glu val thr val pro ala asn gly lys val thr 725 730 735val arg val thr met asp val ser gln phe thr lys glu leu thr lys 740 745 750gln met pro asn gly tyr tyr leu glu gly phe val arg phe arg asp 755 760 765ser gln asp asp gln leu asn arg val asn ile pro phe val gly phe 770 775 780lys gly gln phe glu asn leu ala val ala glu glu ser ile tyr arg785 790 795 800leu lys ser gln gly lys thr gly phe tyr phe asp glu ser gly pro 805 810 815lys asp asp ile tyr val gly lys his phe thr gly leu val thr leu 820 825 830gly ser glu thr asn val ser thr lys thr ile ser asp asn gly leu 835 840 845his thr leu gly thr phe lys asn ala asp gly lys phe ile leu glu 850 855 860lys asn ala gln gly asn pro val leu ala ile ser pro asn gly asp865 870 875 880asn asn gln asp phe ala ala phe lys gly val phe leu arg lys tyr 885 890 895gln gly leu lys ala ser val tyr his ala ser asp lys glu his lys 900 905 910asn pro leu trp val ser pro glu ser phe lys gly asp lys asn phe 915 920 925asn ser asp ile arg phe ala lys ser thr thr leu leu gly thr ala 930 935 940phe ser gly lys ser leu thr gly ala glu leu pro asp gly his tyr945 950 955 960his tyr val val ser tyr tyr pro asp val val gly ala lys arg gln 965 970 975glu met thr phe asp met ile leu asp arg gln lys pro val leu ser 980 985 990gln ala thr phe asp pro glu thr asn arg phe lys pro glu pro leu 995 1000 1005lys asp arg gly leu ala gly val arg lys asp ser val phe tyr 1010 1015 1020leu glu arg lys asp asn lys pro tyr thr val thr ile asn asp 1025 1030 1035ser tyr lys tyr val ser val glu asp asn lys thr phe val glu 1040 1045 1050arg gln ala asp gly ser phe ile leu pro leu asp lys ala lys 1055 1060 1065leu gly asp phe tyr tyr met val glu asp phe ala gly asn val 1070 1075 1080ala ile ala lys leu gly asp his leu pro gln thr leu gly lys 1085 1090 1095thr pro ile lys leu lys leu thr asp gly asn tyr gln thr lys 1100 1105 1110glu thr leu lys asp asn leu glu met thr gln ser asp thr gly 1115 1120 1125leu val thr asn gln ala gln leu ala val val his arg asn gln 1130 1135 1140pro gln ser gln leu thr lys met asn gln asp phe phe ile ser 1145 1150 1155pro asn glu asp gly asn lys asp phe val ala phe lys gly leu 1160 1165 1170lys asn asn val tyr asn asp leu thr val asn val tyr ala lys 1175 1180 1185asp asp his gln lys gln thr pro ile trp ser ser gln ala gly 1190 1195 1200ala ser val ser ala ile glu ser thr ala trp tyr gly ile thr 1205 1210 1215ala arg gly ser lys val met pro gly asp tyr gln tyr val val 1220 1225 1230thr tyr arg asp glu his gly lys glu his gln lys gln tyr thr 1235 1240 1245ile ser val asn asp lys lys pro met ile thr gln gly arg phe 1250 1255 1260asp thr ile asn gly val asp his phe thr pro asp lys thr lys 1265 1270 1275ala leu asp ser ser gly ile val arg glu glu val phe tyr leu 1280 1285 1290ala lys lys asn gly arg lys phe asp val thr glu gly lys asp 1295 1300 1305gly ile thr val ser asp asn lys val tyr ile pro lys asn pro 1310 1315 1320asp gly ser tyr thr ile ser lys arg asp gly val thr leu ser 1325 1330 1335asp tyr tyr tyr leu val glu asp arg ala gly asn val ser phe 1340 1345 1350ala thr leu arg asp leu lys ala val gly lys asp lys ala val 1355 1360 1365val asn phe gly leu asp leu pro val pro glu asp lys gln ile 1370 1375 1380val asn phe thr tyr leu val arg asp ala asp gly lys pro ile 1385 1390 1395glu asn leu glu tyr tyr asn asn ser gly asn ser leu ile leu 1400 1405 1410pro tyr gly lys tyr thr val glu leu leu thr tyr asp thr asn 1415 1420 1425ala ala lys leu glu ser asp lys ile val ser phe thr leu ser 1430 1435 1440ala asp asn asn phe gln gln val thr phe lys ile thr met leu 1445 1450 1455ala thr ser gln ile thr ala his phe asp his leu leu pro glu 1460 1465 1470gly ser arg val ser leu lys thr ala gln asp gln leu ile pro 1475 1480 1485leu glu gln ser leu tyr val pro lys ala tyr gly lys thr val 1490 1495 1500gln glu gly thr tyr glu val val val ser leu pro lys gly tyr 1505 1510 1515arg ile glu gly asn thr lys val asn thr leu pro asn glu val 1520 1525 1530his glu leu ser leu arg leu val lys val gly asp ala ser asp 1535 1540 1545ser thr gly asp his lys val met ser lys asn asn ser gln ala 1550 1555 1560leu thr ala ser ala thr pro thr lys ser thr thr ser ala thr 1565 1570 1575ala lys ala 1580<210> 4<211> 1647<212> prt<213> 化脓性链球菌<400> 4met glu lys lys gln arg phe ser leu arg lys tyr lys ser gly thr1 5 10 15phe ser val leu ile gly ser val phe leu val met thr thr thr val 20 25 30ala ala asp glu leu ser thr met ser glu pro thr ile thr asn his 35 40 45ala gln gln gln ala gln his leu thr asn thr glu leu ser ser ala 50 55 60glu ser lys ser gln asp thr ser gln ile thr leu lys thr asn arg65 70 75 80glu lys glu gln ser gln asp leu val ser glu pro thr thr thr glu 85 90 95leu ala asp thr asp ala ala ser met ala asn thr gly ser asp ala 100 105 110thr gln lys ser ala ser leu pro pro val asn thr asp val his asp 115 120 125trp val lys thr lys gly ala trp asp lys gly tyr lys gly gln gly 130 135 140lys val val ala val ile asp thr gly ile asp pro ala his gln ser145 150 155 160met arg ile ser asp val ser thr ala lys val lys ser lys glu asp 165 170 175met leu ala arg gln lys ala ala gly ile asn tyr gly ser trp ile 180 185 190asn asp lys val val phe ala his asn tyr val glu asn ser asp asn 195 200 205ile lys glu asn gln phe glu asp phe asp glu asp trp glu asn phe 210 215 220glu phe asp ala glu ala glu pro lys ala ile lys lys his lys ile225 230 235 240tyr arg pro gln ser thr gln ala pro lys glu thr val ile lys thr 245 250 255glu glu thr asp gly ser his asp ile asp trp thr gln thr asp asp 260 265 270asp thr lys tyr glu ser his gly met his val thr gly ile val ala 275 280 285gly asn ser lys glu ala ala ala thr gly glu arg phe leu gly ile 290 295 300ala pro glu ala gln val met phe met arg val phe ala asn asp ile305 310 315 320met gly ser ala glu ser leu phe ile lys ala ile glu asp ala val 325 330 335ala leu gly ala asp val ile asn leu ser leu gly thr ala asn gly 340 345 350ala gln leu ser gly ser lys pro leu met glu ala ile glu lys ala 355 360 365lys lys ala gly val ser val val val ala ala gly asn glu arg val 370 375 380tyr gly ser asp his asp asp pro leu ala thr asn pro asp tyr gly385 390 395 400leu val gly ser pro ser thr gly arg thr pro thr ser val ala ala 405 410 415ile asn ser lys trp val ile gln arg leu met thr val lys glu leu 420 425 430glu asn arg ala asp leu asn his gly lys ala ile tyr ser glu ser 435 440 445val asp phe lys asp ile lys asp ser leu gly tyr asp lys ser his 450 455 460gln phe ala tyr val lys glu ser thr asp ala gly tyr asn ala gln465 470 475 480asp val lys gly lys ile ala leu ile glu arg asp pro asn lys thr 485 490 495tyr asp glu met ile ala leu ala lys lys his gly ala leu gly val 500 505 510leu ile phe asn asn lys pro gly gln ser asn arg ser met arg leu 515 520 525thr ala asn gly met gly ile pro ser ala phe ile ser his glu phe 530 535 540gly lys ala met ser gln leu asn gly asn gly thr gly ser leu glu545 550 555 560phe asp ser val val ser lys ala pro ser gln lys gly asn glu met 565 570 575asn his phe ser asn trp gly leu thr ser asp gly tyr leu lys pro 580 585 590asp ile thr ala pro gly gly asp ile tyr ser thr tyr asn asp asn 595 600 605his tyr gly ser gln thr gly thr ser met ala ser pro gln ile ala 610 615 620gly ala ser leu leu val lys gln tyr leu glu lys thr gln pro asn625 630 635 640leu pro lys glu lys ile ala asp ile val lys asn leu leu met ser 645 650 655asn ala gln ile his val asn pro glu thr lys thr thr thr ser pro 660 665 670arg gln gln gly ala gly leu leu asn ile asp gly ala val thr ser 675 680 685gly leu tyr val thr gly lys asp asn tyr gly ser ile ser leu gly 690 695 700asn ile thr asp thr met thr phe asp val thr val his asn leu ser705 710 715 720asn lys asp lys thr leu arg tyr asp thr glu leu leu thr asp his 725 730 735val asp pro gln lys gly arg phe thr leu thr ser his ser leu lys 740 745 750thr tyr gln gly gly glu val thr val pro ala asn gly lys val thr 755 760 765val arg val thr met asp val ser gln phe thr lys glu leu thr lys 770 775 780gln met pro asn gly tyr tyr leu glu gly phe val arg phe arg asp785 790 795 800ser gln asp asp gln leu asn arg val asn ile pro phe val gly phe 805 810 815lys gly gln phe glu asn leu ala val ala glu glu ser ile tyr arg 820 825 830leu lys ser gln gly lys thr gly phe tyr phe asp glu ser gly pro 835 840 845lys asp asp ile tyr val gly lys his phe thr gly leu val thr leu 850 855 860gly ser glu thr asn val ser thr lys thr ile ser asp asn gly leu865 870 875 880his thr leu gly thr phe lys asn ala asp gly lys phe ile leu glu 885 890 895lys asn ala gln gly asn pro val leu ala ile ser pro asn gly asp 900 905 910asn asn gln asp phe ala ala phe lys gly val phe leu arg lys tyr 915 920 925gln gly leu lys ala ser val tyr his ala ser asp lys glu his lys 930 935 940asn pro leu trp val ser pro glu ser phe lys gly asp lys asn phe945 950 955 960asn ser asp ile arg phe ala lys ser thr thr leu leu gly thr ala 965 970 975phe ser gly lys ser leu thr gly ala glu leu pro asp gly his tyr 980 985 990his tyr val val ser tyr tyr pro asp val val gly ala lys arg gln 995 1000 1005glu met thr phe asp met ile leu asp arg gln lys pro val leu 1010 1015 1020ser gln ala thr phe asp pro glu thr asn arg phe lys pro glu 1025 1030 1035pro leu lys asp arg gly leu ala gly val arg lys asp ser val 1040 1045 1050phe tyr leu glu arg lys asp asn lys pro tyr thr val thr ile 1055 1060 1065asn asp ser tyr lys tyr val ser val glu asp asn lys thr phe 1070 1075 1080val glu arg gln ala asp gly ser phe ile leu pro leu asp lys 1085 1090 1095ala lys leu gly asp phe tyr tyr met val glu asp phe ala gly 1100 1105 1110asn val ala ile ala lys leu gly asp his leu pro gln thr leu 1115 1120 1125gly lys thr pro ile lys leu lys leu thr asp gly asn tyr gln 1130 1135 1140thr lys glu thr leu lys asp asn leu glu met thr gln ser asp 1145 1150 1155thr gly leu val thr asn gln ala gln leu ala val val his arg 1160 1165 1170asn gln pro gln ser gln leu thr lys met asn gln asp phe phe 1175 1180 1185ile ser pro asn glu asp gly asn lys asp phe val ala phe lys 1190 1195 1200gly leu lys asn asn val tyr asn asp leu thr val asn val tyr 1205 1210 1215ala lys asp asp his gln lys gln thr pro ile trp ser ser gln 1220 1225 1230ala gly ala ser val ser ala ile glu ser thr ala trp tyr gly 1235 1240 1245ile thr ala arg gly ser lys val met pro gly asp tyr gln tyr 1250 1255 1260val val thr tyr arg asp glu his gly lys glu his gln lys gln 1265 1270 1275tyr thr ile ser val asn asp lys lys pro met ile thr gln gly 1280 1285 1290arg phe asp thr ile asn gly val asp his phe thr pro asp lys 1295 1300 1305thr lys ala leu asp ser ser gly ile val arg glu glu val phe 1310 1315 1320tyr leu ala lys lys asn gly arg lys phe asp val thr glu gly 1325 1330 1335lys asp gly ile thr val ser asp asn lys val tyr ile pro lys 1340 1345 1350asn pro asp gly ser tyr thr ile ser lys arg asp gly val thr 1355 1360 1365leu ser asp tyr tyr tyr leu val glu asp arg ala gly asn val 1370 1375 1380ser phe ala thr leu arg asp leu lys ala val gly lys asp lys 1385 1390 1395ala val val asn phe gly leu asp leu pro val pro glu asp lys 1400 1405 1410gln ile val asn phe thr tyr leu val arg asp ala asp gly lys 1415 1420 1425pro ile glu asn leu glu tyr tyr asn asn ser gly asn ser leu 1430 1435 1440ile leu pro tyr gly lys tyr thr val glu leu leu thr tyr asp 1445 1450 1455thr asn ala ala lys leu glu ser asp lys ile val ser phe thr 1460 1465 1470leu ser ala asp asn asn phe gln gln val thr phe lys ile thr 1475 1480 1485met leu ala thr ser gln ile thr ala his phe asp his leu leu 1490 1495 1500pro glu gly ser arg val ser leu lys thr ala gln asp gln leu 1505 1510 1515ile pro leu glu gln ser leu tyr val pro lys ala tyr gly lys 1520 1525 1530thr val gln glu gly thr tyr glu val val val ser leu pro lys 1535 1540 1545gly tyr arg ile glu gly asn thr lys val asn thr leu pro asn 1550 1555 1560glu val his glu leu ser leu arg leu val lys val gly asp ala 1565 1570 1575ser asp ser thr gly asp his lys val met ser lys asn asn ser 1580 1585 1590gln ala leu thr ala ser ala thr pro thr lys ser thr thr ser 1595 1600 1605ala thr ala lys ala leu pro ser thr gly glu lys met gly leu 1610 1615 1620lys leu arg ile val gly leu val leu leu gly leu thr cys val 1625 1630 1635phe ser arg lys lys ser thr lys asp 1640 1645<210> 5<211> 543<212> prt<213> 化脓性链球菌<400> 5met ala ser glu ser asn lys gln asn thr ala ser thr glu thr thr1 5 10 15thr thr asn glu gln pro lys pro glu ser ser glu leu thr thr glu 20 25 30lys ala gly gln lys thr asp asp met leu asn ser asn asp met ile 35 40 45lys leu ala pro lys glu met pro leu glu ser ala glu lys glu glu 50 55 60lys lys ser glu asp lys lys lys ser glu glu asp his thr glu glu65 70 75 80ile asn asp lys ile tyr ser leu asn tyr asn glu leu glu val leu 85 90 95ala lys asn gly glu thr ile glu asn phe val pro lys glu gly val 100 105 110lys lys ala asp lys phe ile val ile glu arg lys lys lys asn ile 115 120 125asn thr thr pro val asp ile ser ile ile asp ser val thr asp arg 130 135 140thr tyr pro ala ala leu gln leu ala asn lys gly phe thr glu asn145 150 155 160lys pro asp ala val val thr lys arg asn pro gln lys ile his ile 165 170 175asp leu pro gly met gly asp lys ala thr val glu val asn asp pro 180 185 190thr tyr ala asn val ser thr ala ile asp asn leu val asn gln trp 195 200 205his asp asn tyr ser gly gly asn thr leu pro ala arg thr gln tyr 210 215 220thr glu ser met val tyr ser lys ser gln ile glu ala ala leu asn225 230 235 240val asn ser lys ile leu asp gly thr leu gly ile asp phe lys ser 245 250 255ile ser lys gly glu lys lys val met ile ala ala tyr lys gln ile 260 265 270phe tyr thr val ser ala asn leu pro asn asn pro ala asp val phe 275 280 285asp lys ser val thr phe lys glu leu gln arg lys gly val ser asn 290 295 300glu ala pro pro leu phe val ser asn val ala tyr gly arg thr val305 310 315 320phe val lys leu glu thr ser ser lys ser asn asp val glu ala ala 325 330 335phe ser ala ala leu lys gly thr asp val lys thr asn gly lys tyr 340 345 350ser asp ile leu glu asn ser ser phe thr ala val val leu gly gly 355 360 365asp ala ala glu his asn lys val val thr lys asp phe asp val ile 370 375 380arg asn val ile lys asp asn ala thr phe ser arg lys asn leu ala385 390 395 400tyr pro ile ser tyr thr ser val phe leu lys asn asn lys ile ala 405 410 415gly val asn asn arg thr glu tyr val glu thr thr ser thr glu tyr 420 425 430thr ser gly lys ile asn leu ser his gln gly ala tyr val ala gln 435 440 445tyr glu ile leu trp asp glu ile asn tyr asp asp lys gly lys glu 450 455 460val ile thr lys arg arg trp asp asn asn trp tyr ser lys thr ser465 470 475 480pro phe ser thr val ile pro leu gly ala asn ser arg asn ile arg 485 490 495ile met ala arg glu cys thr gly leu ala phe glu trp trp arg lys 500 505 510val ile asp glu arg asp val lys leu ser lys glu ile asn val asn 515 520 525ile ser gly ser thr leu ser pro tyr gly ser ile thr tyr lys 530 535 540<210> 6<211> 571<212> prt<213> 化脓性链球菌<400> 6met ser asn lys lys thr phe lys lys tyr ser arg val ala gly leu1 5 10 15leu thr ala ala leu ile ile gly asn leu val thr ala asn ala glu 20 25 30ser asn lys gln asn thr ala ser thr glu thr thr thr thr asn glu 35 40 45gln pro lys pro glu ser ser glu leu thr thr glu lys ala gly gln 50 55 60lys thr asp asp met leu asn ser asn asp met ile lys leu ala pro65 70 75 80lys glu met pro leu glu ser ala glu lys glu glu lys lys ser glu 85 90 95asp lys lys lys ser glu glu asp his thr glu glu ile asn asp lys 100 105 110ile tyr ser leu asn tyr asn glu leu glu val leu ala lys asn gly 115 120 125glu thr ile glu asn phe val pro lys glu gly val lys lys ala asp 130 135 140lys phe ile val ile glu arg lys lys lys asn ile asn thr thr pro145 150 155 160val asp ile ser ile ile asp ser val thr asp arg thr tyr pro ala 165 170 175ala leu gln leu ala asn lys gly phe thr glu asn lys pro asp ala 180 185 190val val thr lys arg asn pro gln lys ile his ile asp leu pro gly 195 200 205met gly asp lys ala thr val glu val asn asp pro thr tyr ala asn 210 215 220val ser thr ala ile asp asn leu val asn gln trp his asp asn tyr225 230 235 240ser gly gly asn thr leu pro ala arg thr gln tyr thr glu ser met 245 250 255val tyr ser lys ser gln ile glu ala ala leu asn val asn ser lys 260 265 270ile leu asp gly thr leu gly ile asp phe lys ser ile ser lys gly 275 280 285glu lys lys val met ile ala ala tyr lys gln ile phe tyr thr val 290 295 300ser ala asn leu pro asn asn pro ala asp val phe asp lys ser val305 310 315 320thr phe lys glu leu gln arg lys gly val ser asn glu ala pro pro 325 330 335leu phe val ser asn val ala tyr gly arg thr val phe val lys leu 340 345 350glu thr ser ser lys ser asn asp val glu ala ala phe ser ala ala 355 360 365leu lys gly thr asp val lys thr asn gly lys tyr ser asp ile leu 370 375 380glu asn ser ser phe thr ala val val leu gly gly asp ala ala glu385 390 395 400his asn lys val val thr lys asp phe asp val ile arg asn val ile 405 410 415lys asp asn ala thr phe ser arg lys asn pro ala tyr pro ile ser 420 425 430tyr thr ser val phe leu lys asn asn lys ile ala gly val asn asn 435 440 445arg thr glu tyr val glu thr thr ser thr glu tyr thr ser gly lys 450 455 460ile asn leu ser his gln gly ala tyr val ala gln tyr glu ile leu465 470 475 480trp asp glu ile asn tyr asp asp lys gly lys glu val ile thr lys 485 490 495arg arg trp asp asn asn trp tyr ser lys thr ser pro phe ser thr 500 505 510val ile pro leu gly ala asn ser arg asn ile arg ile met ala arg 515 520 525glu cys thr gly leu ala trp glu trp trp arg lys val ile asp glu 530 535 540arg asp val lys leu ser lys glu ile asn val asn ile ser gly ser545 550 555 560thr leu ser pro tyr gly ser ile thr tyr lys 565 570<210> 7<211> 536<212> prt<213> 人工序列<220><223> 白喉毒素的非毒性突变体<400> 7met gly ala asp asp val val asp ser ser lys ser phe val met glu1 5 10 15asn phe ser ser tyr his gly thr lys pro gly tyr val asp ser ile 20 25 30gln lys gly ile gln lys pro lys ser gly thr gln gly asn tyr asp 35 40 45asp asp trp lys glu phe tyr ser thr asp asn lys tyr asp ala ala 50 55 60gly tyr ser val asp asn glu asn pro leu ser gly lys ala gly gly65 70 75 80val val lys val thr tyr pro gly leu thr lys val leu ala leu lys 85 90 95val asp asn ala glu thr ile lys lys glu leu gly leu ser leu thr 100 105 110glu pro leu met glu gln val gly thr glu glu phe ile lys arg phe 115 120 125gly asp gly ala ser arg val val leu ser leu pro phe ala glu gly 130 135 140ser ser ser val glu tyr ile asn asn trp glu gln ala lys ala leu145 150 155 160ser val glu leu glu ile asn phe glu thr arg gly lys arg gly gln 165 170 175asp ala met tyr glu tyr met ala gln ala cys ala gly asn arg val 180 185 190arg arg ser val gly ser ser leu ser cys ile asn leu asp trp asp 195 200 205val ile arg asp lys thr lys thr lys ile glu ser leu lys glu his 210 215 220gly pro ile lys asn lys met ser glu ser pro asn lys thr val ser225 230 235 240glu glu lys ala lys gln tyr leu glu glu phe his gln thr ala leu 245 250 255glu his pro glu leu ser glu leu lys thr val thr gly thr asn pro 260 265 270val phe ala gly ala asn tyr ala ala trp ala val asn val ala gln 275 280 285val ile asp ser glu thr ala asp asn leu glu lys thr thr ala ala 290 295 300leu ser ile leu pro gly ile gly ser val met gly ile ala asp gly305 310 315 320ala val his his asn thr glu glu ile val ala gln ser ile ala leu 325 330 335ser ser leu met val ala gln ala ile pro leu val gly glu leu val 340 345 350asp ile gly phe ala ala tyr asn phe val glu ser ile ile asn leu 355 360 365phe gln val val his asn ser tyr asn arg pro ala tyr ser pro gly 370 375 380his lys thr gln pro phe leu his asp gly tyr ala val ser trp asn385 390 395 400thr val glu asp ser ile ile arg thr gly phe gln gly glu ser gly 405 410 415his asp ile lys ile thr ala glu asn thr pro leu pro ile ala gly 420 425 430val leu leu pro thr ile pro gly lys leu asp val asn lys ser lys 435 440 445thr his ile ser val asn gly arg lys ile arg met arg cys arg ala 450 455 460ile asp gly asp val thr phe cys arg pro lys ser pro val tyr val465 470 475 480gly asn gly val his ala asn leu his val ala phe his arg ser ser 485 490 495ser glu lys ile his ser asn glu ile ser ser asp ser ile gly val 500 505 510leu gly tyr gln lys thr val asp his thr lys val asn ser lys leu 515 520 525ser leu phe phe glu ile lys ser 530 535
背景技术:
技术实现思路
- 还没有人留言评论。精彩留言会获得点赞!