一种负载牙龈间充质干细胞外泌体的矿化胶原凝胶及其制备方法
1.本发明属于生物技术领域,特别是涉及一种用于牙周骨组织修复的负载外泌体的矿化胶原凝胶及其制备方法。
背景技术:
2.牙周炎是以牙周支持组织破坏为特征的疾病,牙槽骨吸收是其主要临床表现之一,随着病程的进展最终将导致牙齿的松动脱落。牙周炎在成人中发病率很高,是其失牙的主要原因。翻瓣植骨术是治疗牙槽骨缺损的有效方法之一,但常规骨移植材料中不含有促进骨组织再生的生物活性成分,缺乏骨诱导性,因此单纯应用骨移植材料进行骨修复难以获得理想的修复效果,而骨重塑是一种复杂的机制,涉及成骨细胞、破骨细胞、干细胞、巨噬细胞等多种细胞的相互作用。
3.牙龈间充质干细胞(gmscs)是一类存在于牙龈固有层的多能干细胞,具有优越的自我更新和多向分化潜能,抗炎和促进组织再生能力强。而近年来多项研究已表明,间充质干细胞的治疗作用主要是其旁分泌作用所介导,因此对间充质干细胞的研究逐渐延伸至其旁分泌产物,特别是外泌体通过调节机体微环境对组织进行修复。外泌体是由细胞分泌的活性细胞外囊泡,粒径仅为30-150nm,富含脂质、蛋白质和遗传物质,是细胞间通讯的重要介质,可作为载体将遗传信息传递到靶细胞,改变其功能,进而调节机体免疫微环境、促进新骨形成、结合生物材料促进骨修复、加速伤口愈合和调节血管生成等。宿主巨噬细胞的极化是组织重塑的重要因素之一,巨噬细胞长期处于抗炎表型(m1型)将会影响生物材料促进组织再生的能力,而抗炎表型的巨噬细胞(m2型)则有利于组织再生和重塑。已有研究表明,牙龈间充质干细胞外泌体可促进炎症环境下的巨噬细胞由m1型向m2型极化,并抑制炎症反应,因此在骨再生领域的研究具有广阔前景。
4.组织工程中的另一要素是生物支架材料,它有利于促进骨缺损处硬组织的再生,最终在原位被降解并被新形成的组织所替代。其中矿化胶原的结构与天然骨骼相似,机械性能良好,具有良好的骨诱导性及优越的生物相容性,可更快的被机体吸收,矿化胶原中的孔隙和粗糙的表面为组织修复与再生过程中的细胞黏附和生长提供了理想的微环境,并且矿化支架材料本身即足以诱导细胞成骨基因的表达,基质重塑以及矿物质形成,有利于骨再生,因此是一种理想的骨修复组织工程支架。壳聚糖是一种具有高生物相容性的高分子材料,具有来源广泛、无毒、免疫原性低和促进愈合等优点,还有良好的吸附、载药和抗菌性能,矿化胶原-壳聚糖凝胶可改善单一组分的不足,显著提升矿化胶原的机械性能和释放能力,并且可以明显改善外泌体在局部的驻留率。因此,开发一种包载间充质干细胞外泌体的矿化胶原凝胶在翻瓣植骨术后促进牙周组织再生方面具有重要临床应用价值。
技术实现要素:
5.针对上述背景中存在的不足,本发明专利目的是提供一种负载牙龈间充质干细胞
外泌体的矿化胶原凝胶及其制备方法。
6.为解决上述技术问题,本发明采用的一个技术方案是:一种负载牙龈间充质干细胞外泌体的矿化胶原凝胶,包括牙龈间充质干细胞外泌体、矿化胶原粉体、壳聚糖和β-甘油磷酸钠;
7.所述牙龈间充质干细胞外泌体由超速离心法从牙龈间充质干细胞条件培养液中分离得到;
8.矿化胶原水凝胶由同步进行的胶原自组装与羟基磷灰石形成制备;所述矿化胶原水凝胶包括:羟基磷灰石、胶原溶液、乙酸溶液、nah2po4溶液、cacl2溶液和naoh溶液。
9.进一步地说,所述矿化胶原凝胶的组分含量为:干细胞外泌体40μg/ml,矿化胶原2-20mg/ml,2%(w/v)壳聚糖溶液,56%(w/v)β-甘油磷酸钠溶液。
10.所述的负载牙龈间充质干细胞外泌体的矿化胶原凝胶的制备方法,包括如下步骤:
11.(1)外泌体提取
12.通过梯度离心法及超速离心法,在牙龈间充质干细胞条件培养液中提取外泌体并鉴定。
13.(2)矿化胶原制备
14.通过同步进行的胶原自组装与羟基磷灰石合成制备矿化胶原水凝胶,随后将水凝胶洗涤后冷冻干燥,获得多孔支架,进一步粉碎后获得矿化胶原粉体。
15.(3)外泌体的温敏凝胶负载
16.稀释外泌体,与矿化胶原粉体混合为悬浊液;
17.配制壳聚糖溶液并加入β-甘油磷酸钠溶液后添加前述的悬浊液并混匀搅拌,即获得负载有外泌体的矿化胶原温敏凝胶。
18.本发明的有益效果至少具有以下几点:
19.1、本发明的负载牙龈间充质干细胞外泌体的矿化胶原凝胶具有抑制牙周炎症和促进牙周骨组织再生的作用,牙龈间充质干细胞外泌体可以抑制巨噬细胞向促炎表型极化和炎症因子的分泌,促进其向抗炎表型极化,进而调节局部免疫微环境。
20.2、本发明的凝胶含有矿化胶原,是增加牙周骨量的潜在方法,矿化胶原不仅具有多孔、粗糙的网络结构,有利于细胞的浸润和附着,还具有骨诱导性,在牙槽骨重塑过程中可刺激新骨形成,矿化胶原的生物相容性良好,在骨形成的早期阶段可为成骨细胞的生长提供支撑,随后可降解,为新骨形成提供空间。
21.3、本发明的凝胶为壳聚糖/β甘油磷酸钠凝胶,具有温敏特性,成胶后可增强矿化胶原支架的机械强度,并缓释组合成分中的牙龈间充质干细胞外泌体和骨形成所需的ca、p等离子,壳聚糖凝胶的抑菌性还可为骨再生维持良好的免疫微环境。
22.4、壳聚糖凝胶可以在行牙周手术时注射于炎症状态下的骨缺损区,缓释牙龈间充质干细胞外泌体,有利于外泌体的靶向修复,因此该组合凝胶为大分子药物提供了新的给药途径,具有广阔的研究前景和重要的临床价值。
附图说明
23.图1是本发明外泌体的形态图;
24.图2是本发明外泌体表征的鉴定图;
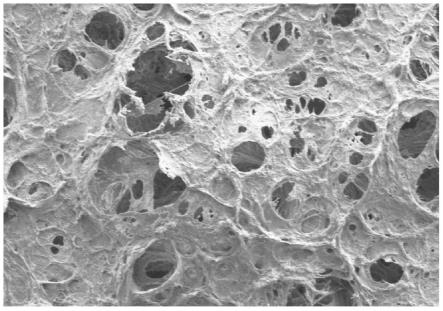
25.图3是本发明负载矿化胶原、外泌体的壳聚糖/β-甘油磷酸钠凝胶的扫描电镜图;
26.图4是本发明培养thp-1来源的巨噬细胞的分组图;
27.图5是本发明外泌体-矿化胶原水凝胶在体外对巨噬细胞mrna的影响结果图。
具体实施方式
28.下面结合附图对本发明的较佳实施例进行详细阐述,以使本发明的优点和特征能更易于被本领域技术人员理解,从而对本发明的保护范围做出更为清楚明确的界定。
29.试验1.牙龈间充质干细胞的分离培养和鉴定
30.(1)细胞培养
31.所获取的牙龈组织均取自因正畸拔牙或阻生齿拔除而就诊于口腔科的牙周健康状况良好的年轻患者。样本取得后,立即放入含有5%青链霉素混合液的培养液里。在生物安全柜中用含5%双抗的pbs多次冲洗,初步刮除牙龈上皮组织。将牙龈组织浸泡在浓度为2mg/ml的dispase酶中,37℃水浴消化50min,使用无菌刀片彻底刮除上皮组织后将牙龈组织分割为数个约1mm2的小组织块后将其浸泡在浓度为2mg/ml的i型胶原酶中,水浴消化50min。离心上述混合液并将沉淀重悬于含有20%体积分数的胎牛血清(fbs)和2%体积分数的双抗α-mem培养液中,充分混匀后置于细胞培养瓶内,置于细胞培养箱(37℃/5%co2)内培养。当细胞呈长梭形、成纤维细胞样,细胞融合度约为70%-80%时,进行传代培养并用有限稀释法进行筛选。
32.(2)细胞鉴定
33.倒置显微镜观察细胞的形态;通过集落形成实验评估细胞形成单克隆的潜能;通过流式细胞术对间充质干细胞表面标志物cd73、cd90和cd105进行分析;对细胞进行成骨和成脂诱导后使用茜素红染色和油红o染色分析其多向分化潜能;
34.试验2.外泌体的提取和鉴定
35.(1)外泌体的提取
36.当p2-5代gmscs的融合度约为60%-70%时,将培养液换为含10%无外泌体fbs的培养液继续培养。48h后,收集gmscs条件培养液,在4℃条件下以300g,20min;2000g,30min;10000g,30min;110000g,70min;110000g,70min进行梯度离心。离心结束后小心去除全部液体,使用100μl pbs反复冲洗离心管底部,将分离出的外泌体全部重悬于pbs中。
37.(2)外泌体的鉴定
38.通过透射电子显微镜对外泌体的形态进行观察;用western blot法对外泌体表面标志物进行鉴定;使用纳米粒度分析仪对外泌体的粒径进行分析;bca法测定外泌体的浓度。
39.透射电子显微镜示,使用超速离心法在牙龈间充质干细胞条件培养液中所获提取物为椭圆形、杯状形态,为外泌体的典型形态(如图1所示)。western blot结果表明,该提取物阳性表达外泌体标志物cd9、cd63、cd81和alix;纳米粒度分析仪分析该提取物粒径约为100nm。(如图2所示)。综上,该提取物为牙龈间充质干细胞外泌体。
40.试验3.外泌体-矿化胶原水凝胶的制备
41.(1)矿化胶原的制备
42.通过同步进行的胶原自组装与羟基磷灰石合成制备矿化胶原水凝胶,随后将水凝胶洗涤后冷冻干燥,获得多孔支架,进一步粉碎后获得矿化胶原粉体。
43.具体操作为:首先,将适量溶于浓度为0.3m乙酸溶液(hac)的酸性胶原储备液在匀速搅拌下加入一定量的1.2m nah2po4溶液,以2m naoh调节至中性。搅拌1h使溶液充分混合,将混合溶液的ph调节至9.0
±
0.2,搅拌状态下逐滴加入浓度为2m的cacl2溶液,使体系中的ca/p比为1.67,再次将ph调节并保持在9.0
±
0.2,以100rpm匀速搅拌2h。以上反应均在4℃条件下进行。将以上获得的白色溶胶转移至5ml或10ml离心管,在低温下以1000rpm离心5min去除气泡后转移至37℃水浴中,引发胶原自组装并促进羟基磷灰石形成。在37℃保温24小时后,将获取的白色凝胶以去离子水充分浸泡72h,随后进行冷冻干燥,获得多孔矿化胶原支架。液氮淬冷后研磨,获得矿化胶原粉体。
44.(2)外泌体的温敏凝胶负载(壳聚糖+β-甘油磷酸钠)
45.将外泌体原液的浓度稀释至200μg/ml后与矿化胶原粉体混合均匀形成外泌体-矿化胶原悬浊液;将壳聚糖在室温下溶于0.1m乙酸溶液,配成终浓度为2%的壳聚糖溶液;将2%的壳聚糖溶液与56%(w/v)β-甘油磷酸钠按照7:3比例混合均匀;将外泌体-矿化胶原悬浊液与前述混合液按照体积比1:5比例混合,保证外泌体的浓度为40μg/ml,在4℃下搅拌均匀后置于37℃,1-5分钟后即获得负载有外泌体的温敏凝胶,其扫描电镜图如图3所示。
46.本体系中,外泌体和矿化胶原促进成骨,壳聚糖能够抗菌,同时具有温敏特性,可作为可注射凝胶用于牙周炎状态下的骨修复或骨扩增。
47.试验4.外泌体-矿化胶原水凝胶在体外对巨噬细胞mrna的鉴定
48.如图4所示,培养thp-1来源的巨噬细胞并分为三组,空白组每孔加入1ml 1640完全培养基;lps组每孔加入1ml含100ng/ml lps和20ng/ml ifn-γ的1640培养基;外泌体-水凝胶组使用transwell小室,下室加入1ml含100ng/ml lps和20ng/ml ifn-γ的1640培养基,上室放置外泌体-矿化胶原壳聚糖水凝胶样本与巨噬细胞进行共培养。48h后,通过trizol法提取各组巨噬细胞mrna后,使用qrt-pcr法对相关mrna进行分析。
49.qrt-pcr结果示,lps/ifn-γ联合刺激后,巨噬细胞炎性基因tnf-α和il-6mrna的表达水平与空白组相比增高(p<0.05)。经外泌体-矿化胶原壳聚糖水凝胶与巨噬细胞进行共培养48h后,tnf-α和il-6mrna的表达水平较lps组明显下降(p<0.05),抗炎基因il-10mrna的表达水平较空白组和lps组显著提升(p<0.05)(如图5所示)。表明外泌体-矿化胶原壳聚糖水凝胶可在mrna水平上抑制巨噬细胞的炎症反应。
50.以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作的等效结构变换,或直接或间接运用在其他相关的技术领域,均同理包括在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1