电阻抗断层成像模型、实验装置和方法与流程
1.本公开涉及医疗器械领域,具体涉及电阻抗断层成像模型、实验装置和方法。
背景技术:
2.电阻抗断层成像(electrical impedance tomography,eit)通过在人体胸部安放的电极组,在激励安全电流的同时测量相应的体表电压,然后利用激励与测量数据,按照相应的图像重建算法,获得能够反映胸腔内部电阻抗分布的动态图像。
3.由于人体正常肺泡在充气情况下具有较高的电阻率,所以eit在床旁可实时观察肺脏的通气状况,从而反映人体呼吸的生理或病理状态。但是由于人体的eit信号相对微弱,因此,建立精确的数据采集系统和图像重建算法是eit成像的基本要素。
4.目前,在呼吸eit领域中,一种普遍认可的、衡量eit数据采集系统和图像重建算法精确程度的方法是利用物理模型进行数据测量与图像重建实验,并进一步分析数据或图像的信噪比等指标。因此,建立准确的物理模型实验装置,对eit数据测量系统和图像重建算法的评估与改进,具有重要意义。
5.但是,目前的大多数eit胸腔物理模型都存在两点主要不足在于:一、仅考虑了肺脏组织,忽略了其他胸腔组织(心脏、骨结构等)对eit的影响;二、现有技术虽然也有类似三维构建模技术公开,但也存在如下重要缺陷:1、一种现有技术所公开的方法是将左右肺3d打印成非实心的空腔组织;如此会导致肺脏的电阻率等同于空气的电阻抗率;而实际的肺生理结构异常复杂,分为肺实质和肺间质;只有肺实质类似与空腔结构;所以整体肺充气情况下的电阻率较空气的电阻率小很多。2、另一种现有技术所公开的方法考虑到采用混合物质构建胸腔器官组织;但所设计的目标器官电阻率过大,超出了人体正常范围。所以,该领域需要具有三维结构,且能够反映胸腔各个脏器真实形状与电阻率特征的物理模型实验装置。标准化建立的该物理模型实验装置可以用于eit数据采集系统和图像重建算法的校准,或者用于临床教学等。
技术实现要素:
6.为了解决相关技术中的问题,本公开实施例提供了一种电阻抗断层成像模型、实验装置和方法。
7.第一方面,本公开实施例中提供了一种电阻抗断层成像模型,包括:
8.三维打印的胸腔骨骼模型、肺脏模型和心脏模型,
9.胸腔骨骼模型、肺脏模型和心脏模型按人体中对应的解剖位置组合,
10.所述胸腔骨骼模型的电阻率为第一电阻率,用于模拟人体的胸腔的电阻率,
11.所述肺脏模型的电阻率为第二电阻率,用于模拟人体的肺脏的电阻率,
12.所述心脏模型的电阻率为第三电阻率,用于模拟人体的心脏的电阻率。
13.结合第一方面,本公开在第一方面的第一种实现方式中,
14.所述胸腔骨骼模型、肺脏模型和心脏模型由下述方式得到:
15.对人体的计算机断层扫描图像进行三维重建,得到三维重建模型;
16.对所述三维重建模型进行分割、修补、平滑、查错,得到计算机三维打印模型;
17.基于所述计算机三维打印模型进行三维打印,得到所述胸腔骨骼模型、肺脏模型和心脏模型。
18.结合第一方面,本公开在第一方面的第二种实现方式中,
19.所述胸腔骨骼模型、肺脏模型和心脏模型的材质为丙烯腈-丁二烯-苯乙烯共聚物和炭黑的混合物。
20.结合第一方面的第二种实现方式,本公开在第一方面的第三种实现方式中,
21.所述胸腔骨骼模型中的胸骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第一混合比;和/或
22.所述胸腔骨骼模型中的肋骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第二混合比;和/或
23.所述胸腔骨骼模型中的脊椎骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第三混合比;和/或
24.所述肺脏模型的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第四混合比;和/或
25.所述心脏模型的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第五混合比。
26.结合第一方面的第三种实现方式,本公开在第一方面的第四种实现方式中,
27.所述第一混合比为4.46
±
0.22:1;和/或
28.所述第二混合比为4.01
±
0.20:1;和/或
29.所述第三混合比为4.09
±
0.20:1;和/或
30.所述第四混合比为3.84
±
0.19:1;和/或
31.所述第五混合比为3.82
±
0.19:1。
32.第二方面,本公开实施例中提供了一种实验装置,其特征在于,包括:
33.根据权利要求1-5任一项所述的电阻抗断层成像模型;
34.绝缘容器,所述电阻抗断层成像模型固定在所述绝缘容器中;
35.电极组,固定于所述绝缘容器的内表面;
36.导电溶液,容置于所述绝缘容器中,并浸没所述电阻抗断层成像模型。
37.结合第二方面,本公开在第二方面的第一种实现方式中,
38.所述绝缘容器包括:有机玻璃椭圆柱状容器,和/或
39.所述绝缘容器的壁厚为4.95-5.05毫米,和/或
40.所述绝缘容器的高度为396-404毫米,和/或
41.所述绝缘容器的椭圆内长轴的长度为346.5-353.5毫米,和/或
42.所述绝缘容器的椭圆内短轴的长度为297-303毫米。
43.结合第二方面,本公开在第二方面的第二种实现方式中,
44.所述电极组的层数为第一值,每层中的电极数为第二值,每层中的电极在所述绝缘容器的内表面均匀分布。
45.结合第二方面的第二种实现方式,本公开在第二方面的第三种实现方式中,
46.所述第一值为2,所述第二值为16。
47.结合第二方面的第三种实现方式,本公开在第二方面的第四种实现方式中,
48.第一层电极组和所述电阻抗断层成像模型的第四第五肋间位置相对应,
49.第二层电极组比第一层电极组高100毫米。
50.结合第二方面,本公开在第二方面的第五种实现方式中,
51.所述导电溶液为生理盐水。
52.结合第二方面,本公开在第二方面的第六种实现方式中,
53.还包括:
54.滑动变阻器组,与所述电极组电性连接。
55.第三方面,本公开实施例中提供了一种构建电阻抗断层成像模型实验装置的方法,其特征在于,包括:
56.获取人体的计算机断层扫描图像;
57.根据所述计算机断层扫描图像进行三维重建,得到三维重建模型;
58.对所述三维重建模型进行分割、修补、平滑、查错,得到计算机三维打印模型;
59.基于所述计算机三维打印模型进行三维打印,得到胸腔骨骼模型、肺脏模型和心脏模型;
60.组合所述胸腔骨骼模型、肺脏模型和心脏模型,得到电阻抗断层成像模型。
61.结合第三方面,本公开在第三方面的第一种实现方式中,还包括:
62.构建固定了电极组的绝缘容器,所述电极组固定于所述绝缘容器的内表面;
63.将所述电阻抗断层成像模型固定在所述绝缘容器中;
64.在所述绝缘容器中加入导电溶液,所述导电溶液浸没所述电阻抗断层成像模型。
65.本公开实施例提供的技术方案可以包括以下有益效果:
66.根据本公开实施例提供的技术方案,通过电阻抗断层成像模型,包括:三维打印的胸腔骨骼模型、肺脏模型和心脏模型,胸腔骨骼模型、肺脏模型和心脏模型按人体中对应的解剖位置组合,所述胸腔骨骼模型的电阻率为第一电阻率,用于模拟人体的胸腔的电阻率,所述肺脏模型的电阻率为第二电阻率,用于模拟人体的肺脏的电阻率,所述心脏模型的电阻率为第三电阻率,用于模拟人体的心脏的电阻率,从而得到精确的三维打印的胸腔骨骼模型、肺脏模型和心脏模型,使得模型更加符合人体的真实解剖结构。
67.而且,真实人体的不同器官的电阻率不同,同一器官在不同频率的激励信号下的电阻率也不相同。而采用不同混合比例的abs/cb精确模拟了胸腔骨骼、心脏、肺脏的不同电阻率,也可以模拟例如肺脏的同一器官在不同频率的激励信号下的不同电阻率。从而对人体胸部的电阻率进行三维精确建模,方便对eit数据采集系统和图像重建算法进行校准和评估,也可方便地用于临床教学等其它用途。
68.应当理解的是,以上的一般描述和后文的细节描述仅是示例性和解释性的,并不能限制本公开。
附图说明
69.结合附图,通过以下非限制性实施方式的详细描述,本公开的其它特征、目的和优点将变得更加明显。在附图中:
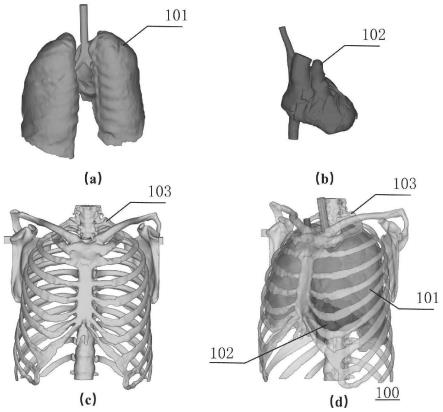
70.图1示出根据本公开一实施例的三维打印的电阻抗断层成像模型;
71.图2示出根据本公开一实施例的容纳电阻抗断层成像模型的实验装置;
72.图3示出根据本公开一实施例的制作电阻抗断层成像模型的方法的流程图;
73.图4示出根据本公开一实施例的制作电阻抗断层成像模型实验装置的方法的流程图。
具体实施方式
74.下文中,将参考附图详细描述本公开的示例性实施方式,以使本领域技术人员可容易地实现它们。此外,为了清楚起见,在附图中省略了与描述示例性实施方式无关的部分。
75.在本公开中,应理解,诸如“包括”或“具有”等的术语旨在指示本说明书中所公开的标签、数字、步骤、行为、部件、部分或其组合的存在,并且不欲排除一个或多个其他标签、数字、步骤、行为、部件、部分或其组合存在或被添加的可能性。
76.另外还需要说明的是,在不冲突的情况下,本公开中的实施例及实施例中的标签可以相互组合。下面将参考附图并结合实施例来详细说明本公开。
77.电阻抗断层成像(electrical impedance tomography,eit)通过在人体胸部安放的电极组,在激励安全电流的同时测量相应的体表电压,然后利用激励与测量数据,按照相应的图像重建算法,获得能够反映胸腔内部电阻抗分布的动态图像。
78.由于人体正常肺泡在充气情况下具有较高的电阻率,所以eit在床旁可实时观察肺脏的通气状况,从而反映人体呼吸的生理或病理状态。但是由于人体的eit信号相对微弱,因此,建立精确的数据采集系统和图像重建算法是eit成像的基本要素。
79.目前,在呼吸eit领域中,一种普遍认可的、衡量eit数据采集系统和图像重建算法精确程度的方法是利用物理模型进行数据测量与图像重建实验,并进一步分析数据或图像的信噪比等指标。因此,建立准确的物理模型实验装置,对eit数据测量系统和图像重建算法的评估与改进,具有重要意义。
80.但是,目前的eit胸腔物理模型都存在两点主要缺陷:一、仅考虑了肺脏组织,忽略了其他胸腔组织(心脏、骨结构等)对eit的影响;二、仅考虑了一个胸腔断层的情况,只构建了单一层的肺物理模型,忽略了eit电流呈场分布,胸腔脏器是三维结构的基本事实。所以,该领域需要具有三维结构,且能够反映胸腔各个脏器真实形状与电阻率特征的物理模型实验装置。标准化建立的该物理模型实验装置可以用于eit数据采集系统和图像重建算法的校准,或者用于临床教学等。
81.为解决上述问题,本公开提出了一种电阻抗断层成像模型、实验装置和方法。
82.图1示出根据本公开一实施例的三维打印的电阻抗断层成像模型。
83.本领域普通技术人员可以理解,图1示例性示出了三维打印的电阻抗断层成像模型,而不构成对本公开的限制。
84.如图1(a)、1(b)、1(c)所示,三维打印(3d打印)的电阻抗断层成像模型包括:3d打印的胸腔骨骼模型103、肺脏模型101和心脏模型102。
85.如图1(d)所示,胸腔骨骼模型103、肺脏模型101和心脏模型102按照人体对应的解剖位置采用例如粘合的方式,组合成完整的3d打印的电阻抗断层成像模型100。
86.在本公开的实施例中,胸腔骨骼模型103、肺脏模型101和心脏模型102均可由熔融沉积成型(fused deposition modeling,fdm)的3d打印技术,使用不同混合比例的丙烯腈-丁二烯-苯乙烯共聚物和炭黑(acrylonitrile butadiene styrene/carbon black,abs/cb)材料,3d打印而成。胸腔骨骼模型103、肺脏模型101和心脏模型102的电阻率各不相同,用于模拟人体各器官的真实电阻率特征。按照人体解剖结构,胸腔包括1块胸骨,12对肋骨和12块脊椎骨。胸骨、肋骨和脊椎骨可以采用不同混合比的abs/cb材料分别打印,以实现不同的电阻率特征。
87.在本公开的实施例中,采用下述方式得到图1中的胸腔骨骼模型103、肺脏模型101和心脏模型102。
88.首先,采用螺旋计算机断层扫描(computed tomography,ct)对人体,例如根据《中国居民营养与慢性病状况报告(2020年)》的平均数值,选择身高170厘米,体重70公斤的,年龄30岁,无吸烟史、胸部疾病史的成年男性作为标准对象进行建模。采用完全匹配人体解剖结构和电阻率特性的标准化模型的优势在于,对于不同小组设计的电阻抗成像系统,可以形成统一的、规范化的、最接近人体真实状况的性能评价平台,避免因为模型的制作差别或不够精准导致的电阻抗成像评价误差。扫描范围包括全部胸部。扫描层厚0.5毫米-1毫米,例如0.625毫米,扫描层数为678层。ct图像采用标准dicom格式保存。
89.其次,采用mimics软件导入胸部ct图像后,分别对模型进行计算机三维重建,得到三维重建模型。
90.最后,针对三维重建模型,针对心脏、肺脏、和胸腔骨骼系统模型进行分割、查错、修补、平滑等操作,分别生成可3d打印的心脏、肺脏、胸腔的计算机三维打印模型。
91.在本公开实施例中,“分割”操作是从ct三维重建模型的图像中确定有哪些目标器官,一般的方法是区域生长法+手工分割。“修补”操作是将目标器官获得后,因为ct图像的误差,有些器官表面会缺一块或多一块,需要对此修正,例如采用手动方式一点一点的修补,该填充的填充,该删除的删除。“平滑”是将目标器官的表面平滑,因为一般三维重建后的器官表面不光,平滑后方便3d打印。“平滑”的处理方法可以是在软件中选择例如高斯低通滤波的合适的滤波器。“查错”是将目标器官和原来的ct图片最后进行对比,确保没有太大的差别。例如,处理方法是在软件中手动调整,一层一层地比对ct图像查错。
92.在本公开实施例中,根据心脏、肺脏、胸腔骨骼的电阻率特性,分别确定打印材料abs/cb的混合比例。例如,对50khz下的电阻率,胸骨以骨密质为主,电阻率约为48.4ωm,abs:cb(v/v)=4.46
±
0.22:1;肋骨以骨松质为主,电阻率约为12.0ωm,abs:cb(v/v)=4.0
±
0.201:1;脊柱骨的电阻率约为14.0ωm,abs:cb(v/v)=4.09
±
0.20:1;肺脏充气状态下的电阻率约为9.7ωm,abs:cb(v/v)=3.84
±
0.19:1;心脏的电阻率约为5.1ωm,abs:cb(v/v)=3.82
±
0.19:1。在本公开实施例中,可以用上述配比作为参考,打印10cm
×
10cm
×
10cm的立方体结构;对打印的立方体进行电阻率特性测量,确保测量获得的电阻率值与目标器官的电阻率值基本一致(误差《5%)。
93.在本公开实施例中,可以根据上述abs/cb混合比例,打印如图1(a)所示的肺脏模型101、如图1(b)所示的心脏模型102、如图1(c)所示的胸腔骨骼模型103,并组装得到如图1(d)所示的电阻抗断层成像模型100。通过使用不同混合比的abs/cb来3d打印胸腔、肺脏和心脏,从而更为真实地模拟人体真实器官的空间电阻率分布。
94.在本公开实施例中,对于不同频率的激励信号,胸腔、肺脏、心脏的电阻率可以不同。500ml潮气量下的激励信号频率对应电阻率如下表所示。
[0095][0096][0097]
在本公开实施例中,对于不同激励信号频率下的心脏电阻率、肺脏电阻率、胸腔电阻率,可以采用不同混合比的abs/cb进行3d打印来模拟,得到一组电阻抗断层成像模型100。
[0098]
图2示出根据本公开一实施例的容纳电阻抗断层成像模型的实验装置。
[0099]
本领域普通技术人员可以理解,图2示例性示出了容纳电阻抗断层成像模型的实验装置,而不构成对本公开的限制。
[0100]
图2a、图2b示出可容纳上述电阻抗断层成像模型100,且能连接eit测量仪器的实验装置。电阻抗断层成像模型100(图2中未示出)固定于容器201中,以构建用于eit设备校准的标准模型。
[0101]
在本公开实施例中,容器201呈椭圆柱状,由有机玻璃快速成型。容器壁厚度为4.95-5.05毫米,例如5毫米;容器高度为396-404毫米,例如400毫米;椭圆内长轴的长度为346.5-353.5毫米,例如350mm;椭圆内短轴的长度为297-303毫米,例如300毫米。容器底座204呈长方体,长400mm,宽350mm,高10mm。容器内表面固定两层平行的电极组202和203,电极组203位于模型100的第四第五肋间位置,电极组202比电极组203高100毫米;电极为银质,厚度0.4mm,直径12.0mm,纯度99.99%。电极组202、203分别有16个等间距分布在同一水平的电极。电极一侧用纯度为99.99%、直径为3毫米的铜丝焊接,穿过容器201内侧壁上的钻孔与容器201外侧的屏蔽线相连。在电极焊接铜丝的一侧涂有导电胶,施加压力使电极与容器内侧壁贴紧粘牢。容器外侧的16根屏蔽线都带碳纤维屏蔽层,长度为例如200cm,交叉缠绕后再套上金属屏蔽网。每根屏蔽线连接最大阻值为例如1mω的滑动变阻器205,以模拟电极-皮肤接触阻抗,从而尽可能减小对电阻抗断层成像模型的仿真误差。
[0102]
在本公开的实施例中,可以在容器201中注入生理盐水,并浸没电阻抗断层成像模型100,用于模拟皮肤的电阻抗。
[0103]
本领域普通技术人员可以理解,容器201、容器底座204的尺寸也可以为其它尺寸,本公开对此不作限定。电极组的层数也可以是1层,或者3层,或者其它层数,本公开对此不作限定。每层的电极个数也可以是12个,或20个,或其它个数,本公开对此不作限定。
[0104]
在本公开的实施例中,本发明采用与真实外形和电阻率值一致的胸腔骨骼模型、
肺脏模型和心脏模型,更加接近人体测量的真实情况,极大减小了实验装置的误差;高纯度的银质电极减低了极化电位的影响;导线采用屏蔽线、交叉缠绕、屏蔽网降低了电磁干扰的影响;屏蔽线外接滑动变阻器,可模仿电极-皮肤接触阻抗;容器中注入生理盐水,模拟皮肤阻抗。本发明实现了对人体胸部的各个器官、皮肤等的电阻率的三维立体精确模拟,建立了人体胸部的eit电阻率标准模型,适用于评估呼吸eit的数据采集系统和成像算法。
[0105]
在本公开的实施例中,如图1所示,电阻抗断层成像模型100包括:3d打印的胸腔骨骼模型103、肺脏模型101和心脏模型102,胸腔骨骼模型103、肺脏模型101和心脏模型102按人体中对应的解剖位置组合,成为电阻抗断层成像模型100。
[0106]
胸腔骨骼模型的电阻率为第一电阻率,例如对50khz下的电阻率,胸骨以骨密质为主,电阻率约为48.4ωm;肋骨以骨松质为主,电阻率约为12.0ωm;脊柱骨的电阻率约为14.0ωm,用于模拟人体的胸腔的电阻率。
[0107]
肺脏模型的电阻率为第二电阻率,例如肺脏充气状态下的电阻率约为9.7ωm,用于模拟人体的肺脏的电阻率。心脏模型的电阻率为第三电阻率,例如约为5.1ωm,用于模拟人体的心脏的电阻率。
[0108]
根据本公开实施例,通过一种电阻抗断层成像模型,包括:三维打印的胸腔骨骼模型、肺脏模型和心脏模型,胸腔骨骼模型、肺脏模型和心脏模型按人体中对应的解剖位置组合,胸腔骨骼模型的电阻率为第一电阻率,用于模拟人体的胸腔的电阻率,肺脏模型的电阻率为第二电阻率,用于模拟人体的肺脏的电阻率,心脏模型的电阻率为第三电阻率,用于模拟人体的心脏的电阻率,从而使得模型更加符合人体的真实解剖结构,模拟人体器官的电阻率。
[0109]
而且,真实人体的不同器官在同一频率下的电阻率不同,同一器官在不同频率的激励信号下的电阻率也不相同。而采用不同混合比例的abs/cb精确模拟了胸腔骨骼、心脏、肺脏的不同电阻率,也可以模拟例如肺脏的同一器官在不同频率的激励信号下的不同电阻率。从而对人体胸部的电阻率进行三维精确建模,方便对eit数据采集系统和图像重建算法进行校准和评估,也可方便地用于临床教学等其它用途。
[0110]
在本公开的实施例中,如前所述,胸腔骨骼模型103、肺脏模型101和心脏模型102由下述方式得到:对例如身高170厘米、体重70公斤、年龄30岁、无吸烟史、无胸部疾病史的成年男性的人体的计算机断层扫描图像进行三维重建,得到三维重建模型;对三维重建模型进行分割、修补、平滑、查错,得到计算机三维打印模型;基于计算机三维打印模型进行三维打印,分别得到胸腔骨骼模型103、肺脏模型101和心脏模型102。
[0111]
在本公开实施例中,“分割”操作是从ct三维重建模型的图像中确定有哪些目标器官,一般的方法是区域生长法+手工分割。“修补”操作是将目标器官获得后,因为ct图像的误差,有些器官表面会缺一块或多一块,需要对此修正,例如采用手动方式一点一点的修补,该填充的填充,该删除的删除。“平滑”是将目标器官的表面平滑,因为一般三维重建后的器官表面不光,平滑后方便3d打印。“平滑”的处理方法可以是在软件中选择例如高斯低通滤波的合适的滤波器。“查错”是将目标器官和原来的ct图片最后进行对比,确保没有太大的差别。例如,处理方法是在软件中手动调整,一层一层地比对ct图像查错。
[0112]
根据本公开实施例,通过胸腔骨骼模型、肺脏模型和心脏模型由下述方式得到:对人体的计算机断层扫描图像进行三维重建,得到三维重建模型;对三维重建模型进行分割、
修补、平滑、查错,得到计算机三维打印模型;基于计算机三维打印模型进行三维打印,得到胸腔骨骼模型、肺脏模型和心脏模型,从而得到精确的三维打印的胸腔骨骼模型、肺脏模型和心脏模型。
[0113]
在本公开实施例中,胸腔骨骼模型、肺脏模型和心脏模型的材质为丙烯腈-丁二烯-苯乙烯共聚物和炭黑的混合物。通过不同的abs/cb混合比,实现不同器官的电阻率特征。
[0114]
根据本公开实施例,通过胸腔骨骼模型、肺脏模型和心脏模型的材质为丙烯腈-丁二烯-苯乙烯共聚物和炭黑的混合物,从而实现不同器官的电阻率的精确模拟。
[0115]
在本公开实施例中,如前所述,胸腔骨骼模型中的胸骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第一混合比;胸腔骨骼模型中的肋骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第二混合比;胸腔骨骼模型中的脊椎骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第三混合比;肺脏模型的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第四混合比;心脏模型的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第五混合比。
[0116]
根据本公开实施例,通过胸腔骨骼模型中的胸骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第一混合比;和/或胸腔骨骼模型中的肋骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第二混合比;和/或胸腔骨骼模型中的脊椎骨的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第三混合比;和/或肺脏模型的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第四混合比;和/或心脏模型的丙烯腈-丁二烯-苯乙烯共聚物和炭黑的体积混合比为第五混合比,从而实现对不同器官的电阻率的精确模拟。
[0117]
在本公开实施例中,如前所述,第一混合比为4.46
±
0.22:1,模拟50khz下的胸骨电阻率48.4ωm;第二混合比为4.01
±
0.20:1,模拟肋骨电阻率12.0ωm;第三混合比为4.09
±
0.20:1,模拟脊柱骨电阻率14.0ωm;第四混合比为3.84
±
0.19:1,模拟肺脏充气状态下的电阻率9.7ωm;第五混合比为3.82
±
0.19:1,模拟心脏的电阻率5.1ωm。
[0118]
根据本公开实施例,通过第一混合比为4.46
±
0.22:1;和/或第二混合比为4.01:1
±
0.20;和/或第三混合比为4.09
±
0.20:1;和/或第四混合比为3.84
±
0.19:1;和/或第五混合比为3.82
±
0.19:1,从而实现对各器官的电阻率的精确模拟。
[0119]
在本公开实施例中,如前对图2的陈述,实验装置,包括:电阻抗断层成像模型100;绝缘容器201,电阻抗断层成像模型100固定在绝缘容器201中;电极组205,固定于绝缘容器201的内表面;导电溶液,容置于绝缘容器201中,并浸没电阻抗断层成像模型100。
[0120]
根据本公开实施例,通过一种实验装置,其特征在于,包括:电阻抗断层成像模型;绝缘容器,电阻抗断层成像模型固定在绝缘容器中;电极组,固定于绝缘容器的内表面;导电溶液,容置于绝缘容器中,并浸没电阻抗断层成像模型,从而精确模拟人体胸部的电阻率。
[0121]
根据本公开实施例,通过绝缘容器包括:有机玻璃椭圆柱状容器,和/或绝缘容器的壁厚为4.95-5.05毫米,和/或绝缘容器的高度为396-404毫米,和/或绝缘容器的椭圆内长轴的长度为346.5-353.5毫米,和/或绝缘容器的椭圆内短轴的长度为297-303毫米,从而良好容纳电阻抗断层成像模型。
[0122]
在本公开实施例中,电极组的层数为第一值,例如2层;每层中的电极数为第二值,
例如16个,每层中的电极在绝缘容器的内表面均匀分布。
[0123]
根据本公开实施例,通过电极组的层数为第一值,每层中的电极数为第二值,每层中的电极在绝缘容器的内表面均匀分布,从而实现对电阻率的精确测量。
[0124]
根据本公开实施例,通过第一层电极组和电阻抗断层成像模型的第四第五肋间位置相对应,第二层电极组比第一层电极组高100毫米,从而实现对电阻率的精确测量。
[0125]
根据本公开实施例,通过导电溶液为生理盐水,从而精确模拟皮肤的电阻率。
[0126]
在本公开实施例中,如前所述,电极连接屏蔽线后,屏蔽线连接最大阻值为例如1mω的滑动变阻器205,以模拟电极-皮肤接触阻抗
[0127]
根据本公开实施例,通过还包括:滑动变阻器组,与电极组电性连接,从而精确模拟电极和皮肤的接触阻抗。
[0128]
图3示出根据本公开一实施例的制作电阻抗断层成像模型的方法的流程图。
[0129]
如图3所示,制作电阻抗断层成像模型的方法的流程包括:步骤s301、s302、s303、s304、s305。
[0130]
在步骤s301中,获取人体的计算机断层扫描图像。
[0131]
在步骤s302中,根据计算机断层扫描图像进行三维重建,得到三维重建模型。
[0132]
在步骤s303中,对三维重建模型进行分割、修补、平滑、查错,得到计算机三维打印模型。
[0133]
在步骤s304中,基于计算机三维打印模型进行三维打印,得到胸腔模型、肺脏模型和心脏模型。
[0134]
在步骤s305中,组合胸腔模型、肺脏模型和心脏模型,得到电阻抗断层成像模型。
[0135]
根据本公开实施例,通过获取人体的计算机断层扫描图像;根据计算机断层扫描图像进行三维重建,得到三维重建模型;对三维重建模型进行分割、修补、平滑、查错,得到计算机三维打印模型;基于计算机三维打印模型进行三维打印,得到胸腔骨骼模型、肺脏模型和心脏模型;组合胸腔骨骼模型、肺脏模型和心脏模型,得到电阻抗断层成像模型,从而获得精确的三维电阻抗断层成像模型。
[0136]
图4示出根据本公开一实施例的制作电阻抗断层成像模型实验装置的方法的流程图。
[0137]
如图4所示,制作电阻抗断层成像模型实验装置的方法的流程除了包括和图3相同的步骤s301-s305,还包括步骤:s401、s402、s403。
[0138]
在步骤s401中,构建固定了电极组的绝缘容器,电极组固定于绝缘容器的内表面。
[0139]
在步骤s402中,将电阻抗断层成像模型固定在绝缘容器中。
[0140]
在步骤s403中,在绝缘容器中加入导电溶液,导电溶液浸没电阻抗断层成像模型。
[0141]
根据本公开实施例,通过还包括:构建固定了电极组的绝缘容器,电极组固定于所述绝缘容器的内表面;将电阻抗断层成像模型固定在绝缘容器中;在绝缘容器中加入导电溶液,导电溶液浸没电阻抗断层成像模型,从而实现三维电阻抗断层成像模型的精确模拟。
[0142]
以上描述仅为本公开的较佳实施例以及对所运用技术原理的说明。本领域技术人员应当理解,本公开中所涉及的发明范围,并不限于上述技术特征的特定组合而成的技术方案,同时也应涵盖在不脱离所述发明构思的情况下,由上述技术特征或其等同特征进行任意组合而形成的其它技术方案。例如上述特征与本公开中公开的(但不限于)具有类似功
能的技术特征进行互相替换而形成的技术方案。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1