一种载药微球及其制备方法与流程
1.本发明涉及医用材料技术领域,具体的涉及一种载药微球及其制备方法。
背景技术:
2.经导管动脉化疗栓塞术(tace)即利用导管将栓塞物注入到病变器官的供应血管内使病变位置萎缩从而达到治疗目的的介入手术。对于目前不能接受肿瘤切除、肝移植的肝细胞癌患者,tace已经成为肝癌治疗的核心手段。随着肝动脉栓塞技术的广泛应用及快速发展,药物洗脱微球(drug-eluting bead,deb)作为新兴栓塞剂应运而生。
3.栓塞微球载药后可以同时实现物理栓塞和化疗的双重作用,目前市场上常见的载药微球多为单一药物,这不仅容易使肿瘤细胞产生抗药性,降低治疗效果,还会造成单一药物副作用的叠加。另外,现有载药微球对一些药物的包载量较低,未能达到临床用药标准。因此,采用多药联合的方法可以解决现有技术的缺陷。
4.本发明提供了一种载药微球及其制备方法,利用该方法可以实现联合载药,提高药物包载量,延长药物释放时间;且能够降低肿瘤细胞的抗药性、减少对人体的副作用。
技术实现要素:
5.本发明提供一种载药微球微球及其制备方法,该方法能显著提高栓塞微球对大分子药物和小分子药物的包载量,延长药物在栓塞微球内释药释放时间。
6.本发明是通过如下技术方案实现的:
7.一种载药微球,载药微球包括多羟基化合物、烷基缩醛类衍生物、烷基磺酸类衍生物,载药微球通过静电吸引作用联合包载大分子药物和小分子药物,载药微球联合经导管动脉化疗栓塞术使用。
8.烷基缩醛类衍生物包括丙烯酰胺基烷基二烷氧基缩醛,n-丙烯酰胺基二甲氧基乙基缩醛中的一种或多种。
9.在另一优选例中,载药微球可以同时实现物理栓塞和化疗的双重作用。
10.在另一优选例中,大分子药物包括pd-1、贝伐单抗中的一种或多种,小分子药物包括阿霉素、伊立替康、表柔比星、吡柔比星中的一种或多种。
11.在另一优选例中,栓塞微球自身化学结构中含有带负电荷的磺酸基,可以通过静电吸附的方式负载带有正电荷的大分子药物和小分子药物。
12.一种制备载药微球的制备方法,包括如下步骤:
13.(1)制备功能化大分子水凝胶:将多羟基聚合物加热溶于纯化水中,待降温冷却后,加入烷基缩醛类衍生物,搅拌并滴加浓盐酸反应,收集粗产物,经洗涤干燥得到所需功能化大分子水凝胶;
14.(2)制备栓塞微球:将烷基磺酸类衍生物、过硫酸钾溶于水中,混合均匀后加入步骤(1)中的功能化大分子水凝胶,得到聚合物单体溶液;将乙酸丁酯、醋酸纤维素和氮气通入反应容器中,加入聚合物单体溶液和四甲基乙二胺,形成油水混合反应体系,反应结束后
用有机溶剂洗涤,烘干得所述栓塞微球;
15.(3)对大分子药物和小分子药物的联合包载:将大分子药物和小分子药物溶解于纯化水中,得到药物混合溶液,将栓塞微球加入以使栓塞微球浸泡于药物混合溶液中,包载完成后收集并烘干,得载药微球。
16.在另一优选例中,有机溶剂包括乙酸丁酯、乙酸乙酯、丙酮。
17.在另一优选例中,搅拌操作选用轴流式搅拌桨,搅拌速度为400-650转/分。
18.在另一优选例中,功能化大分子水凝胶与烷基磺酸类衍生物的比例为1.00-0.12。
19.在另一优选例中,聚合物单体溶液加入时,反应体系温度范围为40-60℃。
20.在另一优选例中,聚乙烯醇溶解后降温至10℃。
21.在另一优选例中,测量不同时间点上清液中两种药物量,通过hplc法可以准确计算出载药微球对两种药物实际载药量和实际载药效率。
22.在另一优选例中,实际载药量=总投药量-上清液剩余药量。
23.在另一优选例中,实际载药效率=实际载药量/总投药量
×
100%。
24.在另一优选例中,累计释放率=累计释药量/载药量
×
100%。
25.实施例数据分析结果如下:
26.实施例9中,阿霉素和贝伐单抗联合载药时,在载药后的60min内,载药效率分别达到98.0%和53.2%,载药量分别达到29.4mg和31.9mg,符合临床医学应用需要。在释药实验中,载药微球在48h的累计释放率低至22.8%,能够对阿霉素起到缓慢释放的作用,此外,载药微球在48h后对贝伐单抗的累计释放率为89.5%,而在先前载药微球单独包载贝伐单抗实验数据中(表14),2h即释放超过了90.0%,因此,联合包载可以较好的延缓贝伐单抗抗体的释放。
27.实施例10中,阿霉素和pd-1联合载药时,在载药后的60min内,载药效率分别达到97.1%和95.7%,载药量分别达到58.3mg和114.8mg,符合临床医学应用需要。在释药实验中,载药微球在48h的累计释放率低至24.7%,能够对阿霉素起到缓慢释放的作用,此外,载药微球在8h后对pd-1的累计释放率超过90.0%,而在先前载药微球单独包载pd-1实验数据中(表13),1h即释放超过了90.0%,因此,联合包载可以较好的延缓pd-1抗体的释放。
28.实施例11中,表柔比星和贝伐单抗联合载药时,在载药后的60min内,载药效率分别达到85.6%和53.9%,载药量分别达到51.4mg和64.7mg,符合临床医学应用需要。在释药实验中,载药微球在48h的累计释放率低至33.5%,能够对表柔比星起到缓慢释放的作用,此外,载药微球在8h后对贝伐单抗的累计释放率超过90.0%,而在先前载药微球单独包载贝伐单抗实验数据中(表14),2h即释放超过了90.0%,因此,联合包载可以较好的延缓贝伐单抗抗体的释放。
29.实施例12中,表柔比星和pd-1联合载药时,在载药后的60min内,载药效率分别达到84.6%和93.5%,载药量分别达到50.8mg和112.2mg,符合临床医学应用需要。在释药实验中,载药微球在48h的累计释放率低至34.2%,能够对表柔比星起到缓慢释放的作用,此外,载药微球在12h后对pd-1的累计释放率超过90.0%,而在先前载药微球单独包载pd-1实验数据中(表13),1h即释放超过了90.0%,因此,联合包载可以较好的延缓pd-1抗体的释放。
30.本发明的技术方案具有如下优点:
31.(1)该载药微球制备方法过程简洁,成本低廉,制备得到的载药微球形状接近完美的圆球形,表面光滑,压缩形变可达到50%以上。
32.(2)该方法制备得到的载药微球能够同时高效包载大分子蛋白药物和小分子化疗药物,提高药物包载量,实现两种药物共同作用,降低单一药物对人体化疗所造成的毒副作用,降低肿瘤细胞的抗药性。
33.(3)该方法制备得到的载药微球联合载药后能对大分子蛋白药物和小分子化疗药物实现缓释作用。
具体实施方式
34.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
35.除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。
36.功能化大分子水凝胶的制备
37.实施例1
38.向盛有纯化水的烧瓶中加入100g聚乙烯醇,搅拌分散均匀。加热升温至96℃,在聚乙烯醇完全溶解后,冷却降温至25℃以下,加入2g丙烯酰胺基烷基二烷氧基缩醛,2gn-丙烯酰胺基二甲氧基乙基缩醛,搅拌10分钟后,向溶液中滴加100ml浓盐酸,滴加结束后继续搅拌6小时,然后收集粗产物,经洗涤干燥后得到所需功能化大分子水凝胶。
39.实施例2
40.向盛有纯化水的烧瓶中加入200g聚乙烯醇,搅拌分散均匀。加热升温至96℃,在聚乙烯醇完全溶解后,冷却降温至25℃以下后,加入4g丙烯酰胺基烷基二烷氧基缩醛,4gn-丙烯酰胺基二甲氧基乙基缩醛,搅拌10分钟后,向溶液中滴加200ml浓盐酸,滴加结束后反应继续搅拌6小时,然后收集粗产物,经洗涤干燥后得到所需功能化大分子水凝胶。
41.聚乙烯醇栓塞微球的制备
42.实施例3
43.将6g 2-丙烯酰胺-2-甲基丙磺酸钠、5g过硫酸钾依次加入至纯化水中,溶解、混合均匀后,加入实施例1制备的功能化大分子凝胶中间体50g并搅拌均匀,得到聚合物单体溶液。加入5g乙酸丁醋、2.5g醋酸纤维素,同时通入氮气气体,搅拌,加热。再依次加入上述聚合物单体溶液和四甲基乙二胺,形成油水混合反应体系,加热、搅拌3小时。该反应中,搅拌桨选用轴流式搅拌桨,搅拌速度在450转/分,聚合物单体溶液加入时反应体系温度控制在40~60℃。反应结束后,将反应混合物过滤收集微球,然后依次用乙酸丁酯,乙酸乙酯和丙酮洗涤,并经真空干燥得聚乙烯醇栓塞微球。
44.实施例4
45.将12g 2-丙烯酰胺-2-甲基丙磺酸钠、10g过硫酸钾依次加入至纯化水中,溶解、混合均匀后,加入实施例1制备的功能化大分子凝胶中间体100g并搅拌均匀,得到聚合物单体溶液。加入10g乙酸丁醋、5g醋酸纤维素,同时通入氮气气体,搅拌,加热,再依次加入上述聚
合物单体溶液和四甲基乙二胺,形成油水混合反应体系,加热、搅拌3小时。该反应中,搅拌桨选用轴流式搅拌桨,搅拌速度在450转/分,聚合物单体溶液加入时反应体系温度控制在40~60℃。反应结束后,将反应混合物过滤收集微球,然后依次用乙酸丁酯,乙酸乙酯和丙酮洗涤,并经真空干燥得聚乙烯醇栓塞微球。
46.栓塞微球对大分子药物和小分子药物的联合包载
47.实施例5
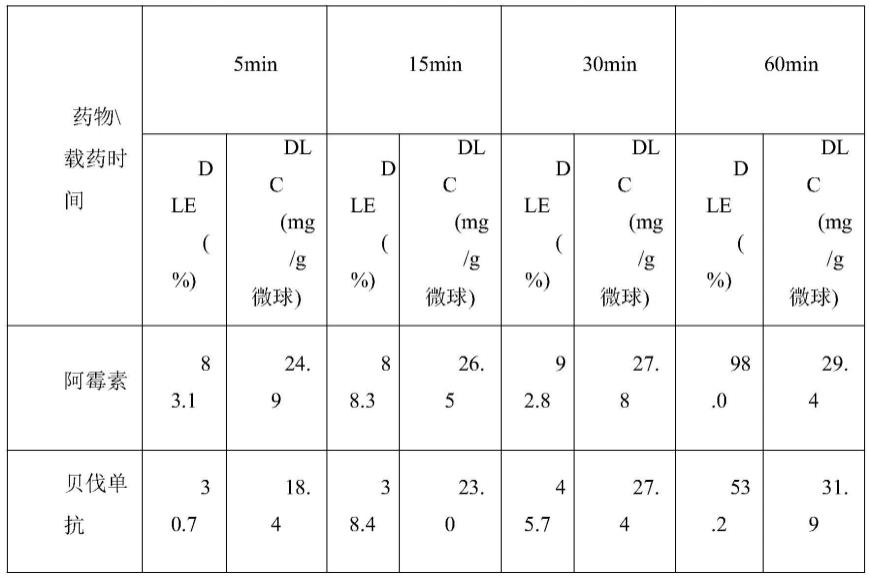
48.栓塞微球对阿霉素和贝伐单抗的联合包载:取纯化水,用0.4μm滤头过滤,配制阿霉素溶液,稀释贝伐单抗注射液,浓度分别为20mg/ml和4mg/ml。取除去生理盐水的栓塞微球0.1g放置于棕色西林瓶中,根据设计投药量吸取药物溶液0.15ml、1.5ml加入至栓塞微球中,轻轻摇晃西林瓶,使得栓塞微球与药物充分混合均匀,开始计时载药。每个样品平行做3组样品。载药5min,15min,30min,1h后提取上清液,通过hplc测定其上清液中两种药物剩余浓度,并计算阿霉素和贝伐单抗的载药效率和载药量,结果如表1所示。
49.实施例6
50.栓塞微球对阿霉素和pd-1的联合包载:取纯化水,用0.4μm滤头过滤,配制阿霉素溶液,稀释pd-1注射液,浓度分别为20mg/ml和4mg/ml。取除去生理盐水的栓塞微球0.1g放置于棕色西林瓶中,根据设计投药量吸取药物溶液0.3ml、3.0ml加入至栓塞微球中,轻轻摇晃西林瓶,使得栓塞微球与药物充分混合均匀,开始计时载药。每个样品平行做3组样品。载药5min,15min,30min,1h后提取上清液,通过hplc测定其上清液中两种药物剩余浓度,并计算阿霉素和pd-1的载药效率和载药量,结果如表2所示。
51.实施例7
52.栓塞微球对表柔比星和贝伐单抗的联合包载:取纯化水,用0.4μm滤头过滤,配制表柔比星溶液,稀释贝伐单抗注射液,浓度分别为20mg/ml和4mg/ml。取除去生理盐水的栓塞微球0.1g放置于棕色西林瓶中,根据设计投药量吸取药物溶液0.3ml、3.0ml加入至微球中,轻轻摇晃西林瓶,使得微球与药物充分混合均匀,开始计时载药。每个样品平行做3组样品。载药5min,15min,30min,1h后提取上清液,通过hplc测定其上清液中两种药物剩余浓度,并计算表柔比星和贝伐单抗的载药效率和载药量,结果如表3所示。
53.实施例8
54.栓塞微球对表柔比星和pd-1的联合包载:取纯化水,用0.4μm滤头过滤,配制表柔比星溶液,稀释pd-1注射液,浓度分别为20mg/ml和4mg/ml。取除去生理盐水的栓塞微球0.1g放置于棕色西林瓶中,根据设计投药量吸取药物溶液0.3ml、3.0ml加入至微球中,轻轻摇晃西林瓶,使得微球与药物充分混合均匀,开始计时载药。每个样品平行做3组样品。载药5min,15min,30min,1h后提取上清液,通过hplc测定其上清液中两种药物剩余浓度,并计算表柔比星和pd-1的载药效率和载药量,结果如表4所示。
55.载药微球体外模拟释药研究
56.实施例9
57.载药微球对阿霉素和贝伐单抗体外释药实验:实施例5得到的载药后的微球在模拟人体生理环境的磷酸盐缓冲液(pbs,ph=7.4,10mm)中进行释放,载药后的微球过滤掉上清液,用新鲜磷酸盐缓冲液(pbs,ph 7.4,10mm)清洗表面后,称取0.2g放入装有50ml磷酸盐缓冲液(pbs,ph 7.4,10mm)的密闭玻璃管中并置于37℃恒温箱中进行释放,在0.5h,1h,2h,
4h,6h,8h,12h,24h,36h,48h取出4ml释放介质,再补充相同体积的新鲜介质。取出的溶液通过hplc依次测定释放溶液中阿霉素的浓度以及贝伐单抗的浓度,并计算两种药物的累计释放率,平行做三组实验,结果分别如表5和表6所示。
58.实施例10
59.载药微球对阿霉素和pd-1体外释药实验:实施例6得到的载药后的微球在模拟人体生理环境的磷酸盐缓冲液(pbs,ph=7.4,10mm)中进行释放,载药后的微球过滤掉上清液,用新鲜磷酸盐缓冲液(pbs,ph 7.4,10mm)清洗表面后,称取0.2g放入装有50ml磷酸盐缓冲液(pbs,ph 7.4,10mm)的密闭玻璃管中并置于37℃恒温箱中进行释放,在0.5h,1h,2h,4h,6h,8h,12h,24h,36h,48h取出4ml释放介质,再补充相同体积的新鲜介质。取出的溶液通过hplc依次测定释放溶液中阿霉素的浓度以及pd-1的浓度,并计算两种药物的累计释放率,平行做三组实验,结果分别如表7和表8所示。
60.实施例11
61.载药微球对表柔比星和贝伐单抗体外释药实验:实施例7得到的载药后的微球在模拟人体生理环境的磷酸盐缓冲液(pbs,ph=7.4,10mm)中进行释放,载药后的微球过滤掉上清液,用新鲜磷酸盐缓冲液(pbs,ph 7.4,10mm)清洗表面后,称取0.2g放入装有50ml磷酸盐缓冲液(pbs,ph 7.4,10mm)的密闭玻璃管中并置于37℃恒温箱中进行释放,在0.5h,1h,2h,4h,6h,8h,12h,24h,36h,48h取出4ml释放介质,再补充相同体积的新鲜介质。取出的溶液通过hplc依次测定释放溶液中表柔比星的浓度以及贝伐单抗的浓度,并计算两种药物的累计释放率,平行做三组实验,结果分别如表9和表10所示。
62.实施例12
63.载药微球对表柔比星和pd-1体外释药实验:实施例7得到的载药后的微球在模拟人体生理环境的磷酸盐缓冲液(pbs,ph=7.4,10mm)中进行释放,载药后的微球过滤掉上清液,用新鲜磷酸盐缓冲液(pbs,ph 7.4,10mm)清洗表面后,称取0.2g放入装有50ml磷酸盐缓冲液(pbs,ph 7.4,10mm)的密闭玻璃管中并置于37℃恒温箱中进行释放,在0.5h,1h,2h,4h,6h,8h,12h,24h,36h,48h取出4ml释放介质,再补充相同体积的新鲜介质。取出的溶液通过hplc依次测定释放溶液中表柔比星的浓度以及pd-1的浓度,并计算两种药物的累计释放率,平行做三组实验,结果分别如表11和表12所示。
64.如下述表中,载药效率简称为dle,载药量简称为dlc,sd代表标准差。
65.表1微球对阿霉素和贝伐单抗的载药效率和载药量
[0066][0067]
表2栓塞微球对阿霉素和pd-1的载药效率和载药量
[0068][0069]
表3栓塞微球对表柔比星和贝伐单抗的载药效率和载药量
[0070][0071]
表4栓塞微球对表柔比星和pd-1的载药效率和载药量
[0072][0073]
表5载药微球对阿霉素累计释放率
[0074][0075][0076]
表6载药微球对贝伐单抗累计释放率
[0077][0078]
表7载药微球对阿霉素累计释放率
[0079][0080][0081]
表8载药微球对pd-1累计释放率
[0082][0083]
表9载药微球对表柔比星累计释放率
[0084][0085]
表10载药微球对贝伐单抗累计释放率
[0086][0087][0088]
表11载药微球对表柔比星累计释放率
[0089][0090]
表12载药微球对pd-1累计释放率
[0091][0092][0093]
表13载药微球对pd-1单独包载时的累计释放率
[0094][0095]
表14载药微球对贝伐单抗单独包载时的累计释放率
[0096][0097]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1