DankasteroneA在制备治疗肝纤维化药物中的应用
dankasterone a在制备治疗肝纤维化药物中的应用
技术领域
1.本发明属于医药技术领域,尤其涉及dankasterone a在制备治疗肝纤维化药物中的应用。
背景技术:
2.肝纤维化(hepatic fibrosis,hf)是多种因素(如hbv、hcv、酒精等)作用于肝脏从而引起细胞外基质(extracellular matrix,ecm)失衡的过程,其进一步发展会导致肝硬化、肝癌,严重影响了患者的生命健康。肝星状细胞(hepaticstellate cells,hsc)是肝脏ecm的主要来源,是肝纤维化形成的细胞学基础,在ecm代谢和各种细胞因子的产生过程中处于中心地位。当肝脏受到损伤后, hsc被激活并分泌多种细胞因子,进一步作用于hsc使之活化增殖,迁移;出现肌成纤维细胞样表型转化,从而合成分泌大量的i型胶原蛋白、iii型胶原蛋白、纤维连接蛋白等多种ecm成分并在肝脏中大量堆积,疤痕组织逐渐代替肝实质,最终形成肝纤维化。因此,抑制hsc增殖、活化、迁移,或促进hsc凋亡是减缓和逆转hf的重要策略,目前已成为研究抗肝纤维化药物的重要靶点。
3.dankasterone a属于结构特殊的ergostane-type(麦角甾)类固醇化合物,特殊之处在于其含有稠合的cis-a/b环结构。麦角甾类化合物在天然化合物中广泛存在,并且很多都有着特殊都生理活性和药理作用。dankasterone a最初由 amagata和numata等人在海绵halichondria japonica中分离获得。专利申请 cn201210044441.2公开了dankasterone a用于制备抗病毒药物的应用,具有抗 hiv病毒活性的作用。
4.但是,目前还未发现相关研究文献公开将dankasterone a应用于制备治疗肝纤维化药物中。
技术实现要素:
5.本发明为解决上述技术问题,提供了dankasterone a在制备治疗肝纤维化药物中的应用。
6.为了能够达到上述所述目的,本发明采用以下技术方案:
7.一种dankasterone a在制备治疗肝纤维化药物中的应用,所述治疗肝纤维化药物以dankasterone a为活性成分和其他药物赋形剂或载体制成。
8.进一步地,所述治疗肝纤维化药物中所述dankasterone a的浓度为5~ 20μm。
9.进一步地,所述治疗肝纤维化药物中所述dankasterone a的浓度为10~ 20μm。
10.进一步地,所述治疗肝纤维化药物中所述dankasterone a的浓度为20μm。
11.进一步地,所述dankasterone a是从天然产物中直接提取或者通过化合合成制得,化学名为(4ar,4br,6ar,7r,10ar)-3,4,4a,4b,5,6,6a,7,8,9-decahydro-4a, 6a-dimethyl-7-[(1r,2e,4r)-1,4,5-trimethyl-2-hexenyl]indeno[1,7a-a]naphthalene-2, 10,12(11h)-trione;分子式为c
28h40
o3;分子量为424.62。
[0012]
进一步地,所述dankasterone a的结构式为甾体类成分,其结构式如下:
[0013][0014]
进一步地,所述治疗肝纤维化药物为肝星状细胞增殖或存活的抑制剂。
[0015]
进一步地,所述治疗肝纤维化药物为肝星状细胞中肝纤维化标志物蛋白表达的抑制剂,该药物通过抑制肝星状细胞存活、增殖、凋亡以及肝纤维化标志物蛋白表达达到抗肝纤维化效果。
[0016]
进一步地,所述治疗肝纤维化药物能促进肝星状细胞凋亡。
[0017]
进一步地,所述治疗肝纤维化药物的剂型为口服剂或注射剂。
[0018]
进一步地,所述口服剂为颗粒剂、胶囊剂、片剂、散剂、滴丸剂、缓释剂中的任意一种。
[0019]
进一步地,所述治疗肝纤维化药物是抑制或逆转肝纤维化的药物。
[0020]
由于本发明采用了以上技术方案,具有以下有益效果:
[0021]
本发明首次提供了dankasterone a在制备治疗肝纤维化药物中的应用。利用人肝星状细胞lx2作为模式细胞,通过试验发现dankasterone a可以降低肝星状细胞lx-2中肝纤维化主要标志物胶原蛋白的表达水平,能显著抑制肝星状细胞lx-2的增殖和迁移能力,并能够诱导肝星状细胞lx-2凋亡,具备抑制或逆转肝纤维化作用,且具有剂量依赖性,在制备治疗肝纤维化药物方面具有良好的应用前景。本发明提供的dankasterone a在制备治疗肝纤维化药物中的新应用对突破肝纤维化治疗瓶颈具有重大意义。
附图说明
[0022]
为了更清楚地说明本发明实例或现有技术中的技术方案,下面将对实施实例或现有技术描述中所需要的附图做简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实例,对于本领域普通技术人员来说,在不付出创造性的前提下,还可以根据这些附图获得其他的附图:
[0023]
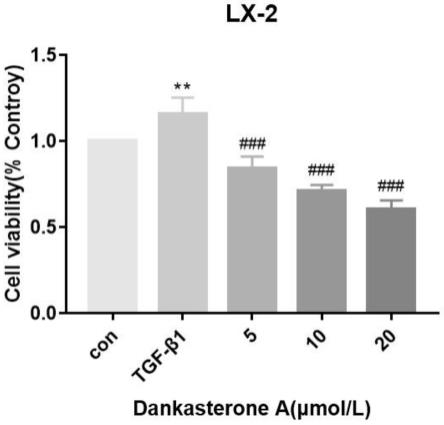
图1为本技术不同浓度的dankasterone a对lx-2细胞增殖活性影响图;
[0024]
图2为本技术细胞划痕实验观察不同浓度的dankasterone a对lx-2细胞迁移影响的倒置显微镜图;
[0025]
图3为本技术细胞划痕实验观察不同浓度的dankasterone a对lx-2细胞迁移能力的影响图;
[0026]
图4为本技术transwell实验观察在不同浓度的dankasterone a干预下对 lx-2细胞迁移影响的倒置显微镜图;
[0027]
图5为本技术transwell实验观察在不同浓度的dankasterone a对lx-2细胞迁移能力的影响图;
[0028]
图6为本技术不同浓度的dankasterone a处理下通过hoechst/pi双荧光染色观察lx-2细胞早期和晚期凋亡情况的倒置荧光显微镜图;
[0029]
图7为本技术不同浓度的dankasterone a处理下使用annexin v-fitc和pi 染料在流式细胞仪下观察lx-2细胞凋亡影响图;
[0030]
图8为本技术不同浓度的dankasterone a处理下对lx-2细胞凋亡影响图;
[0031]
图9为本技术不同浓度的dankasterone a在化学发光成像系统中目的蛋白条带图;
[0032]
图10为本技术不同浓度的dankasterone a对collagen
ꢀⅰ
的蛋白表达水平影响图。
[0033]
附图中:hoechst着色亮蓝色细胞表示早期凋亡,pi着色细胞为晚期凋亡。
具体实施方式
[0034]
下面对本发明的具体实施方式作进一步详细的说明,但本发明并不局限于这些实施方式,任何在本实施例基本精神上的改进或代替,仍属于本发明权利要求所要求保护的范围。
[0035]
实施例1
[0036]
一种dankasterone a在制备治疗肝纤维化药物中的应用,所述治疗肝纤维化药物以dankasterone a为活性成分和其他药物赋形剂或载体制成。
[0037]
进一步地,所述治疗肝纤维化药物中dankasterone a的浓度为5μm;所述 dankasterone a是从天然产物中直接提取或者通过化合合成制得,化学名为(4ar,4br,6ar,7r,10ar)-3,4,4a,4b,5,6,6a,7,8,9-decahydro-4a,6a-dimethyl-7
‑ꢀ
[(1r,2e,4r)-1,4,5-trimethyl-2-hexenyl]indeno[1,7a-a]naphthalene-2,10,12(11h)
ꢀ‑
trione;分子式为c
28h40
o3;分子量为424.62;所述dankasterone a的结构式为甾体类成分,其结构式如下:
[0038][0039]
进一步地,所述治疗肝纤维化药物为肝星状细胞增殖或存活的抑制剂;所述治疗肝纤维化药物为肝星状细胞中肝纤维化标志物蛋白表达的抑制剂,该药物通过抑制肝星状细胞存活、增殖、凋亡以及肝纤维化标志物蛋白表达达到抗肝纤维化效果;所述治疗肝纤维化药物能促进肝星状细胞凋亡;所述治疗肝纤维化药物的剂型为口服剂或注射剂;所述口服剂为颗粒剂、胶囊剂、片剂、散剂、滴丸剂、缓释剂中的任意一种;所述治疗肝纤维化药物是抑制或逆转肝纤维化的药物。
[0040]
实施例2
[0041]
一种dankasterone a在制备治疗肝纤维化药物中的应用,所述治疗肝纤维化药物
以dankasterone a为活性成分和其他药物赋形剂或载体制成。
[0042]
进一步地,所述治疗肝纤维化药物中dankasterone a的浓度为15μm;所述 dankasterone a是从天然产物中直接提取或者通过化合合成制得,化学名为 (4ar,4br,6ar,7r,10ar)-3,4,4a,4b,5,6,6a,7,8,9-decahydro-4a, 6a-dimethyl-7-[(1r,2e,4r)-1,4,5-trimethyl-2-hexenyl]indeno[1,7a-a] naphthalene-2,10,12(11h)-trione;分子式为c
28h40
o3;分子量为424.62;所述 dankasterone a的结构式为甾体类成分,其结构式如下:
[0043][0044]
进一步地,所述治疗肝纤维化药物为肝星状细胞增殖或存活的抑制剂;所述治疗肝纤维化药物为肝星状细胞中肝纤维化标志物蛋白表达的抑制剂,该药物通过抑制肝星状细胞存活、增殖、凋亡以及肝纤维化标志物蛋白表达达到抗肝纤维化效果;所述治疗肝纤维化药物能促进肝星状细胞凋亡;所述治疗肝纤维化药物的剂型为口服剂或注射剂;所述口服剂为颗粒剂、胶囊剂、片剂、散剂、滴丸剂、缓释剂中的任意一种;所述治疗肝纤维化药物是抑制或逆转肝纤维化的药物。
[0045]
实施例3
[0046]
一种dankasterone a在制备治疗肝纤维化药物中的应用,所述治疗肝纤维化药物以dankasterone a为活性成分和其他药物赋形剂或载体制成。
[0047]
进一步地,所述治疗肝纤维化药物中dankasterone a的浓度为10μm;所述 dankasterone a是从天然产物中直接提取或者通过化合合成制得,化学名为 (4ar,4br,6ar,7r,10ar)-3,4,4a,4b,5,6,6a,7,8,9-decahydro-4a,6a-dimethyl-7
‑ꢀ
[(1r,2e,4r)-1,4,5-trimethyl-2-hexenyl]indeno[1,7a-a]naphthalene-2,10,12(11h)
‑ꢀ
trione;分子式为c
28h40
o3;分子量为424.62;所述dankasterone a的结构式为甾体类成分,其结构式如下:
[0048][0049]
进一步地,所述治疗肝纤维化药物为肝星状细胞增殖或存活的抑制剂;所述治疗
肝纤维化药物为肝星状细胞中肝纤维化标志物蛋白表达的抑制剂,该药物通过抑制肝星状细胞存活、增殖、凋亡以及肝纤维化标志物蛋白表达达到抗肝纤维化效果;所述治疗肝纤维化药物能促进肝星状细胞凋亡;所述治疗肝纤维化药物的剂型为口服剂或注射剂;所述口服剂为颗粒剂、胶囊剂、片剂、散剂、滴丸剂、缓释剂中的任意一种;所述治疗肝纤维化药物是抑制或逆转肝纤维化的药物。
[0050]
实施例4
[0051]
一种dankasterone a在制备治疗肝纤维化药物中的应用,所述治疗肝纤维化药物以dankasterone a为活性成分和其他药物赋形剂或载体制成。
[0052]
进一步地,所述治疗肝纤维化药物中dankasterone a的浓度为13μm;所述 dankasterone a是从天然产物中直接提取或者通过化合合成制得,化学名为 (4ar,4br,6ar,7r,10ar)-3,4,4a,4b,5,6,6a,7,8,9-decahydro-4a,6a-dimethyl
‑ꢀ
7-[(1r,2e,4r)-1,4,5-trimethyl-2-hexenyl]indeno[1,7a-a]naphthalene-2,10, 12(11h)-trione;分子式为c
28h40
o3;分子量为424.62;所述dankasterone a的结构式为甾体类成分,其结构式如下:
[0053][0054]
进一步地,所述治疗肝纤维化药物为肝星状细胞增殖或存活的抑制剂;所述治疗肝纤维化药物为肝星状细胞中肝纤维化标志物蛋白表达的抑制剂,该药物通过抑制肝星状细胞存活、增殖、凋亡以及肝纤维化标志物蛋白表达达到抗肝纤维化效果;所述治疗肝纤维化药物能促进肝星状细胞凋亡;所述治疗肝纤维化药物的剂型为口服剂或注射剂;所述口服剂为颗粒剂、胶囊剂、片剂、散剂、滴丸剂、缓释剂中的任意一种;所述治疗肝纤维化药物是抑制或逆转肝纤维化的药物。
[0055]
实施例5
[0056]
一种dankasterone a在制备治疗肝纤维化药物中的应用,所述治疗肝纤维化药物以dankasterone a为活性成分和其他药物赋形剂或载体制成。
[0057]
进一步地,所述治疗肝纤维化药物中dankasterone a的浓度为18μm;所述 dankasterone a是从天然产物中直接提取或者通过化合合成制得,化学名为 (4ar,4br,6ar,7r,10ar)-3,4,4a,4b,5,6,6a,7,8,9-decahydro-4a,6a-dimethyl-7
ꢀ‑
[(1r,2e,4r)-1,4,5-trimethyl-2-hexenyl]indeno[1,7a-a]naphthalene-2,10,12(11h)
‑ꢀ
trione;分子式为c
28h40
o3;分子量为424.62;所述dankasterone a的结构式为载体类成分,其结构式如下:
[0058][0059]
进一步地,所述治疗肝纤维化药物为肝星状细胞增殖或存活的抑制剂;所述治疗肝纤维化药物为肝星状细胞中肝纤维化标志物蛋白表达的抑制剂,该药物通过抑制肝星状细胞存活、增殖、凋亡以及肝纤维化标志物蛋白表达达到抗肝纤维化效果;所述治疗肝纤维化药物能促进肝星状细胞凋亡;所述治疗肝纤维化药物的剂型为口服剂或注射剂;所述口服剂为颗粒剂、胶囊剂、片剂、散剂、滴丸剂、缓释剂中的任意一种;所述治疗肝纤维化药物是抑制或逆转肝纤维化的药物。
[0060]
为了进一步说明本发明能够达到所述技术效果,做以下实验:
[0061]
实验1
[0062]
mtt法检测细胞增殖活性实验。
[0063]
使用含有10%胎牛血清以及100ku/l青霉素和100mg/l链霉素的高糖培养基dmem于37℃、5%co2培养箱中培养lx-2细胞。取对数生长期的lx-2细胞,用0.25%胰蛋白酶消化后,用培养基(10%fbs+1%双抗)调整细胞密度到 5
×
104个/ml,接入96孔板,将细胞分为对照组、tgf-β1(10ng/ml)组、 dankasteronea(5μm)组、dankasteronea(10μm)组、dankasteronea(20μm) 组。每组6个复孔,每孔100μl细胞悬液,并设置空白调零孔,在细胞孔周围加入200μl无菌pbs,37℃,5%co2饱和湿度条件下培养24h后,每孔加入20μlmtt,同等培养条件培养3h,吸出培养基,加入100μldmso振荡10min,酶标仪测定各孔490nm处的吸光度(a),计算细胞增殖率。细胞增殖率=(a实验组-a调零组)/(a对照组-a调零组)
×
100%,结果如图1。
[0064]
从图1可以得出dankasteronea能明显降低lx-2细胞的存活率,且成浓度依赖性。
[0065]
实验2
[0066]
细胞划痕和transwell实验观察dankasteronea对lx-2细胞迁移影响实验。
[0067]
lx-2细胞计数板计数后,按照5
×
105个细胞/孔接种于6孔板中,放入37℃、 5%co2的恒温培养箱中贴壁培养24h。用200移液枪和直尺在贴壁细胞中划出一条无细胞的划痕带,pbs清洗3次,以清除划下的贴壁细胞。药物干预:按照实验分组对各组细胞分别进行相应的处理,模型组:换入含有tgf-β1(10ng/ml) 的完全培养基;dankasteronea干预组:tgf-β1(10ng/ml)与20、10、5μm浓度的药物同时干预。放入37℃、5%co2的恒温培养箱继续培养2d在0h和24h 两个个时间点使用倒置显微镜对细胞划痕进行拍照,使用imagej软件测量划痕面积。划痕迁移率24h=(划痕面积0h-划痕面积24h)/划痕面积0h。transwell 实验:将transwell小室放置在24孔板,细胞浓度为5
×
105/ml通过添加200μl 细胞悬浮在上室和500μl dmem介质含有10%胎牛血清的培养基在下室,放入 37℃、5%co2的恒温培养箱孵化24h。取出上腔室,加入600μl4%多聚甲醛,在室温固定20min,然后将上腔室转入1%结晶紫
染料溶液中,在室温避光染色25min,pbs洗涤2次。将小室置于倒置显微镜下随机选取3个视野拍照,使用imagej软件统计穿膜细胞数所有试验重复3次。结果如图2、图3、图4、图5所示。
[0068]
由图2、图3、图4、图5可知,dankasteronea明显抑制lx-2细胞的迁移能力。
[0069]
实验3
[0070]
细胞凋亡检测实验。
[0071]
分别采用hochest/pi双染色法和流式细胞术检测。调整细胞密度1
×
105个/ml,将其接种于6孔板,按照1
×
105个细胞/孔接种于6孔板中在37℃,5%co2培养箱中培养24h后用4%多聚甲醛固定30min,加入hoechst33342染料避光孵育5min,用pbs清洗3次后加入pi染料避光孵育10min,置于倒置荧光显微镜下观察。细胞流式实验:调整细胞密度为1
×
106个/ml,将其接种于6孔板按照试剂盒说明步骤加入annexinv-fitc和pi染料,用流式细胞仪检测亡细胞,用flowjo7.6分析。混匀后室温避光反应5~15min;流式细胞仪上机检测。结果如图6、图7、图8所示。
[0072]
从图6、图7、图8可知,从流式细胞检测结果可得,与照组比较,tgf-β1组细胞凋亡率下降,但差异无统计学意义;与tgf-β1组比较,dankasteronea5、10、20μm组细胞凋亡率显著增加(p《0.01)。
[0073]
实验4
[0074]
westernblot实验。
[0075]
药物处理lx-2细胞后,6孔板细胞每孔加100μl裂解液,充分裂解细胞后,于4℃,12000rpm离心10min,收集上清。使用bca测定试剂盒测定蛋白浓度。调整蛋白浓度后,与4
×
samplebuffer混匀,置于100℃条件下加热10min,使蛋白质彻底变性,最后将提取好的蛋白样品放在-80℃冰箱中保存备用。使用质量百分数为10%或8%sds-page凝胶电泳,将目的条带转至pvdf膜上,在质量百分数为5%的脱脂牛奶中室温封闭2h。4℃孵育一抗过夜。孵育结束后,tbst清洗3次,每次10min。二抗在室温条件下孵育2h后,tbst清洗3次,每次10min。将pvdf膜浸泡在显色液中,通过化学发光成像系统观察目的蛋白条带。结果如图9、图10所示。
[0076]
从图9、图10可知,与对照组相比,tgf-β1组细胞collagenⅰ蛋白表达显著降低(p《0.05),与tgf-β1组相比,dankasteronea5、10、20μm组细胞collagenⅰ蛋白表达显著降低(p《0.01)。
[0077]
由此可知,dankasteronea能显著抑制肝星状细胞lx-2的增殖,降低肝星状细胞lx-2中肝纤维化主要标志物的蛋白表达,抑制肝星状细胞lx-2的迁移能力和诱导肝星状细胞lx-2凋亡,具备抑制或逆转肝纤维化作用,在制备治疗肝纤维化药物方面具有良好的应用前景。
[0078]
综上所述,本发明首次提供了dankasteronea在制备治疗肝纤维化药物中的应用。本发明提供的dankasteronea在制备治疗肝纤维化药物中的新应用对突破肝纤维化治疗瓶颈具有重大意义。
[0079]
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在没有背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附
权利要求而不是上述说明限定,因此旨在将落在权利要求的等同含义和范围内的所有变化囊括在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1