癸基泛醌在制备治疗肝纤维化药物中的应用的制作方法
1.本发明属于生物医药领域,尤其涉及癸基泛醌在制备治疗肝纤维化药物中的应用。
背景技术:
2.癸基泛醌(decylubiquinone,dub)是辅酶q10的类似物。辅酶q10广泛存在与生物膜中,在能量代谢和抗氧化保护中起着至关重要的作用,是线粒体呼吸链的关键成分。dub因其结构与其相似被广泛研究。有研究表明,dub可以延缓心功能不全和心搏停止,被认为是一种新的抗高血压、降血脂和抗氧化治疗剂。dub还可以通过抑制血管生成来抑制乳腺癌的生长和转移。这些说明dub通过抑制血管生成而对一些疾病产生影响。
3.肝纤维化是一种慢性肝损伤的进展,由多种诱因引起,包括病毒性肝炎、酒精性肝损伤和非酒精性脂肪肝、以及自身免疫性肝病。如果没有有效干预,晚期肝纤维化可能发展为不可逆的肝硬化,这是全球肝脏相关死亡的主要原因。最近的研究表明,病理性血管生成和肝窦毛细血管化与肝纤维化的进展密切相关。在肝纤维化过程中,多种促血管生成因子异常表达,包括血管内皮生长因子(vegfs)、缺氧诱导因子(hifs)、成纤维细胞生长因子(fgfs)、血管生成素(angs)和血小板衍生生长因子(pdgfs)。因此,抗血管生成治疗似乎为阻断或减缓肝纤维化提供了一种新的治疗策略。
技术实现要素:
4.本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明第一个方面提出癸基泛醌在制备抑制collagen i的药物中的应用。
5.本发明的第二个方面提出了癸基泛醌在制备抑制α-sma的药物中的应用。
6.本发明的第三个方面提出了癸基泛醌在制备治疗或辅助治疗肝纤维化的药物中的应用。
7.根据本发明的第一个方面,提出了癸基泛醌在制备抑制collagen i的药物中的应用。
8.在本发明的一些实施方式中,所述药物包括癸基泛醌作为活性成分和药学上可接受的辅料。
9.在本发明的一些实施方式中,所述癸基泛醌的剂量为4mg/kg~10mg/kg。
10.在本发明的一些优选的实施方式中,所述药物中,所述癸基泛醌的剂量为5mg/kg。
11.在本发明的一些更优选的实施方式中,所述药物包括癸基泛醌作为唯一活性成分和药学上可接受的辅料。
12.在本发明的一些更优选的实施方式中,所述药物的剂型为口服剂型,或者注射剂型。
13.在本发明的一些更优选的实施方式中,所述口服剂型为片剂、胶囊剂、口服液体剂、颗粒剂或者散剂。
14.根据本发明的第二个方面,提出了癸基泛醌在制备抑制α-sma的药物中的应用。
15.在本发明的一些实施方式中,所述药物包括癸基泛醌作为活性成分和药学上可接受的辅料。
16.在本发明的一些实施方式中,所述癸基泛醌的剂量为4mg/kg~10mg/kg。
17.在本发明的一些优选的实施方式中,所述药物中,所述癸基泛醌的剂量为5mg/kg。
18.在本发明的一些更优选的实施方式中,所述药物包括癸基泛醌作为唯一活性成分和药学上可接受的辅料。
19.在本发明的一些更优选的实施方式中,所述药物的剂型为口服剂型,或者注射剂型。
20.在本发明的一些更优选的实施方式中,所述口服剂型为片剂、胶囊剂、口服液体剂、颗粒剂或者散剂。
21.根据本发明的第三个方面,提出了癸基泛醌在制备治疗或辅助治疗肝纤维化的药物中的应用。
22.在本发明的一些实施方式中,所述癸基泛醌降低了collagen i的表达水平,进一步地,所述collagen i表达水平为肝组织中collagen i表达水平。
23.在本发明的一些实施方式中,所述癸基泛醌降低了α-sma的表达水平,进一步地,所述α-sma表达水平为肝组织中α-sma表达水平。
24.在本发明中,由于在肝纤维化形成的过程中,激活的星状细胞α-sma和细胞外基质,促进肝纤维化的进展,所以通过测量肝组织中α-sma和collagen i表达水平可以用来评估肝纤维化进展情况。
25.在本发明的一些实施方式中,所述肝纤维化与病毒性肝炎、酒精性肝损伤和非酒精性脂肪肝以及自身免疫性肝病中的至少一种相关。
26.在本发明的一些实施方式中,所述药物包括癸基泛醌作为活性成分和药学上可接受的辅料。
27.在本发明的一些实施方式中,所述癸基泛醌的剂量为4mg/kg~10mg/kg。
28.在本发明的一些优选的实施方式中,所述癸基泛醌的有效剂量为5mg/kg。
29.在本发明的一些更优选的实施方式中,所述药物的剂型为口服剂型,或者注射剂型。
30.在本发明的一些更优选的实施方式中,所述口服剂型为片剂、胶囊剂、口服液体剂、颗粒剂或者散剂。
31.可以理解的是,为了便于用药,可将活性成分癸基泛醌与任何一种或者几种药学上可以接受的辅料加工成特定的剂型。这些辅料可以是稀释剂(例如淀粉、预胶化淀粉、糊精、蔗糖、乳糖、甘露醇以及微晶纤维素等)、吸收剂(例如硫酸钙、磷酸氢钙、轻质氧化镁以及碳酸钙等)、润湿剂(例如水以及乙醇等)、粘合剂(例如羟丙甲纤维素、聚维酮、淀粉浆以及糖浆等)、崩解剂(例如干淀粉、羟甲基淀粉钠、低取代羟丙基纤维素、泡腾崩解剂以及交联聚维酮等)、润滑剂(硬脂酸镁、滑石粉、氢化植物油、聚乙二醇以及微粉硅胶等)、着色剂(例如二氧化钛、日落黄、亚甲蓝以及药用氧化铁等)、包衣材料(例如丙烯酸树脂、羟丙甲纤维素以及聚维酮等)、溶剂(例如注射用水、乙醇、丙二醇以及甘油等)、酸碱调节剂(例如盐酸、乳酸、氢氧化钠、酒石酸以及酒石酸钠等)、抗氧剂(例如亚硫酸钠、焦亚硫酸钠以及硫代
硫酸钠等)、抑菌剂(例如苯酚、苯甲醇以及硫柳汞等),也可以是等渗调节剂(例如氯化钠以及葡萄糖等)。
32.可以理解的是,本发明实施方式所述的口服片剂例包括但不限于肠溶片、包衣片、薄膜衣片、糖衣片、分散片、吸吮片、咀嚼片、泡腾片、划痕片、缓释控释剂型缓释片、缓释包衣片、控释片口腔崩解片、含片、口腔贴片等。
33.可以理解的是,本发明实施方式所述的口服胶囊剂包括但不限于硬胶囊、软胶囊、肠溶胶囊、缓释胶囊、控释胶囊等。
34.可以理解的是,本发明实施方式所述的口服液体剂包括但不限于口服混悬剂、口服乳剂、胶浆剂、口服液、口服乳液、乳剂、胶体溶液、合剂、露剂、滴剂、混悬滴剂等。
35.可以理解的是,本发明实施方式所述的口服颗粒剂包括但不限于肠溶颗粒剂、缓释颗粒剂、细粒剂、茶剂、混悬颗粒剂、泡腾颗粒剂等。
36.可以理解的是,本发明实施方式所述的口服散剂包括但不限于药粉、粉剂、干混悬剂等。
37.可以理解的是,本发明实施方式所述的注射剂型包括但不限于注射液、注射用溶液剂、静脉滴注用注射液、注射用混悬液、注射用无菌粉末、静脉注射针剂、水针、注射用乳剂、粉针剂、针剂、无菌粉针、冻干粉针等。
38.本发明的有益效果为:
39.本发明通过验证癸基泛醌可以减轻ccl4诱导的小鼠肝纤维化,并通过苏木素-伊红染色(h&e染色)、天狼星红染色、免疫组化检测collagenⅰ和α-sma的表达来验证癸基泛醌对肝纤维化的治疗作用,发现癸基泛醌治疗组比dmso对照组胶原的表达量及collagenⅰ和α-sma的表达明显降低,表明癸基泛醌显著减轻了ccl4诱导的小鼠肝纤维化。因此,癸基泛醌可作为一种具有开发前景的防治肝纤维化的药物。
附图说明
40.下面结合附图和实施例对本发明做进一步的说明,其中:
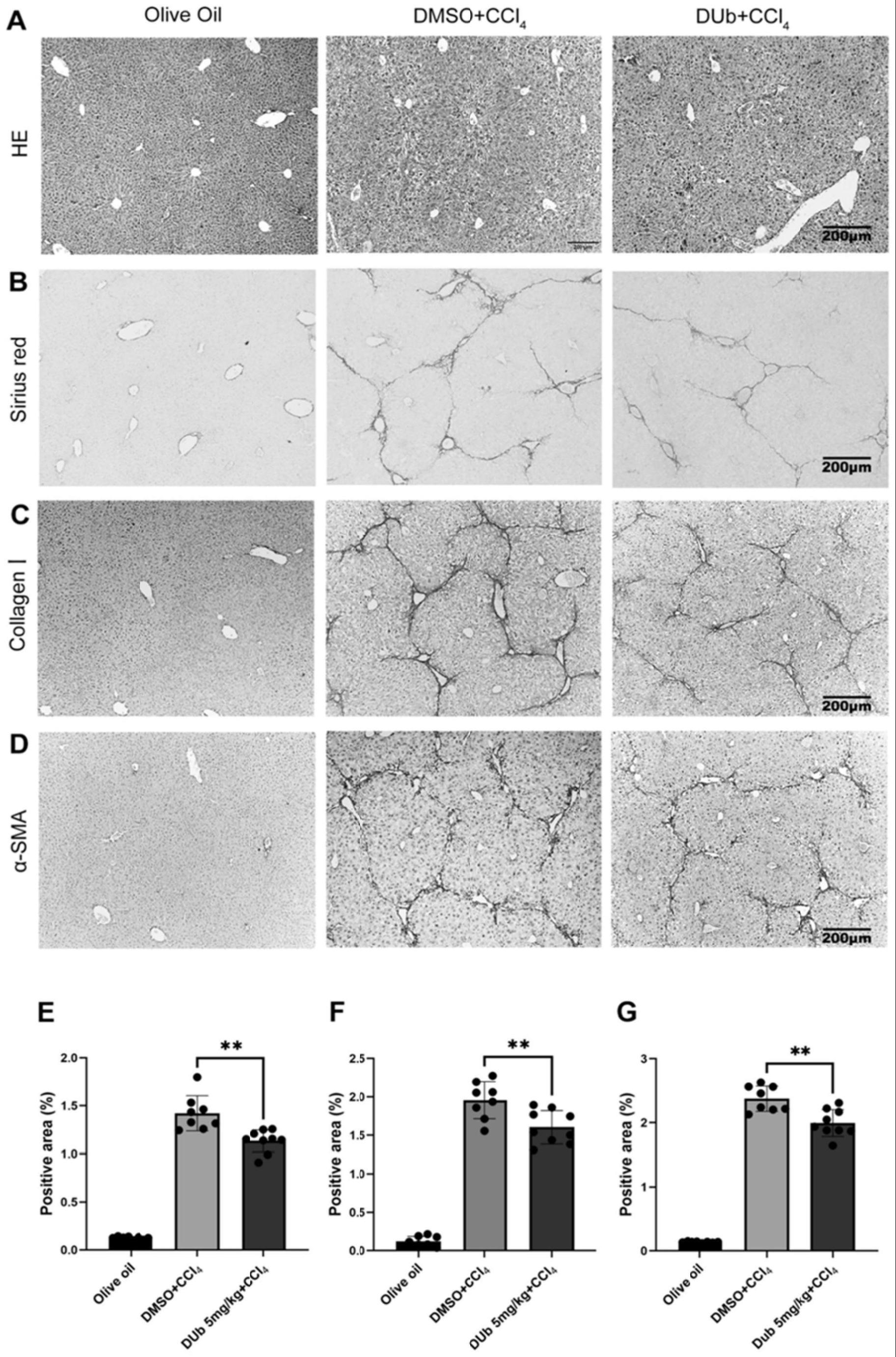
41.图1为本发明实施例癸基泛醌治疗小鼠肝纤维化结果,其中a图为小鼠肝脏组织h&e染色;b图为小鼠肝脏组织天狼星红染色;c图为免疫组化检测collagenⅰ表达;d图为免疫组化检测α-sma表达;e图为小鼠肝脏组织天狼星红染色阳性面积量化柱状图;f图为免疫组化检测collagenⅰ表达量化柱状图;g图为免疫组化检测α-sma表达量化柱状图;*代表p《0.05。
具体实施方式
42.以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
43.实施例
44.以下各实验中所述的癸基泛醌(dub)均购自sigma公司
45.一、肝纤维化模型的构建及治疗
无水乙醇(10s)-二甲苯ⅰ(10s)-二甲苯ⅱ(10s)进行脱水。
65.5.封片:放入通风橱风干,中性树胶封片。
66.结果如图1所示,从b图和e图可以看出,dub治疗组天狼星红染色阳性面积比模型组(dmso+ccl4)更少,说明dub治疗组胶原纤维的数量明显比dmso治疗组少,表明dub减轻了ccl4诱导的肝纤维化。
67.五、免疫组化(ihc)检测collagenⅰ和的α-sma的表达
68.1.脱蜡:将准备好的石蜡切片置于65℃烘箱中烘10min~20min后,将切片依次置于二甲苯ⅰ(25min)-二甲苯ⅱ(25min)-无水乙醇ⅰ(20min)-无水乙醇ⅱ(15min)-95%乙醇(10min)-80%乙醇(5min)-70%乙醇(5min)进行脱蜡。脱蜡后将切片置于0.01m的pbs中摇床洗涤三次,每次5min。
69.2.抗原修复:将组织切片置于柠檬酸缓冲液中高温高压修复14min,自然冷却至室温后用0.01m的pbs洗涤三次,每次5min。
70.3.消除内源性过氧化物酶活性:将组织切片放入3%h2o
2-甲醇溶液中,提前预热30min,放置37℃,30min。从3%h2o
2-甲醇溶液中取出切片,0.01m的pbs洗三次,每次5min。
71.4.封闭:将组织切片上组织周围的溶液擦干,于组织上加上10%bsa盖住组织,将组织切片放置于湿盒中,再将湿盒置于37℃烘箱中封闭1h。
72.5.一抗孵育:用移液器将10%bsa直接吸掉,分别加上预先配置好的一抗后置于4℃冰箱过夜。
73.6.二抗孵育:第二天将组织切片连同湿盒置于室温下复温20min后,用1
×
pbs洗三次,每次5min。擦干组织周围的水分,于组织上加上配置好的二抗,置于湿盒中,37℃烘箱孵育1h。
74.7.dab显色,苏木素复染:从湿盒中拿出组织切片,0.01m的pbs洗三次,每次5min。擦干组织周围的水分,于组织上加上dab substrate kit溶液(现用现配),室温静置约1min,放置于水中停止反应。苏木素染色10s,用流水洗去染色剂,小心不要让水冲掉组织。
75.8.脱水、封片:染色结束后将切片依次置于80%乙醇(10s)-90%乙醇(10s)-95%乙醇(10s)-无水乙醇ⅰ(10s)-无水乙醇ⅱ(10s)-二甲苯ⅰ(10s)-二甲苯ⅱ(10s)进行脱水、透明后,于通风窗晾干,中性树胶封片。
76.结果如图1中c和f所示,从图1的c图和f图可以看出,dub治疗组collagenⅰ的表达量比肝纤维化模型组(dmso+ccl4)中collagenⅰ表达量少,从d图和g图可以看出,dub治疗组相对于肝纤维化模型组α-sma的表达量明显更少,说明dub显著抑制了ccl4诱导的纤维化。
77.上面对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1