一种紫苏籽油纳米颗粒及其制备方法和应用
1.本发明属于生物医药技术领域,具体涉及一种紫苏籽油纳米颗粒及其制备方法和应用。
背景技术:
2.冷应激作为最常见的环境应激元素,一旦超过人体的体温调节能力,可能会导致普通感冒,降低人体免疫力,增加人的易感性,加重其他慢性疾病。随着全球变暖,不可预测的急剧降温现象频繁发生,临床实践中人类不得不应对日益增多的周期性冷应激。因此,人类必须通过提高自身抵抗力或摄入预防药食来增强抗寒能力,尤其是婴儿、老年人和有基础疾病的特殊人群更为必要。
3.中草药的临床应用已取得了许多优势和成果,在世界范围内受到了广泛关注。据《神农本草经》记载,传统中草药紫苏对预防和治疗冷应激引起的普通感冒具有重要的预防和治疗作用,其中紫苏油起着关键作用。现代医学研究也表明,紫苏籽油可通过抗氧化、抗炎、调节免疫功能等作用,预防和治疗包括普通感冒咳嗽和肠道紊乱,糖尿病和心血管慢性疾病,抑郁症和焦虑症等在内的各种疾病。
4.由于紫苏籽油的不稳定、生物利用度低、使用不便等原因,目前医药行业仍缺乏成熟的产品,临床应用受限。紫苏籽油的药理活性成分主要包括α-亚麻酸、黄酮类化合物、甾醇、萜类化合物和迷迭香酸等,这些成分具有挥发性、光解性、氧化性和低生物利用度的共同特征,因此,开发新制剂,克服这些缺陷,成为进一步实现医疗产业化的迫切需要。如何提供一种紫苏籽油纳米颗粒,使其可以增加紫苏籽油的稳定性和生物利用率,成为目前亟待解决的问题。
技术实现要素:
5.针对现有技术的不足,本发明的目的在于提供一种紫苏籽油纳米颗粒及其制备方法和应用。仿生方法已被证明是一种非常有前途的方法,可以提高药物的稳定性、给药率和生物利用度。食用酵母是一种高效的载体,可通过口服途径传递药物治疗多种疾病。本发明将紫苏籽油包裹在酵母壳中,制备得到紫苏籽油纳米颗粒,以提高其稳定性和生物利用度,提供了一种安全有效的新型制剂,以便于制备口服预防和/或治疗冷应激药物。
6.为达到此发明目的,本发明采用以下技术方案:
7.第一方面,本发明提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒包括芯材和壁材,所述芯材包括紫苏籽油,所述壁材包括酵母壳。
8.紫苏籽油具有缓解冷应激的重要作用,由于其不稳定性和生物利用度低,临床应用受到严重限制。本发明将紫苏籽油包裹在酵母壳中,制备得到紫苏籽油纳米颗粒,以提高其稳定性和生物利用度。酵母壳为双亲性的双层脂膜,可以很好的包裹保护紫苏籽油,使其与氧气隔绝,抵御不饱和脂肪酸的自氧化;在实际生活或临床应用中,酵母壳能有效与细胞膜相似相溶,降低药物生物不相溶性,提高紫苏籽油的生物利用度。
9.在本发明中,所述紫苏籽油纳米颗粒的平均粒径为200-500nm(例如可以是200nm、220nm、240nm、260nm、280nm、300nm、305nm、310nm、315nm、320nm、325nm、330nm、335nm、340nm、345nm、350nm、370nm、390nm、410nm、430nm、450nm、470nm、490nm、500nm等)。
10.优选地,所述紫苏籽油纳米颗粒溶液以质量百分含量计,包括紫苏籽油2-10%(例如可以是2%、3%、4%、5%、6%、7%、8%、9%、10%等)和酵母壳10-20%(例如可以是10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%等)。
11.优选地,所述紫苏籽油和酵母壳的质量比为1:(2-10),其中,“2-10”可以是2、3、4、5、6、7、8、9、10等。
12.在本发明中,紫苏籽油中脂肪酸含量为95.48%,其他物质含量为4.52%,其中脂肪酸含量主要有10种,包括α-亚麻酸65.37%、亚油酸13.85%、油酸9.57%、鲸蜡酸4.97%、十八烷酸1.35%、十六烷酸0.14%、二十碳烷酸0.12%、花生酸0.062%、棕榈油酸0.037%和十七烷酸0.012%。
13.在不饱和脂肪酸家族中,ω-6和ω-3对人类健康都是必不可少的。与ω-3相比,ω-6在日常食用油中含量更丰富,因此更容易从饮食中获得。以葵花籽油和大豆油为例,其ω6:ω3比值分别为35:1和8:1。然而,高比例的ω6:ω3可能导致或加剧慢性病的发生风险,目前研究表明,膳食补充剂ω-3对预防和控制肿瘤、糖尿病、认知障碍慢性疾病等具有积极意义。
14.在本发明中,紫苏籽油中不饱和脂肪酸超过89.08%,饱和脂肪酸仅为6.45%。有趣的是,紫苏油中的α-亚麻酸作为一种ω-3,含量超过65.37%。因此,紫苏籽油作为膳食和医疗的ω-3补充剂具有非常重要的应用前景。
15.虽然紫苏籽油在饮食和医药方面具有潜在的应用价值,但实际生产中仍存在许多困境。一方面,α-亚麻酸在提取和保存过程中容易被破坏。在本发明中,长期储存游离紫苏籽油的抗氧化能力会显著降低,而制备成纳米颗粒后,可以有效地保留紫苏油的抗氧化能力,增加存储稳定性。因此,酵母壳包裹的紫苏籽油比游离紫苏籽油更稳定,这是一种很有前景的新型药用营养剂。另一方面,α-亚麻酸在食用过程中易被胃酸破坏,在游离状态下难以吸收利用。在本发明中,为了克服这些缺陷,紫苏籽油与酵母壳偶联,阻断其与氧气的相互作用。酵母壳的良好生物相容性,可以来提高紫苏油的生物利用度,从而使得紫苏籽油在预防和治疗冷应激方面表现出更好的效果。
16.第二方面,本发明提供一种根据第一方面所述的紫苏籽油纳米颗粒的制备方法,所述制备方法包括以下步骤:
17.(1)将酵母壳和生理盐水混合,得到酵母壳溶液;
18.(2)将步骤(1)得到的酵母壳溶液和紫苏籽油混合,得到混合溶液;然后将混合溶液进行超声和自组装,得到所述紫苏籽油纳米颗粒。
19.在本发明中,步骤(1)中,所述生理盐水的浓度为3-5mg/ml(例如可以是3mg/ml、3.5mg/ml、4mg/ml、4.5mg/ml、5mg/ml等)。
20.优选地,步骤(1)中,所述混合后还包括超声,所述超声的频率为10-30khz(例如可以是10khz、12khz、14khz、16khz、18khz、20khz、22khz、24khz、26khz、28khz、30khz等),所述超声的功率为80-100w(例如可以是80w、83w、86w、89w、92w、94w、96w、98w、100w等),所述超声的时间为5-10min(例如可以是5min、6min、7min、8min、9min、10min等)。
21.优选地,所述超声的频次为超声4-6s(例如可以是4s、4.3s、4.6s、4.9s、5.2s、5.5s、5.8s、6s等),间隔4-6s(例如可以是4s、4.3s、4.6s、4.9s、5.2s、5.5s、5.8s、6s等)。
22.在本发明中,步骤(2)中,所述混合溶液中酵母壳的浓度为3.5-10mg/ml(例如可以是3.5mg/ml、3.6mg/ml、3.7mg/ml、3.8mg/ml、3.9mg/ml、4mg/ml、4.1mg/ml、4.2mg/ml、4.3mg/ml、4.4mg/ml、4.5mg/ml、5mg/ml、5.5mg/ml、6mg/ml、6.5mg/ml、7mg/ml、7.5mg/ml、8mg/ml、8.5mg/ml、9mg/ml、9.5mg/ml、10mg/ml等),紫苏籽油的浓度为1.5-5mg/ml(例如可以是1.5mg/ml、1.7mg/ml、1.9mg/ml、2.1mg/ml、2.3mg/ml、2.5mg/ml、3mg/ml、3.5mg/ml、4mg/ml、4.5mg/ml、5mg/ml等)。
23.优选地,步骤(2)中,所述超声的频率为10-30khz(例如可以是10khz、12khz、14khz、16khz、18khz、20khz、22khz、24khz、26khz、28khz、30khz等),所述超声的功率为80-100w(例如可以是80w、83w、86w、89w、92w、94w、96w、98w、100w等),所述超声的时间为8-12min(例如可以是8min、8.5min、9min、9.5min、10min、10.5min、11min、11.5min、12min等)。
24.优选地,步骤(2)中,所述超声的频次为超声4-6s(例如可以是4s、4.3s、4.6s、4.9s、5.2s、5.5s、5.8s、6s等),间隔4-6s(例如可以是4s、4.3s、4.6s、4.9s、5.2s、5.5s、5.8s、6s等)。
25.优选地,步骤(2)中,所述自组装在黑暗条件下进行,所述自组装的温度为20-30℃(例如可以是20℃、21℃、22℃、23℃、24℃、25℃、26℃、27℃、28℃、29℃、30℃等),所述自组装的时间为12-20h(例如可以是12h、13h、14h、15h、16h、17h、18h、19h、20h等)。
26.在本发明中,步骤(1)中,所述酵母壳的制备方法包括以下步骤:
27.(a)将酵母细胞分散在碱溶液中,孵育,得到碱孵育后的酵母细胞碎片;
28.(b)将碱孵育后的酵母细胞碎片分散在酸溶液中,孵育,真空干燥,得到所述酵母壳。
29.步骤(a)中,将酵母细胞分散在碱溶液中,孵育,得到碱孵育后的酵母细胞碎片,解离释放细胞内容物,便于酵母壳的分离;
30.步骤(b)中,将碱孵育后的酵母细胞碎片分散在酸溶液中,孵育,使酵母壳聚集,易于分离获得酵母壳溶液,真空干燥,得到所述酵母壳。
31.优选地,步骤(a)中,所述酵母细胞和碱溶液的质量比为1:(4-12)(其中,“4-12”可以是4、5、6、7、8、9、10、11、12等),所述碱溶液的摩尔浓度为0.8-1.3mol/l(例如可以是0.8mmol/l、0.9mmol/l、1mmol/l、1.1mmol/l、1.2mmol/l、1.3mmol/l等)。
32.优选地,步骤(a)中,所述孵育的温度为75-85℃(例如可以是75℃、76℃、77℃、78℃、79℃、80℃、81℃、82℃、83℃、84℃、85℃等),时间为0.8-1.2h(例如可以是0.8h、0.9h、1h、1.1h、1.2h等)。
33.优选地,步骤(a)中,所述孵育后还需要用去离子水洗涤2-4次(例如可以是2次、3次、4次等),每次洗涤后均采用抽滤后收集固体。
34.优选地,所述碱溶液和酸溶液的体积比为1:(0.8-1.2)(其中,“0.8-1.2”可以是0.8、0.9、1、1.1、1.2等),所述酸溶液的ph为2.5-3.5(例如可以是2.5、2.7、2.9、3.1、3.3、3.5等)。
35.优选地,步骤(b)中,所述孵育的温度为50-60℃(例如可以是50℃、51℃、52℃、53℃、54℃、55℃、56℃、57℃、58℃、59℃、60℃等),时间为0.8-1.2h(例如可以是0.8h、0.9h、
1h、1.1h、1.2h等)。
36.优选地,步骤(b)中,所述真空干燥的温度为-80~-50℃(例如可以是-80℃、-75℃、-70℃、-65℃、-60℃、-55℃、-50℃等)。
37.优选地,步骤(b)中,所述孵育后还包括依次进行地去离子水洗、异丙醇洗和丙酮洗,所述离子水洗的次数为2-4次(例如可以是2次、3次、4次等),所述异丙醇洗的次数为3-5次(例如可以是3次、4次、5次等),所述丙酮洗的次数为1-3次(例如可以是1次、2次、3次等);每次洗涤后均采用抽滤后收集固体。
38.优选地,所述酵母细胞的制备方法包括以下步骤:采用无菌酵母蛋白胨葡萄糖液体培养基从酵母冻干粉中分离纯化酵母细胞,得到酵母细胞培养菌液;然后将酵母细胞培养菌液接种在无菌酵母蛋白胨葡萄糖固体培养基中继续培养,筛选得到单菌落;将得到的单菌落采用液体培养基进一步扩增培养,离心收集菌体,得到酵母细胞。
39.优选地,所述无菌酵母蛋白胨葡萄糖液体培养基按质量浓度计,包括蛋白胨18-22g/l(例如可以是18g/l、19g/l、20g/l、21g/l、22g/l等)、酵母浸膏粉8-12g/l(例如可以是8g/l、9g/l、10g/l、11g/l、12g/l等)和葡萄糖18-22g/l(例如可以是18g/l、19g/l、20g/l、21g/l、22g/l等),所述无菌酵母蛋白胨葡萄糖液体培养基的溶剂包括水。
40.作为本发明优选的技术方案,所述酵母壳的制备方法包括以下步骤:
41.(a)将酵母细胞分散在碱溶液中,75-85℃孵育0.8-1.2h,抽滤,用去离子水洗涤抽滤后得到的固体2-4次,每次洗涤后均采用抽滤后收集固体,得到碱孵育后的酵母细胞碎片;
42.(b)将碱孵育后的酵母细胞碎片分散在酸溶液中,50-60℃孵育0.8-1.2h,抽滤,然后使用去离子水洗涤2-4次,异丙醇洗涤3-5次,丙酮洗涤1-3次,每次洗涤后均采用抽滤后收集固体,真空干燥,得到所述酵母壳。
43.优选地,步骤(a)和步骤(b)中,所述抽滤采用的滤纸孔径各自独立地为5kda-10kda(例如可以是5kda、5.5kda、6kda、6.5kda、7kda、7.5kda、8kda、8.5kda、9kda、9.5kda、10kda等)。
44.在本发明中,步骤(2)中,所述紫苏籽油的制备方法包括以下步骤:将紫苏籽粉碎,过筛,得到紫苏籽干粉;采用索氏提取法提取紫苏籽干粉中的紫苏籽油。
45.优选地,所述过筛采用40-100目(例如可以是40目、50目、60目、70目、80目、90目、100目等)的筛网。
46.优选地,所述提取采用的提取溶剂包括无水乙醚和/或石油醚。
47.优选地,所述紫苏籽粉末和提取溶剂的固液比为1:(2.5-3.5)g/ml(其中,“2.5-3.5”可以是2.5、2.6、2.7、2.8、2.9、3、3.1、3.2、3.3、3.4、3.5等)。
48.优选地,所述提取的温度为30-50℃(例如可以是30℃、35℃、40℃、45℃、50℃等),所述提取的时间为4-6h(例如可以是4h、4.5h、5h、5.5h、6h等)。
49.第三方面,本发明提供一种根据第一方面所述的紫苏籽油纳米颗粒在制备治疗和/或预防冷应激药物中的应用。
50.第四方面,本发明提供一种口服治疗和/或预防冷应激药物,所述口服治疗和/或预防冷应激药物的制备原料包括第一方面所述的紫苏籽油纳米颗粒。
51.相对于现有技术,本发明具有以下有益效果:
52.(1)本发明利用酵母壳包裹紫苏籽油制备紫苏籽油纳米颗粒,采用malvern zeta纳米仪、扫描电镜和高效液相色谱等分析纳米颗粒的特性;并应用小鼠冷应激模型,通过分析小鼠血液生理生化指标评价口服纳米颗粒对小鼠冷应激的缓解作用。
53.(2)本发明中紫苏籽产油率为48.37%,酵母壳得率为16.87%;紫苏籽油纳米溶液的包裹效率为89.21%,为乳白色均一的纳米溶液;紫苏籽油纳米颗粒的平均粒径为316.74nm、表面电荷为+2.9mv。
54.(3)紫苏籽油纳米颗粒在模拟胃酸中稳定,在模拟肠液中能有效释放,释放效率约为91.34%。口服纳米颗粒后,小鼠血液白细胞(wbc)、超氧化物歧化酶(sod)和丙二醛(mda)指标均较模型小鼠恢复,其效果优于口服游离紫苏籽油。通过将紫苏籽油包裹在酵母壳中,形成紫苏籽油纳米颗粒,提高了其稳定性和生物利用度,提供了一种新型的预防和/或治疗冷应激的药物。
附图说明
55.在以下附图中,不同大写字母表示极显著差异(p《0.01),不同小写字母表示有显著差异(p《0.05)。
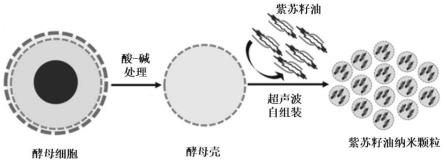
56.图1为紫苏籽油纳米颗粒的制备示意图。
57.图2为紫苏籽油的外观图。
58.图3为酵母壳的外观图。
59.图4为紫苏籽油纳米颗粒的外观图。
60.图5为紫苏籽油纳米颗粒的sem图。
61.图6为紫苏籽油纳米颗粒的粒径分布图。
62.图7为紫苏籽油纳米颗粒的zeta电位图。
63.图8为紫苏籽油、紫苏籽油纳米颗粒和酵母壳的吸收光谱。
64.图9为紫苏籽油纳米颗粒在胃酸和肠液中的释放效率。
65.图10为维生素c、紫苏籽油、胃酸-纳米颗粒和肠液-纳米颗粒的dpph自由基清除能力图。
66.图11为不同时间内紫苏籽油、胃酸-纳米颗粒和肠液-纳米颗粒的dpph自由基清除能力图。
67.图12为nc、csd、tpfo和tnp组小鼠体温变化图。
68.图13为nc、csd、tpfo和tnp组小鼠体重变化图。
69.图14为实验第10天nc、csd、tpfo和tnp组小鼠红细胞计数图。
70.图15为实验第10天nc、csd、tpfo和tnp组小鼠白细胞计数图。
71.图16为实验第10天nc、csd、tpfo和tnp组小鼠血小板计数图。
72.图17为实验第10天nc、csd、tpfo和tnp组小鼠血液sod含量图。
73.图18为实验第10天nc、csd、tpfo和tnp组小鼠血液中丙二醛含量图。
74.图19为实验第10天nc、csd、tpfo和tnp组小鼠空腹血糖水平图。
具体实施方式
75.下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明
了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
76.以下实施例中酵母冻干粉的制备方法包括以下步骤:分离纯化鉴定后的酵母菌,无菌酵母蛋白胨葡萄糖(yepd)液体培养基、28℃、120rmp振荡培养16h,5000rpm离心15min收集菌体,用生理盐水洗涤3次,加入5%(m/m)的全脂奶粉、3%(m/m)的果糖、0.1%(m/m)的水果味香精,混匀后-80℃冷冻固化,真空冷冻干燥36h制得酵母冻干粉。
77.制备例1
78.本制备例提供酵母壳,所述酵母壳的制备方法包括以下步骤:
79.(1)用无菌酵母蛋白胨葡萄糖(yepd)液体培养基从酵母冻干粉中分离纯化酵母细胞,得到酵母细胞培养菌液;然后将酵母细胞培养菌液接种在无菌酵母蛋白胨葡萄糖固体培养基中继续培养,筛选得到单菌落;将得到的单菌落采用液体培养基进一步扩增培养,离心收集菌体,得到酵母细胞;
80.yepd液体培养基配方为:20g蛋白胨、10g酵母浸膏粉和20g葡萄糖,加1l去离子水。
81.(2)收集步骤(1)得到的酵母细胞20g,滴加100ml氢氧化钠溶液(1mol/l),80℃孵育1h,采用5kda滤膜进行抽滤,收集固体,用无菌去离子水洗涤抽滤得到的固体三次,每次洗涤后均采用抽滤(10kda滤膜)收集固体,得到碱孵育后的酵母细胞碎片;
82.(3)将碱孵育后的酵母细胞碎片分散在100ml的hcl(ph 3.0)中,55℃孵育1h,抽滤采用10kda滤膜进行抽滤,收集固体,无菌去离子水洗涤3次,异丙醇洗涤4次,再采用10ml丙酮洗涤2次,每次洗涤后均采用抽滤(5kda)收集固体,洗涤完之后采用-80℃冷冻真空干燥的方法收集酵母壳样品。
83.以上步骤中,所有洗涤步骤采用抽滤后收集固体,抽滤采用滤膜,且边洗涤边玻璃棒搅拌。
84.酵母壳提取效率的计算公式如下所示:
85.酵母壳提取效率(%)=(冻干酵母壳重量/酵母细胞重量)
×
100%;
86.经计算可得,酵母壳的提取效率为16.87%。
87.制备例2
88.本制备例提供紫苏籽油,所述紫苏籽油的制备方法包括以下步骤:将紫苏籽用粉碎机粉碎,过60目筛,制得紫苏籽干粉。将紫苏籽干粉(100g)和无水乙醚(300ml)依次装入索氏提取设备的纤维素套管中,40℃提取5h后,回收乙醚并干燥至恒重,得到所述紫苏籽油。
89.紫苏籽油出油率(%)=(紫苏籽油质量/紫苏籽质量)
×
100%;
90.经计算得紫苏籽油的出油率为48.37%。
91.制备例3
92.本制备例提供酵母壳,与制备1的区别仅在于,将抽滤均替换为离心,用5000rpm的离心机离心5min后,去除上清液,得到沉淀,其他制备方法均同制备例1。
93.经计算可得,酵母壳的提取效率为10.34%。
94.通过制备例1和制备例3的对比可知,离心富集时容易存在洗涤搅拌不充分,富集物质存在杂质的问题。导致壳颜色不纯,且冷冻干燥后,大量的壳存在结块状,颗粒不细腻。
95.而采用抽滤操作,可以有效地去除杂质,冷冻干燥后并不会粘黏结块状,呈现出细粉状。
96.实施例1
97.本实施例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以下步骤:
98.将酵母壳溶于4mg/ml浓度的生理盐水中,在20khz功率、90w超声条件下预处理7min(运行5秒,间隔5秒),得到酵母壳溶液。然后加入10mg/ml的紫苏籽油,紫苏籽油的最终浓度为2mg/ml,酵母壳的最终浓度为4mg/ml,在相同超声条件下处理10min,25℃暗室自组装16h,得到所述紫苏籽油纳米颗粒。
99.如图1所示,紫苏籽油纳米颗粒的制备示意图。酵母细胞经过酸-碱处理,得到酵母壳,将酵母壳和紫苏籽油经过自组装处理,得到所述紫苏籽油纳米颗粒。
100.图2为紫苏籽油的外观图;图3为酵母壳的外观图;图4为紫苏籽油纳米颗粒的外观图,呈乳白色的纳米颗粒溶液。
101.实施例2
102.本实施例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以下步骤:
103.将酵母壳溶于3.8mg/ml浓度的生理盐水中,在18khz功率、92w超声条件下预处理5min(运行5秒,间隔5秒),得到酵母壳溶液。然后加入10.2mg/ml的紫苏籽油,紫苏籽油的最终浓度为1.5mg/ml,酵母壳的最终浓度为4.5mg/ml,在相同超声条件下处理11min,24℃暗室自组装15h,得到所述紫苏籽油纳米颗粒。
104.实施例3
105.本实施例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以下步骤:
106.将酵母壳溶于4.2mg/ml浓度的生理盐水中,在22khz功率、88w超声条件下预处理10min(运行5秒,间隔5秒),得到酵母壳溶液。然后加入9.8mg/ml的紫苏籽油,紫苏籽油的最终浓度为2.5mg/ml,酵母壳的最终浓度为3.5mg/ml,在相同超声条件下处理8min,26℃暗室自组装17h,得到所述紫苏籽油纳米颗粒。
107.实施例4
108.本实施例提供一种紫苏籽油纳米颗粒,与实施例1的区别仅在于,酵母壳的最终浓度为3mg/ml,其他制备步骤同实施例1。
109.实施例5
110.本实施例提供一种紫苏籽油纳米颗粒,与实施例1的区别仅在于,酵母壳的最终浓度为12mg/ml,其他制备步骤同实施例1。
111.实施例6
112.本实施例提供一种紫苏籽油纳米颗粒,与实施例1的区别仅在于,自组装的温度为18℃,时间为22h,其他制备步骤同实施例1。
113.实施例7
114.本实施例提供一种紫苏籽油纳米颗粒,与实施例1的区别仅在于,自组装的温度为32℃,时间为16h,其他制备步骤同实施例1。
115.对比例1
116.本对比例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以
下步骤:
117.(1)称取250g变性淀粉,加入1500g的55℃热水中,高速搅拌使之完全溶解,形成水相;
118.(2)称取20g玉米低聚肽,加入至步骤(1)得到的水相中,高速搅拌使之溶解;
119.(3)称取250g紫苏籽油,即油相,用高速剪切机对步骤(2)中所得水相在10000rpm下进行高速剪切,并缓慢加入油相,在油相完全加入后,保持剪切10min,得到乳状液;
120.(4)应用高压均质机对步骤(3)中所得乳状液于30-60℃均质3次,均质压力为40mpa;
121.(5)将步骤(4)中均质后的乳状液进行喷雾干燥,进风温度为140℃,出风温度为85℃,得到玉米低聚肽紫苏籽油微胶囊颗粒。
122.对比例2
123.本对比例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以下步骤:
124.(1)将超净工作台里面的20w紫外线灯管打开预热20min,使光波稳定在253.7nm。将大豆分离蛋白粉平铺在直径为9cm的玻璃培养皿中,然后放置于垂直距离紫外线灯下20cm处辐照40min;
125.(2)称取步骤(1)处理过的大豆分离蛋白粉15.0g,加入250ml蒸馏水,磁力搅拌器搅拌1h,配置成6.0%(w/v)的悬浊液。在500w的超声功率下处理60min后,4000r/min离心10min去除不溶物,制备得到4.0%(w/v)的大豆分离蛋白溶液;
126.(3)将步骤(2)得到的大豆分离蛋白与壳寡糖按照1:1的质量比混合形成500ml溶液,保持固形物浓度为2.9%(w/v),磁力搅拌器搅拌12h,使其混合均匀。调节混合溶液ph至8.5,100℃水浴加热6h后冷却到室温。
127.(4)在步骤(3)得到的反应液中加入0.5g葡萄酒皮渣多糖(质量百分比占总壁材的3.3%),搅拌混合均匀,混合物中总壁材浓度达到3.0%(w/v)。以此混合物为壁材,调节ph值到5.5后,加入15.0g紫苏籽油,保持芯壁质量比为1:1,30℃、10000r/min乳化30min,形成o/w型乳状液。
128.(5)在进风温度为180℃、出风温度为80℃、进样速度为10ml/min的条件下,将所述o/w型乳状液喷雾干燥获得紫苏籽油微胶囊粉末。
129.对比例3
130.本对比例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以下步骤:
131.(1)配料。室温下,在配料罐中加入重量比为2:4:1的麦芽糊精、变性淀粉和蔗糖3种壁材。
132.(2)溶解灭菌。室温下,加入与壁材2倍重量的水,将步骤(1)的配料制成固形物含量为33.3%的壁材水溶液;80℃水浴,灭菌30min。
133.(3)壁材与芯材的混合与预乳化。将步骤(2)得到的壁材水溶液降温至50℃后,按芯材(紫苏籽油)和壁材1:1的配比加入紫苏籽油,搅拌15min,使其充分混匀,加水配成固形物含量45%的乳化液。
134.(4)高压均质。将步骤(3)得到的乳化液用高压均质机30mpa(300bar)均质2次,
50mpa(500bar)均质3次,得到均一稳定的乳浊液。
135.(5)喷雾干燥。将步骤(4)得到的乳浊液喷雾干燥,雾化器转速为18000rpm/min,进风温度180℃,出风温度80℃,进料温度70℃,进料速度为50l/h,得到紫苏籽油微胶囊粉末。
136.对比例4
137.本对比例提供一种紫苏籽油纳米颗粒,所述紫苏籽油纳米颗粒的制备方法包括以下步骤:
138.配制桃胶-明胶溶液(桃胶和明胶的质量比为1:1,壁材浓度为1.25%),溶解后加入紫苏籽油(芯壁比为1:1),再用高速分散均质机(12000rpm)进行乳化,倒入三口烧瓶中40℃恒温搅拌(300rpm),醋酸调节ph至4.3,进行复合凝聚反应一段时间后,降温至15℃,用氢氧化钠调节ph至6.0,加入转谷氨酰胺酶进行固化,反应2.5h后停止搅拌,固化12h,抽滤洗涤沉淀后得到微胶囊湿囊,将微胶囊湿囊倒入培养皿中,放入冰箱中冷藏过夜,经真空干燥机冷冻干燥即得到粉末状紫苏油产品。
139.测试例
140.测试例一气相色谱-质谱法分析制备例2得到的紫苏籽油
141.采用气相色谱-质谱联用仪(gc-ms),使用db-wax毛细管柱(30m 0.25mm0.25μm),氦气流速为1.0ml/min,温度程序为:50℃加热1分钟,然后以5℃/min的升温速率升至240℃,240℃持续5min。分流模式(80:1)分析40min。进样器温度为280℃,离子源温度为230℃。在单离子监测(sim)模式和电子电离(ei)模式下进行分析,电离能为70ev。基本条件为四级杆温度为150℃,辅助加热温度为250℃,传输线温度为280℃,质量扫描范围为35-455m/z。定性分析在
±
20%的离子比例参考范围内进行。
142.gc-ms对紫苏籽油进行分析发现,紫苏籽油中脂肪酸含量为95.48%,其他物质含量为4.52%,其中脂肪酸含量主要有10种,包括α-亚麻酸65.37%、亚油酸13.85%、油酸9.57%、鲸蜡酸4.97%、十八烷酸1.35%、十六烷酸0.14%、二十碳烷酸0.12%、花生酸0.062%、棕榈油酸0.037%和十七烷酸0.012%。
143.测试例二
144.紫苏籽油纳米颗粒的特性分析
145.测试方法:将实施例1得到的紫苏籽油纳米颗粒加入到马尔文zeta尺寸纳米仪的电极杯中,检测紫苏籽油纳米颗粒的粒径分布和表面电荷。通过扫描电镜对紫苏籽油纳米颗粒的表面特征和尺寸大小进行检测。采用高效液相色谱法测定紫苏籽油纳米颗粒溶液上清中游离紫苏油的浓度。
146.如图5所示,超声自组装后,紫苏籽油纳米颗粒相对均一。如图6所示,紫苏籽油纳米颗粒的平均粒径为316.74nm。如图7所示,紫苏籽油纳米颗粒表面电荷为+2.9mv。如图8所示,紫苏籽油被成功包裹到酵母壳中,载油效率约为89.21%,其中:载油效率(%)=(加入油总量-游离油量)/加入油总量。
147.测试例三
148.紫苏籽油纳米颗粒在模拟胃酸和模拟肠液中的释放率测试
149.测试样本:实施例1制备得到的紫苏籽油纳米颗粒。
150.测试方法:将100μl紫苏籽油纳米颗粒分别放在400μl模拟胃酸或400μl模拟肠液中,采用hplc法测定游离紫苏籽油的浓度,计算紫苏籽油纳米颗粒的释放效率。
151.模拟胃酸的配制:0.85%的生理盐水,加入稀盐酸,加入5mg胃蛋白酶,调节ph至2.2;
152.模拟肠液的配制:0.068g kh2po4溶解于2.5ml加入5mg胰蛋白酶,naoh调节ph至8.6。
153.测试结果如图9所示,紫苏籽油纳米颗粒在模拟胃酸条件下稳定存在,在模拟肠液条件下可有效释放,释放效率约为91.34%。
154.测试例四
155.紫苏籽油纳米颗粒对dpph自由基清除能力测试
156.(一)测试方法:采用dpph法测定紫苏籽油(制备例2)、胃酸-纳米粒子(实施例1)和肠液-纳米粒子(实施例1)的抗氧化能力,具体包括以下步骤:取不同浓度样品500μl,加入500μl 0.1mol/l dpph无水乙醇溶液,室温避光反应30min,于波长517nm处测定吸光度,试验设置空白组(超纯水代替样品)、对照组(无水乙醇代替dpph溶液)及实验组。dpph自由基清除率计算公式为:dpph自由基清除率(%)=1-(ai-aj)/ac
×
100。式中:ai为样品组吸光度;aj为对照组吸光度;ac为空白组吸光度。
157.其中,胃酸-纳米粒子的制备方法包括以下步骤:将紫苏籽油纳米颗粒溶液与模拟胃酸溶液按照1:4混合。
158.肠液-纳米粒子的制备方法包括以下步骤:将紫苏籽油纳米颗粒溶液与模拟肠液溶液按照1:4混合。
159.测试结果如图10所示,与维生素c相比,游离紫苏油具有相似的dpph自由基清除能力,显著高于模拟肠液和模拟胃酸中的紫苏籽油纳米颗粒的自由基清除能力。
160.放置100天后,如图11所示,紫苏籽油纳米颗粒的抗氧化作用比游离状态更稳定;这些结果说明紫将苏籽油包裹到酵母壳中,形成纳米颗粒,有助于提高紫苏籽油的稳定性。
161.(二)采用上述办法测试实施例1-7和对比例1-4提供的紫苏籽油纳米颗粒对dpph自由基清除能力测试,制备当天和常温放置100天后,紫苏籽油纳米颗粒dpph自由基清除能力测试结果如下表1所示:
162.其中,差值=制备当天dpph自由基清除率-放置100天后dpph自由基清除率。
163.表1
164.[0165][0166]
由表1数据可知,本技术实施例1-3制备得到紫苏籽油纳米颗粒可以提高紫苏籽油的稳定性。
[0167]
通过实施例1和实施例4-5的对比可知,制备过程中酵母壳溶液的浓度会影响颗粒的稳定性。
[0168]
通过实施例1和实施例6-7的对比可知,制备过程中自组装的温度会影响颗粒的稳定性。
[0169]
通过实施例1和对比例1-4的对比可知,将紫将苏籽油包裹到酵母壳中最有利于提高紫苏籽油的稳定性。
[0170]
测试例五
[0171]
紫苏籽油纳米颗粒抗小鼠冷应激测试
[0172]
以下测试中tnp组均采用实施例1提供的紫苏籽油纳米颗粒处理。
[0173]
测试方法:动物实验经怀化学院动物伦理与福利委员会批准(怀化:2021(h031755))。雄性km小鼠12只,雌性km小鼠12只(分开饲养管理),购自湖南医科大学实验动物中心,饲养于洁净室,12h光照/12h黑暗,自由进水。随机分为4组(每组3雄3雌),包括阴性对照组(nc组)、冷应激模型组(csd组)、紫苏籽油处理组(tpfo组)、紫苏籽油纳米颗粒处理组(tnp组)。整个过程中,nc组小鼠不给药,保持在26℃环境中饲养管理。csd、tpfo和tnp组小鼠在最后的3天(第7-9天)每天置于4℃室中6小时(上午8点至下午2点)进行急性冷应激
处理。在整个实验过程中,tpfo组和tnp组小鼠分别以每天250mg/kg的剂量通过灌胃给予游离紫苏油、紫苏籽油纳米颗粒。在实验结束时(第10天)收集血样用于成分和细胞的含量测定。
[0174]
如图12所示,在冷应激条件下,tpfo和tnp组小鼠体温较csd组更接近正常体温(nc组),tnp组小鼠对冷应激的抵抗力更强,表明膳食补充紫苏籽油有利于恒温,紫苏籽油纳米颗粒的效果更好。
[0175]
如图13所示,冷应激后csd组小鼠体重略有下降,tpfo组和tnp组小鼠体重增加趋势受到抑制。在实验结束时,nc、tpfo和tnp组的小鼠体重显著高于csd组。
[0176]
如图14和图16所示,四组间rbc(红细胞)和plt(血小板)的血液指数没有显著差异。
[0177]
如图15和图17所示,csd、tpfo和tnp组小鼠wbc(白细胞)计数和血清sod(超氧化物歧化酶)水平较nc组显著降低,且给予小鼠游离紫苏籽油或紫苏籽油纳米颗粒后显著恢复,tnp组的效果更好。
[0178]
如图18所示,csd、tpfo和tnp组小鼠血清mda(丙二醛)水平较nc组显著升高,且给予游离紫苏油或纳米颗粒后显著恢复,且tnp组的效果更好。
[0179]
如图19所示,csd组小鼠空腹血糖水平较nc组显著降低,tpfo组小鼠给予游离紫苏油后显著恢复,给予小鼠紫苏籽油纳米颗粒后tnp组血糖保持较高水平。
[0180]
以上结果表明,紫苏籽油纳米颗粒比游离紫苏油具有更好的冷应激预防作用,将紫苏籽油与酵母壳组装可以提其生物相容性。
[0181]
申请人声明,本发明通过上述实施例来说明本发明的工艺方法,但本发明并不局限于上述工艺步骤,即不意味着本发明必须依赖上述工艺步骤才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明所选用原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1