一种雪菊提取物用于制备治疗脑损伤药物的应用
1.本发明具体涉及一种雪菊提取物用于制备治疗脑损伤药物的应用。
背景技术:
2.雪菊是药食两用植物,雪菊中含有多种药理成分,例如黄酮、生物碱、挥发性油、有机酸、皂苷、氨基酸等。现有研究发现,雪菊中含有300多种天然成分,其中包括30多种黄酮类物质,30多种人体必需的矿物元素,20多种氨基酸,数十种芳香族化合物,还有丰富的有机酸、萜烯类、维生素、木脂体、酶类、多糖等具有生物活性的天然成分。
3.目前黄菊主要作为降血压、降血脂、调节血糖以及抗癌药物使用。本发明的研究发现雪菊提取物还具有治疗脑损伤的功效。
技术实现要素:
4.基于此,本发明提供了一种雪菊提取物的新医药用途,即作为制备治疗脑损伤药物的用途,为雪菊医学研究提供了一种新方向。
5.本发明所述雪菊提取物的制备方法包括以下步骤:
6.(1)将新鲜雪菊置于温度为40℃的恒温干燥箱中干燥3-6h,然后将干燥后的雪菊粉碎过筛,得到雪菊粉;
7.(2)将雪菊粉与提取剂按料液比为1:10~30g/ml混合,室温浸泡1-5h,所述提取剂为乙醇、乙酸乙酯、冰醋酸和丙酮的混合溶液,所述提取剂中乙醇、乙酸乙酯、冰醋酸以及丙酮的体积比为10:2~5:3~7:1~2;
8.(3)将浸泡后的物料加热回流10-12h,过滤后得到滤液和滤渣;
9.(4)将所述滤液进行减压蒸干,得到粗提物;
10.(5)将所述粗提取利用氯仿进行萃取,得到萃取液;
11.(6)将所述萃取液进行减压蒸干,最后利用乙醇进行重结晶,得到雪菊提取物。
12.优选的,步骤(2)所述提取剂中的乙醇为无水乙醇,含水量低于0.2wt%。
13.优选的,步骤(3)所述粗提物与氯仿的料液比为1:10~20g/ml。
14.优选的,所述雪菊提取物中总黄酮和总多酚含量之和大于99wt%,所述总黄酮含量为55-60wt%。
15.与现有技术相比,本发明具有以下有益效果:
16.本发明是利用雪菊提取物作为治疗脑损伤药物使用,并对acr诱导脑损伤的小鼠进行试验,通过试验结果发现,雪菊提取物治疗后的小鼠脑损伤程度得到有效抑制。
附图说明
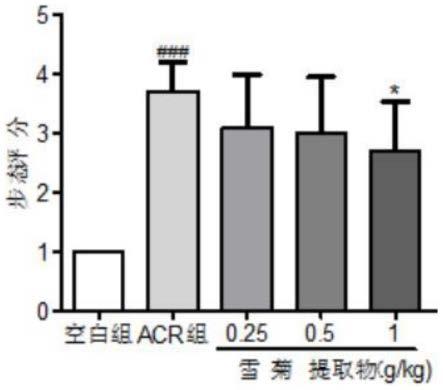
17.图1为雪菊提取物对acr诱导脑损伤的小鼠步态评分的影响;
18.图2为雪菊提取物对acr诱导脑损伤的小鼠后肢支撑力的影响;
19.图3为雪菊提取物对acr诱导脑损伤的小鼠移动格子数和站立次数的影响;
20.图4为雪菊提取物对acr诱导脑损伤的小鼠海马ca1区组织细胞排列影响;
21.图5为雪菊提取物对acr诱导脑损伤的小鼠海马ca3区组织细胞排列影响。
具体实施方式
22.为使本发明的目的、特征和优点能够更加明显易懂,下面结合附图对本发明的具体实施方式做详细的说明。附图中给出了本发明的若干实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容更加透彻全面。
23.实施例1
24.一种雪菊提取物的制备方法,其步骤如下:
25.(1)将新鲜雪菊置于温度为40℃的恒温干燥箱中干燥5h,然后将干燥后的雪菊粉碎过筛,得到雪菊粉;
26.(2)将雪菊粉与提取剂按料液比为1:20g/ml混合,室温浸泡5h,所述提取剂为体积比10:3:5:1的无水乙醇、乙酸乙酯、冰醋酸和丙酮构成的混合溶液;
27.(3)将浸泡后的物料加热回流12h,过滤后得到滤液和滤渣;
28.(4)将所述滤液进行减压蒸干,得到粗提物;
29.(5)将所述粗提取与氯仿的料液比为1:15g/ml进行萃取,得到萃取液;
30.(6)将所述萃取液进行减压蒸干,最后利用乙醇进行重结晶,得到雪菊提取物。
31.经检测,本发明制备的雪菊提取物中总黄酮含量为58.2wt%,总多酚含量为40.9wt%。
32.实施例2
33.一种雪菊提取物的制备方法,其步骤如下:
34.(1)将新鲜雪菊置于温度为40℃的恒温干燥箱中干燥5h,然后将干燥后的雪菊粉碎过筛,得到雪菊粉;
35.(2)将雪菊粉与提取剂按料液比为1:10g/ml混合,室温浸泡5h,所述提取剂为体积比10:3:5:1的无水乙醇、乙酸乙酯、冰醋酸和丙酮构成的混合溶液;
36.(3)将浸泡后的物料加热回流12h,过滤后得到滤液和滤渣;
37.(4)将所述滤液进行减压蒸干,得到粗提物;
38.(5)将所述粗提取与氯仿的料液比为1:15g/ml进行萃取,得到萃取液;
39.(6)将所述萃取液进行减压蒸干,最后利用乙醇进行重结晶,得到雪菊提取物。
40.经检测,本发明制备的雪菊提取物中总黄酮含量为58.4wt%,总多酚含量为41.1wt%。
41.实施例3
42.一种雪菊提取物的制备方法,其步骤如下:
43.(1)将新鲜雪菊置于温度为40℃的恒温干燥箱中干燥5h,然后将干燥后的雪菊粉碎过筛,得到雪菊粉;
44.(2)将雪菊粉与提取剂按料液比为1:30g/ml混合,室温浸泡5h,所述提取剂为体积比10:3:5:1的无水乙醇、乙酸乙酯、冰醋酸和丙酮构成的混合溶液;
45.(3)将浸泡后的物料加热回流12h,过滤后得到滤液和滤渣;
46.(4)将所述滤液进行减压蒸干,得到粗提物;
47.(5)将所述粗提取与氯仿的料液比为1:15g/ml进行萃取,得到萃取液;
48.(6)将所述萃取液进行减压蒸干,最后利用乙醇进行重结晶,得到雪菊提取物。
49.经检测,本发明制备的雪菊提取物中总黄酮含量为58.5wt%,总多酚含量为40.6wt%。
50.利用实施例1制备的雪菊提取物对acr(丙烯酰胺)致对脑损伤的小鼠进行实验,具体实验方法如下:
51.(1)动物分组及处理
52.50只小鼠(icr雄性,体重18-22g)适应性喂养3天称重。随机选取40只小鼠注射丙烯酰胺进行脑损伤建模处理,获得acr诱导脑损伤小鼠,另外10只小鼠为空白组。选取30只acr诱导脑损伤小鼠分别注射雪菊提取物,另外1只为acr组。其中10只acr诱导脑损伤小鼠注射剂量为0.25g/kg,为雪菊提取物低剂量组,10只acr诱导脑损伤小鼠注射剂量为0.5g/kg,为雪菊提取物中剂量组,10只acr诱导脑损伤小鼠注射剂量为1.0g/kg,为雪菊提取物高剂量组。
53.(2)步态评分
54.雪菊提取物对acr诱导脑损伤的小鼠的步态评分结果见图1。与空白组相比,acr组有明显的显著性差异(p《0.001),经观察acr组行走明显不协调、肢体无力、后肢外展、不能支撑体重、呈“一”字脚,表明脑组织受到一定的损伤,造模成功。雪菊提取物高剂量组具有显著性差异(p《0.05)。
55.(3)后肢支撑力
56.对实验小鼠的后肢支撑力进行分析,如图2所示。与空白组相比,acr组小鼠后肢外展小鼠自由落下,它的后肢距离扩大,有显著性差异(p《0.001),原因可能是acr毒性导致小鼠肢体无力、后肢外展、后肢支撑力减小、表明脑组织受到一定的损伤,造模成功。与acr组相比,雪菊提取物中、高剂量组小鼠的后肢距离缩短,有显著性差异(p《0.05,p《0.01)。
57.(4)旷场实验
58.雪菊提取物对acr致小鼠脑损伤下移动格子数和站立次数结果见图3。移动格子数如图3a所示,与空白组相比,acr组移动格子数减少,差异有统计学意义(p《0.001)。与acr组相比,雪菊提取物组(0.25、0.5、1g/kg)移动格子数增加(p《0.001)。站立次数如图3b所示,与空白组相比,acr组站立次数减少(p《0.001)。与acr组相比,雪菊提取物(0.25、0.5、1g/kg)组站立次数上升,差异有统计学意义(p《0.01、p《0.01、p《0.05)。
59.(5)小鼠脑部海马组织病理切片he染色
60.如图4-图5所示,空白组中小鼠海马细胞数目较多,形态结构正常,细胞排列紧密有序,细胞核大而圆,ca1区细胞呈多层均匀分布,排列紧密,ca3区细胞胞体较大。
61.与空白组相比,acr组小鼠海马ca1区和ca3区细胞排列紊乱疏松,数量减少,细胞间距变宽,部分核仁溶解消失。雪菊提取物0.25g/kg组中ca1区与空白组相比细胞数量明显减少,细胞间距变宽,部分核仁溶解消失;ca3区中可见细胞排列紊乱,细胞间距变宽。
62.与acr组相比,雪菊总提取物(0.25g/kg、0.5g/kg、1.00g/kg)组中ca1区细胞着色较浅,细胞数量增加,细胞间距变窄,部分核仁溶解消失;ca3区中可见随着雪菊总提取物的增加而细胞排列变得有序,细胞间距变宽,损伤程度明显减弱。
63.以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1