m5C甲基化调节因子DNMT1、NSun2在肿瘤中的应用的制作方法
本发明涉及医药,具体涉及一种m5c甲基化调节因子dnmt1、nsun2在肿瘤中的应用。
背景技术:
1、细胞应对压力应激时,会出现程序性细胞死亡,称为凋亡。在肿瘤治疗中已发现和阐明了多条凋亡信号通路,被认为是目前癌症治疗中最有希望和最有效的机制。因此,提高细胞凋亡敏感性已成为治疗多药耐药肿瘤(如骨肉瘤)的主要策略。细胞凋亡的启动在很大程度上取决于抗凋亡和促凋亡基因激活的平衡,而基因表达的调控是多层次且有序的。
2、基因的甲基化修饰作为一种重要的表观遗传学修饰手段,参与基因的表达调控。胞嘧啶甲基化(m5c)是基因组dna和mrna中常见的核苷酸修饰,在转录和转录后水平上调节基因表达起关键作用。dna甲基化常发生在启动子区域的cpg岛中,使基因转录失活。dna甲基转移酶i(dnmt1)可甲基化许多抑癌基因的启动子区域,被认为是癌症治疗的一个重要靶点。此外,dnmt1的许多调节因子参与了dna甲基化活化和招募dnmt1到特定基因位点的调控,暗示了dnmt1通过dna甲基化调控基因表达的功能多样性。一些具有众所周知的抗凋亡的致癌基因也被证明通过启动子甲基化在转录中被抑制。例如,在karposi肉瘤细胞系中,抗凋亡基因axl启动子区域cpg岛的低甲基化促进了转录因子sp与其结合,进而使其表达上调。此外,最近发现dnmt1介导的启动子甲基化可以抑制抗凋亡基因bcl2、bclxl和bcl6的表达,从而阻碍细胞生存和肿瘤生长。
3、rnam5c的修饰决定了mrna在转录后多个阶段的命运,包括mrna的剪接、转运和翻译等。nsun2作为一种重要的rna胞嘧啶甲基转移酶,能够维持有丝分裂纺锤体的稳定性,增强cdk1的翻译,减少p27的表达,从而从根本上促进肿瘤细胞增殖。nsun2的缺失促进应激诱导的trna清除,增加皮质、海马体和纹状体神经元的凋亡。据报道,在食管鳞状细胞癌中,nsun2甲基化长链非编码rna(lncrna)nmr可抑制顺铂诱导的细胞凋亡并促进肿瘤进展。但nsun2是否通过mrna甲基化调控凋亡相关基因的表达,进而影响凋亡过程值得进一步研究。
技术实现思路
1、鉴于此,本发明的目的在于提供一种m5c甲基化调节因子dnmt1、nsun2在肿瘤中的应用。
2、本发明的技术方案如下:
3、一种m5c甲基化调节因子在调控肿瘤细胞凋亡中的应用,所述调节因子包括dnmt1和/或nsun2。
4、所述dnmt1通过dna甲基化调控抗凋亡基因axl、notch2、yap1的表达。
5、所述nsun2通过mrna甲基化调控抗凋亡基因axl、notch2、yap1的表达。
6、所述dnmt1通过甲基化nsun2的启动子区域抑制nsun2的表达。
7、所述肿瘤为骨肉瘤。
8、本发明还提供一种m5c甲基化调节因子在制备预防、治疗肿瘤的药物中的应用,所述调节因子包括dnmt1和/或nsun2。
9、本发明还提供一种甲基化调节因子dnmt1、nsun2与化疗药物联用在制备治疗或预防骨肉瘤药物中的应用。
10、所述化疗药物包括自顺铂、卡铂、奥沙利铂、奈达铂、乐铂、阿霉素中的一种或几种。
11、本发明还提供一种抗凋亡基因表达抑制剂,所述抑制剂包括nsun2。
12、所述抗凋亡基因包括axl、notch2、yap1中的一种或几种。
13、越来越多的人认识到真核生物中广泛的核苷酸修饰在生物过程中具有重要作用。在数百种化学修饰中,5-甲基胞嘧啶是一种高度关注的表观遗传修饰,已在基因组dna和各种rna家族中被确认。m5c在dna和rna调控中的双重性促使研究人员研究这两个相同的甲基化成分在不同水平上是否存在某种相互关系或协同作用,以及相关的机制和结果是什么。我们发现dnmt1通过甲基化nsun2的启动子降低nsun2的表达,进而导致相互靶向的抗凋亡基因的启动子dna和mrna上的胞嘧啶甲基化的耦合变化,包括但可能不限于axl、notch2和yap1。我们关注这些基因是因为它们之前被记录的抗细胞凋亡的显著作用。通过它们的dna和mrna之间的胞嘧啶甲基化耦联,在药物诱导的骨肉瘤细胞凋亡中可以实现对基因表达的强大抑制,这明确表明了凋亡相关基因调节机制的复杂性。。本发明在不同的表观遗传水平上,特别是在dna和mrna上,胞嘧啶甲基化可以相互联系,协调决定抗凋亡基因表达和凋亡抗性,明确地为表观遗传调控增加了新的层次。
14、在不同类型肿瘤中,大量的抑癌基因的启动子区高甲基化,这直接使其转录失活,进而维持肿瘤细胞的存活。dnmt1作为dna甲基化的维持酶,负责抑癌基因启动子甲基化。大多数抑癌基因可通过其启动子区的高甲基化促进细胞凋亡我们的研究结果表明dnmt1通过启动子甲基化抑制抗凋亡基因nsun2、axl、notch2和yap1的表达,而nsun2的抑制进一步通过减弱axl、notch2和yap1mrna的甲基化破坏其翻译,最终从转录和转录后两个方面联合增强dnmt1对这些抗凋亡靶点的抑制作用。这一发现不仅强调了dnmt1在调控基因表达方面可能利用的多种模式,而且扩展了我们对dnmt1在肿瘤细胞凋亡中的功能的认识。
15、rnam5c修饰在恶性实体瘤中的研究中得到了极大的重视。许多报道表明nsun2介导的rna甲基化在多种泛癌途径中起着强烈的致癌作用,包括癌细胞增殖、迁移、侵袭和耐药。同时,我们的研究发现,nsun2的缺乏会在给药早期阻碍肿瘤生长,并由于mrnam5c丢失引起的翻译抑制而损害抗凋亡基因表达,进而导致化疗药物引发骨肉瘤细胞凋亡,重申了nsun2的关键作用,并揭示rna胞嘧啶甲基化在肿瘤细胞进展和耐药过程中的重要作用。
16、总的来说,dna甲基转移酶dnmt1被发现通过甲基化nsun2启动子来抑制rna甲基转移酶nsun2的表达,从而在dna和rna胞嘧啶甲基化之间建立关键的耦合,进而影响化疗期间骨肉瘤细胞凋亡抗性。我们的发现无疑为不同表观遗传水平的基因表达控制增加了一层新的层面,并为未来骨肉瘤的治疗提供了新的思路。
17、与现有技术相比,本发明具有如下有益效果:
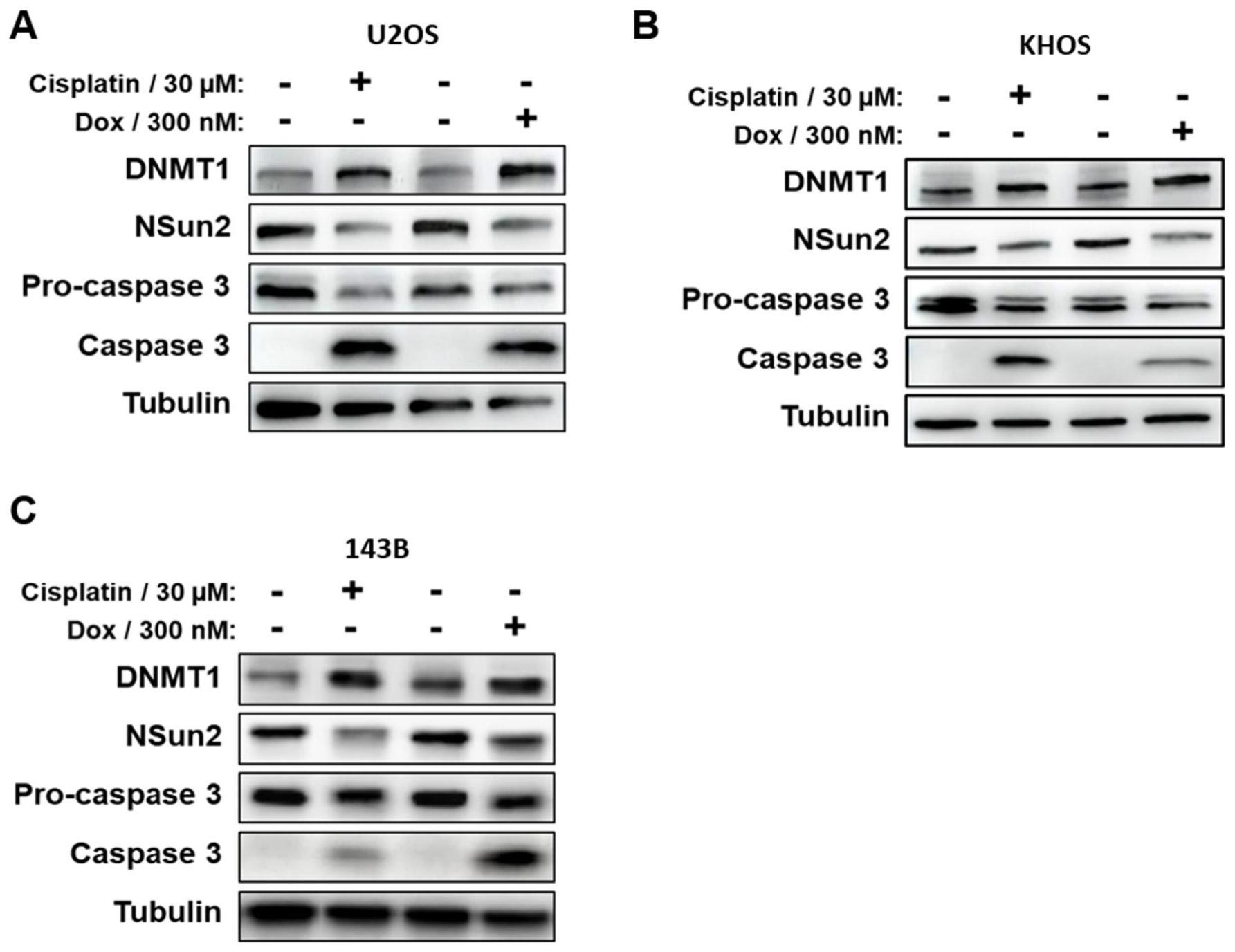
18、1、细胞凋亡是化疗治疗人类癌症的核心机制。在dna和mrna上的5-甲基胞嘧啶(m5c)修饰被证实可独立调控细胞凋亡。然而,它们在细胞凋亡中的相互作用或相互影响尚未被发现。在此,我们发现了dnmt1介导的基因启动子区域甲基化与nsun2介导的mrna甲基化协同调节骨肉瘤细胞凋亡。在化疗药物诱导的骨肉瘤细胞凋亡过程中,dnmt1表达增加,而nsun2表达被抑制。本发明发现dnmt1通过甲基化nsun2启动子抑制nsun2的表达。dnmt1和nsun2分别通过dna甲基化和mrna甲基化调控抗凋亡基因axl、notch2和yap1。当暴露于顺铂或阿霉素时,dnmt1升高,nsun2受到抑制,这些抗凋亡基因的启动子甲基化增强,mrna甲基化减弱,大幅降低了这些抗凋亡基因的表达,从而使骨肉瘤细胞凋亡。本发明的研究结果建立了dna和rna胞嘧啶甲基化相互作用在化疗期间骨肉瘤抗凋亡能力的重要性,为未来骨肉瘤的治疗提供了新的视角,并在表观遗传的不同层次调控基因表达提供了新的见解。
19、2、我们揭示了dna和rna甲基化修饰骨肉瘤细胞凋亡方面的重要联系。dnmt1抑制nsun2的表达,从而使其下游共同靶基因axl、notch2和yap1的启动子和mrna上的胞嘧啶甲基化耦联改变。在这种情况下,dnmt1的升高极大地抑制了这些抗凋亡基因的表达,使骨肉瘤细胞容易在化疗药物诱导下发生凋亡。因此,我们强调了基因组dna和mrna中常见的表观遗传修饰m5c调节抗凋亡基因的表达,进而共同决定骨肉瘤细胞对诱导凋亡药物的耐药性。总之,这些发现将为肿瘤细胞凋亡提供新的见解,并为未来骨肉瘤的治疗开辟新的途径。
- 还没有人留言评论。精彩留言会获得点赞!