一种PD-L1引导的特异性靶向对比剂-多模态成像探针及其制备方法与应用与流程
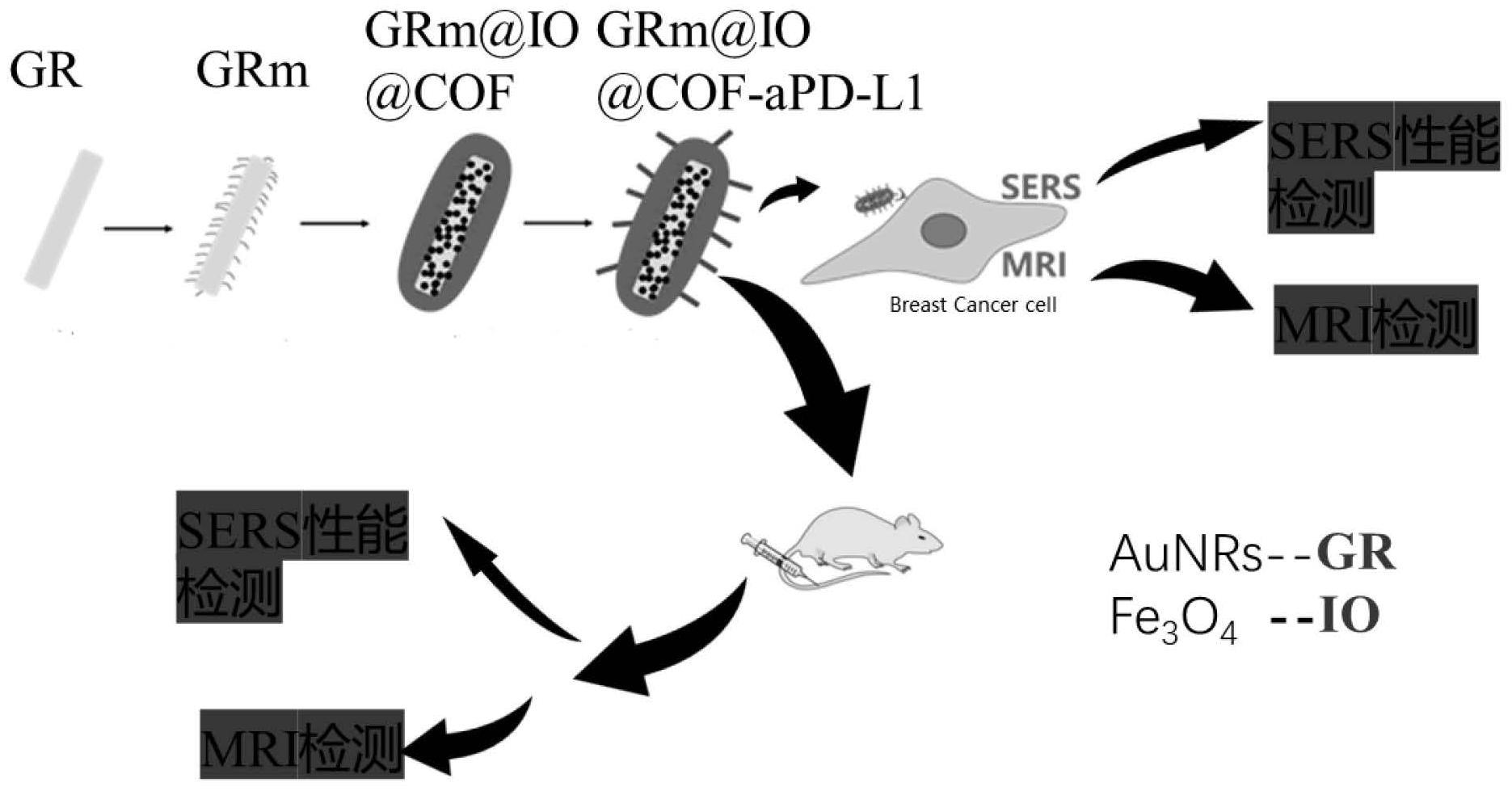
本发明属于生物探针,涉及一种pd-l1引导的特异性靶向对比剂-多模态成像探针及其制备方法与应用。
背景技术:
1、乳腺癌在中年妇女发病率及死亡率均居首位,现有研究证明,早期诊断及准确区分肿瘤边界在乳腺癌的治疗及预后评估中起着重要作用,其中细胞程序性死亡配体1(programmed cell death 1ligand 1,pd-l1)发挥着独特的角色。程序性死亡配体是指可以与细胞程序性死亡受体1相互结合的细胞因子,可传导抑制性信号,抑制cd8+t细胞的增生,且可以间接调节bcl-2基因,抑制淋巴结中抗原特异性t细胞的聚集。
2、目前临床上为了明确乳腺癌的诊断、评价预后、制定治疗方案以及评价疗效,绝大多数情况下均须经过穿刺活检获取病理标本,但因穿刺活检为介入创伤性检查,有时可导致出血、感染,切除过多乳房组织影响乳房外观导致部分患者难以接受。另外,穿刺活检也难以对乳腺病变的进展程度、治疗效果等进行动态评价。同时,乳腺是人体内腺体及淋巴组织非常丰富的器官,影像检查容易出现假阴性,当临床表现以及实验室检查出现异常时,乳腺的病理改变可能已进入转移阶段而无法逆转。因此临床需要一种无创、敏感、患者易于接受,且能动态监测乳腺病理改变的评价手段。
技术实现思路
1、本发明的目的在于针对现有技术出现的不足,提供一种pd-l1引导的特异性靶向对比剂-多模态成像探针及其制备方法与应用。
2、本发明的一个目的通过以下技术方案来实现:
3、一种pd-l1引导的特异性靶向对比剂-多模态成像探针,包括:对比剂组分和特异性抗体组分;
4、所述对比剂组分包括核心及生物相容性材料,所述核心包括贵金属纳米粒子表面负载超顺磁性纳米颗粒,所述生物相容性材料为共价有机框架;
5、所述特异性抗体组分为pd-l1抗体,其结合在所述生物相容性材料表面。
6、在本发明的对比剂-多模态成像探针中,作为优选,所述贵金属纳米粒子为金纳米棒。作为优选,所述超顺磁性纳米颗粒为超顺磁性fe3o4纳米颗粒。
7、在本发明的对比剂-多模态成像探针中,作为优选,所述贵金属纳米粒子的粒径为30~80nm。作为优选,所述超顺磁性纳米颗粒的粒径≤5nm。
8、在本发明的对比剂-多模态成像探针中,作为优选,超顺磁性纳米颗粒与贵金属纳米粒子通过包括共价键的形式结合。
9、在本发明的对比剂-多模态成像探针中,作为优选,所述生物相容性材料包覆在核心表面,厚度为2~5nm。
10、在本发明的对比剂-多模态成像探针中,作为优选,所述共价有机框架为tapb-btca cof,其通过包括tapb和btca的单体制备而得。
11、在本发明的对比剂-多模态成像探针中,作为优选,贵金属纳米粒子、超顺磁性纳米颗粒、和生物相容性材料的物质的量之比为(100~150):(100~150):(50~70)。
12、在本发明的对比剂-多模态成像探针中,作为优选,所述pd-l1引导的特异性靶向对比剂-多模态成像探针的粒径为40~100nm。
13、本发明的另一个目的通过以下技术方案来实现:一种pd-l1引导的特异性靶向对比剂-多模态成像探针的制备方法,包括以下步骤:
14、(1)制备贵金属纳米粒子,在贵金属纳米粒子表面连接拉曼信号分子,然后在贵金属纳米粒子表面连接氨基;
15、(2)制备超顺磁性纳米颗粒,活化超顺磁性纳米颗粒的表面羧基;
16、(3)将步骤(1)的产物和步骤(2)的产物分散于磷酸盐缓冲液中,搅拌,离心得到核心;
17、(4)将核心、tapb和btca加入至乙腈,随后加入乙酸,室温搅拌,离心获得生物相容性材料包覆核心;
18、(5)在生物相容性材料包覆核心中加入pd-l1,搅拌,离心得到pd-l1引导的特异性靶向对比剂-多模态成像探针。
19、本发明的另一个目的通过以下技术方案来实现:
20、一种pd-l1引导的特异性靶向对比剂-多模态成像探针在制备检测乳腺癌病灶的多模态成像对比剂中的应用。
21、与现有技术相比,本发明具有以下有益效果:
22、1、本发明提供的特异性靶向对比剂-多模态成像探针利用特异性抗体组分pd-l1在靶向区域高浓度聚集,并利用对比剂组分中贵金属纳米粒子具有的拉曼信号特性,使靶向组织形成特异性的拉曼信号图像,对肿瘤边界进行微观区分,而超顺磁性纳米颗粒具有磁化特性、改变靶向组织的t1/t2弛豫时间,从而形成靶向组织特征性的mr图像和ct图像,从而实现多模态成像;
23、2、本发明的特异性靶向对比剂-多模态成像探针能够跨膜转运进入体内,顺利进入乳腺癌病灶处,并进行mr/ct/拉曼成像,无需穿刺活检,从而避免出血、感染,甚至大出血、败血症等严重并发症,还能够对乳腺病变的进展程度、治疗效果等进行动态评价,是一种无创、敏感、患者易于接受,且能动态监测乳腺病理改变的评价手段;利用多模态成像,特异性靶向对比剂-多模态成像探针直观反映并量化评价pd-l1在三阴性乳腺癌内的沉积状态,监测乳腺病变情况;
24、3、本发明的特异性靶向对比剂-多模态成像探针的贵金属纳米粒子进一步为金纳米棒,且所述超顺磁性纳米颗粒进一步为粒径≤5nm的超顺磁性纳米颗粒;金纳米棒结构有利于负载粒径≤5nm的超顺磁性纳米颗粒,使得本发明的核心结构更稳定,更有利于跨膜转运;
25、4、本发明核心中的超顺磁性纳米颗粒与贵金属纳米粒子优选为通过包括共价键的形式结合,通过共价键连接的核心结构更稳定;
26、5、本发明包覆在核心表面的共价有机框架为tapb-btca cof,其通过包括tapb和btca的单体制备而得;共价有机框架可溶性良好,其包覆在核心表面,cof的苯环结构又能够与特异性抗体组分共价结合,从而稳定地将核心与特异性抗体组分结合到一起,提高pd-l1引导的特异性靶向对比剂-多模态成像探针的稳定性与安全性;
27、6、本发明采用的pd-l1引导的特异性靶向对比剂-多模态成像探针的制备方法,多得到的纳米磁性颗粒性状稳定,大小均一,粒径大小为40~100nm,穿透力优异,能够顺利进入乳腺癌病灶处,且制作过程简单,规模化生产成本较低。
技术特征:
1.一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,包括:对比剂组分和特异性抗体组分;
2.根据权利要求1所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,所述贵金属纳米粒子为金纳米棒,和或所述超顺磁性纳米颗粒为超顺磁性fe3o4纳米颗粒。
3.根据权利要求1或2所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,所述贵金属纳米粒子的粒径为30~80nm,所述超顺磁性纳米颗粒的粒径≤5nm。
4.根据权利要求1或2所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,超顺磁性纳米颗粒与贵金属纳米粒子通过包括共价键的形式结合。
5.根据权利要求1所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,所述生物相容性材料包覆在核心表面,厚度为2~5nm。
6.根据权利要求1或5所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,所述共价有机框架为tapb-btca cof,其通过包括tapb和btca的单体制备而得。
7.根据权利要求1所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,贵金属纳米粒子、超顺磁性纳米颗粒和生物相容性材料的物质的量之比为(100~150):(100~150):(50~70)。
8.根据权利要求1所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针,其特征在于,所述pd-l1引导的特异性靶向对比剂-多模态成像探针的粒径为40~100nm。
9.如权利要求1所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针的制备方法,其特征在于,包括以下步骤:
10.如权利要求1所述的一种pd-l1引导的特异性靶向对比剂-多模态成像探针在制备检测乳腺癌病灶的多模态成像对比剂中的应用。
技术总结
本发明属于生物探针技术领域,涉及一种PD‑L1引导的特异性靶向对比剂‑多模态成像探针及其制备方法与应用。所述PD‑L1引导的特异性靶向对比剂‑多模态成像探针,包括:对比剂组分和特异性抗体组分;所述对比剂组分包括核心及生物相容性材料,所述核心包括贵金属纳米粒子表面负载超顺磁性纳米颗粒,所述生物相容性材料为共价有机框架;所述特异性抗体组分为PD‑L1抗体,其结合在所述生物相容性材料表面。该探针能通过MR/CT成像直观反映并量化评价PD‑L1在乳腺癌的沉积状态,通过拉曼对肿瘤边界的微观区分,监测乳腺癌进展情况,提供了一种无创诊断、动态评价三阴性乳腺癌的全新多模态成像手段。
技术研发人员:邵国良,潘婷,林杰,吴爱国,武小侠,张定虎,李顺祥
受保护的技术使用者:浙江省肿瘤医院
技术研发日:
技术公布日:2024/1/13
- 还没有人留言评论。精彩留言会获得点赞!