一种载前药功能化外泌体递释系统及其制备方法
本发明属于生物医药,具体涉及一种载前药功能化外泌体递释系统及其制备方法。
背景技术:
0、技术背景
1、三阴性乳腺癌(tnbc)是雌激素受体(er)、孕激素受体(pr)和人表皮生长因子受体2(her2)均为阴性的乳腺癌亚型。由于其丰富的肿瘤干细胞微环境,tnbc是最具侵袭性和最难治疗的乳腺癌类型。近年来,分子分型彻底改变了乳腺癌的治疗,一些亚型被发现对某些治疗药物高度敏感。尽管如此,tnbc仍未被确定为明确的治疗靶点,化疗仍是晚期病例的主要治疗方式。紫杉醇是治疗tnbc最有效的化疗药物之一,它通过稳定微管来抑制细胞分裂。最近的研究表明,证实ptx可以诱导肿瘤细胞中的免疫原性细胞死亡,从而引发特异性抗肿瘤免疫反应。抗pd-l1抗体atezolizumab联合白蛋白结合型紫杉醇显着降低了pd-l1阳性tnbc患者疾病进展的风险,进一步证明紫杉醇诱导的肿瘤细胞免疫原性死亡(icd)可以通过引发广谱抗肿瘤免疫来提高免疫治疗效率。
2、axl受体酪氨酸激酶在包括tnbc在内的各种人类恶性肿瘤类型中显着上调,并且与肿瘤发生和预后不良有关。axl通过加速emt过程,形成正反馈回路,促进化疗耐药、干细胞增强细胞侵袭。此外,激活axl可抑制肿瘤抗原呈递,抑制促炎细胞因子,并破坏免疫浸润以介导肿瘤免疫逃逸和免疫治疗耐药。axl的抑制不仅可以直接抑制肿瘤细胞的生长,还可以逆转肿瘤免疫抑制微环境,增强pd-1阻断的疗效。此外,axl的下调也可以促进肿瘤细胞icd。
3、目前,尽管已经开发出多种axl抑制剂,但大多是非选择性的,axl小分子抑制剂的开发还处于起步阶段。由于axl在多种细胞类型中均有表达,因此这些axl的小分子抑制剂可能存在脱靶毒性,极大地限制了其临床应用。此外,肿瘤细胞不可避免地会通过基因突变产生耐药性,就像它们对其他激酶抑制剂所做的那样。sirna通过降解mrna,可以防止蛋白质结构改变引起的耐药性,是一种潜在的治疗方法。但sirna体内稳定性较差,不易被细胞摄取。此外,紫杉醇水溶性差,生物利用度低,血药浓度持续时间短,无肿瘤靶向性。iii期临床研究(impassion130和impassion131)结果表明,只有纳米级的白蛋白结合型紫杉醇可增强pd-l1阻断疗效,而游离紫杉醇与atezolizumab联合并不能改善pfs或os。此外,免疫治疗抗体、sirna和化疗药物的理化性质在体内差异很大,这使得很难同时作用于同一肿瘤细胞以发挥协同作用。
4、综上所述,将基因治疗/化疗/免疫治疗有机整合是治疗三阴性乳腺癌很有潜力的治疗手段之一。但如何克服毒性,并利用载体实现ptx与sirna、pd-1/pd-l1阻断相互协同成为高效治疗三阴性乳腺癌面临的重要难题。
技术实现思路
1、鉴于上述目前技术领域中存在的不足,本发明的目的在于:通过将基因治疗/化疗/免疫治疗有机整合有机整合到一个平台来解决三阴性乳腺癌的治疗效率低的缺陷,同时通过外泌体的靶向递送以及肿瘤环境响应型前药设计来克服药物的不良反应,达到“高效低毒”治疗三阴性乳腺癌的目点。该外泌体递送系统适合于肌肉注射、皮下注射、皮内注射、瘤内注射、瘤旁注射、经皮给药等方式;且制备方法简便,适于大规模生产。
2、为实现上述技术目的,本发明采用以下技术方案:
3、本发明构建了人和小鼠三阴性乳腺癌ptx耐药细胞系,发现axl在ptx耐药细胞中显着上调,从而导致肿瘤细胞对ptx产生耐药,并通过促进肿瘤细胞上皮间质转换(emt)程序,从而增强肿瘤细胞干性的发生,利用axl-sirna下调axl的表达能够克服ptx耐药并且增强免疫治疗效率。此外,外泌体作为一种新兴的药物/基因内源性纳米递送载体,综合了细胞药物递送和纳米技术的优势:免疫原性低,且能穿透生理屏障,兼具被动靶向及内在的主动靶向能力。本发明通过分析cd8+t细胞免疫检查点表达,发现抗cd3/抗cd28抗体(αcd3/αcd28)活化的cd8+t细胞外泌体表面高表达pd-1,且该外泌体表面的pd-1能够并能与肿瘤细胞表面配体(pd-l1)结合,阻断其与效应性t细胞免疫检查点的结合,实现pd-1/pd-l1免疫检查点阻断治疗。本发明首先将ptx和亲水性阳离子聚合物pll与高浓度gsh响应性二硫键连接形成肿瘤微环境响应的ptx-ss-pll(ptx-pll),其自组装形成肿瘤特异性前药胶束;然后将负电荷的axl-sirna(si-axl)通过与pll的静电相互作用吸附在前药胶束表面,克服了外泌体对游离sirna负载效率低的缺陷;最后利用活化的t细胞来源的外泌体包被,构建共载肿瘤特异性响应ptx-pll前药与siaxl的功能化外泌体仿生递释系统(命名为pp/siaxl@exo),将基因治疗/化疗/免疫治疗有机整合用于治疗tnbc。
4、本发明的有益效果在于:
5、合理设计的pp/siaxl@exo在基因治疗、化疗和免疫治疗之间实现协同效应:si-axl联合外泌体介导的pd-l1阻断逆转t细胞免疫抑制,重塑肿瘤免疫微环境;此外,si-axl克服ptx耐药性,与ptx协同高效诱导icd建立正反馈免疫循环,将冷肿瘤转化为热肿瘤,介导持久的肿瘤特异性免疫记忆效应。基于外泌体良好的生物安全性和肿瘤靶向性,以及肿瘤特异性微环境响应的前药设计,pp/siaxl@exo有效克服了游离siaxl和ptx的脱靶毒性,表现出极高的安全性。
技术特征:
1.一种载前药功能化外泌体递释系统,其特征在于:包括以下部分:ptx-pll前药、axl-sirna(siaxl)、功能化外泌体。
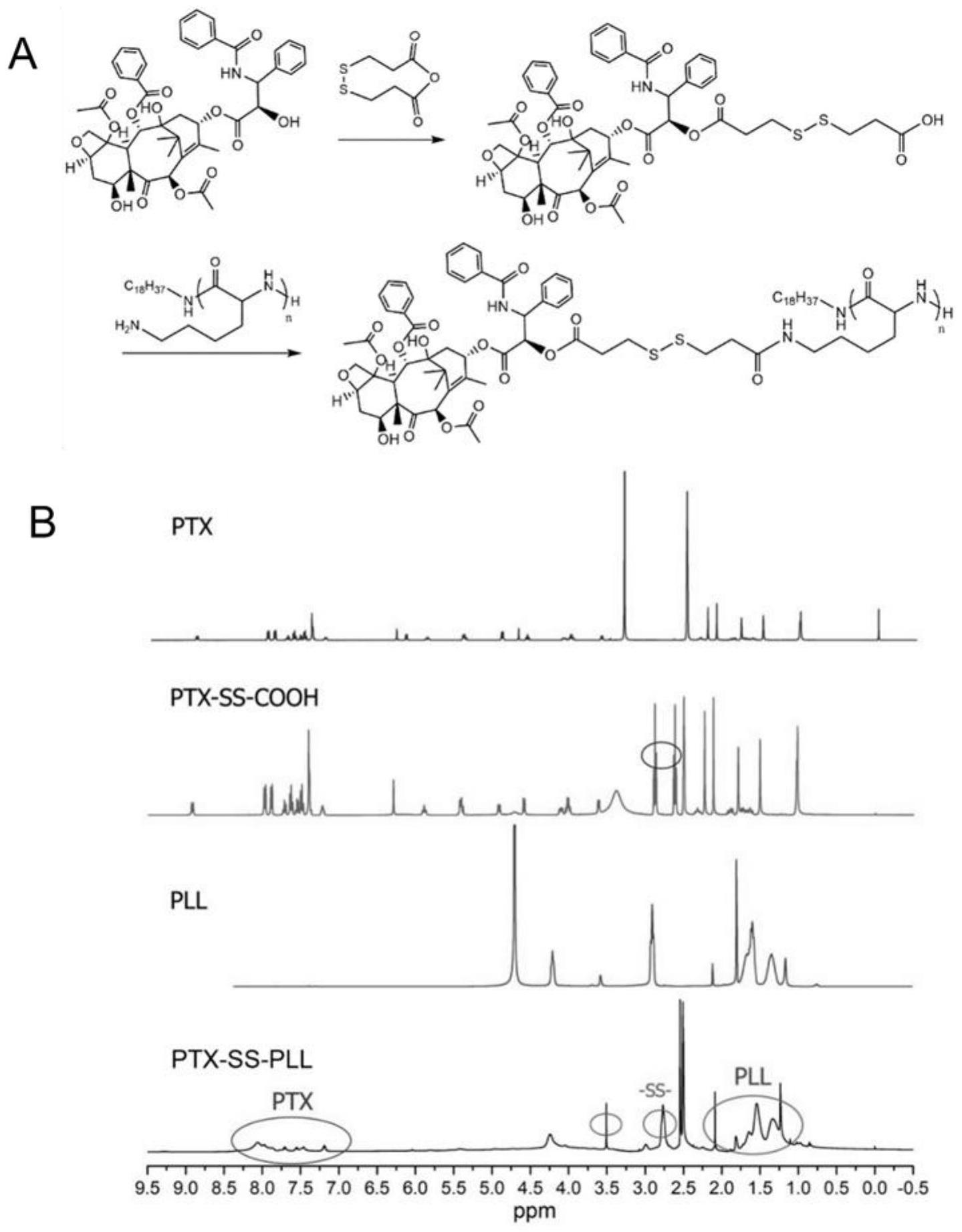
2.如权利要求1所述的载前药功能化外泌体递释系统,其特征在于:前药ptx-pll前药为ptx和亲水性阳离子聚合物pll与高浓度gsh响应性二硫键连接形成ptx-s-s-pll(ptx-pll),其自组装形成肿瘤特异性前药胶束。
3.如权利要求1所述的载前药功能化外泌体递释系统,其特征在于:外泌体部分为活化的t细胞来源的外泌体,表面高表达pd-1。
4.如权利要求1-3任意一项所述的载前药功能化外泌体递释系统的制备方法,其特征在于,包括以下步骤:
5.如权利要求4所述的载前药功能化外泌体递释系统的制备方法,其特征在于:
6.如权利要求4所述的载前药功能化外泌体递释系统的制备方法,其特征在于:
7.如权利要求4所述的载前药功能化外泌体递释系统的制备方法,其特征在于:
8.如权利要求1-7任意一项所述的载前药功能化外泌体递释系统在制备抗肿瘤药物中的应用。
9.如权利要求1-7任意一项所述的载前药功能化外泌体递释系统在制备抗肿瘤药物中的应用,包括其他可使用的辅料。
技术总结
本发明公开了一种载前药功能化外泌体递释系统,包括PTX‑PLL前药、AXL‑siRNA(AXL)以及由活化的T细胞分泌的外泌体。本发明公开的载前药的活化CD8+T细胞外泌体递释系统通过PTX和亲水性阳离子聚合物PLL与GSH响应性二硫键连接形成PTX‑S‑S‑PLL(PTX‑PLL),其自组装形成肿瘤微环境响应的前药胶束。si‑AXL通过与PLL的静电相互作用吸附在前药胶束表面,然后装载到活化的T细胞来源的外泌体(命名为PP/siAXL@EXO)中用于治疗TNBC。PP/siAXL@EXO精准靶向肿瘤位点,阻断并下调肿瘤表面的PD‑L1,然后肿瘤细胞高效摄取。在细胞内,吸附在前药胶束表面的siAXL首先在酸性环境中释放克服PTX耐药并增强胞外的免疫治疗效应,然后通过高浓度GSH降解二硫键释放PTX,从而达到肿瘤特异性杀伤作用。
技术研发人员:陈传荣,张佳利,沈鸣,何杨,盛莉莉
受保护的技术使用者:皖南医学院第一附属医院(皖南医学院弋矶山医院)
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!