基于仿生膜的精准靶向治疗卵巢癌的纳米药物及其制备方法
本发明属于生物医药领域,涉及肿瘤化疗与免疫联合治疗、dna纳米自组装体、仿生膜涂层纳米技术和药物递送系统,特别是指基于仿生膜的精准靶向治疗卵巢癌的纳米药物及其制备方法。
背景技术:
1、卵巢癌是女性生殖系统三大恶性肿瘤之一,通过免疫疗法激活免疫系统,诱导细胞毒性t淋巴细胞杀伤肿瘤细胞在卵巢癌治疗中至关重要。然而由于单一疗法的局限性,加上卵巢癌细胞易转移和易耐药的特点,治疗效果并不理想。因此寻求多种治疗手段联合治疗,以获得持久的临床效果,提高卵巢癌患者总生存期,是治疗卵巢癌的关键。
2、化疗一直是癌症治疗的重要手段,在临床治疗和研究中广泛应用,但面临毒性强、易耐药等缺陷。许多研究将化疗药物和免疫调节剂联合用于抗肿瘤,一方面通过化疗药物直接快速杀死肿瘤细胞,另一方面通过免疫激活剂激活免疫反应持续杀伤肿瘤细胞,这种化疗免疫联合治疗方式能发挥良好的抗肿瘤效果。化疗免疫联合疗法的应用弥补了单一疗法的局限性,提高了抗肿瘤效果。为进一步提高疗效,常采用药物递送系统共递送化疗药和免疫激活剂,提高其肿瘤靶向性和在肿瘤组织中的浓度,然而,目前对化疗免疫疗法的递送策略多为共包封、共递送策略,难以将化疗药物和免疫激活剂分别精准递送至肿瘤中的不同靶细胞,一方面降低了两种药物在其靶细胞中的浓度,另一方面干扰非靶细胞执行其功能,难以高效治疗肿瘤。本课题组前期公开的专利cn115990247a中将化疗与免疫治疗联合起来的dna纳米药物,可通过在细胞膜上开孔,加快化疗药进入肿瘤细胞,并以抗原分子标记肿瘤细胞膜,增强了肿瘤细胞的免疫原性,增效免疫化疗联合治疗;但是该dna纳米药物并无肿瘤细胞靶向性和特异性,为避免对正常组织和器官的副作用,只能在肿瘤部位注射应用,且其共载化疗药和免疫激活剂,不能使其分别递送至肿瘤细胞和免疫细胞,限制了其抗肿瘤疗效。
3、因此,如何设计和制备分别靶向的递送系统,将化疗药物和免疫激活剂分别精准递送至癌细胞和免疫细胞,是进一步提高化疗免疫联合治疗效果的一种有效途径。
技术实现思路
1、本发明提出一种基于仿生膜的精准靶向治疗卵巢癌的纳米药物及其制备方法,通过两种膜的分别靶向作用,将化疗药物和免疫激活剂分别递送至同源癌细胞和免疫细胞,从而增强化疗免疫联合抗卵巢癌的治疗效果。
2、本发明的技术方案是这样实现的:
3、基于仿生膜的精准靶向治疗卵巢癌的纳米药物,所述纳米药物包括a组分和b组分,a组分由卵巢癌细胞膜、dna立方体和化疗药物组成;b组分由大肠杆菌外膜囊泡、dna立方体和肿瘤抗原分子组成。
4、优选的,纳米药物中a组分和b组分的质量比为1:1。
5、优选的,所述dna立方体由长链1ab、2ba、3ab、4ba和短链b14自组装制备得到;其中1ab的碱基序列如seq id no.1所示,2ba的碱基序列如seq id no.2所示,3ab的碱基序列如seq id no.3所示,4ba的碱基序列如seq id no.4所示;b14的碱基序列如seq id no.5所示,其5’端修饰有氨基。
6、优选的,所述肿瘤抗原分子与dna短链b14经交联剂4-(n-马来酰亚胺甲基)环己烷-1-羧酸磺酸基琥珀酰亚胺酯钠盐(sulfo-smcc)连接后再与dna立方体相连。
7、优选的,所述化疗药物均匀嵌入dna立方体的碱基对之间。
8、进一步,所述卵巢癌细胞膜包裹在载有化疗药物的dna立方体的外周,大肠杆菌外膜囊泡包裹在连接有肿瘤抗原分子的dna立方体的外周。
9、优选的,卵巢癌细胞膜包裹载有模型化疗药-阿霉素(dox)的dna立方体,大肠杆菌外膜囊泡包裹连接有模型肿瘤抗原分子-鸡卵清蛋白表位序列(ova257-264)的dna立方体。
10、上述的基于仿生膜的精准靶向策略增效化疗免疫联合治疗卵巢癌的纳米药物,制备步骤为:
11、(1)将dna链1ab、2ba、3ab、4ba与b14按1:1:1:1:4的摩尔比混合,程序降温的条件为:95℃保持5分钟,然后经30分钟匀速降温至80℃并保持5分钟,再以2分钟/1℃的速度降温至40℃,最后以3分钟/1℃降温到4℃,得dna立方体;
12、(2)将步骤(1)的dna立方体(cube)与化疗药物以化疗药物过量的比例恒温震荡反应后,经离心弃上清,得cube-化疗药物;
13、(3)将氨基修饰nh2-短链b14与交联剂sulfo-smcc室温搅拌反应2小时,经超滤除去多余交联剂后,再与肿瘤抗原分子室温搅拌反应过夜,经超滤除去多余的肿瘤抗原分子,即得b14-肿瘤抗原分子。将步骤(1)的dna立方体与b14肿瘤抗原分子按1:4的摩尔比混匀后,以升温至40 ℃然后30分钟内匀速降温至4℃为单次循环,共循环进行4次,得dna立方体-肿瘤抗原分子;
14、(4)将卵巢癌细胞破碎,通过离心去除细胞器等杂质沉淀,再经高速离心后得到癌细胞膜沉淀(im)。将大肠杆菌菌液经离心后去除菌体,取上清经浓缩后进行超速离心,沉淀即为大肠杆菌外膜囊泡(omvs)。
15、(5)将步骤(2)的dna立方体-化疗药物与步骤(4)获得的im以适当比例混合,超声3分钟,得卵巢癌细胞膜包裹的dna立方体-化疗药物这一纳米制剂,为终制剂的a组分;再将步骤(3)的dna立方体-肿瘤抗原分子与步骤(4)获得的omvs以适当比例混合,超声3分钟,得大肠杆菌外膜囊泡包裹的dna立方体-肿瘤抗原分子这一纳米制剂,为终制剂的b组分。
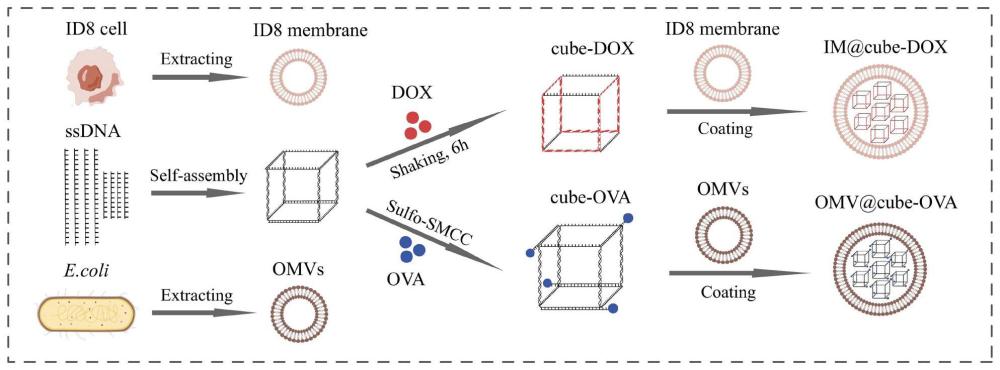
16、进一步以阿霉素和卵清蛋白表位多肽为例,实际中不限于阿霉素和卵清蛋白多肽,制备一种卵巢癌细胞膜包裹dna立方体-阿霉素和大肠杆菌外膜囊泡包裹dna立方体-卵清蛋白表位多肽的a+b组分混合纳米药物(im@cube-dox+omv@cube-ova),其空间结构如图1所示。
17、优选的上述im@cube-dox+omv@cube-ova的制备方法,步骤为:
18、将nh2-修饰的b14与ova利用交联剂sulfo-smcc连接起来,具体方法是将nh2-b14用pbs溶解后与sulfo-smcc按照1:10的摩尔比混合,室温下搅拌反应2小时,再用超滤管离心除去多余sulfo-smcc,然后将产物与ova按照1:10的摩尔比,室温下搅拌反应过夜,再用超滤管离心除去多余ova,即获得b14-ova。
19、将cube与b14-ova按照1:4的摩尔比混匀,从40℃匀速降温历经30分钟到达4℃,该降温过程共循环进行4次,即获得cube-ova;
20、本发明具有以下有益效果:
21、1、本发明利用癌细胞膜和大肠杆菌外膜囊泡分别包裹化疗药物dox和肿瘤抗原ova,使其分别精准靶向同源癌细胞和抗原呈递细胞,增效化疗免疫联合治疗卵巢癌,其疗效显著优于非分别精准靶向策略。
22、2、利用大肠杆菌外膜囊泡包裹肿瘤抗原,既能增强抗原稳定性和抗原呈递细胞的摄取效率,又能作为免疫佐剂,增强免疫激活作用,进而增强抗原特异性t细胞的杀伤作用。
23、3、利用癌细胞膜包裹dna立方体-阿霉素,既能增强其对同源癌细胞的靶向性,又能降低非靶细胞如免疫细胞对其的摄取,从而降低化疗药对免疫细胞的毒性。
24、4、采用dna纳米结构负载ova,能精确控制ova的数量和空间位置,再利用膜包裹后,能增加基于dna纳米结构的纳米药物的稳定性,增强药效。
- 还没有人留言评论。精彩留言会获得点赞!