一种模拟血管壁微纳结构的双层仿生血管的制备方法与流程
本发明属于组织工程领域,具体是一种以血管来源脱细胞基质的纳米纤维膜作为材料采用3d的方式制备模拟血管壁微纳结构的双层仿生血管的方法。
背景技术:
1、感染、创伤、动脉粥样硬化等多种血管疾病均会导致血管缺损,生物制造的人工血管可成为自体血管的替代品,但多数人工血管未能模拟血管壁结构实现结构仿生,导致再生效果有限。由于天然血管壁具有多层纤维平行排列的微纳结构,利用静电纺丝技术可制备平行排列纳米纤维,而同轴生物打印在打印管状结构上具有较大优势,因此将纳米电纺膜与同轴打印墨水结合打印血管,将有可能实现对血管壁微纳结构的模拟,构建双层仿生血管。但是现有的纳米电纺膜大多是采用人工合成的生物可降解聚合物,如聚己内酯(pcl)、聚乳酸(pla)和聚乳酸-聚乙醇酸(plga)等,由于其可加工性及机械性能,最早被用于电纺成纳米纤维膜;但是这种人工合成材料不含细胞识别位点,并且,材料本身的疏水性和酸性降解产物会对细胞产生负面影响,限制了其在生物体内的再生效果。
技术实现思路
1、针对上述现有技术的不足,本发明提供一种模拟血管壁微纳结构的双层仿生血管的制备方法,采用具有良好生物相容性的纳米纤维膜进行制备,制备的仿生血管具有均匀的外径和内径,有良好的吸水性能;纳米纤维能够在血管壁中沿长轴方向有序排列,能够在管壁内外层形成浓度梯度;复合水凝胶能够为细胞提供仿生外环境,使细胞充分伸长并建立细胞连接。
2、为了达到上述技术目的,本发明提供了一种模拟血管壁微纳结构的双层仿生血管的制备方法,包括如下步骤:
3、s1制备血管脱细胞基质:
4、(1)将新鲜猪主动脉预处理后得到血管片,使用75%酒精浸泡20-30min,去除血污并初步消毒;
5、(2)将血管片转移至离心管中,加入0.3% sds溶液,置于摇床中处理24-30h;弃去离心管内液体,用去离子水清洗三次,加入3% tritonx-100溶液,置于摇床中处理24-30h;弃去离心管内液体,用去离子水清洗至无明显泡沫,加入溶解于0.15mol/l nacl的dna酶溶液,置于摇床消化24h;弃去离心管内液体,加入pbs,置于摇床清洗45-48h,去除化学残留;
6、(3)将经过步骤(2)处理后的血管片转移至培养皿中,预冷冻随后使用真空冷冻干燥机冻干12h;并将冻干后的血管片研磨,获得脱细胞血管粉末备用;
7、(4)将胃蛋白酶以1mg/ml浓度溶解于0.01mol/l hcl中,配制成胃蛋白酶-hcl消化液,置于离心管中,按照10mg/ml的浓度加入脱细胞血管粉末,置于恒温摇床在37℃,100-120rpm中消化48~72h,至离心管内无肉眼可见的明显沉淀;然后使用滤网过滤溶液,去除未消化完全的部分,用naoh溶液中和消化液,调节ph至7.4,并将消化液转移至培养皿中,预冷冻随后真空冷冻干燥机冻干10-12h,获得可溶性vdecm;
8、s2.制备纳米纤维膜:
9、(1)称取一定量的pcl和vdecm溶解于六氟异丙醇中,其中pcl在六氟异丙醇中浓度8~12%,pcl与vdecm质量比为3.5-4.5:1;通过超声均质仪超声,形成稳定、无明显颗粒的纺丝液;
10、(2)将纺丝液转移至注射器中,固定在注射泵上,连接19g钝头不锈钢针头,调节注射速率为1ml/h,接受距离14-16cm,针头处连接正压13kv,接收板连接负压13kv,进行电纺;
11、(3)电纺完成后,将纳米纤维膜冻干12-18h,去除溶剂残留得到纳米纤维膜;
12、s3.纳米短纤维的制备;将s2步骤中制备的纳米纤维膜剪成小块,加入叔丁醇高速均质乳化形成纤维悬液,然后转移至孔板中冷冻干燥得到短纳米纤维;其中所述纳米纤维膜与叔丁醇质量比为0.8-1.2mg/ml;
13、s4.制备gelma/fiber复合水凝胶的制备;取s3步骤中短纳米纤维加入去离子水中,然后采用移液枪反复吹打至纤维均匀分散在液体中,再添加4.5-5.5%的gelma,在避光条件下添加0.4-0.6%的lap(光引发剂),最后将混合溶液在36-38℃水浴锅中加热溶解,并搅拌均匀冷却制备成短纳米纤维浓度为1.5%和1%的gelma/fiber复合水凝胶,
14、s5.模拟血管壁微纳结构的双层仿生血管打印:
15、(1)将s4步骤中配制的两种不同浓度的gelma/fiber复合水凝胶分别置于容器中用锡纸包裹避光,置于36-38c水浴加热溶解;形成短纳米纤维浓度为1.5%和1%的gelma/fiber复合打印墨水;
16、(2)将步骤(1)中配制好的两种不同浓度的gelma/fiber复合墨水转移至注射器中,置于室温下避光降温;
17、(3)连接生物3d打印机,内层采用短纳米纤维浓度为1%的gelma/fiber复合打印墨水,外层采用短纳米纤维浓度为1.5%的gelma/fiber复合打印墨水,中间为去离子水,设置打印温度为22℃~25℃;设置内层墨水推挤速度为2mm/min,外层墨水推挤速度为1mm/min,去离子水推挤速度为1mm/min;快速推挤注射泵排出连接管内空气,打开内层注射泵,当墨水开始从针头处挤出时,打开外层注射泵和中间层去离子水注射泵打印出双层双层仿生血管。
18、本发明较优的技术方案:所述s1步骤的步骤(1)中预处理步是将新鲜猪主动脉用流水清洗,去除表面污垢,纵向剪开,去除血管表面结缔组织血管外膜,剪成边长约2-8mm的小片。
19、本发明较优的技术方案:所述s1步骤的步骤(2)中摇床处理的参数为室温、100-120rpm;加入dna酶的浓度为75u/ml。
20、本发明较优的技术方案:所述s1步骤的步骤(3)中血管片使用研磨仪研磨,研磨频率60hz,研磨时间110-120s。
21、本发明较优的技术方案:所述s1步骤的步骤(4)中采用70μm滤网过滤溶液,去除未消化完全的部分,naoh溶液的浓度为10mol/l。
22、本发明较优的技术方案:所述s2步骤中步骤(1)中超声均质仪的功率为120w,超声时间15min。
23、本发明较优的技术方案:所述s3步骤中将纳米纤维膜剪切成约2-3mm2大小的小片置于高速均质乳化器的玻璃杯中,将粉碎刀头伸入匀浆玻璃杯中,调节至适当高度,缓慢提高转速至1万转/秒,工作25-30s,调低转速关闭电源,用镊子将缠绕在粉碎刀头上的纤维取下,混匀悬液;再将粉碎刀头伸入匀浆玻璃杯中重复上述动作3~5次直到获得外观均匀、无明显纤维团块的悬液,然后将纤维悬液转移至24孔板中置于-20℃预冻,随后使用真空冷冻干燥机冻干12h,获得纳米纤维。
24、本发明较优的技术方案:所述s5步骤的步骤(2)中将配制好的复合墨水转移至5ml注射器中,置于22°~23℃的室温下避光降温;
25、本发明较优的技术方案:所述s5步骤的步骤(3)生物3d打印机采用型号为sunpbiomaker 2的3d打印机,打印针头根据纳米纤维直径和长度,以及所需血管的孔径,定制的同轴针头。
26、本发明较优的技术方案:所述s5步骤的步骤(3)中在双层仿生血管挤出的同时用紫外光照交联,使用培养皿接收打印的管道;打印完毕,清洗并烘干同轴针头和连接管。
27、血管脱细胞基质(vascular-derived decellularized extracellular matrix,vdecm)是血管组织脱去细胞成分后留下的基质部分,组织中的细胞与核成分被有效去除,保留了与天然细胞外基质相似的组成成分、生物活性和机械完整性,为细胞提供了促进增殖分化的微环境。
28、本发明通过从猪主动脉提取了血管脱细胞基质;将其与聚己内酯(pcl)混合,利用静电纺丝技术制出具有良好生物相容性的可用于双层仿生血管壁的纳米纤维膜;本发明中的脱细胞基质粉末是将猪的胸主动脉进行了脱细胞,完全去除了免疫原性,经冷冻干燥研磨而制备成的粉末。其来源为天然血管,具有良好的生物相容性,含有促进内皮、平滑肌、成纤维细胞生长的多种生物因子,能够有效的促进相应的人工血管内中外层的组织再生。并且,脱细胞基质粉末为天然组分,有良好的生物降解性,使得血管的降解过程和组织再生能够相匹配。
29、本发明将纳米纤维膜分散为短纤维(fiber)后,添加到甲基丙烯酰化明胶(gelma)水凝胶中,制成gelma/fiber复合墨水,其机械强度与能量损耗能否满足打印要求;并能否利用同轴打印挤出过程中喷头对墨水的剪切力,将短纤维膜片挤压形成平行膜片层,进而实现对天然血管壁纤维有序定向排列的微纳结构模拟。
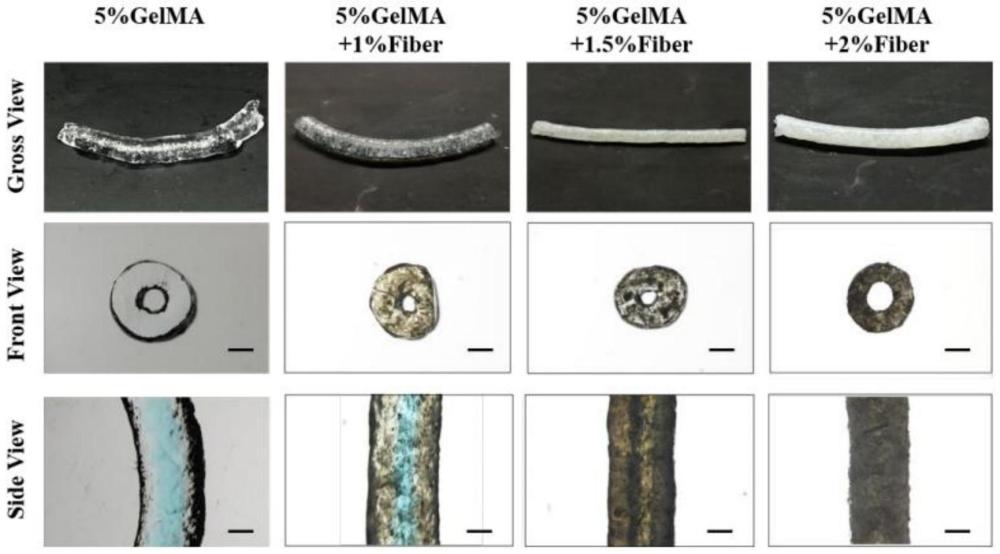
30、本发明制备的仿生血管具有均匀的外径和内径,有良好的吸水性能;纳米纤维能够在血管壁中沿长轴方向有序排列,能够在管壁内外层形成浓度梯度;复合水凝胶能够为细胞提供仿生外环境,使细胞充分伸长并建立细胞连接。
- 还没有人留言评论。精彩留言会获得点赞!