基于抑制肿瘤COX-2和CXCR4的共载脂质纳米胶束及制备方法
本发明属于脂质纳米胶束药物制剂,尤其涉及基于抑制肿瘤cox-2和cxcr4的共载脂质纳米胶束及制备方法。
背景技术:
1、恶性肿瘤是影响人类健康的典型疾病之一。肿瘤微环境(tme)作为肿瘤细胞生长、侵袭和转移所必需的土壤条件,是一个复杂的网络系统,包括细胞成分和非细胞成分,如肿瘤细胞、炎性细胞、成纤维细胞、免疫细胞及分泌的各种细胞因子等。各成分之间密切联系,促进了肿瘤的生长和发展。在多数癌症中,炎症又是肿瘤微环境的重要特征,影响着肿瘤的发生与转移。
2、炎症是肿瘤的重要特征之一。慢性炎症可引发并促进肿瘤的发展。长期慢性炎症能够引起人体正常细胞基因突变形成癌基因,促使细胞癌变并引发癌症。慢性炎症又激活肿瘤细胞中的关键炎症通路,促进多种炎症因子的分泌,实现对多种炎性细胞、免疫抑制细胞的招募,释放大量的肿瘤相关性炎症信号,从而产生促肿瘤炎症(tumor-promotinginflammation),使其成为肿瘤生长的帮凶,促进肿瘤发展、转移以及实现免疫逃逸。《nature reviews clinical oncology》杂志也刊文指出,促肿瘤炎症能够降低机体固有免疫并抑制其适应性免疫应答,是肿瘤治疗失败的重要因素。因此,通过改善肿瘤炎症,降低肿瘤生长与转移,可作为肿瘤研究领域的重要科学问题。
3、环氧合酶-2(cyclooxygenase-2,cox-2)是一种诱导酶,可以促进促炎介质前列腺素2(pge2)产生。cox-2/pge2信号能够招募巨噬细胞、髓源性抑制细胞、肥大细胞等炎性细胞进入肿瘤组织,诱导分泌促肿瘤相关炎症因子和免疫抑制因子,进而促进炎症的发展。另外,cox-2还能够促进细胞增殖、抑制细胞凋亡、促进血管形成,参与肿瘤的发生与发展。有报道称其在不同类型的癌症中过度表达,包括乳腺癌、结肠癌、肺癌、黑色素瘤和前列腺癌等。因此,cox-2有望成为炎性肿瘤的治疗靶点。
4、cxcr4是趋化因子cxcl12的功能受体,能够通过作用于白细胞来调节炎症和免疫过程。cxcl12/cxcr4生物轴能够促进异源三聚体g蛋白的释放,进而激活细胞内各种信号转导途径和下游效应器,促进肿瘤细胞生长与转移、血管生成、上皮间充质转化、促进肿瘤炎症和免疫抑制。cxcr4作为炎性介质又能招募巨噬细胞、髓源性抑制细胞等炎症细胞进入肿瘤。研究发现,cxcr4在许多实体瘤和血液肿瘤中高表达,是肿瘤诊断和治疗的有效靶点。
5、脂质纳米胶束是由两亲性材料自组装而成的纳米结构,与生物膜类似,具有良好的生理环境稳定性和生物相容性,并能够有效装载难溶性药物。通过改变材料的组合,可以实现胶束对药物的最佳装载,并提高稳定性。聚合物胶束由于其体积较小,在生物体内具有良好的通透性和滞留效应,并能进行配体修饰而功能化,因此在药物传递方面具有广泛应用。
6、通过上述分析,现有技术存在的问题及缺陷为:现有技术cxcr4拮抗剂和cox-2抑制剂改善肿瘤相关炎症以及抑制肿瘤细胞的增殖与转移效果差。
技术实现思路
1、为克服相关技术中存在的问题,本发明公开实施例提供了基于抑制肿瘤cox-2和cxcr4的共载脂质纳米胶束及制备方法,本发明的目的就是为了针对改善肿瘤炎症、克服游离药物难溶性问题而提供一种基于抑制肿瘤cox-2和cxcr4的共载脂质纳米胶束及其制备方法,可实现cxcr4拮抗剂和cox-2抑制剂特异性靶向释放,改善肿瘤相关炎症以及抑制肿瘤细胞的增殖与转移,提高炎症肿瘤的治疗效果。
2、所述技术方案如下:基于抑制肿瘤cox-2和cxcr4的共载脂质纳米胶束的制备方法,该方法采用次序包载的方法,将具有截然不同性质的两种药物进行包载,具体包括以下步骤:
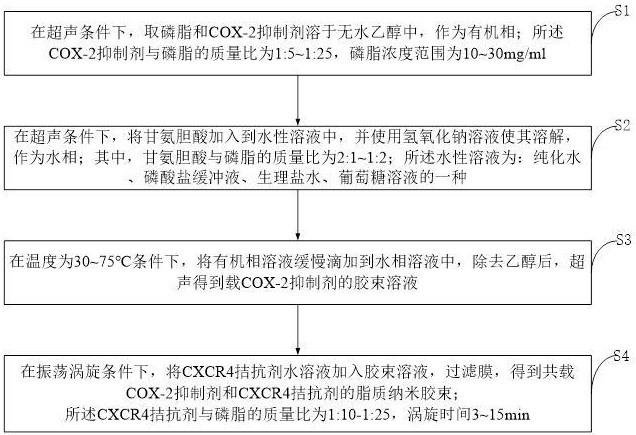
3、s1,在超声条件下,取磷脂和cox-2抑制剂溶于无水乙醇中,作为有机相;所述cox-2抑制剂与磷脂的质量比为1:5~1:25,磷脂浓度范围为10~30mg/ml;
4、s2,在超声条件下,将甘氨胆酸加入到水性溶液中,并使用氢氧化钠溶液使其溶解,作为水相;其中,甘氨胆酸与磷脂的质量比为2:1~1:2;所述水性溶液为:纯化水、磷酸盐缓冲液、生理盐水、葡萄糖溶液的一种;
5、s3,在温度为30~75℃条件下,将有机相溶液缓慢滴加到水相溶液中,除去乙醇后,超声得到载cox-2抑制剂的胶束溶液;
6、s4,在振荡涡旋条件下,将cxcr4拮抗剂水溶液加入胶束溶液,过滤膜,得到共载cox-2抑制剂和cxcr4拮抗剂的脂质纳米胶束;所述cxcr4拮抗剂与磷脂的质量比为1:10-1:25,涡旋时间3~15min。
7、在步骤s1中,所述磷脂选用天然磷脂或选用合成磷脂,所述天然磷脂包括大豆卵磷脂、蛋黄卵磷脂、氢化大豆磷脂中的任意一种或多种,
8、所述合成磷脂包括二棕榈酰磷脂酰胆碱dppc、二油酰磷脂酰甘油dopg、二硬脂酰磷脂酰胆碱dspc中的任意一种或多种;
9、所述cox-2抑制剂为塞来昔布、帕瑞昔布、尼美舒利、美洛昔康、依托考昔中的任意一种。
10、在步骤s2中,所述水性溶液加入甘氨胆酸后的混合溶液的ph值范围为5.0~6.5;氢氧化钠使用浓度为0.1~1m。
11、在步骤s3中,有机相和水相溶液的体积比1:2~1:10,转速范围10~100rpm,除去乙醇方法通过真空旋转蒸发或常压下敞口挥发。
12、进一步,所述的cxcr4拮抗剂为普乐沙福amd3100、motixafortidebkt140、msx-122中的任意一种。
13、本发明的另一目的在于提供一种基于抑制肿瘤cox-2和cxcr4的共载脂质纳米胶束,所述基于抑制肿瘤cox-2和cxcr4的共载脂质纳米胶束利用所述制备方法制备而成,正电性的cxcr4拮抗剂采用静电力作用吸附在共载脂质纳米胶束表面;疏水性的cox-2抑制剂通过物理包封形式装载在共载脂质纳米胶束内部;通过被动靶向进入肿瘤组织后,cxcr4拮抗剂主动靶向cxcr4高表达的肿瘤细胞并从共载脂质纳米胶束表面脱落,进而释放cox-2抑制剂抑制pge2生成,cox-2抑制剂和cxcr4拮抗剂协同降低炎症因子的表达,抑制炎症细胞、免疫抑制细胞的招募,改善促肿瘤炎症。
14、结合上述的所有技术方案,本发明所具备的优点及积极效果为:本发明的制备过程中,使用氢氧化钠调节ph主要作用是使甘氨胆酸溶解,以离子形式存在。若不加氢氧化钠调节酸度,甘氨胆酸不会在pbs溶液中溶解,无法制备纳米胶束。超声有助于胶束的粒径稳定。温度过高或过低都会导致产率下降。
15、甘氨胆酸酸性很强,ph值很低,如果不加氢氧化钠调ph值的话,根本就无法溶解,制备也就没法继续往下进行。ph值必须要在合适的范围。在本发明中,甘氨胆酸既是作为形成脂质纳米胶束的载体材料,还可与cxcr4拮抗剂通过静电结合,得到“药物-甘氨胆酸”的成盐形式,保证药物稳定地吸附在胶束纳米颗粒的表面。
16、本发明合成脂质纳米胶束,改善药物的溶解度,降低药物的毒副作用。纳米胶束因为其具有合适的粒径,可以通过渗透增强和滞留(epr)效应在肿瘤部位蓄积,实现药物的靶向释放,具有良好体内安全性。设计并合成负电性的纳米胶束,具有良好血液相容性,通过静电作用实现与药物的物理连接,通过受体结合实现对肿瘤组织的主动靶向。
17、本发明合成负电性的脂质纳米胶束,cox-2抑制剂为疏水性药物,通过物理包封形式包载于脂质纳米胶束内部;cxcr4拮抗剂呈正电性,与负电性脂质纳米胶束通过静电吸附连接,在体内具有良好的生物安全性,通过epr效应到达肿瘤部位,通过静电结合的cxcr4拮抗剂可以主动靶向cxcr4高表达的肿瘤细胞,由于受体与配体的结合作用力大于cxcr4拮抗剂与负电性胶束的静电吸引力,从而实现amd在与肿瘤细胞上cxcr4靶向结合后,从胶束上响应性脱落。本发明的共载脂质纳米胶束可充分发挥cox-2抑制剂与cxcr4拮抗剂的协同治疗作用,能够同时改善肿瘤炎症,抑制细胞增殖和转移,提高癌症治疗效果。
18、与现有技术相比,本发明制备的共载脂质纳米胶束的平均粒径可控制在10~50nm左右,能够更高效地实现肿瘤渗透,制备方法简便、经济、有效,具有良好的包封率、载药量和稳定性。
- 还没有人留言评论。精彩留言会获得点赞!