一种葡萄糖响应型的遗传物质递送水凝胶及应用
本发明属于生物医药材料,具体涉及一种葡萄糖响应型的遗传物质递送水凝胶及应用。
背景技术:
1、糖尿病慢性创面的治疗是临床治疗中的重大挑战之一,其愈合困难主要源于慢性高糖环境引起的持续性炎症反应、活性氧(ros)水平升高、局部缺氧以及巨噬细胞极化失衡等一系列复杂因素。这些病理特征导致了局部血管生成受阻、成纤维细胞功能受损以及细胞外基质(ecm)沉积不足,从而严重延缓甚至阻碍了伤口的正常愈合。据统计,糖尿病创面患者的截肢率远高于非糖尿病患者,而这些患者的预期寿命也因此显著缩短。
2、根据已有文献,mir-146a作为一种重要的调控因子,在糖尿病创面中普遍表现为下调,而在正常创面中则保持稳定表达。研究表明,过度递送mirna可能引起非特异性基因干扰,甚至导致免疫和代谢异常。
3、为解决糖尿病创面愈合问题,目前已有诸多治疗策略被提出,例如局部使用抗炎药物、抗氧化剂、外用敷料或功能性水凝胶等。然而,这些传统治疗方式存在显著不足。例如,局部抗炎效果有限:高糖环境下,巨噬细胞难以有效从m1型极化向m2型转变,炎症长期持续。另外,抗氧化效率不足:现有抗氧化剂无法快速清除创面高浓度的ros,ros持续累积会进一步破坏组织。最关键的是,缺乏智能响应性:大多数材料难以对创面微环境(如高浓度葡萄糖)产生特异响应,导致药物释放效率低下。因此,在现有技术糖尿病创面中,由于高血糖、ros积累及免疫失调等因素,巨噬细胞的m1型向m2型的转化受到严重抑制,导致长期炎症反应,阻碍创面愈合。硼酸酯键是一种动态共价键,具有动态可逆性,利用其对葡萄糖的敏感性,形成一种葡萄糖响应型的遗传物质递送水凝胶,用于糖尿病创面的治疗,具有积极的意义。
技术实现思路
1、为了解决现有技术中的问题,本发明提供一种葡萄糖响应型的遗传物质递送水凝胶及其应用,利用硼酸酯键对葡萄糖的敏感性,将gox、mno2、mir-146a负载在水凝胶中,结合gox催化降解葡萄糖、mno2纳米颗粒的抗氧化和氧气生成能力,以及mir-146a的精准递送机制,形成葡萄糖响应型的遗传物质递送水凝胶。本发明通过在水凝胶中引入硼酸酯键,实现了高糖环境下水凝胶的形态调控,并达到高糖快速释放gox的目的。降低创面的血糖水平,减轻过氧化氢积累引发的氧化应激,通过mir-146a的环境响应性释放促进巨噬细胞向m2型转化,从而增强创面愈合过程中的抗炎和组织修复功能。水凝胶对创面愈合的促进作用,表现出增强m2巨噬细胞极化、减轻炎症反应并促进血管生成的作用。葡萄糖响应型的遗传物质递送水凝胶系统通过优化水凝胶的结构和功能,为糖尿病创面治疗提供了创新的精准治疗策略,展现了其在基因治疗和局部环境调控方面的巨大应用潜力,为临床转化提供了有力支持。
2、本发明解决其技术问题是采用以下技术方案实现的:
3、本发明的目的在于提供一种葡萄糖响应型的遗传物质递送水凝胶在糖尿病创面药物中的应用,所述葡萄糖响应型的遗传物质递送水凝胶包括gox、负载microrna的中空mno2@pei纳米颗粒。
4、进一步的,所述葡萄糖响应型的遗传物质递送水凝胶中含有硼酸酯键。
5、进一步的,所述microrna为mir-146a。
6、进一步的,所述葡萄糖响应型的遗传物质递送水凝胶促进巨噬细胞由m1型向m2型极化。
7、进一步的,所述gox与负载microrna的中空mno2@pei纳米颗粒的质量比为2:5。
8、进一步的,所述负载microrna的中空mno2@pei纳米颗粒的制备方法为:将中空mno2纳米颗粒加入到pei溶液中磁力搅拌1.5~3h使其分散均匀,离心水洗2次后得到hmno2@pei;用pbs溶解microrna,然后将溶液加入hmno2@pei中进行搅拌,离心水洗后得到所述负载microrna的中空mno2@pei纳米颗粒。
9、进一步的,所述pei溶液还可以用其他阳离子聚合物溶液代替。
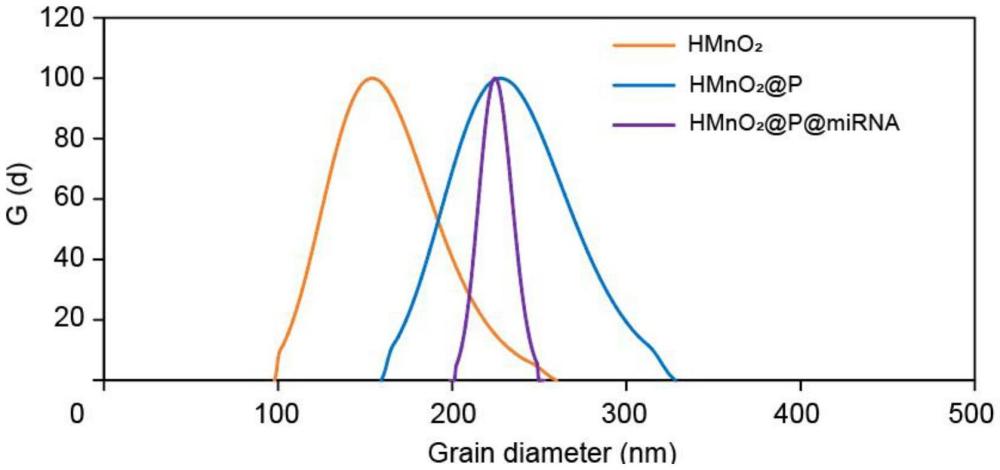
10、进一步的,所述中空mno2纳米颗粒的粒径为150~250nm。
11、进一步的,所述中空mno2纳米颗粒与microrna的质量比为5~20mg:0.5~2od。
12、进一步的,所述葡萄糖响应型的遗传物质递送水凝胶还包括含有硼酸酯键的水凝胶。
13、进一步的,所述含有硼酸酯键的水凝胶为gc-pba+paa-da水凝胶。
14、进一步的,所述葡萄糖响应型的遗传物质递送水凝胶的制备方法为,将gc-pba+paa-da水凝胶、gox、负载microrna的中空mno2@pei纳米颗粒混合后得到。
15、进一步的,所述gc-pba+paa-da水凝胶中gc-pba与paa-da的质量比为1:1。
16、进一步的,所述糖尿病创面包括糖尿病或糖尿病并发症及其治疗过程中所引发的创面。
17、进一步的,所述糖尿病创面包括由糖尿病或糖尿病并发症引起的溃疡、糜烂、坏疽或糖尿病足。
18、与现有技术相比,本发明的有益技术效果在于:
19、本发明利用硼酸酯键对葡萄糖的敏感性,将gox、mno2、mir-146a负载在水凝胶中,结合gox催化降解葡萄糖、mno2纳米颗粒的抗氧化和氧气生成能力,以及mir-146a的精准递送机制,用于糖尿病创面的局部治疗。本发明通过在水凝胶中引入硼酸酯键,实现了高糖环境下水凝胶的形态调控,并达到高糖快速释放gox的目的。
20、通过在水凝胶中负载gox,实现了在高糖环境下的局部血糖调控。gox催化葡萄糖转化为葡萄糖醛酸和过氧化氢,有效降低了创面局部的血糖水平,从而缓解了高糖对细胞功能的持续损害。与传统的系统性胰岛素治疗相比,这一策略展现出更高的创面靶向性,避免了低血糖及胰岛素抵抗等常见副作用。
21、本发明引入mno2纳米颗粒,利用其出色的抗氧化特性,有效清除局部的ros,减轻氧化应激,还能分解gox产生的过氧化氢,防止其在创面微环境中的积累,避免了gox催化过程伴随产生的过氧化氢可能引发氧化应激,对创面愈合产生负面影响。更重要的是,mno2还能够产生氧气,缓解糖尿病创面常见的局部缺氧问题,为创面组织的修复提供了充足的氧气支持。这一策略不仅稳定了创面微环境,还为细胞代谢和组织修复创造了有利条件。
22、本发明通过构建中空mno2纳米颗粒与pei的复合物,确保mir-146a仅在血糖水平较高的创面环境中释放。mno2接枝的pei作为正电荷载体能够有效吸附负电荷的mir-146a。当创面局部环境中糖浓度升高时,由gox催化反应生成的过氧化氢会促使mno2发生构象变化,从而促进mir-146a的释放。这种响应机制确保了在血糖较高的糖尿病创面中释放更多的mir-146a,避免了在相对较低血糖水平的糖尿病创面释放过多mir-146a,过度抑制必要的免疫反应,导致创面清创和修复延迟或mir-146a的过表达引发潜在的自体免疫或代谢异常。mir-146a通过特异性调控fak/nf-κb信号通路,促进巨噬细胞从m1型转化为m2型,增强抗炎和组织修复作用。m2型巨噬细胞在创面愈合后期具有重要作用,能够通过分泌il-10和tgf-β等细胞因子,抑制过度炎症反应,促进血管生成和组织修复。水凝胶处理后的巨噬细胞上清液能够显著促进内皮细胞的迁移和血管生成,同时促进成纤维细胞的迁移,表明该水凝胶通过调控巨噬细胞极化,间接促进了血管生成和组织修复。
23、本发明水凝胶的产氧作用和巨噬细胞m2极化的双重协同效应,促进了创面区域的血管生成。水凝胶处理组创面区域i型和iii型胶原的表达量显著增加,这表明水凝胶通过促进成纤维细胞的活化和迁移,加速了胶原的合成与沉积,从而促进了创面愈合。虽然本研究中的水凝胶系统表现出良好的生物相容性
24、上述说明仅是本发明技术方案的概述,为了能够更清楚了解本发明的技术手段,而可依照说明书的内容予以实施,并且为了让本发明的上述和其它目的、特征和优点能够更明显易懂,以下特举本发明的具体实施方式。
- 还没有人留言评论。精彩留言会获得点赞!