冶炼级氧化铝生产方法(实施方式)与流程
世界各地的氧化铝精炼厂主要使用拜耳技术由低硅(拜耳)铝土矿(其中al2o3/sio2浓度比(氧化铝与二氧化硅之比)不低于3)生产高品质的冶炼级氧化铝。当氧化铝与二氧化硅的比值在3~7的范围时,必须使用拜耳-烧结组合工艺,这是更耗能的工艺。对于高二氧化硅含铝原料,例如霞石和高岭土,在工业上仅使用烧结法,其能源成本比拜耳法的能源成本高约5倍。
同时,正在开发由高硅含铝原料生产氧化铝的酸性方法。其中,盐酸法目前被认为是最合理的方法。
众所周知,氧化铝可以通过盐酸法由高二氧化硅铝土矿来生产,其包括在高达700℃的温度下煅烧含铝原料,将其用盐酸进行处理,通过用气态氯化氢使澄清的氯化物溶液饱和而使六水合氯化铝(alcl3·6h2o)盐析,煅烧氯化铝以生产氧化铝(alumina),使废液热水解,以及精馏所吸收的盐酸,包括在酸处理阶段返回氯化氢,以及分别以水溶液和气体形式盐析(elsnerd.,jenkinsd.h.和sinhah.n.aluminaviahydrochloricacidleachingofhighsilicabauxites-processdevelopment.lightmetals,1984,411-426页)。
根据已知的方法,仅将精馏的盐酸送到原料处理区,这消除酸循环中杂质(例如铁、钠、钾、钙等)的循环和积累,并尽可能减少其在六水合氯化铝中的含量。在结晶alcl3·6h2o后,通过对废液进行完全热水解,将杂质作为氧化物去除。尽管如此,最终产物中的磷含量比冶炼级氧化铝的允许限值高1.5倍。
该方法的缺点还应包括非常复杂的设备和工艺流程以及提供盐酸的完全再生的许多昂贵的设备,这就需要高资本支出来建造使用该技术的氧化铝精炼厂。在结晶alcl3·6h2o后实施废液的完全热水解的区域是非常耗能的区域并且燃料成本显著增加了生产成本。
另外,通过煅烧六水合氯化铝生产的氧化铝与传统的冶炼级氧化铝基本不同,其颗粒强度低、易粉化、堆积密度低1.5至3倍,并且流变特性完全不同(流动性非常差),因此在其运输过程中和在电解生产铝的过程中产生问题。当煅烧这种氧化铝时,几乎不可能同时获得低含量的余氯和α相,这是对冶炼级氧化铝的主要要求之一。如已知方法的创造者所示,如果原料含有任何磷化合物,则几乎其整个体积都将进入最终产物。
已知一种从铝矿石中提取铝和铁的方法(2008年11月27日公开的专利ca2684696);该方法包括准备含铝原料(高岭石族泥板岩),将其用6摩尔盐酸在100~110℃下浸出,将所得的悬浮液分离成固相和液相,将液相和固相的洗涤水蒸馏至90%的程度,包括通过精馏再生氯化氢和将其返回浸出阶段。将剩余的10%液相用苛性碱中和至ph>10,以生产氯化铝溶液并分离出氧化铁沉淀。将氯化铝溶液用盐酸中和至ph=3÷4,并通过液体提取分离出铝,然后转化为铝氢氧化物和氧化物(氧化铝)。
该方法还需要非常大量的热能来提供在原料消耗至90%的程度后煮浓整个液体流和洗涤水,并且大量消耗盐酸和苛性碱,从而从液体中选择性地回收铁和铝。
与所要求保护的方法最接近的是通过盐酸处理原料生产氧化铝的酸碱组合法,其包括分离二氧化硅沉淀物,从澄清的氯化物溶液中结晶出六水合氯化铝,然后将其煅烧以便生产中间氧化铝产物,其由于显著含量的铁和其他杂质(除硅之外),创造者称之为“原始”或“粗”氧化铝。然后用碱性废液浸出中间氧化铝产物,使所得的母液沉淀,水洗,随后煅烧分离出的氢氧化铝,将离开沉淀区的废液和用于洗涤氢氧化铝的水煮浓,并且形成返回到用于浸出中间氧化铝产物的区域的碱性废液(有色金属生产参考.氧化铝精炼.莫斯科:metallurgiya,1970,236-237页)。
基本上,中间氧化铝产物的处理是根据简化的拜耳工艺流程进行的碱性重结晶,其用于去除铁/磷和其他杂质,并在化学组成和物理性质方面生产出冶炼级氧化铝。
所述流程的一个严重缺点是,在酸循环期间,随原料一起输送的铁、钠、钾、钙、镁和其他杂质累积,并且在该方法下,通过在这种情况下深度蒸发氯化物溶液并且最大可能地进行氯化物结晶来解决该问题。粗氧化铝煅烧后,将大量的碱金属氯化物送至拜耳碱循环中;这种氯化物将不可避免地在循环流中积累,并且不提供它们的去除。
已知的生产氧化铝的方法的缺点还包括总计较高的能源成本并且额外的碱损耗高达36-37kg/吨氧化铝。由于这些原因,该方法没有得到工业应用。
本发明基于以下问题:开发一种由低品级(高硅)原料生产冶炼级氧化铝的方法,其允许处理贫瘠的高硅矿石和废料。
技术结果是在由低品级原料生产冶炼级氧化铝时(换言之,在处理贫瘠的高硅矿石和废料时)提高氧化铝的品质并且降低能耗。
通过所提出的生产冶炼级氧化铝的方法,可以解决该问题,并且可以实现上述技术结果,所述方法包括以下阶段:
用盐酸提取含铝原料,
将所得的氯化物浆料分离成废二氧化硅沉淀物和澄清的氯化物溶液,
从澄清的氯化物溶液中结晶出六水合氯化铝,
六水合氯化铝热分解成氧化铝,然后将其煅烧以生产粗氧化铝作为中间产物,
用碱性废液进行粗氧化铝浸出并使所得的铝酸盐溶液沉淀,
对分离的氢氧化铝进行水洗并随后煅烧,并且
将离开沉淀区的废液和用于洗涤氢氧化铝的水煮浓以形成返回到中间氧化铝产物浸出阶段的碱性废液。
另外,为了优化该方法,中间氧化铝产物中的氯离子浓度应保持在0.2重量%~5.0重量%的水平,碱性废液中的氯离子浓度应保持在40~90g/l的水平,并且应将离开沉淀区的废液(总流量的10-40重量%)煮浓,直至分离出要从该过程中去除的含氯化合物晶体。
根据一个实施方式,冶炼级氧化铝生产方法包括以下阶段:
研磨含铝原料,然后将其用盐酸(酸性废液)提取,
将所得的氯化物浆料分离成废二氧化硅沉淀物和澄清的氯化物溶液,
从澄清的氯化物溶液中结晶出六水合氯化铝,
六水合氯化铝热分解成氧化铝,然后将其煅烧以生产粗氧化铝作为中间产物,
用碱性废液进行粗氧化铝浸出并使所得的铝酸盐溶液沉淀,并且随后煅烧分离的氢氧化铝,当将约15%的酸性废液进行热水解时,粗氧化铝中的氯离子浓度保持在0.2%~5.0%,碱性废液中的氯离子浓度保持在40~90g/l的水平,将总流量的10重量%~40重量%的量的沉淀后的碱性废液煮浓,直至分离出要从该过程中去除的含氯化合物晶体。
根据第二实施方式,冶炼级氧化铝生产方法包括以下阶段:
研磨含铝原料,然后将其用盐酸废液(酸性废液)浸出,
将所得的氯化物浆料分离成用水洗涤后倾倒的废二氧化硅沉淀物和澄清的氯化铝溶液,而将用于洗涤目的的水供应至从由煅烧六水合氯化铝产生的烟雾和由热水解过程产生的烟雾中绝热吸收氯化氢的区域,并且洗涤水的量由用于绝热吸收的水量决定,
从澄清的氯化铝溶液中结晶出六水合氯化铝;在分离晶体后,将所得的废液供应到精馏区,在此将废液中的氯化氢浓度降低以形成氯化氢气体,将氯化氢气体干燥然后供应到盐析区;从精馏区排出的废液分为两个不相等的部分:较大的部分直接供应至制备废液,另一部分供应至通过热水解去除杂质,
六水合氯化铝热分解形成氧化铝,随后将其煅烧以生产粗氧化铝作为中间产物,同时煅烧烟雾由用于洗涤废二氧化硅沉淀物的水吸收,
根据拜耳法用碱性废液进行粗氧化铝浸出并使所得的铝酸盐溶液沉淀,
将分离的氢氧化铝水洗并随后煅烧,
将离开沉淀区的废液和用于洗涤氢氧化铝的水煮浓以形成待返回中间氧化铝产物浸出阶段的碱性废液,并且
废液主要用于进行含铝原料浸出,并且其只有一部分通过热水解去除杂质。
该方法的两个实施方式确保了总的技术结果的实现,即在由低品级原料生产冶炼级氧化铝时提高氧化铝品质并且降低能源成本。
作为附加措施,优选实施以下措施:
从沉淀区排出的废液和用于洗涤氢氧化铝的水分两个阶段煮浓,碱金属碳酸盐在第一阶段结晶,碱金属氯化物在第二阶段结晶。
将碱金属氯化物(主要是氯化钠和氯化钾)纯化,并以水溶液的形式进行膜或隔膜电解。
在碱金属氯化物水溶液的膜或隔膜电解过程中形成的氯气和氢气用于合成被送去提取初始含铝原料的盐酸,并且将在碱金属氯化物水溶液的膜或隔膜电解过程中形成的部分碱金属氢氧化物水溶液与返回到中间氧化铝产物浸出阶段的碱性废液混合。
将由碱金属氯化物水溶液的膜或隔膜电解产生的部分碱金属氢氧化物溶液送去中和二氧化硅沉淀物。
附图说明
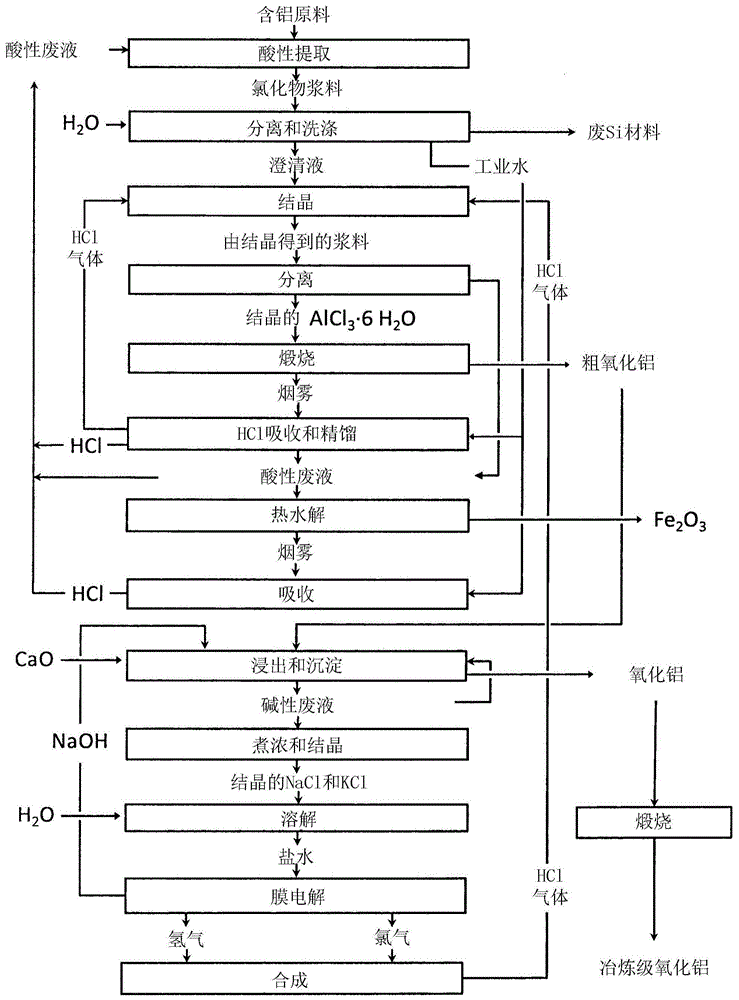
图1——示意性氧化铝生产工艺流程。
通过图1所示的示意性氧化铝生产工艺流程说明本发明,其从流程和模式两方面清楚地说明了该技术的酸和碱循环的合理最优组合,这在总体上提供了技术结果的实现。
例如在高压釜条件下,将粉碎的含铝原料(如高岭土或高岭土泥板岩)用盐酸废液进行酸性提取(浸出)。浸出后,将浆料分离成含有约90%二氧化硅的沉淀物(si材料)和氯化铝溶液。将用水洗涤的si材料倾倒。
将用于洗涤si材料的水供应到从由煅烧六水合氯化铝(ach,alcl3·6h2o)产生的烟雾和由热水解过程产生的烟雾中绝热吸收氯化氢(hcl)的区域。并且氯化铝溶液中的hcl浓度达到17%~19%。在吸收过程中,由于在hcl吸收过程中释放的大量热量,氯化铝溶液自蒸发并且从循环中去除供应的用于洗涤si材料的所有水。值得注意的是,si材料洗涤水的量由在绝热吸收阶段可蒸发的水量决定。
将与si材料分离的氯化铝溶液送去结晶(盐析)区,在此由精馏产生的氯化氢气体鼓泡通过溶液,并且溶液中的hcl浓度达到32%,大部分(~95%)铝沉淀为六水合氯化铝晶体。在分离晶体(结晶颗粒)后,将所得的废液送去精馏区,在此将废液中的hcl浓度降至约22%-27%hcl)并形成气态hcl,将其干燥至~5%h2o的含量并供应到盐析区。从精馏区排出的废液(含有22%~27%hcl)分为两个不相等的部分:较大的部分直接供应至制备酸性废液;另一部分供应至通过热水解去除杂质。
送去热水解的废液的比例由用于浸出的废液中的杂质的允许含量确定。用于热水解的废液的比例约为15%。值得注意的是,氯化铝溶液中的杂质含量比用纯盐酸浸出矿石时的杂质含量增加约6倍。在热水解过程中,废液中所含的所有游离酸和由金属(包括al、fe、ca、mg)氯化物水解形成的hcl进入气相。热水解产物将包括烟雾和由氧化铁(fe2o3)和部分al、ca、mg氧化物和其他微量杂质组成的热水解饼。由热水解产生的烟雾包含再生的hcl,并被送去用si材料洗涤水吸收hcl的区域。
将生产的ach供应到煅烧区以产生粗氧化铝和含有hcl的烟雾。将由煅烧过程产生的烟雾输送到吸收阶段,其中使用si材料洗涤水进行吸收。为了将损失恢复,向送去浸出阶段的废液中加入新鲜酸;而且,可以通过洗涤供应用于精馏的ach产物来添加。
添加新鲜的水以卫生净化由煅烧和热水解过程产生的烟雾(然后用于洗涤si材料)。
该工艺流程的优点在于,大部分废液用于浸出矿石,并且其只有一部分送去通过热水解去除杂质。不存在大而复杂的煮浓和盐精馏区域,热水解区最小化并且与粗氧化铝的生产无关,反而用于杂质的部分去除,这显著降低了能源成本。
应注意,根据现有技术方法的粗氧化铝含有最少量的杂质(包括氯化物)。为了在现有技术方法中实现这一点,必须保持氯化铝溶液含有最低允许水平的杂质,例如铁以及与原料一起投入的钾、钠、钙、镁等;为此,应从这些杂质中纯化酸性废液。例如,现有技术方法表明难以从铁中进行这种纯化。这样做的常用技术是热水解,特别是如类似方法(elsnerd.,jenkinsd.h.和sinhah.n.aluminaviahydrochloricacidleachingofhighsilicabauxites-processdevelopment.lightmetals,1984,423页)所示,在高达850℃的温度下完全蒸发酸性废液,因此在这种情况下能源成本非常高。
根据所要求保护的方法,然后将粗氧化铝输送用于基于已知拜耳法的碱性重结晶。拜耳法的产物是氧化铝,通过煅烧将其转化为冶炼级氧化铝。
为了制备废液,还投入了新鲜的苛性碱,其消耗取决于废泥和氧化铝产物的机械损失,以及粗氧化铝中含有的金属氯化物(alcl3、fecl3、mgcl2、cacl2)在其脱苛化过程中的碱损失。在这种情况下,粗氧化铝中含有的nacl和kcl直接进入溶液而不会引起碱的任何损失。
通过拜耳法(与天然铝土矿处理方法相反)对粗氧化铝的碱性处理的一个特殊特征在于,由于形成的泥浆量极少,因此需要很少的水来洗涤泥浆。因此,可以补偿氧化铝生产过程中的水平衡而不用将整个废液流煮浓,因为添加来洗涤水合物的水量大致对应于与氧化铝产物一起去除的水量。此外,由于少量的泥浆不需要如此大量的冷凝物来洗涤泥浆,因此可以使用浆料-浆料热交换器通过高压釜浸出来回收热量而不用使排放浆料自蒸发。
为了从拜耳循环中去除氯,需要对一部分废液进行深度煮浓和结晶的组合操作。只有在na2o浓度高的区域,nacl在苛性碱溶液中的溶解度才会显著降低;因此,我们谈论的是将一部分废液深度煮浓至苛性碱含量为25%~33%(na2o)。
供应至煮浓区的废液量由拜耳法中氯化物累积的允许水平来确定。溶液中氯化物的可接受水平越高,送去煮浓区的废液比例越小,因此,蒸发水(和热能消耗)的量将为(与粗氧化铝中氯化物的含量相同)。
根据创造者的经验,在工业条件下,拜耳法中使用的废液中氯化物的允许水平为90g/l(对于氯离子cl-)。
在煮浓过程后分离的结晶氯化钠和部分氯化钾送去已知的隔膜或膜电解以释放苛性碱和氢气和氯气,由其合成氯化氢气体。苛性碱和氯化氢分别返回到该工艺的酸和碱部分,以补偿这些试剂不可避免的损失。
因此,所要求保护的方法是闭环工艺流程,使其能够处理低品级(高硅)含铝原料以生产冶炼级氧化铝。
由于粗氧化铝是中间产物,而不是可销售的产物,因此其中与原料一起投入的铁、钾、钠、钙、镁等杂质的含量不必为最低允许含量。因此,可以增加酸循环中这些杂质的浓度,这将降低氯化物溶液蒸发成本。为此,在结晶阶段,可取的是使用简单的设备和易于实施的工艺方法将六水合氯化铝最充分且快速地提取到固相中,而不用担心被送去煅烧区生产粗氧化铝的结晶ach的纯度。此外,为了完全分解氯化物,在煅烧过程中无需深度煅烧产物。一方面,这降低了与煅烧相关的热量成本;另一方面,这不会为在粗氧化铝中形成难溶的α相创造条件。主要以氯化钾、氯化钠、氯化钙和氯化镁为代表的余氯与粗氧化铝一起被提取到工艺流程的酸相中,在此其将不可避免地积累。然而,创造者进行的研究表明,碱性废液中氯离子积累到40~90g/l的水平不会导致拜耳法的性能显著下降。为了避免在该工艺的碱循环中进一步积累氯,将沉淀后的量为总流速的10%~40%的部分废液煮浓直至分离出要从该过程中去除的含氯化合物晶体。实验室实验和循环过程计算表明,该方法足以将碱性废液中的氯离子浓度保持在所需水平,并确保拜耳法的水平衡。
选择方法不可能确定作为所要求保护的方法的这种多链路循环技术的工作参数的最佳组合。创造者通过使用专门开发的过程质热平衡的数学模型解决了这个问题。同时,创造者意外地发现,如果有意使杂质在工艺的酸和碱循环和粗氧化铝(从酸循环到碱循环的中间产物)中积累,则可以降低燃料、热量和电能形式的能耗。
根据基于上述数学模型的优化迭代计算结果进行的数值实验发现如下:如果约15%被送去热水解区,则杂质(铁、钠、钾、镁、钙等)的含量设定在平衡水平,这不会降低从原材料到粗氧化铝的铝回收率,但会导致所述杂质在六水合氯化铝中和进一步在粗氧化铝中的浓度的增加。然而,在该工艺的碱循环中进行粗氧化铝浸出时,铁、钙和镁化合物直接进入不溶性沉淀物中并被除去。在这种情况下,应考虑到送去热水解区的酸性废液的比例越小,与该区中的燃料燃烧相关的能源成本越低。
如在现有技术方法中所提供的,如果在拜耳循环中浸出之前对粗氧化铝进行深度高温煅烧并用水洗涤以去除可溶性氯化物,则可以降低与热水解相关的成本。在这种情况下,粗氧化铝中的氯离子含量降低到万分之几和千分之几,但难溶的α氧化铝的含量增加。其碱处理是通过高温高压釜浸出而实现的,因此导致热能耗的增加。
另一方面,明显的是,如果降低煅烧区的工艺温度或热量和质量交换强度,则能耗将显著降低,但粗氧化铝中的氯含量将增加,并且这种氯离子形式的氯将在该工艺的碱循环中继续积累。从酸循环向碱循环的氯转移将不可避免地导致盐酸和苛性碱的损失。在所要求保护的方法中,这些损失通过从碱循环及其电解处理(产生naoh以及氯气和氢气,由其合成hcl)中去除一些氯化钾和氯化钠来补偿。但是这种再生在从碱性溶液中蒸发氯化钾和氯化钠时需要热能,并且还需要用于电解这些氯化物水溶液的电能。
然而,数值实验表明,尽管优化该过程的热量和质量平衡很复杂,但创造者开发的数学模型允许在酸和碱循环中找到工艺参数的一些不明显的相互联系的备选组合,从而在保持冶炼级氧化铝产物所需品质的同时,使能耗最小化。当粗氧化铝中的氯离子浓度保持在0.2重量%~5.0重量%的水平,碱性废液中的氯离子浓度保持在40~90g/l的水平,并且将离开沉淀区的废液(总流量的10重量%~40重量%)煮浓直至分离出要从该过程中去除的含氯化合物晶体时,这可以实现。在上述工艺参数的最佳组合的存在下,对所要求保护的方法进行了实验实施。
实施例
将540g含铝原料(高岭土泥板岩)粉碎至粒径为<100μm(所述含铝原料以重量%计包含:al2o327.1;sio256.8;fe2o32.0;na2o0.31;k2o<0.15;tio20.48;cao0.45;mgo0.27;p2o5;0.05;11.8),并且与1,650ml的20%盐酸混合,置于高压釜中并在160℃搅拌下保持3小时。通过过滤分离所得的氯化物浆料,用水洗涤固体沉淀物(废si材料)。在70℃下用干燥的氯化氢气体对澄清的氯化铝溶液鼓泡,直至分离出ach晶体而停止。使用过滤器从废液中分离出结晶的ach,并在600℃下煅烧以生产粗氧化铝。将废液用si材料洗涤水稀释至游离20%hcl以产生,将酸性废液送去用酸反复提取高岭土泥板岩,并重复进行上述所有(循环)操作。
在进行上述共6次循环后,酸性废液成分的含量稳定如下(%):alcl320.5-21.5;fecl33.9-4.2;ticl20.001;cacl20.4-0.48;nacl0.1-0.12;kcl0.1-0.11。未观察到含铝原料中铝回收率的降低,其为95.5%~97.5%。每次实验后,用纯盐酸(20%浓度)替换15%体积的废液,以模拟通过热水解或通过用浓硫酸的处理(形成相应金属的低溶解性硫酸盐)从循环中去除杂质。
所得废si材料的平均组成以重量%计如下:al2o32.0;sio290.5;fe2o30.16;na2o0.2;k2o<0.15;tio20.7;cao0.12;mgo<0.025;p2o5;<0.02;4.2。
在酸性废液组成稳定后,进行另外10次循环实验;结果,创造者生产了具有以下组成(重量%)的粗氧化铝:al2o386.0;sio20.08;fe2o32.9;na2o0.61;k2o<0.15;<tio20.05;cao0.3;mgo<0.025;p2o5;0.06;cl-3.5;7.0。
为了在拜耳循环中通过碱处理由粗氧化铝生产冶炼级氧化铝,将500g粗氧化铝在150℃的高压釜中在具有下列组成(g/l)的碱性绿液中溶解2小时:al2o3102.0;na2o174.0;nacl63.3。
所得经过滤的绿液的含量以g/l计如下:al2o3167.3;na2o149.2;nacl57.7。根据拜耳技术对溶液进行沉淀,从而分离出氧化铝,创造者在将其用热水(%)洗涤后,并在1,100℃下煅烧,生产出具有以下化学组成(%)的氧化铝:al2o398.7;;sio20.004;fe2o30.008;na2o0.15;k2o0.01;tio20.001;cao0.004;mgo0.0025;p2o5;0.0007;v2o50.0002;cr2o30.00030.02;cl-0.013。
在使用标准方法测定该氧化铝的物理和机械性能时,创造者发现了以下情况:
尽管碱循环中氯化物的含量很高,但生产的氧化铝完全符合对于‘砂状’冶炼级氧化铝的俄罗斯(gost30558-98‘冶炼级氧化铝’)和国际要求。
由于缺乏类似方法中公布的能耗数据,除类似的方法(elsnerd.,jenkinsd.h.和sinhah.n.aluminaviahydrochloricacidleachingofhighsilicabauxites-processdevelopment.lightmetals,1984,411-426页)之外,创造者对生产1kg氧化铝所消耗的热量和电能进行了计算,并且比较了结果,以比较在本发明说明书中提到的所有技术的节能。结果如下所示。
显然,在处理高二氧化硅原料时的节能方面,所提出的方法仅次于专利族1,然而,后者不能提供冶炼级氧化铝的生产。其他专利族需要更高的能耗。
当约15%的酸性废液进行热水解,中间氧化铝产物中的氯离子浓度保持在0.2重量%~5.0重量%的水平,碱性废液中的氯离子浓度保持在40~90g/l的水平,并且将离开沉淀区的废液(总流量的10重量%~40重量%)煮浓直至分离出要从该过程中去除的含氯化合物晶体时,可以最佳地实现所要求保护的方法规定的节能。基于该方法的酸和碱部分的总质量平衡的数学模型,计算了规定的浓度和流动间隔。在规定的间隔内,在工作参数的任何组合下总计算能耗不超过41.2kj/kg。
尽管说明书引用了某些实施方式,但是对于本领域的专业人员来说,许多修改应该是显而易见的,并且不严格限于实施例、描述和工艺流程。
- 还没有人留言评论。精彩留言会获得点赞!