一种Al-BiOCl/CNTs铝基复合制氢材料及其制备方法和应用与流程
本发明属于能源技术领域,具体是一种al-biocl/cnts铝基复合制氢材料的制备及应用。
背景技术:
氢能作为一种具有应用前景的清洁能源,已得到广泛的关注和研究。近年来al-h2o反应制取氢气的方法引起了广泛关注,铝基制氢材料具有能量密度大、便于储存、原料成本低廉、原料易获得、al-h2o反应产物环境友好、可循环使用等优点。目前铝基复合制氢材料制备方法主要有熔炼法和机械球磨法。
2007年fan等人(fanmq,xuf,sunlx.studiesonhydrogengenerationcharacteristicsofhydrolysisoftheballmillingal-basedmaterialsinpurewater[j].internationaljournalofhydrogenenergy,2007,32(14):2809-2815.)首次采用球磨的方法来制备铝基制氢材料,实现了室温下能产氢765ml/g的效果。但是该技术因首次采用球磨法制备铝基制氢材料,并未考虑金属在球磨过程中的冷焊、团聚问题,因此,该材料产氢性能存在很大的提升空间。
针对上述球磨过程的冷焊、团聚问题,(dupiano等人(dupianop,stamatisd,dreizinel.hydrogenproductionbyreactingwaterwithmechanicallymilledcompositealuminum-metaloxidepowders.internationaljournalofhydrogenenergy.2011;36:4781-91.)研究了各种氧化物与铝的机械球磨,金属氧化物可以在一定程度上阻碍铝粉的冷焊团聚,在此过程中发现铝水反应分为“诱导期、快反应、慢反应”三个阶段。但是该技术存在明显的弊端,即在80度下三个小时才放完氢气,制氢材料的时效性远远不能满足应用要求。
针对上述时效性问题,赵冲等人(chongzhao,fenxu.anovelal-bioclcompositeforhydrogengenerationfromwater.internationaljournalofhydrogenenergy44(13),6655-6662)制备了al-biocl材料,直接将biocl添加到al粉中进行球磨制备制氢材料。材料产氢性能得到明显提升,其中复合材料al-15wt%biocl的性能最好,室温下放氢量1048.4ml/g,产氢速率为491.4ml/gmin,产氢率91.4%,材料在五分钟之内放完氢气。该技术方案虽然可以实现在5min内放完氢气,但是其速率和产氢率都有待提升。
发明人针对上述问题研究发现,仅改变球磨过程的实验参数,无法进一步提高biocl在al中均匀分散,这是现有技术提高制氢材料性能的瓶颈。
技术实现要素:
本发明的目的是提供一种al-biocl/cnts铝基复合制氢材料及其制备方法和应用。
本发明的原理为:首先通过利用cnts上的活性位点,诱导原位制备获得的biocl均匀分散在cnts上;再将biocl/cnts复合材料与铝粉进行球磨,实现biocl在al中的更加均匀的分散并引发原位反应,生成bi、alcl3、bi2o3;利用al和bi可以形成腐蚀电池,生成的盐和金属氧化物能有效催化铝粉可以在室温下快速产氢的原理,实现室温条件、纯水条件下快速高效产氢的目的。
本发明技术方案选择cnts的原理为:1、利用cnts的活性位点,诱导biocl在生成时,在cnts上实现均匀分散;2、cnts具有良好的导电性,可以有效提高铝水反应过程的催化效果;3、cnts还为水分子与铝粉接触提供更多通道,促进反应的进行。
实现本发明目的的技术方案是:
一种al-biocl/cnts铝基复合制氢材料,由al粉和biocl/cnts混合球磨制得,所述biocl/cnts由铋盐与氯化物原位制备biocl负载在cnts上制得;
所述biocl/cnts为微米级球状,所述球体由片层状材料组成。
一种al-biocl/cnts铝基复合制氢材料的制备方法,包括以下步骤:
步骤1)biocl/cnts复合材料的制备,将cnts加入到水中,加入醋酸呈酸性条件,在超声分散均匀后,加入可溶性铋盐五水硝酸铋,继续超声分散并搅拌均匀得到混合溶液,然后将可溶性金属氯化物(氯化钾或氯化钠)加入到上述混合溶液中引发反应生成biocl,同时将biocl负载cnts上,经过滤或离心、洗涤、干燥得到biocl/cnts;
步骤2)al-biocl/cnts铝基复合制氢材料的制备,在惰性气体环境保护下,以满足biocl/cnts材料占总质量的13-18%、球料比为(30-120):1,球磨转速为20-250r/min,球磨时间为60-250min的条件下,将步骤1所得biocl/cnts与al粉进行球磨,得到al-biocl/cnts铝基复合制氢材料。
一种al-biocl/cnts铝基复合制氢材料作为水解制氢材料的应用,单位质量的产氢量为1010.3-1123ml/g、产氢速率为1233-4527ml/gmin及产氢率为90.6-94.9%。
对步骤1所得al-biocl/cnts复合材料进行xrd、sem测试。测试结果表明,制备的biocl纯净无杂质,并附着在cnts上。上述结果表明,biocl/cnts复合材料制备成功。
al-biocl/cnts铝基复合制氢材料产氢性能的测试,采用排水集气法,称取0.1g上述实施例中制备的al-biocl/cnts铝基复合制氢材料,在25℃下,加入10ml的水,收集产生的气体、测定其产氢性能。
经实验证实,cnts诱导原位制备biocl获得的biocl/cnts材料,对均匀分散的技术效果显著。直接将al粉、biocl和cnts混合球磨,放氢量为1075.5ml/g,产氢率为90.9%。在同等条件下,与本发明材料的产氢性能存在显著的差距。
biocl/cnts材料作为催化剂添加量对al-biocl/cnts铝基复合制氢材料产氢性能的影响测试结果表明,制备的al-xwt%biocl/cnts铝基复合材料产氢率都在90%以上,其中87%al-13%biocl/cnts产氢性能最好,其单位质量产氢量可达1123.5ml/g,最大产氢速率可达1233ml/gmin,产氢率达到94.9%。
球磨时间对al-biocl/cnts铝基复合制氢材料产氢性能的影响实验结果表明,不同球磨时间对材料的产氢量略有影响,其中球磨5h的87%al-13%biocl/cnts复合材料产氢性能最好,其单位质量产氢量可达1123.5ml/g,最大产氢速率可达1233ml/gmin,产氢率达到94.9%。
87%al-13%biocl/cnts复合材料与水反应的活化能实验结果表明,不同测试温度下87%al-13%c@bi制氢材料的产氢率都在85%以上,其中在45℃环境下材料完全放氢。其单位质量产氢量可达1183.2ml/g,最大产氢速率可达6540ml/gmin,产氢率达到100%。根据阿伦尼乌斯公式计算可得87%al-13%biocl/cnts制氢材料与水反应的表观活化能为42.2kj/mol,低于al-bi复合材料的活化能45.4kj/mol。
综合上述实验结果可知,biocl/cnts催化剂不仅可以防止金属粉末球磨过程中的团聚,球磨过程中生成单质bi、alcl3、bi2o3可以有效催化铝基材料产氢,此外,cnts还可以在水解过程中发挥电子传输的重要作用,进一步促进材料快速产氢。
本发明相对于现有技术,具有以下优点:
1、biocl/cnts的材料新颖,利用氯化物为诱导剂,合成方法简单,合成过程无毒无害,节省人力物力,适合大规模使用;
2、球磨过程中biocl/cnts复合材料在铝粉中分布更加均匀,一方面更有利于球磨过程中生成bi单质、alcl3和bi2o3;
3、biocl负载在cnts上,避免球磨过程中cnts被剥离为单层的柔性碳包裹al颗粒,影响材料产氢率。
综上所述,本发明利用氯化氧铋能活化磨碎铝粉的特性以及用cnts传输电子优良的特点,将铝粉、biocl/cnts的材料通过球磨制备了铝基复合制氢材料。经过球磨,生成bi单质与铝粉颗粒形成腐蚀电池,alcl3溶于水放热,bi2o3活化铝粉、cnts高效的电子传导率有效地改善了al-h2o反应中电子传输的技术问题。而且合成催化剂的方法简单,产物纯净无杂质;制备铝基复合制氢材料的时间缩短,能广泛用于便携式移动氢源和燃料电池供氢的应用。因此,本发明在氢气制备领域、大规模能源储存、便携式移动氢源、燃料电池供氢的等领域具有广阔的应用前景。
附图说明
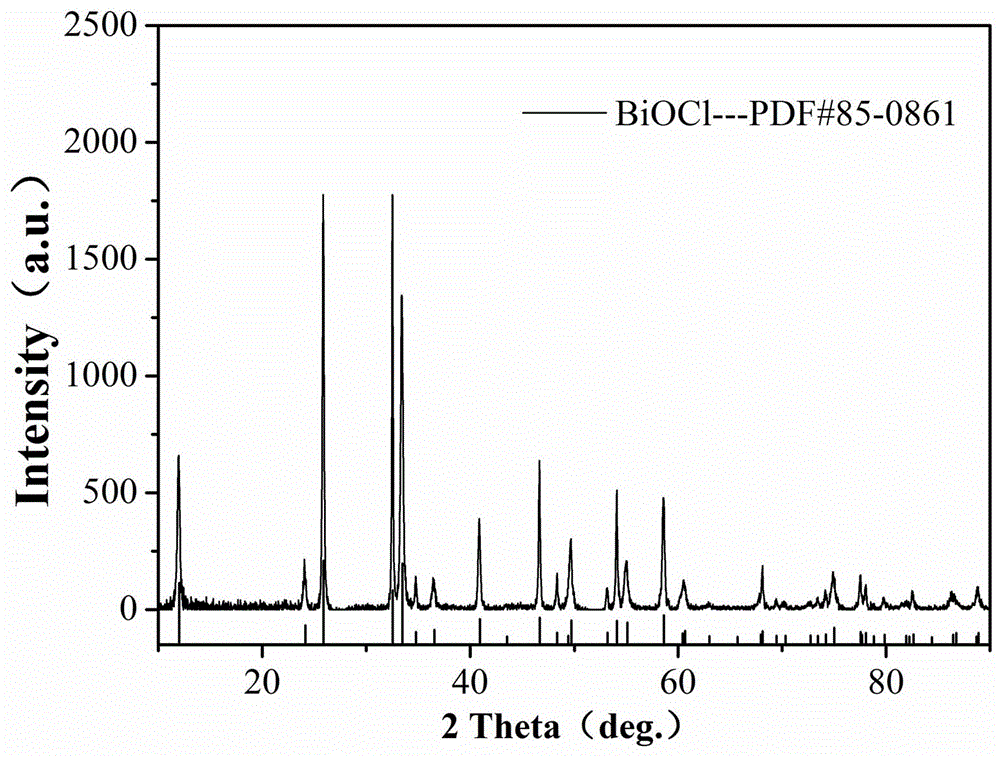
图1为实施例1中biocl/cnts材料的xrd图;
图2为实施例1中biocl/cnts材料的sem图;
图3为实施例1-3中不同biocl/cnts含量的al-biocl/cnts铝基复合制氢材料的放氢速率曲线。
具体实施方式
下面结合实施例对本发明内容作进一步的说明,但不是对本发明的限定。
实施例1
一种biocl/cnts添加量为13%的al-biocl/cnts铝基复合制氢材料的制备方法,包括以下步骤:
步骤1)一种al-biocl/cnts铝基复合制氢材料,其特征在于:将cnts分散在弱酸溶液中,以一定的量之比,让铋盐与无机盐在弱酸性环境下反应,生成biocl/cnts,离心洗涤干燥后;再以一定质量比,将al粉与所得biocl/cnts材料进行球磨制成。
为了证明biocl/cnts复合材料制备成功,对步骤1所得biocl/cnts复合材料进行xrd、sem测试,测试结果如图1、图2所示,biocl以化合物形成存在,并附着在cnts。上述结果表明,biocl/cnts复合材料制备成功;
步骤2)al-biocl/cnts铝基复合制氢材料的制备,在惰性气体环境保护下,以质量比为87:13,称取0.87gal粉和0.13gbiocl/cnts材料以球料比为60:1,球磨转速为250r/min,球磨时间为5h的条件进行球磨,,所得的铝基复合制氢材料命名为87%al-13%biocl/cnts。
al-biocl/cnts铝基复合制氢材料产氢性能测试,采用排水集气法,称取0.1g上述实施例中制备的al-biocl/cnts铝基复合制氢材料,在25℃下,加入10ml的水,收集产生的气体测定其产氢性能。
为了证明本发明cnts诱导原位制备biocl获得的biocl/cnts材料对均匀分散产生的技术效果,通过对比例1,以与实施例1相同biocl和cnts添加量,直接混合进行球磨,制备了87%al-13%(biocl+cnts)。
对比例1
一种直接添加biocl和cnts的al-biocl-cnts铝基复合制氢材料的制备方法,包括以下步骤:在惰性气体环境保护下,以biocl和cnts总添加量占总质量的为13%,直接称取0.87gal粉,0.104gbiocl和0.026gcnts材料,进行球磨,所得铝基复合制氢材料命名为87%al-13%(biocl+cnts)。
测试方法与实施例1相同,测试结果为:对比例1制备的87%al-13%(biocl+cnts)材料放氢量为1075.5ml/g,产氢率为90.9%;在同等条件下,较本发明实施例1材料的产氢量1123.5ml/g,产氢率94.9%的差距显著。
原因在于单独添加的cnts在球磨过程中被剥离为单层碳,包裹部分铝粉,使biocl与铝粉混合不均匀,而通过原位制备的方法,将biocl负载在cnts表面,对bi元素的均匀分布,起到了极大的促进作用,并且biocl/cnts作为独立组分,球磨过程中cnts表层的biocl能与铝粉混合均匀,避免cnts被剥离以及铝粉被碳材料包裹,更有利于球磨过程中铝粉的细化及al、bi腐蚀电池的产生和alcl3、bi2o3的生成。
因此,本发明先制备biocl/cnts,再进行复合球磨的技术起到了显著提高产氢性能的效果。
为了证明biocl/cnts材料作为催化剂添加量对al-biocl/cnts铝基复合制氢材料产氢性能的影响,通过对比例2、实施例2、3、对比例3制备了biocl/cnts材料含量分别为10%、15%、18%和20%的铝基复合制氢材料。
对比例2
一种biocl/cnts添加量为10%的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2称取0.9gal粉和0.1gbiocl/cnts材料,所得铝基复合制氢材料命名为90%al-10%biocl/cnts。
实施例2
一种biocl/cnts添加量为15%的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2称取0.85gal粉和0.15gbiocl/cnts材料,所得铝基复合制氢材料命名为85%al-15%biocl/cnts。
实施例3
一种biocl/cnts添加量为18%的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2称取0.82gal粉和0.18gbiocl/cnts材料,所得铝基复合制氢材料命名为82%al-18%biocl/cnts。
对比例3
一种biocl/cnts添加量为20%的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2称取0.8gal粉和0.2gbiocl/cnts材料,所得铝基复合制氢材料命名为80%al-20%biocl/cnts。
测试方法与实施例1相同,测试结果整理在表1。实验结果表明,实施例1、2、3所制备的al-biocl/cnts铝基复合制氢材料的产氢率都在90%以上,其中87%al-13%biocl/cnts产氢性能最好,其单位质量产氢量可达1123.5ml/g,最大产氢速率可达1233ml/gmin,产氢率达到94.9%。通过对比例2和3可知,biocl/cnts的添加量对al-biocl/cnts铝基复合制氢材料的产氢性能影响显著,且不呈线性关系,不通过实验测试,无法预测产氢性能的变化。
表1在25℃下,不同biocl/cnts含量制得的al-xwt%biocl/cnts材料的产氢性能
为了证明球磨时间对al-biocl/cnts铝基复合制氢材料产氢性能的影响,通过对比例4、实施例4、5制备了球磨时间为1、3、7h的al-biocl/cnts铝基复合制氢材料。
对比例4
一种球磨时间为1h的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2球磨时间为1h,所得的铝基复合制氢材料命名为87%al-13%biocl/cnts-1。
实施例4
一种球磨时间为3h的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2球磨时间为3h,所得的铝基复合制氢材料命名为87%al-13%biocl/cnts-3。
实施例5
一种球磨时间为7h的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2球磨时间为7h,所得的铝基复合制氢材料命名为87%al-13%al-biocl/cnts-7。
测试方法与实施例1相同,测试结果整理在表2。实验结果表明,不同球磨时间材料的产氢量略有差异,其中球磨5h的87%al-13%biocl/cnts复合材料产氢性能最好,其单位质量产氢量可达1123.5ml/g,最大产氢速率可达1233ml/gmin,产氢率达到94.9%。从对比例4、实施例4、5中可以得出,材料的产氢速率在3h达到峰值,由于球磨时间较短,biocl在al中分布不够均匀,此外材料粒径较大导致材料产氢率不如分布更均匀、颗粒度更小的5h的样品。通过对比例4及实施例4、5可知,球磨时间对al-biocl/cnts铝基复合制氢材料的产氢性能影响显著,且不呈线性关系。
表2在25℃下,不同球磨时间制得的87%al-13%biocl/cnts材料的产氢性能
为了计算87%al-13%biocl/cnts复合材料与水反应的活化能,通过实施例6、7、8测试了87%al-13%biocl/cnts在15、35、45℃下的产氢性能。
实施例6
一种测试温度为15℃的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2测试温度为15℃,所得的铝基复合制氢材料命名为87%al-13%biocl/cnts-15。
实施例7
一种测试温度为35℃的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2测试温度为35℃,所得的铝基复合制氢材料命名为87%al-13%biocl/cnts-35。
实施例8
一种测试温度为45℃的al-biocl/cnts铝基复合制氢材料的制备方法,具体步骤中未特别说明的步骤与实施例1相同,不同之处之处在于:所述步骤2测试温度为45℃,所得的铝基复合制氢材料命名为87%al-13%biocl/cnts-45。
测试方法与实施例1基本相同,不同之处在于:测试前通过水浴法,控制反应装置的温度为测试温度。测试结果整理在表3。实验结果表明,不同测试温度下87%al-13%biocl/cnts制氢材料的产氢率都在85%以上,其中在45℃环境下,材料达到理论转化率,其单位质量产氢量可达1183.2ml/g,最大产氢速率可达6450ml/gmin,产氢率达到100%。根据阿伦尼乌斯公式计算可得87%al-13%biocl/cnts制氢材料与水反应的表观活化能为42.2kj/mol,低于al-bi复合材料的活化能45.4kj/mol,表明本发明方法有效提高了铝水反应的化学动力学性能。
表3不同测试温度下87%al-13%biocl/cnts材料的产氢性能
- 还没有人留言评论。精彩留言会获得点赞!